कार्बनिक रसायन विज्ञान तालिका में रासायनिक प्रतिक्रियाएँ। कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकार - नॉलेज हाइपरमार्केट। तंत्र द्वारा रासायनिक प्रतिक्रियाओं का वर्गीकरण
सीएच 3 -सीएच 3 + सीएल 2 - (एचवी) ---- सीएच 3 -सीएच 2 सीएल + एचसीएल
सी 6 एच 5 सीएच 3 + सीएल 2 --- 500 सी --- सी 6 एच 5 सीएच 2 सीएल + एचसीएल
अतिरिक्त प्रतिक्रियाएँ
ऐसी प्रतिक्रियाएँ एकाधिक (दोहरे या तिहरे) बंधन वाले कार्बनिक यौगिकों के लिए विशिष्ट होती हैं। इस प्रकार की प्रतिक्रियाओं में एल्कीन और एल्काइन में हैलोजन, हाइड्रोजन हैलाइड और पानी मिलाने की प्रतिक्रिया शामिल होती है
सीएच 3 -सीएच=सीएच 2 + एचसीएल ---- सीएच 3 -सीएच(सीएल)-सीएच 3
उन्मूलन प्रतिक्रियाएं
ये ऐसी प्रतिक्रियाएं हैं जो कई बंधनों के निर्माण की ओर ले जाती हैं। हाइड्रोजन हैलाइड और पानी को नष्ट करते समय, प्रतिक्रिया की एक निश्चित चयनात्मकता देखी जाती है, जिसे ज़ैतसेव के नियम द्वारा वर्णित किया गया है, जिसके अनुसार कार्बन परमाणु से एक हाइड्रोजन परमाणु समाप्त हो जाता है, जिस पर कम हाइड्रोजन परमाणु होते हैं। उदाहरण प्रतिक्रिया
CH3-CH(Cl)-CH 2 -CH 3 + KOH →CH 3 -CH=CH-CH 3 + HCl
पॉलिमराइजेशन और पॉलीकंडेनसेशन
n(CH 2 =CHCl) (-CH 2 -CHCl)n
रिडॉक्स
ऑक्सीडेटिव प्रतिक्रियाओं में सबसे तीव्र दहन है, जो कार्बनिक यौगिकों के सभी वर्गों की एक प्रतिक्रिया विशेषता है। इस मामले में, दहन की स्थिति के आधार पर, कार्बन को सी (कालिख), सीओ या सीओ 2 में ऑक्सीकरण किया जाता है, और हाइड्रोजन को पानी में परिवर्तित किया जाता है। हालाँकि, कार्बनिक रसायनज्ञों के लिए, दहन की तुलना में बहुत हल्की परिस्थितियों में की गई ऑक्सीकरण प्रतिक्रियाएँ बहुत रुचिकर होती हैं। प्रयुक्त ऑक्सीकरण एजेंट: पानी में Br2 या CCl 4 में Cl2 का घोल; KMnO4 पानी या तनु अम्ल में; कॉपर ऑक्साइड; चांदी (I) या तांबे (II) के ताजा अवक्षेपित हाइड्रॉक्साइड।
3C 2 H 2 + 8KMnO 4 +4H 2 O→3HOOC-COOH + 8MnO 2 + 8KOH
एस्टेरिफिकेशन (और इसकी रिवर्स हाइड्रोलिसिस प्रतिक्रिया)
आर 1 सीओओएच + एचओआर 2 एच+ आर 1 सीओओआर 2 + एच 2 ओ
cycloaddition
वाई आर वाई-आर
‖ + ‖ → ǀ ǀ
आर वाई आर-वाई
‖ + →
11. तंत्र द्वारा कार्बनिक प्रतिक्रियाओं का वर्गीकरण। उदाहरण।
प्रतिक्रिया तंत्र में विस्तृत चरण-दर-चरण विवरण शामिल है रासायनिक प्रतिक्रिएं. इसी समय, यह स्थापित किया जाता है कि कौन से सहसंयोजक बंधन, किस क्रम में और किस तरह से टूटे हैं। प्रतिक्रिया के दौरान नए बांडों के निर्माण का सावधानीपूर्वक वर्णन किया गया है। प्रतिक्रिया तंत्र पर विचार करते समय सबसे पहले प्रतिक्रियाशील अणु में सहसंयोजक बंधन को तोड़ने की विधि पर ध्यान दिया जाता है। ऐसे दो तरीके हैं - होमोलिटिक और हेटेरोलिटिक।
उग्र प्रतिक्रियाएंसहसंयोजक बंधन के होमोलिटिक (कट्टरपंथी) दरार से आगे बढ़ें:

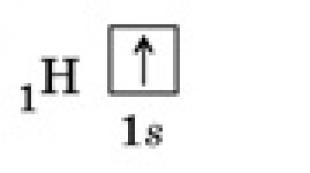
गैर-ध्रुवीय या निम्न-ध्रुवीय सहसंयोजक बंधन (सी-सी, एन-एन, सी-एच) उच्च तापमान पर या प्रकाश के प्रभाव में कट्टरपंथी दरार से गुजरते हैं। सीएच 3 रेडिकल में कार्बन में 7 बाहरी इलेक्ट्रॉन होते हैं (सीएच 4 में एक स्थिर ऑक्टेट शेल के बजाय)। रेडिकल्स अस्थिर होते हैं; वे गायब इलेक्ट्रॉन (एक जोड़ी तक या एक ऑक्टेट तक) को पकड़ लेते हैं। स्थिर उत्पाद बनाने का एक तरीका डिमराइजेशन (दो रेडिकल का संयोजन) है:
सीएच 3 + सीएच 3 सीएच 3 : सीएच 3,
एन + एन एन : एन।
कट्टरपंथी प्रतिक्रियाएँ - ये हैं, उदाहरण के लिए, क्लोरीनीकरण, ब्रोमिनेशन और अल्केन्स के नाइट्रेशन की प्रतिक्रियाएं:

आयनिक प्रतिक्रियाएँ हेटेरोलिटिक बंधन दरार के साथ होता है। इस मामले में, अल्पकालिक कार्बनिक आयन - कार्बोकेशन और कार्बोनियन - कार्बन परमाणु पर चार्ज के साथ मध्यवर्ती रूप से बनते हैं। आयनिक प्रतिक्रियाओं में, बंधनकारी इलेक्ट्रॉन युग्म अलग नहीं होता है, बल्कि पूरी तरह से परमाणुओं में से एक में चला जाता है, इसे आयन में बदल देता है:

दृढ़ता से ध्रुवीय (एच-ओ, सी-ओ) और आसानी से ध्रुवीकरण योग्य (सी-बीआर, सी-आई) बंधन हेटरोलिटिक दरार के लिए प्रवण होते हैं।
अंतर करना न्यूक्लियोफिलिक प्रतिक्रियाएं (न्यूक्लियोफाइल- नाभिक की तलाश, इलेक्ट्रॉनों की कमी वाला स्थान) और इलेक्ट्रोफिलिक प्रतिक्रियाएं (इलेक्ट्रोफाइल- इलेक्ट्रॉनों की तलाश)। यह कथन कि एक विशेष प्रतिक्रिया न्यूक्लियोफिलिक या इलेक्ट्रोफिलिक है, हमेशा अभिकर्मक को संदर्भित करता है। अभिकर्मक- एक सरल संरचना के साथ प्रतिक्रिया में भाग लेने वाला पदार्थ। सब्सट्रेट- अधिक जटिल संरचना वाला एक प्रारंभिक पदार्थ। निवर्तमान समूहएक प्रतिस्थापन योग्य आयन है जो कार्बन से बंधा हुआ है। प्रतिक्रिया उत्पाद- नया कार्बन युक्त पदार्थ (प्रतिक्रिया समीकरण के दाईं ओर लिखा हुआ)।
को न्यूक्लियोफिलिक अभिकर्मक(न्यूक्लियोफाइल) में नकारात्मक रूप से चार्ज किए गए आयन, इलेक्ट्रॉनों के एकाकी जोड़े वाले यौगिक, दोहरे कार्बन-कार्बन बांड वाले यौगिक शामिल हैं। को इलेक्ट्रोफिलिक अभिकर्मक(इलेक्ट्रोफाइल) में धनात्मक रूप से आवेशित आयन, बिना भरे इलेक्ट्रॉन कोश वाले यौगिक (AlCl 3, BF 3, FeCl 3), कार्बोनिल समूहों वाले यौगिक, हैलोजन शामिल हैं। इलेक्ट्रोफाइल कोई भी परमाणु, अणु या आयन है जो एक नया बंधन बनाने की प्रक्रिया में इलेक्ट्रॉनों की एक जोड़ी जोड़ने में सक्षम है। आयनिक प्रतिक्रियाओं की प्रेरक शक्ति विपरीत रूप से आवेशित आयनों या आंशिक आवेश (+ और -) के साथ विभिन्न अणुओं के टुकड़ों की परस्पर क्रिया है।
विभिन्न प्रकार की आयनिक प्रतिक्रियाओं के उदाहरण.
न्यूक्लियोफिलिक प्रतिस्थापन :
इलेक्ट्रोफिलिक प्रतिस्थापन :
न्यूक्लियोफिलिक जोड़ (CN - पहले जोड़ा जाता है, फिर H +):

इलेक्ट्रोफिलिक कनेक्शन (H + पहले जोड़ा जाता है, फिर X -):

न्यूक्लियोफाइल (आधार) की क्रिया द्वारा उन्मूलन :
कार्रवाई पर उन्मूलन इलेक्ट्रोफाइल (एसिड) :
जब रासायनिक प्रतिक्रियाएँ होती हैं, तो कुछ बंधन टूट जाते हैं और अन्य बन जाते हैं। रासायनिक प्रतिक्रियाओं को पारंपरिक रूप से कार्बनिक और अकार्बनिक में विभाजित किया गया है। कार्बनिक अभिक्रियाएँ वे अभिक्रियाएँ मानी जाती हैं जिनमें कम से कम एक अभिकारक एक कार्बनिक यौगिक होता है जो प्रतिक्रिया के दौरान अपनी आणविक संरचना को बदल देता है। कार्बनिक प्रतिक्रियाओं और अकार्बनिक प्रतिक्रियाओं के बीच अंतर यह है कि, एक नियम के रूप में, अणु उनमें शामिल होते हैं। ऐसी प्रतिक्रियाओं की दर कम है, और उत्पाद की उपज आमतौर पर केवल 50-80% है। प्रतिक्रिया दर बढ़ाने के लिए उत्प्रेरकों का उपयोग किया जाता है और तापमान या दबाव बढ़ाया जाता है। आगे, हम कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकारों पर विचार करेंगे।
रासायनिक परिवर्तनों की प्रकृति द्वारा वर्गीकरण
- प्रतिस्थापन प्रतिक्रियाएँ
- अतिरिक्त प्रतिक्रियाएँ
- आइसोमेराइजेशन प्रतिक्रिया और पुनर्व्यवस्था
- ऑक्सीकरण प्रतिक्रियाएँ
- अपघटन प्रतिक्रियाएँ
प्रतिस्थापन प्रतिक्रियाएँ
प्रतिस्थापन प्रतिक्रियाओं के दौरान, प्रारंभिक अणु में एक परमाणु या परमाणुओं के समूह को अन्य परमाणुओं या परमाणुओं के समूहों द्वारा प्रतिस्थापित किया जाता है, जिससे एक नया अणु बनता है। एक नियम के रूप में, ऐसी प्रतिक्रियाएं संतृप्त और सुगंधित हाइड्रोकार्बन की विशेषता होती हैं, उदाहरण के लिए:
अतिरिक्त प्रतिक्रियाएँ
जब अतिरिक्त प्रतिक्रियाएं होती हैं, तो पदार्थों के दो या दो से अधिक अणुओं से एक नए यौगिक का एक अणु बनता है। ऐसी प्रतिक्रियाएँ असंतृप्त यौगिकों के लिए विशिष्ट हैं। हाइड्रोजनीकरण (कमी), हैलोजनीकरण, हाइड्रोहैलोजनेशन, जलयोजन, पोलीमराइजेशन आदि की प्रतिक्रियाएं होती हैं:
- हाइड्रोजनीकरण– हाइड्रोजन अणु का योग:
उन्मूलन प्रतिक्रिया
उन्मूलन प्रतिक्रियाओं के परिणामस्वरूप, कार्बनिक अणु परमाणुओं या परमाणुओं के समूहों को खो देते हैं, और एक या अधिक एकाधिक बंधन युक्त एक नया पदार्थ बनता है। उन्मूलन प्रतिक्रियाओं में प्रतिक्रियाएं शामिल हैं निर्जलीकरण, निर्जलीकरण, निर्जलीकरणऔर इसी तरह।:
आइसोमेराइजेशन प्रतिक्रियाएं और पुनर्व्यवस्था
ऐसी प्रतिक्रियाओं के दौरान, इंट्रामोल्युलर पुनर्व्यवस्था होती है, अर्थात। उदाहरण के लिए, प्रतिक्रिया में भाग लेने वाले पदार्थ के आणविक सूत्र को बदले बिना अणु के एक भाग से दूसरे भाग में परमाणुओं या परमाणुओं के समूहों का संक्रमण: 

ऑक्सीकरण प्रतिक्रियाएँ
ऑक्सीकरण अभिकर्मक के संपर्क के परिणामस्वरूप, इलेक्ट्रॉनों की हानि के कारण कार्बनिक परमाणु, अणु या आयन में कार्बन की ऑक्सीकरण अवस्था बढ़ जाती है, जिसके परिणामस्वरूप एक नए यौगिक का निर्माण होता है: 
संघनन एवं बहुसंघनन अभिक्रियाएँ
नए के निर्माण के साथ कई (दो या अधिक) कार्बनिक यौगिकों की परस्पर क्रिया में शामिल होता है सी-सी कनेक्शनऔर कम आणविक भार यौगिक:
पॉलीकंडेंसेशन एक कम आणविक भार यौगिक की रिहाई के साथ कार्यात्मक समूहों वाले मोनोमर्स से एक बहुलक अणु का निर्माण है। पोलीमराइजेशन प्रतिक्रियाओं के विपरीत, जिसके परिणामस्वरूप पॉलीकंडेनसेशन प्रतिक्रियाओं के परिणामस्वरूप मोनोमर के समान संरचना वाले बहुलक का निर्माण होता है, परिणामी बहुलक की संरचना उसके मोनोमर से भिन्न होती है:
अपघटन प्रतिक्रियाएँ
यह एक जटिल कार्बनिक यौगिक को कम जटिल या सरल पदार्थों में तोड़ने की प्रक्रिया है:

सी 18 एच 38 → सी 9 एच 18 + सी 9 एच 20
तंत्र द्वारा रासायनिक प्रतिक्रियाओं का वर्गीकरण
कार्बनिक यौगिकों में सहसंयोजक बंधनों के टूटने के साथ प्रतिक्रियाओं की घटना दो तंत्रों द्वारा संभव है (यानी, पुराने बंधन के टूटने और नए बंधन के निर्माण का मार्ग) - हेटेरोलिटिक (आयनिक) और होमोलिटिक (रेडिकल)।
हेटरोलाइटिक (आयनिक) तंत्र
हेटरोलिटिक तंत्र के अनुसार आगे बढ़ने वाली प्रतिक्रियाओं में, मध्यवर्ती कण बनते हैं आयनिक प्रकारआवेशित कार्बन परमाणु के साथ। धनात्मक आवेश वाले कणों को कार्बोकेशन कहा जाता है, और ऋणात्मक आवेश वाले कणों को कार्बोनियन कहा जाता है। इस मामले में, यह सामान्य इलेक्ट्रॉन जोड़ी का टूटना नहीं है, बल्कि आयन के गठन के साथ परमाणुओं में से एक में इसका संक्रमण होता है: 
दृढ़ता से ध्रुवीय, उदाहरण के लिए एच-ओ, सी-ओ, और आसानी से ध्रुवीकरण योग्य, उदाहरण के लिए सी-बीआर, सी-आई बांड हेटेरोलिटिक दरार की प्रवृत्ति प्रदर्शित करते हैं।
हेटरोलिटिक तंत्र के अनुसार आगे बढ़ने वाली प्रतिक्रियाओं को विभाजित किया गया है न्यूक्लियोफिलिक और इलेक्ट्रोफिलिक प्रतिक्रियाएं.एक अभिकर्मक जिसमें बंधन बनाने के लिए एक इलेक्ट्रॉन युग्म होता है, उसे न्यूक्लियोफिलिक या इलेक्ट्रॉन-दान कहा जाता है। उदाहरण के लिए, HO - , RO - , Cl - , RCOO - , CN - , R - , NH 2 , H 2 O , NH 3 , C 2 H 5 OH , एल्कीन, एरीन।
एक अभिकर्मक जिसमें एक अधूरा इलेक्ट्रॉन आवरण होता है और एक नया बंधन बनाने की प्रक्रिया में इलेक्ट्रॉनों की एक जोड़ी को जोड़ने में सक्षम होता है, निम्नलिखित धनायनों को इलेक्ट्रोफिलिक अभिकर्मक कहा जाता है: H +, R 3 C +, AlCl 3, ZnCl 2, SO 3। , बीएफ 3, आर-सीएल, आर 2 सी=ओ
न्यूक्लियोफिलिक प्रतिस्थापन प्रतिक्रियाएं
एल्काइल और एरिल हैलाइड्स के लिए विशेषताएँ: 
न्यूक्लियोफिलिक जोड़ प्रतिक्रियाएं 
इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाएं

इलेक्ट्रोफिलिक जोड़ प्रतिक्रियाएं 
होमोलिटिक (कट्टरपंथी तंत्र)
होमोलिटिक (रेडिकल) तंत्र के अनुसार आगे बढ़ने वाली प्रतिक्रियाओं में, पहले चरण में रेडिकल के निर्माण के साथ सहसंयोजक बंधन टूट जाता है। परिणामस्वरूप मुक्त कण एक हमलावर अभिकर्मक के रूप में कार्य करता है। रेडिकल तंत्र द्वारा बंधन विच्छेदन गैर-ध्रुवीय या निम्न-ध्रुवीय सहसंयोजक बंधन (सी-सी, एन-एन, सी-एच) के लिए विशिष्ट है।
मूलक प्रतिस्थापन और मूलक योगात्मक अभिक्रियाओं के बीच अंतर स्पष्ट करें
कट्टरपंथी विस्थापन प्रतिक्रियाएं
अल्केन्स की विशेषता 
कट्टरपंथी जोड़ प्रतिक्रियाएं
एल्कीन और एल्काइन की विशेषता 
इस प्रकार, हमने कार्बनिक रसायन विज्ञान में मुख्य प्रकार की रासायनिक प्रतिक्रियाओं की जांच की
श्रेणियाँ ,प्रतिक्रिया के दौरान, प्रतिक्रियाशील पदार्थों के अणुओं में कुछ रासायनिक बंधन टूट जाते हैं और अन्य बनते हैं। कार्बनिक प्रतिक्रियाओं को टूटने के प्रकार के अनुसार वर्गीकृत किया जाता है रासायनिक बन्धप्रतिक्रियाशील कणों में. उनमें से, प्रतिक्रियाओं के दो बड़े समूहों को प्रतिष्ठित किया जा सकता है - कट्टरपंथी और आयनिक।
रेडिकल प्रतिक्रियाएं ऐसी प्रक्रियाएं हैं जिनमें सहसंयोजक बंधन का होमोलिटिक दरार शामिल होता है। होमोलिटिक क्लीवेज में, बंधन बनाने वाले इलेक्ट्रॉनों की जोड़ी को इस तरह से विभाजित किया जाता है कि प्रत्येक परिणामी कण को एक इलेक्ट्रॉन प्राप्त होता है। होमोलिटिक दरार के परिणामस्वरूप, मुक्त कण बनते हैं:
अयुग्मित इलेक्ट्रॉन वाले तटस्थ परमाणु या कण को मुक्त मूलक कहा जाता है।
आयनिक प्रतिक्रियाएँ ऐसी प्रक्रियाएँ हैं जिनमें सहसंयोजक बंधों का हेटेरोलिटिक दरार शामिल होता है, जब दोनों बंधित इलेक्ट्रॉन पहले से बंधे कणों में से एक के साथ रहते हैं:
हेटेरोलिटिक बंधन दरार के परिणामस्वरूप, आवेशित कण प्राप्त होते हैं: न्यूक्लियोफिलिक और इलेक्ट्रोफिलिक।
न्यूक्लियोफिलिक कण (न्यूक्लियोफाइल) एक ऐसा कण है जिसके बाहरी इलेक्ट्रॉन स्तर में इलेक्ट्रॉनों की एक जोड़ी होती है। इलेक्ट्रॉनों की एक जोड़ी के कारण, एक न्यूक्लियोफाइल एक नया सहसंयोजक बंधन बनाने में सक्षम होता है।
एक इलेक्ट्रोफिलिक कण (इलेक्ट्रोफाइल) एक ऐसा कण होता है जिसका बाहरी इलेक्ट्रॉन स्तर अधूरा होता है। एक इलेक्ट्रोफाइल उस कण के इलेक्ट्रॉनों के कारण एक सहसंयोजक बंधन के निर्माण के लिए अपूर्ण, रिक्त कक्षाएँ प्रस्तुत करता है जिसके साथ वह संपर्क करता है।
कार्बनिक रसायन विज्ञान में, सभी संरचनात्मक परिवर्तनों को प्रतिक्रिया में शामिल कार्बन परमाणु (या परमाणुओं) के सापेक्ष माना जाता है।
उपरोक्त के अनुसार, प्रकाश के प्रभाव में मीथेन के क्लोरीनीकरण को रेडिकल प्रतिस्थापन के रूप में वर्गीकृत किया गया है, एल्कीन में हैलोजन के योग को इलेक्ट्रोफिलिक जोड़ के रूप में, और एल्काइल हैलाइड के हाइड्रोलिसिस को न्यूक्लियोफिलिक प्रतिस्थापन के रूप में वर्गीकृत किया गया है।
प्रतिक्रियाओं के सबसे सामान्य प्रकार हैं:
रासायनिक प्रतिक्रियाओं के मूल प्रकार
मैं। प्रतिस्थापन प्रतिक्रियाएँ(एक या अधिक हाइड्रोजन परमाणुओं का हैलोजन परमाणुओं या एक विशेष समूह से प्रतिस्थापन) आरसीएच 2 एक्स + वाई → आरसीएच 2 वाई + एक्स
द्वितीय. अतिरिक्त प्रतिक्रियाएँ आरसीएच=सीएच 2 + एक्सवाई → आरसीएचएक्स−सीएच 2 वाई
तृतीय. उन्मूलन प्रतिक्रियाएं RCHX−CH 2 Y → RCH=CH 2 + XY
चतुर्थ. आइसोमेराइजेशन (पुनर्व्यवस्था) प्रतिक्रियाएं
वी ऑक्सीकरण प्रतिक्रियाएँ(वायुमंडलीय ऑक्सीजन या ऑक्सीकरण एजेंट के साथ बातचीत)
उपरोक्त प्रकार की प्रतिक्रियाओं में भी वे भेद करते हैं विशेषऔर निजीकृतप्रतिक्रियाएं.
विशिष्ट:
1)हाइड्रोजनीकरण (हाइड्रोजन के साथ अंतःक्रिया)
2) डिहाइड्रोजनीकरण (हाइड्रोजन अणु से उन्मूलन)
3) हैलोजनीकरण (हैलोजन के साथ अंतःक्रिया: एफ 2, सीएल 2, बीआर 2, आई 2)
4) डीहेलोजनेशन (हैलोजन अणु से उन्मूलन)
5) हाइड्रोहैलोजनेशन (हाइड्रोजन हैलाइड के साथ अंतःक्रिया)
6) डिहाइड्रोहैलोजनेशन (हाइड्रोजन हैलाइड अणु से उन्मूलन)
7) जलयोजन (अपरिवर्तनीय प्रतिक्रिया में पानी के साथ बातचीत)
8) निर्जलीकरण (पानी के अणु से विखंडन)
9) हाइड्रोलिसिस (प्रतिवर्ती प्रतिक्रिया में पानी के साथ बातचीत)
10) पोलीमराइजेशन (समान सरल यौगिकों से कई बढ़े हुए कार्बन कंकाल का उत्पादन)
11) पॉलीकंडेनसेशन (दो अलग-अलग यौगिकों से एक बहुविस्तारित कार्बन कंकाल प्राप्त करना)
12) सल्फोनेशन (सल्फ्यूरिक एसिड के साथ प्रतिक्रिया)
13) नाइट्रेशन (नाइट्रिक एसिड के साथ परस्पर क्रिया)
14) क्रैकिंग (कार्बन कंकाल की कमी)
15) पायरोलिसिस (कॉम्प्लेक्स का अपघटन)। कार्बनिक पदार्थउच्च तापमान के प्रभाव में सरल लोगों के लिए)
16) ऐल्किलेशन प्रतिक्रिया (सूत्र में एक ऐल्केन रेडिकल का परिचय)
17) एसाइलेशन प्रतिक्रिया (सूत्र में -C(CH 3)O समूह का परिचय)
18) सुगंधीकरण प्रतिक्रिया (कई एरेन्स के हाइड्रोकार्बन का निर्माण)
19) अणु से डीकार्बाक्सिलेशन प्रतिक्रिया (कार्बोक्सिल समूह -COOH का उन्मूलन)।
20) एस्टरीफिकेशन प्रतिक्रिया (एसिड के साथ अल्कोहल की अंतःक्रिया, या अल्कोहल से एस्टर का उत्पादन या कार्बोज़ाइलिक तेजाब)
21) "सिल्वर मिरर" प्रतिक्रिया (इंटरेक्शन के साथ)। अमोनिया सोल्यूशंससिल्वर(आई) ऑक्साइड)
नाममात्र प्रतिक्रियाएँ:
1) वर्ट्ज़ प्रतिक्रिया (हैलोजेनेटेड हाइड्रोकार्बन के साथ परस्पर क्रिया के दौरान कार्बन कंकाल का बढ़ना सक्रिय धातु)
2) कुचेरोव की प्रतिक्रिया (पानी के साथ एसिटिलीन की प्रतिक्रिया करके एल्डिहाइड का उत्पादन)
3) कोनोवलोव प्रतिक्रिया (पतला नाइट्रिक एसिड के साथ एक अल्केन की बातचीत)
4) वैगनर प्रतिक्रिया (सामान्य परिस्थितियों में थोड़ा क्षारीय या तटस्थ वातावरण में ऑक्सीकरण एजेंट के ऑक्सीजन द्वारा दोहरे बंधन के साथ हाइड्रोकार्बन का ऑक्सीकरण)
5) लेबेडेव प्रतिक्रिया (अल्काडिएन्स का उत्पादन करने के लिए अल्कोहल का निर्जलीकरण और निर्जलीकरण)
6) फ्रीडेल-क्राफ्ट्स प्रतिक्रिया (बेंजीन होमोलॉग प्राप्त करने के लिए क्लोरोअल्केन के साथ एरीन की क्षारीकरण प्रतिक्रिया)
7) ज़ेलिंस्की प्रतिक्रिया (डीहाइड्रोजनेशन द्वारा साइक्लोहेक्सेन से बेंजीन का उत्पादन)
8) किरचॉफ प्रतिक्रिया (सल्फ्यूरिक एसिड की उत्प्रेरक क्रिया के तहत स्टार्च का ग्लूकोज में रूपांतरण)
नगरपालिका बजटीय शैक्षणिक संस्थान
"माध्यमिक विद्यालय क्रमांक 19"
मिचुरिंस्क, ताम्बोव क्षेत्र
रासायनिक प्रतिक्रियाओं के प्रकार
अकार्बनिक रसायन शास्त्र
गोलोवकिना स्वेतलाना अलेक्जेंड्रोवना,
रसायन विज्ञान शिक्षक एमबीओयू माध्यमिक विद्यालय संख्या 19, मिचुरिंस्क
सामग्री
सार………………………………………………………………………….3
परिचय……………………………………………………………………4
परीक्षण विशिष्टता……………………………………………………5
परीक्षण 9वीं कक्षा……………………………………………………15
परीक्षण 11वीं कक्षा……………………………………………………………………24
सूचना संसाधन………………………………………………..33
एनोटेशन.
यह कार्य कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकारों का अध्ययन करने के लिए लेखकों के दृष्टिकोण को दर्शाता है। प्रस्तावित सामग्री बुनियादी और पूर्णकालिक में कार्यरत रसायन विज्ञान शिक्षकों के लिए रुचिकर हो सकती है माध्यमिक विद्यालय, क्योंकि यह कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकारों की बुनियादी अवधारणाओं का सामान्यीकरण प्रदान करता है, जो आपको जीआईए और एकीकृत राज्य परीक्षा की तैयारी करने और इस विषय पर सामग्री तैयार करने की अनुमति देगा।
परिचय।
कार्बनिक रसायन विज्ञान की सामग्री को समझना मुश्किल है, खासकर 9वीं कक्षा में, जहां इसके अध्ययन के लिए बहुत कम समय आवंटित किया जाता है, जिसमें बड़ी मात्रा में सैद्धांतिक सामग्री होती है। कार्बनिक रसायन विज्ञान पर प्रश्न राज्य विज्ञान अकादमी और एकीकृत राज्य परीक्षा के KIM में शामिल किए जाते हैं, जब छात्रों को अंतिम प्रमाणीकरण के लिए तैयार किया जाता है, तो शिक्षक को अक्सर इस सामग्री की गलतफहमी का सामना करना पड़ता है। आप सक्रिय रूप से उपयोग करके शिक्षण प्रक्रिया को तेज कर सकते हैं और कार्बनिक रसायन विज्ञान को आत्मसात करने की गुणवत्ता में सुधार कर सकते हैं आधुनिक प्रौद्योगिकियाँप्रशिक्षण, उदाहरण के लिए, आईसीटी, परीक्षण नियंत्रण प्रौद्योगिकियों का उपयोग। मैनुअल में, शिक्षक छोटी लेकिन जटिल सामग्री का अध्ययन करते समय अपने अनुभव साझा करते हैं।
राज्य परीक्षा और एकीकृत राज्य परीक्षा की तैयारी के लिए परीक्षणों की विशिष्टता
परीक्षण निर्धारित करना– रासायनिक प्रतिक्रियाओं के प्रकार के आधार पर छात्रों के सामान्य शैक्षिक प्रशिक्षण का मूल्यांकन करें।
परीक्षण सामग्री सामग्री की निरंतरता –अकार्बनिक और कार्बनिक रसायन विज्ञान की बुनियादी अवधारणाओं के बीच संबंध दिखाएं।
परीक्षण सामग्री की विशेषताएँ –परीक्षण नियंत्रण के प्रत्येक संस्करण में तीन भाग और कार्य होते हैं। जटिलता और प्रस्तुति के समान स्तर के कार्यों को कार्य के कुछ भागों में समूहीकृत किया जाता है।
भाग एइसमें 10 बहुविकल्पीय कार्य शामिल हैं बुनियादी स्तरकठिनाई A1, A2….A10
भाग बीबढ़े हुए कठिनाई स्तर B1, B2, B3 का उत्तर चुनने के लिए 3 कार्य शामिल हैं
पार्टसीइसमें 1 कार्य शामिल है जटिलता का उच्च स्तर.
तालिका 1 कार्य के भागों द्वारा कार्यों का वितरण।
बहु विकल्पीय प्रश्नअध्ययन की गई सामग्री के मुख्य भाग की जाँच करें: भाषा रसायन विज्ञान, रासायनिक बंधन, कार्बनिक पदार्थों के गुणों का ज्ञान, रासायनिक प्रतिक्रियाओं के प्रकार और स्थिति।
कठिनाई के बढ़े हुए स्तर के कार्यवे बढ़े हुए स्तर पर रेडॉक्स प्रतिक्रियाओं के बारे में ज्ञान का परीक्षण करते हैं। कार्य बहुविकल्पीय कार्य प्रदान करता है।
जटिलता के बढ़े हुए स्तर के कार्यों को पूरा करने से आप छात्रों को उनकी तैयारी के स्तर के अनुसार अलग कर सकते हैं और इस आधार पर उन्हें उच्च ग्रेड दे सकते हैं।
दीर्घ उत्तरीय प्रश्न- परीक्षण में सबसे कठिन. ये कार्य निम्नलिखित सामग्री तत्वों के आत्मसात का परीक्षण करते हैं: किसी पदार्थ की मात्रा, किसी पदार्थ का दाढ़ आयतन और दाढ़ द्रव्यमान, किसी विघटित पदार्थ का द्रव्यमान अंश।
4. परीक्षण की जा रही गतिविधियों की सामग्री, कौशल और प्रकार के अनुसार परीक्षण कार्यों का वितरण।
परीक्षण कार्यों की सामग्री का निर्धारण करते समय, रसायन विज्ञान पाठ्यक्रम में व्याप्त प्रत्येक सामग्री ब्लॉक की मात्रा को ध्यान में रखा गया था।
5. नेतृत्व समय
परीक्षण पूरा करने के लिए 45 मिनट आवंटित किए गए हैं (1 पाठ)
व्यक्तिगत कार्यों को पूरा करने के लिए आवंटित समय का अनुमानित वितरण:
भाग ए के प्रत्येक कार्य के लिए 2 मिनट तक।
भाग बी के प्रत्येक कार्य के लिए 5 मिनट तक।
भाग सी के प्रत्येक कार्य के लिए 10 मिनट तक।
6. व्यक्तिगत कार्यों और समग्र रूप से कार्य के लिए मूल्यांकन प्रणाली
भाग ए में प्रत्येक कार्य को सही ढंग से पूरा करने पर 1 अंक प्राप्त होता है।
भाग बी में प्रत्येक कार्य को सही ढंग से पूरा करने पर 2 अंक प्राप्त होते हैं;
उत्तर तत्वों में से एक में त्रुटि हुई - 1 अंक।
भाग सी में कार्यों का समापन परिवर्तनशील है, कार्य सी1 का सही और पूर्ण समापन - 4 अंक,
सभी कार्यों को पूरा करने के लिए छात्रों द्वारा प्राप्त अंकों का सारांश दिया गया है। रेटिंग पांच-बिंदु पैमाने पर दी जाती है।
7. मूल्यांकन का क्रम:
0% - 25% - "1" अंक से
26% - 50% - "2" अंक से प्राप्त किये गये
51% - 75% - "3" अंक से
76% - 85% - "4" अंक से
86% - 100% - "5" अंक से
कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकार
रासायनिक प्रतिक्रिया - यह पदार्थों में एक परिवर्तन है जिसमें पुराने रासायनिक बंधन टूट जाते हैं और कणों (परमाणु, आयन) के बीच नए रासायनिक बंधन बनते हैं जिनसे पदार्थ बनते हैं।
रासायनिक प्रतिक्रियाओं को वर्गीकृत किया गया है:
1. अभिकर्मकों और उत्पादों की संख्या और संरचना द्वारा
इस प्रकार की प्रतिक्रिया में आइसोमेराइजेशन प्रतिक्रियाएं शामिल हो सकती हैं, जो न केवल गुणात्मक, बल्कि पदार्थों के अणुओं की मात्रात्मक संरचना को भी बदले बिना होती हैं।![]()
कार्बनिक रसायन विज्ञान में अपघटन अभिक्रियाएँ, अपघटन अभिक्रियाओं के विपरीत अकार्बनिक रसायन शास्त्र, उनकी अपनी विशिष्टताएँ हैं। उन्हें जोड़ के विपरीत प्रक्रियाओं के रूप में माना जा सकता है, क्योंकि वे अक्सर कई बंधनों या चक्रों के निर्माण में परिणत होते हैं।
CH3-CH2-C=-CH CH3-C=-C-CH3
एथिल एसिटिलीन डाइमिथाइल एसिटिलीन



एक अतिरिक्त प्रतिक्रिया में प्रवेश करने के लिए, एक कार्बनिक अणु में एक एकाधिक बंधन (या चक्र) होना चाहिए, यह अणु मुख्य (सब्सट्रेट) होगा। उस स्थान पर एक सरल अणु (अक्सर एक अकार्बनिक पदार्थ, एक अभिकर्मक) जोड़ा जाता है जहां एकाधिक बंधन टूट जाता है या रिंग खुल जाती है। अधिकतर, एकाधिक बंधन या चक्र बनते हैं।![]()



![]()
उनकी विशिष्ट विशेषता बातचीत है साधारण पदार्थजटिल के साथ. कार्बनिक रसायन विज्ञान में "प्रतिस्थापन" की अवधारणा अकार्बनिक रसायन विज्ञान की तुलना में व्यापक है। यदि मूल पदार्थ के अणु में किसी परमाणु या कार्यात्मक समूह को किसी अन्य परमाणु या समूह द्वारा प्रतिस्थापित किया जाता है, तो ये भी प्रतिस्थापन प्रतिक्रियाएँ हैं।

विनिमय प्रतिक्रियाएँ जटिल पदार्थों के बीच होने वाली प्रतिक्रियाएँ हैं जिनमें उनके घटक भागों का स्थान विनिमय होता है। आमतौर पर इन प्रतिक्रियाओं को आयनिक माना जाता है। इलेक्ट्रोलाइट समाधानों में आयनों के बीच प्रतिक्रियाएं लगभग पूरी तरह से गैसों, वर्षा और कमजोर इलेक्ट्रोलाइट्स के निर्माण की ओर बढ़ती हैं।![]()

2. तापीय प्रभाव से
ऊष्माक्षेपी प्रतिक्रियाएँ ऊर्जा की रिहाई के साथ होती हैं।
इनमें लगभग सभी यौगिक प्रतिक्रियाएँ शामिल हैं।
प्रकाश के निकलने के साथ होने वाली ऊष्माक्षेपी प्रतिक्रियाओं को दहन प्रतिक्रियाओं के रूप में वर्गीकृत किया जाता है। एथिलीन का हाइड्रोजनीकरण ऊष्माक्षेपी अभिक्रिया का एक उदाहरण है। यह कमरे के तापमान पर चलता है.
ऊर्जा के अवशोषण के साथ एंडोथर्मिक प्रतिक्रियाएं होती हैं।
जाहिर है, लगभग हर कोई उनसे जुड़ाव महसूस करेगा अपघटन प्रतिक्रियाएँ,
सीएच 2 =सीएच 2 + एच 2 → सीएच 3 -सीएच 3

3. उत्प्रेरक के उपयोग के अनुसार
वे बिना उत्प्रेरक के चलते हैं।
चूँकि जीवित जीवों की कोशिकाओं में होने वाली सभी जैव रासायनिक प्रतिक्रियाएँ प्रोटीन प्रकृति के विशेष जैविक उत्प्रेरक - एंजाइमों की भागीदारी से होती हैं, वे सभी उत्प्रेरक या, अधिक सटीक रूप से, एंजाइमेटिक होते हैं।


4. दिशा से
वे एक साथ दो विपरीत दिशाओं में बहती हैं।
ऐसी अधिकांश प्रतिक्रियाएँ हैं।
कार्बनिक रसायन विज्ञान में, उत्क्रमणीयता का संकेत प्रक्रियाओं के नामों-विलोमों से परिलक्षित होता है:
हाइड्रोजनीकरण - निर्जलीकरण,
जलयोजन - निर्जलीकरण,
पोलीमराइजेशन - डीपोलीमराइजेशन।
सभी प्रतिक्रियाएँ प्रतिवर्ती हैंएस्टरीफिकेशन (विपरीत प्रक्रिया, जैसा कि आप जानते हैं, हाइड्रोलिसिस कहलाती है) और प्रोटीन हाइड्रोलिसिस, एस्टर, कार्बोहाइड्रेट, पॉलीन्यूक्लियोटाइड। इन प्रक्रियाओं की प्रतिवर्तीता एक जीवित जीव की सबसे महत्वपूर्ण संपत्ति - चयापचय को रेखांकित करती है।
इन परिस्थितियों में वे केवल एक ही दिशा में प्रवाहित होते हैं।
इनमें अवक्षेप, गैस या थोड़ा अलग करने वाले पदार्थ (पानी) के निर्माण के साथ होने वाली सभी विनिमय प्रतिक्रियाएं और सभी दहन प्रतिक्रियाएं शामिल हैं।
5. एकत्रीकरण की स्थिति के अनुसार
वे अभिक्रियाएँ जिनमें अभिकारक और प्रतिक्रिया उत्पाद एकत्रीकरण की विभिन्न अवस्थाओं (विभिन्न चरणों में) में होते हैं।
वे अभिक्रियाएँ जिनमें अभिकारक और प्रतिक्रिया उत्पाद एकत्रीकरण की एक ही स्थिति (एक ही चरण में) में होते हैं।


6. पदार्थ बनाने वाले रासायनिक तत्वों की ऑक्सीकरण अवस्था को बदलकर
रासायनिक तत्वों की ऑक्सीकरण अवस्थाओं को बदले बिना होने वाली अभिक्रियाएँ। इनमें शामिल हैं, उदाहरण के लिए, सभी आयन विनिमय प्रतिक्रियाएं, साथ ही कई जुड़ने वाली प्रतिक्रियाएं, कई अपघटन प्रतिक्रियाएं, एस्टरीफिकेशन प्रतिक्रियाएं
तत्वों की ऑक्सीकरण अवस्था में परिवर्तन के साथ होने वाली अभिक्रियाएँ। इनमें कई प्रतिक्रियाएं शामिल हैं, जिनमें सभी प्रतिस्थापन प्रतिक्रियाएं, साथ ही संयोजन और अपघटन की प्रतिक्रियाएं शामिल हैं जिनमें कम से कम एक साधारण पदार्थ शामिल होता है।
HCOOH + CH 3 OH → HCOOCH3 + H2O

7. प्रवाह तंत्र के अनुसार.
वे प्रतिक्रिया के दौरान बनने वाले रेडिकल्स और अणुओं के बीच जाते हैं।
जैसा कि आप पहले से ही जानते हैं, सभी प्रतिक्रियाओं में पुराने रासायनिक बंधन टूट जाते हैं और नए रासायनिक बंधन बनते हैं। प्रारंभिक पदार्थ के अणुओं में बंधन को तोड़ने की विधि प्रतिक्रिया के तंत्र (पथ) को निर्धारित करती है। यदि कोई पदार्थ सहसंयोजक बंधन से बनता है, तो इस बंधन को तोड़ने के दो तरीके हो सकते हैं: हेमोलिटिक और हेटेरोलिटिक। उदाहरण के लिए, अणुओं सीएल2, सीएच4 आदि के लिए, बंधनों के हेमोलिटिक दरार का एहसास होता है, इससे अयुग्मित इलेक्ट्रॉनों, यानी मुक्त कणों के साथ कणों का निर्माण होगा।
वे उन आयनों के बीच जाते हैं जो पहले से मौजूद हैं या प्रतिक्रिया के दौरान बने हैं।
विशिष्ट आयनिक प्रतिक्रियाएँ समाधान में इलेक्ट्रोलाइट्स के बीच परस्पर क्रिया होती हैं। आयन न केवल समाधानों में इलेक्ट्रोलाइट्स के पृथक्करण के दौरान बनते हैं, बल्कि विद्युत निर्वहन, हीटिंग या विकिरण के प्रभाव में भी बनते हैं। उदाहरण के लिए, Ŷ-किरणें पानी और मीथेन अणुओं को आणविक आयनों में परिवर्तित करती हैं।
अलग ढंग से आयनिक तंत्रएल्कीन में हाइड्रोजन हैलाइड, हाइड्रोजन, हैलोजन मिलाने की प्रतिक्रियाएं, अल्कोहल का ऑक्सीकरण और निर्जलीकरण, हैलोजन के साथ अल्कोहल हाइड्रॉक्सिल का प्रतिस्थापन होता है; एल्डिहाइड और एसिड के गुणों को दर्शाने वाली प्रतिक्रियाएं। इस मामले में, आयन ध्रुवीय सहसंयोजक बंधों के हेटरोलिटिक दरार से बनते हैं।

8. प्रतिक्रिया शुरू करने वाली ऊर्जा के प्रकार से।




इनकी शुरुआत उच्च ऊर्जा विकिरण से होती है - एक्स-रे, परमाणु विकिरण (Ý-किरणें, ए-कण - He2+, आदि)। विकिरण प्रतिक्रियाओं की सहायता से बहुत तेजी से रेडियोपॉलीमराइजेशन, रेडियोलिसिस (विकिरण अपघटन) आदि किए जाते हैं।
उदाहरण के लिए, बेंजीन से फिनोल के दो-चरणीय उत्पादन के बजाय, इसे विकिरण के प्रभाव में पानी के साथ बेंजीन की प्रतिक्रिया करके प्राप्त किया जा सकता है। इस मामले में, रेडिकल्स [·OH] और [·H·] पानी के अणुओं से बनते हैं, जिसके साथ बेंजीन प्रतिक्रिया करके फिनोल बनाता है:
C6H6 + 2[OH] -> C6H5OH + H20
रेडियोवल्केनाइजेशन का उपयोग करके रबर का वल्कनीकरण सल्फर के बिना किया जा सकता है, और परिणामस्वरूप रबर पारंपरिक से भी बदतर नहीं होगा
इनका आरंभ तापीय ऊर्जा से होता है। इनमें सभी एंडोथर्मिक प्रतिक्रियाएं और कई एक्सोथर्मिक प्रतिक्रियाएं शामिल हैं, जिनकी शुरुआत के लिए गर्मी की प्रारंभिक आपूर्ति की आवश्यकता होती है, यानी प्रक्रिया की शुरुआत।
इनका आरंभ प्रकाश ऊर्जा से होता है। एचसीएल संश्लेषण की फोटोकैमिकल प्रक्रियाओं या ऊपर चर्चा की गई क्लोरीन के साथ मीथेन की प्रतिक्रिया के अलावा, इनमें द्वितीयक वायुमंडलीय प्रदूषक के रूप में क्षोभमंडल में ओजोन का उत्पादन शामिल है।
पादप कोशिकाओं में होने वाली सबसे महत्वपूर्ण प्रक्रिया प्रकाश संश्लेषण भी इसी प्रकार की प्रतिक्रिया से संबंधित है।इनकी शुरुआत होती है बिजली. प्रसिद्ध इलेक्ट्रोलिसिस प्रतिक्रियाओं के अलावा, हम इलेक्ट्रोसिंथेसिस प्रतिक्रियाओं को भी इंगित करेंगे, उदाहरण के लिए, अकार्बनिक ऑक्सीकरण एजेंटों के औद्योगिक उत्पादन के लिए प्रतिक्रियाएं।
9वीं कक्षा के लिए परीक्षण कार्य
विकल्प 1।
भाग ए
ए1. कौन से मॉडल एल्केन अणुओं से मेल खाते हैं?

ए) ए को छोड़कर सब कुछ
बी) बी को छोड़कर सब कुछ
ग) बी को छोड़कर सब कुछ
घ) जी को छोड़कर सब कुछ
ए2. अल्केन्स किस अभिकर्मक के साथ प्रतिक्रिया कर सकते हैं:
ए) बीआर 2 (समाधान)
बी) सीएल 2 (प्रकाश)
ग) एच 2 एसओ 4
घ) NaOH
ए3. एचसीएल के साथ 1,3-ब्यूटाडीन की प्रतिक्रिया में नहीं बन सकता है
ए) 3-क्लोरोब्यूटीन-1 सी) 1-क्लोरोब्यूटीन-2
बी) 4-क्लोरोब्यूटेन-1 डी) 2,3-डाइक्लोरोब्यूटेन
ए4. वह पदार्थ जिसके साथ फॉर्मिक एसिड, उचित परिस्थितियों में, रेडॉक्स प्रतिक्रिया में प्रवेश करता है:
क) तांबा;
बी) कॉपर (II) हाइड्रॉक्साइड;
ग) कॉपर (II) क्लोराइड;
d) कॉपर (II) सल्फेट।
ए5. पानी के साथ एस्टर की अन्योन्यक्रिया को कहा जा सकता है:
क) जलयोजन;
बी) निर्जलीकरण;
ग) हाइड्रोलिसिस;
घ) हाइड्रोजनीकरण।
ए6. परिवर्तनों की श्रृंखला में
प्रतिक्रियाएँ "ए" और "बी" क्रमशः हैं:
क) जलयोजन और ऑक्सीकरण;
बी) ऑक्सीकरण और जलयोजन;
ग) जलयोजन और जलयोजन;
डी) ऑक्सीकरण और ऑक्सीकरण।
ए7. कार्बोनिल यौगिकों के अणुओं में दोहरे बंधन की उपस्थिति के कारण होने वाली प्रतिक्रिया है:
ए) परिग्रहण;
बी) अपघटन;
ग) प्रतिस्थापन;
घ) विनिमय।
ए8. सिल्वर ऑक्साइड के अमोनिया घोल का उपयोग करके इसे पहचानना असंभव है:
ए) इथेनॉल और इथेनॉल;
बी) प्रोपेनल और प्रोपेनोन;
ग) प्रोपेनल और ग्लिसरीन;
घ) ब्यूटेनल और 2-मिथाइलप्रोपेनल।
ए9. जब प्रोपेनल अतिरिक्त हाइड्रोजन के संपर्क में आता है, तो यह बनता हैमैं:
क) शराब सीमित करना;
बी) असंतृप्त शराब;
ग) असंतृप्त हाइड्रोकार्बन;
घ) संतृप्त हाइड्रोकार्बन।
ए10. एसीटैल्डिहाइडजलयोजन पर गठित:
ए) इथेन;
बी) एथीन;
ग) एटिना;
घ) इथेनॉल।
भाग बी
पहले में। समीकरण के साथ प्रतिक्रिया के प्रकार का मिलान करें
प्रतिक्रिया प्रकार
दो पर। 10.4 ग्राम वजन वाली एसिटिलीन में 14.6 ग्राम वजन वाला हाइड्रोजन क्लोराइड मिलाया गया। प्रतिक्रिया उत्पाद का सूत्र _____ है।
तीन बजे। 1 किलो वजन वाले तकनीकी कैल्शियम कार्बाइड से 260 लीटर (एनएस) की मात्रा वाला एसिटिलीन प्राप्त किया गया था। कैल्शियम कार्बाइड नमूने में निहित अशुद्धियों का द्रव्यमान अंश (% में) ____ है _____. (अपना उत्तर निकटतम सौवें भाग में लिखें)।
भाग सी.
सी 1. उन प्रतिक्रिया समीकरणों को लिखें जिनका उपयोग निम्नलिखित को पूरा करने के लिए किया जा सकता है
BaCl2
परिवर्तन: सी ओ
विकल्प 2।
भाग ए प्रत्येक कार्य A1-A10 के लिए चार उत्तर विकल्प दिए गए हैं,
जिनमें से केवल एक ही सही है। उत्तर संख्या पर गोला लगायें।
A1. अल्केन्स की प्रतिक्रिया विशेषता
ए) परिग्रहण
बी) प्रतिस्थापन
ग) जलयोजन
घ) विनिमय
ए2. कौन से हाइड्रोकार्बन पोलीमराइजेशन प्रतिक्रियाओं की विशेषता रखते हैं?
ए) सीएच
4बी) सी 2 एच 4
ग) सी 6 एच 6
घ) सी 2 एच 5 ओएच
ए3. एक पदार्थ जिसके साथ मीथेन विस्थापन प्रतिक्रिया से गुजरती है।
ए) सीएल 2 (प्रकाश)
बी) एच 2 ओ
ग) एच 2 एसओ 4
घ) NaOH
ए4. कौन सा पदार्थ पोटेशियम परमैंगनेट द्वारा आसानी से ऑक्सीकृत हो जाता है?
एसी 2 एच 6
बी) सी 2 एच 2
ग) सी 2 एच 5 ओएच
घ) सी 6 एच 6
ए5. कौन सा पदार्थ निर्जलीकरण प्रतिक्रिया के अधीन हो सकता है?
एसी 2 एच 4
बी) सी 2 एच 5 ओएच
ग) सीएच 4
घ) सी एच 3 सीओएच
ए6. परिवर्तनों की श्रृंखला में सी 2 एच 6 - एसिटिलीन - ईथेन प्रतिक्रियाएं "ए" और "बी" - यह मेल खाती है
ए) जलयोजन और हाइड्रोजनीकरण
बी) जलयोजन और ऑक्सीकरण
ग) डिहाइड्रोजनीकरण और हाइड्रोजनीकरण
घ) ऑक्सीकरण और जलयोजन
ए7. उस प्रतिक्रिया का क्या नाम है जो एस्टर उत्पन्न करती है?
ए) परिग्रहण
बी) प्रतिस्थापन
ग) एस्टरीफिकेशन
घ) अपघटन
ए8. जब एथिलीन पानी के साथ प्रतिक्रिया करता है तो बनता है।
ए) शराब को सीमित करना
बी) असंतृप्त अल्कोहल
ग) संतृप्त हाइड्रोकार्बन
घ) असंतृप्त हाइड्रोकार्बन
ए9. एसिटिक एसिड बनता है:
ए) इथेन
बी) एथीन
ग) एटिना
घ) इथेनॉल
ए10. वसा के लिए कौन सी प्रतिक्रिया विशिष्ट है?
ए) परिग्रहण
बी) ऑक्सीकरण
ग) हाइड्रोलिसिस
घ) प्रतिस्थापन
भाग बीकार्य B1 पूरा करते समय, पत्राचार स्थापित करें। Q2 और Q3, गणना करें और उत्तर लिखें।
पहले में। पदार्थ के साथ प्रतिक्रिया के प्रकार का मिलान करें
प्रतिक्रिया प्रकार
दो पर।पूर्ण दहन के लिए आवश्यक ऑक्सीजन की मात्रा 50 लीटर है। मीथेन (n.s.) ___l के बराबर है।
तीन बजे।हाइड्रोकार्बन में 16.28% हाइड्रोजन होता है। एक हाइड्रोकार्बन का सूत्र निर्धारित करें यदि हाइड्रोजन के लिए इसका वाष्प घनत्व 43 है।
भाग सी. कार्य C1 के उत्तर के लिए, एक अलग फॉर्म (शीट) का उपयोग करें
कार्य संख्या और उसका उत्तर लिखिए।
सी1. मात्रा की गणना करें कार्बन डाईऑक्साइड, 48 लीटर ऑक्सीजन में 56 लीटर मीथेन के दहन के दौरान जारी किया गया
जवाब
विकल्प 1
भाग ए
भाग बी
भाग सी
उन प्रतिक्रिया समीकरणों को लिखें जिनका उपयोग निम्नलिखित को पूरा करने के लिए किया जा सकता है BaCl 2
परिवर्तन: सी ओ 2 → Na 2 CO 3 → X → CO 2. दूसरी प्रक्रिया के लिए, प्रतिक्रिया के लिए एक आयनिक समीकरण लिखें।
उत्तर
विकल्प 2
भाग ए
ए 1
भाग बी
भाग सी
ग्रेड 11 के लिए परीक्षण कार्य
विकल्प 1।
भाग ए प्रत्येक कार्य A1-A10 के लिए चार उत्तर विकल्प दिए गए हैं,
जिनमें से केवल एक ही सही है। उत्तर संख्या पर गोला लगायें।
ए1. वर्ट्ज़ प्रतिक्रिया विवरण से मेल खाती है:
1. एसिटिलीन जलयोजन
2. कार्बन कंकाल का बढ़ाव
3. धातुओं के साथ नाइट्रो डेरिवेटिव की कमी अम्लीय वातावरण
4. इथेनॉल का एक साथ निर्जलीकरण और निर्जलीकरण
ए2. ग्लूकोज और सुक्रोज को इसके द्वारा अलग किया जा सकता है:
1. नाइट्रिक एसिड
2. सिल्वर ऑक्साइड का अमोनिया घोल
3. पानी
4. सोडियम हाइड्रॉक्साइड।
ए3. प्रतिक्रिया के माध्यम से एथिलीन से इथेनॉल का उत्पादन किया जा सकता है
1. जलयोजन
2. हाइड्रोजनीकरण
3.हैलोजनीकरण
4. हाइड्रोहैलोजनीकरण
ए4. सिल्वर ऑक्साइड के अमोनिया घोल के साथ प्रतिक्रिया की विशेषता है
1. प्रोपेनॉल-1
2. प्रस्तावना
3. प्रोपेनॉल-2
4. डाइमिथाइल ईथर
ए5. एथिल फॉर्मेट का क्षारीय जल अपघटन उत्पन्न करता है
1. फॉर्मेल्डिहाइड और इथेनॉल
2. फॉर्मिक एसिड और इथेनॉल
3. फॉर्मिक एसिड नमक और इथेनॉल
4. फॉर्मेल्डिहाइड और फॉर्मिक एसिड
ए6. कुचेरोव प्रतिक्रिया की एक विशिष्ट विशेषता पदार्थों की परस्पर क्रिया है
1. हाइड्रोजन के साथ
2. क्लोरीन के साथ
3. पानी के साथ
4. अम्ल के साथ
ए7. ज़िनिन प्रतिक्रिया, सुगंधित हाइड्रोकार्बन की विशेषता, का एक अलग नाम है
1. क्लोरीनीकरण
2. ब्रोमिनेशन
3. नाइट्रेशन
4. हाइड्रोजनीकरण
ए8. पॉलीहाइड्रिक अल्कोहल की गुणात्मक प्रतिक्रिया उनकी परस्पर क्रिया है
1. कॉपर ऑक्साइड के साथ (द्वितीय)
2. कॉपर हाइड्रॉक्साइड के साथ (द्वितीय)
3. तांबे के साथ
4. कॉपर ऑक्साइड के साथ (मैं)
ए9. इथेनॉल की प्रतिक्रिया के दौरान हाइड्रोक्लोरिक एसिडसल्फ्यूरिक अम्ल की उपस्थिति में बनता है
1. एथिलीन
2. क्लोरोइथेन
3. 1,2-डाइक्लोरोइथेन
4. विनाइल क्लोराइड
ए10. इथेनॉल के विपरीत, एसिटिक एसिड के साथ प्रतिक्रिया करता है
1. मैग्नीशियम
2. कॉपर हाइड्रॉक्साइड (द्वितीय)
3. ऑक्सीजन
4. हाइड्रोजन
भाग बी
उन्हें आरोही क्रम में लिखें
पहले में। रचना C 5 H 10 O 2 के एस्टर के हाइड्रोलिसिस के उत्पाद हो सकते हैं
1. पेंटानल और मेथनॉल
2. प्रोपेनोइक एसिड और इथेनॉल
3. इथेनॉल और ब्यूटेनल
4. ब्यूटेनोइक एसिड और मेथनॉल
5. एथेनोइक एसिड और प्रोपेनॉल
6. फॉर्मेल्डिहाइड और पेंटानॉल
दो पर। साथ चींटी का तेजाबइंटरैक्ट करना
1. ना 2 सीओ 3
2.एचसीएल
3.ओह
4.एच 2 एस
5. CuSO 4
6. घन(ओएच)2
तीन बजे। वे पदार्थ जिनके साथ α-एमिनोप्रोपेनोइक एसिड परस्पर क्रिया कर सकता है
1. ईथेन
2. पोटेशियम हाइड्रॉक्साइड
3. पोटैशियम क्लोराइड
4. सल्फ्यूरिक एसिड
5. डाइमिथाइल ईथर
6. हाइड्रोजन क्लोराइड
भाग सी. कार्य C1 के उत्तर के लिए, एक अलग फॉर्म (शीट) का उपयोग करें
कार्य संख्या और उसका उत्तर लिखिए।
सी1.प्रोपेन के उत्प्रेरक ऑक्सीकरण के परिणामस्वरूप, 55.5 ग्राम वजन वाला प्रोपियोनिक एसिड प्राप्त हुआ, प्रतिक्रिया उत्पाद उपज का द्रव्यमान अंश 60% है। ली गई प्रोपेन की मात्रा की गणना करें (संख्या)।
विकल्प 2
भाग ए प्रत्येक कार्य A1-A10 के लिए चार उत्तर विकल्प दिए गए हैं,
जिनमें से केवल एक ही सही है। उत्तर संख्या पर गोला लगायें।
ए1.सामान्य परिस्थितियों में प्रत्येक दो पदार्थ ब्रोमीन जल के साथ प्रतिक्रिया करते हैं:
1. बेंजीन और टोल्यूनि
2. साइक्लोहेक्सेन और प्रोपेन
3. एथिलीन और बेंजीन
4. फिनोल और एसिटिलीन
ए2. एथिलीन प्रतिक्रिया के परिणामस्वरूप बनता है:
1. एसिटिलीन जलयोजन
2. सोडियम के साथ क्लोरोमेथेन
3. हाइड्रोजन क्लोराइड के साथ एसिटिलीन
4. इथेनॉल निर्जलीकरण
ए3. प्रतिक्रिया द्वारा एथिलीन से इथेनॉल का उत्पादन किया जा सकता है
1. हाइड्रेशन
2. हाइड्रोजनीकरण
3. हैलोजनीकरण
4. हाइड्रोहैलोजनीकरण
ए4. एसिटिलीन ट्रिमराइजेशन प्रतिक्रिया के परिणामस्वरूप, निम्नलिखित बनता है:
1. हेक्सेन
2. हेक्सेन
3. एटैन
4. बेंजीन
ए5.सीएम के जलीय घोल के साथ एथिलीन के ऑक्सीकरण के दौराननहीं 4 बनता है:
1. एटैन
2. इथेनॉल
3. ग्लिसरॉल
4. इथाइलीन ग्लाइकॉल
ए6. 2-क्लोरोब्यूटेन का क्षारीय हाइड्रोलिसिस मुख्य रूप से उत्पन्न करता है:
1. ब्यूटेनॉल-2
2. ब्यूटेनॉल-1
3. ब्यूटेनल
4. ब्यूटेनोन
ए7. क्लोरीन के साथ प्रतिस्थापन प्रतिक्रिया में शामिल हैं:
1. ईथेन 2. एथिन 3 . ब्यूटेन 2 4. बुटान
ए8. पॉलीहाइड्रिक अल्कोहल के लिए एक विशिष्ट प्रतिक्रिया इनके साथ अंतःक्रिया है:
1. एच 2
2. घन
3. एजी 2 ओ (एनएच 3 समाधान)
4. घन(ओएच)2
ए9.लेबेडेव विधि का उपयोग करके कृत्रिम रबर के उत्पादन के लिए मोनोमर है:
1. ब्यूटेन 2
2. एटैन
3. ईथीलीन
4. ब्यूटाडीन-1,3
ए10.ब्यूटेनॉल-2 और पोटेशियम क्लोराइड की परस्पर क्रिया से बनते हैं:
1. 1-क्लोरोब्यूटेन और 2-क्लोरोब्यूटेन
2. 2-क्लोरोब्यूटेन और KOH का अल्कोहल घोल
3. 1-क्लोरोब्यूटेन और KOH का अल्कोहल घोल
4. 2-क्लोरोब्यूटेन और जलीय KOH घोल
भाग बी कार्य B1-B3 पूरा करते समय, तीन उत्तर विकल्प चुनें और
उन्हें आरोही क्रम में लिखें
पहले में। रचना C 6 H 12 O 2 के एस्टर के हाइड्रोलिसिस के उत्पाद हो सकते हैं
1 . इथेनल और डाइमिथाइल ईथर
2 . प्रोपेनोइक एसिड और प्रोपेनॉल
3 . मिथाइल एसीटेट और ब्यूटेन
4 . एथेनोइक एसिड और ब्यूटेनॉल
5. पेंटानोइक एसिड और मेथनॉल
6. प्रोपेनल और एथेनेडिओल
दो पर। अल्केन्स इनके साथ परस्पर क्रिया करते हैं:
1 . [ एजी(एनएच 3) 2 ]ओह
2 . H2O
3 . बीआर 2
4 . KMnO4(H+)
5 . Ca(OH)2
6 . घन(ओएच)2
तीन बजे। मिथाइलथाइलामाइन इसके साथ परस्पर क्रिया करता है:
1 . एटैन
2 . पोटेशियम हाइड्रोक्साइड
3. हाइड्रोब्रोमिक एसिड
4 . ऑक्सीजन
5 . प्रोपेन
6 . पानी
भाग सी. कार्य C1 के उत्तर के लिए, एक अलग फॉर्म (शीट) का उपयोग करें
कार्य संख्या और उसका उत्तर लिखिए।
सी1.जब पोटेशियम हाइड्रॉक्साइड के 7% घोल के 160 ग्राम को 9.0 ग्राम के साथ उबाला जाता है तो अमोनिया गैस निकलती है। अमोनियम क्लोराइड, 75 ग्राम पानी में घोला गया। परिणामी घोल में अमोनिया का द्रव्यमान अंश निर्धारित करें।
जवाब
विकल्प 1
भाग ए
ए 1
भाग बी
पहले में
भाग सी
सही उत्तर की सामग्री और मूल्यांकन के लिए निर्देश (उत्तर के अन्य शब्दों की अनुमति है जो इसके अर्थ को विकृत नहीं करते हैं)
प्रतिक्रिया तत्व:
1. प्रतिक्रिया समीकरण संकलित किया गया है
3सी 2 एच 2  सी 6 एच 6
सी 6 एच 6
2. एसिटिलीन और बेंजीन की मात्रा निर्धारित की गई
एन(सी 2 एच 2) = 10.08/22.4 = 0.45 मोल
प्रतिक्रिया समीकरण के अनुसारएन(सी 2 एच 2) : एन(सी 6 एच 6) =3:1
एन(सी 6 एच 6) = 0.45/3 = 0.15 मोल
3. बेंजीन के सैद्धांतिक द्रव्यमान की गणना की जाती है
एम(सी 6 एच 6) = 0.15 मोल * 78 ग्राम/मोल = 11.7 ग्राम
4. बेंजीन के व्यावहारिक द्रव्यमान की गणना की जाती है
एम(सी 6 एच 6) पीआर = 0.7 * 11.7 = 8.19 ग्राम
विकल्प 2
भाग ए
भाग बी
भाग सी
सी 1 1. जब पोटेशियम हाइड्रॉक्साइड के 7% घोल के 160 ग्राम को 9.0 ग्राम के साथ उबाला जाता है तो अमोनिया गैस निकलती है। अमोनियम क्लोराइड, 75 ग्राम पानी में घोला गया। परिणामी घोल में अमोनिया का द्रव्यमान अंश निर्धारित करें।
सही उत्तर और मूल्यांकन निर्देशों की सामग्री प्रतिक्रिया तत्व:- प्रतिक्रिया समीकरण तैयार किया गया है:
- घोल में क्षार पदार्थ का द्रव्यमान और मात्रा, साथ ही अमोनियम क्लोराइड पदार्थ की मात्रा की गणना की जाती है:
- घोल में जो पदार्थ अधिक मात्रा में है उसे दर्शाया गया है:
- घोल में अमोनिया का द्रव्यमान और उसका द्रव्यमान अंश निर्धारित किया गया
*टिप्पणी। यदि उत्तर में उत्तर तत्वों में से किसी एक में गणना में कोई त्रुटि है, जिसके कारण गलत उत्तर हुआ, तो कार्य पूरा करने का स्कोर केवल 1 अंक कम हो जाता है।
सूचनात्मक संसाधन.
आर्टेमेंको ए.आई. अद्भुत दुनियाकार्बनिक रसायन विज्ञान। - एम.: बस्टर्ड, 2004.
गेब्रियलियन ओ.एस., ओस्ट्रौमोव आई.जी. शिक्षक की पुस्तिका. रसायन विज्ञान। 10 वीं कक्षा। - एम.: बस्टर्ड, 2004।
कोरोशचेंको ए.एस., मेदवेदेव यू.एन. रसायन विज्ञान जीआईए मानक परीक्षण कार्य- एम.: "परीक्षा", 2009.
कुज़नेत्सोवा एन.ई., लेवकिना ए.एन., रसायन विज्ञान में समस्या पुस्तक, 9वीं कक्षा। - एम.: प्रकाशन केंद्र "वेंटाना - ग्राफ", 2004।
कुज़नेत्सोवा एन.ई., टिटोवा आई.एम., गारा एन.एन., झेगिन ए.यू. रसायन विज्ञान। - 9 वां दर्जा। - एम.: प्रकाशन केंद्र "वेंटाना - ग्राफ", 2002।
पोटापोव वी.एम. कार्बनिक रसायन विज्ञान। - एम.: शिक्षा, 1976.
एक युवा रसायनज्ञ का विश्वकोश शब्दकोश। - एम.: शिक्षाशास्त्र - प्रेस, 1997।
पिचुगिना जी.वी. रसायन विज्ञान और रोजमर्रा की जिंदगीव्यक्ति। - एम.: बस्टर्ड, 2005।
http://www.fipi.ru/
कार्बनिक पदार्थों की प्रतिक्रियाओं को औपचारिक रूप से चार मुख्य प्रकारों में विभाजित किया जा सकता है: प्रतिस्थापन, जोड़, उन्मूलन (उन्मूलन) और पुनर्व्यवस्था (आइसोमेराइजेशन)। यह स्पष्ट है कि कार्बनिक यौगिकों की प्रतिक्रियाओं की संपूर्ण विविधता को प्रस्तावित वर्गीकरण (उदाहरण के लिए, दहन प्रतिक्रियाएं) के ढांचे में कम नहीं किया जा सकता है। हालाँकि, इस तरह के वर्गीकरण से अकार्बनिक पदार्थों के बीच होने वाली प्रतिक्रियाओं के वर्गीकरण के साथ सादृश्य स्थापित करने में मदद मिलेगी जो पहले से ही अकार्बनिक रसायन विज्ञान के पाठ्यक्रम से परिचित हैं।
एक नियम के रूप में, मुख्य कार्बनिक मिश्रणप्रतिक्रिया में भाग लेने वाले को सब्सट्रेट कहा जाता है, और प्रतिक्रिया के अन्य घटक को पारंपरिक रूप से अभिकर्मक माना जाता है।
प्रतिस्थापन प्रतिक्रियाएँ
वे प्रतिक्रियाएँ जिनके परिणामस्वरूप मूल अणु (सब्सट्रेट) में एक परमाणु या परमाणुओं के समूह को अन्य परमाणुओं या परमाणुओं के समूहों के साथ प्रतिस्थापित किया जाता है, प्रतिस्थापन प्रतिक्रियाएँ कहलाती हैं।
प्रतिस्थापन प्रतिक्रियाओं में संतृप्त और सुगंधित यौगिक शामिल होते हैं, जैसे, उदाहरण के लिए, अल्केन्स, साइक्लोअल्केन्स या एरेन्स।
आइए हम ऐसी प्रतिक्रियाओं के उदाहरण दें।
प्रकाश के प्रभाव में, मीथेन अणु में हाइड्रोजन परमाणुओं को हैलोजन परमाणुओं द्वारा प्रतिस्थापित किया जा सकता है, उदाहरण के लिए, क्लोरीन परमाणु:
CH4 + Cl2→ CH3Cl + HCl
हाइड्रोजन को हैलोजन से बदलने का एक अन्य उदाहरण बेंजीन का ब्रोमोबेंजीन में रूपांतरण है:
लेखन के इस रूप के साथ, अभिकर्मकों, उत्प्रेरक और प्रतिक्रिया की स्थिति को तीर के ऊपर लिखा जाता है, और अकार्बनिक प्रतिक्रिया उत्पादों को इसके नीचे लिखा जाता है।
अतिरिक्त प्रतिक्रियाएँ
वे अभिक्रियाएँ जिनमें क्रियाशील पदार्थों के दो या दो से अधिक अणु मिलकर एक हो जाते हैं, योगात्मक अभिक्रियाएँ कहलाती हैं।
असंतृप्त यौगिक, जैसे कि एल्कीन या एल्काइन, योगात्मक प्रतिक्रियाओं से गुजरते हैं। इस पर निर्भर करते हुए कि कौन सा अणु अभिकर्मक के रूप में कार्य करता है, हाइड्रोजनीकरण (या कमी), हैलोजनीकरण, हाइड्रोहैलोजनेशन, जलयोजन और अन्य अतिरिक्त प्रतिक्रियाओं को प्रतिष्ठित किया जाता है। उनमें से प्रत्येक को कुछ शर्तों की आवश्यकता होती है।
1
. हाइड्रोजनीकरण - एकाधिक बंधन के माध्यम से हाइड्रोजन अणु के जुड़ने की प्रतिक्रिया:CH3-CH = CH2 + H2 → CH3-CH2-CH3
प्रोपेन प्रोपेन
2
. हाइड्रोहैलोजनीकरण - हाइड्रोजन हैलाइड योग प्रतिक्रिया (उदाहरण के लिए, हाइड्रोक्लोरिनेशन):CH2=CH2 + HCl → CH3-CH2-Cl
एथीन क्लोरोइथेन
3
. हैलोजनीकरण - हलोजन जोड़ प्रतिक्रिया (उदाहरण के लिए, क्लोरीनीकरण):CH2=CH2 + Cl2 → CH2Cl-CH2Cl
एथीन 1,2-डाइक्लोरोइथेन
4
. बहुलकीकरण - एक विशेष प्रकार की अतिरिक्त प्रतिक्रिया जिसमें छोटे आणविक भार वाले पदार्थ के अणु एक दूसरे के साथ मिलकर बहुत अधिक आणविक भार वाले पदार्थ के अणु बनाते हैं - मैक्रोमोलेक्यूल्स।पॉलिमराइजेशन प्रतिक्रियाएं
- ये एक कम-आणविक पदार्थ (मोनोमर) के कई अणुओं को एक बहुलक के बड़े अणुओं (मैक्रोमोलेक्यूल्स) में संयोजित करने की प्रक्रियाएं हैं।पोलीमराइज़ेशन प्रतिक्रिया का एक उदाहरण पराबैंगनी विकिरण और एक रेडिकल पोलीमराइज़ेशन सर्जक आर की कार्रवाई के तहत एथिलीन (एथीन) से पॉलीथीन का उत्पादन है।
कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकार
उन्मूलन प्रतिक्रियाएं
वे अभिक्रियाएँ जिनके परिणामस्वरूप मूल यौगिक के एक अणु से कई नए पदार्थों के अणुओं का निर्माण होता है, विलोपन या विलोपन अभिक्रियाएँ कहलाती हैं।
ऐसी प्रतिक्रियाओं के उदाहरणों में विभिन्न कार्बनिक पदार्थों से एथिलीन का उत्पादन शामिल है।

कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकार
उन्मूलन प्रतिक्रियाओं में विशेष महत्व हाइड्रोकार्बन के थर्मल विभाजन की प्रतिक्रिया है, जिस पर अल्केन्स का टूटना आधारित है - सबसे महत्वपूर्ण तकनीकी प्रक्रिया:

ज्यादातर मामलों में, मूल पदार्थ के एक अणु से एक छोटे अणु के टूटने से परमाणुओं के बीच एक अतिरिक्त एन-बंध का निर्माण होता है। उन्मूलन प्रतिक्रियाएँ कुछ शर्तों के तहत और कुछ अभिकर्मकों के साथ होती हैं। दिए गए समीकरण इन परिवर्तनों के केवल अंतिम परिणाम को दर्शाते हैं।
आइसोमेराइजेशन प्रतिक्रियाएं
वे अभिक्रियाएँ जिनके परिणामस्वरूप एक पदार्थ के अणु समान गुणात्मक और मात्रात्मक संरचना वाले, अर्थात समान आणविक सूत्र वाले अन्य पदार्थों के अणुओं से बनते हैं, आइसोमेराइजेशन प्रतिक्रियाएँ कहलाती हैं।
ऐसी प्रतिक्रिया का एक उदाहरण रैखिक अल्केन्स के कार्बन कंकाल का शाखित अल्केन्स में आइसोमेराइजेशन है, जो उच्च तापमान पर एल्यूमीनियम क्लोराइड पर होता है:
कार्बनिक रसायन विज्ञान में रासायनिक प्रतिक्रियाओं के प्रकार
1
. यह किस प्रकार की प्रतिक्रिया है:क) मीथेन से क्लोरोमेथेन का उत्पादन;
बी) बेंजीन से ब्रोमोबेंजीन प्राप्त करना;
ग) एथिलीन से क्लोरोइथेन का उत्पादन;
घ) इथेनॉल से एथिलीन का उत्पादन;
ई) ब्यूटेन का आइसोब्यूटेन में रूपांतरण;
च) इथेन डीहाइड्रोजनीकरण;
छ) ब्रोमोइथेन का इथेनॉल में रूपांतरण?
2
. कौन सी प्रतिक्रियाएँ विशिष्ट हैं: ए) अल्केन्स; बी) एल्केन्स? प्रतिक्रियाओं के उदाहरण दीजिए.3
. आइसोमेराइजेशन प्रतिक्रियाओं की विशेषताएं क्या हैं? किसी एक के एलोट्रोपिक संशोधन उत्पन्न करने वाली प्रतिक्रियाओं के साथ उनमें क्या समानता है रासायनिक तत्व? उदाहरण दो।4.
किन प्रतिक्रियाओं में (जोड़, प्रतिस्थापन, उन्मूलन, आइसोमेराइजेशन) मॉलिक्यूलर मास्समूल कनेक्शन:ए) बढ़ता है;
बी) घट जाती है;
ग) नहीं बदलता;
घ) क्या यह अभिकर्मक के आधार पर बढ़ता या घटता है?