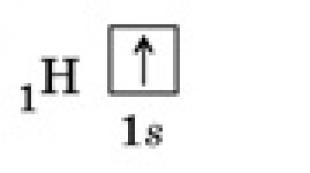
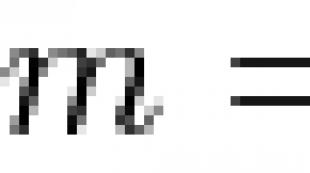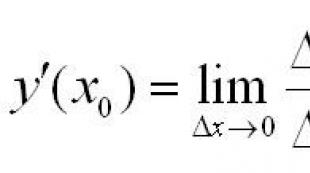रसायन विज्ञान की बुनियादी अवधारणाएँ और नियम। हीमोग्लोबिन का मोलर द्रव्यमान हीमोग्लोबिन आणविक भार
15. किसी दिए गए तापमान पर, 2 96 10 3 mol/g पदार्थ को कुछ अधिशोषक द्वारा 0.2 mol/l की सांद्रता वाले सर्फेक्टेंट घोल से अधिशोषित किया जाता है। यदि स्थिरांक 0 07 mol/l है, तो अधिशोषक की सोखने की क्षमता (mol/g में) निर्धारित करें।
[अवशोषक क्षमता 4 00 10 3 मोल/ग्राम]
16. फ्रायंडलिच समीकरण का उपयोग करके, यदि 1 ग्राम कोयला हो तो घोल में एसिटिक एसिड की संतुलन सांद्रता की गणना करें
17. जब एसीटोन को पानी में घोला जाता है तो अधिशोषण का प्रकार निर्धारित करें, यदि पानी में एसीटोन की सांद्रता 29 ग्राम/लीटर है, सतह
समाधान तनाव - 59 4 |
3 एन/एम, सतह तनाव |
||||||
पानी - 73 49 10 |
3 एन/एम, टी |
||||||
[अवशोषण सकारात्मक, |
6 मोल एम2] |
||||||
18. आइसोब्यूट्रिक एसिड घोल की सांद्रता 0.125 से 0.250 mol/l तक बढ़ने के साथ, इसकी सतह का तनाव 55.1 से घटकर 47.9 mN/m हो गया, और आइसोवालेरिक एसिड घोल की सांद्रता 43.2 से 35.0 mN/m हो गई। 293 K पर दी गई सांद्रता सीमा में पदार्थों के सोखने के मूल्यों की तुलना करें।
19. यदि निम्नलिखित प्रयोगात्मक डेटा ज्ञात हो, तो निर्धारित करें कि बढ़ती सांद्रता (T 298 K) के साथ जलीय घोल से सर्फेक्टेंट सोखने की मात्रा बढ़ती है या घटती है:
[समाधान में सर्फैक्टेंट सांद्रता बढ़ने के साथ सोखना 2 12 10 6 से बढ़कर 9 09 10 6 मोलम 2 हो जाता है]
20. प्रायोगिक डेटा (T 288 K) के अनुसार जलीय घोल से ब्यूटिरिक एसिड का सोखना बढ़ती सांद्रता के साथ कितनी बार बदलेगा:
सी 102, |
|||||
3 , एन/एम |

21. कैल्शियम क्लोराइड और सल्फ्यूरिक एसिड के 1% घोल को समान मात्रा में मिलाएं (घनत्व 1 ग्राम/एमएल के बराबर मानते हुए)। परिणामी कैल्शियम सल्फेट सॉल के मिसेल के सूत्र लिखिए।
[दाना ऋणात्मक रूप से आवेशित होता है]
22. 0.001 mol/l की सांद्रता वाले सिल्वर नाइट्रेट के घोल की कितनी मात्रा को cNaCl 0.002 mol/l वाले सोडियम क्लोराइड के 10 ml घोल में मिलाया जाना चाहिए ताकि एक सॉल प्राप्त हो सके जिसके कण धनात्मक रूप से आवेशित हों? सोल मिसेल की संरचना का एक आरेख लिखिए।
[ग्रेन्युल धनात्मक रूप से चार्ज है, AgNO3 घोल की मात्रा 0.02 लीटर से अधिक होनी चाहिए]
23. नकारात्मक रूप से आवेशित कणों वाला सॉल प्राप्त करने के लिए 0.003 mol/L की सांद्रता वाले मैंगनीज (II) क्लोराइड के 15 मिलीलीटर घोल में 0.001 mol/L की सांद्रता वाले अमोनियम सल्फाइड की कितनी न्यूनतम मात्रा मिलाई जानी चाहिए?
24. प्रशियन ब्लू Fe 4 Fe CN 6 3 का एक दाना विद्युत क्षेत्र में एनोड की ओर बढ़ता है। कौन सा पदार्थ स्टेबलाइज़र के रूप में कार्य करता है? मिसेल का सूत्र लिखिए।
[स्टेबलाइज़र - K4 Fe CN 6 ]
25. 0.03% NaCl घोल (1 ग्राम/मिली) के 100 मिलीलीटर में 0.001 श्री एग्नो 3 घोल का 250 मिलीलीटर मिलाया गया। ल्यूमिसेल सॉल का सूत्र लिखिए। निम्नलिखित में से कौन सा इलेक्ट्रोलाइट्स सबसे कम जमावट सीमा के साथ इस सॉल के जमाव का कारण बनेगा: KCl, Ba NO 3 2,
K2 CrO 4 , MgSO 4 , AlCl3 ?
[ग्रेन्युल नकारात्मक रूप से चार्ज होता है, इसलिए, कौयगुलांट आयन धनायन होते हैं। AlCl3 के लिए न्यूनतम जमावट सीमा]
26. K2 SiO 3 और HCl के विलयनों पर अभिक्रिया करके एक सिलिकिक अम्ल सॉल प्राप्त किया गया। सॉल मिसेल का सूत्र लिखें और निर्धारित करें कि यदि काउंटर विद्युत क्षेत्र में कैथोड में चले जाते हैं तो कौन सा इलेक्ट्रोलाइट्स अधिक मात्रा में था?
[अतिरिक्त K2 SiO 3 ]

27. 0.002 M AgNO3 घोल के 0.03 लीटर में 0.001 M FeCl 3 घोल की कितनी मात्रा मिलाई जानी चाहिए ताकि सिल्वर क्लोराइड सोल के कण विद्युत क्षेत्र में एनोड की ओर बढ़ें? मिसेलसोल का सूत्र लिखिए।
[FeCl3 की मात्रा 0.02 लीटर से अधिक होनी चाहिए]
28. सोडियम सल्फेट और पोटेशियम क्लोराइड के साथ आयरन (III) हाइड्रॉक्साइड हाइड्रोसोल की जमावट सीमा क्रमशः 0.32 और 20.50 mmol/l है। कोलाइडल सॉल कणों के आवेश का चिन्ह निर्धारित करें। इन इलेक्ट्रोलाइट्स की जमावट क्षमता की गणना करें और गणना किए गए शुल्ज़-हार्डी नियम के साथ उनके अनुपात की तुलना करें।
29. एक निश्चित सॉल के संबंध में इलेक्ट्रोलाइट्स की जमावट क्षमता निम्न क्रम में घटती है: NH 4 3 PO 4 NH 4 2 SO 4 NH 4 NO3। कोलाइडल कणों का आवेश चिन्ह क्या है? इलेक्ट्रोलाइट्स के उदाहरण दीजिए जिनकी स्कंदन क्षमता लगभग उपरोक्त के बराबर होगी।
[सोल कण धनात्मक रूप से आवेशित होते हैं, आयनों की स्कंदन क्षमता मुश्किल से कम होती है: PO 3 4 SO 2 4 NO 3 ]
30. मैग्नीशियम सल्फेट के साथ सॉल की जमावट सीमा नाइट्रेटोम्बेरियम की तुलना में कम है। सोल कण कैसे आवेशित होते हैं? हम पोटेशियम फॉस्फेट के साथ उसी सॉल के हेकोएग्यूलेशन के बारे में क्या कह सकते हैं?
31. 1.5 लीटर की मात्रा के साथ गोल्ड सल्फाइड सॉल का जमाव 0.2 मोल/लीटर की सांद्रता के साथ 570 मिलीलीटर सोडियम क्लोराइड समाधान के साथ हुआ। सोडियम आयन सॉल की जमावट सीमा की गणना करें।
32. सोल हाइड्रॉक्साइड और आयरन फॉस्फेट आयनों के जमाव की सीमा 0.37 mmol/l है। 750 मिली सॉल को जमाने के लिए 5% सोडियम फॉस्फेट घोल (105 ग्राम/मिली) की कितनी मात्रा की आवश्यकता होगी?
[Na 3 PO 4 घोल की मात्रा 0.87 मिली है]
33. 2-लीटर एल्यूमीनियम हाइड्रॉक्साइड सॉल का स्पष्ट जमाव तब हुआ जब K4 Fe CN 6 सांद्रता 0.01 mol/l के साथ 10.6 मिलीलीटर घोल मिलाया गया। हेक्सासायनोफेरेट आयनों द्वारा सॉल के जमाव के लिए सीमा की गणना करें; एल्युमिनियम हाइड्रॉक्साइड सोल मिसेलस का सूत्र लिखिए।
34. कैल्शियम आयनों के साथ गोल्ड सल्फाइड सॉल के जमाव की सीमा 0.69 mmol/l है। 100 मिलीलीटर सॉल को जमाने के लिए 0.5 mol/l की कैल्शियम क्लोराइड सांद्रता वाले घोल की कितनी मात्रा की आवश्यकता होती है?
[CaCl2 विलयन का आयतन 0 15 10 3 लीटर है]
35. सोल के कोलाइडल कणों के चार्ज का संकेत निर्धारित करें यदि इलेक्ट्रोलाइट्स के साथ इसके जमाव के दौरान निम्नलिखित जमावट थ्रेशोल्ड (एमएमओएल / एल में) प्राप्त होते हैं: सी पीसी KNO3 300; सी पीसी एमजीसीएल2 320; सी पीसी Na3 PO4 0 6.
[सकारात्मक]
36. Na2 SO4 या MgCl2 में से किस इलेक्ट्रोलाइट्स में 0.01 mol/l के पोटेशियम आयोडाइड सांद्रण वाले घोल और 0.015 mol/l के सिल्वर नाइट्रेट सांद्रण वाले घोल के बराबर मात्रा में मिश्रण से प्राप्त सिल्वर आयोडाइड सॉल के लिए अधिक स्कंदन क्षमता होगी। मैं?
[Na2SO4 की स्कंदन क्षमता अधिक है]
37. 10 मिलीलीटर AgI के ऋणावेशित सॉल को जमा देने के लिए, 1 mol/l की KNO3 सांद्रता वाले घोल का 1.5 ml या 0.1 mol/l की Ca NO3 2 सांद्रता वाले घोल का 0.5 ml या 0.2 ml का Ca NO3 2 सांद्रण वाला घोल लें। 0.01 mol/l की Al NO3 सांद्रता वाले घोल की आवश्यकता होती है। क्या नियम c p 1 z 6 सत्य है?
[नियम लगभग लागू किया जाता है]
38. KAuO2 द्वारा स्थिर सोने के सॉल के मिसेल का सूत्र लिखिए। किस इलेक्ट्रोलाइट - NaCl, BaCl2, FeCl3 - की जमावट सीमा कम होगी?
[FeCl3 के मामले में जमावट सीमा कम है]
39. 22 Æ C पर जैतून के तेल का घनत्व 960 kg m3 है, और इस तापमान पर पानी का घनत्व 996 kg m3 है। एक विस्कोमीटर से जैतून का तेल 21 मिनट 15.6 सेकंड में और उतनी ही मात्रा में पानी प्रवाहित होता है
पानी 22 एच2 ओ 9 58 10 4 एन एस एम2। |
||
[जैतून के तेल की चिपचिपाहट 841 3 |
10 4 एन एस एम2 ] |
|
40. केरोसिन की श्यानता 20 पर |
Æ C 1 8 के बराबर है |
10 3 पास, और विज़- |
समान परिस्थितियों में पानी की हड्डी - 1 005 10 |
3 Pa s (N s m2)। |
|
मिट्टी के तेल का घनत्व निर्धारित करें यदि यह ज्ञात हो कि विस्कोमीटर से मिट्टी के तेल के प्रवाह का समय 53 s है, और पानी की समान मात्रा 24 s है। जल का घनत्व 998 kg m3 है।
[मिट्टी के तेल का घनत्व 809 4 किग्रा घन मीटर है]
41. 0.1 मोल/लीटर सोडियम एसीटेट सांद्रण वाले 100 मिली घोल और 0.2 मोल/लीटर एसिटिक एसिड सांद्रण वाले 25 मिली घोल से तैयार एसीटेट बफर में वैद्युतकणसंचलन के दौरान प्रोटीन कण pI 4 0) किस इलेक्ट्रोड में चले जाएंगे /एल?
[इस बफर समाधान में प्रोटीन नकारात्मक रूप से चार्ज होता है और इलेक्ट्रोफोरेसिस के दौरान एनोड में चला जाता है]
42. घोल में प्रोटीन का मिश्रण होता है: ग्लोब्युलिन (पीआई 7), एल्ब्यूमिन (पीआई 4 9) और कोलेजन (पीआई 4 0)। किस pH मान पर इन प्रोटीनों को इलेक्ट्रोफोरेटिक रूप से अलग किया जा सकता है?
[प्रोटीन को पीएच 4-9 पर इलेक्ट्रोफोरेटिक रूप से अलग किया जा सकता है]
43. यदि पीआई 4 और पीएच 5 है तो इलेक्ट्रोफोरेसिस के दौरान प्रोटीन कण किस इलेक्ट्रोड की ओर बढ़ेंगे?
[प्रोटीन कण एनोड की ओर बढ़ेंगे]
44. हीमोग्लोबिन pI 6 68 को 1 5 10 6 mol/l की हाइड्रोजन आयन सांद्रता वाले बफर समाधान में रखा गया था। वैद्युतकणसंचलन के दौरान हीमोग्लोबिन अणुओं की गति की दिशा निर्धारित करें। यह ज्ञात है कि लाल रक्त कोशिकाओं में पीएच 7 25 है। इस पीएच मान पर हीमोग्लोबिन अणुओं पर क्या चार्ज होता है।
[हीमोग्लोबिन अणु कैथोड की ओर बढ़ेंगे; पीएच 7 पर 25 हीमोग्लोबिन अणुओं पर ऋणात्मक आवेश होता है]
45. शारीरिक तापमान पर 1 किलो m3 की द्रव्यमान सांद्रता वाले जलीय प्रोटीन घोल का आसमाटिक दबाव 292.7 Pa है। औसत दाढ़ द्रव्यमान से प्रोटीन का आणविक द्रव्यमान निर्धारित करें (प्रोटीन अणु आइसोडायमेट्रिक है)।
[सापेक्ष आणविक भार 87,940 है]
46. 25 सेंट्रेशन पर औसत आसमाटिक दबाव की गणना करें - 4,176 किलोग्राम एम3;
पॉलीस्टाइनिन का दाढ़ द्रव्यमान, यदि Æ C 120.9 Pa के बराबर है, और द्रव्यमान con- 1 Pa m6 kg2 है।
47. क्या जिलेटिन (पीआई 4 7) 0 Æ सी पर घटकों की समान सामग्री के साथ एसीटेट बफर में फूल जाएगा? आप जिलेटिन की सूजन प्रक्रिया की पहचान कैसे कर सकते हैं? अपना जवाब समझाएं।
[आइसोइलेक्ट्रिक बिंदु के पास सूजन न्यूनतम है]
48. जब 200 ग्राम वजनी रबर फूला, तो 964 मिलीलीटर क्लोरोफॉर्म (1 9 ग्राम मिलीलीटर) अवशोषित हो गया। रबर की सूजन की डिग्री और परिणामी जेली की प्रतिशत संरचना की गणना करें।
[915 8%; रबर 9 84%; क्लोरोफॉर्म 90 16%]
49. बहुलक के औसत दाढ़ द्रव्यमान की गणना करें यदि इसकी विशिष्ट श्यानता 0 126 m3 kg, स्थिरांक K 5 10 5, 0 67 है।
50. 0.0025 mol/kg के बराबर मोलल सांद्रता वाला घोल तैयार करने के लिए पॉलिमर का कितना द्रव्यमान लिया जाना चाहिए,
यदि विलायक का द्रव्यमान 1.5 किग्रा है? मोनोमर का दाढ़ द्रव्यमान 100 ग्राम/मोल है। पोलीमराइजेशन की डिग्री - 100।
51. 5 और 3 के समविद्युत बिंदु वाले दो एंजाइमों को किस pH मान पर वैद्युतकणसंचलन द्वारा अलग किया जाना चाहिए? pH 4.6 वाले विलयन में एंजाइम कण कैसे आवेशित होते हैं?
और 7.9?
[पीएच 4 पर अलग किया जाना चाहिए; pH 4 6 " " और " " पर, pH 7 9 " " और " " पर चार्ज]
52. विस्कोमेट्रिक विधि से निम्नलिखित डेटा का उपयोग करके पॉलीमेथाइल मेथैक्रिलेट का दाढ़ द्रव्यमान निर्धारित करें:
एकाग्रता |
||||||
समाधान, किग्रा एम3 |
||||||
चिपचिपाहट कम हो गई |
||||||
आईयूडी समाधान |
||||||
बेंजीन में |
स्थिरांक: के
105 ] |
53. कुछ बीएमसी का दाढ़ द्रव्यमान 600,000 है। यदि पदार्थ का द्रव्यमान सांद्रण 6 ग्राम/लीटर है तो घोल का दाढ़ सांद्रण क्या है? 27 पर ऐसे घोल का आसमाटिक दबाव क्या है?Æ सी?
54. 1 लीटर घोल में 5 ग्राम एमाइलोज होता है। ऐसे घोल का आसमाटिक दबाव 27 पर हैÆ C 0.15 मिमी Hg के बराबर है। कला। एमाइलोज़ के दाढ़ द्रव्यमान की गणना करें।
55. 0.1 mol/L की PrtCl सांद्रता वाला एक प्रोटीन घोल झिल्ली के एक तरफ रखा जाता है, और 0.2 mol/L की सोडियम क्लोराइड सांद्रता वाला एक घोल दूसरी तरफ रखा जाता है। संतुलन स्थापित होने पर झिल्ली के दोनों किनारों पर क्लोराइड की सांद्रता की गणना करें।
56. जिलेटिन की स्वर्ण संख्या निर्धारित करने के लिए, 1% जिलेटिन समाधान का 0.1 मिलीलीटर 9.9 मिलीलीटर लाल सोने के सोल में जोड़ा गया था। फिर मूल समाधान 1 2 के 10 क्रमिक तनुकरणों की एक श्रृंखला की गई और प्रत्येक परखनली में 1 मिलीलीटर जोड़ा गया 10%
सोडियम क्लोराइड घोल. पहले पांच टेस्ट ट्यूबों में, कोई बदलाव नहीं देखा गया, लेकिन 6-10 टेस्ट ट्यूबों में घोल ने नीले रंग का रंग प्राप्त कर लिया। स्वर्णिम संख्या क्या है?
57. 2.5 kg m द्रव्यमान सांद्रता वाले जिलेटिन के जलीय घोल के 293 K पर आसमाटिक दबाव निर्धारित करें 3 .
जिलेटिन का दाढ़ द्रव्यमान 104,600 है, और गुणांक
0 69 पा एम6 |
किलो 2. |
58. डिफेनिलफॉर्मामाइड घोल में विभिन्न सांद्रता पर पॉलीएक्रिलोनिट्राइल का आणविक भार 293 K पर 75,000 और 39,100 है, और आंतरिक चिपचिपाहट क्रमशः 0.299 और 0.110 है। मार्क-हाउविंक समीकरण में गुणांक और K निर्धारित करें।
59. प्युलुलेंट मैनिंजाइटिस का निदान करते समय, मस्तिष्कमेरु द्रव प्रोटीन की सुरक्षात्मक संख्या निर्धारित की जाती है। इस संख्या की गणना करें यदि यह ज्ञात हो कि NaNO के द्रव्यमान अंश वाले 2 मिलीलीटर घोल की क्रिया के तहत 20 मिलीलीटर AgBr सॉल के जमाव को रोकने के लिए 3 10% इस सोल में 1 लीटर में 2 ग्राम प्रोटीन युक्त 3 मिलीलीटर मस्तिष्कमेरु द्रव मिलाने की आवश्यकता है।
60. आइसो-इक्लेक्टिक अवस्था में 26 ग्राम/लीटर हीमोग्लोबिन वाले घोल का आसमाटिक दबाव 0.0117 ग्राम/लीटर सोडियम क्लोराइड वाले घोल के आसमाटिक दबाव के बराबर होता है। घोल का घनत्व 1 ग्राम/मिलीलीटर, तापमान 25 के बराबर लेंÆ सी, वान्ट हॉफ के नियम से विचलन की उपेक्षा की जा सकती है। हीमोग्लोबिन के आणविक (दाढ़) द्रव्यमान की गणना करें।
आवेदन
1. बुनियादी भौतिक स्थिरांक
अवोगाद्रो स्थिरांक, एन ए 6 02 1023 मोल 1। सार्वभौमिक गैस स्थिरांक, आर 8 31 जे मोल
बोल्ट्ज़मान स्थिरांक, k R N A 1 38 10 23 J K. गैस का सामान्य दाढ़ आयतन, V 0 22 4 l mol। प्लैंक स्थिरांक, h 6 63 10 34 J s.
2. दशमलव गुणकों और फ्रेमवर्क इकाइयों और उनके पदनामों के निर्माण के लिए कारक और प्राथमिकताएँ
कारक, |
कारक, |
||||||
जिस पर |
जिस पर |
||||||
गुणा |
गुणा |
||||||
मुख्य |
मुख्य |
||||||
1012 |
|||||||
| मीटर | |||||||
किलोग्राम |
|||||||
विद्युत धारा की शक्ति |
|||||||
थर्मोडायनामिक तापमान |
|||||||
पदार्थ की मात्रा |
|||||||
व्युत्पन्न मात्राएँ |
स्थान और समय |
||||||
वर्ग मीटर |
|||||||
घन मापी |
|||||||
रफ़्तार |
मीटर प्रति सेकंड |
||||||
यांत्रिक व्युत्पन्न |
और थर्मल मात्रा |
||||||
घनत्व |
किलोग्राम प्रति |
किग्रा एम3 |
|||||
घन मापी |
|||||||
ताकत, वजन |
|||||||
दबाव |
|||||||
ऊर्जा, कार्य, ऊष्मा की मात्रा, |
|||||||
थर्मोडायनामिक क्षमता |
|||||||
एन्ट्रापी |
जूल प्रति केल्विन |
||||||
विद्युत व्युत्पन्न |
और चुंबकीय मात्रा |
||||||
बिजली की मात्रा |
|||||||
थर्मोडायनामिक क्षमता |
|||||||
विद्युत वोल्टेज |
|||||||
विद्युतीय संभाव्यता, |
|||||||
वैद्युतवाहक बल |
|||||||
विद्युतीय प्रतिरोध |
|||||||
प्रोटीन पदार्थों का सबसे महत्वपूर्ण वर्ग है जो जीवित जीवों को बनाते हैं। कई प्रोटीन उत्प्रेरक के रूप में कार्य करते हैं। हीमोग्लोबिन फेफड़ों से ऊतकों तक ऑक्सीजन भी पहुंचाता है।
25-1. हीमोग्लोबिन का दाढ़ द्रव्यमान g/mol है। लाल रक्त कोशिकाओं में औसत हीमोग्लोबिन सामग्री 15 ग्राम/100 मिली है। रक्त में हीमोग्लोबिन (एम) की दाढ़ सांद्रता निर्धारित करें।
25-3. हेनरी का नियम इस प्रकार बताया गया है:
घुलनशीलता = कГ´ आंशिक दबाव ( कजी - हेनरी स्थिरांक)
ऑक्सीजन के लिए हेनरी स्थिरांक 1.3 x 10 –3 mol/l/atm है। हवा के साथ संतुलन में पानी में दो ऑक्सीजन अणुओं के बीच औसत दूरी का अनुमान लगाएं।
25-4. एक हीमोग्लोबिन अणु चार ऑक्सीजन अणुओं को बांध सकता है। ऑक्सीजन युक्त रक्त में दो ऑक्सीजन अणुओं के बीच औसत दूरी का अनुमान लगाएं। परिणाम की तुलना प्रश्न 25-2 और 25-3 के उत्तर से करें। ऑक्सीजन को केंद्रित करने और इसे ऊतकों तक पहुंचाने के संदर्भ में हीमोग्लोबिन की प्रभावशीलता के बारे में निष्कर्ष निकालें जहां ऑक्सीजन का आंशिक दबाव कम है।
25-6. हीमोग्लोबिन अणु में कितने विभिन्न अमीनो एसिड होते हैं?
25-7. ट्रिप्सिन लाइसिन और आर्जिनिन के कार्बोक्सिल समूहों द्वारा गठित पेप्टाइड बांड को हाइड्रोलाइज करता है। उदाहरण के लिए, नीचे दिया गया पेप्टाइड
ट्रिप्सिन की क्रिया के बाद, यह निम्नलिखित पेप्टाइड्स में टूट जाता है:
हीमोग्लोबिन को डाइसल्फ़ाइड बांड और एल्किलेशन में कमी के अधीन किया गया था, और फिर ट्रिप्सिन की कार्रवाई के तहत पूर्ण हाइड्रोलिसिस किया गया था। हाइड्रोलिसिस उत्पादों में कितने अमीनो एसिड अवशेष (औसतन) शामिल होंगे?
हीमोग्लोबिन का दाढ़ द्रव्यमान
हीमोग्लोब आई एन (एचबी) (से हेमो. और अव्यक्त. ग्लोबस - बॉल), मनुष्यों, कशेरुकियों और कुछ अकशेरुकी जीवों के रक्त में एक लाल लौह युक्त वर्णक; शरीर में यह श्वसन अंगों से ऊतकों तक ऑक्सीजन (O2) पहुंचाने का कार्य करता है; ऊतकों से श्वसन अंगों तक कार्बन डाइऑक्साइड के स्थानांतरण में भी महत्वपूर्ण भूमिका निभाता है। अधिकांश अकशेरुकी जीवों में, ग्लिसरीन रक्त में स्वतंत्र रूप से घुल जाता है; कशेरुक और कुछ अकशेरुकी जीवों में यह लाल रक्त कोशिकाओं - एरिथ्रोसाइट्स में पाया जाता है, जो उनके सूखे अवशेषों का 94% तक होता है। एरिथ्रोसाइट्स में शामिल गैस का दाढ़ द्रव्यमान लगभग, प्लाज्मा में घुला हुआ होता है - तक। रासायनिक प्रकृति के अनुसार जी. एक जटिल प्रोटीन है - क्रोमोप्रोटीन , प्रोटीन ग्लोबिन और लौह पोर्फिरिन - हेम से मिलकर। उच्चतर जानवरों और मनुष्यों में, रक्त में लगभग 17,000 के दाढ़ द्रव्यमान के साथ 4 मोनोमर सबयूनिट होते हैं; दो मोनोमर्स में से प्रत्येक में 141 अमीनो एसिड अवशेष होते हैं ( ए-श्रृंखला), अन्य दो - 146 अवशेष प्रत्येक ( बी-जंजीरें)।
इन पॉलीपेप्टाइड्स की स्थानिक संरचनाएँ काफी हद तक समान हैं। वे विशिष्ट "हाइड्रोफोबिक पॉकेट" बनाते हैं जिसमें हीम अणु स्थित होते हैं (प्रत्येक सबयूनिट के लिए एक)। हीम में शामिल लौह परमाणु के 6 समन्वय बंधों में से 4 पाइरोल रिंगों के नाइट्रोजन की ओर निर्देशित होते हैं; 5वां हिस्टिडाइन के इमिडाज़ोल रिंग के नाइट्रोजन से जुड़ा है, जो पॉलीपेप्टाइड्स से संबंधित है और 87वें स्थान पर स्थित है ए-चेन और 92वें स्थान पर बी-जंजीरें; छठा बंधन पानी के अणु या ऑक्सीजन सहित अन्य समूह (लिगैंड्स) की ओर निर्देशित होता है। उपइकाइयाँ हाइड्रोजन, नमक और अन्य गैर-सहसंयोजक बंधों द्वारा एक-दूसरे से शिथिल रूप से जुड़ी हुई हैं और मुख्य रूप से सममित डिमर के गठन के साथ एमाइड्स और बढ़ी हुई नमक सांद्रता के प्रभाव में आसानी से अलग हो जाती हैं ( ए बी) और आंशिक रूप से ए-और बी-मोनोमर्स. गैस अणु की स्थानिक संरचना का अध्ययन एक्स-रे विवर्तन विश्लेषण (एम. पेरुत्स, 1959) द्वारा किया गया था।
अमीनो एसिड का क्रम ए-और बी-कई उच्चतर जानवरों और मनुष्यों में जी की श्रृंखलाओं को पूरी तरह से स्पष्ट कर दिया गया है। टेट्रामर में इकट्ठे किए गए हीम अणु में, सभी 4 हीम अवशेष सतह पर स्थित होते हैं और O2 के साथ प्रतिक्रियाएं आसानी से पहुंच योग्य होती हैं। O 2 का योग हीम में Fe 2+ परमाणु की सामग्री द्वारा सुनिश्चित किया जाता है। यह प्रतिक्रिया प्रतिवर्ती है और O2 के आंशिक दबाव (तनाव) पर निर्भर करती है। फेफड़ों की केशिकाओं में, जहां O 2 वोल्टेज लगभग 100 है एमएमएचजी. कला।, G. O 2 (ऑक्सीकरण प्रक्रिया) के साथ जुड़कर ऑक्सीजन युक्त G. - ऑक्सीजन युक्त हीमोग्लोबिन में बदल जाता है। ऊतक केशिकाओं में, जहां O2 तनाव काफी कम होता है (लगभग)। 40 मिमी एचजी. कला।), ऑक्सीहीमोग्लोबिन का हीमोग्लोबिन और O2 में पृथक्करण होता है; उत्तरार्द्ध अंगों और ऊतकों की कोशिकाओं में प्रवेश करता है, जहां O 2 का आंशिक दबाव और भी कम होता है (5-20)। एमएमएचजी. सेमी।); कोशिकाओं के भीतर गहराई में यह लगभग शून्य हो जाता है। हीमोग्लोबिन में O 2 का जुड़ना और ऑक्सीहीमोग्लोबिन का हीमोग्लोबिन और O 2 में पृथक्करण हीमोग्लोबिन अणु में गठनात्मक (स्थानिक) परिवर्तनों के साथ-साथ डिमर्स और मोनोमर्स में इसके प्रतिवर्ती अपघटन के साथ होता है, जिसके बाद टेट्रामर्स में एकत्रीकरण होता है।
O 2 और अन्य गुणों के साथ प्रतिक्रिया करने पर गैस के गुण बदल जाते हैं: ऑक्सीजन युक्त गैस गैस की तुलना में 70 गुना अधिक मजबूत एसिड होती है, जो ऊतकों में बंधने और CO 2 को फेफड़ों में छोड़ने में बड़ी भूमिका निभाती है। स्पेक्ट्रम के दृश्य भाग में अवशोषण बैंड की विशेषता है: जी में एक अधिकतम (554 पर) है एमएमके), ऑक्सीजन युक्त गैस के दो मैक्सिमा 578 और 540 हैं एमएमके. जी. सीओ 2 को सीधे जोड़ने में सक्षम है (ग्लोबिन के एनएच 2-समूहों के साथ सीओ 2 की प्रतिक्रिया के परिणामस्वरूप); इस मामले में, कार्बेमोग्लोबिन बनता है - एक अस्थिर यौगिक जो फेफड़ों की केशिकाओं में हीमोग्लोबिन और सीओ 2 में आसानी से विघटित हो जाता है।
मानव रक्त में जी. की मात्रा औसतन 13-16 होती है जी%(या साली के अनुसार 78%-96%); महिलाओं में जी पुरुषों की तुलना में थोड़ा कम होता है। ओटोजेनेसिस के दौरान जी के गुण बदल जाते हैं। इसलिए, वे भ्रूण जी., भ्रूण जी. (भ्रूण) - एचबीएफ, और वयस्क जी. - एचबीए के बीच अंतर करते हैं। भ्रूण की कोशिकाओं में ऑक्सीजन के प्रति आकर्षण वयस्कों की तुलना में अधिक होता है, जिसका महत्वपूर्ण शारीरिक महत्व होता है और भ्रूण के शरीर में O2 की कमी के प्रति अधिक प्रतिरोध सुनिश्चित होता है। रक्त में जी की मात्रा का निर्धारण सामान्य परिस्थितियों में और विभिन्न प्रकार की बीमारियों में, विशेषकर रक्त रोगों में, रक्त के श्वसन कार्य को चिह्नित करने के लिए महत्वपूर्ण है। जी की मात्रा विशेष उपकरणों - हेमोमीटर द्वारा निर्धारित की जाती है।
कुछ बीमारियों के लिए, साथ ही जन्मजात रक्त विसंगतियों के लिए (देखें)। hemoglobinopathies ) असामान्य (पैथोलॉजिकल) रक्त कोशिकाएं एरिथ्रोसाइट्स में दिखाई देती हैं, जो अमीनो एसिड अवशेषों के प्रतिस्थापन द्वारा सामान्य से भिन्न होती हैं ( - या बी-जंजीरें. असामान्य जी की 50 से अधिक किस्मों की पहचान की गई है, इस प्रकार, सिकल सेल एनीमिया में जी पाया गया है बी- एन-टर्मिनस से छठे स्थान पर स्थित ग्लूटामिक एसिड की श्रृंखला को वेलिन द्वारा प्रतिस्थापित किया जाता है। हीमोग्लोबिन एफ या एच सामग्री से जुड़ी लाल रक्त कोशिका असामान्यताएं अंतर्निहित हैं थैलेसीमिया , मेथेमोग्लोबिनेमिया . कुछ असामान्य जठरांत्र संबंधी मार्ग का श्वसन कार्य गंभीर रूप से ख़राब हो जाता है, जो विभिन्न रोग स्थितियों का कारण बनता है ( रक्ताल्पता और आदि।)। जी के गुण तब बदल सकते हैं जब शरीर को जहर दिया जाता है, उदाहरण के लिए, कार्बन मोनोऑक्साइड के साथ, जो गठन का कारण बनता है Carboxyhemoglobin , या जहर जो मेथेमोग्लोबिन के निर्माण के साथ Fe 2+ हीम को Fe 3+ में परिवर्तित करते हैं। ये जी. डेरिवेटिव ऑक्सीजन ले जाने में सक्षम नहीं हैं। जी. अणु के प्रोटीन भाग की अनूठी संरचना के कारण विभिन्न जानवरों की प्रजाति विशिष्टता होती है। लाल रक्त कोशिकाओं के विनाश के दौरान जारी जी., गठन का स्रोत है पित्त पिगमेंट.
मांसपेशी ऊतक में मांसपेशी जी होती है - Myoglobin , दाढ़ द्रव्यमान, संरचना और गुणों के संदर्भ में, जी सबयूनिट्स (मोनोमर्स) के करीब। कुछ पौधों में जी के एनालॉग पाए गए हैं (उदाहरण के लिए, लेगहीमोग्लोबिन फलियों की गांठों में पाया जाता है)।
लिट.:कोरज़ुएव पी. ए., हीमोग्लोबिन, एम., 1964; गौरोवित्ज़ एफ., रसायन विज्ञान और प्रोटीन के कार्य, ट्रांस। अंग्रेजी से, दूसरा संस्करण, एम., 1965, पृ. 303-23; इनग्राम वी., मैक्रोमोलेक्युलस का जैवसंश्लेषण, ट्रांस। अंग्रेजी से, एम., 1966, पृ. 188-97; रैपोपोर्ट एस.एम., मेडिकल बायोकैमिस्ट्री, ट्रांस। जर्मन से, एम., 1966; पेरुट्ज़ एम., हीमोग्लोबिन अणु, संग्रह में: अणु और कोशिकाएं, एम., 1966; ज़करकंदल ई.; हीमोग्लोबिन का विकास, ibid.; फैनेली ए.आर., एंटोनिनी ई., कैपुटो ए., हीमोग्लोबिन और मायोग्लोबिन, "प्रोटीन रसायन विज्ञान में प्रगति", 1964, वी. 19, पृ. 73-222; एंटोनिनी ई., ब्रूनोरी एम., हीमोग्लोबिन, "बायोकैमिस्ट्री की वार्षिक समीक्षा", 1970, वी. 39, पृ. 977-1042.
जी. वी. एंड्रीन्को, एस. ई. सेवेरिन।
एक हीमोग्लोबिन अणु के द्रव्यमान की गणना करें: ग्राम में और परमाणु द्रव्यमान इकाइयों में।
एक हीमोग्लोबिन अणु के द्रव्यमान की गणना करें (आणविक सूत्र C 2954 H 4516 N 780 O 806 S 12 Fe 4):
क) ग्राम में; बी) परमाणु द्रव्यमान इकाइयों में।
आइए हम समस्या का एक संक्षिप्त विवरण और इसे हल करने के लिए आवश्यक अतिरिक्त डेटा लिखें।
ए) हीमोग्लोबिन अणु के द्रव्यमान की गणना करने के लिए, आपको इसका दाढ़ द्रव्यमान जानना होगा:
एम (हीमोग्लोबिन) = 2954·12 + 4516·1 + 780·14 + + 806·16 + 12·32 + 4·56 =( जी/मोल)
आगे का तर्क दो तरीकों से किया जा सकता है।
विधि 1: पदार्थ की मात्रा से.
किसी पदार्थ की मात्रा एक सुविधाजनक सार्वभौमिक मात्रा है जो हमें किसी पदार्थ के परमाणुओं या अणुओं की संख्या, द्रव्यमान और आयतन से संबंधित करने की अनुमति देती है।
जहाँ m द्रव्यमान है, M दाढ़ द्रव्यमान है, N परमाणुओं या अणुओं की संख्या है, N A = 6.02 10 23 मोल-1– अवोगाद्रो स्थिरांक.
इन सूत्रों को मिलाकर, हम द्रव्यमान को अणुओं की संख्या के रूप में व्यक्त कर सकते हैं:
परिणामी सूत्र में N = 1, M = प्रतिस्थापित करें जी/मोल, एन ए = 6.02·10 23 मोल-1, हम देखतें है
विधि 2: अनुपात का उपयोग करना।
हीमोग्लोबिन अणुओं का द्रव्यमान 6.02 10 23 है जी;
और 1 हीमोग्लोबिन अणु का द्रव्यमान m है जी.
बी) एक अणु का पूर्ण द्रव्यमान सापेक्ष आणविक द्रव्यमान को 1 ए से गुणा करने के बराबर होता है। खाओ।
सापेक्ष आणविक द्रव्यमान संख्यात्मक रूप से दाढ़ द्रव्यमान के बराबर होता है।
उत्तर:एक हीमोग्लोबिन अणु का द्रव्यमान है:
ए) 1.07·10-19 जी; बी ० ए। खाओ।
विद्यार्थियों की ओर से विद्यार्थियों के लिए एक परियोजना! हम विश्वविद्यालय में उत्तीर्ण होने को 50% तक सरल बनाते हैं। हम पढ़ाई पर 40% समय बचाते हैं। आनंद को 200% बढ़ाएँ!
रसायनज्ञ की पुस्तिका 21
रसायन विज्ञान और रासायनिक प्रौद्योगिकी
हीमोग्लोबिन आणविक भार
जैविक ऑक्सीकरण-कमी प्रतिक्रियाओं में आयरन प्राथमिक इलेक्ट्रॉन वाहक के रूप में कार्य करता है। लौह आयन, Fe+ और Fe+ दोनों, मानव शरीर में मौजूद होते हैं और, इलेक्ट्रॉन वाहक के रूप में कार्य करते हुए, लगातार एक ऑक्सीकरण अवस्था से दूसरे में बदलते रहते हैं। इसे साइटोक्रोम के उदाहरण का उपयोग करके चित्रित किया जा सकता है। लौह आयन आणविक ऑक्सीजन के परिवहन और भंडारण का भी काम करते हैं - जो सभी कशेरुकियों के जीवन के लिए आवश्यक कार्य है। इस प्रणाली में केवल Re(P) ही कार्य करता है। चयापचय प्रक्रियाओं की ऑक्सीजन की जरूरतों को पूरा करने के लिए, अधिकांश जानवरों के पूरे शरीर में तरल पदार्थ घूमता रहता है और ऑक्सीजन को बाहरी स्रोत से अवशोषित करके ऊतकों के माइटोकॉन्ड्रिया में स्थानांतरित करता है। यहां श्वसन श्रृंखला के लिए ऑक्सीडेटिव फास्फारिलीकरण और एटीपी उत्पादन में मध्यस्थता करना आवश्यक है। हालाँकि, जीवित प्राणियों में श्वसन का समर्थन करने के लिए पानी में ऑक्सीजन की घुलनशीलता बहुत कम है। इसलिए, रक्त में आमतौर पर प्रोटीन होते हैं जो ऑक्सीजन को विपरीत रूप से बांधते हैं। ये प्रोटीन अणु मांसपेशियों (ऊतकों) में ऑक्सीजन के प्रवेश की सुविधा प्रदान करते हैं और ऑक्सीजन भंडारण के रूप में भी काम कर सकते हैं।
दूसरी ओर, टीएमवी का आणविक भार लगभग 40 मिलियन माना जाता था, और पहले ऐसा लगा कि टीएमवी की संरचना को समझना मायोग्लोबिन और हीमोग्लोबिन के बहुत छोटे अणुओं की संरचना की तुलना में बहुत अधिक कठिन होगा, जिसे जॉन केंड्रू ने कहा था। और मैक्स पेरुट्ज़ ने कई वर्षों तक संघर्ष किया, लेकिन कभी भी जीवविज्ञानी की रुचि का कोई परिणाम नहीं मिला।
हीमोग्लोबिन
हीमोग्लोबिन (एचबी) (से हेमो. और अव्यक्त. ग्लोबस - बॉल), मनुष्यों, कशेरुकियों और कुछ अकशेरुकी जीवों का लाल लौह युक्त रक्त वर्णक
हीमोग्लोबिन और उसके यौगिकों का अवशोषण स्पेक्ट्रा: 1 - हीमोग्लोबिन; 2 - ऑक्सीहीमोग्लोबिन; 3 - कार्बोक्सीहीमोग्लोबिन; 4 - मेथेमोग्लोबिन: बी, सी, डी, ई, एफ, जी - सौर स्पेक्ट्रम की मुख्य फ्रौनहोफर रेखाएं, तरंग दैर्ध्य संख्याओं द्वारा इंगित की जाती हैं।
मानव ऑक्सीहीमोग्लोबिन पृथक्करण वक्र।
हीमोग्लोबिन
प्रोटीन अणु के आकार के आधार पर, फाइब्रिलर और गोलाकार प्रोटीन को प्रतिष्ठित किया जाता है; एक विशेष समूह में जटिल प्रोटीन होते हैं, जिसमें अमीनो एसिड के अलावा, कार्बोहाइड्रेट, न्यूक्लिक एसिड आदि शामिल होते हैं। ग्लोबिन और आयरन पोर्फिरिन - हेम। उच्चतर जानवरों और मनुष्यों में, रक्त में लगभग 17,000 के दाढ़ द्रव्यमान के साथ 4 मोनोमर सबयूनिट होते हैं; दो मोनोमर्स में 141 अमीनो एसिड अवशेष (?-श्रृंखला) होते हैं, अन्य दो में - 146 अवशेष (?-श्रृंखला) होते हैं।
इन पॉलीपेप्टाइड्स की स्थानिक संरचनाएँ काफी हद तक समान हैं। वे विशिष्ट "हाइड्रोफोबिक पॉकेट" बनाते हैं जिसमें हीम अणु स्थित होते हैं (प्रत्येक सबयूनिट के लिए एक)। हीम में शामिल लौह परमाणु के 6 समन्वय बंधों में से 4 पाइरोल रिंगों के नाइट्रोजन की ओर निर्देशित होते हैं; 5वां हिस्टिडाइन के इमिडाज़ोल रिंग के नाइट्रोजन से जुड़ा है, जो पॉलीपेप्टाइड्स से संबंधित है और α-श्रृंखला में 87वें स्थान पर और β-श्रृंखला में 92वें स्थान पर स्थित है; छठा बंधन पानी के अणु या ऑक्सीजन सहित अन्य समूहों (लिगैंड्स) की ओर निर्देशित होता है। उपइकाइयाँ हाइड्रोजन, नमक और अन्य गैर-सहसंयोजक बंधों द्वारा एक-दूसरे से शिथिल रूप से जुड़ी होती हैं और एमाइड्स और बढ़ी हुई नमक सांद्रता के प्रभाव में आसानी से अलग हो जाती हैं और मुख्य रूप से सममित डिमर (??) और आंशिक रूप से?- और?-मोनोमर्स बनाती हैं। हीमोग्लोबिन अणु की स्थानिक संरचना का अध्ययन 1959 में अंग्रेजी बायोकेमिस्ट मैक्स फर्डिनेंड पेरुट्ज़ द्वारा एक्स-रे विवर्तन विश्लेषण द्वारा किया गया था।
कई उच्चतर जानवरों और मनुष्यों में हीमोग्लोबिन की α- और β-श्रृंखलाओं में अमीनो एसिड की व्यवस्था का क्रम पूरी तरह से स्पष्ट किया गया है। टेट्रामर में इकट्ठे किए गए हीम अणु में, सभी 4 हीम अवशेष सतह पर स्थित होते हैं और O2 के साथ प्रतिक्रियाएं आसानी से पहुंच योग्य होती हैं। O 2 का योग हीम में Fe 2+ परमाणु की सामग्री द्वारा सुनिश्चित किया जाता है। यह प्रतिक्रिया प्रतिवर्ती है और O2 के आंशिक दबाव (तनाव) पर निर्भर करती है। केशिकाओं में केशिकाएं सबसे छोटी वाहिकाएं होती हैं जो अंगों और ऊतकों में प्रवेश करती हैं। वे धमनियों को वेन्यूल्स (सबसे छोटी नसें) से जोड़ते हैं और रक्त परिसंचरण को बंद कर देते हैं; उनकी दीवारों के माध्यम से रक्त और ऊतकों (रक्त केशिकाओं) के बीच पदार्थों का आदान-प्रदान होता है। लसीका केशिकाएं लसीका वाहिकाओं का निर्माण करती हैं, ऊतकों से तरल पदार्थ के बहिर्वाह को बढ़ावा देती हैं, और शरीर से विदेशी कणों और रोगजनक बैक्टीरिया को हटा देती हैं। फेफड़े, जहां ओ 2 तनाव लगभग 100 मिमी एचजी है। कला।, जी। ओ 2 (ऑक्सीकरण प्रक्रिया ऑक्सीजनेशन - ऑक्सीजन के साथ संतृप्ति) के साथ जुड़ता है, ऑक्सीजन युक्त जी - ऑक्सीजन युक्त हीमोग्लोबिन में बदल जाता है। ऊतक केशिकाओं में, जहां O 2 तनाव बहुत कम (लगभग 40 मिमी Hg) होता है, ऑक्सीहीमोग्लोबिन हीमोग्लोबिन और ऑक्सीजन O 2 में विघटित हो जाता है; उत्तरार्द्ध अंगों और ऊतकों की कोशिकाओं में प्रवेश करता है, जहां ओ 2 का आंशिक दबाव और भी कम (5-20 मिमी एचजी) होता है; कोशिकाओं के भीतर गहराई में यह लगभग शून्य हो जाता है। हीमोग्लोबिन में O 2 का जुड़ना और ऑक्सीहीमोग्लोबिन का हीमोग्लोबिन और O 2 में पृथक्करण हीमोग्लोबिन अणु में गठनात्मक (स्थानिक) परिवर्तनों के साथ-साथ डिमर्स और मोनोमर्स में इसके प्रतिवर्ती अपघटन के साथ होता है, जिसके बाद टेट्रामर्स में एकत्रीकरण होता है।
ऑक्सीजन O 2 के साथ प्रतिक्रिया करने पर हीमोग्लोबिन के अन्य गुण भी बदल जाते हैं: ऑक्सीजन युक्त हीमोग्लोबिन हीमोग्लोबिन की तुलना में 70 गुना अधिक मजबूत एसिड होता है, जो ऊतकों में बंधन और फेफड़ों में CO 2 को छोड़ने में एक बड़ी भूमिका निभाता है। विशिष्ट अवशोषण बैंड स्पेक्ट्रम के दृश्य भाग में हैं: जियोग्लोबिन में एक अधिकतम (554 mmk पर) है, और ऑक्सीजन युक्त गैस में 578 और 540 mmk पर दो मैक्सिमा हैं। जी सीधे कार्बन डाइऑक्साइड (कार्बन डाइऑक्साइड) सीओ 2 जोड़ने में सक्षम है (ग्लोबिन के एनएच 2-समूहों के साथ सीओ 2 की प्रतिक्रिया के परिणामस्वरूप); इस मामले में, कार्बेमोग्लोबिन बनता है - एक अस्थिर यौगिक जो फेफड़ों की केशिकाओं में हीमोग्लोबिन और सीओ 2 में आसानी से विघटित हो जाता है।
चावल। 1. हीमोग्लोबिन और उसके यौगिकों का अवशोषण स्पेक्ट्रा: 1 - हीमोग्लोबिन; 2 - ऑक्सीहीमोग्लोबिन; 3 - कार्बोक्सीहीमोग्लोबिन; 4 - मेथेमोग्लोबिन: बी, सी, डी, ई, एफ, जी - सौर स्पेक्ट्रम की मुख्य फ्रौनहोफर रेखाएं, तरंग दैर्ध्य संख्याओं द्वारा इंगित की जाती हैं।
मानव रक्त में हीमोग्लोबिन की मात्रा औसतन % (या साली के अनुसार 78% - 96%) होती है; महिलाओं में जी पुरुषों की तुलना में थोड़ा कम होता है। ओटोजेनेसिस के दौरान जी के गुण बदल जाते हैं। इसलिए, वे भ्रूण जी., भ्रूण जी. (भ्रूण) - एचबीएफ, और वयस्क जी. - एचबीए के बीच अंतर करते हैं। भ्रूण की कोशिकाओं में ऑक्सीजन के प्रति आकर्षण वयस्कों की तुलना में अधिक है, जिसमें एक महत्वपूर्ण शारीरिक शारीरिक, शारीरिक स्थिति है - यानी। एक जिसमें प्रणालियों और अंगों के सामान्य कामकाज से कोई विचलन नहीं होता है। महत्व और भ्रूण के शरीर में O2 की कमी के प्रति अधिक प्रतिरोध सुनिश्चित करता है। रक्त में जी की मात्रा का निर्धारण सामान्य परिस्थितियों में और विभिन्न प्रकार की बीमारियों में, विशेषकर रक्त रोगों में, रक्त के श्वसन कार्य को चिह्नित करने के लिए महत्वपूर्ण है। जी की मात्रा विशेष उपकरणों - हेमोमीटर द्वारा निर्धारित की जाती है।
कुछ बीमारियों के साथ-साथ जन्मजात विसंगतियों में भी विसंगति भ्रूण के विकास में गड़बड़ी के कारण शरीर की एक संरचनात्मक या कार्यात्मक असामान्यता है। तीव्र रूप से व्यक्त विसंगतियों को विकृतियाँ या विकृतियाँ कहा जाता है। लाल रक्त कोशिकाओं में रक्त, असामान्य (पैथोलॉजिकल) जी दिखाई देता है, (- या?-श्रृंखलाओं में अमीनो एसिड अवशेषों के प्रतिस्थापन द्वारा सामान्य लोगों से भिन्न होता है। असामान्य जी की 50 से अधिक किस्मों की पहचान की गई है। इस प्रकार, सिकल सेल एनीमिया, जी. β-श्रृंखलाओं में पाया गया है, जिसमें ग्लूटामिक एसिड, एन-टर्मिनस से छठे स्थान पर है, जो हीमोग्लोबिन एफ या एच की सामग्री से जुड़े एरिथ्रोसाइट्स की विसंगतियों का आधार है थैलेसीमिया। थैलेसीमिया (ग्रीक थैलासा - समुद्र और हाइमा - रक्त से) एक भूमध्यसागरीय रोग है, वंशानुगत हेमोलिटिक एनीमिया, पहली बार भूमध्यसागरीय क्षेत्रों के निवासियों में पहचाना गया (1925), हीमोग्लोबिन के संश्लेषण में गड़बड़ी के कारण होता है। मेथेमोग्लोबिनेमिया। कुछ असामान्य हीमोग्लोबिन का श्वसन कार्य गंभीर रूप से ख़राब हो जाता है, जो शरीर में विषाक्तता होने पर विभिन्न रोग स्थितियों (एनीमिया, आदि) का कारण बनता है, उदाहरण के लिए, कार्बन मोनोऑक्साइड, जो कार्बोक्सीहीमोग्लोबिन के निर्माण का कारण बनता है , या जहर जो मेथेमोग्लोबिन के निर्माण के साथ Fe 2+ हीम को Fe 3+ में परिवर्तित करते हैं। ये जी. डेरिवेटिव ऑक्सीजन ले जाने में सक्षम नहीं हैं। जी. अणु के प्रोटीन भाग की अनूठी संरचना के कारण विभिन्न जानवरों की प्रजाति विशिष्टता होती है। लाल रक्त कोशिकाओं के विनाश के दौरान जारी जी, पित्त वर्णक के निर्माण का स्रोत है।
मांसपेशियों के ऊतकों में मांसपेशी हीमोग्लोबिन होता है - मायोग्लोबिन मायोग्लोबिन एक गोलाकार प्रोटीन है जो मांसपेशियों में ऑक्सीजन जमा करता है। , दाढ़ द्रव्यमान, संरचना और गुणों के संदर्भ में, जी सबयूनिट्स (मोनोमर्स) के करीब। जी. के एनालॉग्स कुछ पौधों में पाए गए हैं (उदाहरण के लिए, लेगहीमोग्लोबिन फलियों की गांठों में पाया जाता है)।
चावल। 2. मानव ऑक्सीहीमोग्लोबिन का पृथक्करण वक्र।
हीमोग्लोबिन के बारे में अधिक जानकारी का अध्ययन साहित्य में किया जा सकता है: कोरज़ुएव पी. ए., हीमोग्लोबिन, एम., 1964; गौरोवित्ज़ एफ., रसायन विज्ञान और प्रोटीन के कार्य, ट्रांस। अंग्रेजी से, दूसरा संस्करण, एम., 1965, पृ. 303 - 23; इनग्राम वी., मैक्रोमोलेक्युलस का जैवसंश्लेषण, ट्रांस। अंग्रेजी से, एम., 1966, पृ. 188-97; रैपोपोर्ट एस.एम., मेडिकल बायोकैमिस्ट्री, ट्रांस। जर्मन से, एम., 1966; पेरुट्ज़ एम., हीमोग्लोबिन अणु, संग्रह में: अणु और कोशिकाएं, एम., 1966; ज़करकंदल ई.; विकास विकास (जीव विज्ञान में) जीवित प्रकृति का अपरिवर्तनीय ऐतिहासिक विकास है। जीवों की परिवर्तनशीलता, आनुवंशिकता और प्राकृतिक चयन द्वारा निर्धारित। यह अस्तित्व की स्थितियों के लिए उनके अनुकूलन, प्रजातियों के गठन और विलुप्त होने, बायोगेकेनोज और समग्र रूप से जीवमंडल के परिवर्तन के साथ है। हीमोग्लोबिन, ibid.; फैनेली ए.आर., एंटोनिनी ई., कैपुटो ए., हीमोग्लोबिन और मायोग्लोबिन, "प्रोटीन रसायन विज्ञान में प्रगति", 1964, वी. 19, पृ. 73 - 222; एंटोनिनी ई., ब्रूनोरी एम., हीमोग्लोबिन, "बायोकैमिस्ट्री की वार्षिक समीक्षा", 1970, वी. 39, पृ. 977 - 1042. (जी. वी. एंड्रिएन्को, एस. ई. सेवेरिन)
कुछ और दिलचस्प खोजें:
- जानकारी का उपयोग करने से पहले अपने डॉक्टर से परामर्श लें! मार्क ट्वेन: स्वास्थ्य के बारे में किताबें पढ़ते समय सावधान रहें। आप टाइपिंग त्रुटि के कारण मर सकते हैं।
लेख पर टिप्पणियाँ
अपने रक्त की संरचना को बेहतर बनाने और हीमोग्लोबिन बढ़ाने के लिए बनाएं यह दलिया।
1 गिलास कुट्टू और 1 गिलास केफिर मिलाएं और 12 घंटे के लिए छोड़ दें। स्वादानुसार शहद मिलाएं.
इस दलिया को नाश्ते में या शाम को खाएं. अन्य अनाजों की तुलना में, कुट्टू में कम कार्बोहाइड्रेट होते हैं, इसलिए यह अधिक वजन वाले लोगों और मधुमेह रोगियों के लिए बहुत उपयोगी है।
हीमोग्लोबिन बढ़ाने के लिए: 300 ग्राम कच्ची गाजर और चुकंदर को मोटे कद्दूकस पर पीस लें, इसमें 300 ग्राम शहद मिलाएं। हिलाओ और ठंडा करो।
1 बड़ा चम्मच लें. दिन में 1 बार, सुबह खाली पेट 30 मिनट तक। खाने से पहले।
एक सप्ताह में हीमोग्लोबिन बढ़कर सामान्य (शायद दोगुना!) हो जाएगा।
मांस के बिना हीमोग्लोबिन कैसे बढ़ाएं?
निम्नलिखित उत्पादों से भी हीमोग्लोबिन का स्तर बढ़ाया जा सकता है:
चोकर, गेहूं का दलिया, खुबानी, सूखे खुबानी, डार्क चॉकलेट, हरे सेब, अनाज की ब्रेड, लाल अंगूर, चुकंदर, फलियां, बादाम, अनार, आलूबुखारा का रस, आलूबुखारा, किशमिश, मटर, टमाटर का रस, ब्रसेल्स स्प्राउट्स, ब्रोकोली, मूंगफली का मक्खन, दलिया, अनानास (ताजा और डिब्बाबंद)।
ये सभी खाद्य पदार्थ आयरन से भरपूर होते हैं, जो हीमोग्लोबिन बढ़ाते हैं। और सूचीबद्ध उत्पादों में से कई लौह सामग्री में मांस के बराबर हैं।
हीमोग्लोबिन बढ़ाने के खास नुस्खे
निम्नलिखित व्यंजनों में से, वह चुनें जो आपके लिए सबसे उपयुक्त हो, और इसे शरीर के लिए "विटामिन पूरक" के रूप में निरंतर उपयोग करने का प्रयास करें।
1) एक गिलास अखरोट और एक गिलास कच्चा कुट्टू पीस लें, इसमें एक गिलास शहद मिलाएं, सभी चीजों को मिला लें, रोज एक चम्मच खाएं।
2) अखरोट, सूखे खुबानी, शहद, किशमिश - सभी 1:1 के अनुपात में - पीसें और अच्छी तरह मिलाएं, प्रति दिन 1-3 बड़े चम्मच खाएं (न केवल हीमोग्लोबिन बढ़ाने के लिए, बल्कि शरीर को प्रदान करने के लिए भी सर्वोत्तम व्यंजनों में से एक) आवश्यक विटामिन )
3) 1 गिलास आलूबुखारा, सूखे खुबानी, अखरोट, किशमिश पीस लें, शहद मिलाएं, छिलके सहित 1-2 नींबू मिलाएं (नींबू की जगह एलोवेरा का रस मिला सकते हैं), प्रतिदिन 1-3 चम्मच खाएं।
4) 100 मिलीलीटर ताजा निचोड़ा हुआ चुकंदर का रस, 100 मिलीलीटर गाजर का रस, मिलाएं और पिएं (वस्तुतः 2 दिनों में हीमोग्लोबिन बढ़ाता है)।
5) 1/2 कप सेब का रस, 1/4 कप चुकंदर का रस और 1/4 कप गाजर का रस मिलाकर दिन में 1-2 बार पियें।
6) 1/2 कप ताजा निचोड़ा हुआ सेब का रस, 1/2 कप घर का बना क्रैनबेरी रस, 1 बड़ा चम्मच ताजा निचोड़ा हुआ चुकंदर का रस, हिलाएं और पियें।
7) कच्चा अनाज 1/2 कप, धोकर, 1 कप केफिर डालें और रात भर के लिए छोड़ दें, सुबह दलिया तैयार है, आप खा सकते हैं.
8) 1/2 गिलास सूखी रेड वाइन अच्छी गुणवत्ता, 5-7 मिनट के लिए पानी के स्नान में वाष्पित; 1/4 कप उबली बिछुआ, 1 बड़ा चम्मच पिघला हुआ मक्खन, गर्म पियें।
हीमोग्लोबिन का दाढ़ द्रव्यमान
हीमोग्लोबिन, एचबी ( हीमोग्लोबिनम; यूनानी हैमा रक्त + लैट। ग्लोबस बॉल), एक हेमोप्रोटीन है, जो हीम युक्त क्रोमोप्रोटीन से संबंधित एक जटिल प्रोटीन है; फेफड़ों से ऊतकों तक ऑक्सीजन का स्थानांतरण करता है और ऊतकों से श्वसन अंगों तक कार्बन डाइऑक्साइड के स्थानांतरण में शामिल होता है। जी. सभी कशेरुकियों और कुछ अकशेरुकी जानवरों (कीड़े, मोलस्क, आर्थ्रोपोड, इचिनोडर्म) के एरिथ्रोसाइट्स में पाया जाता है, साथ ही कुछ फलियों की जड़ की गांठों में भी पाया जाता है। मोल. मानव लाल रक्त कोशिकाओं का भार (द्रव्यमान) बराबर होता है; एक एरिथ्रोसाइट में लगभग होता है। जी.जी. के 400 मिलियन अणु पानी में अत्यधिक घुलनशील हैं, अल्कोहल, क्लोरोफॉर्म और ईथर में अघुलनशील हैं, और अच्छी तरह से क्रिस्टलीकृत होते हैं (जी. क्रिस्टल का आकार हर जानवर में अलग-अलग होता है)।
जी की संरचना में एक साधारण प्रोटीन - ग्लोबिन और एक लौह युक्त कृत्रिम (गैर-प्रोटीन) समूह - हेम (क्रमशः अणु के वजन से 96 और 4%) शामिल हैं। 2.0 से नीचे पीएच पर, हीम अणु हीम और ग्लोबिन में विभाजित हो जाता है।
हेम (सी 34 एच 32 ओ 4 एन 4) एक लौह प्रोटोपोर्फिरिन है - द्विसंयोजक लौह के साथ प्रोटोपोर्फिरिन IX का एक जटिल यौगिक। आयरन प्रोटोपोर्फिरिन कोर के केंद्र में स्थित है और पाइरोल कोर के चार नाइट्रोजन परमाणुओं से जुड़ा है (चित्र 1): दो समन्वय बंधन और दो हाइड्रोजन प्रतिस्थापन बांड।
चूंकि लोहे की समन्वय संख्या 6 है, दो संयोजकताएं अप्रयुक्त रहती हैं, उनमें से एक का एहसास तब होता है जब हीम ग्लोबिन से जुड़ जाता है, और दूसरा ऑक्सीजन या अन्य लिगैंड्स - सीओ, एफ +, एज़ाइड्स, पानी (छवि 2) से जुड़ जाता है। वगैरह।
Fe 3+ के साथ प्रोटोपॉर्फिन IX के कॉम्प्लेक्स को हेमेटिन कहा जाता है। हेमेटिन (क्लोरहेमिन, हेमिन) का हाइड्रोक्लोरिक एसिड नमक आसानी से उत्सर्जित होता है। क्रिस्टलीय रूप (तथाकथित टेकमैन क्रिस्टल)। हीम में नाइट्रोजन यौगिकों (अमोनिया, पाइरीडीन, हाइड्राज़ीन, एमाइन, अमीनो एसिड, प्रोटीन, आदि) के साथ जटिल यौगिक बनाने की क्षमता होती है, जिससे हेमोक्रोमोजेन में बदल जाता है (देखें)। चूंकि हीम सभी पशु प्रजातियों में समान है, हीमोग्लोबिन के गुणों में अंतर हीमोग्लोबिन अणु - ग्लोबिन के प्रोटीन भाग की संरचनात्मक विशेषताओं के कारण होता है।
ग्लोबिन
ग्लोबिन एक एल्ब्यूमिन-प्रकार का प्रोटीन है जिसके अणु में चार पॉलीपेप्टाइड श्रृंखलाएं होती हैं: दो अल्फा श्रृंखलाएं (प्रत्येक में 141 अमीनो एसिड अवशेष होते हैं) और दो बीटा श्रृंखलाएं जिनमें 146 अमीनो एसिड अवशेष होते हैं। इस प्रकार, जी अणु का प्रोटीन घटक विभिन्न अमीनो एसिड के 574 अवशेषों से निर्मित होता है। प्राथमिक संरचना, यानी, मनुष्यों और कई जानवरों में ग्लोबिन की पॉलीपेप्टाइड श्रृंखलाओं में अमीनो एसिड के आनुवंशिक रूप से निर्धारित अनुक्रम का पूरी तरह से अध्ययन किया गया है। मानव ग्लोबिन की एक विशिष्ट विशेषता इसकी संरचना में अमीनो एसिड आइसोल्यूसीन और सिस्टीन की अनुपस्थिति है। अल्फा और बीटा श्रृंखला में एन-टर्मिनल अवशेष वेलिन अवशेष हैं। अल्फा श्रृंखलाओं के सी-टर्मिनल अवशेषों को आर्जिनिन अवशेषों द्वारा दर्शाया जाता है, और बीटा श्रृंखलाओं को हिस्टिडीन अवशेषों द्वारा दर्शाया जाता है। प्रत्येक श्रृंखला में अंतिम स्थान पर टायरोसिन अवशेषों का कब्जा होता है।
क्रिस्टल के एक्स-रे संरचनात्मक विश्लेषण ने इसके अणु की स्थानिक संरचना की मुख्य विशेषताओं की पहचान करना संभव बना दिया [एम। पेरुट्ज़]। यह पता चला कि अल्फा और बीटा श्रृंखलाओं में विभिन्न लंबाई के पेचदार खंड होते हैं, जो अल्फा हेलीकॉप्टर (द्वितीयक संरचना) के सिद्धांत के अनुसार बनाए जाते हैं; अल्फा श्रृंखला में 7 और बीटा श्रृंखला में 8 पेचदार खंड हैं जो गैर-पेचदार खंडों से जुड़े हुए हैं। एन-टर्मिनस से शुरू होने वाले हेलिकल खंड, लैटिन वर्णमाला (ए, बी, सी, डी, ई, एफ, जी, एच) के अक्षरों द्वारा निर्दिष्ट होते हैं, और गैर-पेचदार खंड या हेलिकॉप्टर के घूर्णन के कोण होते हैं संगत पदनाम (एबी, बीसी, सीडी, डीई और आदि)। ग्लोबिन श्रृंखला के एमाइन (एन) या कार्बोक्सिल (सी) छोर पर गैर-पेचदार क्षेत्रों को क्रमशः एनए या एचसी नामित किया गया है। अमीनो एसिड अवशेषों को प्रत्येक खंड में क्रमांकित किया गया है और, इसके अलावा, श्रृंखला के एन-टर्मिनस से इस अवशेषों की संख्या कोष्ठक में दी गई है।
अंतरिक्ष में सर्पिल और गैर-सर्पिल खंड एक निश्चित तरीके से व्यवस्थित होते हैं, जो निर्धारित करते हैं तृतीयक संरचनाग्लोबिन चेन. उत्तरार्द्ध जी की अल्फा और बीटा श्रृंखलाओं में लगभग समान है, उनकी प्राथमिक संरचना में महत्वपूर्ण अंतर के बावजूद। यह अमीनो एसिड के ध्रुवीय और हाइड्रोफोबिक समूहों की विशिष्ट व्यवस्था के कारण होता है, जिससे हाइड्रोफोबिक कोर के गठन के साथ ग्लोब्यूल के आंतरिक भाग में गैर-ध्रुवीय समूहों का संचय होता है। प्रोटीन के ध्रुवीय समूह जलीय वातावरण का सामना करते हैं, इसके संपर्क में रहते हैं। प्रत्येक ग्लोबिन श्रृंखला के अंदर, सतह के पास, एक हाइड्रोफोबिक गुहा ("हीम पॉकेट") होती है, जिसमें हीम स्थित होता है, इस प्रकार उन्मुख होता है कि इसके गैर-ध्रुवीय प्रतिस्थापन अणु के आंतरिक भाग में निर्देशित होते हैं, जो हाइड्रोफोबिक कोर का हिस्सा बन जाते हैं। परिणाम लगभग है. हीम और ग्लोबिन के बीच 60 गैर-ध्रुवीय संपर्क और अल्फा और बीटा श्रृंखलाओं के साथ हीम के एक या दो ध्रुवीय (आयनिक) संपर्क, जिसमें हाइड्रोफोबिक "पॉकेट" से निकलने वाले हीम के प्रोपियोनिक एसिड के अवशेष शामिल होते हैं। ग्लोबिन की हाइड्रोफोबिक गुहा में हीम का स्थान हीम के Fe 2+ में ऑक्सीजन के प्रतिवर्ती योग की संभावना प्रदान करता है, बिना बाद के Fe 3+ के ऑक्सीकरण के और विभिन्न पशु प्रजातियों के हीमोग्लोबिन की विशेषता है। इसकी पुष्टि हेम के पास गैर-ध्रुवीय संपर्कों में किसी भी बदलाव के प्रति जी की अत्यधिक संवेदनशीलता से होती है। इस प्रकार, हेमेटोपोर्फिरिन में हीम के प्रतिस्थापन से हीम के गुणों का तीव्र उल्लंघन होता है।
हाइड्रोफोबिक गुहा में हीम के आसपास के कुछ अमीनो एसिड अवशेष अपरिवर्तनीय अमीनो एसिड में से हैं, यानी, अमीनो एसिड जो विभिन्न पशु प्रजातियों के लिए समान हैं और जी के कार्य के लिए आवश्यक हैं। अपरिवर्तनीय अमीनो एसिड के बीच बडा महत्वतीन को आवंटित: हिस्टिडाइन अवशेष, तथाकथित। समीपस्थ हिस्टिडाइन्स (ए-चेन में 87वां स्थान और पी-चेन में 92वां स्थान), डिस्टल हिस्टिडाइन्स (ए-चेन में 58वां स्थान और (5-चेन) में 63वां स्थान), साथ ही वेलिन अवशेष ई-11 (अल्फा में 62वां स्थान) श्रृंखला और बीटा श्रृंखला में 67वां स्थान)।
तथाकथित के बीच संबंध प्रॉक्सिमल हिस्टिडीन और हीम आयरन ही एकमात्र रसायन है। उनके बीच का बंधन (हीम के Fe 2+ परमाणु का पांचवां समन्वय बंधन साकार होता है) और सीधे हीम में ऑक्सीजन के जुड़ाव को प्रभावित करता है। "डिस्टल" हिस्टिडाइन सीधे तौर पर हीम से जुड़ा नहीं है और ऑक्सीजन निर्धारण में भाग नहीं लेता है। इसका महत्व Fe 2+ परमाणु को अपरिवर्तनीय ऑक्सीकरण (जाहिरा तौर पर ऑक्सीजन और नाइट्रोजन के बीच हाइड्रोजन बंधन के गठन के कारण) के खिलाफ स्थिर करना है। वेलिन अवशेष (ई-11) हेम्स में ऑक्सीजन जोड़ने की दर का एक प्रकार का नियामक है: बीटा श्रृंखलाओं में यह स्थिर रूप से स्थित होता है ताकि यह उस स्थान पर कब्जा कर ले जहां ऑक्सीजन जुड़नी चाहिए, जिसके परिणामस्वरूप ऑक्सीजनेशन फ्लै चेन से शुरू होता है .
अणु का प्रोटीन भाग और कृत्रिम समूह एक दूसरे पर गहरा प्रभाव डालते हैं। ग्लोबिन हीम के कई गुणों को बदल देता है, जिससे उसे ऑक्सीजन को बांधने की क्षमता मिल जाती है। हेम ग्लोबिन प्रतिरोध प्रदान करता है कार्रवाई, हीटिंग, एंजाइमों द्वारा पाचन और जी के क्रिस्टलीकरण गुणों की विशेषताओं को निर्धारित करता है।
हीम अणुओं से जुड़ी पॉलीपेप्टाइड श्रृंखलाएं चार मुख्य भाग बनाती हैं - हीम अणु की उपइकाइयाँ एक दूसरे के साथ उनके संबंध (बिछाने) की प्रकृति और अंतरिक्ष में उनका स्थान हीम की चतुर्धातुक संरचना की विशेषताओं से निर्धारित होती हैं: ए- और। पी-चेन समरूपता की धुरी के चारों ओर टेट्राहेड्रोन के कोनों पर स्थित हैं, इसके अलावा, अल्फा चेन पी-चेन के शीर्ष पर स्थित हैं और उनके बीच निचोड़ा हुआ प्रतीत होता है, और सभी चार हेम एक दूसरे से बहुत दूर हैं (चित्र) .3). कुल मिलाकर, 6.4 X 5.5 X 5.0 एनएम के आयाम वाला एक टेट्रामेरिक गोलाकार कण बनता है। चतुर्धातुक संरचना α-α और β-β श्रृंखलाओं के बीच नमक बंधन और α और β श्रृंखलाओं (α1-β1 और α2-β2) के बीच दो प्रकार के संपर्कों द्वारा स्थिर होती है। α1-β1 संपर्क सबसे व्यापक हैं, जिनमें 34 अमीनो एसिड अवशेष शामिल हैं, और अधिकांश इंटरैक्शन गैर-ध्रुवीय हैं। α1-β2 संपर्क में 19 अमीनो एसिड अवशेष होते हैं, कुछ हाइड्रोजन बांड के अपवाद के साथ, अधिकांश बांड भी गैर-ध्रुवीय होते हैं। इस संपर्क में स्थित सभी अवशेष अध्ययन की गई सभी पशु प्रजातियों में समान हैं, जबकि α1-β1 संपर्कों में 1/3 अवशेष भिन्न-भिन्न हैं।
मानव ग्रंथि विषमांगी है, जो इसकी संरचना बनाने वाली पॉलीपेप्टाइड श्रृंखलाओं में अंतर के कारण है। इस प्रकार, एक वयस्क के रक्त ग्लूकोज, जो रक्त ग्लूकोज (एचबीए) का 95-98% बनाता है, में दो α- और दो β-चेन होते हैं; G. (HbA2) का छोटा अंश, 2.0-2.5% की अधिकतम सामग्री तक पहुँचने पर, इसमें दो α- और दो σ-श्रृंखलाएँ होती हैं; भ्रूण हीमोग्लोबिन (HbF), या भ्रूण हीमोग्लोबिन, जो एक वयस्क के रक्त में 0.1-2% होता है, में दो α- और दो γ-श्रृंखलाएं होती हैं।
जन्म के बाद पहले महीनों में भ्रूण जी को एचबीए द्वारा प्रतिस्थापित किया जाता है। यह थर्मल विकृतीकरण के लिए महत्वपूर्ण प्रतिरोध की विशेषता है, जिस पर रक्त में इसकी सामग्री निर्धारित करने के तरीके आधारित हैं।
पॉलीपेप्टाइड श्रृंखलाओं की संरचना के आधार पर, जी के सूचीबद्ध प्रकारों को निम्नानुसार नामित किया गया है: एचबीए - एचबीα2β2 के रूप में, एचबीए2 - एचबीα2σ2 के रूप में, और एचबीएफ - एचबीα2γ के रूप में। हेमटोपोइएटिक तंत्र की जन्मजात विसंगतियों और बीमारियों के साथ, असामान्य प्रकार के हेमटोपोइजिस दिखाई देते हैं, उदाहरण के लिए, सिकल सेल एनीमिया (देखें), थैलेसीमिया (देखें), गैर-एंजाइमी मूल के जन्मजात मेथेमोग्लोबिनेमिया (मेटेमोग्लोबिनेमिया देखें), आदि। सबसे आम प्रतिस्थापन एक जोड़ी पॉलीपेप्टाइड श्रृंखला में एक एकल अमीनो एसिड का।
हीम लौह परमाणु की वैधता और हीम अणु में लिगैंड के प्रकार के आधार पर, बाद वाला कई रूपों में हो सकता है। अपचयित हाइड्रोजन (डीऑक्सी-एचबी) में मुक्त छठी संयोजकता के साथ Fe 2+ होता है; जब इसमें O 2 मिलाया जाता है, तो हाइड्रोजन का एक ऑक्सीजनयुक्त रूप (HbO 2) बनता है। जब HbO 2 कई ऑक्सीकरण एजेंटों (पोटेशियम फेरिकैनाइड, नाइट्राइट, क्विनोन, आदि) के संपर्क में आता है, तो Fe 2+ मेथेमोग्लोबिन के निर्माण के साथ Fe 3+ में ऑक्सीकृत हो जाता है, जो O 2 को स्थानांतरित करने में असमर्थ होता है। माध्यम के पीएच मान के आधार पर, मेथेमोग्लोबिन के अम्लीय और क्षारीय रूप होते हैं, जिसमें छठे लिगैंड के रूप में एच 2 ओ या ओएच समूह होता है। स्वस्थ लोगों के रक्त में मेथेमोग्लोबिन की सांद्रता 0.83+0.42% होती है।
मेथेमोग्लोबिन में हाइड्रोजन फ्लोराइड, हाइड्रोसायनिक एसिड और अन्य पदार्थों को मजबूती से बांधने की क्षमता होती है। इस गुण का उपयोग शहद में किया जाता है। हाइड्रोसायनिक जहर से पीड़ित लोगों को बचाने का अभ्यास। जी के विभिन्न व्युत्पन्न अवशोषण स्पेक्ट्रा (तालिका) में भिन्न हैं।
तरंग दैर्ध्य (अधिकतम अवशोषण पर), एनएम
सहस्राब्दी प्रकाश अवशोषण गुणांक, ई
मेथेमोग्लोबिन (मेट-एचबी; पीएच 7.0-7.4)
हीमोग्लोबिन के कार्यात्मक गुण. गैस की मुख्य बायोल भूमिका शरीर और बाहरी वातावरण के बीच गैस विनिमय में भागीदारी है। जी. फेफड़ों से ऊतकों तक रक्त द्वारा ऑक्सीजन के स्थानांतरण और ऊतकों से फेफड़ों तक कार्बन डाइऑक्साइड के परिवहन को सुनिश्चित करता है (गैस विनिमय देखें)। कम महत्वपूर्ण नहीं हैं बफ़र गुणजी., रक्त में शक्तिशाली हीमोग्लोबिन और ऑक्सीहीमोग्लोबिन बफर सिस्टम बनाता है, इस प्रकार शरीर में एसिड-बेस संतुलन को बनाए रखने में योगदान देता है (देखें)। बफर सिस्टम, एसिड बेस संतुलन)।
HbO 2 की ऑक्सीजन क्षमता O 2 की 1.39 मिली प्रति 1 ग्राम HbO 2 है। जी की ऑक्सीजन को बांधने और छोड़ने की क्षमता उसके ऑक्सीजन पृथक्करण वक्र (ओडीसी) द्वारा परिलक्षित होती है, जो ओ 2 (पीओ 2) के आंशिक दबाव के आधार पर ऑक्सीजन के साथ जी की संतृप्ति के प्रतिशत को दर्शाती है।
ऑक्सीजन के टेट्रामेरिक अणुओं में एस-आकार का सीडीके होता है, जो इंगित करता है कि ऑक्सीजन फेफड़ों में अपेक्षाकृत कम आंशिक दबाव पर ऑक्सीजन का इष्टतम बंधन प्रदान करता है और ऊतकों में ऑक्सीजन के अपेक्षाकृत उच्च आंशिक दबाव पर रिलीज करता है (चित्र 4)। ऊतकों तक ऑक्सीजन की अधिकतम डिलीवरी को रक्त में उच्च आंशिक दबाव के संरक्षण के साथ जोड़ा जाता है, जो ऊतकों में गहराई तक ऑक्सीजन के प्रवेश को सुनिश्चित करता है। मिमी एचजी में ऑक्सीजन के आंशिक दबाव का मान। कला।, जब 50% गैस ऑक्सीजनित होती है, तो ऑक्सीजन के लिए गैस की आत्मीयता का माप होता है और इसे P50 नामित किया जाता है।
जी के चारों शीर्षों में ऑक्सीजन का योग क्रमिक रूप से होता है। जी के सीडीके की एस-आकार की प्रकृति इंगित करती है कि पहला ऑक्सीजन अणु जी के साथ बहुत धीरे-धीरे जुड़ता है, यानी, जी के लिए इसकी आत्मीयता कम है, क्योंकि डीऑक्सीहीमोग्लोबिन अणु में नमक संपर्कों को तोड़ना आवश्यक है। हालाँकि, पहले ऑक्सीजन अणु के जुड़ने से इसके लिए शेष तीन हीमों की आत्मीयता बढ़ जाती है, और हीम का आगे ऑक्सीजनीकरण बहुत तेजी से होता है (चौथे हीम का ऑक्सीकरण पहले की तुलना में 500 गुना तेजी से होता है)। नतीजतन, ऑक्सीजन-बाध्यकारी केंद्रों के बीच एक सहकारी बातचीत होती है। कार्बन मोनोऑक्साइड (CO) प्रतिक्रिया के पैटर्न ऑक्सीजन के समान हैं, लेकिन CO के लिए कार्बन मोनोऑक्साइड की आत्मीयता O2 की तुलना में लगभग 300 गुना अधिक है, जो कार्बन मोनोऑक्साइड को अत्यधिक विषाक्त बनाती है। इस प्रकार, हवा में CO की सांद्रता 0.1% के बराबर होने पर, आधे से अधिक रक्त गैस ऑक्सीजन से नहीं, बल्कि कार्बन मोनोऑक्साइड से जुड़ी होती है। ऐसे में कार्बोक्सीहीमोग्लोबिन बनता है, जो ऑक्सीजन का परिवहन करने में असमर्थ होता है।
हीमोग्लोबिन ऑक्सीजनेशन की प्रक्रिया के नियामक। ऑक्सीजनेशन और डीऑक्सीजनेशन की प्रक्रियाएं हाइड्रोजन आयनों, कार्बनिक फॉस्फेट, अकार्बनिक लवण, तापमान, कार्बन डाइऑक्साइड और कुछ अन्य पदार्थों से काफी प्रभावित होती हैं जो फिजियोल के अनुसार ऑक्सीजन के लिए हाइड्रोजन की आत्मीयता की मात्रा को नियंत्रित करती हैं। शरीर अनुरोध. माध्यम के पीएच मान पर ऑक्सीजन के प्रति ऑक्सीजन की आत्मीयता की निर्भरता को बोहर प्रभाव कहा जाता है (वेरिगो प्रभाव देखें)। वहाँ "खट्टा" (पीएच) हैं<6) и «щелочной» эффект Бора (pH>6). सबसे बड़ा फ़िज़ियोल. जो बात मायने रखती है वह है "क्षारीय" बोह्र प्रभाव। इसका आणविक तंत्र हीमोग्लोबिन अणु में कई सकारात्मक रूप से चार्ज किए गए कार्यात्मक समूहों की उपस्थिति के कारण होता है, जिनमें से पृथक्करण स्थिरांक हीमोग्लोबिन अणु के अंदर पड़ोसी प्रोटीन श्रृंखलाओं के नकारात्मक चार्ज समूहों के बीच नमक पुलों के गठन के कारण डीऑक्सीहीमोग्लोबिन में बहुत अधिक होता है। ऑक्सीजनेशन के दौरान, हीमोग्लोबिन अणु में होने वाले गठनात्मक परिवर्तनों के कारण, नमक पुल नष्ट हो जाते हैं, नकारात्मक रूप से चार्ज किए गए समूहों का पीएच बदल जाता है और प्रोटॉन घोल में छोड़ दिए जाते हैं। नतीजतन, ऑक्सीजनेशन से गैस अणु से एक प्रोटॉन (एच +) अलग हो जाता है और, इसके विपरीत, पीएच मान में बदलाव होता है, यानी, अप्रत्यक्ष रूप से माध्यम के एच + आयनों की एकाग्रता, गैस में ऑक्सीजन के जुड़ाव को प्रभावित करती है। इस प्रकार, एच + एक लिगैंड बन जाता है जो अधिमानतः डीऑक्सीहीमोग्लोबिन से जुड़ता है और इस तरह ऑक्सीजन के लिए इसकी आत्मीयता को कम कर देता है, यानी, पीएच में अम्लीय पक्ष में बदलाव से सीडीसी दाईं ओर शिफ्ट हो जाता है। ऑक्सीजनेशन की प्रक्रिया एंडोथर्मिक है, और तापमान में वृद्धि जी अणु से ऑक्सीजन के विभाजन को बढ़ावा देती है, अंगों की बढ़ी हुई गतिविधि और रक्त के तापमान में वृद्धि से सीडीसी में दाईं ओर बदलाव होगा, और ऑक्सीजन की डिलीवरी होगी। ऊतकों में वृद्धि होगी.
एरिथ्रोसाइट्स में स्थानीयकृत कार्बनिक फॉस्फेट द्वारा ऑक्सीजनेशन प्रक्रिया का एक अनूठा विनियमन किया जाता है। विशेष रूप से, 2,3-डिफोस्फोग्लिसरेट (डीपीजी) ऑक्सीजन के लिए जी की आत्मीयता को काफी कम कर देता है, जिससे ऑक्सीहीमोग्लोबिन से ओ 2 को हटाने को बढ़ावा मिलता है। जी पर डीपीजी का प्रभाव घटते पीएच मान (फिजियोल, क्षेत्र के भीतर) के साथ बढ़ता है, इसलिए जी के सीडीके पर इसका प्रभाव कम पीएच मान पर अधिक हद तक प्रकट होता है। डीपीजी मुख्य रूप से 1:1 मोलर अनुपात में डीऑक्सीहीमोग्लोबिन से बंधता है, इसके अणु की आंतरिक गुहा में प्रवेश करता है और बीटा श्रृंखला के वेलिन अवशेषों के दो अल्फा-एनएच 2 समूहों के साथ 4 नमक पुल बनाता है और, जाहिरा तौर पर, हिस्टिडीन एच के दो इमिडाज़ोल समूहों के साथ। 21 (143) बीटा श्रृंखलाएँ। बढ़ते तापमान के साथ डीपीजी का प्रभाव कम हो जाता है, यानी, डीपीजी को जी अणु से बांधने की प्रक्रिया ऊष्माक्षेपी होती है। इससे यह तथ्य सामने आता है कि डीपीजी की उपस्थिति में, तापमान पर ऑक्सीजनेशन प्रक्रिया की निर्भरता काफी हद तक गायब हो जाती है। नतीजतन, रक्त द्वारा ऑक्सीजन की सामान्य रिहाई व्यापक तापमान सीमा पर संभव हो जाती है। एक समान प्रभाव, हालांकि कुछ हद तक, एटीपी, पाइरिडोक्सल फॉस्फेट और अन्य कार्बनिक फॉस्फेट द्वारा डाला जाता है। इस प्रकार, एरिथ्रोसाइट्स में कार्बनिक फॉस्फेट की सांद्रता पर महत्वपूर्ण प्रभाव पड़ता है श्वसन क्रियाजी., इसे जल्दी से विभिन्न फ़िज़ियोल, और पैटोल, बिगड़ा हुआ ऑक्सीजनेशन से जुड़ी स्थितियों * (वायुमंडल में ऑक्सीजन सामग्री में परिवर्तन, रक्त की हानि, नाल के माध्यम से मां से भ्रूण तक ऑक्सीजन परिवहन का विनियमन, आदि) के अनुकूल बनाता है। इस प्रकार, एनीमिया और हाइपोक्सिया के साथ, एरिथ्रोसाइट्स में डीपीजी की सामग्री बढ़ जाती है, जो सीडीसी को दाईं ओर स्थानांतरित कर देती है और ऊतकों में ऑक्सीजन की अधिक रिहाई का कारण बनती है। कई तटस्थ लवण (एसीटेट, फॉस्फेट, पोटेशियम और सोडियम क्लोराइड) भी ऑक्सीजन के लिए जी की आत्मीयता को कम करते हैं। यह प्रभाव पदार्थ की प्रकृति पर निर्भर करता है और कार्बनिक फॉस्फेट के प्रभाव के समान होता है। उच्च नमक सांद्रता की उपस्थिति में, ऑक्सीजन के लिए जी की आत्मीयता न्यूनतम तक पहुंच जाती है - विभिन्न लवणों और डीपीजी के लिए समान सीमा तक, यानी, जी अणु पर समान बंधन केंद्रों के लिए लवण और डीपीजी दोनों एक दूसरे के साथ प्रतिस्पर्धा करते हैं। इसलिए, उदाहरण के लिए, ऑक्सीजन के लिए जी की आत्मीयता पर डीपीजी का प्रभाव 0.5 एम सोडियम क्लोराइड की उपस्थिति में गायब हो जाता है।
1904 में, चौ. बोह्र एट अल। रक्त में कार्बन डाइऑक्साइड के आंशिक दबाव में वृद्धि के साथ ऑक्सीजन के लिए जी की आत्मीयता में कमी देखी गई।
कार्बन डाइऑक्साइड सामग्री में वृद्धि से मुख्य रूप से पर्यावरण के पीएच में बदलाव होता है, लेकिन मूल्य में इस तरह की कमी के साथ P50 मान अपेक्षा से कहीं अधिक कम हो जाता है।
पीएच मान. यह निम्नलिखित योजना के अनुसार कार्बामेट्स (कार्बेमोग्लोबिन) के गठन के साथ अल्फा श्रृंखलाओं के अपरिवर्तित अल्फा-एनएच 2 समूहों और संभवतः गैस की बीटा श्रृंखलाओं के साथ कार्बन डाइऑक्साइड के विशिष्ट संबंध के कारण है:
डीऑक्सीहीमोग्लोबिन HbO2 की तुलना में अधिक कार्बन डाइऑक्साइड को बांधता है। एरिथ्रोसाइट्स में, डीपीजी की उपस्थिति प्रतिस्पर्धात्मक रूप से कार्बामेट्स के निर्माण को रोकती है। कार्बामेट तंत्र की मदद से आराम करने वाले स्वस्थ लोगों के शरीर से 15% तक कार्बन डाइऑक्साइड निकाल दिया जाता है। रक्त की 70% से अधिक बफर क्षमता इसमें मौजूद गैस द्वारा प्रदान की जाती है, जिससे कार्बन डाइऑक्साइड के हस्तांतरण में गैस की महत्वपूर्ण अप्रत्यक्ष भागीदारी भी होती है। जैसे ही रक्त ऊतकों से बहता है, HbO 2 डीऑक्सीहीमोग्लोबिन में बदल जाता है, जबकि H+ आयनों को बांधता है और इस तरह H 2 CO 3 को HCO 3 - में परिवर्तित करता है। इस प्रकार, जी की प्रत्यक्ष और अप्रत्यक्ष भागीदारी के साथ, ऊतकों से रक्त में आने वाले 90% से अधिक कार्बन डाइऑक्साइड बंध जाता है और फेफड़ों में स्थानांतरित हो जाता है।
यह महत्वपूर्ण है कि सीडीसी शिफ्ट (एच +, डीपीजी, सीओ 2) के ये सभी नियामक आपस में जुड़े हुए हैं, जो कई उभरती रोग स्थितियों में बहुत महत्वपूर्ण है। इस प्रकार, एरिथ्रोसाइट्स में डीपीजी की सांद्रता में वृद्धि उनके चयापचय में जटिल परिवर्तनों का परिणाम है, जिसमें पीएच मान में वृद्धि मुख्य स्थिति है। एसिडोसिस और एल्कलोसिस में, H+ और DPG के बीच संबंध के कारण भी, P50 मान बराबर हो जाता है।
हीमोग्लोबिन चयापचय
जी का जैवसंश्लेषण एरिथ्रोसाइट्स (एरिथ्रोब्लास्ट्स, नॉर्मोब्लास्ट्स, रेटिकुलोसाइट्स) के युवा रूपों में होता है, जहां जी की संरचना में शामिल लौह परमाणु प्रवेश करते हैं और δ- के गठन के साथ पोर्फिरिन रिंग के संश्लेषण में भाग लेते हैं। अमीनोलेवुलिनिक एसिड. उत्तरार्द्ध के दो अणु पाइरोल व्युत्पन्न में परिवर्तित हो जाते हैं - पोर्फिरिन का अग्रदूत। ग्लोबिन अमीनो एसिड से बनता है, यानी प्रोटीन संश्लेषण के सामान्य तरीके से। जी. का क्षय एरिथ्रोसाइट्स में शुरू होता है, जिससे उनका जीवन चक्र पूरा होता है। हेम को अल्फा-मेथिन ब्रिज के माध्यम से ऑक्सीकृत किया जाता है, जिससे संबंधित पाइरोल रिंगों के बीच का बंधन टूट जाता है।
परिणामी जी. व्युत्पन्न को वर्डोग्लोबिन (हरा रंगद्रव्य) कहा जाता है। यह बहुत अस्थिर है और आसानी से लौह आयन (Fe 3+), डिनेचर्ड ग्लोबिन और बिलीवरडीन में टूट जाता है।
जी के अपचय में हैप्टोग्लोबिन-हीमोग्लोबिन कॉम्प्लेक्स (एचपी-एचबी) का बहुत महत्व है। रक्तप्रवाह में एरिथ्रोसाइट से बाहर निकलने पर, जी एचपी-एचबी कॉम्प्लेक्स में अपरिवर्तनीय रूप से हैप्टोग्लोबिन (देखें) से बंध जाता है। प्लाज्मा में एचपी की पूरी मात्रा समाप्त होने के बाद, जी गुर्दे की समीपस्थ नलिकाओं द्वारा अवशोषित हो जाता है। ग्लोबिन का बड़ा हिस्सा 1 घंटे के भीतर किडनी में टूट जाता है।
एचपी-एचबी कॉम्प्लेक्स में हीम अपचय यकृत, अस्थि मज्जा और प्लीहा की रेटिकुलोएन्डोथेलियल कोशिकाओं द्वारा पित्त वर्णक के निर्माण के साथ किया जाता है (देखें)। इस प्रक्रिया में निकलने वाला लोहा बहुत तेजी से चयापचय पूल में प्रवेश करता है और नए लौह अणुओं के संश्लेषण में उपयोग किया जाता है।
हीमोग्लोबिन सांद्रता निर्धारित करने के तरीके। वेजेज में, अभ्यास में, जी को आमतौर पर सैली हेमोमीटर का उपयोग करके वर्णमिति विधि द्वारा निर्धारित किया जाता है, जो जी से बनने वाले हेमिन की मात्रा को मापने पर आधारित होता है (हीमोग्लोबिनोमेट्री देखें)। हालाँकि, रक्त में बिलीरुबिन और मेथेमोग्लोबिन की सामग्री के साथ-साथ कुछ पैटोल स्थितियों के आधार पर, विधि त्रुटि +30% तक पहुँच जाती है। स्पेक्ट्रोफोटोमेट्रिक अनुसंधान विधियां अधिक सटीक हैं (स्पेक्ट्रोफोटोमेट्री देखें)।
रक्त में कुल हीमोग्लोबिन निर्धारित करने के लिए, सायनमेथेमोग्लोबिन विधि का उपयोग किया जाता है, जो सभी हीमोग्लोबिन डेरिवेटिव (डीऑक्सी-एचबी, एचबीओ 2, एचबीसीओ, मेट-एचबी, आदि) को सियान-मेट-एचबी में बदलने और ऑप्टिकल घनत्व को मापने पर आधारित है। 540 एनएम पर समाधान का. इसी उद्देश्य के लिए, पाइरीडीन-हेमोक्रोमोजेनिक विधि का उपयोग किया जाता है। एचबीओ 2 की सांद्रता आमतौर पर 542 एनएम पर प्रकाश अवशोषण या गैसोमेट्रिक विधि (बाध्य ऑक्सीजन की मात्रा द्वारा) द्वारा निर्धारित की जाती है।
नैदानिक अभ्यास में हीमोग्लोबिन
जी की मात्रात्मक सामग्री और गुणात्मक संरचना का निर्धारण अन्य हेमेटोल के साथ संयोजन में किया जाता है। कई पैथोल्स, लाल रक्त स्थितियों (एनीमिया, एरिथ्रेमिया और माध्यमिक एरिथ्रोसाइटोसिस) के निदान के लिए संकेतक (हेमटोक्रिट, लाल रक्त कोशिकाओं की संख्या, उनकी आकृति विज्ञान, आदि), रक्त हानि की डिग्री का आकलन, निर्जलीकरण के दौरान रक्त का गाढ़ा होना शरीर और जलन, आदि), उपचार के दौरान हीमो-ट्रांसफ्यूजन की प्रभावशीलता का आकलन करने के लिए, आदि।
आम तौर पर, एल. ई. यारुस्तोव्स्काया एट अल के अनुसार, पुरुषों के लिए रक्त में जी की सामग्री औसतन 14.5 + 0.06 ग्राम% (भिन्नता 13.0-16.0 ग्राम%) और महिलाओं के लिए 12.9 + 0.07 ग्राम% (12.0- 14.0 ग्राम%) होती है। (1969); उतार-चढ़ाव शरीर की उम्र और संवैधानिक विशेषताओं, शारीरिक पर निर्भर करता है। गतिविधि, आहार, जलवायु, आसपास की हवा में ऑक्सीजन का आंशिक दबाव। रक्त में जी की सांद्रता एक सापेक्ष मूल्य है, जो न केवल रक्त में कुल जी की पूर्ण मात्रा पर निर्भर करती है, बल्कि प्लाज्मा की मात्रा पर भी निर्भर करती है। रक्त में जी की निरंतर मात्रा के साथ प्लाज्मा की मात्रा में वृद्धि जी का निर्धारण करते समय कम अनुमानित आंकड़े दे सकती है और एनीमिया की नकल कर सकती है।
जी सामग्री के अधिक संपूर्ण मूल्यांकन के लिए, अप्रत्यक्ष संकेतकों का भी उपयोग किया जाता है: रंग संकेतक का निर्धारण, एक लाल रक्त कोशिका में औसत जी सामग्री, हेमटोक्रिट सूचकांक के संबंध में औसत सेलुलर जी एकाग्रता, आदि।
एनीमिया के गंभीर रूपों में होने वाली, रक्त में जी की एकाग्रता में एक निश्चित महत्वपूर्ण मूल्य तक कमी - 2-3 ग्राम% और नीचे (हीमोग्लोबिनोपेनिया, ऑलिगोक्रोमिया) - आमतौर पर मृत्यु की ओर ले जाती है, हालांकि, कुछ प्रकार के क्रोनिक एनीमिया के साथ , व्यक्तिगत रोगी, प्रतिपूरक तंत्र के विकास के कारण, ऐसी एकाग्रता के अनुकूल होते हैं।
पैटोल में, स्थितियां, जी की सामग्री और लाल रक्त कोशिकाओं की संख्या हमेशा समानांतर में नहीं बदलती है, जो एनीमिया के वर्गीकरण में परिलक्षित होती है (एनीमिया के सामान्य, हाइपो- और हाइपरक्रोमिक रूपों को प्रतिष्ठित किया जाता है); एरिथ्रेमिया और सेकेंडरी एरिथ्रोसाइटोसिस की विशेषता जी (हाइपरक्रोमिया) की बढ़ी हुई सांद्रता और एक ही समय में लाल रक्त कोशिकाओं की संख्या में वृद्धि है।
लगभग सारा रक्त ग्लूकोज लाल रक्त कोशिकाओं के अंदर पाया जाता है; इसका एक भाग एचपी-एचबी कॉम्प्लेक्स के रूप में प्लाज्मा में होता है। नि:शुल्क प्लाज्मा ग्लूकोज सामान्यतः 0.02-2.5 मिलीग्राम% होता है (जी.वी. डर्विज़ और एन.के. बयाल्को के अनुसार)। कुछ हेमोलिटिक एनीमिया में प्लाज्मा में मुक्त हेमोलिसिस की मात्रा बढ़ जाती है, जो मुख्य रूप से इंट्रावास्कुलर हेमोलिसिस (हीमोग्लोबिनेमिया देखें) के साथ होती है।
कई सामान्य प्रकार के हीमोग्लोबिन की उपस्थिति के साथ-साथ विभिन्न मूल के असामान्य हीमोग्लोबिन के कुछ रोगों के रक्त में उपस्थिति (हीमोग्लोबिनोपैथी देखें) के कारण, एरिथ्रोसाइट्स में हीमोग्लोबिन की गुणात्मक संरचना निर्धारित करने पर बहुत ध्यान दिया जाता है ("हीमोग्लोबिन सूत्र") ”)। इस प्रकार, जी. प्रकार एचबीएफ और एचबीए2 की बढ़ी हुई मात्रा का पता लगाना आमतौर पर बीटा थैलेसीमिया के कुछ रूपों की विशेषता है।
अन्य हेमेटोल के साथ एचबीएफ सामग्री में भी वृद्धि देखी गई। रोग (तीव्र ल्यूकेमिया, अप्लास्टिक एनीमिया, पैरॉक्सिस्मल नॉक्टर्नल हीमोग्लोबिनुरिया, आदि), साथ ही संक्रामक हेपेटाइटिस, भ्रूण के हीमोग्लोबिन और गर्भावस्था की स्पर्शोन्मुख वंशानुगत दृढ़ता। रक्त में HbA2 अंश की सांद्रता कुछ अस्थिर गैसों और नशे की उपस्थिति में बढ़ जाती है और आयरन की कमी वाले एनीमिया में घट जाती है।
मानव ओण्टोजेनेसिस में परिवर्तन होता है विभिन्न प्रकार केभ्रूण में (18 सप्ताह तक) सामान्य हीमोग्लोबिन पी (आदिम) पाया जाता है; इसकी किस्मों को Hb Gower1 और Hb Gower2 के समान ही नामित किया गया है।
प्राथमिक हेमटोपोइजिस की प्रबलता विटेलिन हेमटोपोइजिस की अवधि से मेल खाती है, और उसके बाद आने वाली हेपेटिक हेमटोपोइजिस की अवधि में, एचबीएफ को मुख्य रूप से संश्लेषित किया जाता है।
अस्थि मज्जा हेमटोपोइजिस की अवधि के दौरान "वयस्क" एचबीए का संश्लेषण तेजी से तेज होता है; नवजात शिशु में एचबीएफ सामग्री जी की कुल मात्रा का 70-90% तक होती है (शेष 10-30% एचबीए अंश पर पड़ता है)। जीवन के पहले वर्ष के अंत तक, एचबीएफ एकाग्रता आमतौर पर 1-2% तक कम हो जाती है, और एचबीए सामग्री तदनुसार बढ़ जाती है।
ज्ञातव्य है कि सेंट. जी के 200 असामान्य (पैथोलॉजिकल या असामान्य) वेरिएंट, जिनकी उपस्थिति ग्लोबिन पॉलीपेप्टाइड श्रृंखलाओं के निर्माण में विभिन्न वंशानुगत दोषों के कारण होती है।
एल पॉलिंग, इटानो (एन. ए. इटानो) और अन्य की खोज। 1949 में पैटोल, हीमोग्लोबिन एस (अंग्रेजी: सिकल सेल सिकल सेल) ने आणविक रोगों के अध्ययन की नींव रखी। लाल रक्त कोशिकाओं में असामान्य रक्त कोशिकाओं की उपस्थिति आमतौर पर (लेकिन हमेशा नहीं) वंशानुगत हेमोलिटिक एनीमिया सिंड्रोम के विकास की ओर ले जाती है (देखें)।
वर्णित अधिकांश हीमोग्लोबिन वेरिएंट को पैथोलॉजिकल नहीं, बल्कि जी एस शहद के दुर्लभ असामान्य रूप माना जाना चाहिए। हीमोग्लोबिन एस, सी, डी, ई, बार्ट, एच, एम और अस्थिर हीमोग्लोबिन के एक बड़े समूह (लगभग 60) का एक निश्चित महत्व होता है, अस्थिर हीमोग्लोबिन को असामान्य हीमोग्लोबिन कहा जाता है, जिसके परिणामस्वरूप अमीनो एसिड में से एक को प्रतिस्थापित किया जाता है , अणु ऑक्सीकरण एजेंटों, हीटिंग और कई अन्य कारकों की कार्रवाई के प्रति अस्थिर हो जाता है। जीएम-समूह हेम-ग्लोबिन संपर्कों के क्षेत्र में पॉलीपेप्टाइड श्रृंखलाओं में अमीनो एसिड प्रतिस्थापन के परिणामस्वरूप उत्पन्न होते हैं, जिससे न केवल अणु की अस्थिरता होती है, बल्कि मेथेमोग्लोबिन गठन की प्रवृत्ति भी बढ़ जाती है। एम-हीमोग्लोबिनोपैथी अक्सर वंशानुगत मेथेमोग्लोबिनेमिया का कारण होता है (देखें)।
जी का वर्गीकरण प्रारंभ में उन्हें लैटिन वर्णमाला के अक्षरों से खोलने के क्रम में चित्रित करने पर आधारित था; सामान्य "वयस्क" जी के लिए एक अपवाद बनाया गया है, जिसे अक्षर ए और भ्रूण जी (एचबीएफ) द्वारा निर्दिष्ट किया गया है। अक्षर S असामान्य सिकल सेल G. (HbB का पर्यायवाची) को इंगित करता है। इस प्रकार, ए से एस तक लैटिन वर्णमाला के अक्षरों को एक्स इंटरनेशनल हेमेटोल में अपनाए गए एक के अनुसार जी के आम तौर पर स्वीकृत पदनाम माना जाता था। कांग्रेस (स्टॉकहोम, 1964) जी. नामकरण के बाद से नए वेरिएंट को नामित करने के लिए वर्णमाला के शेष अक्षरों का उपयोग करने की अनुशंसा नहीं की जाती है।
अब जी के नए खोजे गए रूपों को शहर (क्षेत्र), अस्पताल या प्रयोगशाला के नाम का उपयोग करके खोज के स्थान के आधार पर नाम देने की प्रथा है जहां नए जी की पहली बार खोज की गई थी, और इसके जैव रासायनिक सूत्र, स्थान का संकेत (कोष्ठकों में) दिया गया है। और प्रभावित सर्किट में अमीनो एसिड प्रतिस्थापन की प्रकृति। उदाहरण के लिए, एचबी कोलन (अल्फा 2 बीटा 2 98 वैल->मेट) का मतलब है कि हीमोग्लोबिन कोलन में मेथिओनिन के साथ अमीनो एसिड वेलिन की बीटा पॉलीपेप्टाइड श्रृंखलाओं में से एक के 98 वें स्थान पर प्रतिस्थापन हुआ था।
जी की सभी किस्में भौतिक और रासायनिक विशेषताओं में एक दूसरे से भिन्न होती हैं। और शारीरिक गुण, और कुछ कार्यात्मक गुणों द्वारा भी, जिस पर क्लिनिक में जी के विभिन्न प्रकारों का पता लगाने के तरीके आधारित हैं। ऑक्सीजन के प्रति परिवर्तित आकर्षण वाली असामान्य गैसों के एक नए वर्ग की खोज की गई है। जी की टाइपिंग वैद्युतकणसंचलन और कई अन्य प्रयोगशाला विधियों (क्षार प्रतिरोध और थर्मल विकृतीकरण, स्पेक्ट्रोफोटोमेट्री, आदि के लिए परीक्षण) का उपयोग करके की जाती है।
उनकी इलेक्ट्रोफोरेटिक गतिशीलता के आधार पर, जी को तेज गति से चलने वाली, धीमी गति से चलने वाली और सामान्य (एचबीए के समान गतिशीलता वाली) में विभाजित किया गया है। हालाँकि, अमीनो एसिड अवशेषों को बदलने से हमेशा अणु के आवेश में बदलाव नहीं होता है, इसलिए इलेक्ट्रोफोरेसिस का उपयोग करके कुछ वेरिएंट का पता नहीं लगाया जा सकता है।
फोरेंसिक चिकित्सा में हीमोग्लोबिन
फॉरेंसिक मेडिसिन में जी और इसके डेरिवेटिव का निर्धारण जी में परिवर्तन का कारण बनने वाले पदार्थों के साथ विषाक्तता का निदान करते समय भौतिक साक्ष्य या किसी भी तरल पदार्थ में रक्त की उपस्थिति स्थापित करने के लिए किया जाता है, ताकि भ्रूण या नवजात शिशु के रक्त को एक वयस्क के रक्त से अलग किया जा सके। . विवादित पितृत्व, मातृत्व और बच्चों के प्रतिस्थापन की जांच में वंशानुगत विशेषताओं के उपयोग के साथ-साथ भौतिक साक्ष्य के आधार पर रक्त को अलग-अलग करने के प्रमाण हैं।
जानवरों को मानव हीमोग्लोबिन से प्रतिरक्षित करके, हीमोग्लोबिन-अवक्षेपण सीरा प्राप्त किया गया। इन सीरा की मदद से जी पर जांचे गए दाग में मानव रक्त की उपस्थिति स्थापित की जा सकती है।
दागों में रक्त की उपस्थिति निर्धारित करने के लिए, माइक्रोस्पेक्ट्रल विश्लेषण और माइक्रोक्रिस्टलाइन प्रतिक्रियाओं का उपयोग किया जाता है। पहले मामले में, हेमोक्रोमोजन को क्षार और एक कम करने वाले एजेंट द्वारा हेमोक्रोमोजन में परिवर्तित किया जाता है, जिसमें एक विशिष्ट अवशोषण स्पेक्ट्रम होता है (हेमोक्रोमोजन देखें), या हेमोक्रोमोजन पर केंद्रित सल्फ्यूरिक एसिड द्वारा कार्य किया जाता है, जिससे हेमेटोपोर्फिरिन का निर्माण होता है स्पेक्ट्रम के दृश्य भाग में विशिष्ट अवशोषण स्पेक्ट्रम।
रक्त की उपस्थिति निर्धारित करने के लिए माइक्रोक्रिस्टलाइन प्रतिक्रियाओं में से, हेमोक्रोमोजन और हेमिन हाइड्रोक्लोराइड के क्रिस्टल के उत्पादन पर आधारित परीक्षण सबसे अधिक बार उपयोग किए जाते हैं। जी के लिए जांचे गए दाग वाले ऊतक से हेमिन क्रिस्टल प्राप्त करने के लिए, एक धागा लें और इसे एक ग्लास स्लाइड पर रखें, इसमें सोडियम क्लोराइड के कई क्रिस्टल और केंद्रित एसिटिक एसिड (टीचमैन के अभिकर्मक) की कुछ बूंदें मिलाएं। गर्म करने पर (रक्त की उपस्थिति में), जी से हेमिन हाइड्रोक्लोराइड (टीचमैन क्रिस्टल) के क्रिस्टल - भूरे रंग के तिरछे समांतर चतुर्भुज - बनते हैं, कभी-कभी जी से आयोडीन-हेमिन क्रिस्टल प्राप्त करने के लिए प्रतिक्रियाओं का उपयोग किया जाता है - आकार में छोटे काले क्रिस्टल समचतुर्भुज प्रिज्म.
कुछ विषाक्तता के दौरान रक्त में जी के व्युत्पन्न स्पेक्ट्रोस्कोपी से पाए जाते हैं। उदाहरण के लिए, कार्बन मोनोऑक्साइड विषाक्तता के मामले में, पीड़ितों के रक्त में कार्बोक्सीहीमोग्लोबिन पाया जाता है; मेथेमोग्लोबिन बनाने वाले पदार्थों के साथ विषाक्तता के मामले में, मेथेमोग्लोबिन का पता लगाया जाता है।
शिशुहत्या के मामलों में, विभिन्न भौतिक साक्ष्यों पर नवजात या भ्रूण के रक्त की उपस्थिति स्थापित करना आवश्यक हो सकता है। चूंकि भ्रूण और नवजात शिशु के रक्त में एचबीएफ और एक वयस्क के रक्त में एचबीए की उच्च सामग्री होती है, इसलिए वे अपने भौतिक और रासायनिक गुणों से अलग होते हैं। नवजात शिशु (भ्रूण) और एक वयस्क के गुण, जी को आसानी से अलग किया जा सकता है।
व्यवहार में, क्षारीय विकृतीकरण का सबसे अधिक उपयोग किया जाता है, क्योंकि भ्रूण ग्रंथि वयस्क ग्रंथि की तुलना में क्षार की क्रिया के प्रति अधिक प्रतिरोधी होती है। जी के परिवर्तन स्पेक्ट्रोस्कोपी, स्पेक्ट्रोफोटोमेट्रिक या फोटोमेट्रिक रूप से निर्धारित होते हैं।
पॉलीपेप्टाइड श्रृंखलाओं का संश्लेषण संरचनात्मक और (संभवतः) नियामक जीन के नियंत्रण में किया जाता है। संरचनात्मक जीन पॉलीपेप्टाइड श्रृंखलाओं के विशिष्ट अमीनो एसिड अनुक्रम को निर्धारित करते हैं, जबकि नियामक जीन उनके संश्लेषण की दर निर्धारित करते हैं (जीन देखें)।
मनुष्यों में मौजूदा 6 प्रकार की सामान्य जी श्रृंखलाएं (Hbα, Hbβ, Hbγ, Hbδ, Hbε, Hbζ) क्रमशः 6 जीन लोकी (α, β, γ, δ, ε, ζ) द्वारा एन्कोड की जाती हैं। ऐसा माना जाता है कि α श्रृंखलाओं के लिए दो लोकी हो सकते हैं। इसके अलावा, 5 अलग-अलग γ-चेन की खोज की गई, जो अलग-अलग लोकी द्वारा एन्कोड किए गए हैं। इस प्रकार, कुल मिलाकर, एक व्यक्ति में 7 से 10 जोड़े संरचनात्मक जीन हो सकते हैं जो जी के संश्लेषण को नियंत्रित करते हैं।
विकास के चरणों के अध्ययन से पता चला है कि मनुष्यों में गर्भाशय जीवन के पहले भाग में विभिन्न जी के संश्लेषण का एक स्पष्ट और अच्छी तरह से संतुलित आनुवंशिक विनियमन होता है। गिरफ्तार. α, γ, ζ, ε-चेन की लोकी (भ्रूण के जीवन की प्रारंभिक अवधि में केवल थोड़े समय के लिए)। जन्म के बाद, गामा चेन लोकस के बंद होने के साथ-साथ, β और δ चेन लोकी सक्रिय हो जाते हैं। इस स्विच के परिणामस्वरूप, भ्रूण के हीमोग्लोबिन (HbF) को वयस्क हीमोग्लोबिन - HbA द्वारा HbA2 के एक छोटे अंश के साथ प्रतिस्थापित किया जाता है।
अस्पष्ट प्रश्न बने हुए हैं: जीन लोकी का स्थान जो गुणसूत्रों पर जी के संश्लेषण को निर्धारित करता है, उनका जुड़ाव, विशिष्ट सक्रियण की निर्भरता और नियामक जीन की कार्रवाई पर ओटोजेनेसिस की अवधि के साथ जुड़े जी के संरचनात्मक जीन का दमन, हास्य कारकों का प्रभाव (उदाहरण के लिए, हार्मोन), आदि।
ग्लोबिन श्रृंखलाओं का संश्लेषण कोशिका में प्रोटीन संश्लेषण का एक विशेष उदाहरण है।
यद्यपि जी. संश्लेषण के नियमन में अभी भी बहुत कुछ अस्पष्ट है, प्रमुख तंत्र वे प्रतीत होते हैं जो डीएनए से एमआरएनए (मैसेंजर आरएनए) के प्रतिलेखन की दर को नियंत्रित करते हैं। ग्लोबिन संश्लेषण के लिए विशेष रूप से जिम्मेदार डीएनए का सटीक लक्षण वर्णन प्राप्त नहीं किया गया है। हालाँकि, 1972 में, कई प्रयोगशालाएँ एक साथ एक जीन को संश्लेषित करने में सफल रहीं जो जी के संश्लेषण को नियंत्रित करता है। यह एंजाइम रिवर्स ट्रांसक्रिपटेस (जेनेटिक इंजीनियरिंग देखें) का उपयोग करके किया गया था।
जी. अणु के हीम भाग को एक श्रृंखला का उपयोग करके अलग से संश्लेषित किया जाता है एंजाइमेटिक प्रतिक्रियाएँ, क्रेब्स चक्र से सक्रिय सक्सिनेट (स्यूसिनिक एसिड) से शुरू होता है और केंद्र में एक लोहे के परमाणु के साथ एक जटिल प्रोटोपोर्फिरिन रिंग के साथ समाप्त होता है।
प्रोटीन संश्लेषण की प्रक्रिया के दौरान, ग्लोबिन श्रृंखलाएं अपना विशिष्ट विन्यास ले लेती हैं, और हीम को एक विशेष जेब में "डाला" जाता है। इसके बाद, टेट्रामर बनाने के लिए पूर्ण श्रृंखलाओं का संयोजन होता है।
विशिष्ट डीएनए का संश्लेषण एरिथ्रोसाइट्स के अग्रदूतों में केवल ऑर्थोक्रोमिक नॉर्मोब्लास्ट चरण तक होता है। इस अवधि के दौरान, ग्लोबिन की पॉलीपेप्टाइड श्रृंखलाओं का अंतिम सेट बनाया जाता है, इसे हीम के साथ जोड़ा जाता है, और सभी प्रकार के आरएनए और आवश्यक एंजाइम बनते हैं।
जी. संश्लेषण के वंशानुगत विकारों को दो बड़े समूहों में विभाजित किया गया है:
1)तथाकथित हीमोग्लोबिन की प्राथमिक संरचना के संरचनात्मक वेरिएंट या विसंगतियाँ - "गुणात्मक" हीमोग्लोबिनोपैथी जैसे एचबी, एस, सी, डी, ई, एम, साथ ही अस्थिर हीमोग्लोबिन और ओ 2 के लिए बढ़ी हुई आत्मीयता के साथ हीमोग्लोबिनोपैथी के कारण होने वाली बीमारियाँ (हीमोग्लोबिनोपैथी देखें),
2) ग्लोबिन की पॉलीपेप्टाइड श्रृंखलाओं में से एक के संश्लेषण की बिगड़ा दर के परिणामस्वरूप उत्पन्न होने वाली स्थितियाँ - "मात्रात्मक" हीमोग्लोबिनोपैथी या थैलेसीमिया (देखें)।
संरचनात्मक वेरिएंट के साथ, जी अणु की स्थिरता और कार्य बदल सकता है। थैलेसीमिया में, ग्लोबिन की संरचना सामान्य हो सकती है। चूँकि दोनों प्रकार के आनुवंशिक दोष कई मानव आबादी में आम हैं, ऐसे व्यक्ति जो जी के संरचनात्मक संस्करण और थैलेसीमिया के लिए एक साथ विषमयुग्मजी होते हैं, अक्सर देखे जाते हैं। विभिन्न जीनों का संयोजन हीमोग्लोबिनोपैथियों का एक बहुत ही जटिल स्पेक्ट्रम बनाता है। कुछ मामलों में, उत्परिवर्तन जी. के संश्लेषण को बदलने के तंत्र को प्रभावित कर सकता है, जो उदाहरण के लिए, वयस्कों में भ्रूण जी. के संश्लेषण को जारी रखने की ओर ले जाता है। इन स्थितियों को सामूहिक रूप से भ्रूण के हीमोग्लोबिन की वंशानुगत दृढ़ता कहा जाता है।
फ़्यूज़न वेरिएंट में एचबी लेपोर, एंटी-लेपोर और केन्या म्यूटेंट शामिल हैं। यह सबसे अधिक संभावना है कि जी की ये संरचनात्मक विसंगतियाँ बारीकी से जुड़े जी जीनों के बीच असमान गैर-समरूप अर्धसूत्रीविभाजन के परिणामस्वरूप उत्पन्न हुईं, उदाहरण के लिए, एचबी लेपोर में α-श्रृंखलाएं सामान्य हैं, और अन्य पॉलीपेप्टाइड श्रृंखलाएं हैं। इसमें δ- अनुक्रम का भाग और β- अनुक्रम पॉलीपेप्टाइड श्रृंखला का भाग शामिल होता है।
चूँकि उत्परिवर्तन किसी भी जीन में हो सकता है जो जीन के संश्लेषण को निर्धारित करता है, कई स्थितियाँ उत्पन्न हो सकती हैं जिनमें व्यक्ति एक या अधिक लोकी में असामान्य जीन के एलील के लिए होमोज़ायगोट्स, हेटेरोज़ायगोट्स या डबल हेटेरोज्यगोट्स होंगे।
जी के 200 से अधिक संरचनात्मक रूप ज्ञात हैं, उनमें से 120 से अधिक की विशेषता बताई गई है, और कई मामलों में जी के संरचनात्मक परिवर्तन को इसके असामान्य कार्य के साथ जोड़ना संभव हो गया है। एक बिंदु उत्परिवर्तन (आनुवंशिक कोड में एकल आधार का प्रतिस्थापन) के परिणामस्वरूप जी के एक नए संस्करण के उद्भव के लिए सबसे सरल तंत्र को एचबीएस (योजना) के उदाहरण का उपयोग करके प्रदर्शित किया जा सकता है।
भौतिक-रासायनिक पर अमीनो एसिड प्रतिस्थापन का प्रभाव। जी अणु के गुण, स्थिरता और कार्य पिछले अमीनो एसिड की जगह लेने वाले अमीनो एसिड के प्रकार और अणु में उसकी स्थिति पर निर्भर करते हैं। कई उत्परिवर्तन (लेकिन सभी नहीं) हीमोग्लोबिन अणु (एचबीएम, अस्थिर हीमोग्लोबिन, ओ 2 के लिए परिवर्तित आत्मीयता वाले हीमोग्लोबिन) या इसके विन्यास और कई भौतिक-रासायनिक के कार्य और स्थिरता को महत्वपूर्ण रूप से बदलते हैं। गुण (एचबीएस और एचबीसी)।
हीमोग्लोबिन अस्थिर होते हैं
अस्थिर हीमोग्लोबिन असामान्य हीमोग्लोबिन का एक समूह है जो विशेष रूप से ऑक्सीकरण एजेंटों, गर्मी और कई अन्य कारकों की कार्रवाई के प्रति संवेदनशील होता है, जिसे उनके अणुओं में कुछ अमीनो एसिड अवशेषों के दूसरों के साथ आनुवंशिक रूप से निर्धारित प्रतिस्थापन द्वारा समझाया जाता है; ऐसे हीमोग्लोबिन का वहन अक्सर हीमोग्लोबिनोपैथी के रूप में प्रकट होता है (देखें)।
उन लोगों के एरिथ्रोसाइट्स में जो अस्थिर जी के वाहक हैं, तथाकथित। हेंज निकाय, जो अस्थिर रक्त कोशिकाओं (हेंज निकायों के साथ जन्मजात हेमोलिटिक एनीमिया) के विकृत अणुओं का संचय हैं। 1952 में, आई. ए. कैथी ने सुझाव दिया कि यह बीमारी वंशानुगत थी। फ्रिक (पी. फ्रिक), गिट्ज़िग (डब्ल्यू. एच. हिट्ज़िग) और वेटके (के. बेटके) ने 1962 में पहली बार एचबी ज्यूरिख के उदाहरण का उपयोग करते हुए साबित किया कि हेंज शरीर में हेमोलिटिक एनीमिया अस्थिर हीमोग्लोबिन की उपस्थिति से जुड़ा है। कैरेल (आर. डब्ल्यू. कैरेल) और जी. लेहमैन ने 1969 में ऐसी हीमोग्लोबिनोपैथियों के लिए एक नया नाम प्रस्तावित किया - अस्थिर जी के संचरण के कारण होने वाला हेमोलिटिक एनीमिया।
हीम अणुओं की अस्थिरता हीम के संपर्क में अमीनो एसिड अवशेषों के प्रतिस्थापन के कारण हो सकती है; एक गैर-ध्रुवीय अमीनो एसिड अवशेष को एक ध्रुवीय के साथ बदलना; प्रोलिन अवशेष के साथ किसी अमीनो एसिड अवशेष के प्रतिस्थापन के कारण अणु की द्वितीयक संरचना का उल्लंघन; α1β1- और α2β2-संपर्कों के क्षेत्र में अमीनो एसिड अवशेषों का प्रतिस्थापन, जिससे हीमोग्लोबिन अणु का मोनोमर्स और डिमर्स में पृथक्करण हो सकता है; कुछ अमीनो एसिड अवशेषों का विलोपन (नुकसान); सबयूनिट का बढ़ाव, उदाहरण के लिए, दो अस्थिर हीमोग्लोबिन - एचबी क्रैन्सटन और एचबी टाक में उनके सी-टर्मिनस से जुड़े हाइड्रोफोबिक खंड के कारण सामान्य हीमोग्लोबिन की तुलना में लंबी बीटा श्रृंखलाएं होती हैं।
अस्थिर गैसों का वर्गीकरण, जे.
लगभग वर्णित है. 90 अस्थिर जी., और जी. अणु की बीटा श्रृंखलाओं में अमीनो एसिड अवशेषों के प्रतिस्थापन वाले वेरिएंट अल्फा श्रृंखलाओं में ऐसे अवशेषों के प्रतिस्थापन की तुलना में लगभग 4 गुना अधिक पाए जाते हैं।
अस्थिर जी का वहन एक ऑटोसोमल प्रमुख तरीके से विरासत में मिला है, और वाहक हेटेरोज़ायगोट्स हैं। कुछ मामलों में, अस्थिर जी के परिवहन की घटना एक सहज उत्परिवर्तन का परिणाम है। जी की स्थिरता में कमी से न केवल इसकी आसानी से वर्षा होती है, बल्कि कुछ मामलों में हीम की हानि भी होती है। हीमोग्लोबिन अणु के ए- और (3-श्रृंखला) के संपर्क बिंदुओं पर अमीनो एसिड अवशेषों का प्रतिस्थापन ऑक्सीजन के लिए अणु की आत्मीयता, हीम की परस्पर क्रिया और हीमोग्लोबिन के टेट्रामर्स, डिमर्स और मोनोमर्स के बीच संतुलन को प्रभावित कर सकता है। अस्थिर हीमोग्लोबिन के लिए जीन के लिए विषमयुग्मजी लोग, सामान्य और असामान्य दोनों, अस्थिर जी।, हालांकि, बाद वाला जल्दी से विकृत हो जाता है और कार्यात्मक रूप से निष्क्रिय हो जाता है।
गंभीर हेमोलिटिक एनीमिया आमतौर पर उन रोगियों में देखा जाता है जो उच्च स्तर की आणविक अस्थिरता के साथ अस्थिर जी के वाहक होते हैं।
अन्य अस्थिर जी. वेज ले जाने पर, अभिव्यक्तियाँ आमतौर पर मध्यम गंभीरता या पूरी तरह से महत्वहीन होती हैं। कुछ मामलों में (एचबी रिवरडेल-ब्रोंक्स, एचबी ज्यूरिख, आदि), अस्थिर जी का वहन कुछ दवाएं (सल्फोनामाइड्स, एनाल्जेसिक, आदि) लेने या संक्रमण के संपर्क में आने के बाद हेमोलिटिक संकट के रूप में प्रकट होता है। कुछ मरीज़, उदाहरण के लिए, एचबी हैमरस्मिथ, एचबी ब्रिस्टल, एचबी सिडनी आदि के वाहक, मेट- और सल्फ़हीमोग्लोबिन के बढ़ते गठन के कारण त्वचा के सायनोसिस का अनुभव करते हैं। अस्थिर जी के परिवहन के कारण होने वाली हीमोग्लोबिनोपैथियों को अन्य एटियलजि के हेमोलिटिक और हाइपोक्रोमिक एनीमिया से अलग किया जाना चाहिए और, सबसे पहले, आयरन की कमी और पेंटोस-फॉस्फेट चक्र, ग्लाइकोलाइसिस, आदि के एंजाइमों की आनुवंशिक रूप से निर्धारित कमी से जुड़े हेमोलिटिक एनीमिया के साथ।
अधिकांश लोग जो अस्थिर जी के वाहक हैं, उन्हें विशेष उपचार की आवश्यकता नहीं होती है। हेमोलिसिस के लिए, पुनर्स्थापना चिकित्सा उपयोगी है। अस्थिर जी के सभी वाहकों को हेमोलिसिस (सल्फोनामाइड्स, सल्फोन्स, एनाल्जेसिक इत्यादि) को उत्तेजित करने वाली ऑक्सीकरण दवाओं से परहेज करने की सिफारिश की जाती है। रक्त आधान का संकेत केवल गहरे एनीमिया के विकास के साथ ही दिया जाता है। प्लीहा और हाइपरस्प्लेनिज़्म द्वारा लाल रक्त कोशिकाओं के बढ़ते अनुक्रम के साथ गंभीर हेमोलिसिस के मामले में, स्प्लेनेक्टोमी का संकेत दिया जाता है (देखें)। हालाँकि, सेप्टिसीमिया विकसित होने के जोखिम के कारण आमतौर पर बच्चों (6 वर्ष से कम उम्र) में स्प्लेनेक्टोमी नहीं की जाती है।
अस्थिर हीमोग्लोबिन की पहचान के तरीके
इसकी अस्थिरता की पहचान के लिए हीमोग्लोबिन थर्मोलेबिलिटी का अध्ययन सबसे महत्वपूर्ण परीक्षण है। इसे 1962 में ए.जी. ग्रिम्स और ए. मीस्लर और 1964 में डेसी द्वारा प्रस्तावित किया गया था और इसमें एक घंटे के लिए 50-60° पर 0.1 एम फॉस्फेट या ट्रिस-एचसीएल बफर, पीएच 7.4 के साथ पतला हेमोलिसेट्स शामिल है। इस मामले में, अस्थिर ग्लाइकोसाइड विकृत और अवक्षेपित होते हैं, और समाधान में शेष थर्मोस्टेबल हाइड्रॉक्साइड की मात्रा 541 एनएम पर स्पेक्ट्रोफोटोमेट्रिक रूप से निर्धारित की जाती है और सूत्र का उपयोग करके गणना की जाती है:
/ * 100 = = थर्मोस्टेबल हीमोग्लोबिन (प्रतिशत),
जहां ई 541 एनएम की तरंग दैर्ध्य पर विलुप्त होने का मान है।
थर्मोलैबाइल जी की सापेक्ष सामग्री 100% के बराबर है - थर्मोस्टेबल जी की मात्रा (प्रतिशत में)।
कैरेल और के (आर. काउ) ने 1972 में हेमोलिसेट्स को 17% आइसोप्रोपेनॉल-ट्रिस बफर, पीएच 7.4 के मिश्रण में 30 मिनट के लिए 37° पर इनक्यूबेट करने का प्रस्ताव रखा।
एरिथ्रोसाइट्स का हेमोलिसिस पानी के कारण हो सकता है, क्योंकि इस उद्देश्य के लिए कार्बन टेट्राक्लोराइड या क्लोरोफॉर्म के उपयोग से अस्थिर रक्त कोशिकाओं का आंशिक विकृतीकरण होता है और प्राप्त आंकड़ों का विरूपण होता है।
अस्थिर जी के निर्धारण के लिए सबसे आम तरीका हिस्टोकेमिकल है, हेंज निकायों की पहचान करने की विधि। इस मामले में, लाल रक्त कोशिकाओं को क्रिस्टल वायलेट, मिथाइल वायलेट से रंग दिया जाता है, या एसिटाइलफेनिलहाइड्रेज़िन के साथ प्रतिक्रिया का उपयोग किया जाता है। रक्त को प्रारंभिक तौर पर 24 घंटे के लिए 37° पर रखा जाता है। यह ध्यान में रखा जाना चाहिए कि हेंज बॉडी अन्य हेमोलिटिक एनीमिया, थैलेसीमिया, मेथेमोग्लोबिन बनाने वाले एजेंटों के साथ विषाक्तता और कुछ एंजाइमोपैथी में भी पाई जा सकती है।
कागज या सेल्युलोज एसीटेट पर हेमोलिसेट्स का इलेक्ट्रोफोरेटिक पृथक्करण अक्सर परिणाम नहीं देता है, क्योंकि कई अस्थिर हेमोलिसेट्स में, अणु में अमीनो एसिड अवशेषों के प्रतिस्थापन से अणु के इलेक्ट्रोफोरेटिक गुण नहीं बदलते हैं। इस संबंध में अधिक जानकारीपूर्ण पॉलीएक्रिलामाइड और स्टार्च जैल में इलेक्ट्रोफोरेसिस (इलेक्ट्रोफोरेसिस देखें) या आइसोइलेक्ट्रिक फोकसिंग हैं।
कई रोगियों में जो अस्थिर जी के वाहक हैं, मूत्र लगातार या कभी-कभी डिपाइरोल्स के गठन के कारण गहरे रंग का हो जाता है, जो एरिथ्रोसाइट्स में अस्थिर जी की उपस्थिति का काफी सटीक संकेत के रूप में कार्य करता है।
ग्रंथ सूची: व्लादिमीरोव जी.ई. और पेंटेलेवा एन.एस. कार्यात्मक जैव रसायन, एल., 1965; और आर और एल. आई. हीमोग्लोबिन और उनके गुण, एम., 1975, ग्रंथ सूची; कोरज़ुएव पी. ए. हीमोग्लोबिन, एम., 1964, ग्रंथ सूची; कुशकोवस्की एम.एस. हीमोग्लोबिन क्षति के नैदानिक रूप, एल., 1968; पेरू टीसी एम. हीमोग्लोबिन अणु, पुस्तक में: अणु और कोशिकाएं, संस्करण। जी. एम. फ्रैंक, ट्रांस. अंग्रेजी से, पी. 7, एम., 1966; टी यू-एम और एन के बारे में ए.के. सामग्री साक्ष्य की फोरेंसिक मेडिकल जांच के बुनियादी सिद्धांत, एम., 1975, ग्रंथ सूची; उसपेन्स्काया वी.डी. हैप्टोग्लोबिन के संश्लेषण और अपचय के स्थान और हीमोग्लोबिन चयापचय में इसकी भूमिका पर, वोप्र। शहद। रसायन विज्ञान, खंड 16, संख्या 3, पृ. 227, 1970, ग्रंथ सूची; हैरिस जी. मानव जैव रासायनिक आनुवंशिकी के बुनियादी सिद्धांत, ट्रांस। अंग्रेजी से, पी. 15, एम., 1973; शेरोनोव यू. और शेरोनोवा एन. ए. हीमोग्लोबिन की संरचना और कार्य, आणविक बायोल, वी. 9, संख्या 1, पी। 145, 1975, ग्रंथ सूची; सी एच ए जी ए सी एच ई एस. परिवर्तित ऑक्सीजन बन्धुता के साथ हीमोग्लोबिन, क्लिन। हेमेट., वी. 3, पृ. 357, 1974, ग्रंथ सूची; गिब्लेट ई.आर. मानव रक्त में जेनेटिक मार्कर, फिलाडेल्फिया, 1969; हीमोग्लोबिन और लाल कोशिका संरचना और कार्य, एड। जी.जे. ब्रेवर द्वारा, एन.वाई.-एल., 1972; ह्युहेन्सई. आर. हीमोग्लोबिन अल्फा-चेन संश्लेषण का आनुवंशिक नियंत्रण, हेमेटोलोगिया, वी. 8, पृ. 61, 1974, ग्रंथ सूची; लेह-मानएच. एक। हंट एस एम ए एन आर. जी. मैन्स हीमोग्लोबिन्स, फिलाडेल्फिया, 1974; पी-आर यू टी जेड एम. एफ. क्रोनियन व्याख्यान, 1968, हीमोग्लोबिन अणु, प्रोक, रॉय, समाज। वी., वी. 173, पृ. 113, 1969; पी ई रुत ज़ एम. एफ* ए. लेहमैन एच. मानव हीमोग्लोबिन की आणविक विकृति विज्ञान, प्रकृति (लंदन), वी. 219, पृ. 902, 1968; रफटनएफ. जे. ऑक्सीजन, कार्बन डाइऑक्साइड और हीमोग्लोबिन, बायोकेम की परस्पर क्रिया पर कुछ हालिया काम। जे., वी. 117, पृ. 801, 1970;एस टी ए एम ए-टोयानोपोनलोस जी. ए. NuteP. ई. हीमोग्लोबिन का आनुवंशिक नियंत्रण, क्लिन। हेमेट., वी. 3, पृ. 251, 1974, ग्रंथ सूची; वैन असेंडेलफ़्ट ओ. डब्ल्यू. हीमोग्लोबिन डेरिवेटिव्स की स्पेक्ट्रोफोटोमेट्री, एसेन, 1970; हीमोग्लोबिन, ब्रिट, मेड के कुछ विकारों के लिए वेदरॉल डी. जे. आणविक आधार। जे., वी. 4, पृ. 451, 516, 1974; वेदरॉल डी. जे. ए. क्लेग जे.बी. थैलेसीमिया का आणविक आधार, ब्रिटेन। जे. हेमेट., वी. 31, सप्ल., पृ. 133, 1975; विंट्रो-बी ई एम.एम. क्लिनिकल हेमेटोलॉजी, फिलाडेल्फिया, 1974।
हीमोग्लोबिन अस्थिर होते हैं- डिडकोवस्की एन.ए. एट अल। हीमोग्लोबिन वोल्गा फीट 27 (बी9) ऐलेनिन->एसपारटिक एसिड (गंभीर अस्थिरता के साथ नया असामान्य हीमोग्लोबिन), समस्याएं, हेमटोल, और अतिप्रवाह, रक्त, खंड 22, संख्या 4, पी। 30, 1977, ग्रंथ सूची; आई डी ई एल एल-एस ओ एन एल. आई., डिडकोवस्की एन. ए. और एर्मिलचेंको जी. वी. हेमोलिटिक एनीमिया, एम., 1975, बिब्लियोग्र.; यू एन एन एच. एफ. में, बी. जी. ए को भूल जाओ। आर ए एन एन ई वाई एच. एम. मानव हीमोग्लोबिन, फिलाडेल्फिया, 1977, ग्रंथ सूची; लेहमैन एच. ए. के वाई-एन ओ विद एच. पी. ए. मानव हीमोग्लोबिन वेरिएंट और उनकी विशेषताएं, एम्स्टर्डम, 1976।
ए.पी. एंड्रीवा; यू. एन. टोकरेव (रत्न और जीन.), ए. के. तुमानोव (अदालत); यू. एन. टोकरेव, वी. एम. बेलोस्टोत्स्की।
रसायन विज्ञान की बुनियादी अवधारणाएँ और नियम।
मोलर द्रव्यमान, पदार्थ की मात्रा, अवोगाद्रो स्थिरांक।
गैस का मोलर आयतन.
I. किसी पदार्थ की संरचनात्मक इकाई के द्रव्यमान की गणना।
9 ग्राम पानी के नमूने में हाइड्रोजन परमाणुओं की संख्या निर्धारित करें।
M(H2O) = 18 g\mol
n(H2O) = 9/18= 0.5 मोल
सूत्र से यह पता चलता है कि H2O के 1 मोल में 2 मोल हाइड्रोजन परमाणु होते हैं, अर्थात। n(H) = 2×0.5 mol = 1 mol.
अमोनियम हाइड्रोजन फॉस्फेट के 26.4 ग्राम नमूने में हाइड्रोजन परमाणुओं की संख्या निर्धारित करें।
M(NH4)2HPO4 = 132 g\mol
n((NH4)2HPO4) = 26.4/132= 0.2 mol
n(H) =0.2×9= 1.8 मोल
उत्तर: 1.8 मोल
मिश्रण में इथेनॉल C2H5OH है जिसका वजन 46 ग्राम है और पानी का वजन 72 ग्राम है। मिश्रण में ऑक्सीजन परमाणुओं की संख्या निर्धारित करें।
n(C2H5OH) = 46/46 = 0.1 मोल n(O) =0.1×1= 0.1 मोल
n(H2O) =72/18 = 0.4 मोल n(O) =0.4×1= 0.4 मोल n(O) =0.1+0.4=0.5 मोल
मिश्रण में एसिटिक एसिड CH3COOH का वजन 6 ग्राम और फॉर्मिक एसिड HCOOH का वजन 9.2 ग्राम है। मिश्रण में ऑक्सीजन परमाणुओं की संख्या निर्धारित करें।
n(CH3COOH) =6 /60 = 0.1 मोल n(O) =0.1×2= 0.2 मोल
n(HCOOH) =9.2/46 = 0.2 मोल n(O) =0.2×2= 0.4 मोल n(O) =0.2+0.4=0.6 मोल
12.04 1022 पानी के अणुओं वाले पानी के नमूने का द्रव्यमान निर्धारित करें।
n(H2O) = NNA= 12.04∙10226.02∙1023=0.2 mol
m(H2O) = 0.2×18= 3.6 ग्राम
6.021022 कॉपर परमाणुओं वाले कॉपर सल्फेट के नमूने का द्रव्यमान निर्धारित करें।
उत्तर: 16
3.011022 हाइड्रोजन परमाणुओं वाले अमोनियम सल्फेट के नमूने के द्रव्यमान की गणना करें।
n(H) =NNA=3.0110226.02∙1023=0.05 mol
यौगिक में 8 ऑक्सीजन परमाणु हैं
n(NH4)2SO4 = 0.05 /8 = 0.00625 mol
m = 0.00625 ×132 g\mol = 0.825 g.
मैग्नीशियम हाइड्रोजन सल्फेट के नमूने का द्रव्यमान निर्धारित करें यदि यह ज्ञात हो कि इसमें 3.6121023 ऑक्सीजन परमाणु हैं।
n(O) =NNA = 3.612×10236.02×1023=0.6 मोल
n Mg(HSO4)2 = 0.6/8= 0.075 mol
मी = 0.075×218= 16.35 ग्राम
30.1 1022 सोडियम परमाणुओं और 6.021024 हाइड्रोजन परमाणुओं वाले पानी में सोडियम सल्फेट के घोल का द्रव्यमान निर्धारित करें।
n (Na) =NNA =30.1∙10226.02∙1023=0.5 mol
सूत्र में 2 सोडियम परमाणु हैं, इसलिए: n(Na2 SO4) = 0.5/2 = 0.25 mol
m पदार्थ (Na2SO4) = 0.25 × 142 g\mol = 35.5 g
n(H) =NNA= 6.02∙10246.02∙1023=10 mol
n(H2O) = 10/2=5 मोल
m(H2O) =5×18=90 ग्राम
m समाधान = m पदार्थ (Na2 SO4) + m (H2O) = 35.5 + 90 = 125.5 ग्राम।
12.04 1022 कार्बन परमाणुओं और 24.08 1022 ऑक्सीजन परमाणुओं वाले पानी में इथेनॉल C2H5OH के घोल का द्रव्यमान निर्धारित करें।
n (सी) =NNA= 12.04∙10226.02∙1023=0.2 मोल
n (C2H5OH) = 0.2/2 = 0.1 मोल
m(C2H5OH) = 0.1 ×46 = 4.6 ग्राम
n(O) =NNA =2.405∙10236.02∙1023=0.4 mol
n(H2O) =0.4/1=0.4 मोल
m(H2O) =0.4×18= 7.2 ग्राम
mसमाधान = m पदार्थ + m(H2O) = 4.6 + 7.2 = 11.8 ग्राम
एक सोडियम परमाणु के द्रव्यमान की गणना करें।
मा = एम (ना) / एनए = 23/ 6.021023 = 3.8210-23 ग्राम।
तीन कैल्शियम परमाणुओं का द्रव्यमान ज्ञात कीजिए।
मा=3 एम (सीए) / एनए = (3×40) / 6.021023 = 19.910-23 ग्राम
7 पानी के अणुओं के द्रव्यमान की गणना करें।
मा=7 एम (एच2ओ) / एनए = (7×18) / 6.021023 = 20.910-23 ग्राम
एक SO3 अणु का द्रव्यमान निर्धारित करें
मा= एम (एसओ3) / एनए = 80 /6.021023 = 13.3 10-23 ग्राम
सिलिकॉन (IV) ऑक्साइड की पाँच सूत्र इकाइयों के द्रव्यमान (g में) की गणना करें।
mfe=5×Mr×u=5×60×1.66∙10-27=4.98∙10-22 ग्राम।
द्रव्यमान की गणना करें:
सोडियम परमाणु (जी)
मा = एम (ना) / एनए = 23/ 6.021023 = 3.8210-23 ग्राम
ma=ArNa×u=23×1.6610-27 = 3.8210-23 ग्राम
सफेद फास्फोरस P4 के पांच अणु (किग्रा)
उत्तर: 1.02910-24 किग्रा
रम्बिक सल्फर S8 (g) के दस अणु
उत्तर: 4.2510-21 ग्राम
ओजोन O3 के तीन अणु (amu में)
ma=3×16×3×a.u.m=144a.u.m.
फुलरीन अणु C60 (मिलीग्राम)
मिमी = श्री(सी60)×यू = 1195.210-27 = 1.19510-24 किग्रा = 1.19510-21 ग्राम = 1.195 10-18 मिलीग्राम
कैफीन के तीन अणु С8Н10O2N4(किग्रा)
उत्तर: 9.6610-25 किग्रा
अमोनियम धनायन (जी)
ma=श्री(NH4+)×u = 18×1.6610-27 = 2.9910-23 ग्राम
आयनों SO42-(जी)
उत्तर: 1.5910-22 ग्राम।
हीमोग्लोबिन अणु С2954H4516N780O806S12Fe4 (मिलीग्राम)
उत्तर: 1.0710-16 मि.ग्रा
सोडियम क्लोराइड की सूत्र इकाई (जी)
पोटेशियम हाइड्रॉक्साइड की छह सूत्र इकाइयाँ (किग्रा)
बेरियम ऑक्साइड की तीन सूत्र इकाइयाँ (जी)
एक सल्फर अणु का द्रव्यमान आठ ऑक्सीजन परमाणुओं के द्रव्यमान के बराबर होता है। इसके अणु में कितने सल्फर परमाणु हैं?
maO=(8×16)×1.6610-27=2.12∙10-26 ग्राम
आइए हम अणु की संरचना की कल्पना Sx के रूप में करें
X = परमाणु के mm अणु = 2.12∙10-26Ar∙u = 2.12∙10-2632×1.66∙10-27 = 4 परमाणु
सुक्रोज अणु C12H22O11 का द्रव्यमान सफेद फास्फोरस P4 के अणु के द्रव्यमान से कितनी गुना अधिक है (उत्तर: 2.76 गुना)
मीथेन CH4 और ऑक्सीजन के नमूनों में अणुओं की संख्या समान होती है। ऑक्सीजन के द्रव्यमान और मीथेन के द्रव्यमान का अनुपात ज्ञात कीजिए (उत्तर: 2)
मैग्नीशियम के नमूने में हीरे के कार्बन परमाणुओं की संख्या तीन गुना है। मैग्नीशियम नमूने के द्रव्यमान और हीरे के नमूने के द्रव्यमान के अनुपात की गणना करें (उत्तर: 6)
द्वितीय. किसी पदार्थ की रासायनिक मात्रा की अवधारणा का उपयोग करके गणना।
रासायनिक मात्रा की गणना करें:
3.01 1024 H2 अणुओं वाले भाग में हाइड्रोजन
n (H2) =NNA=3.01∙10246.02∙1023=5 mol
5.6 dm3 के एक भाग में नाइट्रोजन (उत्तर: 0.25 mol)
14.2 ग्राम वजन वाले नमूने में सोडियम सल्फेट (उत्तर: 0.1 मोल)
किसी पदार्थ के अणु का द्रव्यमान 1.0610-22 ग्राम है, पदार्थ के दाढ़ द्रव्यमान की गणना करें।
M= ma×NA=1.06∙10-22×6.02∙1023=64 g\mol
पदार्थों के संकेतित भागों में अणुओं की संख्या निर्धारित करें:
3.25 मोल O2 (उत्तर: 1.961024)
11.5 मोल H2 (उत्तर: 6.921024)
40 मोल NH3(उत्तर: 2.411025)
0.0125 mol H2O (उत्तर: 7.521021)
पदार्थों के संकेतित भागों में रासायनिक मात्रा की गणना करें:
3.921023 O2 अणु (उत्तर: 0.651 mol)
14.7 1024 आर्गन परमाणु (उत्तर: 24.4 मोल)
2.451023 सूत्र इकाइयाँ Na3PO4 (उत्तर: 0.407 mol)
17.34 1024 H2SO4 अणु (उत्तर: 28.8 मोल)
पदार्थों के संकेतित भागों के लिए रासायनिक मात्रा की गणना करें:
5.6 dm3 हीलियम (उत्तर: 0.25 mol)
1.12 dm3SO2 (उत्तर: 0.05 mol)
5 m3 NH3 (उत्तर: 2.23102 mol)
300 सेमी3 एचसीएल (उत्तर: 1.3410-2 मोल)
पदार्थों के संकेतित भागों की मात्रा निर्धारित करें:
3.2 mol H2S (dm3) (उत्तर: 71.7 dm3)
0.05 मोल CH4 (सेमी3) (उत्तर: 1120 सेमी3)
300 mol O2 (m3) (उत्तर: 6.72 m3)
1.14 मोल आर्गन (dm3) (उत्तर: 25.5 dm3)
1.12 1023 अणुओं वाले नाइट्रोजन के एक हिस्से की मात्रा (dm3) की गणना करें।
n(H2) =NNA= 1.12∙10236.02∙1023=0.18 mol
वी (एच2) = 0.18×22.4 = 4 डीएम3
ऑक्सीजन के 2 किलो हिस्से की मात्रा की गणना करें (उत्तर: 1400 dm3)
3.45 dm3 आयतन वाले अमोनिया के एक हिस्से में अणुओं की संख्या की गणना करें (उत्तर: 9.271022)
अमोनिया के उस हिस्से के द्रव्यमान की गणना करें जिसमें 5.43 · 1024 अणु हैं। (उत्तर: 153 ग्राम)।
यादगार होने के अलावा, .com डोमेन अद्वितीय हैं: यह अपनी तरह का एकमात्र .com नाम है। अन्य एक्सटेंशन आमतौर पर केवल अपने .com समकक्षों पर ट्रैफ़िक लाते हैं। प्रीमियम .com डोमेन मूल्यांकन के बारे में अधिक जानने के लिए, नीचे दिया गया वीडियो देखें:
अपनी वेब साइट को टर्बोचार्ज करें। कैसे जानने के लिए हमारा वीडियो देखें।
अपनी वेब उपस्थिति में सुधार करें
एक बेहतरीन डोमेन नाम के साथ ऑनलाइन ध्यान आकर्षित करें
वेब पर पंजीकृत सभी डोमेन में से 73% .com हैं। कारण सरल है: .com वह जगह है जहां अधिकांश वेब ट्रैफ़िक होता है। एक प्रीमियम .com का मालिक होने से आपको बेहतर एसईओ, नाम पहचान और अपनी साइट को अधिकार की भावना प्रदान करने सहित कई लाभ मिलते हैं।
यहाँ अन्य लोग क्या कह रहे हैं
2005 से, हमने हजारों लोगों को सही डोमेन नाम पाने में मदद की है
- रयान से फोन पर बात की और उसने मेरे सभी सवालों में मेरी मदद की! बेहतरीन ग्राहक सेवा और आसानी से उपलब्ध। यह प्रक्रिया आसान और अपेक्षाकृत त्वरित थी, केवल तीन कार्यदिवसों में पूरी हो गई। यह उन लोगों के लिए अत्यधिक अनुशंसित है जो bigdomains.com से एक डोमेन खरीदने पर विचार कर रहे हैं। एक तृतीय-पक्ष शामिल होता है जिसे namebright.com कहा जाता है, लेकिन कोई अतिरिक्त शुल्क नहीं है और वे सर्वर से डोमेन के हस्तांतरण की सुविधा प्रदान करते हैं। प्रोत्साहित करना - सैमी लैम, 10/14/2019
- सच कहूं तो HugeDomains.com से डोमेन खरीदने से पहले, मैं बहुत डरा हुआ था क्योंकि मैंने कुछ वेबसाइट पर कुछ नकारात्मक समीक्षा पढ़ी थी.. लेकिन एक मौका लेने का फैसला किया। खरीद के बाद मुझे आश्चर्य हुआ, यह अविश्वसनीय था कि मेरी डोमेन नाम खरीद सफल रही और सबसे अच्छी बात यह थी कि मैंने इसे अन्य रजिस्ट्रार के साथ स्थानांतरित कर दिया और फिर से आश्चर्यचकित रह गया क्योंकि मेरा डोमेन नाम 30 मिनट के भीतर स्थानांतरित हो गया.. खरीद से हस्तांतरण तक कुल समय कम था 2 घंटे.... HugeDomain.com और NameBright.com को बहुत-बहुत धन्यवाद -संदीप राजपूत, 10/14/2019
- तेज़ और सुचारू सौदा और स्थानांतरण। इसकी अनुशंसा कर सकते हैं! - टॉम, 12/10/2019
- अधिक