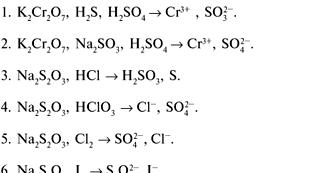Քիմիայի ներկայացում. Կարբոքսիլաթթուներ - ներկայացում. «Կարբոքսիլաթթուներ» թեմայով շնորհանդես Մոնոբազային կարբոքսիլաթթուներ ներկայացում
1. Պարզի՛ր կարբոքսիլաթթուների ֆունկցիոնալ խումբը և ընդհանուր բանաձևը:
2. Ձևակերպիր սահմանում.
3. Ուսումնասիրել կարբոքսիլաթթուների դասակարգումը.
4. Վարպետ նոմենկլատուրային հմտություններ:
5. Հաշվի առեք ֆիզիկական և Քիմիական հատկություններամենակարևոր կարբոքսիլաթթուները.
6. Պարզի՛ր որոշ կարբոքսիլաթթուների կիրառման ոլորտները:
Ներբեռնել:
Նախադիտում:
Ներկայացման նախադիտումներից օգտվելու համար ստեղծեք Google հաշիվ և մուտք գործեք այն՝ https://accounts.google.com
Սլայդի ենթագրեր.
Առաջադրանքներ 1. Պարզե՛ք կարբոքսիլաթթուների ֆունկցիոնալ խումբը և ընդհանուր բանաձևը: 2. Ձևակերպիր սահմանում. 3. Ուսումնասիրել կարբոքսիլաթթուների դասակարգումը. 4. Վարպետ նոմենկլատուրային հմտություններ: 5. Դիտարկենք ամենակարևոր կարբոքսիլաթթուների ֆիզիկական և քիմիական հատկությունները: 6. Պարզի՛ր որոշ կարբոքսիլաթթուների կիրառման ոլորտները:
Բոլոր կարբոքսիլաթթուներն ունեն ֆունկցիոնալ խումբ՝ C OH O Կարբոնիլ խումբ Հիդրօքսիլ խումբ Կարբոքսիլ խումբ Ընդհանուր բանաձև R C OH O C n H 2n +1 C Կամ հագեցված միհիմն թթուների համար O OH. Ի՞նչ են կոչվում կարբոքսիլաթթուները: Կարբոքսիլաթթուները օրգանական միացություններ են, որոնց մոլեկուլները պարունակում են կարբոքսիլ խումբ՝ COOH, կապված ածխաջրածնային ռադիկալի հետ։ ? Ինչպե՞ս են կարբոքսիլաթթուները գենետիկորեն կապված ալդեհիդների նախկինում ուսումնասիրված դասի հետ: R C O H + [O] R C O OH [O]= KM nO 4, K 2 Cr 2 O 7+ H 2 SO 4 կոնց.
Կարբոքսիլային թթուների դասակարգումը Կախված կարբոքսիլային խմբերի քանակից Միահիմն Երկհիմնական (քացախային) (օքսալային) CH 3 C C - CO OH Բազմհիմնային (կիտրոնային) O OH O HO N 2 C - C O OH HC - C O OH H 2 C - C O OH. Կախված ռադիկալի բնույթից Հագեցած (պրոպիոնիկ) O CH 3- CH 2- C OH Չհագեցած (ակրիլ) O CH 2 =CH-C OH Արոմատիկ (բենզոիկ) CO OH C ատոմների պարունակության հիման վրա՝ C 1 -C. 9 - ավելի ցածր, 10-ով կամ ավելի - ավելի բարձր
Դասակարգել առաջարկվող թթուները 1) C H 3 - CH 2 - CH 2 - CH 2 - COOH 2) HOOC - CH 2 - CH 2 - COOH 3) COOH 4) CH 3 - (C H 2) 7 - CH = CH - ( CH 2) 7 - COOH 5) HOOC - CH 2 - CH - CH 2 - COOH COOH CH 3 1. Միահիմք, սահմանափակող, ստորին 2. Երկհիմնական, սահմանափակող, ստորին 3. Միահիմք, սահմանափակող, ստորին 4. Միահիմք, չհագեցած, ամենաբարձր 5. .Պոլիբազային, վերջնական, ամենացածր
ԱԾԽԱԹԹՈՒՆԵՐԻ ԱՆՎԱՆԱԿԱՆՈՒԹՅՈՒՆ ԱԼԿԱՆ + ՕՀ + ՕՀԻԹԹՈՒ ՄԵԹԱՆ ՕՀԻԹԹՈՒ (ՖՈՄԻԹԹՈՒ)
CH3 – COOH 1 2 ԷԹԱՆԱԿԱՆ ԹԹՈՒ (քացախաթթու) CH3 – CH2 – CH2 - COOH 1 2 3 4 ԲՈՒՏԱՆԱԿԱՆ ԹԹՈՒ (ԲՈՒՏՐԻԱԹԹՈՒ)
CH3 – CH2 – CH2 – CH2 – COOH ՊԵՆՏԱՆԹԹՈՒ (ՎԱԼԵՐԻԱՆ ԹԹՈՒ) 1 2 3 4 5 HOOC – COOH ԷԹԱՆԱԿԱՆ ԹԹՈՒ (ՕՔՍԱԼԻԹԹՈՒ) 1 2
Կարբոքսիլաթթուների հոմոլոգ շարք Քիմիական բանաձևԹթվի սիստեմատիկ անվանումը Թթվային տրիվիալ անվանումը Թթվային մնացորդի անվանումը HCOO N ձևաֆորմատ CH3COO N քացախային ացետատ CH3CH2COO N պրոպիոնային պրոպիոն CH3CH2CH2COO N բուտիրատ՝ CH3CH2CH2CH2COO N Վալերիկ վալերին՝ CH4-CO3 (Capron CH2-COCH) (CH2)8 – COO N կապրիկ կապրիկ CH3-(CH2)14 – COO N պալմիտիկ պալմիտատ CH3-(CH2)16- COO N ստեարային ստեարատ Մեթան Էթան Պրոպան Բութան Պենտան Հեքսան Դեկան Հեքսադեկան օկտադեկան
Կարբոքսիլաթթուների անվանման ալգորիթմ՝ 1. Մենք գտնում ենք ածխածնի ատոմների հիմնական շղթան և համարակալում այն՝ սկսած կարբոքսիլային խմբից։ 2. Նշում ենք փոխարինողների դիրքը և նրանց անվանում(ներ)ը: 3. Արմատից հետո, շղթայում նշելով ածխածնի ատոմների թիվը, գալիս է «-ic» թթու վերջածանցը։ 4. Եթե կան մի քանի կարբոքսիլ խմբեր, ապա «- ova»-ից առաջ մի թիվ է դրվում (-di, - երեք...) Օրինակ՝ 3-մեթիլբութան + -ova = 3-մեթիլբուտանաթթու.
ՏՎԵ՛Ք ՆՅՈՒԹԵՐԻ ԱՆՎԱՆՈՒՄԸ ԸՍՏ ՄԻՋԱԶԳԱՅԻՆ ԱՆՎԱՆԱԿԱՆՈՒԹՅԱՆ (2 – ՄԵԹԻԼՊՐՈՊԱՆԹԹՈՒ) CH3 – CH – COOH 2. CH3 – CH2 – CH – CH – COOH 3. CH3 – CH = CH – CH – COOH 4. – CH – COOH (2, 3 – ԴԻՄԵԹԻԼ ՊԵՏԱՆԱԿԱՆ ԹԹՈՒ) (2 – ՄԵԹԻԼ ՊԵՏԱՆԱԿԱՆ ԹԹՈՒ) (2 – ԷԹԻԼԲՈՒՏԱՆԹԹՈՒ) CH3 CH3 CH3 CH3 C 2 H 5
: 1 . Ընտրեք բառի արմատը, որի հիման վրա գրեք ածխածնի կմախքը կազմի մեջ, որը ներառում է կարբոքսիլ խումբ: 2. Ածխածնի ատոմները համարակալում ենք՝ սկսած կարբոքսիլային խմբից։ 3. Փոխարինիչներ նշում ենք ըստ համարակալման։ 4. Անհրաժեշտ է ավելացնել բացակայող ջրածնի ատոմները (ածխածինը քառավալենտ է): 5. Ստուգեք, արդյոք բանաձեւը ճիշտ է գրված: 2-մեթիլ բութանաթթու. Օրինակ՝ կարբոքսիլաթթուների բանաձևերը գրելու ալգորիթմ
ՖԻԶԻԿԱԿԱՆ ՀԱՏԿՈՒԹՅՈՒՆՆԵՐ C 1 – C 3 Հեղուկներ բնորոշ սուր հոտով, շատ լուծվող ջրում C 4 – C 9 Մածուցիկ յուղոտ հեղուկներ՝ տհաճ հոտով, վատ լուծվող ջրում C 10 և ավելի Անհոտ պինդ նյութեր, ջրի մեջ չլուծվող
Ֆիզիկական վիճակ Հեղուկ Գույն անգույն թափանցիկ հեղուկ Հոտ կծու քացախային Լուծելիությունը ջրում լավ է Եռման կետ 118 º C Հալման կետ 17 º C Քացախաթթվի ֆիզիկական հատկություններ.
Ստորին կարբոքսիլաթթուները հեղուկներ են. ավելի բարձր - պինդ նյութեր, որքան մեծ է թթվի հարաբերական մոլեկուլային քաշը, այնքան քիչ է նրա հոտը: Աճող հարաբերականով մոլեկուլային քաշըթթվային լուծելիությունը նվազում է Կախվածությունը ֆիզիկական հատկություններԿարբոքսիլային թթուներ մոլեկուլի կառուցվածքից. Ալդեհիդների հոմոլոգ շարքը սկսվում է երկու գազային նյութերից (սենյակային ջերմաստիճանում), և կարբոքսիլաթթուների մեջ գազեր չկան։ Սա ինչի՞ հետ է կապված։
Կարբոքսիլաթթուների քիմիական հատկությունները I. Տարածված է անօրգանական թթուների հետ Լուծվող կարբոքսիլաթթուները տարանջատվում են ջրային լուծույթներում. CH 3 – COOH CH 3 – COO + H + Արդյո՞ք միջինը թթվային է: Ինչպե՞ս կփոխվի ցուցիչների գույնը թթվային միջավայր? Լակմուս (մանուշակ) - դառնում է կարմիր Մեթիլ նարնջագույն - դառնում է վարդագույն Ֆենոֆթալեին - չի փոխում գույնը 2. Մետաղների հետ փոխազդեցությունը էլեկտրաքիմիական լարման շարքում մինչև ջրածինը. 2CH 3 - COOH + M գ Քացախաթթու (CH 3 -COO) 2 Մգ Մագնեզիումի ացետատ + H 2 2CH 3 - COOH + Zn Քացախաթթու (CH 3 –COO) 2 Zn Ցինկի ացետատ + H 2 Երբ մետաղը փոխազդում է կարբոքսիլաթթվի լուծույթի հետ, առաջանում են ջրածին և աղ.
3. Փոխազդեցություն հիմնական օքսիդների հետ՝ 2 CH 3 – COOH + C u O Քացախաթթու t (CH 3 – COO) 2 C u Պղնձի ացետատ + H 2 O 4. Փոխազդեցություն մետաղների հիդրօքսիդների հետ (չեզոքացման ռեակցիա) CH 3 – COOH + HO. – Na Քացախաթթու CH 3 COO Na Նատրիումի ացետատ + H 2 O 5. Փոխազդեցություն ավելի թույլ և ցնդող թթուների աղերի հետ (օրինակ՝ ածխածնի, սիլիցիումի, ջրածնի սուլֆիդ, ստեարիկ, պալմիտիկ...) 2CH 3 – COOH Քացախաթթու + Na 2 CO 3 նատրիումի կարբոնատ 2CH 3 COO Na Նատրիումի ացետատ + H 2 CO 3 CO 2 H 2 O 2 CH3 – COOH + Cu(OH) 2 Քացախաթթու (CH3COO) 2 Cu Պղնձի ացետատ + H2O
Մրջնաթթվի «Արծաթի հայելի» ռեակցիայի առանձնահատկությունները H-CO OH + Ag 2 O t 2Ag + H 2 CO 3 CO 2 H 2 O Մրջնաթթու Արծաթի օքսիդ արծաթ
Բնության մեջ հայտնվելը և կարբոքսիլաթթուների օգտագործումը Մաթանաթթու (Մեթանաթթու) - Քիմիական բանաձև CH2O2 կամ HCOOH: - Մրջնաթթուն հայտնաբերվել է կարմիր մրջյունների թթվային սեկրեցներում 1670 թվականին անգլիացի բնագետ Ջոն Ռեյի կողմից։ Մրջնաթթուն առկա է նաև եղինջի լավագույն մազերի, մեղվի թույնի, սոճու ասեղների մեջ և այլն: մեծ քանակությամբհայտնաբերվել է տարբեր մրգերում, հյուսվածքներում, օրգաններում, կենդանիների և մարդու սեկրեցներում:
Հարց. Ինչո՞ւ չես կարող մրջյունի կծածի կամ եղինջի խայթոցի հատվածը ջրով թրջել: Սա միայն հանգեցնում է ցավի ավելացման: Ինչու՞ է ցավը թուլանում, եթե վիրավոր տարածքը թրջվում է ամոնիակով: Էլ ի՞նչ կարելի է օգտագործել այս դեպքում: Երբ մածուցիկ թթուն լուծվում է ջրի մեջ, տեղի է ունենում գործընթաց էլեկտրոլիտիկ դիսոցացիա HCOOH HCOO + H Արդյունքում շրջակա միջավայրի թթվայնությունը մեծանում է, իսկ մաշկի կոռոզիայի պրոցեսն ուժեղանում է։ Որպեսզի ցավը թուլանա, պետք է չեզոքացնել թթուն, ինչի համար պետք է օգտագործել ալկալային ռեակցիա ունեցող լուծույթներ, օրինակ՝ ամոնիակի լուծույթ։ HCOOH + N H4OH HCOO NH4 + H2O կամ HCOOH + NaHCO3 HCOO Na + CO2 + H2O
Քացախաթթու (էթանաթթու) Սա մարդու կողմից ստացված և օգտագործված առաջին թթունն է: «Ծնվել է» ավելի քան 4 հազար տարի առաջ Հին Եգիպտոս. 17-18-րդ դարերի վերջին Ռուսաստանում այն կոչվում էր «թթու խոնավություն»: Առաջին անգամ այն ստացանք գինու թթվացման ժամանակ։ Լատինական անվանումը Acetum acidum է, այստեղից էլ առաջացել է աղերի անվանումը՝ ացետատներ։ Սառցադաշտային քացախաթթուն 16.8 º C-ից ցածր ջերմաստիճանում կարծրանում է և դառնում սառույցի նման. Քացախային էություն - 70% թթվային լուծույթ: - Սեղանի քացախ - 6% կամ 9% թթվային լուծույթ: Քացախաթթու - հայտնաբերված է կենդանիների սեկրեցներում (մեզ, լեղ, կղանք), բույսերում (մասնավորապես, կանաչ տերևներում), թթու կաթում և պանիրում; - առաջացել է գինու և գարեջրի խմորման, փտելու, թթվելու, շատերի օքսիդացման ժամանակ. օրգանական նյութեր;
Քացախաթթվի կիրառությունները - Քացախաթթվի ջրային լուծույթները լայնորեն օգտագործվում են սննդի արդյունաբերության մեջ ( սննդային հավելում E-260) և կենցաղային խոհարարություն, ինչպես նաև պահածոյացում. դեղերի արտադրության մեջ, օրինակ՝ ասպիրին; արհեստական մանրաթելեր, օրինակ, մետաքսի ացետատ; ինդիգո ներկեր, ոչ դյուրավառ թաղանթ, օրգանական ապակի; լաքի լուծիչներ; բույսերի պաշտպանության քիմիական միջոցներ, բույսերի աճի խթանիչներ; Նատրիումի ացետատ CH3COO N a-ն օգտագործվում է որպես փոխներարկման համար նախատեսված արյան կոնսերվանտ; Կալիումի ացետատ CH3COOK – որպես միզամուղ; Կապարի ացետատ (CH3COO) 2 Pb - մեզի մեջ շաքարի որոշման համար; Երկաթի (III) (CH3COO)3Fe, ալյումինի (CH3COO) 3Al-ի և քրոմի (III) (CH3COO) 3Cr-ի ացետատներն օգտագործվում են տեքստիլ արդյունաբերության մեջ մաշկային ներկման համար. Պղնձի (II) ացետատ (CH3COO) 2 C u-ն բույսերի վնասատուների դեմ պայքարի պատրաստուկի մի մասն է, այսպես կոչված, փարիզյան կանաչ;
Քացախաթթվի օգտագործումը Սպիրտային քացախի օգտագործումը կոսմետոլոգիայում հայտնի է։ Մասնավորապես՝ մազերին փափկություն և փայլ հաղորդելու համար պերմի և մշտական ներկումից հետո։ Դրա համար խորհուրդ է տրվում մազերը ողողել տաք ջրով` ալկոհոլային քացախի ավելացումով (3-4 ճաշի գդալ քացախ 1 լիտր ջրի դիմաց): Ժողովրդական բժշկության մեջ քացախն օգտագործվում է որպես ջերմության ոչ սպեցիֆիկ միջոց։ գլխացավերի դեպքում՝ օգտագործելով լոսյոններ. միջատների խայթոցների համար, օգտագործելով կոմպրեսներ: անփոխարինելի է օծանելիքի արտադրության մեջ Գիտեի՞ք, որ - Եթե ժանգոտ ընկույզը պետք է պտտել, խորհուրդ է տրվում երեկոյան վրան քացախաթթվով թաթախված լաթ դնել: Առավոտյան շատ ավելի հեշտ կլինի այս ընկույզը հանելը: - Օրվա ընթացքում օրգանիզմում 400 գ քացախաթթու է գոյանում: Սա բավական կլիներ 8 լիտր սովորական քացախ պատրաստելու համար
Բոլոր թթուներից Դա, իհարկե, պրիմա է: Ներկայացրե՛ք ամենուր՝ և՛ տեսանելի, և՛ անտեսանելի: Այն առկա է կենդանիների և բույսերի մեջ, տեխնոլոգիան և բժշկությունը հավերժ նրա հետ են: Նրա սերունդները ացետատներ են՝ շատ անհրաժեշտ «տղերք»: Հայտնի ասպիրինը, ինչպես լավ ջենթլմենը, նվազեցնում է հիվանդի ջերմությունը և վերականգնում առողջությունը։ Սա պղնձի ացետատ է: Նա բույսերի ընկերն ու եղբայրն է, Սպանում է նրանց թշնամիներին: Թթուն դեռևս որոշակի կիրառություն ունի. այն մեզ հագցնում է ացետատ մետաքս: Իսկ ով սիրում է պելմենի, քացախը վաղուց գիտի։ Կա նաև կինոյի հարցը. Դե, բոլորը պետք է իմանան, որ առանց ացետատ ֆիլմի մենք չենք կարող կինո տեսնել։ Իհարկե, կան այլ կիրառումներ. Եվ դուք գիտեք նրանց առանց կասկածի: Բայց հիմնականը, որ ասվում է, ընկերներ, այն է, որ «արդյունաբերության հացը» քացախաթթու է։ CH 3 COOH CH3COOH Պղնձի ացետատի ջրային լուծույթ
Կիտրոնաթթու COOH HOOC – CH 2 – C – CH 2 – COOH OH Օքսալաթթու HOOC –– COOH Մրջնաթթու H –– COOH Ացետիլսալիցիլաթթու COOH OCOCH 3 Թարթաթթու HOOC – CH - CH –– COOH OH OH Կաթնաթթու CH 3 - CH –– COOH OH խնձորաթթու HOOC – CH - CH 2 –– COOH OH սուկինաթթու HOOC – CH 2 - CH 2 –– COOH բենզոյաթթու COOH ասկորբինաթթու HO OH H =O HOH 2 C-NONS O Քացախաթթու H 3 C – – COOH կարբոքսիլաթթուներ՝ ըստ թթվայնության բարձրացման
Եզրակացություններ 1. Կարբոքսիլաթթուները օրգանական միացություններ են, որոնց մոլեկուլները պարունակում են կարբոքսիլ խումբ՝ COOH՝ կապված ածխաջրածնային ռադիկալի հետ։ 2. Կարբոքսիլային թթուները դասակարգվում են. ըստ հիմնականության (միա-, երկ- և բազմաբազային) ըստ ածխաջրածնային ռադիկալի (հագեցած, չհագեցած և արոմատիկ) ըստ C ատոմների պարունակության (ցածր և բարձր): 3. Կարբոքսիլաթթվի անվանումը բաղկացած է. ալկանի + օվալաթթու անվանումը. 4. Կարբոքսիլաթթվի մոլեկուլային զանգվածի մեծացման հետ թթվի լուծելիությունն ու ուժը նվազում են։ 5. Ինչպես անօրգանական թթուները, լուծվող կարբոքսիլաթթուները տարանջատվում են ջրային լուծույթում՝ առաջացնելով ջրածնի իոններ և փոխելով ցուցիչի գույնը։ Փոխազդում են մետաղների (մինչև H), հիմնային և ամֆոտերային օքսիդների և հիդրօքսիդների և ավելի թույլ թթուների աղերի հետ՝ առաջացնելով աղեր։ 6 Լայնորեն տարածված են բնության մեջ և ունեն մեծ գործնական նշանակություն մարդկանց համար։
Տնային առաջադրանք § 14, վարժություն թիվ 6 վարժություն թիվ 9 Կլեոպատրա թագուհին պալատական բժշկի խորհրդով ոսկերիչներին հայտնի ամենամեծ մարգարիտը լուծեց քացախի մեջ, իսկ հետո ստացված լուծույթը որոշ ժամանակ վերցրեց։ Ի՞նչ արձագանք տվեց Կլեոպատրան: Ի՞նչ կապ էր նա վերցնում: 3. Պատրաստեք զեկույց ավելի բարձր կարբոքսիլաթթուների մասին
Շնորհակալություն ուշադրության համար
Կարբոքսիլաթթուներ
Սլայդներ՝ 41 Բառեր՝ 1295 Հնչյուններ՝ 24 Էֆեկտներ՝ 62Կարբոքսիլաթթուներ. Բոլոր կարբոքսիլաթթուները ունեն ֆունկցիոնալ խումբ: Ի՞նչ են կոչվում կարբոքսիլաթթուները: Ինքնակառավարման առաջադրանք. Կարբոքսիլաթթուների անվանացանկը. Բնության մեջ կարբոքսիլաթթուներ. Կարբոքսիլաթթուների ընդհանուր բանաձևը. Կարբոքսիլ խմբի կառուցվածքը. Կարբոքսիլաթթուների ֆիզիկական հատկությունները. Հագեցած կարբոքսիլաթթուների ֆիզիկական հատկությունները. Կարբոքսիլաթթուների քիմիական հատկությունները. Ռեակցիան հալոգենների հետ. Կարբոքսիլաթթուների պատրաստում. Կարբոքսիլաթթվի մոլեկուլները ձևավորում են դիմերներ։ Կրկնել կարբոքսիլաթթուների որոշումը: Անվանակարգ եթերներ. Էսթերները բնության մեջ. Պղնձի ացետատ. - Թթուներ 1.ppt
Կարբոքսիլաթթուների փոխազդեցությունը
Սլայդներ՝ 14 Բառեր՝ 359 Հնչյուններ՝ 0 Էֆեկտներ՝ 0Կարբոքսիլաթթուներ. Հագեցած միահիմն կարբոքսիլաթթուների բաղադրությունը համապատասխանում է O R – C OH ընդհանուր բանաձևին: Դասակարգում. Թթուների օրինակներ. Իզոմերիզմ. Կառուցվածք. Ֆիզիկական և քիմիական հատկություններ. Ստորին կարբոքսիլաթթուները սուր հոտով հեղուկներ են, որոնք շատ լուծելի են ջրում: CH3COOH + SOCl2 CH3COCl + HCl + SO2: Ստանալու մեթոդները. 4. Եթերների հիդրոլիզ. 5. Թթվային անհիդրիդների հիդրոլիզ. Պատրաստման հատուկ մեթոդներ. Առանձին թթուների համար կան պատրաստման հատուկ մեթոդներ՝ կարբոքսիլաթթուների օգտագործումը։ Սոսինձ. Թունաքիմիկատներ. Կոնսերվանտ, համեմունք: Օծանելիք, կոսմետիկա. - Carboxylic acids.ppt
Կարբոքսիլաթթուների հատկությունները
Սլայդներ՝ 21 Բառեր՝ 424 Հնչյուններ՝ 0 Էֆեկտներ՝ 96Կարբոքսիլաթթուներ. Օրգանական քիմիա 11-րդ դասարան. -COOH կարբոքսիլ խումբ: Մեթանադիոաթթու (դիկարբոքսիլաթթու): 2-հիդրօքսիպրոպանետրիկ թթու (2-հիդրօքսի-1,2,3-պրոպանետրիկարբոքսիլաթթու): Ֆիզիկական հատկություններ. Մոլեկուլի բևեռացում. Ջրածնային կապերի առաջացման հնարավորությունը. Բարձր եռման կետեր. Քացախաթթվի դիմեր: Լուծելիություն ջրի մեջ. Կարբոքսիլ խմբի կառուցվածքը. Ռադիկալներ. Նուկլեոֆիլներ. Էլեկտրոֆիլներ. Քիմիական հատկություններ. Նրանք ցույց են տալիս թթուների ընդհանուր հատկությունները: Կարբոքսիլաթթու. Մագնեզիումի կարբոքսիլատ. Էթանաթթու. Մագնեզիումի էթանատ. Կալցիումի էթատ. Նատրիումի մեթան. - Կարբոքսիլաթթուներ 1.ppt
Բնության մեջ կարբոքսիլաթթուներ
Սլայդներ՝ 20 բառ՝ 379 հնչյուններ՝ 0 էֆեկտներ՝ 0Կարբոքսիլաթթուներ. Որոշ սովորական թթուների բանաձևեր և անվանումներ. Թթվային մնացորդների բանաձևեր և անվանումներ. Ստորին կարբոքսիլաթթուներ: - անգույն հեղուկներ՝ սուր հոտով: Քանի որ մոլային զանգվածը մեծանում է, եռման կետը մեծանում է: ...Կարբոքսիլաթթուները բնության մեջ՝ C2H5COOH – ծառի խեժ. C3H7COOH – կարագ։ C4H9COOH – վալերիան խոտի արմատներ: C6H5COOH – մեխակի յուղ: Ամենապարզ կարբոքսիլաթթուները. Նկատի ունեցեք, որ... թթուն HCOOH մտնում է «արծաթե հայելու» ռեակցիայի մեջ, ինչպես ալդեհիդները: Եվ քայքայվում է ջրահեռացնող նյութերի ազդեցության տակ. Ստանալով կարբոքսիլաթթուներ: - Կարբոքսիլաթթուներ 2.ppt
Կարբոքսիլաթթու
Սլայդներ՝ 9 բառ՝ 193 հնչյուններ՝ 0 էֆեկտներ՝ 0Ներկայացում. Կարբոքսիլաթթուներ. Դասի նպատակը. Դիտարկենք միջազգային և չնչին նոմենկլատուրաների հիմունքները, կարբոքսիլաթթուների օգտագործումը: Վերլուծել կարբոքսիլային խմբի կառուցվածքը և գուշակել կարբոքսիլաթթուների քիմիական վարքը: Կարբոքսիլաթթուների դասակարգում. Ըստ կարբոքսիլ խմբերի քանակի. Անսահմանափակ: Անուշաբույր. Մոնոբազային. Դիբազային. Պոլիբազային. Սահման. Ըստ ածխաջրածնային ռադիկալի տեսակի. Սահմանափակող շարքի միահիմն թթուների ընդհանուր բանաձևը. CnH2n+1COOH որտեղ n-ը կարող է լինել զրո: Ամենապարզ կարբոքսիլաթթուները. Որոշ կարբոքսիլաթթուների բանաձևեր և անվանումներ. - Կարբոքսիլաթթուներ 3.ppt
Կարբոնաթթուներ
Սլայդներ՝ 14 բառ՝ 889 հնչյուններ՝ 0 էֆեկտներ՝ 0Կարբոքսիլաթթուներ. Կառուցվածք. Մոլեկուլում մեկ կարբոքսիլ խումբ պարունակող օրգանական թթուները միահիմն են։ Երկու կարբոքսիլ խմբեր պարունակող կարբոքսիլաթթուները կոչվում են երկհիմնական։ Օքսալաթթու. Հագեցած (կամ հագեցած) կարբոքսիլաթթուները ածխաջրածնային ռադիկալում α-պարտատոմսեր չեն պարունակում։ Օրինակ՝ բենզոյական թթու՝ անվանակարգ և իզոմերիզմ։ Ածխածնի ատոմների համարակալումը սկսվում է կարբոքսիլ խմբից։ Մեթան (մորթաթթու): Էթանդիոնիկ (օքսալաթթու): Հագեցած միահիմն կարբոքսիլաթթուների ֆիզիկական հատկությունները. Քիմիական հատկություններ. - Կարբոքսիլաթթուներ 4.ppt
Չհագեցած կարբոքսիլաթթուներ
Սլայդներ՝ 11 բառ՝ 305 հնչյուններ՝ 0 էֆեկտներ՝ 37Չհագեցած կարբոքսիլաթթուներ. Ֆիզիկական հատկություններ. Իզոմերիզմ. Ստանալու մեթոդները. Քիմիական հատկություններ. Կենսաբանական կառուցվածքը. Դիմում. Ակրիլաթթու. Մետակրիլաթթու. CH2=CH-coon. CH2=c-coon. CH3. Օլեինաթթու. CH3 – (CH2)7-CH=CH-(CH2)7 -կոն. Լինոլեինաթթու. CH3-(CH2)4-CH=CH-CH2-CH=CH-(CH2)7-coon. Լինոլենիկ թթու. CH3-SN2-CH=CH-CH2-CH=CH-CH2-CH=CH-(CH2)7-coon. Չհագեցած կարբոքսիլաթթուների իզոմերիզմ. Ածխածնային շղթա. Կրկնակի պարտատոմսերի դիրքեր. Երկրաչափական (cis-trans isomerism). Օլեինաթթվի երկրաչափական իզոմերներ. Ազոտի օքսիդներ. Էլայդիկ թթու. - Կարբոքսիլաթթուներ 5.ppt
Քացախային և ստեարաթթուներ
Սլայդներ՝ 14 Բառեր՝ 236 Հնչյուններ՝ 0 Էֆեկտներ՝ 0Դասարան 9 Դաս 6. Կարբոքսիլաթթուներ. Դասի պլան. Կարբոքսիլաթթուների հայեցակարգը. Քացախաթթու. Ստեարաթթու. Հարցեր և վարժություններ. 1. Կարբոքսիլաթթուների հասկացությունը. Կարբոքսիլ խմբի կառուցվածքային բանաձևն է՝ O C O H. -Coon. Կարբոքսիլաթթու. Կարբոքսիլատ անիոն. Կարբոքսիլաթթուների շարքում կան տոննա հայտնի «անձեր»: Թթուներում կան կարբոքսիլային խմբեր, բայց այստեղ բոլոր թթուները ուժեղ չեն։ 2. Քացախաթթու. Քացախաթթուն CH3COOH-ը օրգանական թթուներից ամենահինն է: Մաքուր քացախաթթուն գունավոր հեղուկ է, սուր հոտով: Քացախաթթուն մեծ քանակությամբ օգտագործվում է քիմիական արդյունաբերության մեջ։ - Կարբոքսիլաթթուներ 6.ppt
Կարբոքսիլաթթուների քիմիա
Սլայդներ՝ 14 Բառեր՝ 341 Հնչյուններ՝ 0 Էֆեկտներ՝ 0Կարբոքսիլաթթուներ. Դասախոսություն. 1. Թթուների որոշում. 2. Հոմոլոգ շարք. Ամենապարզ ներկայացուցիչները հագեցած մոնոբազային կարբոքսիլաթթուներ են: Կարբոնիլ և հիդրօքսիլ խմբեր, որոնք կազմում են մեկ ֆունկցիոնալ կարբոքսիլ խումբ։ Կարբոքսիլաթթուների հատկությունները կախված են առկայությունից: Փոխարինումը տեղի է ունենում ածխածնի 2-րդ ատոմում և տեղի է ունենում կատալիզատորի վրա: Այս ռեակցիան միջանկյալ է ամինաթթուների արտադրության համար: Թթուների կարբոքսիլային խումբ. Ալդեհիդային խումբ. Օլեինաթթու. 9,10 - դիբրոմոստեարաթթու: Օլեինաթթուն պատկանում է ավելի բարձր չհագեցած կարբոքսիլաթթուներին: - Carboxylic acids chemistry.ppt
Կարբոքսիլաթթուների դասեր
Սլայդներ՝ 33 Բառեր՝ 809 Հնչյուններ՝ 0 Էֆեկտներ՝ 13Թթվածին պարունակող օրգանական միացություններ. Կարբոքսիլաթթուներ. Կարբոքսիլաթթուների պատրաստում. Ընդհանուր բանաձև. Սահմանում. Կարբոքսիլաթթուների դասակարգում. Կարբոքսիլաթթուների դասակարգումն ըստ ածխաջրածնային ռադիկալի բնույթի. Կարբոքսիլաթթուների դասակարգումն ըստ ֆունկցիոնալ խմբերի. Մոնոբազային կարբոքսիլաթթուների ներկայացուցիչներ. Թթուների հոմոլոգ շարք: Կարբոքսիլաթթուների անվանացանկը. Կարբոքսիլաթթուների իզոմերիզմ. Կարբոքսիլաթթուների ֆիզիկական հատկությունները. Կարբոքսիլաթթուների կիրառում. Արտադրություն օրգանական միացություններ. Մեթիլբուտանաթթու. Ֆունկցիոնալ խումբ. - Կարբոքսիլաթթուների դասեր.ppt
Կարբոքսիլաթթուների օրինակներ
Սլայդներ՝ 15 բառ՝ 563 հնչյուններ՝ 0 էֆեկտներ՝ 10Կարբոքսիլաթթուներ. Ուսումնասիրեք կառուցվածքը. Սրանք օրգանական նյութեր են: Վալերիկ թթու. Ցուցանիշ. Մրջնաթթու. Կարբոքսիլաթթուների դասակարգում. Օքսալաթթու. Կիտրոնաթթու. Քացախաթթու. Կարբոքսիլաթթուների քիմիական հատկությունները. Նրանք կազմում են եթերներ: Ստեարաթթու. Թթուներ. - Կարբոքսիլաթթուների օրինակներ.ppt
Կարբոքսիլաթթուների հատկությունները
Սլայդներ՝ 24 Բառեր՝ 328 Հնչյուններ՝ 0 Էֆեկտներ՝ 0Քիմիայի դասի մշակում. Ֆունկցիոնալ խմբի հայեցակարգը. Գուցե նա, ով կարծում է, որ կարող է: Բնութագրե՛ք օրգանական նյութերի նոր դասը: Թթու. Թթվային հատկություններ. Կարբոքսիլ խումբ. Մոնոբազային կարբոքսիլաթթուներ. Օրգանական նյութեր. Բնութագրման պլան. Կարբոքսիլաթթուներ. Դասակարգում. Կառուցվածքային իզոմերիզմ. Ֆիզիկական հատկություններ. Dimer կառուցվածքը. Էլեկտրոնային տեղաշարժ. Քիմիական հատկություններ. Ջրային լուծույթում տարանջատում. Հատկություններ. - Կարբոքսիլաթթուների հատկությունները.ppt
Կարբոքսիլաթթուները և դրանց հատկությունները
Սլայդներ՝ 28 Բառեր՝ 1463 Հնչյուններ՝ 0 Էֆեկտներ՝ 65Կարբոքսիլաթթուներ. Թթուների հայտնաբերում. Հետաքրքիր պատմական փաստեր՝ կապված օրգանական թթուների հետ. Եղինջ պարունակող մածուցիկ թթու. Բնության մեջ կարբոքսիլաթթուներ. Մրջնաթթուն առաջին անգամ մեկուսացվել է 17-րդ դարում։ Քացախաթթուն լայնորեն տարածված է բնության մեջ։ Օրգանական նյութեր. R-COOH. Կարբոքսիլաթթուների անվանացանկը. Դասակարգում. Dicarboxylic թթուներ. Կարբոքսիլաթթուների անվանման ալգորիթմ. Կարբոքսիլաթթուների բանաձևերը գրելու ալգորիթմ. Անվանեք նյութը: Էթանային կամ քացախաթթու: Քլորաքացախաթթու կամ քլորէթանաթթու: Ո՞ր թթունն է ավելի ուժեղ: - Կարբոքսիլաթթուները և դրանց հատկությունները.pptx
Կարբոքսիլաթթուների քիմիական հատկությունները
Սլայդներ՝ 17 բառ՝ 666 հնչյուններ՝ 0 էֆեկտներ՝ 25Կարբոքսիլաթթուների քիմիական հատկությունները. Ճանապարհ դեպի գիտելիք. Քիմիական հատկություններ. Ֆունկցիոնալ խումբ. Կարբոքսիլաթթուների բանաձևեր. Կարբոքսիլաթթուների անվանումը. Կարբոքսիլաթթուների աննշան անուններ. Կարբոքսիլ խմբի կառուցվածքը. Մրջնաթթու. Սալիցիլաթթու. Օքսալաթթու. Անօրգանական թթուների քիմիական հատկությունները. Կարբոքսիլաթթուների ընդհանուր հատկությունները. Կարբոքսիլաթթուներ. Առաջադրանք. - Կարբոքսիլաթթուների քիմիական հատկությունները.ppt
Կարբոքսիլաթթվի ածանցյալներ
Սլայդներ՝ 19 Բառեր՝ 412 Հնչյուններ՝ 0 Էֆեկտներ՝ 127Կարբոքսիլաթթուների ֆունկցիոնալ ածանցյալներ. Կարբոքսիլ. Կետոն. Կարբոքսիլաթթուների փոխարինող ապրանքներ. Էսթերներ. Էստերիֆիկացում. Մեթան (մորթաթթու): Ամիդներ. Մետանամիդ. Էսթերների և ամիդների քիմիական հատկությունները. Թթվային հիդրոլիզ. Հետադարձելի գործընթաց. Կատալիզատոր. Ամիդների հիդրոլիզ. Նուկլեոֆիլից հեռանալը. Եթերների հիդրոլիզ. Հանքային թթուների եթերներ. Ծծմբաթթվի եթերներ. Ֆոսֆորական թթվի եթերներ. - կարբոքսիլաթթուների ածանցյալներ.ppt
Հագեցած կարբոքսիլաթթուներ
Սլայդներ՝ 41 Բառեր՝ 1517 Հնչյուններ՝ 24 Էֆեկտներ՝ 62Մոնոհիմն կարբոքսիլաթթուների կառուցվածքը. Կարբոքսիլաթթուներ. Բոլոր կարբոքսիլաթթուները ունեն ֆունկցիոնալ խումբ: Ինքնակառավարման առաջադրանք. Չնչին անուններ. Հոմոլոգ շարք. Ֆիզիկական հատկություններ. Կարբոքսիլաթթուների քիմիական հատկությունները. Արձագանքեք հիմնական օքսիդների հետ: Այս թթուներից ո՞րն է ավելի ուժեղ: Կարբոքսիլաթթուների պատրաստում. Էթան. Սահմանում. Օրգանական նյութեր. Ընտրեք կարբոքսիլաթթվի բանաձևը: Կրկնել կարբոքսիլաթթուների որոշումը: Տեսություն. Եթերների նոմենկլատուրա. Իզոբուտիլացետատ. Անվանեք կարբոքսիլաթթուները: Դիմեթիլհեքսանաթթու. Պղնձի ացետատ. - Հագեցած կարբոքսիլաթթուներ.ppt
Հագեցած միահիմն կարբոքսիլաթթուներ
Սլայդներ՝ 13 բառ՝ 764 հնչյուններ՝ 1 էֆեկտներ՝ 20Հագեցած կարբոքսիլաթթուների կառուցվածքը և անվանակարգը: Հագեցած միահիմն կարբոքսիլաթթուներ: Կարբոքսիլաթթուներ. Իզոմերիզմի տեսակները. Ածխածնի ատոմ. Անվանեք կարբոքսիլաթթուները: Չնչին անուններ. Մոնոբազային կարբոքսիլաթթուներ. Ֆիզիկական հատկություններ. Հայտնաբերման պատմություն. Մրջնաթթու. Գազային նյութեր. Օրգանական նյութեր. - Սահմանափակել միահիմն կարբոքսիլաթթուները.ppt
Ճարպաթթու
Սլայդներ՝ 44 Բառեր՝ 2065 Հնչյուններ՝ 0 Էֆեկտներ՝ 0Պոլիչհագեցած ճարպաթթուները որպես ազդանշանային մոլեկուլներ: 1. Լիպիդոմիկա և լիպիդոլոգիա. Դասական պարադիգմ. Հետգենոմիկ դարաշրջանի պարադիգմ. Լիպիդոմիկայի նկատմամբ հետաքրքրությունը կապված է. 1. Բջիջների ուսումնասիրության ընդհանուր մոտեցումների փոփոխությունների հետ: Լիպիդոլոգիա. Հյուսվածքներ և բջիջներ. Լիպիդային էքստրակտներ. Լիպիդային պրոֆիլ. Ֆերմենտներ, սպիտակուցներ. Համակարգի կառավարում. Լիպիդոմիկա. Լիպիդոմիկայի տեղը այլ «-ոմիկաների» մեջ։ Համակարգի կառուցում. Կանխատեսում. Ախտորոշում. Բուժում. 2. Արախիդոնաթթու և այլ պոլիենային ճարպաթթուներ՝ որպես ազդանշանային մոլեկուլներ: n-6 Linoleic (18:2n-6) g-linolenic (18:3n-6) Dihomo-g - linolenic (18:3n-6) Arachidonic (20:4n-6) Docosatetraenoic (22:4n-6) Docosapentaenoic. (22:5n-6): - Fatty acids.ppt
Օմեգա թթու
Սլայդներ՝ 12 բառ՝ 617 հնչյուններ՝ 0 էֆեկտներ՝ 0OMEGA 3 և OMEGA 6 պոլիչհագեցած ճարպաթթուներ (PUFAs): Խաթարված է լորձաթաղանթների և մաշկի էպիթելի կառուցվածքը և գործառույթը: Բնորոշ է նաև մաշկի վնասվածքը՝ առաջանում են մաշկաբանական խանգարումներ, հակվածություն կա վարակվելու ենթամաշկային տիզերով։ OMEGA 3 խմբին պատկանող էիկոզապենտաենային և դոկոսահեքսաենային ճարպաթթուները դանդաղեցնում են ուռուցքների աճը։ PUFA-ների անբավարար ընդունման դեպքում կենդանիները նկատում են ավելի դանդաղ աճ, պտղաբերության նվազում և ֆիզիոլոգիական վիճակի վատթարացում: Վերջերս ուսումնասիրություններ են իրականացվել, որոնք ցույց են տալիս OMEGA 3 և OMEGA 6 ճարպաթթուների ազդեցությունը որպես իմունային համակարգի մոդուլատորներ: -


Առաջադրանքներ 1. Պարզե՛ք կարբոքսիլաթթուների ֆունկցիոնալ խումբը և ընդհանուր բանաձևը: 2. Ձևակերպիր սահմանում. 3. Ուսումնասիրել կարբոքսիլաթթուների դասակարգումը. 4. Վարպետ նոմենկլատուրային հմտություններ: 5. Դիտարկենք ամենակարևոր կարբոքսիլաթթուների ֆիզիկական և քիմիական հատկությունները: 6. Պարզի՛ր որոշ կարբոքսիլաթթուների կիրառման ոլորտները:

Բոլոր կարբոքսիլաթթուներն ունեն ֆունկցիոնալ խումբ Կարբոնիլ խումբ O - C Հիդրօքսիլ խումբ OH Կարբոքսիլ խումբ Ընդհանուր բանաձև R C O OH Կամ հագեցած միհիմն թթուների համար O OH Cn H2n+1C. Ի՞նչ են կոչվում կարբոքսիլաթթուները: Կարբոքսիլաթթուները օրգանական միացություններ են, որոնց մոլեկուլները պարունակում են կարբոքսիլ խումբ՝ COOH, կապված ածխաջրածնային ռադիկալի հետ։ ? Ինչպե՞ս են կարբոքսիլաթթուները գենետիկորեն կապված ալդեհիդների նախկինում ուսումնասիրված դասի հետ: R C O H + [O] R C O OH [O]= KMnO4, K2Cr2O7+ H2SO4 խտ. Կարբոքսիլաթթուները օրգանական միացություններ են, որոնց մոլեկուլները պարունակում են կարբոքսիլ խումբ՝ COOH, կապված ածխաջրածնային ռադիկալի հետ։ Ռ Ք

Կարբոքսիլային թթուների դասակարգումը Կախված կարբոքսիլային խմբերի քանակից Միահիմն Երկհիմն (քացախային) (օքսալային) O OH CH3C C - CO OH O HO Կախված ռադիկալի բնույթից Հագեցած (պրոպիոնիկ) O CH3- CH2-C OH Չհագեցած (ակրիլ) O CH2= CH-C OH Բազմհիմն (կիտրոն) O H2C – C OH HC - C O OH O H2C - C OH Անուշաբույր (բենզոիկ) C O OH Ըստ C ատոմների պարունակության՝ C1C9 ցածր, C10 և բարձր.

Դասակարգեք առաջարկվող թթուները 1) CH3 – CH2 – CH2 – CH2 COOH 1. Միահիմք, հագեցած, ցածր 2) HOOC CH2 CH2 COOH 2. Երկհիմնական, հագեցած, ցածր 3) COOH CH3 3. Միաբազային, հագեցած, ցածր 4) CH3 – ( CH2 )7 –CH = CH (CH2)7 COOH 4. Միաբազային, չհագեցած, ավելի բարձր 5) HOOC –CH2 CH – CH2 COOH COOH 5. Բազմաբազային, հագեցած, ցածր

ԱԾԽԱԹԹՈՒՆԵՐԻ ԱՆՎԱՆԱԿԱՆԱԿԱՆՈՒԹՅՈՒՆ ՔԱՐԲՈՔՍԻԼ ԹԹՎՆԵՐԻ ԱՆՎԱՆԱԿԱՆՈՒԹՅՈՒՆ ԱԼԿԱՆԱԹԹՈՒ + ՕԲ + ԱՆԻԹԹՈՒ ԱԼԿԱՆ ՄԵԹԱՆԱԿԱՆ ԹԹՎԻ ՄԵԹԱՆ ԹԹՈՒ (FOMIC ACID)

2 1 CH3 – COOH COOH CH3 – էթանաթթու թթու (քացախաթթու)) 33 44 11 COOH CH3 – CH2 – CH2 COOH CH3 – CH2 – CH2 22 ԲՈՒՏԱՆԱԿԱՆ ԹԹՈՒ ԲՈՒՏԱԹԹՈՒ (ԲՈՒՏԻԿԱԹԹՈՒ)

44 22 55 11 COOH CH3 – CH2 – CH2 – CH2 – COOH CH3 – CH2 – CH2 – CH2 – 33 ՊԵՆՏԱՆԱԿԱՆ ԹԹՈՒ ՊԵՆՏԱՆ (ՎԱԼԵՐԻԱՆ ԹԹՈՒ) (ՎԱԼԵՐԻԱՆ ԹԹՈՒ) 22 NOOS – NOOS – NOOH ACID 11 (COOHVAACOIDIC) Օքսալաթթու)

Կարբոքսիլային թթուների հոմոլոգ շարք Քիմիական բանաձև Թթվի համակարգային անվանում Թթվային մնացորդի անվանումը Ֆորմատ ացետատ պրոպիոնատ բուտիրատ կապրիկատ HCOOH CH3COOH CH3CH2COOH CH3CH2CH2COOH2CH2CH3 Պրոպան բութան գրիչ tanovaya hexane մածուցիկ քացախաթթու propionic նավթ նեյլոնե valerian valerinate CH3(CH2)8 – COOH Decane capric CH3(CH2)14 – COOH CH3(CH2)16 COOH Hexadecane Octadecane Palmitic palmitate Stearic stearate

Կարբոքսիլաթթուների անվանման ալգորիթմ՝ 1. Գտե՛ք ածխածնի ատոմների հիմնական շղթան և համարակալե՛ք այն՝ սկսած կարբոքսիլ խմբից։ 2. Նշում ենք փոխարինողների դիրքը և նրանց անվանում(ներ)ը: 3. Արմատից հետո, շղթայում նշելով ածխածնի ատոմների թիվը, գալիս է «օիկ» թթու վերջածանցը։ 4. Եթե կան մի քանի կարբոքսիլ խմբեր, ապա «ova»-ից առաջ մի թիվ է դրվում (di, երեք...) Օրինակ՝ 4 CH3 3 CH 2 CH2 1 COOH CH3 3 մեթիլբութան + ձվաբջիջ = 3մեթիլբուտանաթթու.

ՆՅՈՒԹԵՐԻՆ ԱՆՎԱՆՎԵԼ ՆՅՈՒԹԵՐԻՆ ԱՆՎԱՆՎԵԼ ՀԱՄԱՁԱՅՆ ՄԻՋԱԶԳԱՅԻՆ ԱՆՎԱՆԱԿԱՆՈՒԹՅԱՆԸ (2 – ՄԵԹԻԼՊՐՈՊԱՆ (2 – ՄԵԹԻԼՊՐՈՊԱՆՈԹԹԹՈՒ) CH3 – CH – COOH 1.1. CH3 – CH – COOH CH3CH3 2. CH3 – CH2 – CH – CH – COOH 2. CH3 – CH2 – CH – CH – COOH CH3CH3 CH3CH3 (2, 3 – DIMETHYL PENTA PENTA (2, 3 – DIMETHYL NNOVAICID) CH3 – CH = CH – CH – COOH 3. CH3 – CH = CH – CH – COOH CH3CH3 4. HOOC – CH2 – CH – COOH 4. HOOC – CH2 – CH – COOH CC22NNH55 (2 – ՄԵԹԻԼՊԵՆՏ (2 – ACIDME). ) ԹԹՈՒ) ՊԵՆՏԵՆԵՆ – 3– 3 – ՕՎԱ – ՕՎԱ (2 – ԷԹԻԼ ԲՈՒՏԱՆ (2 – ԷԹԻԼ ԲՈՒՏԱՆԵԴԻՈԹԹԹՈՒ)

Կարբոքսիլաթթուների բանաձևերը գրելու ալգորիթմ. 1. Ընտրեք բառի արմատը, որի հիման վրա գրեք ածխածնային կմախքը բաղադրության մեջ, որը ներառում է կարբոքսիլ խումբ: 2. Ածխածնի ատոմները համարակալում ենք՝ սկսած կարբոքսիլային խմբից։ 3. Փոխարինիչներ նշում ենք ըստ համարակալման։ 4. Անհրաժեշտ է ավելացնել բացակայող ջրածնի ատոմները (ածխածինը քառավալենտ է): 5. Ստուգեք, արդյոք բանաձեւը ճիշտ է գրված: Օրինակ՝ 4 3 2 1 C C C COOH 2methylbutanoic թթու: 4 3 2 1 C C C COOH 4 3 2 1 CH3 CH2 CH COOH CH3 CH3

ՖԻԶԻԿԱԿԱՆ ՀԱՏԿՈՒԹՅՈՒՆՆԵՐ ՖԻԶԻԿԱԿԱՆ ՀԱՏԿՈՒԹՅՈՒՆՆԵՐ CC11 – – CC33 Հեղուկներ՝ բնորոշ սուր հոտով Հեղուկներ՝ բնորոշ սուր հոտով, կծու հոտով, շատ լուծելի են ջրում, շատ լուծելի են ջրում CC44 – C – C99 Մածուցիկ յուղոտ Մածուցիկ յուղոտ մածուցիկ անտուր յուղոտ հեղուկներ, որոնք պարունակում են հեղուկներ , ջրում վատ լուծվող ջրում CC1010 և ավելին Պինդ, Պինդ, անհոտ, անհոտ, չլուծվող ջրի մեջ չլուծվող ջրում

Քացախաթթվի ֆիզիկական հատկությունները. Ֆիզիկական վիճակ հեղուկ Գույն անգույն թափանցիկ հեղուկ Հոտ կծու քացախաթթու Ջրում լուծելիությունը լավ է Եռման ջերմաստիճանը 118 º C Հալման ջերմաստիճանը 17 º C

Կարբոքսիլաթթուների ֆիզիկական հատկությունների կախվածությունը մոլեկուլի կառուցվածքից. Ստորին կարբոքսիլաթթուները հեղուկներ են. ավելի բարձր - պինդ նյութեր, որքան մեծ է թթվի հարաբերական մոլեկուլային քաշը, այնքան քիչ է նրա հոտը: Քանի որ թթվի հարաբերական մոլեկուլային քաշը մեծանում է, լուծելիությունը նվազում է. Սա ինչի՞ հետ է կապված։

Կարբոքսիլաթթուների քիմիական հատկությունները Կարբոքսիլաթթուների քիմիական հատկությունները I. Տարածված անօրգանական թթուների հետ տարանջատում. 1. Լուծվող կարբոքսիլաթթուներ ջրային լուծույթներում CH3 – COOH CH3 – COO + H + Արդյո՞ք միջինը թթվային է: Ինչպե՞ս կփոխվի ցուցիչների գույնը թթվային միջավայրում: 2. Էլեկտրաքիմիական լարման շարքի մետաղների հետ փոխազդեցություն մինչև ջրածին. Լակմուս (մանուշակագույն) - դառնում է կարմիր Մեթիլ նարնջագույն - դառնում է վարդագույն Ֆենոֆթալեին - չի փոխում գույնը 2CH3 - COOH + Mg Քացախաթթու 2CH3 COOH + Zn Քացախաթթու (CH3 -COO) 2 մգ մագնեզիումի ացետատ (CH3 – COO) 2Zn Ցինկի ացետատ + H2 + H2 Երբ մետաղը փոխազդում է կարբոքսիլաթթվի լուծույթի հետ, առաջանում են ջրածին և I աղ: Տարածված է անօրգանական թթուների հետ

3. Փոխազդեցություն հիմնային օքսիդների հետ՝ 2 CH3 – COOH + CuO Քացախաթթու (CH3 – COO) 2Сu Պղնձի ացետատ t + H2O 4. Փոխազդեցություն մետաղների հիդրօքսիդների հետ (չեզոքացման ռեակցիա) CH3 – COOH + HO –Na Քացախաթթու 2CH3 – COOH + Cu. (OH)2 Քացախաթթու CH3COONa Նատրիումի ացետատ + H2O (CH3COO) 2Cu Պղնձի ացետատ + H2O 5. Փոխազդեցություն ավելի թույլ և ցնդող թթուների աղերի հետ (օրինակ՝ ածխածնային, սիլիցիում, ջրածնի սուլֆիդ, ստեարիկ, պալմիտիկ...) 2CH3–COOH Քացախաթթու + Na2CO3 նատրիումի կարբոնատ 2CH3COONa Նատրիումի ացետատ + H2CO3 CO2 H2O

Մրջնաթթվի «Արծաթի հայելի» ռեակցիա O + Ag2O t 2Ag + H2CO3 H C OH Մրջնաթթու Արծաթի օքսիդ արծաթ CO2 H2O

Բնության մեջ հայտնվելը և կարբոքսիլաթթուների օգտագործումը Մաթանաթթու (Մեթանաթթու) - Քիմիական բանաձև CH2O2 կամ HCOOH: Մրջնաթթուն հայտնաբերվել է կարմիր մրջյունների թթվային սեկրեցներում 1670 թվականին անգլիացի բնագետ Ջոն Ռեյի կողմից։ Մրջնաթթուն առկա է նաև եղինջի լավագույն մազերում՝ մեղվի թույնի, սոճու ասեղների մեջ և փոքր քանակությամբ հայտնաբերվում է տարբեր մրգերում, հյուսվածքներում, օրգաններում, ինչպես նաև կենդանիների և մարդկանց սեկրեցներում:


Հարց. Ինչո՞ւ չես կարող մրջյունի կծածի կամ եղինջի խայթոցի հատվածը ջրով թրջել: Սա միայն հանգեցնում է ցավի ավելացման: Ինչու՞ է ցավը թուլանում, եթե վիրավոր տարածքը թրջվում է ամոնիակով: Էլ ի՞նչ կարելի է օգտագործել այս դեպքում: Մրջնաթթուն ջրում լուծելիս տեղի է ունենում էլեկտրոլիտիկ տարանջատման գործընթաց՝ HCOOH HCOO + H Արդյունքում շրջակա միջավայրի թթվայնությունը մեծանում է, իսկ մաշկի կոռոզիայի պրոցեսն ուժեղանում է։ Որպեսզի ցավը թուլանա, պետք է չեզոքացնել թթուն, ինչի համար պետք է օգտագործել ալկալային ռեակցիա ունեցող լուծույթներ, օրինակ՝ ամոնիակի լուծույթ։ HCOOH + NH4OH HCOONH4 + H2O կամ HCOOH + NaHCO3 HCOONa + CO2 + H2O

Քացախաթթու (էթանաթթու) Սա մարդու կողմից ստացված և օգտագործված առաջին թթունն է: «Ծնվել է» ավելի քան 4 հազար տարի առաջ Հին Եգիպտոսում: 17-18-րդ դարերի վերջին Ռուսաստանում այն կոչվում էր «թթու խոնավություն»: Առաջին անգամ այն ստացանք գինու թթվացման ժամանակ։ Լատինական անվանումը Acetum acidum է, այստեղից էլ առաջացել է աղերի անվանումը՝ ացետատներ։ Սառցադաշտային քացախաթթուն 16,8 ºС-ից ցածր ջերմաստիճանում կարծրանում է և դառնում սառույցի պես 70% թթվային լուծույթ: Սեղանի քացախ 6% կամ 9% թթվային լուծույթ: Քացախաթթուն հայտնաբերվում է կենդանիների սեկրեցներում (մեզ, լեղ, կղանք), բույսերում (մասնավորապես կանաչ տերևներ), թթու կաթում և պանիրում; առաջանում է գինու և գարեջրի խմորման, փտման, թթվացման և շատ օրգանական նյութերի օքսիդացման ժամանակ.

Քացախաթթվի կիրառում Քացախաթթվի կիրառում Քացախաթթվի ջրային լուծույթները լայնորեն օգտագործվում են սննդի արդյունաբերության մեջ (սննդային հավելում E 260) և կենցաղային խոհարարության, ինչպես նաև պահածոյացման մեջ. արտադրության մեջ՝ դեղեր, HP, ասպիրին; արհեստական մանրաթելեր, օրինակ՝ մետաքսի ացետատ; ինդիգո ներկեր, ոչ դյուրավառ թաղանթ, օրգանական ապակի; լաքի լուծիչներ; բույսերի պաշտպանության քիմիական միջոցներ, բույսերի աճի խթանիչներ; Նատրիումի ացետատ CH3COONa-ն օգտագործվում է որպես փոխներարկման համար նախատեսված արյան կոնսերվանտ; Կալիումի ացետատ CH3COOK – որպես միզամուղ; Կապարի ացետատ (CH3COO) 2 Pb մեզի մեջ շաքարի որոշման համար; Երկաթի (III) (CH3COO)3Fe, ալյումինի (CH3COO)3Al և քրոմի (III) (CH3COO)3Cr-ի ացետատներն օգտագործվում են տեքստիլ արդյունաբերության մեջ մաշված ներկման համար. Պղնձի (II) ացետատը (CH3COO)2Cu ներառված է բույսերի վնասատուների դեմ պայքարի պատրաստման մեջ, այսպես կոչված, փարիզյան կանաչ; Քացախաթթվի ջրային լուծույթները լայնորեն օգտագործվում են սննդի արդյունաբերության (սննդային հավելում E 260) և կենցաղային խոհարարության, ինչպես նաև պահածոյացման մեջ; արտադրության մեջ՝ դեղեր, HP, ասպիրին; Արհեստական մանրաթելեր, օրինակ Միզամուղ; Պղնձի ացետատ (II) (CH3COO)2Cu բույսերի վնասատուների դեմ պայքարի պատրաստուկի մի մասն է, այսպես կոչված, փարիզյան կանաչ;

Քացախաթթվի օգտագործումը Սպիրտային քացախի օգտագործումը կոսմետոլոգիայում հայտնի է։ Մասնավորապես՝ մազերին փափկություն և փայլ հաղորդելու համար պերմի և մշտական ներկումից հետո։ Դրա համար խորհուրդ է տրվում մազերը ողողել տաք ջրով` ալկոհոլային քացախի ավելացումով (1 լիտր ջրի դիմաց 34 ճաշի գդալ քացախ): Ժողովրդական բժշկության մեջ քացախն օգտագործվում է որպես ջերմության ոչ սպեցիֆիկ միջոց։ գլխացավերի դեպքում՝ օգտագործելով լոսյոններ. միջատների խայթոցների համար, օգտագործելով կոմպրեսներ: Իսկ դուք գիտե՞ք, որ եթե ժանգոտ ընկույզը պետք է պտտել, ապա երեկոյան խորհուրդ է տրվում վրան քացախաթթվի մեջ թաթախված լաթ դնել։ Առավոտյան շատ ավելի հեշտ կլինի այս ընկույզը հանելը: Օրվա ընթացքում օրգանիզմում առաջանում է 400 գ քացախաթթու. Դա բավական կլիներ 8 լիտր սովորական քացախը դարձնելու համար, որն անփոխարինելի է օծանելիքի արտադրության մեջ.

N N S C 3 O O Բոլոր թթուներից Դա, իհարկե, պրիմա է: Ներկայացրե՛ք ամենուր՝ և՛ տեսանելի, և՛ անտեսանելի: Այն առկա է կենդանիների և բույսերի մեջ, տեխնոլոգիան և բժշկությունը հավերժ նրա հետ են: Նրա սերունդները շատ անհրաժեշտ «տղերք» են: Հայտնի ասպիրինը, ինչպես լավ ջենթլմենը, նվազեցնում է հիվանդի ջերմությունը և վերականգնում առողջությունը։ Սա պղնձի ացետատ է: Նա բույսերի ընկերն ու եղբայրն է, Սպանում է նրանց թշնամիներին: Թթուն դեռևս որոշակի կիրառություն ունի. այն մեզ հագցնում է ացետատ մետաքս: Իսկ ով սիրում է պելմենի, քացախը վաղուց գիտի։ Կա նաև կինոյի հարցը. Դե, բոլորը պետք է իմանան, որ առանց ացետատ ֆիլմի մենք չենք կարող կինո տեսնել։ Իհարկե, կան այլ կիրառումներ. Եվ դուք գիտեք նրանց առանց կասկածի: Բայց հիմնականը, որ ասվում է, ընկերներ, այն է, որ «արդյունաբերության հացը» քացախաթթու է։ Պղնձի ացետատի CH3COOH ջրային լուծույթ
Եզրակացություններ 1. Կարբոքսիլաթթուները օրգանական միացություններ են, որոնց մոլեկուլները պարունակում են կարբոքսիլ խումբ՝ COOH, որը կապված է ածխաջրածնային ռադիկալի հետ: 2.Կարբոքսիլաթթուները դասակարգվում են՝ ըստ հիմնականության (մեկ, երկու և բազմաբազային) ըստ ածխաջրածնային ռադիկալի (հագեցած, չհագեցած և անուշաբույր) ըստ C ատոմների պարունակության (ստորին և բարձր) 3. Կարբոքսիլաթթվի անվանումը կազմված է անունից. ալկան + օվալաթթու: 4. Կարբոքսիլաթթվի մոլեկուլային զանգվածի մեծացման հետ թթվի լուծելիությունն ու ուժը նվազում են։ 5. Ինչպես անօրգանական թթուները, լուծվող կարբոքսիլաթթուները տարանջատվում են ջրային լուծույթում՝ առաջացնելով ջրածնի իոններ և փոխելով ցուցիչի գույնը։ Փոխազդում են մետաղների (մինչև H), հիմնային և ամֆոտերային օքսիդների և հիդրօքսիդների և ավելի թույլ թթուների աղերի հետ՝ առաջացնելով աղեր։ 6 Լայնորեն տարածված են բնության մեջ և ունեն մեծ գործնական նշանակություն մարդկանց համար։

Տնային առաջադրանք 1. 2. §14, վարժություն թիվ 6 վարժություն թիվ 9 Կլեոպատրա թագուհին պալատական բժշկի խորհրդով ոսկերիչներին հայտնի ամենամեծ մարգարիտը լուծեց քացախի մեջ, իսկ հետո որոշ ժամանակ վերցրեց ստացված լուծույթը։ Ի՞նչ արձագանք տվեց Կլեոպատրան: Ի՞նչ կապ էր նա վերցնում: 3. Պատրաստեք զեկույց ավելի բարձր կարբոքսիլաթթուների մասին

«Մաթեմատիկան այն լեզուն է, որով գրված է բնության գիրքը»
ԳԱԼԻԵՈ ԳԱԼԻԼԻ - ԻՏԱԼԻԱ ՄԱԹԵՄԱՏԻԿՈՍ, ՖԻԶԻԿՈՍ, ԱՍՏՂԱԳԻՏ


Գիտելիքների թարմացում
Ալդեհիդները օրգանական նյութեր են, որոնց մոլեկուլները պարունակում են ատոմների ֆունկցիոնալ խումբ՝ COH՝ կապված ածխաջրածնային ռադիկալի հետ։
Կարբոնիլ - - C = O;
Ալդեհիդային - - C = O
1. Ի՞նչ միացություններ են ալդեհիդները:
2. Ո՞ր ֆունկցիոնալ խումբն է կոչվում կարբոնիլ, որը՝ ալդեհիդ: Ո՞րն է նրանց միջև տարբերությունը:
3. Ո՞ր ռեակցիաներն են առավել բնորոշ ալդեհիդներին:
4. Թվարկե՛ք թթվածին պարունակող միացությունների հետ կապված օրգանական միացությունների հիմնական դասերը:
Ավելացման և օքսիդացման ռեակցիաներ.
Ալկոհոլներ, ալդեհիդներ, կետոններ, կարբոքսիլաթթուներ, ածխաջրեր:


Դասի նպատակները
Ուսումնական:
Աշակերտներին ծանոթացնել կարբոքսիլաթթուների հայեցակարգին և դրանց դասակարգմանը. կարբոքսիլային թթուների հատկությունները (այրում, էսթերիֆիկացում)՝ օգտագործելով ձևային և քացախաթթուների օրինակը. կարբոքսիլաթթուների կիրառում` հիմնվելով դրանց հատկությունների վրա:
Ուսումնական:
Խթանել դրական վերաբերմունք քիմիայի նկատմամբ:
Զարգացնող: զարգացնել ուսումնասիրված նյութերը անվանելու կարողություն՝ օգտագործելով չնչին և միջազգային նոմենկլատուրա. որոշել ռեակցիաների տեսակները, որոնցում մտնում են կարբոքսիլաթթուները. բնութագրել կարբոքսիլաթթուների կառուցվածքը և հատկությունները. բացատրել կարբոքսիլաթթուների ռեակտիվության կախվածությունը դրանց մոլեկուլների կառուցվածքից. իրականացնել քիմիական փորձ՝ քացախաթթվի աղեր ստանալու համար. օգտագործել ձեռք բերված գիտելիքներն ու հմտությունները գործնական գործունեություն(անվտանգ աշխատանք նյութերի հետ լաբորատորիայում և տանը); տվյալ կոնցենտրացիաների լուծույթներ պատրաստելու ունակություն.

Կարբոքսիլաթթուներ (կառուցվածք)
Կարբոքսիլ
խումբ
ածխաջրեր օնիլ խումբ
հիդր օքսիլ խումբ




Դասակարգում
Ռադիկալի բնույթով
Ըստ կարբոքսիլային խմբերի քանակի՝ մեկ, երկու, երեք հիմնական
Ո՞ր դասին են պատկանում հետևյալ թթուները.
Չ 3 - C = O
O = C – C = O
ԲԱՅՑ ՆԱ
Չ 2 = CH – C = O
- C = O

համակարգված և տրիվիալ նոմենկլատուրա
N-COOH - մեթան ov այա (մրջյուն)
Չ 3 -COOH – էթան ov այա (քացախ)
NOOS-COON – էթան դիո վայա (օքսալ)
ՆՈՈՍ-ՍՆ 2 -Չ 2 -COOH - բութան դիով եւ ես
(սաթի)
ՀԵՏ 6 Ն 5 COOH - բենզոիկ
ՀԵՏ 17 Ն 35 COOH – ստեարիկ
ՀԵՏ 17 Ն 33 COOH - oleic

հարցում
- Անվանեք նյութերը.
Չ 2 - Չ - Չ – ԿԱԶՄ
Չ 3 Չ 3 Չ 3
Չ 3
Չ 3 - C – CH 2 – ԿԱԶՄ
Չ 3
- 2 մեթիլբուտանաթթու
- 2,2 դիմեթիլպրոպանաթթու
- 3,3 երկքլորէքսանաթթու

Ֆիզիկական հատկություններ
- ՀԵՏ 1 - ՀԵՏ 3 հեղուկներ՝ բնորոշ սուր հոտով
- ՀԵՏ 4 - ՀԵՏ 9 մածուցիկ յուղոտ հեղուկներ՝ տհաճ հոտով
- գ Գ 10 չլուծվող պինդ նյութեր
- Կարբոքսիլաթթուները միջմոլեկուլային ջրածնային կապերի առկայության պատճառով ունեն բարձր եռման կետ և գոյություն ունեն հիմնականում դիմերների տեսքով։
- Հարաբերական մոլեկուլային քաշի ավելացման հետ մեկտեղ ավելանում է հագեցած միաբազային թթուների եռման կետը

Ն–Ս
Մրջնաթթու
- Պարունակվում է մրջյունների թունավոր գեղձերի, եղինջի և եղևնի ասեղների մեջ։
- 10 անգամ ավելի ուժեղ, քան բոլոր կարբոքսիլաթթուները:
- Այն ստացվել է 1831 թվականին Տ.Փելուզի կողմից հիդրոցիանաթթվից։
Օգտագործված:
- որպես կաշի ներկելու և դաբաղելու միջոց
- բժշկության մեջ
- բանջարեղեն պահածոյացնելիս
- որպես նեյլոնի, նեյլոնի, պոլիվինիլի լուծիչ

Մրջնաթթվի հատկությունները և օգտագործումը
- Անգույն հեղուկ՝ սուր հոտով, ջրի մեջ շատ լուծելի .
- Այն կարող է դրսևորել ինչպես թթուներին, այնպես էլ ալդեհիդներին բնորոշ հատկություններ:

Չ 3 - ՀԵՏ
Քացախաթթու
Հանդիպում է որոշ բույսերի, քրտինքի, մեզի, մաղձի մեջ։ Մարդու օրգանիզմն օրական արտազատում է 0,5 կգ այս թթու։
- Հայտնի է անհիշելի ժամանակներից։
- IN մաքուր ձևհատկացված 1700 թ
- 1845 թվականին Գ.Կոլբեն այն ձեռք է բերել սինթետիկ եղանակով։
- Այն կարող է ձևավորվել նաև սինթետիկ (բակտերիաների ազդեցության տակ գինու թթվացում)։

Քիմիական հատկություններ
Փոխազդեցություն ակտիվ մետաղների հետ:
2CH 3 COOH + Mg = (CH 3 COO) 2 Mg+H 2
Փոխազդեցություն ալկալիների հետ:
Չ 3 COOH + NaOH = CH 3 COONa + H 2 Օ
Փոխազդեցությունը հիմնական օքսիդների հետ:
2CH 3 COOH + CaO = (CH 3 COO) 2 Ca+H 2 Օ
Փոխազդեցություն աղերի հետ.
2CH 3 COOH+Na 2 CO 3 = 2CH 3 COONa + H 2 O+CO 2
Ալկոհոլների հետ փոխազդեցություն
Չ 3 COOH + HOC 2 Հ 5 =CH 3 -CO-O-C 2 Հ 5 +Հ 2 Օ
էթիլացետատ
եթեր
Բնության մեջ եթերները հանդիպում են ծաղիկների, մրգերի և հատապտուղների մեջ։ Դրանք օգտագործվում են մրգային ջրերի և օծանելիքի արտադրության մեջ։

Քացախաթթվի հատկությունները և օգտագործումը
Անգույն հեղուկ, բնորոշ հոտ, ջրի մեջ լուծվող, լավ լուծիչ շատ օրգանական նյութերի համար, վտանգավոր է մաշկի հետ շփման դեպքում:

Կարբոքսիլաթթուների պատրաստում
- Առաջնային սպիրտների և ալդեհիդների օքսիդացում (թթվածին կատալիզատորի վրա և KMnO 4 ; Կ 2 Քր 2 Օ 7 ):
R-CH 2 Օհ → RCOH → RCOOH
- մեթանի կատալիտիկ օքսիդացում.
2CH 4 + 3O 2 → 2H–COOH + 2H 2 Օ
- բութանի կատալիտիկ օքսիդացում.
2CH 3 -Չ 2 -Չ 2 -Չ 3 +5Օ 2 → 4CH 3 COOH + 2H 2 Օ
- Արոմատիկ թթուները սինթեզվում են բենզոլի հոմոլոգների օքսիդացումով. KMnO-ի լուծույթները կարող են օգտագործվել որպես օքսիդացնող նյութ: 4 կամ Կ 2 Քր 2 Օ 7 թթվային միջավայրում.
Գ 6 Հ 5 Չ 3 ՀԵՏ 6 Ն 5 COOH+H 2 Օ
(5C 6 Հ 5 Չ 3 + 6KMnO 4 +9H 2 ԱՅՍՊԵՍ 4 → 5C 6 Հ 5 COOH + 3K 2 ԱՅՍՊԵՍ 4 + 6MnSO 4 +14 ժ 2 Օ)

դիմումը
- Մրջնաթթու– բժշկության մեջ, մեղվաբուծության մեջ, օրգանական սինթեզում, լուծիչների և կոնսերվանտների արտադրության մեջ. որպես ուժեղ վերականգնող նյութ:
- Քացախաթթու- սննդի և քիմիական արդյունաբերության մեջ (ցելյուլոզային ացետատի արտադրություն, որից արտադրվում են ացետատ մանրաթել, օրգանական ապակի, թաղանթ; ներկանյութերի, դեղամիջոցների և էսթերների սինթեզի համար):
- Բուտիրաթթու– բուրավետիչ հավելումների, պլաստիկացնողների և ֆլոտացիոն ռեակտիվների արտադրության համար:
- Օքսալաթթու– մետալուրգիական արդյունաբերությունում (մաքրում):
- Ստեարիկ C17H35COOH և պալմիտիկ թթու C 15 H 31 COOH – որպես մակերևութային ակտիվ նյութեր, քսանյութեր մետաղամշակման մեջ:

Վերահսկիչ հարցեր
- Ո՞ր նյութն է առաջացնում եղինջի և մեդուզայի խայթող բջիջների խայթող ազդեցությունը.
ա) մածուցիկ թթու, բ) մակաբույծ ալդեհիդ
2. Ինչպե՞ս թեթևացնել եղինջի սեկրեցներից առաջացած այրվածքի ցավը.
ա) լվանալ ջրով, բ) լվանալ թույլ ալկալային լուծույթով,
գ) լվանալ քացախաթթվի թույլ լուծույթով:
3. Կառուցվածքային բանաձեւմածուցիկ թթու կարելի է գրել այսպես HO-SON: Հետևաբար, այս թթուն կլինի երկակի ֆունկցիա ունեցող նյութ։ Ինչպես կարող եք դա անվանել.
ա) սպիրտ, բ) ալդեհիդային սպիրտ, գ) թթու
4. Հնարավո՞ր է դիտարկել քանակական հարաբերությունների անցումը որակականի` օգտագործելով կարբոքսիլաթթուների ֆիզիկական հատկությունների փոփոխությունների օրինակը հոմոլոգ շարքում:

5. Առաջարկվող բանաձևերից գրի՛ր կարբոքսիլաթթուների բանաձևերը և անվանի՛ր դրանք.
Չ 3 , Չ 3 COOH, C 2 Ն 5 Օհ, ՍՆ 3 ՔՆԵԼ, Ս 2 Ն 4 , ՀԵՏ 15 Ն 31 COOH, C 6 Ն 6 , ՀԵՏ 5 Ն 11 COOH, C 3 Ն 7 UNS
6. Ինչ նյութերի հետ կփոխազդի քացախաթթուն.
ա) ցինկ, նատրիումի օքսիդ, մագնեզիումի հիդրօքսիդ, նատրիումի կարբոնատ, սպիրտ (էթիլ)
բ) ցինկ, նատրիումի օքսիդ, մագնեզիումի հիդրօքսիդ, նատրիումի կարբոնատ, մեթան
Գրե՛ք ռեակցիայի հավասարումները։

ՓՈԽԱԶԳԱՅԻՆ ԳԻՏԵԼԻՔՆԵՐԻ ՍՏՈՒԳՈՒՄ
1) ա; 2) բ; 3) բ;
4) հնարավոր է` ելնելով ֆիզիկական և քիմիական հատկություններից.
5) Չ 3 COOH, C 15 Ն 31 COOH, C 5 Ն 11 COOH, C 3 Ն 7 COOH; 6) ա.
2CH 3 COOH + Zn = (CH 3 ՍՈՈ) 2 Zn + H 2
2CH 3 COOH + MgO = (CH 3 ՍՈՈ) 2 Mg + H 2 ՄԱՍԻՆ
2CH 3 COOH + Mg (OH) 2 = (CH 3 ՍՈՈ) 2 Mg + 2H 2 ՄԱՍԻՆ
2CH 3 COOH + Na 2 CO 3 = 2CH 3 COONa + H 2 CO 3
Չ 3 COOH + C 2 Ն 5 ՆԱ = CH 3 COO C 2 Ն 5 + Ն 2 ՄԱՍԻՆ


Շնորհակալություն ուշադրության համար
Տնային առաջադրանք՝ էջ 153 - 157
Քիմիա, տեխնիկական մասնագիտությունների դասագիրք, Մ, «Ակադեմիա», 2011 թ.
Պատրաստել պրեզենտացիաներ կարբոքսիլաթթուների առանձին տեսակների համար (թարթառ, կաթնաթթու, խնձորաթթու, կիտրոն և այլն):
Աշխատանքային տետր էջ 21.
Պատրաստվելու համար գործնական աշխատանք«Քացախաթթվի ուսուցումը և դրա հետ կապված փորձերը»