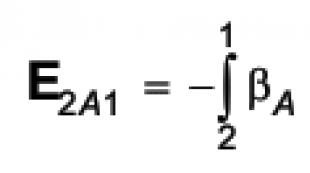Քիմիայի հիմնական հասկացություններն ու օրենքները. Հեմոգլոբինի մոլային զանգված Հեմոգլոբինի մոլեկուլային քաշը
15. Տրված ջերմաստիճանում 0,2 մոլ/լ կոնցենտրացիա ունեցող մակերեւութային ակտիվ նյութի լուծույթից ներծծվում է 2 96 10 3 մոլ/գ նյութ ինչ-որ ներծծվող նյութով: Որոշեք ներծծող նյութի կլանման հզորությունը (մոլ/գ-ով), եթե հաստատունը a 0 07 մոլ/լ է:
[ներծծող հզորությունը 4 00 10 3 մոլ/գ]
16. Օգտագործելով Ֆրեյնդլիխի հավասարումը, հաշվարկեք քացախաթթվի հավասարակշռության կոնցենտրացիան լուծույթում, եթե 1 գ ածուխ.
17. Որոշեք ադսորբցիայի տեսակը, երբ ացետոնը լուծվում է ջրում, եթե ացետոնի կոնցենտրացիան ջրում 29 գ/լ է, մակերես.
լուծման լարվածություն - 59 4 |
3 Ն/մ, մակերեսային լարվածություն |
||||||
ջուր - 73 49 10 |
3 Ն/մ, Տ |
||||||
[կլանումը դրական, |
6 մոլ մ2] |
||||||
18. Իզոբուտիրաթթվի լուծույթի 0,125-ից 0,250 մոլ/լ-ի կոնցենտրացիայի բարձրացմամբ նրա մակերեւութային լարվածությունը նվազել է 55,1-ից 47,9 մՆ/մ, իսկ իզովալերաթթվի լուծույթինը՝ 43,2-ից 35,0 մՆ/մ։ Համեմատեք նյութերի կլանման արժեքները տվյալ կոնցենտրացիայի միջակայքում 293 Կ.
19. Որոշեք, թե արդյոք ջրային լուծույթներից մակերեւութային ակտիվ նյութի կլանման քանակությունը մեծանում է, թե նվազում կոնցենտրացիայի ավելացման հետ (T 298 K), եթե հայտնի են հետևյալ փորձարարական տվյալները.
[կլանումը մեծանում է 2 12 10 6-ից մինչև 9 09 10 6 մոլմ2՝ լուծույթում մակերեւութային ակտիվ նյութի կոնցենտրացիայի աճով]
20. Քանի՞ անգամ կփոխվի յուղաթթվի կլանումը ջրային լուծույթից կոնցենտրացիայի ավելացման հետ՝ ըստ փորձարարական տվյալների (T 288 K).
գ 102, |
|||||
3, N/m |

21. Կալցիումի քլորիդի և ծծմբաթթվի 1%-անոց լուծույթների խառնած հավասար ծավալները (ընդունելով 1 գ/մլ հավասար խտություններ): Գրե՛ք ստացված կալցիումի սուլֆատ լուծի միցելների բանաձևերը։
[հատիկը բացասական լիցքավորված է]
22. Ի՞նչ ծավալով արծաթի նիտրատի 0,001 մոլ/լ կոնցենտրացիայով լուծույթ պետք է ավելացնել 10 մլ նատրիումի քլորիդի cNaCl 0,002 մոլ/լ լուծույթին, որպեսզի ստացվի լուծ, որի հատիկները դրական լիցքավորված են: Գրի՛ր սոլ միցելի կառուցվածքի գծապատկեր:
[հատիկը դրական լիցքավորված է, AgNO 3 լուծույթի ծավալը պետք է լինի ավելի քան 0,02 լ]
23. 0,001 մոլ/լ կոնցենտրացիայով ամոնիումի սուլֆիդի ո՞ր նվազագույն ծավալը պետք է ավելացնել 0,003 մոլ/լ խտությամբ մանգանի(II) քլորիդի 15 մլ լուծույթին՝ բացասական լիցքավորված մասնիկներով լուծ ստանալու համար:
24. Պրուսական կապույտ Fe 4 Fe CN 6 3 հատիկն էլեկտրական դաշտում շարժվում է դեպի անոդ։ Ո՞ր նյութն է ծառայում որպես կայունացուցիչ: Գրի՛ր միցելի բանաձևը.
[կայունացուցիչ - K4 Fe CN 6]
25. 100 մլ 0,03% NaCl լուծույթին (1 գ/մլ) ավելացրել են 250 մլ 0,001 Mr AgNO 3 լուծույթ: Գրե՛ք լյումինել sol-ի բանաձևը. Հետևյալ էլեկտրոլիտներից որն է այս լուծույթի կոագուլյացիա առաջացնել կոագուլյացիայի ամենացածր շեմով. KCl, Ba NO 3 2,
K2 CrO 4, MgSO 4, AlCl3?
[հատիկը բացասական լիցքավորված է, հետևաբար, կոագուլանտ իոնները կատիոններ են։ AlCl3-ի կոագուլյացիայի ամենացածր շեմը]
26. K2 SiO 3-ի և HCl-ի լուծույթների փոխազդեցությամբ ստացվել է սիլիցիումաթթվի լուծ: Գրե՛ք արևի միցելի բանաձևը և որոշե՛ք, թե էլեկտրոլիտներից որն է ավելցուկ, եթե էլեկտրական դաշտում հակաիոնները շարժվում են դեպի կաթոդ:
[ավելցուկ K2 SiO 3]

27. Ի՞նչ ծավալով 0,001 M FeCl 3 լուծույթ պետք է ավելացնել 0,03 լ 0,002 M AgNO 3 լուծույթին, որպեսզի արծաթի քլորիդի sol մասնիկներն էլեկտրական դաշտում շարժվեն դեպի անոդը: Գրի՛ր միցելեզոլի բանաձևը.
[FeCl 3-ի ծավալը պետք է լինի ավելի քան 0,02 լ]
28. Նատրիումի սուլֆատով և կալիումի քլորիդով երկաթի(III) հիդրօքսիդի հիդրոզոլի կոագուլյացիայի շեմերը համապատասխանաբար 0,32 և 20,50 մմոլ/լ են: Որոշեք կոլոիդ sol մասնիկների լիցքի նշանը: Հաշվեք այս էլեկտրոլիտների մակարդման ունակությունը և համեմատեք դրանց հարաբերակցությունը հաշվարկված Շուլց-Հարդի կանոնի հետ:
29. Էլեկտրոլիտների մակարդման ունակությունը որոշակի sol-ի նկատմամբ նվազում է հաջորդականությամբ՝ NH 4 3 PO 4 NH 4 2 SO 4 NH 4 NO3: Ո՞րն է կոլոիդային մասնիկների լիցքի նշանը: Բերե՛ք էլեկտրոլիտների օրինակներ, որոնց կոագուլյացիայի ունակությունը մոտավորապես հավասար կլինի վերը նշվածին:
[sol մասնիկները դրական լիցքավորված են, իոնների մակարդման ունակությունը գրեթե չի նվազում. PO 3 4 SO 2 4 NO 3 ]
30. Մագնեզիումի սուլֆատով լուծույթի կոագուլյացիայի շեմը փոքր է նիտրատոմբարիումից: Ինչպե՞ս են լիցքավորված արևի մասնիկները: Ի՞նչ կարող ենք ասել նույն սոլի կալիումի ֆոսֆատով հեկոագուլյացիայի մասին։
31. Ոսկու սուլֆիդային sol-ի կոագուլյացիա՝ 1,5 լ ծավալով, տեղի է ունեցել 0,2 մոլ/լ խտությամբ 570 մլ նատրիումի քլորիդի լուծույթի ավելացմամբ։ Հաշվեք նատրիումի իոնային լուծի կոագուլյացիայի շեմը:
32. Արոլ հիդրօքսիդի և երկաթի ֆոսֆատի իոնների կոագուլյացիայի շեմը 0,37 մմոլ/լ է: Ի՞նչ ծավալով նատրիումի ֆոսֆատի 5% լուծույթ (105 գ/մլ) է անհրաժեշտ 750 մլ լուծույթը կոագուլացնելու համար.
[Na 3 PO 4 լուծույթի ծավալը 0,87 մլ է]
33. 2 լիտրանոց ալյումինի հիդրօքսիդ լուծույթի թափանցիկ կոագուլյացիա է տեղի ունեցել, երբ ավելացվել է 10,6 մլ K4 Fe CN 6 0,01 մոլ/լ կոնցենտրացիայով լուծույթ: Հաշվարկել հեքասացիանոֆերատ իոններով լուծույթի կոագուլյացիայի շեմը. գրե՛ք ալյումինի հիդրօքսիդի արոլի միցելների բանաձևը.
34. Ոսկու սուլֆիդային sol-ի կալցիումի իոններով կոագուլյացիայի շեմը 0,69 մմոլ/լ է: 0,5 մոլ/լ կալցիումի քլորիդի կոնցենտրացիայով ի՞նչ ծավալի լուծույթ է անհրաժեշտ 100 մլ լուծույթը կոագուլացնելու համար.
[CaCl2 լուծույթի ծավալը 0 15 10 3 լ]
35. Որոշեք sol-ի կոլոիդային մասնիկների լիցքի նշանը, եթե էլեկտրոլիտներով դրա կոագուլյացիայի ժամանակ ստացվում են կոագուլյացիայի հետևյալ շեմերը (մմոլ/լ). c pc KNO3 300; c pc MgCl2 320; c PC Na3 PO4 0 6.
[դրական]
36. Na2 SO4 կամ MgCl2 էլեկտրոլիտներից որն ավելի մեծ մակարդման ունակություն կունենա արծաթի յոդիդի լուծույթի համար, որը ստացվում է կալիումի յոդիդի 0,01 մոլ/լ կոնցենտրացիայով լուծույթի և 0,015 մոլ/լ արծաթի նիտրատի կոնցենտրացիայով լուծույթի հավասար ծավալների խառնմամբ։ լ?
[Na2 SO4-ի մակարդման ունակությունն ավելի մեծ է]
37. 10 մլ AgI-ի բացասական լիցքավորված լուծույթը կոագուլացնելու համար 1 մոլ/լ KNO3 կոնցենտրացիայով 1,5 մլ լուծույթ կամ 0,1 մոլ/լ Ca NO3 2 կոնցենտրացիայով 0,5 մլ կամ 0,1 մոլ/լ 0,2 մլ լուծույթ։ պահանջվում է Al NO3 0,01 մոլ/լ կոնցենտրացիայով լուծույթ: Ճի՞շտ է արդյոք c p 1 z 6 կանոնը:
[կանոնը կատարվում է մոտավորապես]
38. Գրի՛ր KAuO2-ով կայունացված ոսկու լուծի միցելի բանաձևը. Ո՞ր էլեկտրոլիտը` NaCl, BaCl2, FeCl3, կունենա կոագուլյացիայի ավելի ցածր շեմ:
[մակարդման շեմն ավելի ցածր է FeCl3-ի դեպքում]
39. Ձիթապտղի յուղի խտությունը 22 Æ C ջերմաստիճանում 960 կգ մ3 է, իսկ ջրի խտությունը այս ջերմաստիճանում՝ 996 կգ մ3։ Ձիթապտղի յուղը հոսում է մածուցիկաչափով 21 րոպե 15,6 վայրկյանում, և նույն ծավալով ջուր
ջուր 22 H2 O 9 58 10 4 N s m2. |
||
[ձիթապտղի յուղի մածուցիկություն 841 3 |
10 4 N վ մ2 ] |
|
40. Կերոսինի մածուցիկությունը 20-ում |
Æ C-ն հավասար է 1 8-ի |
10 3 Pa s, և vis- |
ոսկոր ջրի նույն պայմաններում - 1 005 10 |
3 Pa s (N s m2): |
|
Որոշեք կերոսինի խտությունը, եթե հայտնի է, որ մածուցիկաչափից կերոսինի հոսքի ժամանակը 53 վ է, իսկ ջրի նույն ծավալը՝ 24 վ։ Ջրի խտությունը 998 կգ մ3 է։
[կերոսինի խտությունը 809 4 կգ մ3 է]
41. Դեպի ո՞ր էլեկտրոդը կշարժվեն սպիտակուցի մասնիկները pI 4 0) էլեկտրոֆորեզի ժամանակ ացետատային բուֆերում պատրաստված 100 մլ նատրիումի ացետատի 0,1 մոլ/լ կոնցենտրացիայով և 25 մլ քացախաթթվի 0,2 մոլ կոնցենտրացիայով լուծույթից։ /լ?
[Այս բուֆերային լուծույթում սպիտակուցը բացասական լիցքավորված է և էլեկտրոֆորեզի ժամանակ տեղափոխվում է դեպի անոդ]
42. Լուծույթը պարունակում է սպիտակուցների խառնուրդ՝ գլոբուլին (pI 7), ալբումին (pI 4 9) և կոլագեն (pI 4 0): Ի՞նչ pH արժեքով կարելի է այս սպիտակուցները բաժանել էլեկտրոֆորետիկ եղանակով:
[սպիտակուցները կարելի է բաժանել էլեկտրոֆորետիկ եղանակով՝ pH 4-9-ում]
43. Դեպի ո՞ր էլեկտրոդը կտեղափոխվեն սպիտակուցի մասնիկները էլեկտրոֆորեզի ժամանակ, եթե նրա pI-ն 4 է, իսկ pH-ը՝ 5:
[սպիտակուցի մասնիկները կշարժվեն դեպի անոդ]
44. Հեմոգլոբինը pI 6 68 դրվել է բուֆերային լուծույթի մեջ, որի կոնցենտրացիան ջրածնի իոն է 1 5 10 6 մոլ/լ: Էլեկտրաֆորեզի ժամանակ որոշել հեմոգլոբինի մոլեկուլների շարժման ուղղությունը: Հայտնի է, որ արյան կարմիր բջիջներում pH-ը 7 25 է։ Ի՞նչ լիցք ունեն հեմոգլոբինի մոլեկուլները այս pH արժեքի դեպքում։
[հեմոգլոբինի մոլեկուլները կշարժվեն դեպի կաթոդ; pH 7 25 հեմոգլոբինի մոլեկուլներն ունեն բացասական լիցք]
45. 1 կգ մ3 զանգվածային կոնցենտրացիայով սպիտակուցի ջրային լուծույթի օսմոտիկ ճնշումը ֆիզիոլոգիական ջերմաստիճանում 292,7 Պա է: Սպիտակուցի մոլեկուլային զանգվածը որոշել միջին մոլային զանգվածից (սպիտակուցի մոլեկուլը իզոդիմետրիկ է)։
[հարաբերական մոլեկուլային քաշը 87,940 է]
46. Հաշվել միջին օսմոտիկ ճնշումը 25 ցենտրոնում – 4176 կգ մ3;
պոլիստիրոլի մոլային զանգվածը, եթե Æ C-ն հավասար է 120,9 Պա, իսկ զանգվածը՝ 1 Pa m6 կգ2:
47. Արդյո՞ք ժելատինը (pI 4 7) 0 Æ C ջերմաստիճանում ացետատային բուֆերում կուռչի՞ բաղադրիչների հավասար պարունակությամբ: Ինչպե՞ս կարող եք բացահայտել ժելատինի այտուցվածության գործընթացը: Բացատրեք ձեր պատասխանը:
[ուռուցքը նվազագույն է իզոէլեկտրական կետի մոտ]
48. Երբ 200 գ կշռող կաուչուկը ուռել է, ներծծվել է 964 մլ քլորոֆորմ (1 9 գ մլ): Հաշվե՛ք ռետինի այտուցվածության աստիճանը և ստացված դոնդողի տոկոսային բաղադրությունը։
[ 915 8%; ռետինե 9 84%; քլորոֆորմ 90 16%]
49. Հաշվե՛ք պոլիմերի միջին մոլային զանգվածը, եթե նրա բնորոշ մածուցիկությունը 0 126 մ3 կգ է, հաստատուն K 5 10 5, 0 67։
50. Ինչ պոլիմերային զանգված պետք է վերցնել 0,0025 մոլ/կգ մոլալային կոնցենտրացիայով լուծույթ պատրաստելու համար,
եթե լուծիչի զանգվածը 1,5 կգ է. Մոնոմերի մոլային զանգվածը 100 գ/մոլ է։ Պոլիմերացման աստիճանը՝ 100։
51. Ի՞նչ pH արժեքով պետք է էլեկտրոֆորեզով առանձնացվեն 5 և 3 իզոէլեկտրական կետերով երկու ֆերմենտները: Ինչպե՞ս են ֆերմենտային մասնիկները լիցքավորվում pH 4,6 լուծույթներում:
իսկ 7.9?
[պետք է առանձնացնել pH 4-ում; լիցքավորումներ pH 4 6 " " և " ", pH 7 9 " " և " "]
52. Որոշե՛ք պոլիմեթիլմետակրիլաթի մոլային զանգվածը՝ օգտագործելով մածուցիկական մեթոդի հետևյալ տվյալները.
Համակենտրոնացում |
||||||
լուծույթ, կգ մ3 |
||||||
Նվազեցված մածուցիկություն |
||||||
ՆԱՄ լուծույթ |
||||||
բենզոլում |
հաստատուններ՝ Կ
105 ] |
53. Որոշ BMC-ի մոլային զանգվածը 600000 է:Որքա՞ն է լուծույթի մոլային կոնցենտրացիան, եթե նյութի զանգվածային կոնցենտրացիան 6 գ/լ է: Որքա՞ն է նման լուծույթի օսմոտիկ ճնշումը 27-ումÆ C?
54. 1 լիտր լուծույթը պարունակում է 5 գ ամիլոզա։ Նման լուծույթի օսմոտիկ ճնշումը 27-ումÆ C-ն հավասար է 0,15 մմ Hg-ի: Արվեստ. Հաշվե՛ք ամիլոզայի մոլային զանգվածը:
55. Մեմբրանի մի կողմում դրվում է 0,1 մոլ/լ PrtCl կոնցենտրացիայով սպիտակուցի լուծույթ, մյուս կողմում՝ նատրիումի քլորիդի 0,2 մոլ/լ կոնցենտրացիայով լուծույթ։ Հաշվեք քլորիդների կոնցենտրացիան մեմբրանի երկու կողմերում, երբ հավասարակշռություն է հաստատվում:
56. Ժելատինի ոսկե թիվը որոշելու համար կարմիր ոսկու 9,9 մլ լուծույթին ավելացրել են 0,1 մլ 1% ժելատինի լուծույթ։ Այնուհետև իրականացվել է սկզբնական լուծույթի 10 հաջորդական նոսրացումների շարք: Յուրաքանչյուր փորձանոթին ավելացվել է 1 մլ: 10%
նատրիումի քլորիդի լուծույթ: Առաջին հինգ փորձանոթներում փոփոխություններ չեն նկատվել, սակայն 6-10 փորձանոթներում լուծումը ձեռք է բերել կապույտ երանգ: Ո՞րն է ոսկե թիվը:
57. Որոշել օսմոտիկ ճնշումը ժելատինի ջրային լուծույթում 25 կգ մ զանգվածային կոնցենտրացիայով 293 Կ. 3 .
Ժելատինի մոլային զանգվածը 104600 է, իսկ գործակիցը
0 69 Պա մ6 |
կգ 2. |
58. Դիֆենիլֆորմամիդի լուծույթում տարբեր կոնցենտրացիաներում պոլիակրիլոնիտրիլի մոլեկուլային զանգվածը 75000 և 39100 է 293 Կ-ում, իսկ ներքին մածուցիկությունը՝ համապատասխանաբար 0,299 և 0,110: Որոշե՛ք Մարկ–Հաուվինկ հավասարման մեջ գործակիցները և K–ն։
59. Թարախային մենինգիտի ախտորոշման ժամանակ որոշվում է ողնուղեղային հեղուկի սպիտակուցների պաշտպանիչ թիվը։ Հաշվե՛ք այս թիվը, եթե հայտնի է, որ 20 մլ AgBr լուծույթի կոագուլյացիայի կանխարգելման համար 2 մլ NaNO զանգվածային բաժնով լուծույթի ազդեցության տակ. 3 Պահանջվում է 10%՝ այս լուծույթին ավելացնելով 3 մլ ողնուղեղային հեղուկ, որը պարունակում է 2 գ սպիտակուց 1 լիտրում:
60. 26 գ/լ հեմոգլոբին պարունակող լուծույթի օսմոտիկ ճնշումը իզոէկլեկտիկ վիճակում հավասար է 0,0117 գ/լ նատրիումի քլորիդ պարունակող լուծույթի օսմոտիկ ճնշմանը։ Վերցրեք լուծույթների խտությունը 1 գ/մլ, ջերմաստիճանը 25Æ C, Վան Հոֆի օրենքից շեղումը կարելի է անտեսել: Հաշվե՛ք հեմոգլոբինի մոլեկուլային (մոլային) զանգվածը։
ԴԻՄՈՒՄ
1. ՀԻՄՆԱԿԱՆ ՖԻԶԻԿԱԿԱՆ ԿՈՍՏԱՆՏՆԵՐ
Ավոգադրոյի հաստատունը, N A 6 02 1023 մոլ 1. Ունիվերսալ գազի հաստատուն, R 8 31 J մոլ
Բոլցմանի հաստատունը, k R N A 1 38 10 23 J K. Գազի նորմալ մոլային ծավալը, V 0 22 4 լ մոլ. Պլանկի հաստատուն, h 6 63 10 34 J s.
2. ՏԱՆԱՆԱԿԱՆ ԲԱԶՄԱԿԱՆՆԵՐԻ ԵՎ ՇՐՋԱՆԱԿՆԵՐԻ ՄԻԱՎՈՐՆԵՐԻ ԵՎ ՆՐԱՆՑ ԱՆՎԱՆՈՒՄՆԵՐԻ ՁԵՎԱՎՈՐՄԱՆ ԳՈՐԾՈՆՆԵՐԸ ԵՎ ՆԱԽԱՊԱՏՎՈՒԹՅՈՒՆՆԵՐԸ.
Գործոն, |
Գործոն, |
||||||
որի վրա |
որի վրա |
||||||
բազմապատկվում է |
բազմապատկվում է |
||||||
հիմնական |
հիմնական |
||||||
1012 |
|||||||
| մետր | |||||||
կիլոգրամ |
|||||||
Էլեկտրական հոսանքի ուժ |
|||||||
Թերմոդինամիկական ջերմաստիճան |
|||||||
Նյութի քանակությունը |
|||||||
Ստացված քանակություններ |
տարածություն և ժամանակ |
||||||
քառակուսի մետր |
|||||||
խորանարդ մետր |
|||||||
Արագություն |
մետր վայրկյանում |
||||||
Մեխանիկական ածանցյալներ |
և ջերմային քանակություններ |
||||||
Խտություն |
կիլոգրամ մեկ |
կգ մ3 |
|||||
խորանարդ մետր |
|||||||
Ուժ, քաշ |
|||||||
Ճնշում |
|||||||
Էներգիա, աշխատանք, ջերմության քանակ, |
|||||||
թերմոդինամիկական ներուժ |
|||||||
Էնտրոպիա |
ջոուլ մեկ կելվինի համար |
||||||
Էլեկտրական ածանցյալներ |
և մագնիսական մեծություններ |
||||||
Էլեկտրաէներգիայի քանակը |
|||||||
թերմոդինամիկական ներուժ |
|||||||
Էլեկտրական լարում |
|||||||
էլեկտրական ներուժ, |
|||||||
էլեկտրաշարժիչ ուժ |
|||||||
Էլեկտրական դիմադրություն |
|||||||
Սպիտակուցները նյութերի ամենակարևոր դասն են, որոնք կազմում են կենդանի օրգանիզմները։ Շատ սպիտակուցներ գործում են որպես կատալիզատորներ: Հեմոգլոբինը նաև թթվածին է տեղափոխում թոքերից հյուսվածքներ։
25-1. Հեմոգլոբինի մոլային զանգվածը գ/մոլ է։ Արյան կարմիր բջիջներում հեմոգլոբինի միջին պարունակությունը 15 գ / 100 մլ է: Որոշեք արյան մեջ հեմոգլոբինի (M) մոլային կոնցենտրացիան:
25-3։ Հենրիի օրենքը ասվում է հետևյալ կերպ.
լուծելիություն = կՄասնակի ճնշում ( կГ – Հենրիի հաստատուն)
Հենրիի հաստատունը թթվածնի համար 1,3 x 10 –3 մոլ/լ/ատմ է: Գնահատեք օդի հետ հավասարակշռված ջրի մեջ թթվածնի երկու մոլեկուլների միջին հեռավորությունը:
25-4։ Հեմոգլոբինի մոլեկուլը կարող է կապել մինչև չորս թթվածնի մոլեկուլ: Գնահատեք թթվածնի երկու մոլեկուլների միջև միջին հեռավորությունը թթվածնով հագեցած արյան մեջ: Արդյունքը համեմատեք 25-2 և 25-3 հարցերի պատասխանների հետ: Եզրակացություն արեք հեմոգլոբինի արդյունավետության մասին թթվածնի խտացման և այն հյուսվածքներին հասցնելու առումով, որտեղ թթվածնի մասնակի ճնշումը ցածր է:
25-6։ Քանի՞ տարբեր ամինաթթուներ է պարունակում հեմոգլոբինի մոլեկուլը:
25-7։ Տրիպսինը հիդրոլիզացնում է լիզինի և արգինինի կարբոքսիլ խմբերից առաջացած պեպտիդային կապերը։ Օրինակ, ստորև բերված պեպտիդը
տրիփսինի ազդեցությունից հետո այն բաժանվում է հետևյալ պեպտիդների.
Հեմոգլոբինը ենթարկվել է դիսուլֆիդային կապերի կրճատման և ալկիլացման, այնուհետև տրիփսինի ազդեցության տակ լրիվ հիդրոլիզացվել է։ Քանի՞ ամինաթթուների մնացորդներից (միջինում) կազմված կլինեն հիդրոլիզի արտադրանքը:
Հեմոգլոբինի մոլային զանգված
Հեմոգլոբ i n (Hb) (ից հեմո. եւ լատ. globus - գնդակ), կարմիր երկաթ պարունակող պիգմենտ մարդկանց, ողնաշարավորների և որոշ անողնաշարավորների արյան մեջ. մարմնում այն կատարում է թթվածինը (O 2) շնչառական օրգաններից հյուսվածքներ տեղափոխելու գործառույթը. Նաև կարևոր դեր է խաղում ածխաթթու գազի հյուսվածքներից շնչառական օրգաններ տեղափոխելու գործում: Անողնաշարավորների մեծ մասում գլիցերինն ազատորեն լուծվում է արյան մեջ. ողնաշարավորների և որոշ անողնաշարավորների մոտ այն հանդիպում է արյան կարմիր բջիջներում՝ էրիթրոցիտներում, որոնք կազմում են դրանց չոր մնացորդի մինչև 94%-ը: Էրիտրոցիտներում ընդգրկված գազի մոլային զանգվածը մոտ է, պլազմայում լուծված՝ մինչև. Ըստ քիմիական բնույթի՝ Գ.-ն բարդ սպիտակուց է՝ քրոմպրոտեին , որը բաղկացած է սպիտակուցի գլոբինից և երկաթի պորֆիրինից՝ հեմից։ Բարձրակարգ կենդանիների և մարդկանց մոտ արյունը բաղկացած է 4 մոնոմերային ենթամիավորներից՝ մոտ 17000 մոլային զանգվածով; երկու մոնոմեր յուրաքանչյուրը պարունակում է 141 ամինաթթու մնացորդ ( ա-շղթա), մյուս երկուսը՝ 146-ական մնացորդ ( բ- շղթաներ):
Այս պոլիպեպտիդների տարածական կառուցվածքները հիմնականում նման են: Նրանք ձևավորում են բնորոշ «ջրոֆոբ գրպաններ», որոնցում տեղակայված են հեմի մոլեկուլները (յուրաքանչյուր ենթամիավորի համար մեկը): Հեմում ներառված երկաթի ատոմի 6 կոորդինացիոն կապերից 4-ն ուղղված են պիրոլի օղակների ազոտին. 5-րդը կապված է հիստիդինի իմիդազոլ օղակի ազոտին, որը պատկանում է պոլիպեպտիդներին և գտնվում է 87-րդ տեղում։ ա-շղթա և 92-րդ տեղում բ- շղթաներ; 6-րդ կապն ուղղված է ջրի մոլեկուլին կամ այլ խմբի (լիգանդներին), ներառյալ թթվածինը։ Ստորաբաժանումները թույլ կապված են միմյանց հետ ջրածնի, աղի և այլ ոչ կովալենտային կապերի միջոցով և հեշտությամբ տարանջատվում են ամիդների և աղի ավելացված կոնցենտրացիաների ազդեցության տակ՝ հիմնականում սիմետրիկ դիմերների ձևավորմամբ ( ա բ) և մասամբ ա-Եվ բ- մոնոմերներ. Գազի մոլեկուլի տարածական կառուցվածքն ուսումնասիրվել է ռենտգենյան դիֆրակցիոն անալիզով (M. Peruts, 1959):
Ամինաթթուների հաջորդականությունը ա-Եվ բ-Լիովին պարզաբանված են մի շարք բարձրակարգ կենդանիների և մարդկանց Գ.-ի շղթաները: Հեմի մոլեկուլում, որը հավաքվում է տետրամերի մեջ, բոլոր 4 հեմի մնացորդները գտնվում են մակերեսի վրա, և O 2-ի հետ ռեակցիաները հեշտությամբ հասանելի են: O 2-ի ավելացումն ապահովվում է հեմում Fe 2+ ատոմի պարունակությամբ։ Այս ռեակցիան շրջելի է և կախված է O 2-ի մասնակի ճնշումից (լարվածությունից): Թոքերի մազանոթներում, որտեղ O 2 լարումը մոտ 100 է մմ Hg. Արվեստ., Գ.-ը միանում է O 2-ի հետ (թթվածնացման պրոցես)՝ վերածվելով թթվածնով Գ.- թթվածնած հեմոգլոբինի։ Հյուսվածքային մազանոթներում, որտեղ O2 լարվածությունը զգալիորեն ցածր է (մոտ. 40 մմ Hg. Արվեստ.), օքսիհեմոգլոբինը տարանջատվում է G. և O 2-ի; վերջինս մտնում է օրգանների և հյուսվածքների բջիջներ, որտեղ O 2-ի մասնակի ճնշումն էլ ավելի ցածր է (5-20 մմ Hg. սմ.); բջիջների խորքում այն իջնում է գրեթե զրոյի: O 2-ի ավելացումը հեմոգլոբինին և օքսիհեմոգլոբինի տարանջատումը հեմոգլոբինի և O 2-ի ուղեկցվում է հեմոգլոբինի մոլեկուլի կոնֆորմացիոն (տարածական) փոփոխություններով, ինչպես նաև դրա շրջելի տարրալուծմամբ դիմերների և մոնոմերների, որին հաջորդում է ագրեգացումը տետրամերների:
Գազի հատկությունները փոխվում են O 2-ի հետ արձագանքելիս և այլ հատկություններ. Սպեկտրի տեսանելի մասում կլանման գոտիները բնորոշ են. Գ.-ն ունի մեկ առավելագույնը (554-ում. մմկ), թթվածնային գազն ունի երկու առավելագույնը 578 և 540 մմկ. G.-ն ունակ է ուղղակիորեն միացնել CO 2-ը (CO 2-ի ռեակցիայի արդյունքում NH 2 -գլոբինի խմբերի հետ); Այս դեպքում ձևավորվում է կարբհեմոգլոբին՝ անկայուն միացություն, որը հեշտությամբ քայքայվում է թոքերի մազանոթներում՝ դառնալով հեմոգլոբին և CO 2:
Մարդու արյան մեջ Գ.-ի քանակը միջինում 13-16 է G%(կամ 78%-96% ըստ Սալիի); կանանց մոտ Գ.-ն փոքր-ինչ պակաս է, քան տղամարդկանց մոտ։ Գ–ի հատկությունները փոփոխվում են օնտոգենեզի ընթացքում։ Ուստի նրանք տարբերակում են սաղմնային Գ., պտղի Գ. (պտուղ)՝ HbF, մեծահասակ Գ.՝ HbA: Պտղի բջիջների թթվածնային կապն ավելի բարձր է, քան մեծահասակների մոտ, ինչը զգալի ֆիզիոլոգիական նշանակություն ունի և ապահովում է պտղի մարմնի ավելի մեծ դիմադրություն O 2-ի անբավարարությանը: Արյան մեջ Գ.-ի քանակի որոշումը կարևոր է նորմալ պայմաններում արյան շնչառական ֆունկցիան բնութագրելու և բազմաթիվ հիվանդությունների, հատկապես արյան հիվանդությունների դեպքում: Գ–ի քանակը որոշվում է հատուկ սարքերով՝ հեմոմետրերով։
Որոշ հիվանդությունների, ինչպես նաև արյան բնածին անոմալիաների համար (տես. Հեմոգլոբինոպաթիաներ ) էրիթրոցիտներում հայտնվում են աննորմալ (ախտաբանական) արյան բջիջներ, որոնք նորմալներից տարբերվում են ամինաթթվի մնացորդի փոխարինմամբ ( - կամ բ- շղթաներ. Հայտնաբերվել են աննորմալ Գ.-ի ավելի քան 50 սորտեր, այսպիսով, մանգաղ բջջային անեմիայում հայտնաբերվել է Գ. բ- շղթաները, որոնց գլուտամինաթթուն, որը գտնվում է N-վերջնակետից 6-րդ տեղում, փոխարինվում է վալինով: Արյան կարմիր բջիջների անոմալիաները, որոնք կապված են հեմոգլոբին F կամ H պարունակության հետ, հիմքում ընկած են թալասեմիա , մետեմոգլոբինեմիա . Որոշ աննորմալ աղեստամոքսային տրակտների շնչառական ֆունկցիան խիստ խաթարված է, ինչը հանգեցնում է տարբեր պաթոլոգիական պայմանների ( անեմիա և այլն): Գ.-ի հատկությունները կարող են փոխվել, երբ մարմինը թունավորվում է, օրինակ՝ ածխածնի օքսիդով, որն առաջացնում է ձևավորումը. կարբոքսիհեմոգլոբին , կամ թույներ, որոնք Fe 2+ հեմը վերածում են Fe 3+՝ մետեմոգլոբինի առաջացմամբ։ Այս G. ածանցյալները ունակ չեն թթվածին կրելու։ G. տարբեր կենդանիներ ունեն տեսակների յուրահատկություն՝ պայմանավորված մոլեկուլի սպիտակուցային մասի յուրահատուկ կառուցվածքով։ Արյան կարմիր բջիջների քայքայման ժամանակ ազատված Գ լեղու պիգմենտներ.
Մկանային հյուսվածքը պարունակում է մկանային G. - միոգլոբին , մոլային զանգվածով, բաղադրությամբ և հատկություններով մոտ են Գ–ի ենթամիավորներին (մոնոմերներ)։ Որոշ բույսերում հայտնաբերվել են Գ–ի անալոգներ (օրինակ. լեգեմոգլոբին հայտնաբերված լոբազգիների հանգույցներում):
Լիտ.: Korzhuev P. A., Հեմոգլոբին, Մ., 1964; Գաուրովից Ֆ., Քիմիա և սպիտակուցների գործառույթներ, տրանս. անգլերենից, 2-րդ հրատ., Մ., 1965, էջ. 303-23; Ինգրամ Վ., Մակրոմոլեկուլների կենսասինթեզ, տրանս. անգլերենից, Մ., 1966, էջ. 188-97 թթ. Rapoport S. M., Բժշկական կենսաքիմիա, թարգման. գերմաներենից, Մ., 1966; Perutz M., Hemoglobin molecule, հավաքածուում՝ Molecules and Cells, M., 1966; Ցուկերքանդլ Է. Հեմոգլոբինի էվոլյուցիան, նույն տեղում; Fanelli A. R., Antonini E., Caputo A., Hemoglobin and myoglobin, «Advances in Protein Chemistry», 1964, v. 19, էջ. 73-222; Antonini E., Brunori M., Hemoglobin, “Annual Review of Biochemistry”, 1970, v. 39, էջ. 977-1042 թթ.
G. V. Andreenko, S. E. Severin.
Հաշվե՛ք հեմոգլոբինի մեկ մոլեկուլի զանգվածը՝ գրամներով և ատոմային զանգվածի միավորներով։
Հաշվե՛ք հեմոգլոբինի մեկ մոլեկուլի զանգվածը (մոլեկուլային բանաձև C 2954 H 4516 N 780 O 806 S 12 Fe 4).
ա) գրամներով; բ) ատոմային զանգվածի միավորներով.
Եկեք գրենք խնդրի համառոտ շարադրանքը և դրա լուծման համար անհրաժեշտ լրացուցիչ տվյալները:
ա) Հեմոգլոբինի մոլեկուլի զանգվածը հաշվարկելու համար անհրաժեշտ է իմանալ նրա մոլային զանգվածը.
M (հեմոգլոբին) = 2954·12 + 4516·1 + 780·14 + + 806·16 + 12·32 + 4·56 =( գ/մոլ)
Հետագա հիմնավորումը կարող է իրականացվել երկու եղանակով.
Մեթոդ 1. նյութի քանակով:
Նյութի քանակությունը հարմար ունիվերսալ մեծություն է, որը թույլ է տալիս կապել ատոմների կամ մոլեկուլների քանակը, նյութի զանգվածը և ծավալը։
որտեղ m-ը զանգված է, M-ը մոլային զանգված է, N-ը ատոմների կամ մոլեկուլների թիվն է, N A = 6,02 10 23 մոլ – 1- Ավոգադրոյի հաստատունը:
Այս բանաձևերը համադրելով՝ մենք կարող ենք զանգվածը արտահայտել մոլեկուլների քանակով.
Փոխարինելով ստացված բանաձևով N = 1, M = գ/մոլ, N A = 6,02·10 23 մոլ – 1, գտնում ենք
Մեթոդ 2. համամասնությունների օգտագործում:
6,02 10 23 հեմոգլոբինի մոլեկուլների զանգվածը կազմում է Գ;
իսկ հեմոգլոբինի 1 մոլեկուլի զանգվածը մ է Գ.
բ) Մոլեկուլի բացարձակ զանգվածը հավասար է հարաբերական մոլեկուլային զանգվածին բազմապատկած 1 ա. ուտել.
Հարաբերական մոլեկուլային զանգվածը թվայինորեն հավասար է մոլային զանգվածին։
Պատասխան.Հեմոգլոբինի մեկ մոլեկուլի զանգվածը հետևյալն է.
ա) 1,07·10 –19 Գ; բ) ա. ուտել.
Նախագիծ ուսանողներից ուսանողների համար: Մենք 50%-ով պարզեցնում ենք բուհ անցնելը։ 40%-ով ժամանակ ենք խնայում սովորելու վրա։ Բարձրացրեք ուրախությունը 200%-ով:
Քիմիկոս ձեռնարկ 21
Քիմիա և քիմիական տեխնոլոգիա
Հեմոգլոբինի մոլեկուլային քաշը
Երկաթը գործում է որպես էլեկտրոնի առաջնային կրիչ կենսաբանական օքսիդացում-վերականգնման ռեակցիաներում: Երկաթի իոնները՝ և՛ Fe+, և՛ Fe+, առկա են մարդու մարմնում և, հանդես գալով որպես էլեկտրոնների կրիչներ, անընդհատ փոխվում են մի օքսիդացման վիճակից մյուսը։ Սա կարելի է պատկերացնել՝ օգտագործելով ցիտոքրոմների օրինակը: Երկաթի իոնները նաև ծառայում են մոլեկուլային թթվածին տեղափոխելու և պահելու համար՝ ֆունկցիա, որն անհրաժեշտ է բոլոր ողնաշարավորների կյանքի համար: Այս համակարգում աշխատում է միայն Re(P): Նյութափոխանակության գործընթացների թթվածնի կարիքները բավարարելու համար կենդանիների մեծամասնության մեջ հեղուկ է շրջանառվում ամբողջ մարմնով և թթվածին է տեղափոխում՝ այն արտաքին աղբյուրից ներծծելով հյուսվածքների միտոքոնդրիա: Այստեղ անհրաժեշտ է, որ շնչառական շղթան միջնորդի օքսիդատիվ ֆոսֆորիլացմանը և ATP-ի արտադրությանը: Այնուամենայնիվ, ջրի մեջ թթվածնի լուծելիությունը շատ ցածր է կենդանի էակների շնչառությունը ապահովելու համար: Հետեւաբար, արյունը սովորաբար պարունակում է սպիտակուցներ, որոնք շրջելիորեն կապում են թթվածինը: Այս սպիտակուցային մոլեկուլները հեշտացնում են թթվածնի ներթափանցումը մկաններ (հյուսվածքներ) և կարող են նաև ծառայել որպես թթվածնի պահեստ:
Մյուս կողմից, TMV-ի մոլեկուլային քաշը համարվում էր մոտ 40 միլիոն, և սկզբում թվում էր, որ TMV-ի կառուցվածքը հասկանալն անչափ ավելի դժվար կլինի, քան միոգլոբինի և հեմոգլոբինի շատ ավելի փոքր մոլեկուլների կառուցվածքը, որը Ջոն Քենդրյուն էր: և Մաքս Պերուցը երկար տարիներ պայքարել է, բայց երբեք չի ստացել կենսաբանին հետաքրքրող որևէ արդյունք:
Հեմոգլոբին
Հեմոգլոբին (Hb) (ից հեմո. եւ լատ. globus - գնդակ), մարդկանց, ողնաշարավորների և որոշ անողնաշարավորների արյան կարմիր պիգմենտ, որը պարունակում է երկաթ
Հեմոգլոբինի և դրա միացությունների կլանման սպեկտրները. 1 - հեմոգլոբին; 2 - օքսիհեմոգլոբին; 3 - կարբոքսիհեմոգլոբին; 4 - մետեմոգլոբին. B, C, D, E, F, G - արեգակնային սպեկտրի հիմնական Fraunhofer գծերը, ալիքի երկարությունները նշված են թվերով:
Մարդու օքսիհեմոգլոբինի տարանջատման կորը.
Հեմոգլոբին
Կախված սպիտակուցի մոլեկուլի ձևից՝ առանձնանում են ֆիբրիլային և գնդաձև սպիտակուցները, հատուկ խումբը բաղկացած է բարդ սպիտակուցներից, որոնք, բացի ամինաթթուներից, ներառում են ածխաջրեր, նուկլեինաթթուներ և այլն։ գլոբին և երկաթի պորֆիրին - հեմ: Բարձրակարգ կենդանիների և մարդկանց մոտ արյունը բաղկացած է 4 մոնոմերային ենթամիավորներից՝ մոտ 17000 մոլային զանգվածով; երկու մոնոմերները պարունակում են 141 ամինաթթուների մնացորդ (?-շղթա), մյուս երկուսը՝ 146 մնացորդ (?-շղթա):
Այս պոլիպեպտիդների տարածական կառուցվածքները հիմնականում նման են: Նրանք ձևավորում են բնորոշ «ջրոֆոբ գրպաններ», որոնցում տեղակայված են հեմի մոլեկուլները (յուրաքանչյուր ենթամիավորի համար մեկը): Հեմում ներառված երկաթի ատոմի 6 կոորդինացիոն կապերից 4-ն ուղղված են պիրոլի օղակների ազոտին. 5-րդը կապված է հիստիդինի իմիդազոլ օղակի ազոտին, որը պատկանում է պոլիպեպտիդներին և գտնվում է α-շղթայում 87-րդ և β-շղթայի 92-րդ տեղում; 6-րդ կապն ուղղված է ջրի մոլեկուլին կամ այլ խմբերին (լիգանդներին), ներառյալ թթվածինը։ Ստորաբաժանումները թույլ կապված են միմյանց հետ ջրածնի, աղի և այլ ոչ կովալենտային կապերով և հեշտությամբ տարանջատվում են ամիդների և աղի ավելացված կոնցենտրացիաների ազդեցության տակ՝ ձևավորելով հիմնականում սիմետրիկ դիմերներ (??) և մասամբ?- և?-մոնոմերներ: Հեմոգլոբինի մոլեկուլի տարածական կառուցվածքը 1959 թվականին ռենտգենյան դիֆրակցիոն անալիզի միջոցով ուսումնասիրվել է անգլիացի կենսաքիմիկոս Մաքս Ֆերդինանդ Պերուցի կողմից։
Մի շարք բարձրակարգ կենդանիների և մարդկանց մոտ ամինաթթուների դասավորվածության հաջորդականությունը հեմոգլոբինի α- և β-շղթաներում լիովին պարզաբանված է: Հեմի մոլեկուլում, որը հավաքվում է տետրամերի մեջ, բոլոր 4 հեմի մնացորդները գտնվում են մակերեսի վրա, և O 2-ի հետ ռեակցիաները հեշտությամբ հասանելի են: O 2-ի ավելացումն ապահովվում է հեմում Fe 2+ ատոմի պարունակությամբ։ Այս ռեակցիան շրջելի է և կախված է O 2-ի մասնակի ճնշումից (լարվածությունից): Մազանոթներում Մազանոթները ամենափոքր անոթներն են, որոնք թափանցում են օրգաններ և հյուսվածքներ։ Նրանք միացնում են զարկերակները վենուլների հետ (ամենափոքր երակները) և փակում արյան շրջանառությունը; դրանց պատերի միջոցով տեղի է ունենում նյութերի փոխանակում արյան և հյուսվածքների (արյան մազանոթների) միջև։ Լիմֆատիկ մազանոթները ձևավորում են լիմֆատիկ անոթներ, նպաստում են հյուսվածքներից հեղուկի արտահոսքին և օրգանիզմից հեռացնում օտար մասնիկները և պաթոգեն բակտերիաները։ թոքեր, որտեղ O 2 լարվածությունը մոտ 100 մմ Hg է: Արտ., Գ. միանում է O 2-ի հետ (թթվածնացման պրոցես Թթվածնացում – հագեցվածություն թթվածնով.) վերածվելով թթվածնով Գ–ի` թթվածինացված հեմոգլոբինի։ Հյուսվածքային մազանոթներում, որտեղ O 2 լարվածությունը շատ ավելի ցածր է (մոտ 40 մմ Hg), օքսիհեմոգլոբինը տարանջատվում է հեմոգլոբինի և թթվածնի O 2-ի; վերջինս մտնում է օրգանների և հյուսվածքների բջիջներ, որտեղ O 2-ի մասնակի ճնշումը նույնիսկ ավելի ցածր է (5-20 մմ Hg); բջիջների խորքում այն իջնում է գրեթե զրոյի: O 2-ի ավելացումը հեմոգլոբինին և օքսիհեմոգլոբինի տարանջատումը հեմոգլոբինի և O 2-ի ուղեկցվում է հեմոգլոբինի մոլեկուլի կոնֆորմացիոն (տարածական) փոփոխություններով, ինչպես նաև դրա շրջելի տարրալուծմամբ դիմերների և մոնոմերների, որին հաջորդում է ագրեգացումը տետրամերների:
Հեմոգլոբինի այլ հատկությունները նույնպես փոխվում են O 2 թթվածնի հետ արձագանքելիս. թթվածնով հագեցած հեմոգլոբինը 70 անգամ ավելի ուժեղ թթու է, քան հեմոգլոբինը: Սա մեծ դեր է խաղում հյուսվածքներում կապվելու և թոքերում CO 2-ի արտազատման գործում: Հատկանշական կլանման գոտիները գտնվում են սպեկտրի տեսանելի մասում. գեոգլոբինը ունի մեկ առավելագույնը (554 մմկկ), իսկ թթվածնով պարունակվող գազը՝ երկու առավելագույնը՝ 578 և 540 մմ: G.-ն ունակ է ուղղակիորեն ավելացնել ածխածնի երկօքսիդ (ածխածնի երկօքսիդ) CO 2 (CO 2-ի ռեակցիայի արդյունքում NH2-գլոբինի խմբերի հետ); Այս դեպքում ձևավորվում է կարբհեմոգլոբին՝ անկայուն միացություն, որը հեշտությամբ քայքայվում է թոքերի մազանոթներում՝ դառնալով հեմոգլոբին և CO 2:
Բրինձ. 1. Հեմոգլոբինի և դրա միացությունների կլանման սպեկտրները՝ 1 - հեմոգլոբին; 2 - օքսիհեմոգլոբին; 3 - կարբոքսիհեմոգլոբին; 4 - մետեմոգլոբին. B, C, D, E, F, G - արեգակնային սպեկտրի հիմնական Fraunhofer գծերը, ալիքի երկարությունները նշված են թվերով:
Մարդու արյան մեջ հեմոգլոբինի քանակը միջինում կազմում է % (կամ 78% - 96% ըստ Սալիի); կանանց մոտ Գ.-ն փոքր-ինչ պակաս է, քան տղամարդկանց մոտ։ Գ–ի հատկությունները փոփոխվում են օնտոգենեզի ընթացքում։ Ուստի նրանք տարբերակում են սաղմնային Գ., պտղի Գ. (պտուղ)՝ HbF, մեծահասակ Գ.՝ HbA: Պտղի բջիջներում թթվածնի նկատմամբ մերձությունը ավելի բարձր է, քան մեծահասակների մոտ, որն ունի զգալի ֆիզիոլոգիական ֆիզիոլոգիական, ֆիզիոլոգիական վիճակ, այսինքն. մեկը, որտեղ չկան շեղումներ համակարգերի և օրգանների բնականոն գործունեությունից: նշանակությունը և ապահովում է պտղի մարմնի ավելի մեծ դիմադրություն O 2-ի անբավարարությանը: Արյան մեջ Գ.-ի քանակի որոշումը կարևոր է նորմալ պայմաններում արյան շնչառական ֆունկցիան բնութագրելու և բազմաթիվ հիվանդությունների, հատկապես արյան հիվանդությունների դեպքում: Գ–ի քանակը որոշվում է հատուկ սարքերով՝ հեմոմետրերով։
Որոշ հիվանդությունների, ինչպես նաև բնածին անոմալիաների դեպքում Անոմալիան մարմնի կառուցվածքային կամ ֆունկցիոնալ անոմալիա է, որը պայմանավորված է սաղմի զարգացման խանգարումներով: Կտրուկ արտահայտված անոմալիաները կոչվում են արատներ կամ դեֆորմացիաներ։ արյան կարմիր բջիջներում հայտնվում են աննորմալ (պաթոլոգիական) Գ., որոնք նորմալներից տարբերվում են ամինաթթվի մնացորդի փոխարինմամբ (- կամ?-շղթաներում: Հայտնաբերվել է աննորմալ Գ.-ի ավելի քան 50 տեսակ: Այսպիսով, մանգաղ բջջային անեմիա, որի β-շղթաներում հայտնաբերվել է Գ. հունարեն th?lassa - ծով և h?ima - արյուն) միջերկրածովյան հիվանդություն է, ժառանգական հեմոլիտիկ անեմիա, որն առաջին անգամ հայտնաբերվել է (1925 թ.) Միջերկրական ծովի շրջանների բնակիչների մոտ: Պատճառված է հեմոգլոբինի սինթեզի խանգարումներով, մետեմոգլոբինեմիա: Շնչառական ֆունկցիա որոշ աննորմալ հեմոգլոբիններ կտրուկ խանգարվում են, ինչը հանգեցնում է տարբեր պաթոլոգիական պայմանների (սակավարյունություն և այլն): Հեմոգլոբինի հատկությունները կարող են փոխվել, երբ մարմինը թունավորվում է, օրինակ՝ ածխածնի երկօքսիդը, որն առաջացնում է կարբոքսիհեմոգլոբինի ձևավորում, կամ թույներ, որոնք փոխակերպում են Fe. 2+ հեմը Fe 3+-ի մեջ մետեմոգլոբինի ձևավորմամբ: Այս G. ածանցյալները ունակ չեն թթվածին կրելու։ G. տարբեր կենդանիներ ունեն տեսակների յուրահատկություն՝ պայմանավորված մոլեկուլի սպիտակուցային մասի յուրահատուկ կառուցվածքով։ Լեղու պիգմենտների առաջացման աղբյուրն է կարմիր արյան բջիջների քայքայման ժամանակ թողարկված Գ.
Մկանային հյուսվածքը պարունակում է մկանային հեմոգլոբին - միոգլոբին Միոգլոբինը գնդաձեւ սպիտակուց է, որը մկաններում թթվածին է կուտակում: , մոլային զանգվածով, բաղադրությամբ և հատկություններով մոտ են Գ–ի ենթամիավորներին (մոնոմերներ)։ Գ–ի անալոգները հայտնաբերվել են որոշ բույսերում (օրինակ՝ լեգեմոգլոբինը հանդիպում է լոբազգիների հանգույցներում)։
Բրինձ. 2. Մարդու օքսիհեմոգլոբինի դիսոցման կորը:
Հեմոգլոբինի մասին ավելի մանրամասն կարելի է ուսումնասիրել գրականության մեջ՝ Korzhuev P. A., Hemoglobin, M., 1964; Գաուրովից Ֆ., Քիմիա և սպիտակուցների գործառույթներ, տրանս. անգլերենից, 2-րդ հրատ., Մ., 1965, էջ. 303 - 23; Ինգրամ Վ., Մակրոմոլեկուլների կենսասինթեզ, տրանս. անգլերենից, Մ., 1966, էջ. 188 - 97; Rapoport S. M., Բժշկական կենսաքիմիա, թարգման. գերմաներենից, Մ., 1966; Perutz M., Hemoglobin molecule, հավաքածուում՝ Molecules and Cells, M., 1966; Ցուկերքանդլ Է. Էվոլյուցիան Էվոլյուցիան (կենսաբանության մեջ) կենդանի բնության անշրջելի պատմական զարգացումն է։ Որոշվում է օրգանիզմների փոփոխականությամբ, ժառանգականությամբ և բնական ընտրությամբ։ Այն ուղեկցվում է գոյության պայմաններին նրանց հարմարեցմամբ, տեսակների ձևավորման և անհետացման, կենսաերկրոցենոզների և ամբողջ կենսոլորտի փոխակերպմամբ։ հեմոգլոբին, նույն տեղում; Fanelli A. R., Antonini E., Caputo A., Hemoglobin and myoglobin, «Advances in Protein Chemistry», 1964, v. 19, էջ. 73 - 222; Antonini E., Brunori M., Hemoglobin, “Annual Review of Biochemistry”, 1970, v. 39, էջ. 977 - 1042. (G. V. Andreenko, S. E. Severin)
Գտեք այլ հետաքրքիր բան.
- Տեղեկատվությունն օգտագործելուց առաջ խորհրդակցեք ձեր բժշկի հետ: Մարկ Տվեն. Զգույշ եղեք առողջության մասին գրքեր կարդալիս: Դուք կարող եք մահանալ տառասխալից:
Մեկնաբանություններ հոդվածի վերաբերյալ
Արյան բաղադրությունը բարելավելու և հեմոգլոբինը բարձրացնելու համար պատրաստեք այս շիլան։
1 բաժակ հնդկաձավարն ու 1 բաժակ կեֆիրը խառնում ենք ու թողնում 12 ժամ։ Ավելացնել մեղր ըստ ճաշակի:
Այս շիլան կերեք նախաճաշին կամ երեկոյան։ Համեմատած այլ ձավարեղենի՝ հնդկաձավարը քիչ ածխաջրեր է պարունակում, ուստի այն շատ օգտակար է ավելորդ քաշ ունեցողների և դիաբետով հիվանդների համար։
Հեմոգլոբինը բարձրացնելու համար 300 գ հում գազարն ու ճակնդեղը քերել խոշոր քերիչով, ավելացնել 300 գ մեղր։ Խառնել ու սառեցնել։
Վերցրեք 1 ճ.գ. Օրական 1 անգամ, առավոտյան դատարկ ստամոքսին 30 րոպե։ ուտելուց առաջ.
Մեկ շաբաթից հեմոգլոբինը կբարձրանա նորմալ (գուցե կրկնակի):
Ինչպես բարձրացնել հեմոգլոբինը առանց մսի
Հեմոգլոբինի մակարդակը կարող է բարձրացվել նաև հետևյալ ապրանքներով.
թեփ, ցորենի շիլա, ծիրան, չորացրած ծիրան, մուգ շոկոլադ, կանաչ խնձոր, հացահատիկային հաց, կարմիր խաղող, ճակնդեղ, լոբազգիներ, նուշ, նուռ, սալորաչիր, սալոր, չամիչ, ոլոռ, լոլիկի հյութ, բրյուսելյան կաղամբ, բրոկկոլի, գետնանուշ կարագ, վարսակի ալյուր, արքայախնձոր (թարմ և պահածոյացված):
Այս բոլոր մթերքները հարուստ են երկաթով, որը բարձրացնում է հեմոգլոբինը։ Իսկ թվարկված ապրանքներից շատերը երկաթի պարունակությամբ համեմատելի են մսի հետ։
Հեմոգլոբինի բարձրացման հատուկ բաղադրատոմսեր
Հետևյալ բաղադրատոմսերից ընտրեք ձեզ ամենահամապատասխանը և փորձեք այն շարունակաբար օգտագործել՝ որպես «վիտամինային հավելում» օրգանիզմի համար։
1)Մի բաժակ ընկույզն ու մի բաժակ հում հնդկաձավարը մանրացրեք, մի բաժակ մեղր ավելացրեք, ամեն ինչ խառնեք, ամեն օր մեկ ճաշի գդալ կերեք։
2) Ընկույզ, չորացրած ծիրան, մեղր, չամիչ - բոլորը 1:1 հարաբերակցությամբ - մանրացնել և մանրակրկիտ խառնել, ուտել օրական 1-3 ճաշի գդալ (լավագույն բաղադրատոմսերից մեկը ոչ միայն հեմոգլոբինը բարձրացնելու, այլև օրգանիզմին ապահովելու համար: անհրաժեշտ վիտամիններ):
3) 1 բաժակ սալորաչիր, ծիրանի չիր, ընկույզ, չամիչ մանրացնել, ավելացնել մեղր, ավելացնել կեղևով 1-2 կիտրոն (կիտրոնի փոխարեն կարելի է ավելացնել ալոեի հյութ), ուտել օրական 1-3 ճաշի գդալ։
4) 100 մլ ճակնդեղի թարմ քամած հյութ, 100 մլ գազարի հյութ, խառնել և խմել (բառացիորեն 2 օրում բարձրացնում է հեմոգլոբինը)։
5) 1/2 բաժակ խնձորի հյութ, 1/4 բաժակ ճակնդեղի հյութ և 1/4 բաժակ գազարի հյութ, խառնել և խմել օրը 1-2 անգամ։
6) 1/2 բաժակ թարմ քամած խնձորի հյութ, 1/2 բաժակ տնական լոռամրգի հյութ, 1 ճաշի գդալ թարմ քամած ճակնդեղի հյութ, խառնել և խմել։
7) Հում հնդկաձավար 1/2 բաժակ, լվանալ, լցնել 1 բաժակ կեֆիր և թողնել ամբողջ գիշեր, առավոտյան շիլան պատրաստ է, կարող եք ուտել։
8) 1/2 բաժակ լավ որակի կարմիր չոր գինի, գոլորշիացված ջրային բաղնիքում 5-7 րոպե; 1/4 բաժակ եփած եղինջ, 1 ճաշի գդալ հալած կարագ, խմել տաք.
Հեմոգլոբինի մոլային զանգված
ՀԵՄՈԳԼՈԲԻՆ, Hb ( հեմոգլոբին; հունարեն haima արյուն + լատ. globus ball), հեմոպրոտեին է, բարդ սպիտակուց, որը պատկանում է հեմ պարունակող քրոմպրոտեիններին. իրականացնում է թթվածնի փոխանցումը թոքերից հյուսվածքներ և մասնակցում է ածխաթթու գազի տեղափոխմանը հյուսվածքներից դեպի շնչառական օրգաններ։ Գ.-ն հանդիպում է բոլոր ողնաշարավորների և որոշ անողնաշարավոր կենդանիների էրիթրոցիտներում (որդեր, փափկամարմիններ, հոդվածոտանիներ, էխինոդերմներ), ինչպես նաև որոշ հատիկաընդեղենների արմատային հանգույցներում։ Մոլ. Մարդու կարմիր արյան բջիջների քաշը (զանգվածը) հավասար է. Մեկ էրիթրոցիտը պարունակում է մոտավորապես. G. G.-ի 400 միլիոն մոլեկուլները շատ լուծելի են ջրում, անլուծելի են սպիրտի, քլորոֆորմի և եթերի մեջ և լավ բյուրեղանում են (G. բյուրեղների ձևը տարբեր կենդանիներից տարբերվում է):
Գ.-ի բաղադրությունը ներառում է պարզ սպիտակուց՝ գլոբին և երկաթ պարունակող պրոթեզային (ոչ սպիտակուցային) խումբ՝ հեմ (մոլեկուլի համապատասխանաբար 96 և 4% կշռով)։ 2.0-ից ցածր pH-ի դեպքում հեմի մոլեկուլը բաժանվում է հեմի և գլոբինի:
Հեմը (C 34 H 32 O 4 N 4) երկաթի պրոտոպորֆիրին է - պրոտոպորֆիրին IX-ի բարդ միացություն երկվալենտ երկաթով: Երկաթը գտնվում է պրոտոպորֆիրինի միջուկի կենտրոնում և կապված է պիրոլի միջուկների չորս ազոտի ատոմների հետ (նկ. 1)՝ երկու կոորդինացիոն կապ և երկու ջրածնի փոխարինող կապ։
Քանի որ երկաթի կոորդինացիոն թիվը 6 է, երկու վալենտներ մնում են չօգտագործված, դրանցից մեկը իրացվում է, երբ հեմը կապվում է գլոբինի հետ, իսկ երկրորդը միանում է թթվածին կամ այլ լիգանդներ՝ CO, F+, ազիդներ, ջուր (նկ. 2), և այլն:
Պրոտոպորֆին IX-ի կոմպլեքսը Fe 3+-ով կոչվում է հեմատին։ Հեմատինի աղաթթվի աղը (քլորհեմին, հեմին) հեշտությամբ արտազատվում է: բյուրեղային ձև (այսպես կոչված Teichmann բյուրեղներ): Հեմը ազոտային միացությունների (ամոնիակ, պիրիդին, հիդրազին, ամիններ, ամինաթթուներ, սպիտակուցներ և այլն) հետ բարդ միացություններ առաջացնելու հատկություն ունի՝ դրանով իսկ վերածվելով հեմոքրոմոգենի (տես)։ Քանի որ հեմը նույնն է կենդանիների բոլոր տեսակների մեջ, հեմոգլոբինների հատկությունների տարբերությունները պայմանավորված են հեմոգլոբինի մոլեկուլի սպիտակուցային մասի՝ գլոբինի կառուցվածքային առանձնահատկություններով։
Գլոբին
Գլոբինը ալբումինի տիպի սպիտակուց է, որն իր մոլեկուլում պարունակում է չորս պոլիպեպտիդ շղթաներ՝ երկու ալֆա շղթա (յուրաքանչյուրը պարունակում է 141 ամինաթթու մնացորդ) և երկու բետա շղթաներ, որոնք պարունակում են 146 ամինաթթուների մնացորդ։ Այսպիսով, G. մոլեկուլի սպիտակուցային բաղադրիչը կառուցված է տարբեր ամինաթթուների 574 մնացորդներից: Առաջնային կառուցվածքը, այսինքն՝ մարդկանց և մի շարք կենդանիների գլոբինի պոլիպեպտիդային շղթաներում ամինաթթուների գենետիկորեն որոշված հաջորդականությունը լիովին ուսումնասիրվել է։ Մարդու գլոբինի տարբերակիչ առանձնահատկությունը նրա բաղադրության մեջ ամինաթթուների՝ isoleucine և cystine բացակայությունն է։ Ալֆա և բետա շղթաներում N-տերմինալ մնացորդները վալինային մնացորդներ են: Ալֆա շղթաների C-տերմինալ մնացորդները ներկայացված են արգինինի մնացորդներով, իսկ բետա շղթաները՝ հիստիդինի մնացորդներով։ Յուրաքանչյուր շղթայում նախավերջին դիրքը զբաղեցնում են թիրոզինի մնացորդները։
Բյուրեղների ռենտգենյան կառուցվածքային վերլուծությունը հնարավորություն է տվել բացահայտել նրա մոլեկուլի տարածական կառուցվածքի հիմնական առանձնահատկությունները [M. Perutz]: Պարզվեց, որ ալֆա և բետա շղթաները պարունակում են տարբեր երկարությունների պարուրաձև հատվածներ, որոնք կառուցված են ալֆա պարույրների սկզբունքով (երկրորդական կառուցվածք); Ալֆա շղթան ունի 7, իսկ բետա շղթան ունի 8 պարուրաձև հատված, որոնք միացված են ոչ պտուտակավոր հատվածներով։ Պտուտակաձև հատվածները, սկսած N վերջնակետից, նշանակվում են լատինական այբուբենի տառերով (A, B, C, D, E, F, G, H), իսկ պարույրների ոչ պտուտակավոր հատվածները կամ պտտման անկյուններն ունեն. համապատասխան նշում (AB, BC, CD, DE և այլն): Գլոբինի շղթայի ամին (N) կամ կարբոքսիլ (C) ծայրի ոչ պտուտակավոր շրջանները համապատասխանաբար նշանակվում են NA կամ HC: Ամինաթթուների մնացորդները համարակալված են յուրաքանչյուր հատվածում և, բացի այդ, այս մնացորդի համարակալումը շղթայի N վերջնակետից տրված է փակագծերում:
Պտուտակաձև և ոչ պտուտակավոր հատվածները տարածության մեջ դասավորված են որոշակի ձևով, ինչը որոշում է գլոբինային շղթաների երրորդական կառուցվածքը։ Վերջինս գրեթե նույնական է Գ–ի ալֆա և բետա շղթաներում՝ չնայած դրանց առաջնային կառուցվածքի զգալի տարբերություններին։ Դա պայմանավորված է ամինաթթուների բևեռային և հիդրոֆոբ խմբերի հատուկ դասավորությամբ, ինչը հանգեցնում է ոչ բևեռային խմբերի կուտակմանը գլոբուլի ներքին մասում՝ հիդրոֆոբ միջուկի ձևավորմամբ։ Սպիտակուցի բևեռային խմբերը բախվում են ջրային միջավայրին՝ շփվելով նրա հետ։ Յուրաքանչյուր գլոբինային շղթայի ներսում, մակերեսի մոտ, կա հիդրոֆոբ խոռոչ («հեմ գրպան»), որի մեջ գտնվում է հեմը՝ ուղղված այնպես, որ դրա ոչ բևեռային փոխարինողները ուղղվեն դեպի մոլեկուլի ներքին մասը՝ դառնալով հիդրոֆոբ միջուկի մի մասը։ Արդյունքը մոտ. Հեմի և գլոբինի միջև 60 ոչ բևեռային շփում և հեմի մեկ կամ երկու բևեռային (իոնային) շփում ալֆա և բետա շղթաներով, որոնք ներառում են հիդրոֆոբ «գրպանից» դուրս եկող հեմի պրոպիոնաթթվի մնացորդներ: Հեմի տեղակայումը գլոբինի հիդրոֆոբ խոռոչում ապահովում է Fe 2+ հեմին թթվածնի հետադարձելի ավելացման հնարավորություն՝ առանց վերջինիս Fe 3+ օքսիդացման և բնորոշ է տարբեր կենդանատեսակների հեմոգլոբիններին։ Դա հաստատում է Գ.-ի ծայրահեղ զգայունությունը հեմի մոտ ոչ բևեռային շփումների ցանկացած փոփոխության նկատմամբ։ Այսպիսով, հեմատոֆիրինում հեմի փոխարինումը հեմատոպորֆիրինով հանգեցնում է հեմի հատկությունների կտրուկ խախտման։
Որոշ ամինաթթուների մնացորդներ, որոնք շրջապատում են հեմը հիդրոֆոբ խոռոչում, անփոփոխ ամինաթթուներից են, այսինքն՝ ամինաթթուները, որոնք նույնն են կենդանիների տարբեր տեսակների համար և կարևոր են G-ի ֆունկցիայի համար: Անփոփոխ ամինաթթուներից երեքը մեծ նշանակություն ունեն: հիստիդինի մնացորդներ, այսպես կոչված. պրոքսիմալ հիստիդիններ (87-րդ դիրք a- և 92-րդ դիրքում P-շղթաներում), հեռավոր հիստիդիններ (58-րդ դիրք a- և 63-րդ դիրքերում (5-շղթաներում), ինչպես նաև վալինային մնացորդ E-11 (62-րդ դիրք ալֆայում): շղթա և 67-րդ տեղը բետա շղթայում):
Կապը այսպես կոչված պրոքսիմալ հիստիդինը և հեմ երկաթը միակ քիմիական նյութն են: նրանց միջև կապը (իրականացվում է հեմի Fe 2+ ատոմի հինգերորդ կոորդինացիոն կապը) և ուղղակիորեն ազդում է հեմին թթվածնի ավելացման վրա։ «Դիստալ» հիստիդինը ուղղակիորեն կապված չէ հեմի հետ և չի մասնակցում թթվածնի ամրագրմանը: Դրա կարևորությունը Fe 2+ ատոմի կայունացումն է անշրջելի օքսիդացման դեմ (ըստ երևույթին, թթվածնի և ազոտի միջև ջրածնային կապի ձևավորման պատճառով): Վալինի մնացորդը (E-11) մի տեսակ կարգավորիչ է թթվածնի ավելացման արագությունը հեմերին. բետա շղթաներում այն գտնվում է ստերևային այնպես, որ այն զբաղեցնում է թթվածնի միացման տեղը, ինչի արդյունքում թթվածնացումը սկսվում է շղթաներով: .
Մոլեկուլի սպիտակուցային մասը և պրոթեզային խումբը ուժեղ ազդեցություն ունեն միմյանց վրա։ Գլոբինը փոխում է հեմի շատ հատկություններ՝ տալով նրան թթվածին կապելու ունակություն։ Հեմը ապահովում է գլոբինի դիմադրությունը դեղամիջոցների գործողությանը, տաքացմանը, ֆերմենտների քայքայմանը և որոշում է Գ–ի բյուրեղացման հատկությունների բնութագրերը։
Պոլիպեպտիդային շղթաները, որոնց կցված են հեմ մոլեկուլները, կազմում են չորս հիմնական մաս՝ հեմի մոլեկուլի ենթամիավորներ: Նրանց կապի բնույթը (դնելը) միմյանց հետ և տեղակայումը տարածության մեջ որոշվում են հեմի չորրորդական կառուցվածքի առանձնահատկություններով. P-շղթաները տեղակայված են քառաեդրոնի անկյուններում համաչափության առանցքի շուրջը, ավելին, ալֆա շղթաները ընկած են p-շղթաների վերևում և կարծես սեղմված են նրանց միջև, և բոլոր չորս հեմերը հեռու են միմյանցից (նկ. . 3). Ընդհանուր առմամբ, ձևավորվում է 6,4 X 5,5 X 5,0 նմ չափերով քառամերիկ գնդաձև մասնիկ: Չորրորդական կառուցվածքը կայունացվում է α-α և β-β շղթաների միջև աղային կապերով և α և β շղթաների երկու տեսակի շփումներով (α1-β1 և α2-β2): α1-β1 կոնտակտներն ամենաընդարձակն են, ներառում են 34 ամինաթթուների մնացորդներ, և փոխազդեցությունների մեծ մասը ոչ բևեռային են: α1-β2 կոնտակտը բաղկացած է 19 ամինաթթուների մնացորդներից, կապերի մեծ մասը նույնպես ոչ բևեռային է, բացառությամբ մի քանի ջրածնային կապերի։ Այս կոնտակտում տեղակայված բոլոր մնացորդները նույնն են բոլոր ուսումնասիրված կենդանիների տեսակների մեջ, մինչդեռ α1-β1 կոնտակտներում մնացորդների 1/3-ը տարբերվում է:
Մարդու գեղձը տարասեռ է, ինչը պայմանավորված է նրա բաղադրությունը կազմող պոլիպեպտիդային շղթաների տարբերությամբ։ Այսպիսով, չափահաս մարդու արյան գլյուկոզան, որը կազմում է արյան գլյուկոզի (HbA) 95-98%-ը, պարունակում է երկու α- և երկու β-շղթա; G.-ի փոքր մասնաբաժինը (HbA2), հասնելով 2,0-2,5% առավելագույն պարունակության, պարունակում է երկու α- և երկու σ-շղթա; Պտղի հեմոգլոբինը (HbF) կամ պտղի հեմոգլոբինը, որը մեծահասակների արյան մեջ կազմում է 0,1-2%, բաղկացած է երկու α- և երկու γ-շղթաներից։
Պտղի Գ.-ն փոխարինվում է HbA-ով ծնվելուց հետո առաջին ամիսներին։ Այն բնութագրվում է ջերմային դենատուրացիայի նկատմամբ զգալի դիմադրությամբ, որի վրա հիմնված են արյան մեջ դրա պարունակության որոշման մեթոդները։
Կախված պոլիպեպտիդային շղթաների կազմից՝ G.-ի թվարկված տեսակները նշանակվում են հետևյալ կերպ՝ HbA՝ Hbα2β2, HbA2՝ Hbα2σ2 և HbF՝ Hbα2γ։ Արյունաստեղծ ապարատի բնածին անոմալիաների և հիվանդությունների դեպքում ի հայտ են գալիս արյունաստեղծության աննորմալ տեսակներ, օրինակ՝ մանգաղ բջջային անեմիա (տես), թալասեմիա (տես), ոչ ֆերմենտային ծագման բնածին մեթեմոգլոբինեմիա (տես Մեթեմոգլոբինեմիա) և այլն։ Ամենատարածված փոխարինումը։ մեկ ամինաթթու մեկ զույգ պոլիպեպտիդ շղթաներում:
Կախված հեմի երկաթի ատոմի վալենտությունից և հեմի մոլեկուլում լիգանդի տեսակից՝ վերջինս կարող է լինել մի քանի ձևերով։ Կրճատված ջրածինը (դեօքսի-Hb) ունի Fe 2+՝ ազատ վեցերորդ վալենտությամբ, երբ O 2 ավելացվում է դրան, ձևավորվում է ջրածնի թթվածնային ձև (HbO 2): Երբ HbO 2-ը ենթարկվում է մի շարք օքսիդացնող նյութերի (կալիումի ֆերիցանիդ, նիտրիտներ, քինոններ և այլն), Fe 2+-ը օքսիդանում է մինչև Fe 3+՝ ձևավորելով մետեմոգլոբին, որն ի վիճակի չէ փոխանցել O2-ը: Կախված միջավայրի pH արժեքից՝ առանձնանում են մետեմոգլոբինի թթվային և ալկալային ձևեր, որոնք պարունակում են H 2 O կամ OH խումբ՝ որպես վեցերորդ լիգան: Առողջ մարդկանց արյան մեջ մետեմոգլոբինի կոնցենտրացիան կազմում է 0,83 + 0,42%:
Մեթեմոգլոբինն ունի ֆտորաջրածնի, հիդրոցյանաթթու և այլ նյութեր ամուր կապելու հատկություն։ Այս հատկությունն օգտագործվում է մեղրի մեջ։ հիդրոցիանից թունավորված մարդկանց փրկելու պրակտիկա. Գ–ի տարբեր ածանցյալները տարբերվում են կլանման սպեկտրներով (Աղյուսակ)։
Ալիքի երկարությունը (առավելագույն կլանման դեպքում), նմ
Միլիլիվալենտ լույսի կլանման գործակից, E
Մեթեմոգլոբին (met-Hb; pH 7.0-7.4)
Հեմոգլոբինի ֆունկցիոնալ հատկությունները. Գազի հիմնական կենսաբանական դերը մասնակցությունն է մարմնի և արտաքին միջավայրի միջև գազի փոխանակմանը: Գ–ն ապահովում է արյան միջոցով թթվածնի տեղափոխումը թոքերից հյուսվածքներ և ածխաթթու գազի տեղափոխումը հյուսվածքներից թոքեր (տես Գազափոխանակություն)։ Պակաս կարևոր չեն հեմոգլոբինի բուֆերային հատկությունները, որոնք արյան մեջ ձևավորում են հզոր հեմոգլոբին և օքսիհեմոգլոբին բուֆերային համակարգեր՝ դրանով իսկ նպաստելով օրգանիզմում թթու-բազային հավասարակշռության պահպանմանը (տես Բուֆերային համակարգեր, Թթու-բազային հավասարակշռություն)։
HbO 2-ի թթվածնի հզորությունը կազմում է 1,39 մլ O 2 1 գ HbO 2-ի դիմաց: G.-ի թթվածինը կապելու և արձակելու ունակությունը արտացոլվում է նրա թթվածնի դիսոցման կորով (ODC), որը բնութագրում է G.-ի թթվածնով հագեցվածության տոկոսը կախված O 2-ի մասնակի ճնշումից (pO 2):
Թթվածնի տետրամերային մոլեկուլներն ունեն S-աձև CDK, ինչը ցույց է տալիս, որ թթվածինը ապահովում է թթվածնի օպտիմալ կապը թոքերի համեմատաբար ցածր մասնակի ճնշման դեպքում և թողարկում հյուսվածքներում թթվածնի մասնակի համեմատաբար բարձր ճնշման դեպքում (նկ. 4): Հյուսվածքներին թթվածնի առավելագույն մատակարարումը զուգորդվում է արյան մեջ մասնակի բարձր ճնշման պահպանման հետ, որն ապահովում է թթվածնի ներթափանցումը հյուսվածքների խորքը։ Թթվածնի մասնակի ճնշման արժեքը մմ Hg-ով: Արվեստ., երբ գազի 50%-ը թթվածնացված է, թթվածնի նկատմամբ գազի հարաբերակցության չափանիշն է և նշանակվում է P50:
Գ–ի չորս հեմերին թթվածնի ավելացումը տեղի է ունենում հաջորդաբար։ G.-ի CDK-ի S-աձեւ բնույթը ցույց է տալիս, որ թթվածնի առաջին մոլեկուլը շատ դանդաղ է միանում G.-ին, այսինքն՝ նրա մերձեցումը G.-ի նկատմամբ ցածր է, քանի որ անհրաժեշտ է կոտրել աղի կոնտակտները դեզօքսիհեմոգլոբինի մոլեկուլում։ Այնուամենայնիվ, թթվածնի առաջին մոլեկուլի ավելացումը մեծացնում է մնացած երեք հեմերի մերձեցումը դրա նկատմամբ, և հեմի հետագա թթվածնացումը տեղի է ունենում շատ ավելի արագ (չորրորդ հեմի թթվածնացումը տեղի է ունենում 500 անգամ ավելի արագ, քան առաջինը): Հետևաբար, կա թթվածին կապող կենտրոնների միջև համագործակցային փոխազդեցություն: Ածխածնի երկօքսիդի (CO) ռեակցիայի օրինաչափությունները նույնն են, ինչ թթվածինը, բայց CO-ի նկատմամբ ածխածնի մոնօքսիդի հարաբերակցությունը գրեթե 300 անգամ ավելի բարձր է, քան O2-ի, ինչը ածխածնի երկօքսիդը դարձնում է խիստ թունավոր: Այսպիսով, օդում CO կոնցենտրացիայի դեպքում, որը հավասար է 0,1%, արյան գազի կեսից ավելին կապված է ոչ թե թթվածնի, այլ ածխածնի երկօքսիդի հետ: Այս դեպքում առաջանում է կարբոքսիհեմոգլոբին, որն ի վիճակի չէ տեղափոխել թթվածինը։
Հեմոգլոբինի թթվածնացման գործընթացի կարգավորիչներ. Թթվածնացման և թթվածնացման գործընթացների վրա մեծապես ազդում են ջրածնի իոնները, օրգանական ֆոսֆատները, անօրգանական աղերը, ջերմաստիճանը, ածխաթթու գազը և որոշ այլ նյութեր, որոնք ֆիզիոլի համաձայն վերահսկում են թթվածնի նկատմամբ ջրածնի հարաբերակցությունը: մարմնի պահանջները. Թթվածնի հարաբերության կախվածությունը թթվածնի նկատմամբ միջավայրի pH արժեքից կոչվում է Բորի էֆեկտ (տես Վերիգո էֆեկտ)։ Կան «թթու» (pH<6) и «щелочной» эффект Бора (pH>6). Ամենամեծ ֆիզիոլ. Կարևորը «ալկալային» Բորի էֆեկտն է: Դրա մոլեկուլային մեխանիզմը պայմանավորված է հեմոգլոբինի մոլեկուլում մի շարք դրական լիցքավորված ֆունկցիոնալ խմբերի առկայությամբ, որոնց դիսոցացման հաստատունները շատ ավելի բարձր են դեզօքսիհեմոգլոբինում՝ հեմոգլոբինի մոլեկուլի ներսում հարևան սպիտակուցային շղթաների բացասական լիցքավորված խմբերի միջև աղի կամուրջների ձևավորման պատճառով։ Թթվածնացման ժամանակ հեմոգլոբինի մոլեկուլում տեղի ունեցող կոնֆորմացիոն փոփոխությունների պատճառով առաջանում են աղի կամուրջներ։ Հետևաբար, թթվածնացումը հանգեցնում է գազի մոլեկուլից պրոտոնի (H +) անջատմանը և, ընդհակառակը, pH արժեքի փոփոխությունը, այսինքն՝ միջավայրի H + իոնների կոնցենտրացիան անուղղակիորեն ազդում է գազի մեջ թթվածնի ավելացման վրա: Այսպիսով, H +-ը դառնում է լիգանդ, որը գերադասելիորեն կապվում է դեզօքսիհեմոգլոբինին և դրանով իսկ նվազեցնում է թթվածնի հետ կապված նրա կապը, այսինքն՝ pH-ի փոփոխությունը դեպի թթվային կողմը առաջացնում է CDC-ի տեղաշարժ դեպի աջ: Թթվածնացման գործընթացը էնդոթերմիկ է, և ջերմաստիճանի բարձրացումը նպաստում է թթվածնի պառակտմանը G մոլեկուլից: Հետևաբար, օրգանների ակտիվության բարձրացումը և արյան ջերմաստիճանի բարձրացումը կհանգեցնեն CDC-ի աջ տեղափոխմանը և թթվածնի մատակարարմանը: դեպի հյուսվածքները կավելանան:
Թթվածնացման գործընթացի յուրահատուկ կարգավորումն իրականացվում է էրիթրոցիտներում տեղայնացված օրգանական ֆոսֆատներով։ Մասնավորապես, 2,3-diphosphoglycerate (DPG) զգալիորեն նվազեցնում է G.-ի մերձեցումը թթվածնի նկատմամբ՝ նպաստելով O 2-ի հեռացմանը օքսիհեմոգլոբինից։ DPG-ի ազդեցությունը G.-ի վրա մեծանում է pH-ի նվազման հետ (ֆիզիոլում, տարածաշրջանում), հետևաբար նրա ազդեցությունը Գ.-ի CDK-ի վրա ավելի մեծ չափով դրսևորվում է ցածր pH արժեքների դեպքում: DPG-ն հիմնականում կապվում է դեզօքսիհեմոգլոբինին 1:1 մոլային հարաբերակցությամբ՝ մտնելով նրա մոլեկուլի ներքին խոռոչը և ձևավորելով 4 աղի կամուրջներ բետա շղթաների վալինային մնացորդների երկու ալֆա-NH 2 խմբերով և, ըստ երևույթին, հիստիդինների երկու իմիդազոլ խմբերի հետ: 21 (143) բետա շղթաներ: DPG-ի ազդեցությունը նվազում է ջերմաստիճանի բարձրացման հետ, այսինքն՝ DPG-ի G-ի մոլեկուլին միանալու գործընթացը էկզոթերմիկ է: Սա հանգեցնում է նրան, որ DPG-ի առկայության դեպքում թթվածնացման գործընթացի կախվածությունը ջերմաստիճանից մեծապես անհետանում է: Հետևաբար, արյան կողմից թթվածնի նորմալ արտազատումը հնարավոր է դառնում ջերմաստիճանի լայն տիրույթում: Նմանատիպ ազդեցություն, թեև ավելի փոքր չափով, գործում է ATP-ի, պիրիդոքսալ ֆոսֆատի և այլ օրգանական ֆոսֆատների կողմից: Այսպիսով, օրգանական ֆոսֆատների կոնցենտրացիան էրիթրոցիտներում զգալի ազդեցություն ունի Գ.-ի շնչառական ֆունկցիայի վրա՝ արագ հարմարեցնելով այն տարբեր ֆիզիոլի և պատոլի, պայմանների, որոնք կապված են թթվածնացման խանգարման հետ (մթնոլորտում թթվածնի պարունակության փոփոխություն, արյան կորուստ, կարգավորում: թթվածնի տեղափոխումը մորից պտուղ պլասենցայի միջոցով և այլն): Այսպիսով, անեմիայի և հիպոքսիայի դեպքում ավելանում է DPG-ի պարունակությունը էրիթրոցիտներում, ինչը CDC-ն տեղափոխում է աջ և առաջացնում թթվածնի ավելի մեծ արտազատում դեպի հյուսվածքներ: Շատ չեզոք աղեր (ացետատներ, ֆոսֆատներ, կալիումի և նատրիումի քլորիդներ) նույնպես նվազեցնում են թթվածնի նկատմամբ Գ. Այս ազդեցությունը կախված է նյութի բնույթից և նման է օրգանական ֆոսֆատների ազդեցությանը։ Աղի բարձր կոնցենտրացիայի առկայության դեպքում G.-ի հարաբերակցությունը թթվածնի նկատմամբ հասնում է նվազագույնի՝ նույն չափով տարբեր աղերի և DPG-ի համար, այսինքն՝ և՛ աղերը, և՛ DPG-ն մրցակցում են միմյանց հետ G մոլեկուլի վրա նույն կապող կենտրոնների համար: Այսպիսով, օրինակ, DPG-ի ազդեցությունը թթվածնի նկատմամբ Գ.-ի հարաբերակցության վրա անհետանում է 0,5 մ նատրիումի քլորիդի առկայության դեպքում:
Դեռևս 1904 թվականին Չ.Բորը և այլք. ցույց է տվել թթվածնի նկատմամբ Գ–ի հակվածության նվազում՝ արյան մեջ ածխաթթու գազի մասնակի ճնշման բարձրացմամբ։
Ածխածնի երկօքսիդի պարունակության աճը հիմնականում հանգեցնում է շրջակա միջավայրի pH-ի փոփոխության, սակայն P50-ի արժեքը նվազում է ավելի մեծ չափով, քան սպասվում էր արժեքի նման նվազման դեպքում:
pH արժեքները. Սա պայմանավորված է ածխածնի երկօքսիդի հատուկ փոխհարաբերությամբ ալֆա շղթաների չլիցքավորված ալֆա-NH2 խմբերի և, հնարավոր է, գազի բետա շղթաների հետ՝ կարբամատների (կարբհեմոգլոբին) ձևավորման հետ հետևյալ սխեմայի համաձայն.
Դեզօքսիհեմոգլոբինը կապում է ավելի շատ ածխածնի երկօքսիդ, քան HbO 2-ը: Էրիտրոցիտներում DPG-ի առկայությունը մրցակցային կերպով արգելակում է կարբամատների ձևավորումը։ Կարբամատ մեխանիզմի օգնությամբ առողջ մարդկանց օրգանիզմից հանգստի ժամանակ դուրս է բերվում ածխաթթու գազի մինչև 15%-ը։ Արյան բուֆերային հզորության ավելի քան 70%-ն ապահովում է դրանում առկա գազը, ինչը նաև հանգեցնում է գազի զգալի անուղղակի մասնակցությանը ածխաթթու գազի տեղափոխմանը։ Երբ արյունը հոսում է հյուսվածքների միջով, HbO 2-ը վերածվում է դեզօքսիհեմոգլոբինի՝ միաժամանակ կապելով H+ իոնները և դրանով իսկ փոխակերպելով H 2 CO 3-ը HCO 3 -ի: Այսպիսով, Գ.-ի ուղղակի և անուղղակի մասնակցությամբ հյուսվածքներից արյուն եկող ածխաթթու գազի ավելի քան 90%-ը կապվում և տեղափոխվում է թոքեր։
Կարևոր է, որ CDC հերթափոխի այս բոլոր կարգավորիչները (H +, DPG, CO 2) փոխկապակցված են, ինչը մեծ նշանակություն ունի մի շարք ձևավորվող պաթոլային պայմաններում: Այսպիսով, էրիթրոցիտներում DPG-ի կոնցենտրացիայի ավելացումը դրանց նյութափոխանակության բարդ փոփոխությունների արդյունք է, որի դեպքում pH-ի բարձրացումը հիմնական պայմանն է։ Ացիդոզի և ալկալոզի դեպքում, նաև H+-ի և DPG-ի միջև փոխհարաբերությունների պատճառով, P50 արժեքը հավասարվում է:
Հեմոգլոբինի նյութափոխանակություն
Գ–ի կենսասինթեզը տեղի է ունենում էրիթրոցիտների երիտասարդ ձևերում (էրիթրոբլաստներ, նորմոբլաստներ, ռետիկուլոցիտներ), որտեղ ներթափանցում են Գ–ի բաղադրության մեջ ընդգրկված երկաթի ատոմները։ Գլիցինը և սուկցինաթթուն մասնակցում են պորֆիրին օղակի սինթեզին՝ δ– ձևավորմամբ։ ամինոլևուլինաթթու: Վերջինիս երկու մոլեկուլները վերածվում են պիրոլի ածանցյալի՝ պորֆիրինի նախադրյալի։ Գլոբինը ձևավորվում է ամինաթթուներից, այսինքն՝ սպիտակուցի սինթեզի սովորական եղանակով։ Գ.-ի քայքայումը սկսվում է էրիթրոցիտներից՝ ավարտելով նրանց կյանքի ցիկլը։ Հեմը օքսիդանում է ալֆա-մեթին կամրջի միջոցով՝ կոտրելով կապը համապատասխան պիրոլի օղակների միջև։
Ստացված G. ածանցյալը կոչվում է վերդոգլոբին (կանաչ պիգմենտ): Այն շատ անկայուն է և հեշտությամբ տրոհվում է երկաթի իոնի (Fe 3+), դենատուրացված գլոբինի և բիլիվերդինի։
Գ–ի կատաբոլիզմում մեծ նշանակություն ունի հապտոգլոբին–հեմոգլոբին համալիրը (Hp–Hb)։ Էրիտրոցիտից արյան հոսք դուրս գալուց հետո Գ.-ն անդառնալիորեն կապվում է հապտոգլոբինին (տես) Hp-Hb համալիրում։ Պլազմայում Hp-ի ամբողջ քանակի սպառումից հետո երիկամների մոտակա խողովակներով ներծծվում է Գ. Գլոբինի հիմնական մասը քայքայվում է երիկամներում 1 ժամվա ընթացքում։
Հեմի կատաբոլիզմը Hp-Hb համալիրում իրականացվում է լյարդի, ոսկրածուծի և փայծաղի ռետիկուլոէնդոթելային բջիջներով՝ լեղու պիգմենտների ձևավորմամբ (տես)։ Այս գործընթացում արձակված երկաթը շատ արագ մտնում է նյութափոխանակության ավազան և օգտագործվում է նոր երկաթի մոլեկուլների սինթեզում:
Հեմոգլոբինի կոնցենտրացիայի որոշման մեթոդներ. Սեպերում, պրակտիկայում, Գ.-ն սովորաբար որոշվում է գունաչափական մեթոդով՝ օգտագործելով Սալի հեմոմետրը՝ հիմնվելով Գ.-ից առաջացած հեմինի քանակի չափման վրա (տես Հեմոգլոբինոմետրիա)։ Այնուամենայնիվ, կախված արյան մեջ բիլիրուբինի և մետեմոգլոբինի պարունակությունից, ինչպես նաև պատոլի որոշ պայմաններում մեթոդի սխալը հասնում է +30% -ի: Առավել ճշգրիտ են սպեկտրոֆոտոմետրիկ հետազոտության մեթոդները (տես Սպեկտրաֆոտոմետրիա)։
Արյան մեջ ընդհանուր հեմոգլոբինը որոշելու համար օգտագործվում է ցիանմետեմոգլոբինի մեթոդը, որը հիմնված է հեմոգլոբինի բոլոր ածանցյալների (դեօքսի-Hb, HbO 2, HbCO, met-Hb և այլն) փոխակերպման և օպտիկական խտության չափման վրա: լուծույթը 540 նմ. Նույն նպատակով կիրառվում է պիրիդին-հեմոքրոգենիկ մեթոդը։ HbO 2-ի կոնցենտրացիան սովորաբար որոշվում է լույսի կլանմամբ 542 նմ կամ գազաչափական մեթոդով (կապված թթվածնի քանակով):
Հեմոգլոբինը կլինիկական պրակտիկայում
Գ–ի քանակական պարունակության և որակական բաղադրության որոշումը կիրառվում է այլ հեմատոլի հետ համատեղ։ ցուցանիշներ (հեմատոկրիտ, կարմիր արյան բջիջների քանակը, դրանց ձևաբանությունը և այլն) մի շարք պաթոլների, արյան կարմիր վիճակների (սակավարյունություն, էրիթրեմիա և երկրորդային էրիթրոցիտոզ) ախտորոշման համար, արյան կորստի աստիճանի գնահատում, արյան խտացում ջրազրկման ժամանակ: մարմին և այրվածքներ և այլն), թերապիայի ընթացքում հեմո-տրանսֆուզիոնների արդյունավետությունը գնահատելու և այլն:
Ըստ Լ. Ե. Յարուստովսկայայի և այլոց, արյան մեջ G.-ի պարունակությունը սովորաբար կազմում է միջինը 14,5 + 0,06 գ% տղամարդկանց համար (տարբերակներ 13,0-16,0 գ%), իսկ կանանց մոտ՝ 12,9 + 0,07 գ% (12,0- 14,0 գ%)։ (1969); տատանումները կախված են մարմնի տարիքից և սահմանադրական բնութագրերից, ֆիզիկական. ակտիվություն, սննդակարգ, կլիմա, թթվածնի մասնակի ճնշում շրջակա օդում: Գ–ի կոնցենտրացիան արյան մեջ հարաբերական արժեք է, որը կախված է ոչ միայն արյան մեջ ընդհանուր Գ–ի բացարձակ քանակից, այլև պլազմայի ծավալից։ Արյան մեջ Գ–ի մշտական քանակով պլազմայի ծավալի ավելացումը կարող է թերագնահատված թվեր տալ Գ–ի որոշման ժամանակ և ընդօրինակել անեմիան։
Գ–ի պարունակության ավելի ամբողջական գնահատման համար օգտագործվում են նաև անուղղակի ցուցիչներ՝ գունային ցուցիչի որոշում, արյան մեկ կարմիր գնդում Գ–ի միջին պարունակությունը, հեմատոկրիտի ինդեքսի նկատմամբ բջջային Գ–ի միջին կոնցենտրացիան և այլն։
Անեմիայի ծանր ձևերի դեպքում արյան մեջ Գ.-ի կոնցենտրացիայի նվազումը մինչև որոշակի կրիտիկական արժեք՝ 2-3 գ% և ավելի ցածր (հեմոգլոբինոպենիա, օլիգոքրոմեմիա) սովորաբար հանգեցնում է մահվան, սակայն, քրոնիկական անեմիայի որոշ տեսակների դեպքում։ , առանձին հիվանդներ, փոխհատուցման մեխանիզմների մշակման շնորհիվ, հարմարվում են նման համակենտրոնացմանը։
Պատոլում միշտ չէ, որ զուգահեռաբար փոխվում են պայմանները, Գ.-ի պարունակությունը և էրիթրոցիտների քանակը, ինչը արտացոլվում է անեմիայի դասակարգման մեջ (առանձնացվում են անեմիայի նորմալ, հիպո- և հիպերքրոմային ձևերը); Էրիթրեմիան և երկրորդային էրիթրոցիտոզը բնութագրվում են G.-ի կոնցենտրացիայի ավելացմամբ (հիպերքրոմեմիա) և միաժամանակ արյան կարմիր գնդիկների քանակի ավելացմամբ։
Գրեթե ամբողջ արյան գլյուկոզան գտնվում է կարմիր արյան բջիջների ներսում. դրա մի մասը գտնվում է պլազմայում՝ Hp-Hb համալիրի տեսքով: Ազատ պլազմային գլյուկոզան սովորաբար կազմում է 0,02-2,5 մգ% (ըստ Գ.Վ. Դերվիզի և Ն.Կ. Բյալկոյի): Ազատ հեմոլիզի պարունակությունը պլազմայում մեծանում է որոշ հեմոլիտիկ անեմիաների դեպքում, որոնք առաջանում են հիմնականում ներանոթային հեմոլիզով (տես Հեմոգլոբինեմիա)։
Հեմոգլոբինների մի քանի նորմալ տեսակների առկայության, ինչպես նաև արյան մեջ տարբեր ծագման աննորմալ հեմոգլոբինների որոշ հիվանդությունների (տես Հեմոգլոբինոպաթիաներ) հայտնվելու պատճառով մեծ ուշադրություն է դարձվում էրիթրոցիտներում հեմոգլոբինի որակական կազմի որոշմանը («հեմոգլոբինի բանաձև »): Այսպիսով, G. տեսակի HbF-ի և HbA2-ի ավելացված քանակի հայտնաբերումը սովորաբար բնորոշ է բետա թալասեմիայի որոշ ձևերին:
HbF-ի պարունակության աճ է նկատվել նաև այլ հեմատոլի դեպքում: հիվանդություններ (սուր լեյկոզ, ապլաստիկ անեմիա, պարոքսիզմալ գիշերային հեմոգլոբինուրիա և այլն), ինչպես նաև վարակիչ հեպատիտ, պտղի հեմոգլոբինի ասիմպտոմատիկ ժառանգական համառություն և հղիություն: HbA2 ֆրակցիայի կոնցենտրացիան արյան մեջ մեծանում է որոշակի անկայուն գազերի և թունավորումների առկայության դեպքում և նվազում երկաթի դեֆիցիտի անեմիայի դեպքում:
Մարդկանց մոտ օնտոգենեզի ընթացքում տեղի է ունենում նորմալ հեմոգլոբինների տարբեր տեսակների փոփոխություն, պտղի մեջ (մինչև 18 շաբաթական) հայտնաբերվում է առաջնային կամ պարզունակ հեմոգլոբին P (պրիմիտիվ); դրա սորտերը նշանակված են նույնը, ինչ Hb Gower1-ը և Hb Gower2-ը:
Առաջնային արյունաստեղծության գերակշռությունը համապատասխանում է վիտալինային արյունաստեղծման ժամանակաշրջանին, իսկ հաջորդող լյարդային արյունաստեղծման ժամանակաշրջանում գերակշռում է HbF-ը սինթեզվում։
«Մեծահասակների» HbA-ի սինթեզը կտրուկ ուժեղանում է ոսկրածուծի արյունաստեղծման շրջանում. HbF-ի պարունակությունը նորածին երեխայի մոտ կազմում է G.-ի ընդհանուր քանակի մինչև 70-90%-ը (մնացած 10-30%-ը բաժին է ընկնում HbA ֆրակցային): Կյանքի առաջին տարվա վերջում HbF-ի կոնցենտրացիան սովորաբար նվազում է մինչև 1-2%, իսկ HbA-ի պարունակությունը համապատասխանաբար աճում է:
Հայտնի է, որ Սբ. Գ–ի 200 աննորմալ (ախտաբանական կամ արտասովոր) տարբերակներ, որոնց ի հայտ գալը պայմանավորված է գլոբինի պոլիպեպտիդային շղթաների առաջացման տարբեր ժառանգական արատներով։
Լ. Փոլինգի, Իտանոյի (Ն. Ա. Իտանո) և այլոց բացահայտումը: 1949 թվականին patol, hemoglobin S-ը ( անգլ. ՝ sickle cell sickle cell ) հիմք դրեց մոլեկուլային հիվանդությունների ուսումնասիրությանը։ Արյան կարմիր բջիջներում աննորմալ արյան բջիջների առկայությունը սովորաբար (բայց ոչ միշտ) հանգեցնում է ժառանգական հեմոլիտիկ անեմիայի համախտանիշի զարգացմանը (տես):
Նկարագրված հեմոգլոբինի տարբերակների մեծ մասը պետք է համարել ոչ թե պաթոլոգիական, այլ G.S մեղրի բավականին հազվադեպ արտասովոր ձևեր: Որոշակի նշանակություն ունեն հեմոգլոբինները S, C, D, E, Bart, H, M և անկայուն հեմոգլոբինների մեծ խումբը (մոտ 60): Անկայուն հեմոգլոբինները կոչվում են աննորմալ հեմոգլոբիններ, որոնցում ամինաթթուներից մեկի փոխարինման արդյունքում. , մոլեկուլը դառնում է անկայուն օքսիդացնող նյութերի, տաքացման և մի շարք այլ գործոնների ազդեցության նկատմամբ։ GM-խմբերը առաջանում են ամինաթթուների փոխարինման արդյունքում պոլիպեպտիդային շղթաներում հեմ-գլոբինի կոնտակտների տարածքում, ինչը հանգեցնում է ոչ միայն մոլեկուլի անկայունության, այլև մետեմոգլոբինի ձևավորման հակվածության աճին: M-հեմոգլոբինոպաթիան հաճախ ժառանգական մետեմոգլոբինեմիայի պատճառն է (տես):
Գ–ի դասակարգումն ի սկզբանե հիմնված էր դրանք լատինական այբուբենի տառերով բացման հերթականությամբ պատկերելու վրա. Բացառություն է արվում նորմալ «չափահաս» Գ.-ի համար, որը նշվում է A տառով և պտղի G.-ի (HbF) համար: S տառը ցույց է տալիս աննորմալ մանգաղաձև G. (հոմանիշ HbB): Այսպիսով, լատիներեն այբուբենի տառերը A-ից S-ը համարվում էին G-ի ընդհանուր ընդունված անվանումները Համաձայն X International Hematol-ում ընդունվածի: Կոնգրես (Ստոկհոլմ, 1964) Գ. նոմենկլատուրա այսուհետ խորհուրդ չի տրվում օգտագործել այբուբենի մնացած տառերը նոր տարբերակներ նշանակելու համար:
Այժմ ընդունված է անվանել Գ-ի նոր հայտնաբերված ձևերը ըստ հայտնաբերման վայրի՝ օգտագործելով քաղաքի (տարածաշրջանի), հիվանդանոցի կամ լաբորատորիայի անվանումը, որտեղ առաջին անգամ հայտնաբերվել է նոր Գ.-ն և նշելով (փակագծերում) նրա կենսաքիմիական բանաձևը, գտնվելու վայրը։ և վնասված շղթայում ամինաթթուների փոխարինման բնույթը: Օրինակ, Hb Koln (ալֆա 2 բետա 2 98 val->met) նշանակում է, որ հեմոգլոբին Քոլնում ամինաթթվի վալինի բետա պոլիպեպտիդային շղթաներից մեկի 98-րդ դիրքում փոխարինվել է մեթիոնինով:
Գ–ի բոլոր սորտերը միմյանցից տարբերվում են ֆիզիկական և քիմիական բնութագրերով։ և ֆիզիկական հատկություններով, իսկ ոմանք՝ նաև ֆունկցիոնալ հատկություններով, որոնց վրա հիմնված են կլինիկայում Գ–ի տարբեր տարբերակների հայտնաբերման մեթոդները։ Հայտնաբերվել է աննորմալ գազերի նոր դաս՝ թթվածնի նկատմամբ փոխված կապով: Գ–ի մեքենագրումն իրականացվում է էլեկտրաֆորեզի և մի շարք այլ լաբորատոր մեթոդների միջոցով (ալկալիակայունության և ջերմային դենատուրացիայի թեստեր, սպեկտրոֆոտոմետրիա և այլն)։
Ելնելով էլեկտրաֆորետիկ շարժունակությունից՝ Գ–ները բաժանվում են արագաշարժի, դանդաղաշարժի և նորմալի (ունենալով նույն շարժունակությունը, ինչ HbA–ն)։ Այնուամենայնիվ, ամինաթթուների մնացորդների փոխարինումը միշտ չէ, որ հանգեցնում է մոլեկուլի լիցքի փոփոխության, ուստի որոշ տարբերակներ չեն կարող հայտնաբերվել էլեկտրոֆորեզի միջոցով:
Հեմոգլոբինը դատական բժշկության մեջ
Գ.-ն և նրա ածանցյալները դատաբժշկական բժշկության մեջ որոշված են՝ պարզելու արյան առկայությունը իրեղեն ապացույցների վրա կամ ցանկացած հեղուկում՝ Գ.-ում փոփոխություններ առաջացնող նյութերով թունավորումը ախտորոշելիս, տարբերելու պտղի կամ նորածնի պատկանող արյունը մեծահասակի արյունից։ . Ապացույցներ կան ժառանգական հատկանիշների կիրառման մասին վիճելի հայրության, մայրության և երեխաների փոխարինման, ինչպես նաև իրեղեն ապացույցների վրա արյան անհատականացման նպատակով:
Կենդանիներին մարդու հեմոգլոբինով իմունիզացնելու միջոցով ստացվել են հեմոգլոբին նստեցնող շիճուկներ: Այս շիճուկների օգնությամբ կարելի է հաստատել մարդու արյան առկայությունը Գ–ի վրա հետազոտված բիծում։
Բծերի մեջ արյան առկայությունը որոշելու համար օգտագործվում են միկրոսպեկտրային անալիզ և միկրոբյուրեղային ռեակցիաներ: Առաջին դեպքում հեմոքրոմոգենը ալկալիով և վերականգնող նյութով վերածվում է հեմոքրոմոգենի, որն ունի բնորոշ կլանման սպեկտր (տես Հեմոքրոմոգեն), կամ հեմոքրոմոգենի վրա գործում է խտացված ծծմբաթթու, որը հանգեցնում է հեմատոպորֆիրինի առաջացմանը։ բնորոշ կլանման սպեկտրը սպեկտրի տեսանելի մասում:
Արյան առկայությունը որոշելու համար միկրոբյուրեղային ռեակցիաներից առավել հաճախ օգտագործվում են հեմոքրոմոգենի և հեմինի հիդրոքլորիդի բյուրեղների արտադրության վրա հիմնված թեստերը: Գ.-ի համար հետազոտված բիծով հյուսվածքից հեմինի բյուրեղներ ստանալու համար վերցրեք թել և դրեք ապակե սլայդի վրա, ավելացրեք մի քանի բյուրեղ նատրիումի քլորիդ և մի քանի կաթիլ խտացված քացախաթթու (Teichmann-ի ռեագենտ): Տաքացնելիս (արյան առկայությամբ) Գ.-ից առաջանում են հեմինի հիդրոքլորիդի բյուրեղներ (Teichmann crystals)՝ շագանակագույն թեք զուգահեռականներ, երբեմն ռեակցիաներ են օգտագործում Գ–ից յոդ-հեմին բյուրեղներ ստանալու համար՝ մանր սև բյուրեղներ՝ ձևով։ ռոմբիկ պրիզմաներ.
Որոշ թունավորումների ժամանակ արյան մեջ սպեկտրոսկոպիկ եղանակով հայտնաբերվում են Գ–ի ածանցյալներ։ Օրինակ՝ շմոլ գազով թունավորման դեպքում տուժածների արյան մեջ հայտնաբերվում է կարբոքսիհեմոգլոբին, մեթեմոգլոբին առաջացնող նյութերով թունավորման դեպքում՝ մետեմոգլոբին։
Մանկասպանության դեպքում կարող է անհրաժեշտ լինել տարբեր ֆիզիկական ապացույցների հիման վրա պարզել նորածնի կամ պտղի արյան առկայությունը: Քանի որ պտղի և նորածնի արյան մեջ կա HbF-ի բարձր պարունակություն, իսկ մեծահասակի արյան մեջ՝ HbA, նրանք առանձնանում են իրենց ֆիզիկական և քիմիական հատկություններով։ հատկությունները, հեշտությամբ կարելի է տարբերակել նորածնի (պտղի) և մեծահասակի Գ.
Գործնականում առավել հաճախ օգտագործվում է ալկալային դենատուրացիա, քանի որ պտղի գեղձը ավելի դիմացկուն է ալկալիների գործողության նկատմամբ, քան մեծահասակների գեղձը: Գ–ի փոփոխությունները որոշվում են սպեկտրոսկոպիկ, սպեկտրոֆոտոմետրիկ կամ ֆոտոմետրիկ եղանակով։
Պոլիպեպտիդային շղթաների սինթեզն իրականացվում է կառուցվածքային և (հնարավոր է) կարգավորող գեների հսկողության ներքո։ Կառուցվածքային գեները որոշում են պոլիպեպտիդային շղթաների հատուկ ամինաթթուների հաջորդականությունը, մինչդեռ կարգավորող գեները որոշում են դրանց սինթեզի արագությունը (տես Գեն)։
Մարդկանց մոտ գոյություն ունեցող 6 տիպի նորմալ g շղթաները (Hbα, Hbβ, Hbγ, Hbδ, Hbε, Hbζ) կոդավորված են համապատասխանաբար 6 գենային լոկուսներով (α, β, γ, δ, ε, ζ): Ենթադրվում է, որ α շղթաների համար կարող է լինել երկու տեղ։ Բացի այդ, հայտնաբերվել են 5 տարբեր γ-շղթաներ, որոնք կոդավորված են տարբեր տեղանքներով։ Այսպիսով, ընդհանուր առմամբ, մարդը կարող է ունենալ 7-ից 10 զույգ կառուցվածքային գեն, որոնք վերահսկում են Գ-ի սինթեզը։
Զարգացման փուլերի ուսումնասիրությունը ցույց է տվել, որ մարդկանց մոտ առկա է տարբեր Գ–ների սինթեզի հստակ և հավասարակշռված գենետիկական կարգավորում, արգանդային կյանքի առաջին կեսում մարդկանց մոտ Գլ. arr. α, γ, ζ, ε-շղթաների տեղակայանքներ (վերջինս միայն կարճ ժամանակով, սաղմնային կյանքի վաղ շրջանում)։ Ծնվելուց հետո, գամմա շղթայի տեղանքի անջատման հետ միաժամանակ, ակտիվանում են β և δ շղթայական տեղորոշիչները։ Այս անջատման արդյունքում պտղի հեմոգլոբինը (HbF) փոխարինվում է մեծահասակների հեմոգլոբիններով՝ HbA՝ HbA2-ի փոքր մասնաբաժնով:
Մնում են անհասկանալի հարցեր՝ Գ.-ի սինթեզը քրոմոսոմների վրա որոշող գենային տեղանքների տեղակայումը, դրանց կապը, Գ.-ի կառուցվածքային գեների հատուկ ակտիվացման և ռեպրեսիայի կախվածությունը՝ կապված օնտոգենեզի ժամանակաշրջանների հետ, կարգավորիչ գեների գործողությունից, հումորալ գործոնների ազդեցությունը (օրինակ, հորմոններ) և այլն:
Գլոբինի շղթաների սինթեզը բջջում սպիտակուցի սինթեզի հատուկ օրինակ է:
Թեև Գ. սինթեզի կարգավորման հարցում դեռևս պարզ չէ, հիմնական մեխանիզմները, թվում է, նրանք են, որոնք վերահսկում են ԴՆԹ-ից mRNA-ի (մեսենջեր ՌՆԹ) արտագրման արագությունը: Գլոբինի սինթեզի համար հատուկ պատասխանատու ԴՆԹ-ի ճշգրիտ բնութագրում չի ստացվել: Այնուամենայնիվ, 1972թ.-ին մի քանի լաբորատորիաների հաջողվեց միաժամանակ սինթեզել G-ի սինթեզը կարգավորող գեն: Սա արվեց հակադարձ տրանսկրիպտազ ֆերմենտի միջոցով (տես Գենետիկական ճարտարագիտություն):
Հեմի մոլեկուլի հեմ մասը սինթեզվում է առանձին՝ օգտագործելով մի շարք ֆերմենտային ռեակցիաներ՝ սկսած Կրեբսի ցիկլից ակտիվ սուկցինատից (սուկցինատից) և վերջացրած պրոտոպորֆիրինի բարդ օղակով՝ կենտրոնում երկաթի ատոմով։
Սպիտակուցների սինթեզի գործընթացում գլոբինային շղթաները ստանում են իրենց բնորոշ կոնֆիգուրացիան, և հեմը «մտցվում» է հատուկ գրպանում։ Հաջորդը, ավարտված շղթաների համադրությունը տեղի է ունենում տետրամերի ձևավորման համար:
Հատուկ ԴՆԹ-ի սինթեզը տեղի է ունենում էրիթրոցիտների պրեկուրսորներում միայն մինչև օրթոխրոմային նորմոբլաստային փուլը։ Այդ ընթացքում ստեղծվում է գլոբինի պոլիպեպտիդային շղթաների վերջնական հավաքածուն, այն զուգակցվում է հեմի հետ, և ձևավորվում են ՌՆԹ-ի բոլոր տեսակները և անհրաժեշտ ֆերմենտները։
Գ.սինթեզի ժառանգական խանգարումները բաժանվում են երկու մեծ խմբի.
1) այսպես կոչված հեմոգլոբինի առաջնային կառուցվածքի կառուցվածքային տարբերակներ կամ անոմալիաներ՝ «որակական» հեմոգլոբինոպաթիաներ, ինչպիսիք են Hb, S, C, D, E, M, ինչպես նաև անկայուն հեմոգլոբինով և հեմոգլոբինոպաթիաներով առաջացած հիվանդություններ՝ O 2-ի նկատմամբ ավելացված մերձեցմամբ (տես Հեմոգլոբինոպաթիաներ),
2) պայմաններ, որոնք առաջանում են գլոբինի պոլիպեպտիդային շղթաներից մեկի սինթեզի խախտման հետևանքով` «քանակական» հեմոգլոբինոպաթիաներ կամ թալասեմիա (տես):
Կառուցվածքային տարբերակների դեպքում G մոլեկուլի կայունությունը և գործառույթը կարող է փոխվել: Թալասեմիայի դեպքում գլոբինի կառուցվածքը կարող է նորմալ լինել: Քանի որ գենետիկական արատների երկու տեսակներն էլ տարածված են մարդկային շատ պոպուլյացիաներում, հաճախ նկատվում են անհատներ, որոնք միաժամանակ հետերոզիգոտ են G.-ի կառուցվածքային տարբերակի և թալասեմիայի համար: Տարբեր գեների համակցությունները կազմում են հեմոգլոբինոպաթիաների շատ բարդ սպեկտր: Որոշ դեպքերում մուտացիաները կարող են ազդել Գ.-ի սինթեզի փոխարկման մեխանիզմների վրա, ինչը հանգեցնում է, օրինակ, մեծահասակների մոտ պտղի Գ.-ի սինթեզի շարունակմանը։ Այս պայմանները հավաքականորեն կոչվում են պտղի հեմոգլոբինի ժառանգական կայունություն:
Fusion տարբերակները ներառում են Hb Lepore, anti-Lepore և Kenya mutants: Ամենայն հավանականությամբ, G.-ի կառուցվածքային այս անոմալիաները առաջացել են սերտ կապված G գեների միջև անհավասար ոչ հոմոլոգ մեիոտիկ հատման արդյունքում: Որպես արդյունք, օրինակ, Hb Lepore-ում α-շղթաները նորմալ են, իսկ մյուս պոլիպեպտիդային շղթաները: պարունակում են δ- հաջորդականության մի մասը և β- հաջորդականության պոլիպեպտիդ շղթաների մի մասը:
Քանի որ մուտացիաները կարող են առաջանալ գեների սինթեզը որոշող ցանկացած գենում, կարող են առաջանալ մի քանի իրավիճակներ, երբ անհատները կլինեն հոմոզիգոտներ, հետերոզիգոտներ կամ կրկնակի հետերոզիգոտներ աննորմալ գեների ալելների համար մեկ կամ մի քանի տեղամասերում:
Հայտնի են Գ–ի ավելի քան 200 կառուցվածքային տարբերակներ, բնութագրվել են ավելի քան 120–ը, և շատ դեպքերում հնարավոր է եղել Գ–ի կառուցվածքային փոփոխությունը կապել նրա անոմալ ֆունկցիայի հետ։ Կետային մուտացիայի արդյունքում Գ–ի նոր տարբերակի առաջացման ամենապարզ մեխանիզմը (գենետիկ կոդի մեջ մեկ բազայի փոխարինում) կարելի է ցույց տալ HbS–ի (սխեմայի) օրինակով։
Ամինաթթուների փոխարինման ազդեցությունը ֆիզիկաքիմիական. G. մոլեկուլի հատկությունները, կայունությունը և գործառույթը կախված են նախորդին փոխարինած ամինաթթվի տեսակից և մոլեկուլում նրա դիրքից։ Մի շարք մուտացիաներ (բայց ոչ բոլորը) էապես փոխում են հեմոգլոբինի մոլեկուլի գործառույթն ու կայունությունը (HbM, անկայուն հեմոգլոբիններ, հեմոգլոբիններ՝ O 2-ի նկատմամբ փոփոխված կապակցությամբ) կամ դրա կազմաձևը և մի շարք ֆիզիկաքիմիական: հատկություններ (HbS և HbC):
Հեմոգլոբինները անկայուն են
Անկայուն հեմոգլոբինները աննորմալ հեմոգլոբինների խումբ են, որոնք հատկապես զգայուն են օքսիդացնող նյութերի, ջերմության և մի շարք այլ գործոնների ազդեցության նկատմամբ, ինչը բացատրվում է իրենց մոլեկուլներում որոշ ամինաթթուների մնացորդների գենետիկորեն որոշված փոխարինմամբ մյուսներով. Նման հեմոգլոբինների փոխադրումը հաճախ դրսևորվում է որպես հեմոգլոբինոպաթիա (տես):
Անկայուն Գ.-ի կրող մարդկանց էրիթրոցիտներում, այսպես կոչված. Հայնցի մարմիններ, որոնք արյան անկայուն բջիջների դենատուրացված մոլեկուլների կուտակումներ են (բնածին հեմոլիտիկ անեմիա Հայնցի մարմիններով)։ 1952 թվականին Ի. Ա. Քեթին առաջարկեց, որ այս հիվանդությունը ժառանգական է: Frick (P. Frick), Gitzig (W. H. Hitzig) և Vetke (K. Betke) 1962 թվականին առաջին անգամ, օգտագործելով Hb Ցյուրիխի օրինակը, ապացուցեցին, որ հեմոլիտիկ անեմիան Heinz մարմինների հետ կապված է անկայուն հեմոգլոբինների առկայության հետ։ Carrell-ը (R. W. Carrell) և G. Lehmann-ը 1969 թվականին առաջարկել են նոր անվանում նման հեմոգլոբինոպաթիաների համար՝ հեմոլիտիկ անեմիա, որն առաջացել է անկայուն Գ.
Հեմի մոլեկուլների անկայունությունը կարող է պայմանավորված լինել հեմի հետ շփման մեջ ամինաթթուների մնացորդների փոխարինմամբ. ոչ բևեռային ամինաթթուների մնացորդի փոխարինում բևեռայինով; մոլեկուլի երկրորդական կառուցվածքի խախտում, որը պայմանավորված է ցանկացած ամինաթթվի մնացորդի փոխարինմամբ պրոլինի մնացորդով. ամինաթթուների մնացորդների փոխարինում α1β1- և α2β2-շփումների տարածքում, ինչը կարող է հանգեցնել հեմոգլոբինի մոլեկուլի տարանջատմանը մոնոմերների և դիմերների. որոշ ամինաթթուների մնացորդների ջնջում (կորուստ); ենթամիավորների երկարացում, օրինակ՝ երկու անկայուն հեմոգլոբիններ՝ Hb Cranston-ը և Hb Tak-ը, ունեն երկարացված բետա շղթաներ՝ համեմատած նորմալ հեմոգլոբինի հետ՝ իրենց C-վերնամասին կցված հիդրոֆոբ հատվածի պատճառով:
Անկայուն գազերի դասակարգումը, որն առաջարկել է Ջ.
Նկարագրված է մոտ. 90 անկայուն G., իսկ G. մոլեկուլի բետա շղթաներում ամինաթթուների մնացորդների փոխարինմամբ տարբերակները հայտնաբերվում են մոտավորապես 4 անգամ ավելի հաճախ, քան ալֆա շղթաներում նման մնացորդների փոխարինմամբ:
Անկայուն Գ–ի փոխադրումը ժառանգվում է աուտոսոմային գերիշխող եղանակով, իսկ կրողները՝ հետերոզիգոտներ։ Որոշ դեպքերում անկայուն Գ.-ի փոխադրման առաջացումը ինքնաբուխ մուտացիայի արդյունք է։ Գ–ի կայունության նվազումը հանգեցնում է ոչ միայն նրա հեշտ տեղումների, այլ որոշ դեպքերում՝ հեմի կորստի։ Ամինաթթուների մնացորդների փոխարինումը հեմոգլոբինի մոլեկուլի a- և (3-շղթաների) շփման կետերում կարող է ազդել մոլեկուլի հարաբերակցության վրա թթվածնի, հեմերի փոխազդեցության և տետրամերների, դիմերների և հեմոգլոբինի մոնոմերների միջև: մարդիկ հետերոզիգոտ են անկայուն հեմոգլոբինի գեների համար, ինչպես նորմալ, այնպես էլ աննորմալ, անկայուն Գ., սակայն վերջինս արագորեն դենատուրայում է և դառնում ֆունկցիոնալ ոչ ակտիվ:
Ծանր հեմոլիտիկ անեմիա սովորաբար նկատվում է մոլեկուլային անկայունության բարձր աստիճանով անկայուն Գ.-ի կրող հիվանդների մոտ։
Այլ անկայուն G. սեպ կրելիս դրսևորումները սովորաբար միջին ծանրության են կամ բոլորովին աննշան: Որոշ դեպքերում (Hb Riverdale-Bronx, Hb Zurich և այլն) անկայուն Գ.-ի փոխադրումը դրսևորվում է հեմոլիտիկ ճգնաժամերի տեսքով՝ որոշակի դեղամիջոցներ ընդունելուց (սուլֆոնամիդներ, ցավազրկողներ և այլն) կամ վարակների ենթարկվելուց հետո։ Որոշ հիվանդներ, օրինակ՝ Hb Hammersmith, Hb Bristol, Hb Sydney և այլն կրողներ, ունենում են մաշկի ցիանոզ, որն առաջանում է մետ- և սուլֆհեմոգլոբինների ձևավորման ավելացման պատճառով: Անկայուն Գ.-ի փոխադրմամբ առաջացած հեմոգլոբինոպաթիաները պետք է տարբերվեն այլ էթոլոգիայի հեմոլիտիկ և հիպոքրոմ սակավարյունությունից և, առաջին հերթին, երկաթի դեֆիցիտի և հեմոլիտիկ անեմիայի հետ կապված պենտոզաֆոսֆատ ցիկլի ֆերմենտների գենետիկորեն որոշված անբավարարության, գլիկոլիզի և այլնի հետ։
Անկայուն Գ.-ի կրող մարդկանց մեծ մասը հատուկ բուժման կարիք չունի։ Հեմոլիզի համար վերականգնողական թերապիան օգտակար է։ Անկայուն Գ–ի բոլոր կրողներին խորհուրդ է տրվում ձեռնպահ մնալ հեմոլիզ հրահրող օքսիդացնող դեղամիջոցներից (սուլֆոնամիդներ, սուլֆոններ, ցավազրկողներ և այլն)։ Արյան փոխներարկումը ցուցված է միայն խորը անեմիայի զարգացման դեպքում։ Ծանր հեմոլիզի դեպքում՝ փայծաղի կողմից էրիթրոցիտների ավելացած սեկվեստրով և հիպերսպլենիզմով, ցուցված է փայծաղի հեռացում (տես): Այնուամենայնիվ, սպլենէկտոմիան երեխաների մոտ (մինչև 6 տարեկան) սովորաբար չի իրականացվում՝ սեպտիկեմիայի զարգացման ռիսկի պատճառով։
Անկայուն հեմոգլոբինների հայտնաբերման մեթոդներ
Հեմոգլոբինի ջերմամոլության ուսումնասիրությունը ամենակարևոր թեստն է նրա անկայունությունը պարզելու համար: Այն առաջարկվել է A. G. Grimes-ի և A. Meisler-ի կողմից 1962-ին և Dacey-ի կողմից 1964-ին և բաղկացած է ինկուբացիոն հեմոլիզատներից, որոնք նոսրացված են 0,1 M ֆոսֆատով կամ Tris-HCl բուֆերով, pH 7,4, 50-60 ° մեկ ժամվա ընթացքում: Այս դեպքում անկայուն գլիկոզիդները դենատուրացվում և նստվածք են ստանում, և լուծույթում մնացած ջերմակայուն հիդրօքսիդի քանակը որոշվում է սպեկտրոֆոտոմետրիկ եղանակով՝ 541 նմ և հաշվարկվում է բանաձևով.
/ * 100 = = ջերմակայուն հեմոգլոբին (տոկոս),
որտեղ E-ը մարման արժեքն է 541 նմ ալիքի երկարության վրա:
Ջերմակայուն Գ.-ի հարաբերական պարունակությունը հավասար է 100%-ի` ջերմակայուն Գ.-ի քանակին (տոկոսներով):
Carrell-ը և Kay-ը (R. Kau) 1972թ.-ին առաջարկեցին հեմոլիզատները ինկուբացնել 17% իզոպրոպանոլ-Տրիս բուֆերի խառնուրդում, pH 7.4 37°-ում 30 րոպե:
Էրիտրոցիտների հեմոլիզը կարող է առաջանալ ջրի պատճառով, քանի որ այդ նպատակով ածխածնի տետրաքլորիդի կամ քլորոֆորմի օգտագործումը հանգեցնում է անկայուն արյան բջիջների մասնակի դենատուրացիայի և ստացված տվյալների աղավաղման:
Անկայուն Գ.-ի որոշման ամենատարածված մեթոդը հիստոքիմիական է՝ Հայնցի մարմինների նույնականացման մեթոդը։ Այս դեպքում արյան կարմիր բջիջները ներկվում են բյուրեղյա մանուշակով, մեթիլ մանուշակով կամ օգտագործվում է ռեակցիա ացետիլֆենիլհիդրազինի հետ։ Արյունը նախնական պահվում է 24 ժամ 37°-ում։ Պետք է հիշել, որ Հայնցի մարմինները կարող են հայտնաբերվել նաև այլ հեմոլիտիկ անեմիաների, թալասեմիայի, մետեմոգլոբին ձևավորող նյութերով թունավորումների և որոշ ֆերմենտների դեպքում:
Թղթի կամ ցելյուլոզայի ացետատի վրա հեմոլիզատների էլեկտրաֆորետիկ տարանջատումը հաճախ արդյունք չի տալիս, քանի որ շատ անկայուն հեմոլիզատներում մոլեկուլում ամինաթթուների մնացորդների փոխարինումը չի փոխում մոլեկուլի էլեկտրաֆորետիկ հատկությունները: Այս առումով առավել տեղեկատվական են էլեկտրոֆորեզը պոլիակրիլամիդի և օսլայի գելերում (տես Էլեկտրաֆորեզ) կամ իզոէլեկտրական ֆոկուսը։
Շատ հիվանդների մոտ, ովքեր անկայուն Գ.-ի կրողներ են, մեզը մշտապես կամ երբեմն ձեռք է բերում մուգ գույն՝ դիպիրոլների առաջացման պատճառով, որը ծառայում է որպես էրիթրոցիտներում անկայուն Գ.-ի առկայության բավականին ճշգրիտ նշան։
Մատենագիտություն. Վլադիմիրով Գ. Ե. և Պանտելեևա Ն. Ս. Ֆունկցիոնալ կենսաքիմիա, Լ., 1965; And r and to L. I. Hemoglobins and their properties, M., 1975, bibliogr.; Korzhuev P. A. Hemoglobin, M., 1964, Bibliogr.; Կուշակովսկի Մ. Ս. Հեմոգլոբինի վնասման կլինիկական ձևեր, Լ., 1968; Peru TC M. Hemoglobin molecule, գրքում՝ Molecules and Cells, ed. G. M. Frank, թարգմ. անգլերենից, էջ. 7, Մ., 1966; t u-m and n about in A.K. Նյութական ապացույցների դատաբժշկական փորձաքննության հիմունքներ, Մ., 1975, մատենագր.; Ուսպենսկայա Վ.Դ. Հապտոգլոբինի սինթեզի և կատաբոլիզմի տեղի և հեմոգլոբինի նյութափոխանակության մեջ նրա դերի մասին, Վոպր. մեղր. քիմիա, հատոր 16, թիվ 3, էջ 16, էջ 16, էջ 16, էջ 16, էջ 13, էջ 16, էջ 16, էջ 16, էջ 13, էջ 13, էջ 11, էջ 16, էջ 13, էջ 16, էջ 13, էջ 13, էջ 13, էջ 13, էջ 13, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 16, էջ 11, էջ. 227, 1970, մատենագր.; Հարիս Գ. Մարդու կենսաքիմիական գենետիկայի հիմունքները, տրանս. անգլերենից, էջ. 15, Մ., 1973; Sharonov Yu. A. and Sharonova N. A. Structure and functions of hemoglobin, Molecular Biol., v. 9, No 1, p. 145, 1975, մատենագր.; C h a g a c h e S. Հեմոգլոբիններ՝ փոփոխված թթվածնի կապակցությամբ, Clin. Haemat., v. 3, էջ. 357, 1974, մատենագր.; Giblett E. R. Գենետիկական մարկերներ մարդու արյան մեջ, Ֆիլադելֆիա, 1969; Հեմոգլոբինի և կարմիր բջիջների կառուցվածքը և գործառույթը, խմբ. by G. J. Brewer, N. Y.-L., 1972; HuehnsE. R. Հեմոգլոբինի ալֆա-շղթայի սինթեզի գենետիկ հսկողություն, Հեմատոլոգիա, v. 8, էջ. 61, 1974, մատենագր.; Լեհ-մաննՀ. ա. Hunt s m a n R. G. Man’s hemoglobins, Philadelphia, 1974; P e-r u t z M. F. The croonian lecture, 1968, The hemoglobin molecule, Proc, roy, Soc. Վ., գ. 173, էջ. 113, 1969; Պ ե րութ զ Մ Ֆ* ա. Lehmann H. Մարդկային հեմոգլոբինի մոլեկուլային պաթոլոգիա, Բնություն (Լոնդ.), v. 219, էջ. 902, 1968; Ռութոն Ֆ. J. Որոշ վերջին աշխատանքներ թթվածնի, ածխածնի երկօքսիդի և հեմոգլոբինի փոխազդեցությունների վերաբերյալ, Biochem. Ջ., գ. 117, էջ. 801, 1970;Ս տ ա մ ա-տոյաննոպոնլոս Գ.ա. NuteP. E. Հեմոգլոբինների գենետիկական հսկողություն, Clin. Haemat., v. 3, էջ. 251, 1974, մատենագր.; Van Assendelft O. W. Հեմոգլոբինի ածանցյալների սպեկտրոֆոտոմետրիա, Assen, 1970; Weatherall D. J. Մոլեկուլային հիմք հեմոգլոբինի որոշ խանգարումների համար, Բրիտ, բժշկ. Ջ., գ. 4, էջ. 451, 516, 1974; Եղանակը D. J. a. Clegg J. B. Թալասեմիայի մոլեկուլային հիմքը, Բրիտ. J. Haemat., v. 31, լրացում, էջ. 133, 1975; Wintro-b e M. M. Կլինիկական արյունաբանություն, Ֆիլադելֆիա, 1974 թ.
Հեմոգլոբինները անկայուն են- Didkovsky N.A. et al. Hemoglobin Volga ft 27 (B9) alanine->aspartic թթու (նոր աննորմալ հեմոգլոբին ծանր անկայունությամբ), Խնդիրներ, հեմատոլ և արտահոսք, արյուն, հատոր 22, թիվ 4, էջ. 30, 1977, մատենագր.; I d e l l-s o n L. I., Didkovsky N. A. and Ermilchenko G. V. Hemolytic anemias, M., 1975, bibliogr.; In u n n H. F., Forget B. G. a. R a n n e y H. M. Human hemoglobins, Philadelphia, 1977, bibliogr.; Lehmann H.a. K y-n o h P. A. Մարդու հեմոգլոբինի տարբերակները և դրանց բնութագրերը, Ամստերդամ, 1976 թ.
Ա.Պ. Անդրեևա; Յու. Ն. Տոկարև (գոհար և գեն.), Ա. Կ. Թումանով (դատարան); Յու.Ն.Տոկարև, Վ.Մ.Բելոստոցկի.
Քիմիայի հիմնական հասկացություններն ու օրենքները.
Մոլային զանգված, նյութի քանակություն, Ավոգադրոյի հաստատուն։
Գազի մոլային ծավալը.
I. Նյութի կառուցվածքային միավորի զանգվածի հաշվարկ.
Որոշեք ջրածնի ատոմների թիվը 9 գ ջրի նմուշում:
M(H2O) = 18 գ\մոլ
n(H2O) = 9/18= 0,5 մոլ
Բանաձևից հետևում է, որ 1 մոլ H2O պարունակում է 2 մոլ ջրածնի ատոմ, այսինքն. n(H) = 2×0.5 մոլ = 1 մոլ.
Որոշեք ջրածնի ատոմների քանակը ամոնիումի ջրածնային ֆոսֆատի 26,4 գ նմուշում:
M(NH4)2HPO4 = 132 գ\մոլ
n((NH4)2HPO4) = 26.4/132= 0.2 մոլ
n(H) =0.2×9= 1.8 մոլ
Պատասխան՝ 1,8 մոլ
Խառնուրդը բաղկացած է էթանոլից C2H5OH՝ 46 գ կշռող և 72 գ կշռող ջրից, որոշե՛ք խառնուրդում թթվածնի ատոմների քանակը։
n(C2H5OH) = 46/46 = 0.1 մոլ n(O) =0.1×1= 0.1 մոլ
n(H2O) =72/18 = 0.4 մոլ n(O) =0.4×1= 0.4 մոլ n(O) =0.1+0.4=0.5 մոլ
Խառնուրդը բաղկացած է քացախաթթվից CH3COOH՝ 6 գ կշռող և մաթնաթթվից՝ HCOOH 9,2 գ զանգվածով։Որոշեք խառնուրդում թթվածնի ատոմների քանակը։
n(CH3COOH) =6 /60 = 0.1 մոլ n(O) =0.1×2= 0.2 մոլ
n(HCOOH) =9.2/46 = 0.2 մոլ n(O) =0.2×2= 0.4 մոլ n(O) =0.2+0.4=0.6 մոլ
Որոշե՛ք 12,04 1022 ջրի մոլեկուլ պարունակող ջրի նմուշի զանգվածը։
n(H2O) = NNA= 12.04∙10226.02∙1023=0.2 մոլ
m(H2O) = 0,2×18= 3,6 գ
Որոշե՛ք 6,021022 պղնձի ատոմ պարունակող պղնձի սուլֆատի նմուշի զանգվածը։
Պատասխան՝ 16
Հաշվե՛ք 3,011022 ջրածնի ատոմ պարունակող ամոնիումի սուլֆատի նմուշի զանգվածը։
n(H) =NNA=3.0110226.02∙1023=0.05 մոլ
միացությունում կա թթվածնի 8 ատոմ
n(NH4)2SO4 = 0,05 /8 = 0,00625 մոլ
մ = 0,00625 × 132 գ\մոլ = 0,825 գ:
Որոշե՛ք մագնեզիումի ջրածնի սուլֆատի նմուշի զանգվածը, եթե հայտնի է, որ այն պարունակում է 3,6121023 թթվածնի ատոմ։
n(O) =NNA = 3,612×10236,02×1023=0,6 մոլ
n Mg(HSO4)2 = 0,6/8= 0,075 մոլ
մ = 0,075×218= 16,35 գ
Որոշե՛ք նատրիումի սուլֆատի լուծույթի զանգվածը ջրի մեջ, որը պարունակում է 30,1 1022 նատրիումի ատոմ և 6,021024 ջրածնի ատոմ։
n (Na) =NNA =30.1∙10226.02∙1023=0.5 մոլ
Բանաձևը պարունակում է նատրիումի 2 ատոմ, հետևաբար՝ n(Na2 SO4) = 0,5/2 = 0,25 մոլ
մ նյութ (Na2 SO4) = 0,25 × 142 գ\մոլ = 35,5 գ
n(H) =NNA= 6.02∙10246.02∙1023=10 մոլ
n(H2O) = 10/2=5 մոլ
m(H2O) =5×18=90 գ
m լուծում = m նյութ (Na2 SO4) + m (H2O) = 35,5 + 90 = 125,5 գ:
Որոշե՛ք էթանոլի C2H5OH 12,04 1022 ածխածնի ատոմ և 24,08 1022 թթվածնի ատոմ պարունակող էթանոլի լուծույթի զանգվածը։
n (C) =NNA= 12.04∙10226.02∙1023=0.2 մոլ
n (C2H5OH) = 0.2/2 = 0.1 մոլ
m(C2H5OH) = 0,1 × 46 = 4,6 գ
n(O) =NNA =2.405∙10236.02∙1023=0.4 մոլ
n(H2O) =0.4/1=0.4 մոլ
m(H2O) =0,4×18= 7,2 գ
msolution = m նյութ + m(H2O) = 4.6 + 7.2 = 11.8 գ
Հաշվե՛ք նատրիումի մեկ ատոմի զանգվածը։
ma= M (Na) / NA = 23/ 6.021023 = 3.8210-23 գ.
Գտե՛ք կալցիումի երեք ատոմների զանգվածը:
ma=3 M (Ca) / NA = (3×40) / 6.021023 = 19.910-23 գ
Հաշվե՛ք ջրի 7 մոլեկուլների զանգվածը։
ma=7 M (H2O) / NA = (7×18) / 6,021023 = 20,910-23 գ
Որոշե՛ք SO3 մոլեկուլի զանգվածը
ma= M (SO3) / NA = 80 /6,021023 = 13,3 10-23 գ
Հաշվե՛ք սիլիցիումի (IV) օքսիդի հինգ բանաձևային միավորների զանգվածը (գ-ով):
mfe=5×Mr×u=5×60×1,66∙10-27=4,98∙10-22 գ.
Հաշվեք զանգվածը.
Նատրիումի ատոմ (գ)
ma= M (Na) / NA = 23/ 6.021023 = 3.8210-23 գ
ma=ArNa×u=23×1,6610-27 = 3,8210-23 գ
Սպիտակ ֆոսֆորի հինգ մոլեկուլ P4 (կգ)
Պատասխան՝ 1.02910-24 կգ
S8 ռոմբիկ ծծմբի տասը մոլեկուլ (գ)
Պատասխան՝ 4,2510-21 գ
Օզոնի երեք մոլեկուլ O3 (ամուում)
ma=3×16×3×a.u.m=144a.u.m.
Ֆուլերենի մոլեկուլներ C60 (մգ)
մմ = Mr(C60)×u = 1195,210-27 = 1,19510-24 կգ = 1,19510-21 գ = 1,195 10-18 մգ
Կոֆեինի երեք մոլեկուլ С8Н10O2N4 (կգ)
Պատասխան՝ 9.6610-25 կգ
Ամոնիումի կատիոն (գ)
ma=Mr(NH4+)×u = 18×1,6610-27 = 2,9910-23 գ
Անիոն SO42-(գ)
Պատասխան՝ 1,5910-22 գ.
Հեմոգլոբինի մոլեկուլներ С2954H4516N780O806S12Fe4 (մգ)
Պատասխան՝ 1,0710-16 մգ
Նատրիումի քլորիդի բանաձևի միավոր (գ)
Կալիումի հիդրօքսիդի վեց բանաձև միավոր (կգ)
Բարիումի օքսիդի երեք բանաձևային միավոր (գ)
Ծծմբի մոլեկուլի զանգվածը հավասար է թթվածնի ութ ատոմների զանգվածին։ Քանի՞ ծծմբի ատոմ կա նրա մոլեկուլում:
maO=(8×16)×1,6610-27=2,12∙10-26 գ
Եկեք պատկերացնենք մոլեկուլի բաղադրությունը որպես Sx, ապա
X = ատոմի մմոլեկուլներ = 2,12∙10-26Ar∙u = 2,12∙10-2632×1,66∙10-27 = 4 ատոմ
Քանի՞ անգամ է սախարոզայի C12H22O11 մոլեկուլի զանգվածը մեծ սպիտակ ֆոսֆորի P4 մոլեկուլի զանգվածից (պատասխան՝ 2,76 անգամ)
Մեթանի CH4-ի և թթվածնի նմուշները պարունակում են նույն թվով մոլեկուլներ: Գտե՛ք թթվածնի զանգվածի և մեթանի զանգվածի հարաբերությունը (պատասխան՝ 2)
Մագնեզիումի նմուշն ալմաստում ածխածնի ատոմների քանակով երեք անգամ ավելի է: Հաշվեք մագնեզիումի նմուշի զանգվածի հարաբերակցությունը ադամանդի նմուշի զանգվածին (պատասխան՝ 6)
II. Հաշվարկներ՝ օգտագործելով նյութի քիմիական քանակի հայեցակարգը:
Հաշվեք քիմիական քանակությունը.
Ջրածինը 3,01 1024 H2 մոլեկուլ պարունակող մասում
n (H2) =NNA=3.01∙10246.02∙1023=5 մոլ
Ազոտ 5,6 դմ3 չափաբաժինով (պատասխան՝ 0,25 մոլ)
Նատրիումի սուլֆատ 14,2 գ կշռող նմուշում (պատասխան՝ 0,1 մոլ)
Նյութի մոլեկուլի զանգվածը 1,0610-22 գ է։Հաշվե՛ք նյութի մոլային զանգվածը։
M= ma×NA=1,06∙10-22×6,02∙1023=64 գ\մոլ
Որոշեք նյութերի նշված մասերում մոլեկուլների քանակը.
3,25 մոլ O2 (պատասխան՝ 1,961024)
11,5 մոլ H2 (պատասխան՝ 6,921024)
40 մոլ NH3 (պատասխան՝ 2.411025)
0,0125 մոլ H2O (պատասխան՝ 7,521021)
Հաշվեք քիմիական քանակությունը նյութերի նշված մասերում.
3,921023 O2 մոլեկուլներ (պատասխան՝ 0,651 մոլ)
14,7 1024 արգոնի ատոմ (պատասխան՝ 24,4 մոլ)
2.451023 բանաձեւի միավորներ Na3PO4 (պատասխան՝ 0.407 մոլ)
17,34 1024 H2SO4 մոլեկուլներ (պատասխան՝ 28,8 մոլ)
Հաշվարկել քիմիական քանակությունը նյութերի նշված մասերի համար.
5,6 դմ3 հելիում (պատասխան՝ 0,25 մոլ)
1,12 dm3SO2 (պատասխան՝ 0,05 մոլ)
5 մ3 NH3 (պատասխան՝ 2,23102 մոլ)
300 սմ3 HCl (պատասխան՝ 1,3410-2 մոլ)
Որոշեք նյութերի նշված մասերի ծավալները.
3,2 մոլ H2S (դմ3) (պատասխան՝ 71,7 դմ3)
0,05 մոլ CH4 (սմ3) (պատասխան՝ 1120 սմ3)
300 մոլ O2 (մ3) (պատասխան՝ 6,72 մ3)
1,14 մոլ արգոն (դմ3) (պատասխան՝ 25,5 դմ3)
Հաշվե՛ք ազոտի 1,12 1023 մոլեկուլ պարունակող մասի ծավալը (դմ3):
n(H2) =NNA= 1.12∙10236.02∙1023=0.18 մոլ
V (H2) = 0,18×22,4 = 4 դմ3
Հաշվե՛ք թթվածնի 2 կգ մասի ծավալը (պատասխան՝ 1400 դմ3)
Հաշվե՛ք մոլեկուլների քանակը ամոնիակի 3,45 դմ3 ծավալով մասում (պատասխան՝ 9,271022)
Հաշվե՛ք 5,43 1024 մոլեկուլ պարունակող ամոնիակի մասի զանգվածը։ (պատասխան՝ 153 գ):
Բացի հիշարժան լինելուց, .com տիրույթները եզակի են. սա իր տեսակի մեջ միակ և միակ .com անվանումն է: Այլ ընդարձակումները սովորաբար ուղղակի երթևեկություն են տանում դեպի իրենց .com գործընկերները: Պրեմիում .com տիրույթի գնահատումների մասին ավելին իմանալու համար դիտեք ստորև ներկայացված տեսանյութը.
Տուրբո լիցքավորեք ձեր վեբ կայքը: Դիտեք մեր տեսանյութը՝ իմանալու համար, թե ինչպես:
Բարելավեք ձեր վեբ ներկայությունը
Ուշադրություն դարձրեք առցանց հիանալի տիրույթի անունով
Համացանցում գրանցված բոլոր տիրույթների 73%-ը .coms են: Պատճառը պարզ է. .com-ն այն վայրն է, որտեղ տեղի է ունենում վեբ տրաֆիկի մեծ մասը: Պրեմիում .com-ի սեփականատերը ձեզ մեծ առավելություններ է տալիս, ներառյալ ավելի լավ SEO-ն, անունների ճանաչումը և ձեր կայքին հեղինակության զգացում տրամադրելը:
Ահա թե ինչ են ասում մյուսները
2005 թվականից ի վեր մենք հազարավոր մարդկանց օգնել ենք ստանալ կատարյալ տիրույթի անունը
- Հեռախոսով խոսեցի Ռայանի հետ, և նա օգնեց ինձ իմ բոլոր հարցերում: Գերազանց հաճախորդների սպասարկում և մատչելի: Գործընթացը հեշտ էր և համեմատաբար արագ՝ տեղի ունենալով ընդամենը երեք աշխատանքային օրվա ընթացքում: Խիստ խորհուրդ կտայի նրանց, ովքեր մտածում են տիրույթ գնել largedomains.com-ից. Երրորդ կողմը ներգրավվում է namebright.com անունով, բայց լրացուցիչ վճար չկա, և նրանք հեշտացնում են տիրույթների փոխանցումը սերվերներից: Ողջույններ - Սեմմի Լամ, 14.10.2019թ
- Անկեղծ ասած, նախքան HugeDomains.com-ից տիրույթ գնելը, ես շատ վախեցա, քանի որ որոշ վեբկայքում կարդացի բացասական ակնարկներ, բայց որոշեցի օգտվել հնարավորությունից: Գնումից հետո ես զարմացա, անհավանական էր, որ իմ դոմենի գնումը հաջող էր, և լավագույնն այն էր, որ ես այն փոխանցեցի այլ ռեգիստրատորի և կրկին hugggggggeeee զարմացա, քանի որ իմ տիրույթի անունը փոխանցվում է 30 րոպեի ընթացքում: Գնումից մինչև փոխանցում ընդհանուր ժամանակն ավելի քիչ էր, քան 2 ժամ.... Չափից շատ շնորհակալություն HugeDomain.com-ին և NameBright.com-ին - Սանդիպ Ռաջպուտ, 14.10.2019թ
- Արագ և սահուն գործարք և փոխանցում: Կարող եք խորհուրդ տալ: - Թոմ, 12/10/2019
- Ավելին