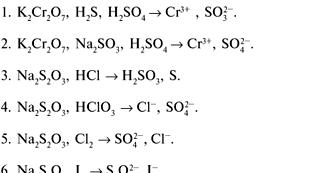យន្តការនៃការបង្កើតចំណងអុកស៊ីសែនអ៊ីយ៉ូដ។ ជំពូក III ។ ការភ្ជាប់គីមីនិងរចនាសម្ព័ន្ធម៉ូលេគុល។ និយមន័យនៃ Ionic Bond
ចំណងអ៊ីយ៉ុងលេចឡើងនៅពេលដែល electronegativity ខុសគ្នាយ៉ាងខ្លាំងពីគ្នាទៅវិញទៅមក (នៅលើមាត្រដ្ឋាន Pauling Δχ > 1.7) ហើយវាកើតឡើងកំឡុងពេលអន្តរកម្មនៃអ៊ីយ៉ុងដែលបង្កើតឡើងពីធាតុដែលត្រូវបានកំណត់ដោយលក្ខណៈគីមីខុសគ្នាខ្លាំង។
ចំណងអ៊ីយ៉ុងគឺជាការទាក់ទាញអេឡិចត្រូស្ទិករវាងអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយគ្នាដែលត្រូវបានបង្កើតឡើងជាលទ្ធផលនៃការផ្លាស់ទីលំនៅពេញលេញនៃគូអេឡិចត្រុងធម្មតាពីអាតូមនៃធាតុមួយទៅអាតូមនៃធាតុផ្សេងទៀត។
អាស្រ័យលើលក្ខណៈបុគ្គលនៃអាតូមនៃធាតុមួយចំនួន ទំនោរដែលកំពុងកើតមានគឺបាត់បង់អេឡិចត្រុង និងបំប្លែងទៅជាអ៊ីយ៉ុងដែលមានបន្ទុកវិជ្ជមាន (cations) ខណៈដែលអាតូមនៃធាតុផ្សេងទៀត ផ្ទុយទៅវិញមានទំនោរទទួលបានអេឡិចត្រុង ដោយហេតុនេះប្រែទៅជាបន្ទុកអវិជ្ជមាន។ អ៊ីយ៉ុង (anions) ដូចដែលកើតឡើងជាមួយអាតូមនៃសូដ្យូមទូទៅ និងក្លរីនដែលមិនមែនជាលោហៈធម្មតា។
គំរូតាមលក្ខខណ្ឌនៃការបង្កើតអ៊ីយ៉ុង Na + និង Cl - ដោយការផ្ទេរពេញលេញនៃអេឡិចត្រុងវ៉ាឡង់ពីអាតូមសូដ្យូមទៅអាតូមក្លរីន
សមត្ថភាពនៃធាតុដើម្បីបង្កើតអ៊ីយ៉ុងសាមញ្ញ (ដែលមកពីអាតូមតែមួយ) ត្រូវបានកំណត់ដោយការកំណត់រចនាសម្ព័ន្ធអេឡិចត្រូនិចនៃអាតូមដាច់ស្រយាលរបស់ពួកគេ ក៏ដូចជាតម្លៃនៃ electronegativity ថាមពល ionization និងទំនាក់ទំនងអេឡិចត្រុង (អប្បបរមាដែលត្រូវការដើម្បី ដកអេឡិចត្រុងចេញពីអ៊ីយ៉ុងអវិជ្ជមានដែលត្រូវគ្នានៅចម្ងាយគ្មានកំណត់)។ វាច្បាស់ណាស់ថា cations ត្រូវបានបង្កើតឡើងយ៉ាងងាយស្រួលដោយអាតូមនៃធាតុដែលមានថាមពលអ៊ីយ៉ូដទាប - លោហធាតុផែនដីអាល់កាឡាំង និងអាល់កាឡាំង (Na, K, Cs, Rb, Ca, Ba, Sr ជាដើម) ។ ការបង្កើត cations សាមញ្ញនៃធាតុផ្សេងទៀតគឺទំនងជាតិចជាង, ដោយសារតែនេះត្រូវបានផ្សារភ្ជាប់ជាមួយនឹងការចំណាយនៃថាមពលដ៏ធំសម្រាប់ ionization នៃអាតូម។
anions សាមញ្ញត្រូវបានបង្កើតឡើងយ៉ាងងាយស្រួលដោយ p-ធាតុនៃក្រុមទីប្រាំពីរ (Cl, Br, I) ដោយសារតែភាពស្និទ្ធស្នាលរបស់អេឡិចត្រុងខ្ពស់។ ការបន្ថែមអេឡិចត្រុងមួយទៅអាតូម O, S, N ត្រូវបានអមដោយការបញ្ចេញថាមពល។ ហើយការបន្ថែមអេឡិចត្រុងផ្សេងទៀតដើម្បីបង្កើតជា anions សាមញ្ញដែលមានបន្ទុកច្រើនគឺមិនអំណោយផលខ្លាំង។
ដូច្នេះសមាសធាតុដែលមានអ៊ីយ៉ុងសាមញ្ញមានតិចតួច។ ពួកវាត្រូវបានបង្កើតឡើងយ៉ាងងាយស្រួលដោយអន្តរកម្មនៃលោហៈអាល់កាឡាំងនិងអាល់កាឡាំងផែនដីជាមួយ halogens ។
លក្ខណៈពិសេសនៃការភ្ជាប់អ៊ីយ៉ុង
1. គ្មានទិសដៅ. បន្ទុកអគ្គិសនីនៃអ៊ីយ៉ុងកំណត់ការទាក់ទាញ និងការច្រានចោលរបស់ពួកគេ ហើយជាទូទៅកំណត់សមាសភាព stoichiometric នៃសមាសធាតុ។ អ៊ីយ៉ុងអាចត្រូវបានគេគិតថាជាបាល់សាកដែលវាលកម្លាំងត្រូវបានចែកចាយស្មើគ្នាគ្រប់ទិសទីក្នុងលំហ។ ដូច្នេះ ជាឧទាហរណ៍ នៅក្នុងបរិវេណ NaCl អ៊ីយ៉ុងសូដ្យូម Na+ អាចធ្វើអន្តរកម្មជាមួយអ៊ីយ៉ុងក្លរួ Cl- ក្នុងទិសដៅណាមួយ ដោយទាក់ទាញចំនួនជាក់លាក់នៃពួកវា។
Non-directionality គឺជាទ្រព្យសម្បត្តិនៃការភ្ជាប់អ៊ីយ៉ុង ដោយសារសមត្ថភាពរបស់អ៊ីយ៉ុងនីមួយៗដើម្បីទាក់ទាញអ៊ីយ៉ុងនៃសញ្ញាផ្ទុយទៅនឹងខ្លួនវាក្នុងទិសដៅណាមួយ។
ដូច្នេះការមិនតម្រង់ទិសត្រូវបានពន្យល់ដោយការពិតដែលថាវាលអគ្គីសនីនៃអ៊ីយ៉ុងមានភាពស៊ីមេទ្រីស្វ៊ែរហើយថយចុះជាមួយនឹងចម្ងាយគ្រប់ទិសដៅដូច្នេះអន្តរកម្មរវាងអ៊ីយ៉ុងកើតឡើងដោយមិនគិតពីទិសដៅ។
2. មិនឆ្អែត។វាច្បាស់ណាស់ថាអន្តរកម្មនៃអ៊ីយ៉ុងពីរនៃសញ្ញាផ្ទុយគ្នាមិនអាចនាំទៅរកសំណងទៅវិញទៅមកពេញលេញនៃវាលកម្លាំងរបស់ពួកគេ។ ដូច្នេះ អ៊ីយ៉ុងដែលមានបន្ទុកជាក់លាក់មួយរក្សាសមត្ថភាពក្នុងការទាក់ទាញអ៊ីយ៉ុងផ្សេងទៀតនៃសញ្ញាផ្ទុយនៅគ្រប់ទិសទី។ ចំនួនអ៊ីយ៉ុង "ទាក់ទាញ" បែបនេះត្រូវបានកំណត់ត្រឹមតែទំហំធរណីមាត្ររបស់ពួកគេ និងកម្លាំងរុញច្រានទៅវិញទៅមក។
ភាពមិនឆ្អែត គឺជាទ្រព្យសម្បត្តិនៃការភ្ជាប់អ៊ីយ៉ុង ដែលបង្ហាញឱ្យឃើញពីសមត្ថភាពនៃអ៊ីយ៉ុងដែលមានបន្ទុកជាក់លាក់ដើម្បីភ្ជាប់ចំនួនអ៊ីយ៉ុងនៃសញ្ញាផ្ទុយ។
3. ប៉ូលនៃអ៊ីយ៉ុង។នៅក្នុងចំណងអ៊ីយ៉ុង អ៊ីយ៉ុងនីមួយៗដែលជាអ្នកផ្ទុកបន្ទុកអគ្គិសនី គឺជាប្រភពនៃវាលអគ្គីសនីកម្លាំង ដូច្នេះនៅពេលដែលចម្ងាយរវាងអ៊ីយ៉ុងនៅជិត ពួកវាមានឥទ្ធិពលលើគ្នាទៅវិញទៅមក។
Polarization នៃអ៊ីយ៉ុងគឺជាការខូចទ្រង់ទ្រាយនៃសែលអេឡិចត្រុងរបស់វានៅក្រោមឥទ្ធិពលនៃវាលកម្លាំងអគ្គិសនីនៃអ៊ីយ៉ុងមួយផ្សេងទៀត។
4. សមត្ថភាពប៉ូឡារីស និងប៉ូឡារីសនៃអ៊ីយ៉ុង។កំឡុងពេលប៉ូល អេឡិចត្រុងនៅក្នុងស្រទាប់ខាងក្រៅត្រូវរងការផ្លាស់ទីលំនៅខ្លាំងបំផុត។ ប៉ុន្តែនៅក្រោមសកម្មភាពនៃវាលអគ្គិសនីដូចគ្នាអ៊ីយ៉ុងផ្សេងគ្នាត្រូវបានខូចទ្រង់ទ្រាយទៅដឺក្រេផ្សេងគ្នា។ អេឡិចត្រុងខាងក្រៅដែលខ្សោយជាងត្រូវបានភ្ជាប់ទៅនឹងស្នូល ប៉ូលលីសកាន់តែងាយស្រួលកើតឡើង។
Polarizability គឺជាការផ្លាស់ទីលំនៅដែលទាក់ទងនៃស្នូល និងសែលអេឡិចត្រុងនៅក្នុងអ៊ីយ៉ុងមួយ នៅពេលដែលប៉ះពាល់នឹងវាលអគ្គីសនីនៃអ៊ីយ៉ុងមួយទៀត។ សមត្ថភាពប៉ូលនៃអ៊ីយ៉ុងគឺជាសមត្ថភាពរបស់ពួកគេក្នុងការបញ្ចេញឥទ្ធិពលខូចទ្រង់ទ្រាយលើអ៊ីយ៉ុងផ្សេងទៀត។
ថាមពលប៉ូលអាស្រ័យលើបន្ទុក និងទំហំនៃអ៊ីយ៉ុង។ បន្ទុករបស់អ៊ីយ៉ុងកាន់តែធំ វាលរបស់វាកាន់តែរឹងមាំ ពោលគឺ គុណអ៊ីយ៉ុងដែលមានបន្ទុកមានសមត្ថភាពប៉ូលខ្លាំងបំផុត។
លក្ខណៈសម្បត្តិនៃសមាសធាតុអ៊ីយ៉ុង
នៅក្រោមលក្ខខណ្ឌធម្មតា សមាសធាតុអ៊ីយ៉ុងមានជាសារធាតុរឹងគ្រីស្តាល់ដែលមានចំណុចរលាយ និងរំពុះខ្ពស់ ដូច្នេះហើយត្រូវបានចាត់ទុកថាមិនងាយនឹងបង្កជាហេតុ។ ឧទាហរណ៍ ចំណុចរលាយ និងរំពុះនៃ NaCl គឺ 801 0 C និង 1413 0 C រៀងគ្នា CaF 2 - 1418 0 C និង 2533 0 C ។ ក្នុងសភាពរឹង សមាសធាតុអ៊ីយ៉ុងមិនដំណើរការទេ។ អគ្គិសនី. ពួកវារលាយខ្លាំងក្នុង និងខ្សោយ ឬមិនរលាយក្នុងទាំងអស់។ សារធាតុរំលាយដែលមិនមានប៉ូល(ប្រេងកាត ប្រេងសាំង) ។ នៅក្នុងសារធាតុរំលាយប៉ូល សមាសធាតុអ៊ីយ៉ុងបំបែក (បំបែក) ទៅជាអ៊ីយ៉ុង។ នេះត្រូវបានពន្យល់ដោយការពិតដែលថាអ៊ីយ៉ុងមានច្រើនជាងនេះ។ ថាមពលខ្ពស់។ដំណោះស្រាយដែលអាចទូទាត់សងសម្រាប់ថាមពលនៃការបំបែកទៅជាអ៊ីយ៉ុងក្នុងដំណាក់កាលឧស្ម័ន។
ប្រវែងតំណ -ចម្ងាយអន្តរនុយក្លេអ៊ែរ។ ចម្ងាយនេះកាន់តែខ្លី ចំណងគីមីកាន់តែរឹងមាំ។ ប្រវែងនៃចំណងអាស្រ័យលើកាំនៃអាតូមដែលបង្កើតវា៖ អាតូមតូចជាង ចំណងរវាងពួកវាខ្លីជាង។ ឧទាហរណ៍ប្រវែងតំណភ្ជាប់ មិនតិចជាងប្រវែងចំណង H-N (ដោយសារការផ្លាស់ប្តូរអាតូមអុកស៊ីសែនតិច) ។

ចំណងអ៊ីយ៉ុង គឺជាករណីធ្ងន់ធ្ងរនៃចំណងកូវ៉ាលេនប៉ូល
ការភ្ជាប់ដែក។
តម្រូវការជាមុនសម្រាប់ការបង្កើតប្រភេទនៃការតភ្ជាប់នេះគឺ:
1) វត្តមាននៃចំនួនតិចតួចនៃអេឡិចត្រុងនៅកម្រិតខាងក្រៅនៃអាតូម;
2) វត្តមានរបស់ទទេ (គន្លងទំនេរ) នៅលើកម្រិតខាងក្រៅនៃអាតូមដែក
3) ថាមពលអ៊ីយ៉ូដទាប។
ចូរយើងពិចារណាអំពីការបង្កើតចំណងដែកដោយប្រើសូដ្យូមជាឧទាហរណ៍។ វ៉ាឡេនអេឡិចត្រុងនៃសូដ្យូម ដែលស្ថិតនៅលើកម្រិតរង 3s អាចផ្លាស់ទីបានយ៉ាងងាយស្រួលតាមរយៈគន្លងទទេនៃស្រទាប់ខាងក្រៅ៖ តាមបណ្តោយ 3p និង 3d ។ នៅពេលដែលអាតូមចូលមកជិតគ្នាជាលទ្ធផលនៃការបង្កើតបន្ទះគ្រីស្តាល់ វ៉ាឡង់គន្លងនៃអាតូមជិតខាងត្រួតលើគ្នា ដោយសារអេឡិចត្រុងផ្លាស់ទីដោយសេរីពីគន្លងមួយទៅគន្លងមួយទៀត បង្កើតចំណងរវាងអាតូមទាំងអស់នៃគ្រីស្តាល់លោហៈ។
នៅថ្នាំងនៃបន្ទះឈើគ្រីស្តាល់ មានអ៊ីយ៉ុងដែក និងអាតូមដែលមានបន្ទុកវិជ្ជមាន ហើយរវាងពួកវាមានអេឡិចត្រុងដែលអាចផ្លាស់ទីដោយសេរីនៅទូទាំងបន្ទះគ្រីស្តាល់។ អេឡិចត្រុងទាំងនេះក្លាយជាធម្មតាចំពោះអាតូម និងអ៊ីយ៉ុងទាំងអស់នៃលោហៈ ហើយត្រូវបានគេហៅថា "ឧស្ម័នអេឡិចត្រុង" ។ ចំណងរវាងអ៊ីយ៉ុងលោហៈដែលមានបន្ទុកវិជ្ជមានទាំងអស់ និងអេឡិចត្រុងសេរីនៅក្នុងបន្ទះគ្រីស្តាល់ដែកត្រូវបានគេហៅថា ចំណងលោហៈ .
វត្តមាននៃចំណងលោហៈគឺដោយសារតែ លក្ខណៈសម្បត្តិរាងកាយលោហធាតុ និងយ៉ាន់ស្ព័រ៖ ភាពរឹង ចរន្តអគ្គិសនី ចរន្តកំដៅ ភាពបត់បែន ភាពបត់បែន ភាពរលោងនៃលោហធាតុ។ អេឡិចត្រុងឥតគិតថ្លៃអាចផ្ទុកកំដៅ និងអគ្គិសនី ដូច្នេះពួកវាជាហេតុផលសម្រាប់លក្ខណៈសម្បត្តិរូបវន្តសំខាន់ដែលបែងចែកលោហៈពីលោហៈមិនមែនលោហធាតុ - ចរន្តអគ្គិសនី និងកម្ដៅខ្ពស់។
ចំណងអ៊ីដ្រូសែន។
ចំណងអ៊ីដ្រូសែនកើតឡើងរវាងម៉ូលេគុលដែលមានអ៊ីដ្រូសែន និងអាតូមដែលមាន EO ខ្ពស់ (អុកស៊ីហ្សែន ហ្វ្លុយអូរីន អាសូត)។ មូលបត្របំណុល Covalent H-O, H-F, H-N គឺប៉ូលខ្លាំង ដោយសារតែបន្ទុកវិជ្ជមានលើសប្រមូលផ្តុំនៅលើអាតូមអ៊ីដ្រូសែន ហើយបន្ទុកអវិជ្ជមានលើសនៅលើប៉ូលទល់មុខ។ រវាងបង្គោលដែលមានបន្ទុកផ្ទុយគ្នា កម្លាំងនៃការទាក់ទាញអេឡិចត្រូស្តាតកើតឡើង - ចំណងអ៊ីដ្រូសែន។
ចំណងអ៊ីដ្រូសែនអាចជាអន្តរម៉ូលេគុល ឬអ៊ីនត្រាម៉ូលេគុល។ ថាមពលនៃចំណងអ៊ីដ្រូសែនគឺប្រហែលដប់ដងតិចជាងថាមពលនៃចំណង covalent ធម្មតា ប៉ុន្តែទោះជាយ៉ាងណាក៏ដោយ ចំណងអ៊ីដ្រូសែនដើរតួយ៉ាងសំខាន់ក្នុងដំណើរការគីមីសាស្ត្រ និងជីវសាស្ត្រជាច្រើន។ ជាពិសេស ម៉ូលេគុល DNA គឺជាបណ្តុំទ្វេ ដែលខ្សែសង្វាក់នុយក្លេអូទីតពីរត្រូវបានភ្ជាប់ដោយចំណងអ៊ីដ្រូសែន។ ចំណងអ៊ីដ្រូសែនអន្តរម៉ូលេគុលរវាងម៉ូលេគុលទឹក និងអ៊ីដ្រូសែនហ្វ្លុយអូរីត អាចត្រូវបានបង្ហាញ (ដោយចំនុច) ដូចខាងក្រោម៖

សារធាតុដែលមានចំណងអ៊ីដ្រូសែនមានបន្ទះគ្រីស្តាល់ម៉ូលេគុល។ វត្តមាននៃចំណងអ៊ីដ្រូសែននាំទៅរកការបង្កើតសហការីម៉ូលេគុល ហើយជាលទ្ធផល ការកើនឡើងនៃចំណុចរលាយ និងរំពុះ។
បន្ថែមពីលើប្រភេទសំខាន់ៗដែលបានរាយបញ្ជីនៃចំណងគីមី វាក៏មានកម្លាំងសកលនៃអន្តរកម្មរវាងម៉ូលេគុលណាមួយដែលមិននាំទៅដល់ការបំបែក ឬការបង្កើតចំណងគីមីថ្មី។ អន្តរកម្មទាំងនេះត្រូវបានគេហៅថាកងកម្លាំង van der Waals ។ ពួកវាកំណត់ការទាក់ទាញនៃម៉ូលេគុលនៃសារធាតុដែលបានផ្តល់ឱ្យ (ឬសារធាតុផ្សេងៗ) ដល់គ្នាទៅវិញទៅមកក្នុងសភាពរាវ និងរឹងនៃការប្រមូលផ្តុំ។
ប្រភេទផ្សេងៗនៃចំណងគីមីកំណត់អត្ថិភាព ប្រភេទផ្សេងៗបន្ទះឈើគ្រីស្តាល់ (តារាង) ។
សារធាតុដែលមានម៉ូលេគុលមាន រចនាសម្ព័ន្ធម៉ូលេគុល. សារធាតុទាំងនេះរួមមានឧស្ម័ន វត្ថុរាវ ក៏ដូចជាសារធាតុរឹងដែលមានបន្ទះគ្រីស្តាល់ម៉ូលេគុល ដូចជាអ៊ីយ៉ូត។ អង្គធាតុរឹងដែលមានអាតូម អ៊ីយ៉ុង ឬបន្ទះដែកមាន រចនាសម្ព័ន្ធមិនមែនម៉ូលេគុលពួកវាមិនមានម៉ូលេគុលទេ។
តុ
| លក្ខណៈពិសេសនៃបន្ទះឈើគ្រីស្តាល់ | ប្រភេទបន្ទះឈើ | |||
| ម៉ូលេគុល | អ៊ីយ៉ុង | នុយក្លេអ៊ែរ | លោហៈ | |
| ភាគល្អិតនៅថ្នាំងបន្ទះឈើ | ម៉ូលេគុល | សារធាតុ cation និង anions | អាតូម | ជាតិដែក និងអាតូម |
| ធម្មជាតិនៃការតភ្ជាប់រវាងភាគល្អិត | កម្លាំងអន្តរកម្មអន្តរម៉ូលេគុល (រួមទាំងចំណងអ៊ីដ្រូសែន) | ចំណងអ៊ីយ៉ុង | មូលបត្របំណុល Covalent | ការភ្ជាប់ដែក |
| កម្លាំងមូលបត្របំណុល | ខ្សោយ | ជាប់លាប់ | ប្រើប្រាស់បានយូរណាស់។ | ភាពខ្លាំងផ្សេងៗគ្នា |
| លក្ខណៈរូបវន្តពិសេសនៃសារធាតុ | រលាយទាបឬ sublimating, រឹងទាប, ច្រើនរលាយក្នុងទឹក | Refractory, រឹង, ផុយ, ច្រើនរលាយក្នុងទឹក។ សូលុយស្យុង និងរលាយ ធ្វើចរន្តអគ្គិសនី | refractory ខ្លាំង, រឹង, អនុវត្តមិនរលាយក្នុងទឹក។ | ចរន្តអគ្គិសនី និងកម្ដៅខ្ពស់ ភាពរលោងនៃលោហធាតុ ភាពធន់។ |
| ឧទាហរណ៍នៃសារធាតុ | សារធាតុសាមញ្ញ - មិនមែនលោហធាតុ (នៅក្នុងសភាពរឹង): Cl 2, F 2, Br 2, O 2, O 3, P 4, ស្ពាន់ធ័រ, អ៊ីយ៉ូត (លើកលែងតែស៊ីលីកុន, ពេជ្រ, ក្រាហ្វិច); សារធាតុស្មុគ្រស្មាញដែលមានអាតូមមិនមែនលោហធាតុ (លើកលែងតែអំបិលអាម៉ូញ៉ូម): ទឹក ទឹកកកស្ងួត អាសុីត ហាលីតដែលមិនមែនជាលោហធាតុៈ PCl 3, SiF 4, CBr 4, SF 6, បញ្ហាសរិរាង្គ៖ អ៊ីដ្រូកាបូន ជាតិអាល់កុល phenols aldehydes ។ល។ | អំបិល៖ សូដ្យូមក្លរួ បារីយ៉ូម នីត្រាត ជាដើម។ អាល់កាឡាំង៖ ប៉ូតាស្យូមអ៊ីដ្រូសែន កាល់ស្យូមអ៊ីដ្រូសែន អំបិលអាម៉ូញ៉ូម៖ NH 4 Cl, NH 4 NO 3 ជាដើម។ (សមាសធាតុនៃលោហធាតុដែលមិនមែនជាលោហធាតុ) | ពេជ្រ, ក្រាហ្វិច, ស៊ីលីកុន, បូរ៉ុន, ហ្រ្គេនញ៉ូម, ស៊ីលីកុនអុកស៊ីដ (IV) - ស៊ីលីកា, ស៊ីស៊ី (កាបូរុនឌុម), ផូស្វ័រខ្មៅ (ភី) ។ | ទង់ដែង ប៉ូតាស្យូម ស័ង្កសី ដែក និងលោហធាតុផ្សេងទៀត។ |
| ការប្រៀបធៀបសារធាតុដោយចំណុចរលាយ និងរំពុះ។ | ||||
| ដោយសារតែកម្លាំងអន្តរកម្មអន្តរម៉ូលេគុលខ្សោយ សារធាតុបែបនេះមានចំណុចរលាយ និងរំពុះទាបបំផុត។ លើសពីនេះទៅទៀត ទម្ងន់ម៉ូលេគុលនៃសារធាតុកាន់តែធំ t 0 pl កាន់តែខ្ពស់។ វាមាន។ ករណីលើកលែងគឺជាសារធាតុដែលម៉ូលេគុលអាចបង្កើតចំណងអ៊ីដ្រូសែន។ ឧទាហរណ៍ HF មាន t0 pl ខ្ពស់ជាង HCl ។ | សារធាតុមាន t 0 pl. ខ្ពស់ ប៉ុន្តែទាបជាងសារធាតុដែលមានបន្ទះអាតូមិក។ ការចោទប្រកាន់កាន់តែខ្ពស់នៃអ៊ីយ៉ុងដែលមានទីតាំងនៅក្នុងបន្ទះឈើ និងចម្ងាយរវាងពួកវាកាន់តែខ្លី ចំណុចរលាយនៃសារធាតុកាន់តែខ្ពស់។ ឧទាហរណ៍ t 0 pl ។ CaF 2 ខ្ពស់ជាង t 0 pl ។ ខេអេហ្វ។ | ពួកគេមាន t 0 pl ខ្ពស់បំផុត។ ចំណងរវាងអាតូមនៅក្នុងបន្ទះឈើកាន់តែរឹងមាំ t 0 pl កាន់តែខ្ពស់។ មានសារធាតុ។ ឧទាហរណ៍ Si មាន t0 pl ទាបជាង C ។ | លោហៈមាន t0 pl. ផ្សេងគ្នា: ពី -37 0 C សម្រាប់បារតដល់ 3360 0 C សម្រាប់ tungsten ។ |
ទីមួយគឺការបង្កើតចំណងអ៊ីយ៉ុង។ (ទីពីរគឺការអប់រំ ដែលនឹងត្រូវបានពិភាក្សាខាងក្រោម)។ នៅពេលដែលចំណងអ៊ីយ៉ុងត្រូវបានបង្កើតឡើង អាតូមដែកបាត់បង់អេឡិចត្រុង ហើយអាតូមមិនមែនលោហធាតុទទួលបានអេឡិចត្រុង។ ជាឧទាហរណ៍ សូមពិចារណារចនាសម្ព័ន្ធអេឡិចត្រូនិចនៃអាតូមសូដ្យូម និងក្លរីន៖
ណា ១ស ២ ២ស ២ 2 ទំ ៦ 3 ស 1 - អេឡិចត្រុងមួយនៅកម្រិតខាងក្រៅ
Cl 1s 2 2s ២ 2 ទំ ៦ 3 s ២ 3 ទំ 5 — អេឡិចត្រុងប្រាំពីរនៅកម្រិតខាងក្រៅ
ប្រសិនបើអាតូមសូដ្យូមបរិច្ចាគអេឡិចត្រុងតែ 3s របស់វាទៅអាតូមក្លរីន នោះក្បួន octet នឹងពេញចិត្តសម្រាប់អាតូមទាំងពីរ។ អាតូមក្លរីននឹងមានអេឡិចត្រុងប្រាំបីនៅលើស្រទាប់ទីបីខាងក្រៅ ហើយអាតូមសូដ្យូមក៏នឹងមានអេឡិចត្រុងប្រាំបីនៅលើស្រទាប់ទីពីរដែលឥឡូវនេះបានក្លាយជាស្រទាប់ខាងក្រៅ:
Na+1s2 ២ ស ២ 2 ទំ 6
Cl - 1s 2 2s 2 2 ទំ ៦ 3 s ២ 3 ទំ ៦ - អេឡិចត្រុងប្រាំបីនៅកម្រិតខាងក្រៅ
ក្នុងករណីនេះស្នូលនៃអាតូមសូដ្យូមនៅតែមានប្រូតុងចំនួន 11 ប៉ុន្តែ ចំនួនសរុបអេឡិចត្រុងបានថយចុះមកត្រឹម 10។ នេះមានន័យថាចំនួននៃភាគល្អិតដែលត្រូវបានចោទប្រកាន់ជាវិជ្ជមានគឺមួយច្រើនជាងចំនួននៃការចោទប្រកាន់អវិជ្ជមាន ដូច្នេះបន្ទុកសរុបនៃ "អាតូម" សូដ្យូមគឺ +1 ។
ក្លរីន "អាតូម" ឥឡូវនេះមាន 17 ប្រូតុង និង 18 អេឡិចត្រុង ហើយមានបន្ទុក -1 ។
អាតូមដែលត្រូវបានចោទប្រកាន់ដែលបង្កើតឡើងដោយការបាត់បង់ឬទទួលបានអេឡិចត្រុងមួយឬច្រើនត្រូវបានគេហៅថា អ៊ីយ៉ុង. អ៊ីយ៉ុងដែលមានបន្ទុកវិជ្ជមានត្រូវបានគេហៅថា cationsហើយការចោទប្រកាន់អវិជ្ជមានត្រូវបានគេហៅថា អ៊ីយ៉ុង.
សារធាតុអ៊ីយ៉ុង និងអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយគ្នាត្រូវបានទាក់ទាញគ្នាទៅវិញទៅមកដោយកម្លាំងអេឡិចត្រូនិក។ ការទាក់ទាញនៃអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយគ្នាត្រូវបានគេហៅថាការភ្ជាប់អ៊ីយ៉ុង។
. វាកើតឡើងនៅក្នុង សមាសធាតុដែលបង្កើតឡើងដោយលោហៈមួយ និងមិនមែនលោហធាតុមួយ ឬច្រើន។
សមាសធាតុខាងក្រោមបំពេញតាមលក្ខណៈវិនិច្ឆ័យនេះហើយមានលក្ខណៈអ៊ីយ៉ុង៖ MgCl 2, Fel 2, CuF, Na 2 0, Na 2 S0 4, Zn(C 2 H 3 0 2) ២.
មានវិធីមួយផ្សេងទៀតដើម្បីពណ៌នាសមាសធាតុអ៊ីយ៉ូដ៖
នៅក្នុងរូបមន្តទាំងនេះ ចំនុចបង្ហាញតែអេឡិចត្រុងដែលមាននៅក្នុងសំបកខាងក្រៅ ( វ៉ាឡង់អេឡិចត្រុង ) រូបមន្តបែបនេះត្រូវបានគេហៅថារូបមន្ត Lewis ក្នុងកិត្តិយសរបស់អ្នកគីមីវិទ្យាជនជាតិអាមេរិក G. N. Lewis ដែលជាស្ថាបនិកម្នាក់ (រួមជាមួយ L. Pauling) នៃទ្រឹស្តីនៃការផ្សារភ្ជាប់គីមី។
ការផ្ទេរអេឡិចត្រុងពីអាតូមលោហធាតុទៅអាតូមដែលមិនមែនជាលោហធាតុ និងការបង្កើតអ៊ីយ៉ុងគឺអាចធ្វើទៅបានដោយសារតែការពិតដែលថាមិនមែនលោហធាតុមាន electronegativity ខ្ពស់ ហើយលោហៈមាន electronegativity ទាប។
ដោយសារតែការទាក់ទាញខ្លាំងនៃអ៊ីយ៉ុងទៅគ្នាទៅវិញទៅមក សមាសធាតុអ៊ីយ៉ុងភាគច្រើនរឹង ហើយមានចំណុចរលាយខ្ពស់គួរសម។
ចំណងអ៊ីយ៉ុងត្រូវបានបង្កើតឡើងដោយការផ្ទេរអេឡិចត្រុងពីអាតូមដែកទៅអាតូមដែលមិនមែនជាលោហធាតុ។ អ៊ីយ៉ុងជាលទ្ធផលត្រូវបានទាក់ទាញគ្នាទៅវិញទៅមកដោយកម្លាំងអេឡិចត្រូស្តាត។
ចំណងអ៊ីយ៉ុង
(សម្ភារៈពីគេហទំព័រ http://www.hemi.nsu.ru/ucheb138.htm ត្រូវបានប្រើ)
ការភ្ជាប់អ៊ីយ៉ុងកើតឡើងតាមរយៈការទាក់ទាញអេឡិចត្រូស្ទិករវាងអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយគ្នា។ អ៊ីយ៉ុងទាំងនេះត្រូវបានបង្កើតឡើងជាលទ្ធផលនៃការផ្ទេរអេឡិចត្រុងពីអាតូមមួយទៅអាតូមមួយទៀត។ ចំណងអ៊ីយ៉ុងមួយត្រូវបានបង្កើតឡើងរវាងអាតូមដែលមានភាពខុសគ្នាធំនៅក្នុង electronegativity (ជាធម្មតាធំជាង 1.7 នៅលើមាត្រដ្ឋាន Pauling) ឧទាហរណ៍រវាងលោហៈអាល់កាឡាំង និងអាតូម halogen ។
ចូរយើងពិចារណាពីការកើតឡើងនៃចំណងអ៊ីយ៉ុងដោយប្រើឧទាហរណ៍នៃការបង្កើត NaCl ។
ពីរូបមន្តអេឡិចត្រូនិចនៃអាតូម
Na 1s 2 2s 2 2p 6 3s 1 និង
Cl 1s 2 2s 2 2p 6 3s 2 3p ៥
វាអាចត្រូវបានគេមើលឃើញថាដើម្បីបញ្ចប់កម្រិតខាងក្រៅ វាជាការងាយស្រួលសម្រាប់អាតូមសូដ្យូមក្នុងការបោះបង់ចោលអេឡិចត្រុងមួយជាជាងទទួលបានប្រាំពីរ ហើយសម្រាប់អាតូមក្លរីនវាងាយស្រួលក្នុងការទទួលបានអេឡិចត្រុងមួយជាជាងទទួលបានប្រាំពីរ។ នៅក្នុងប្រតិកម្មគីមី អាតូមសូដ្យូមផ្តល់ឱ្យឡើងនូវអេឡិចត្រុងមួយ ហើយអាតូមក្លរីនយកវា។ ជាលទ្ធផល សែលអេឡិចត្រុងនៃអាតូមសូដ្យូម និងក្លរីនត្រូវបានបំប្លែងទៅជាសំបកអេឡិចត្រុងដែលមានស្ថេរភាពនៃឧស្ម័នដ៏ថ្លៃថ្នូ (ការកំណត់រចនាសម្ព័ន្ធអេឡិចត្រូនិនៃស៊ីអ៊ីតសូដ្យូម
Na + 1s 2 2s 2 2p 6 ,
និងការកំណត់រចនាសម្ព័ន្ធអេឡិចត្រូនិចនៃក្លរីន anion គឺ
Cl – - 1s 2 2s 2 2p 6 3s 2 3p 6) ។
អន្តរកម្មអេឡិចត្រូស្ទិចនៃអ៊ីយ៉ុងនាំទៅរកការបង្កើតម៉ូលេគុល NaCl ។
ធម្មជាតិនៃចំណងគីមីត្រូវបានឆ្លុះបញ្ចាំងជាញឹកញាប់នៅក្នុងស្ថានភាពនៃការប្រមូលផ្តុំ និងលក្ខណៈសម្បត្តិរូបវន្តនៃសារធាតុ។ សមាសធាតុអ៊ីយ៉ុងដូចជាសូដ្យូមក្លរួ NaCl គឺរឹង និងអាចទប់ទល់បាន ពីព្រោះវាមានកម្លាំងខ្លាំងនៃការទាក់ទាញអេឡិចត្រូស្តាតរវាងការចោទប្រកាន់នៃអ៊ីយ៉ុង "+" និង "–" របស់ពួកគេ។
អ៊ីយ៉ុងក្លរីនដែលមានបន្ទុកអវិជ្ជមានទាក់ទាញមិនត្រឹមតែអ៊ីយ៉ុង Na+ របស់វាប៉ុណ្ណោះទេ ថែមទាំងអ៊ីយ៉ុងសូដ្យូមផ្សេងទៀតនៅជុំវិញវាផងដែរ។ នេះនាំឱ្យមានការពិតដែលថានៅជិតអ៊ីយ៉ុងណាមួយមិនមានអ៊ីយ៉ុងមួយដែលមានសញ្ញាផ្ទុយទេប៉ុន្តែមានច្រើន។
រចនាសម្ព័ន្ធនៃគ្រីស្តាល់នៃក្លរួ sodium NaCl ។
តាមពិតមានអ៊ីយ៉ុងសូដ្យូម 6 នៅជុំវិញអ៊ីយ៉ុងក្លរីននីមួយៗ និង 6 ក្លរីនអ៊ីយ៉ុងជុំវិញអ៊ីយ៉ុងសូដ្យូមនីមួយៗ។ ការវេចខ្ចប់អ៊ីយ៉ុងដែលបានបញ្ជាទិញនេះត្រូវបានគេហៅថាគ្រីស្តាល់អ៊ីយ៉ុង។ ប្រសិនបើអាតូមក្លរីនតែមួយត្រូវបានញែកដាច់ពីគ្នាក្នុងគ្រីស្តាល់ នោះក្នុងចំណោមអាតូមសូដ្យូមជុំវិញវា មិនអាចរកឃើញក្លរីនដែលមានប្រតិកម្មនោះទេ។
ការទាក់ទាញគ្នាទៅវិញទៅមកដោយកម្លាំងអេឡិចត្រូស្តាត អ៊ីយ៉ុងមានការស្ទាក់ស្ទើរយ៉ាងខ្លាំងក្នុងការផ្លាស់ប្តូរទីតាំងរបស់ពួកគេក្រោមឥទ្ធិពលនៃកម្លាំងខាងក្រៅ ឬការកើនឡើងនៃសីតុណ្ហភាព។ ប៉ុន្តែប្រសិនបើសូដ្យូមក្លរួត្រូវបានរលាយ ហើយបន្តត្រូវបានកំដៅក្នុងកន្លែងទំនេរ វាហួត បង្កើតជាម៉ូលេគុល NaCl diatomic ។ នេះបង្ហាញថាកម្លាំងនៃចំណង covalent មិនត្រូវបានបិទទាំងស្រុងនោះទេ។
លក្ខណៈជាមូលដ្ឋាននៃចំណងអ៊ីយ៉ុង និងលក្ខណៈសម្បត្តិនៃសមាសធាតុអ៊ីយ៉ុង
1. ចំណងអ៊ីយ៉ុង គឺជាចំណងគីមីដ៏រឹងមាំ។ ថាមពលនៃចំណងនេះគឺនៅលើលំដាប់ 300 - 700 kJ / mol ។
2. មិនដូចចំណង covalent ទេ ចំណងអ៊ីយ៉ុងគឺមិនមានទិសដៅទេ ព្រោះអ៊ីយ៉ុងអាចទាក់ទាញអ៊ីយ៉ុងនៃសញ្ញាផ្ទុយមកខ្លួនវាក្នុងទិសដៅណាមួយ។
3. មិនដូចចំណង covalent ទេ ចំណងអ៊ីយ៉ុងគឺមិនឆ្អែតទេ ចាប់តាំងពីអន្តរកម្មនៃអ៊ីយ៉ុងនៃសញ្ញាផ្ទុយគ្នាមិននាំទៅរកសំណងទៅវិញទៅមកពេញលេញនៃវាលកម្លាំងរបស់ពួកគេ។
4. ក្នុងអំឡុងពេលនៃការបង្កើតម៉ូលេគុលជាមួយនឹងចំណងអ៊ីយ៉ុង ការផ្ទេរពេញលេញនៃអេឡិចត្រុងមិនកើតឡើងទេ ដូច្នេះចំណងអ៊ីយ៉ុងមួយរយភាគរយមិនមាននៅក្នុងធម្មជាតិទេ។ នៅក្នុងម៉ូលេគុល NaCl ចំណងគីមីអ៊ីយ៉ុង 80% ប៉ុណ្ណោះ។
5. សមាសធាតុដែលមានចំណងអ៊ីយ៉ុង គឺជាសារធាតុរឹងគ្រីស្តាល់ដែលមានចំណុចរលាយ និងរំពុះខ្ពស់។
6. សមាសធាតុអ៊ីយ៉ុងភាគច្រើនគឺរលាយក្នុងទឹក។ ដំណោះស្រាយ និងការរលាយនៃសមាសធាតុអ៊ីយ៉ុងធ្វើចរន្តអគ្គិសនី។
ការភ្ជាប់ដែក
គ្រីស្តាល់លោហៈមានរចនាសម្ព័ន្ធខុសគ្នា។ ប្រសិនបើអ្នកពិនិត្យមើលដុំដែកសូដ្យូម អ្នកនឹងឃើញថារូបរាងរបស់វាខុសពីអំបិលតុ។ សូដ្យូមគឺជាលោហធាតុទន់ កាត់ដោយកាំបិតបានយ៉ាងងាយដោយញញួរ វាអាចរលាយបានយ៉ាងងាយស្រួលក្នុងពែងនៅលើចង្កៀងអាល់កុល (ចំណុចរលាយ 97.8 o C) ។ នៅក្នុងគ្រីស្តាល់សូដ្យូម អាតូមនីមួយៗត្រូវបានហ៊ុំព័ទ្ធដោយអាតូមស្រដៀងគ្នាចំនួនប្រាំបីផ្សេងទៀត។

រចនាសម្ព័ន្ធគ្រីស្តាល់នៃលោហៈ Na ។
តួរលេខបង្ហាញថា អាតូម Na នៅចំកណ្តាលគូបមានអ្នកជិតខាងចំនួន 8 ។ ប៉ុន្តែអាចនិយាយដូចគ្នាអំពីអាតូមផ្សេងទៀតនៅក្នុងគ្រីស្តាល់ ព្រោះពួកវាសុទ្ធតែដូចគ្នាទាំងអស់។ គ្រីស្តាល់មានបំណែកដដែលៗ "គ្មានកំណត់" ដែលបង្ហាញក្នុងរូបភាពនេះ។
អាតូមលោហធាតុនៅកម្រិតថាមពលខាងក្រៅមានអេឡិចត្រុង valence មួយចំនួនតូច។ ដោយសារថាមពលអ៊ីយ៉ូដនៃអាតូមដែកមានកម្រិតទាប អេឡិចត្រុង valence ត្រូវបានរក្សាខ្សោយនៅក្នុងអាតូមទាំងនេះ។ ជាលទ្ធផល អ៊ីយ៉ុងដែលមានបន្ទុកវិជ្ជមាន និងអេឡិចត្រុងសេរីលេចឡើងនៅក្នុងបន្ទះគ្រីស្តាល់នៃលោហធាតុ។ ក្នុងករណីនេះ ជាតិដែក cations ស្ថិតនៅក្នុងថ្នាំងនៃបន្ទះឈើគ្រីស្តាល់ ហើយអេឡិចត្រុងផ្លាស់ទីដោយសេរីនៅក្នុងវាលនៃមជ្ឈមណ្ឌលវិជ្ជមាន បង្កើតបានជា "ឧស្ម័នអេឡិចត្រុង" ។
វត្តមានរបស់អេឡិចត្រុងដែលមានបន្ទុកអវិជ្ជមានរវាង cations ពីរបណ្តាលឱ្យ cation នីមួយៗមានអន្តរកម្មជាមួយអេឡិចត្រុងនេះ។
ដូច្នេះ ការភ្ជាប់លោហធាតុគឺជាការផ្សារភ្ជាប់រវាងអ៊ីយ៉ុងវិជ្ជមាននៅក្នុងគ្រីស្តាល់ដែកដែលកើតឡើងតាមរយៈការទាក់ទាញនៃអេឡិចត្រុងដែលផ្លាស់ទីដោយសេរីនៅទូទាំងគ្រីស្តាល់។
ចាប់តាំងពី valence អេឡិចត្រុងនៅក្នុងលោហៈមួយត្រូវបានចែកចាយស្មើៗគ្នានៅទូទាំងគ្រីស្តាល់ ចំណងលោហធាតុ ដូចជាចំណងអ៊ីយ៉ុង គឺជាចំណងដែលមិនមានទិសដៅ។ មិនដូចចំណង covalent ទេ ចំណងលោហធាតុ គឺជាចំណងមិនឆ្អែត។ ចំណងលោហៈក៏ខុសគ្នាពីចំណង covalent នៅក្នុងកម្លាំង។ ថាមពលនៃចំណងលោហធាតុគឺប្រហែល 3 ទៅ 4 ដងតិចជាងថាមពលនៃចំណង covalent ។
ដោយសារតែការចល័តខ្ពស់នៃឧស្ម័នអេឡិចត្រុងលោហៈត្រូវបានកំណត់លក្ខណៈដោយចរន្តអគ្គិសនីនិងកំដៅខ្ពស់។
គ្រីស្តាល់លោហធាតុមើលទៅសាមញ្ញណាស់ ប៉ុន្តែតាមពិតរចនាសម្ព័ន្ធអេឡិចត្រូនិចរបស់វាស្មុគស្មាញជាងគ្រីស្តាល់អំបិលអ៊ីយ៉ុងទៅទៀត។ មិនមានអេឡិចត្រុងគ្រប់គ្រាន់នៅក្នុងសែលអេឡិចត្រុងខាងក្រៅនៃធាតុលោហធាតុដើម្បីបង្កើតជាចំណង "octet" covalent ឬ ionic bond ពេញលេញ។ ដូច្នេះនៅក្នុងស្ថានភាពឧស្ម័ន លោហធាតុភាគច្រើនមានម៉ូលេគុលម៉ូណូតូមិច (ឧទាហរណ៍ អាតូមនីមួយៗមិនភ្ជាប់គ្នា)។ ឧទាហរណ៍ធម្មតាគឺចំហាយបារត។ ដូច្នេះចំណងលោហធាតុរវាងអាតូមដែកកើតឡើងតែក្នុងសភាពរាវ និងរឹងនៃការប្រមូលផ្តុំ។
ចំណងលោហធាតុអាចត្រូវបានពិពណ៌នាដូចខាងក្រោមៈ អាតូមដែកមួយចំនួននៅក្នុងគ្រីស្តាល់លទ្ធផលបានបោះបង់ចោលអេឡិចត្រុងវ៉ាឡង់របស់ពួកគេទៅចន្លោះរវាងអាតូម (សម្រាប់សូដ្យូមនេះគឺ ... 3s1) ប្រែទៅជាអ៊ីយ៉ុង។ ដោយសារអាតូមលោហៈទាំងអស់នៅក្នុងគ្រីស្តាល់គឺដូចគ្នា នោះនីមួយៗមានឱកាសស្មើគ្នាក្នុងការបាត់បង់អេឡិចត្រុងវ៉ាឡង់។
និយាយម្យ៉ាងទៀតការផ្ទេរអេឡិចត្រុងរវាងអាតូមដែកអព្យាក្រឹតនិងអ៊ីយ៉ូដកើតឡើងដោយគ្មានការប្រើប្រាស់ថាមពល។ ក្នុងករណីនេះ អេឡិចត្រុងមួយចំនួនតែងតែស្ថិតនៅចន្លោះអាតូមក្នុងទម្រង់ជា "ឧស្ម័នអេឡិចត្រុង"។
អេឡិចត្រុងសេរីទាំងនេះ ជាដំបូង រក្សាអាតូមដែកនៅចម្ងាយលំនឹងជាក់លាក់មួយពីគ្នាទៅវិញទៅមក។
ទីពីរ ពួកវាផ្តល់ឱ្យលោហៈនូវលក្ខណៈ "ចែងចាំងនៃលោហធាតុ" (អេឡិចត្រុងសេរីអាចធ្វើអន្តរកម្មជាមួយពន្លឺ quanta)។
ទីបី អេឡិចត្រុងឥតគិតថ្លៃផ្តល់លោហៈជាមួយនឹងចរន្តអគ្គិសនីល្អ។ ចរន្តកំដៅខ្ពស់នៃលោហធាតុក៏ត្រូវបានពន្យល់ផងដែរដោយវត្តមានរបស់អេឡិចត្រុងសេរីនៅក្នុងលំហអន្តរអាតូមិក - ពួកគេងាយស្រួល "ឆ្លើយតប" ទៅនឹងការផ្លាស់ប្តូរថាមពល និងរួមចំណែកដល់ការផ្ទេរយ៉ាងលឿនរបស់វានៅក្នុងគ្រីស្តាល់។

គំរូសាមញ្ញនៃរចនាសម្ព័ន្ធអេឡិចត្រូនិចនៃគ្រីស្តាល់ដែក។
******** ដោយប្រើសូដ្យូមលោហៈជាឧទាហរណ៍ ចូរយើងពិចារណាពីធម្មជាតិនៃចំណងលោហធាតុ តាមទស្សនៈនៃគំនិតអំពីគន្លងអាតូមិក។ អាតូមសូដ្យូម ក៏ដូចជាលោហធាតុដទៃទៀតដែរ ខ្វះអេឡិចត្រុងវ៉ាឡង់ ប៉ុន្តែមានអ័រប៊ីតាល់សេរី។ អេឡិចត្រុង 3s តែមួយគត់នៃសូដ្យូម មានសមត្ថភាពផ្លាស់ទីទៅគន្លងជិតខាងដោយសេរី និងជិតដោយថាមពលណាមួយ។ នៅពេលដែលអាតូមនៅក្នុងគ្រីស្តាល់ចូលមកជិតគ្នា នោះគន្លងខាងក្រៅនៃអាតូមជិតខាងត្រួតលើគ្នា ដែលអនុញ្ញាតឱ្យអេឡិចត្រុងដែលបានផ្តល់ឱ្យឡើងដើម្បីផ្លាស់ទីដោយសេរីពេញគ្រីស្តាល់។
ទោះជាយ៉ាងណាក៏ដោយ "ឧស្ម័នអេឡិចត្រុង" មិនមានភាពច្របូកច្របល់ដូចដែលវាហាក់ដូចជា។ អេឡិចត្រុងសេរីនៅក្នុងគ្រីស្តាល់ដែកស្ថិតនៅក្នុងគន្លងត្រួតស៊ីគ្នា ហើយត្រូវបានចែករំលែកក្នុងកម្រិតមួយចំនួន បង្កើតបានជាអ្វីមួយដូចជាចំណង covalent ។ សូដ្យូម ប៉ូតាស្យូម rubidium និងធាតុលោហធាតុផ្សេងទៀតមានអេឡិចត្រុងចែករំលែកតិចតួច ដូច្នេះគ្រីស្តាល់របស់ពួកគេមានភាពផុយស្រួយ និងអាចរលាយបាន។ នៅពេលដែលចំនួនអេឡិចត្រុង valence កើនឡើង កម្លាំងនៃលោហៈជាទូទៅកើនឡើង។
ដូច្នេះ ចំណងលោហធាតុមាននិន្នាការត្រូវបានបង្កើតឡើងដោយធាតុដែលអាតូមមានអេឡិចត្រុងតិចតួចនៅក្នុងសំបកខាងក្រៅរបស់វា។ អេឡិចត្រុង valence ទាំងនេះ ដែលអនុវត្តចំណងលោហធាតុ ត្រូវបានចែករំលែកយ៉ាងច្រើន ដែលពួកគេអាចផ្លាស់ទីពេញគ្រីស្តាល់លោហៈ និងផ្តល់នូវចរន្តអគ្គិសនីខ្ពស់នៃលោហៈ។
គ្រីស្តាល់ NaCl មិនធ្វើចរន្តអគ្គិសនីទេ ពីព្រោះមិនមានអេឡិចត្រុងទំនេរនៅក្នុងចន្លោះរវាងអ៊ីយ៉ុង។ អេឡិចត្រុងទាំងអស់ដែលផ្តល់ដោយអាតូមសូដ្យូមត្រូវបានរក្សាយ៉ាងរឹងមាំដោយអ៊ីយ៉ុងក្លរីន។ នេះគឺជាភាពខុសគ្នាដ៏សំខាន់មួយរវាងគ្រីស្តាល់អ៊ីយ៉ុង និងលោហៈធាតុ។
អ្វីដែលអ្នកដឹងឥឡូវនេះអំពីការភ្ជាប់លោហធាតុ ជួយពន្យល់ពីការបត់បែនខ្ពស់ (ភាពធន់) នៃលោហៈភាគច្រើន។ លោហៈអាចត្រូវបានរុញភ្ជាប់ទៅជាសន្លឹកស្តើងហើយទាញចូលទៅក្នុងខ្សែ។ ការពិតគឺថាស្រទាប់នីមួយៗនៃអាតូមនៅក្នុងគ្រីស្តាល់លោហៈអាចរុញគ្នាទៅវិញទៅមកបានយ៉ាងងាយស្រួល: "ឧស្ម័នអេឡិចត្រុង" ចល័តធ្វើឱ្យចលនារបស់អ៊ីយ៉ុងវិជ្ជមាននីមួយៗទន់ភ្លន់ជានិច្ចដោយការពារពួកវាពីគ្នាទៅវិញទៅមក។
ជាការពិតណាស់ គ្មានអ្វីដូចនេះអាចធ្វើបានជាមួយអំបិលតុទេ ទោះបីជាអំបិលក៏ជាសារធាតុគ្រីស្តាល់ដែរ។ នៅក្នុងគ្រីស្តាល់អ៊ីយ៉ុង អេឡិចត្រុងវ៉ាឡង់ត្រូវបានចងយ៉ាងតឹងរ៉ឹងទៅនឹងស្នូលនៃអាតូម។ ការផ្លាស់ប្តូរនៃស្រទាប់មួយនៃអ៊ីយ៉ុងទាក់ទងទៅនឹងមួយផ្សេងទៀតនាំអ៊ីយ៉ុងនៃបន្ទុកដូចគ្នានៅជិតគ្នានិងបណ្តាលឱ្យមានការច្រានចោលយ៉ាងខ្លាំងរវាងពួកវាដែលបណ្តាលឱ្យមានការបំផ្លិចបំផ្លាញនៃគ្រីស្តាល់ (NaCl គឺជាសារធាតុផុយស្រួយ) ។

ការផ្លាស់ប្តូរនៃស្រទាប់នៃគ្រីស្តាល់អ៊ីយ៉ុង បណ្តាលឱ្យមានរូបរាងនៃកម្លាំងច្របូកច្របល់ដ៏ធំរវាងអ៊ីយ៉ុងដូចជា និងការបំផ្លាញគ្រីស្តាល់។
ការរុករក
- ការដោះស្រាយបញ្ហារួមបញ្ចូលគ្នាដោយផ្អែកលើលក្ខណៈបរិមាណនៃសារធាតុមួយ។
- ដោះស្រាយបញ្ហា។ ច្បាប់នៃភាពស្ថិតស្ថេរនៃសមាសធាតុនៃសារធាតុ។ ការគណនាដោយប្រើគោលគំនិតនៃ "ម៉ាស់ថ្គាម" និង "បរិមាណគីមី" នៃសារធាតុមួយ។
កម្រណាស់។ សារធាតុគីមីមានអាតូមនីមួយៗមិនទាក់ទងគ្នានៃធាតុគីមី។ នៅក្រោមលក្ខខណ្ឌធម្មតា មានតែឧស្ម័នមួយចំនួនតូចដែលហៅថា ឧស្ម័នដ៏ថ្លៃថ្នូ មានរចនាសម្ព័ន្ធនេះ៖ អេលីយ៉ូម អ៊ីយ៉ូត អាហ្គុន គ្រីបតុន ស៊ីណុន និងរ៉ាដុន។ ភាគច្រើនជាញឹកញាប់ សារធាតុគីមីមិនមានអាតូមដាច់ពីគ្នាទេ ប៉ុន្តែការរួមផ្សំរបស់វាទៅជាក្រុមផ្សេងៗ។ សមាគមអាតូមបែបនេះអាចរាប់ចំនួនអាតូមពីរបី រាប់រយ រាប់ពាន់ ឬសូម្បីតែអាតូមច្រើនទៀត។ កម្លាំងដែលផ្ទុកអាតូមទាំងនេះនៅក្នុងក្រុមបែបនេះត្រូវបានគេហៅថា ចំណងគីមី.
ម្យ៉ាងវិញទៀត យើងអាចនិយាយបានថា ចំណងគីមីគឺជាអន្តរកម្មដែលផ្តល់នូវការភ្ជាប់នៃអាតូមនីមួយៗទៅក្នុងរចនាសម្ព័ន្ធស្មុគស្មាញ (ម៉ូលេគុល អ៊ីយ៉ុង រ៉ាឌីកាល់ គ្រីស្តាល់ ។ល។)។
ហេតុផលសម្រាប់ការបង្កើតចំណងគីមីគឺថាថាមពលនៃរចនាសម្ព័ន្ធស្មុគស្មាញគឺតិចជាងថាមពលសរុបនៃអាតូមនីមួយៗដែលបង្កើតវា។
ដូច្នេះជាពិសេសប្រសិនបើអន្តរកម្មនៃអាតូម X និង Y បង្កើតម៉ូលេគុល XY នេះមានន័យថាថាមពលខាងក្នុងនៃម៉ូលេគុលនៃសារធាតុនេះគឺទាបជាងថាមពលខាងក្នុងនៃអាតូមនីមួយៗដែលវាត្រូវបានបង្កើតឡើង:
អ៊ី(XY)< E(X) + E(Y)
សម្រាប់ហេតុផលនេះ នៅពេលដែលចំណងគីមីត្រូវបានបង្កើតឡើងរវាងអាតូមនីមួយៗ ថាមពលត្រូវបានបញ្ចេញ។
អេឡិចត្រុងនៃស្រទាប់អេឡិចត្រុងខាងក្រៅដែលមានថាមពលចងទាបបំផុតជាមួយស្នូល ហៅថា valence. ឧទាហរណ៍នៅក្នុង boron ទាំងនេះគឺជាអេឡិចត្រុងនៃកម្រិតថាមពលទី 2 - 2 អេឡិចត្រុងក្នុងមួយ 2 ស-គន្លង និង ១ គុណ ២ ទំ-គន្លង៖
នៅពេលដែលចំណងគីមីត្រូវបានបង្កើតឡើង អាតូមនីមួយៗមានទំនោរទៅរកការកំណត់រចនាសម្ព័ន្ធអេឡិចត្រូនិចនៃអាតូមឧស្ម័នដ៏ថ្លៃថ្នូ ពោលគឺឧ។ ដូច្នេះមានអេឡិចត្រុង 8 នៅក្នុងស្រទាប់អេឡិចត្រុងខាងក្រៅរបស់វា (2 សម្រាប់ធាតុនៃសម័យកាលដំបូង) ។ បាតុភូតនេះត្រូវបានគេហៅថាក្បួន octet ។
វាអាចទៅរួចសម្រាប់អាតូមដើម្បីសម្រេចបាននូវការកំណត់រចនាសម្ព័ន្ធអេឡិចត្រុងនៃឧស្ម័នដ៏ថ្លៃថ្នូ ប្រសិនបើដំបូងអាតូមតែមួយចែករំលែកអេឡិចត្រុងវ៉ាឡង់ខ្លះជាមួយអាតូមផ្សេងទៀត។ ក្នុងករណីនេះគូអេឡិចត្រុងទូទៅត្រូវបានបង្កើតឡើង។
អាស្រ័យលើកម្រិតនៃការចែករំលែកអេឡិចត្រុង ចំណង covalent, ionic និង metallic អាចត្រូវបានសម្គាល់។
សម្ព័ន្ធកូវ៉ាឡង់
ចំណង Covalent ភាគច្រើនកើតឡើងរវាងអាតូមនៃធាតុមិនមែនលោហធាតុ។ ប្រសិនបើអាតូមមិនមែនលោហធាតុដែលបង្កើតជាចំណង covalent ជាកម្មសិទ្ធិរបស់ធាតុគីមីផ្សេងគ្នា ចំណងបែបនេះត្រូវបានគេហៅថា ចំណងប៉ូល័រកូវ៉ាឡង់។ ហេតុផលសម្រាប់ឈ្មោះនេះស្ថិតនៅក្នុងការពិតដែលថាអាតូម ធាតុផ្សេងគ្នាពួកគេក៏មានសមត្ថភាពខុសៗគ្នាក្នុងការទាក់ទាញគូអេឡិចត្រុងធម្មតា។ ជាក់ស្តែង នេះនាំឱ្យមានការផ្លាស់ទីលំនៅនៃគូអេឡិចត្រុងធម្មតាឆ្ពោះទៅរកអាតូមមួយ ដែលជាលទ្ធផលនៃបន្ទុកអវិជ្ជមានមួយផ្នែកត្រូវបានបង្កើតឡើងនៅលើវា។ នៅក្នុងវេន បន្ទុកវិជ្ជមានមួយផ្នែកត្រូវបានបង្កើតឡើងនៅលើអាតូមផ្សេងទៀត។ ឧទាហរណ៍ នៅក្នុងម៉ូលេគុលអ៊ីដ្រូសែនក្លរួ គូអេឡិចត្រុងត្រូវបានផ្លាស់ប្តូរពីអាតូមអ៊ីដ្រូសែនទៅអាតូមក្លរីន៖
ឧទាហរណ៍នៃសារធាតុដែលមានចំណងកូវ៉ាឡេនប៉ូល៖
CCl 4, H 2 S, CO 2, NH 3, SiO 2 ជាដើម។
ចំណងមិនប៉ូលនៃ covalent ត្រូវបានបង្កើតឡើងរវាងអាតូមដែលមិនមែនជាលោហធាតុដូចគ្នា។ ធាតុគីមី. ដោយសារអាតូមដូចគ្នាបេះបិទ សមត្ថភាពរបស់ពួកគេក្នុងការទាក់ទាញអេឡិចត្រុងរួមគ្នាក៏ដូចគ្នាដែរ។ ក្នុងន័យនេះ គ្មានការផ្លាស់ទីលំនៅរបស់គូអេឡិចត្រុងត្រូវបានគេសង្កេតឃើញទេ៖
យន្តការខាងលើសម្រាប់ការបង្កើតចំណង covalent នៅពេលដែលអាតូមទាំងពីរផ្តល់អេឡិចត្រុងដើម្បីបង្កើតជាគូអេឡិចត្រុងធម្មតា ត្រូវបានគេហៅថាការផ្លាស់ប្តូរ។
វាក៏មានយន្តការអ្នកផ្តល់ជំនួយផងដែរ។
នៅពេលដែលចំណង covalent ត្រូវបានបង្កើតឡើងដោយយន្តការអ្នកផ្តល់ជំនួយ គូអេឡិចត្រុងរួមគ្នាត្រូវបានបង្កើតឡើងដោយគន្លងពេញនៃអាតូមមួយ (ជាមួយអេឡិចត្រុងពីរ) និងគន្លងទទេនៃអាតូមមួយទៀត។ អាតូមដែលផ្តល់អេឡិចត្រុងមួយគូត្រូវបានគេហៅថា ម្ចាស់ជំនួយ ហើយអាតូមដែលមានគន្លងទំនេរត្រូវបានគេហៅថាអ្នកទទួល។ អាតូមដែលបានផ្គូផ្គងអេឡិចត្រុង ឧទាហរណ៍ N, O, P, S ដើរតួជាអ្នកផ្តល់គូអេឡិចត្រុង។
ឧទាហរណ៍ យោងទៅតាមយន្តការអ្នកផ្តល់ជំនួយ ការបង្កើតកូវ៉ាឡង់ទីបួន ការតភ្ជាប់ N-Hនៅក្នុងអាម៉ូញ៉ូម cation NH 4 +:
បន្ថែមពីលើភាពរាងប៉ូល ចំណង covalent ក៏ត្រូវបានកំណត់លក្ខណៈដោយថាមពលផងដែរ។ ថាមពលចំណងគឺជាថាមពលអប្បបរមាដែលត្រូវការដើម្បីបំបែកចំណងរវាងអាតូម។
ថាមពលភ្ជាប់ថយចុះជាមួយនឹងការកើនឡើងកាំនៃអាតូមដែលជាប់។ ដោយសារយើងដឹងថារ៉ាឌីអាតូមិកកើនឡើងជាក្រុមតូចៗ យើងអាចសន្និដ្ឋានថាកម្លាំងនៃចំណង halogen-hydrogen កើនឡើងជាស៊េរី៖
ហ៊ី< HBr < HCl < HF
ផងដែរ ថាមពលនៃចំណងអាស្រ័យទៅលើពហុគុណរបស់វា - ភាពច្រើននៃចំណង ថាមពលរបស់វាកាន់តែធំ។ Bond multiplicity សំដៅលើចំនួននៃគូអេឡិចត្រុងដែលបានចែករំលែករវាងអាតូមពីរ។
ចំណងអ៊ីយ៉ុង
ការភ្ជាប់អ៊ីយ៉ុងអាចត្រូវបានចាត់ទុកថាជាករណីធ្ងន់ធ្ងរនៃការភ្ជាប់កូវ៉ាឡង់។ ការតភ្ជាប់ប៉ូល។. ប្រសិនបើនៅក្នុងចំណង covalent-polar គូអេឡិចត្រុងធម្មតាត្រូវបានផ្លាស់ប្តូរផ្នែកខ្លះទៅអាតូមមួយគូ នោះនៅក្នុងចំណងអ៊ីយ៉ុង វាស្ទើរតែទាំងស្រុង "ផ្តល់ឱ្យ" ទៅអាតូមមួយ។ អាតូមដែលបរិច្ចាគអេឡិចត្រុង ទទួលបានបន្ទុកវិជ្ជមាន ហើយក្លាយជា cationហើយអាតូមដែលបានយកអេឡិចត្រុងពីវាទទួលបានបន្ទុកអវិជ្ជមានហើយក្លាយជា អ៊ីយ៉ុង.
ដូច្នេះ ចំណងអ៊ីយ៉ុង គឺជាចំណងដែលបង្កើតឡើងដោយការទាក់ទាញអេឡិចត្រូស្ទិកនៃ cations ទៅ anions ។
ការបង្កើតចំណងប្រភេទនេះគឺជារឿងធម្មតាក្នុងអំឡុងពេលអន្តរកម្មនៃអាតូមនៃលោហធាតុធម្មតា និងមិនមែនលោហធាតុធម្មតា។
ឧទាហរណ៍ប៉ូតាស្យូមហ្វ្លុយអូរី។ ប៉ូតាស្យូម cation ត្រូវបានបង្កើតឡើងដោយការដកអេឡិចត្រុងមួយចេញពីអាតូមអព្យាក្រឹត ហើយអ៊ីយ៉ុងហ្វ្លុយអូរីនត្រូវបានបង្កើតឡើងដោយការបន្ថែមអេឡិចត្រុងមួយទៅអាតូមហ្វ្លុយអូរីន៖

កម្លាំងទាក់ទាញអេឡិចត្រិចកើតឡើងរវាងអ៊ីយ៉ុងដែលជាលទ្ធផល បង្កើតបានជាសមាសធាតុអ៊ីយ៉ុង។
នៅពេលដែលចំណងគីមីត្រូវបានបង្កើតឡើង អេឡិចត្រុងពីអាតូមសូដ្យូមបានឆ្លងទៅអាតូមក្លរីន ហើយអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយគ្នាត្រូវបានបង្កើតឡើង ដែលមានផ្នែកខាងក្រៅពេញលេញ។ កម្រិតថាមពល.
វាត្រូវបានបង្កើតឡើងថា អេឡិចត្រុងពីអាតូមលោហៈមិនត្រូវបានផ្ដាច់ចេញទាំងស្រុងនោះទេ ប៉ុន្តែត្រូវបានផ្លាស់ប្តូរឆ្ពោះទៅរកអាតូមក្លរីនតែប៉ុណ្ណោះ ដូចជានៅក្នុងចំណងកូវ៉ាលេន។
សមាសធាតុគោលពីរភាគច្រើនដែលមានអាតូមដែកគឺអ៊ីយ៉ុង។ ឧទហរណ៍អុកស៊ីដ, halides, sulfides, nitrides ។
ការភ្ជាប់អ៊ីយ៉ុងក៏កើតឡើងរវាង cations សាមញ្ញ និង anions សាមញ្ញ (F −, Cl −, S 2-) ក៏ដូចជារវាង cations សាមញ្ញ និង anions ស្មុគស្មាញ (NO 3 −, SO 4 2-, PO 4 3-, OH −) ។ ដូច្នេះ សមាសធាតុអ៊ីយ៉ុងរួមមាន អំបិល និងមូលដ្ឋាន (Na 2 SO 4, Cu(NO 3) 2, (NH 4) 2 SO 4), Ca(OH) 2, NaOH)។
ការភ្ជាប់ដែក
ប្រភេទនៃចំណងនេះត្រូវបានបង្កើតឡើងនៅក្នុងលោហធាតុ។
អាតូមនៃលោហធាតុទាំងអស់មានអេឡិចត្រុងនៅក្នុងស្រទាប់អេឡិចត្រុងខាងក្រៅរបស់ពួកគេដែលមានថាមពលភ្ជាប់ទាបជាមួយនឹងស្នូលនៃអាតូម។ សម្រាប់លោហធាតុភាគច្រើនដំណើរការនៃការបាត់បង់អេឡិចត្រុងខាងក្រៅគឺមានភាពស្វាហាប់អំណោយផល។
ដោយសារអន្តរកម្មខ្សោយជាមួយស្នូល អេឡិចត្រុងទាំងនេះនៅក្នុងលោហធាតុគឺចល័តខ្លាំងណាស់ ហើយដំណើរការខាងក្រោមកើតឡើងជាបន្តបន្ទាប់នៅក្នុងគ្រីស្តាល់លោហៈនីមួយៗ៖
M 0 - ne - = M n + ដែល M 0 គឺជាអាតូមដែកអព្យាក្រឹត ហើយ M n + គឺជា cation នៃលោហៈដូចគ្នា។ រូបខាងក្រោមផ្តល់នូវការបង្ហាញពីដំណើរការដែលកើតឡើង។
នោះគឺអេឡិចត្រុង "ប្រញាប់" ឆ្លងកាត់គ្រីស្តាល់ដែកដោយបំបែកចេញពីអាតូមដែកមួយបង្កើត cation ពីវាភ្ជាប់ជាមួយ cation មួយទៀតបង្កើតជាអាតូមអព្យាក្រឹត។ បាតុភូតនេះត្រូវបានគេហៅថា "ខ្យល់អេឡិចត្រុង" ហើយការប្រមូលផ្តុំនៃអេឡិចត្រុងដោយឥតគិតថ្លៃនៅក្នុងគ្រីស្តាល់នៃអាតូមមិនមែនលោហធាតុត្រូវបានគេហៅថា "ឧស្ម័នអេឡិចត្រុង" ។ ប្រភេទនៃអន្តរកម្មរវាងអាតូមដែកនេះត្រូវបានគេហៅថាចំណងលោហធាតុ។
ចំណងអ៊ីដ្រូសែន
ប្រសិនបើអាតូមអ៊ីដ្រូសែននៅក្នុងសារធាតុមួយត្រូវបានផ្សារភ្ជាប់ទៅនឹងធាតុដែលមានអេឡិចត្រូណិចទ័រខ្ពស់ (អាសូត អុកស៊ីហ្សែន ឬហ្វ្លុយអូរីន) សារធាតុនោះត្រូវបានកំណត់លក្ខណៈដោយបាតុភូតហៅថាការភ្ជាប់អ៊ីដ្រូសែន។
ដោយសារអាតូមអ៊ីដ្រូសែនត្រូវបានផ្សារភ្ជាប់ទៅនឹងអាតូមអេឡិចត្រុង បន្ទុកវិជ្ជមានមួយផ្នែកត្រូវបានបង្កើតឡើងនៅលើអាតូមអ៊ីដ្រូសែន ហើយបន្ទុកអវិជ្ជមានមួយផ្នែកត្រូវបានបង្កើតឡើងនៅលើអាតូមនៃធាតុអេឡិចត្រូនិ។ ក្នុងន័យនេះ ការទាក់ទាញអេឡិចត្រូស្ទិចអាចកើតឡើងរវាងអាតូមអ៊ីដ្រូសែនដែលគិតជាវិជ្ជមានដោយផ្នែកនៃម៉ូលេគុលមួយ និងអាតូមអេឡិចត្រុងនៃមួយទៀត។ ឧទាហរណ៍ ការភ្ជាប់អ៊ីដ្រូសែនត្រូវបានសង្កេតឃើញសម្រាប់ម៉ូលេគុលទឹក៖
វាគឺជាចំណងអ៊ីដ្រូសែនដែលពន្យល់ពីចំណុចរលាយខ្ពស់មិនធម្មតានៃទឹក។ បន្ថែមពីលើទឹក ចំណងអ៊ីដ្រូសែនដ៏រឹងមាំក៏ត្រូវបានបង្កើតឡើងនៅក្នុងសារធាតុដូចជា អ៊ីដ្រូសែនហ្វ្លុយអូរី អាម៉ូញាក់ អាស៊ីតដែលមានអុកស៊ីហ្សែន ផូណុល អាល់កុល និងអាមីន។