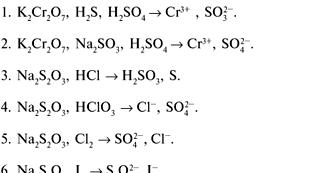Химия презентациясы. Карбон қышқылдары – презентация. Презентация на тему «карбон қышқылдары» Бір негізді карбон қышқылдары презентация
1. Карбон қышқылдарының функционалдық тобын және жалпы формуласын табыңыз.
2. Анықтаманы тұжырымдаңыз.
3. Карбон қышқылдарының жіктелуін оқып үйрену.
4. Номенклатуралық дағдыларды меңгеру.
5. Физикалық және Химиялық қасиеттеріең маңызды карбон қышқылдары.
6. Кейбір карбон қышқылдарының қолдану аймақтарын табыңыз.
Жүктеп алу:
Алдын ала қарау:
Презентацияны алдын ала қарауды пайдалану үшін Google есептік жазбасын жасаңыз және оған кіріңіз: https://accounts.google.com
Слайдтағы жазулар:
Тапсырмалар 1. Карбон қышқылдарының функционалдық тобын және жалпы формуласын табыңыз. 2. Анықтаманы тұжырымдаңыз. 3. Карбон қышқылдарының жіктелуін оқып үйрену. 4. Номенклатуралық дағдыларды меңгеру. 5. Ең маңызды карбон қышқылдарының физикалық және химиялық қасиеттерін қарастырыңыз. 6. Кейбір карбон қышқылдарының қолдану аймақтарын табыңыз.
Барлық карбон қышқылдарының функционалдық тобы бар - C OH O Карбонил тобы Гидроксил тобы Карбоксил тобы Жалпы формула R C OH O C n H 2n +1 C Немесе қаныққан бір негізді қышқылдар үшін O OH? Карбон қышқылдары қалай аталады? Карбон қышқылдары – молекулаларында көмірсутек радикалымен байланысқан карбоксил тобы, COOH бар органикалық қосылыстар. ? Карбон қышқылдарының бұрын зерттелген альдегидтер класымен генетикалық байланысы қандай? R C O H + [O] R C O OH [O]= KM nO 4, K 2 Cr 2 O 7+ H 2 SO 4 конц.
Карбон қышқылдарының жіктелуі Карбоксил топтарының санына байланысты Бір негізді Екі негізді (сірке) (оксалдық) CH 3 C C - CO OH Көп негізді (лимон) O OH O HO N 2 C - C O OH HC - C O OH H 2 C - C O OH Радикалдың табиғатына байланысты Қаныққан (пропионды) O CH 3- CH 2- C OH Қанықпаған (акрил) O CH 2 =CH-C OH Хош иісті (бензойлық) CO OH С атомдарының құрамы бойынша: C 1 -C 9 - төмен, 10 немесе одан жоғары - жоғары
Ұсынылған қышқылдарды жіктеңіз 1) C H 3 - CH 2 - CH 2 - CH 2 - COOH 2) HOOC - CH 2 - CH 2 - COOH 3) COOH 4) CH 3 - (C H 2) 7 - CH = CH - ( CH 2) 7 - COOH 5) HOOC - CH 2 - CH - CH 2 - COOH COOH CH 3 1. Бір негізді, шекті, төменгі 2. Екі негізді, шекті, төменгі 3. Бір негізді, шекті, төменгі 4. Бір негізді, қанықпаған, ең жоғары 5. .Көп негізді, соңғы, ең төменгі
КӨМІРБЕК ҚЫШҚЫЛДАРЫНЫҢ НОМЕНКЛАТУРАСЫ АЛКАН + ОН + ОН ҚЫШҚЫЛЫ МЕТАН ОН ҚЫШҚЫЛЫ (ТҰМҚЫЗДЫҚ)
CH3 – COOH 1 2 ЭТАН ҚЫШҚЫЛЫ (сірке Қышқылы) СН3 – СН2 – СН2 - СООН 1 2 3 4 БУТАН ҚЫШҚЫЛЫ (БҰТРАЛ ҚЫШЫЛЫ)
СН3 – СН2 – СН2 – СН2 – КООН ПЕНТАН ҚЫШҚЫЛЫ (ВАЛЕРИЯЛЫҚ ҚЫСҚЫЛ) 1 2 3 4 5 HOOC – COOH ЭТАН ҚЫШЫЛЫ (ҚЫЗЫЛДЫҚ ҚЫСҚЫЛ) 1 2
Карбон қышқылдарының гомологиялық қатары Химиялық формулаҚышқылдың жүйелі атауы Қышқылдың тривиальды атауы Қышқылдық қалдықтың атауы HCOO N Құмырсқа форматы CH3COO N Сірке ацетаты CH3CH2COO N CH3CH2CH2COO кезіндегі пропионды пропион N CH3CH2CH2CH2COO кезіндегі бутират N CH3-(COCHN3-тегі) валерик валерин CH3-(COCHN2) Capron (CH2 )8 – COO N CH3-(CH2) 14 – COO N пальмитикалық пальмитат CH3-(CH2)16- COO N Стеарикалық стеарат Метан этан пропан бутан пентан гексан декан гексадекан октадекан
Карбон қышқылдарын атау алгоритмі: 1. Көміртек атомдарының негізгі тізбегін тауып, оны карбоксил тобынан бастап нөмірлейміз. 2. Орынбасарлардың орнын және олардың атын (аттарын) көрсетеміз. 3. Тізбектегі көміртегі атомдарының санын білдіретін түбірден кейін «-ic» қышқылы жұрнағы келеді. 4. Егер бірнеше карбоксил топтары болса, онда «- ova» (-ди, - үш...) алдына сан қойылады Мысал: 3-метилбутан + -ова = 3-метилбутан қышқылы
ЗАТТАРДЫҢ ХАЛЫҚАРАЛЫҚ НОМЕНКЛАТУРАСЫ БОЙЫНША АТАУЫН ДЕҢІЗ (2 – метилпропан қышқылы) CH3 – CH – COOH 2. CH3 – CH2 – CH – CH – COOH 3. CH3 – CH = CH – CH – HOOS 42. – CH – COOH (2, 3 – диметил пентан қышқылы) (2 – МЕТИЛПЕНТЕН – 3 – IC қышқылы) (2 – ЭТИЛБУТАН ҚЫШЫЛЫ) СН3 СН3 СН3 СН3 С 2 Н 5
: 1. Құрамында карбоксил тобы бар көміртек қаңқасын жазып алатын сөздің түбірін таңдаңыз. 2. Көміртек атомдарын карбоксил тобынан бастап нөмірлейміз. 3. Орынбасарларды нөмірлеуге сәйкес көрсетеміз. 4. Жетіспейтін сутегі атомдарын қосу керек (көміртек төрт валентті). 5. Формуланың дұрыс жазылғанын тексеріңіз. 2-метилбутан қышқылы. Мысалы: Карбон қышқылдарының формулаларын жазу алгоритмі
ФИЗИКАЛЫҚ ҚАСИЕТТЕР C 1 – C 3 Өзіне тән өткір иісі бар сұйықтықтар, суда жақсы ериді C 4 – C 9 Жағымсыз иісі бар тұтқыр майлы сұйықтықтар, суда нашар ериді C 10 және одан да көп Иіссіз қатты заттар, суда ерімейді.
Физикалық күйі сұйық Түсі түссіз мөлдір сұйықтық Иісі өткір сірке суда ерігіштігі жақсы Қайнау температурасы 118 º C Балқу температурасы 17 º С Сірке қышқылының физикалық қасиеттері:
Төменгі карбон қышқылдары сұйық болып табылады; жоғары – қатты заттар қышқылдың салыстырмалы молекулалық салмағы неғұрлым көп болса, оның иісі де аз болады. Туыстық ұлғаюымен молекулалық салмаққышқылдың ерігіштігі тәуелділікті төмендетеді физикалық қасиеттерімолекуланың құрылымындағы карбон қышқылдары: Альдегидтердің гомологиялық қатары екі газ тәрізді заттардан басталады (бөлме температурасында), ал карбон қышқылдарының арасында газдар болмайды. Бұл немен байланысты?
Карбон қышқылдарының химиялық қасиеттері I. Бейорганикалық қышқылдармен ортақ Еритін карбон қышқылдары сулы ерітінділерде диссоциацияланады: CH 3 – COOH CH 3 – COO + H + Орта қышқылды ма? Индикаторлардың түсі қалай өзгереді қышқыл орта? Лакмус (күлгін) - қызыл түске боялады Метил-апельсин - қызғылт түске боялады Фенофталеин - түсін өзгертпейді 2. Электрохимиялық кернеу қатарындағы металдармен сутегіге дейін әрекеттесу: 2CH 3 - COOH + M г Сірке қышқылы (CH 3 -COO) 2 М г. Магний ацетаты + H 2 2CH 3 - COOH + Zn Сірке қышқылы (CH 3 –COO) 2 Zn Мырыш ацетаты + H 2 Металл карбон қышқылы ерітіндісімен әрекеттескенде сутегі мен тұз түзіледі.
3. Негізгі оксидтермен әрекеттесу: 2 CH 3 – COOH + C u O Сірке қышқылы t (CH 3 – COO) 2 C u Мыс ацетаты + H 2 O 4. Металл гидроксидтерімен әрекеттесу (бейтараптандыру реакциясы) CH 3 – COOH + H O – Na Сірке қышқылы CH 3 COO Na Натрий ацетаты + H 2 O 5. Әлсіз және ұшқыш қышқылдардың тұздарымен әрекеттесуі (мысалы, көміртегі, кремний, күкіртсутек, стеарин, пальмитин...) 2CH 3 – COOH Сірке қышқылы + Na 2 CO 3 натрий карбонаты 2CH 3 COO Na Натрий ацетаты + H 2 CO 3 CO 2 H 2 O 2 CH3 – COOH + Cu(OH) 2 Сірке қышқылы (CH3COO) 2 Cu Мыс ацетаты + H2O
Құмырсқа қышқылының ерекше қасиеттері «Күміс айна» реакциясы H- CO OH + Ag 2 O t 2Ag + H 2 CO 3 CO 2 H 2 O Құмырсқа қышқылы Күміс оксиді күміс
Табиғатта пайда болуы және карбон қышқылдарының қолданылуы Құмырсқа қышқылы (метан қышқылы) - Химиялық формуласы CH2O2, немесе HCOOH. - Құмырсқа қышқылын 1670 жылы ағылшын табиғат зерттеушісі Джон Рэй ашқан. Құмырсқа қышқылы сонымен қатар қалақайдың ең жақсы түктерінде, ара уында, қарағай инелерінде және т.б. үлкен мөлшерлерәртүрлі жемістерде, ұлпаларда, органдарда, жануарлар мен адамның секрецияларында кездеседі.
Сұрақ: Неліктен құмырсқа шаққан жерді немесе қалақай шаққанда сумен сулауға болмайды? Бұл тек ауырсынудың күшеюіне әкеледі. Жараланған жер аммиакпен суланған болса, ауырсыну неге басылады? Бұл жағдайда тағы не қолдануға болады? Құмырсқа қышқылы суда еріген кезде процесс жүреді электролиттік диссоциация: HCOOH HCOO + H Нәтижесінде қоршаған ортаның қышқылдығы артып, терінің коррозия процесі күшейеді. Ауырсынуды азайту үшін қышқылды бейтараптандыру керек, ол үшін сілтілі реакциясы бар ерітінділерді, мысалы, аммиак ерітіндісін пайдалану керек. HCOOH + N H4OH HCOO NH4 + H2O немесе HCOOH + NaHCO3 HCOO Na + CO2 + H2O
Сірке қышқылы (этан қышқылы) Бұл адам алған және қолданған бірінші қышқыл. 4 мың жылдан астам уақыт бұрын «туылған». Ежелгі Египет. 17-18 ғасырлар тоғысында Ресейде ол «қышқыл ылғал» деп аталды. Біз оны бірінші рет шарап ашыту кезінде алғанбыз. Латынша атауы - Acetum acidum, сондықтан тұздардың атауы - ацетаттар. Мұзды сірке қышқылы 16,8 ºС төмен температурада қатып, мұз тәрізді болады - Сірке эссенциясы - 70% қышқыл ерітіндісі. - асханалық сірке суы - 6% немесе 9% қышқыл ерітіндісі. Сірке қышқылы - жануарлардың секрецияларында (зәрде, өтте, нәжісте), өсімдіктерде (атап айтқанда, жасыл жапырақтарда), қышқыл сүтте және ірімшікте болады; - шарап пен сыраны ашыту, шіру, қышқылдау, көптеген тотығу кезінде түзіледі органикалық заттар;
Сірке қышқылының қолданылуы - Сірке қышқылының судағы ерітінділері тамақ өнеркәсібінде кеңінен қолданылады ( тағамдық қосымшаЕ-260) және тұрмыстық аспаздық, сондай-ақ консервілеуде; өндірісінде: препараттар, мысалы, аспирин; жасанды талшықтар, мысалы, жібек ацетаты; индиго бояғыштары, жанбайтын пленка, органикалық шыны; лак еріткіштері; өсімдіктерді қорғаудың химиялық құралдары, өсімдіктердің өсу стимуляторлары; Натрий ацетаты CH3COO N a трансфузияға арналған қанға арналған консервант ретінде қолданылады; Калий ацетаты CH3COOK – диуретик ретінде; Қорғасын ацетаты (CH3COO) 2 Pb – зәрдегі қантты анықтау үшін; Тоқыма өнеркәсібінде морданды бояу үшін темір (III) (CH3COO)3Fe, алюминий (CH3COO) 3Al және хром (III) (CH3COO) 3Cr ацетаттары қолданылады; Мыс (II) ацетаты (CH3COO) 2 C u Париж жасылы деп аталатын өсімдік зиянкестерімен күресуге арналған препараттың бөлігі болып табылады;
Сірке қышқылын қолдану Косметологияда алкогольді сірке суын қолдану белгілі. Атап айтқанда, пермь және тұрақты бояудан кейін шашқа жұмсақтық пен жылтыр беру. Ол үшін шашыңызды спирттік сірке суын (1 литр суға 3-4 ас қасық сірке суы) қосып жылы сумен шаю ұсынылады. Халықтық медицинада сірке суын спецификалық емес антипиретик ретінде қолданады. лосьондарды қолдану арқылы бас ауруы үшін. компресстерді қолдану арқылы жәндіктердің шағуы үшін. парфюмерия өнімдерін өндіруде таптырмайтын нәрсе Сіз білесіз бе - Тот басқан гайканы бұрап алу қажет болса, кешке сірке қышқылына малынған шүберек қою ұсынылады? Таңертең бұл гайканы бұрап алу әлдеқайда оңай болады. -Тәулік ішінде организмде 400 г сірке қышқылы түзіледі? Бұл 8 литр кәдімгі сірке суын алу үшін жеткілікті болады
Барлық қышқылдардың ішінде бұл, әрине, прима. Барлық жерде көрінетін және көрінбейтін түрде көрсетіңіз. Ол жануарлар мен өсімдіктерде бар, Техника мен медицина онымен мәңгі. Оның ұрпақтары - ацетаттар - өте қажет «жігіттер». Белгілі аспирин, жақсы джентльмен сияқты, науқастың қызуын төмендетеді және денсаулығын қалпына келтіреді. Бұл мыс ацетаты. Өсімдіктерге дос, ағайын, Дұшпанды өлтіреді. Қышқылдың әлі де біраз пайдасы бар - ол бізді ацетатты жібекпен киеді. Ал тұшпараны жақсы көретін адам сірке суын бұрыннан біледі. Кино туралы да сұрақ бар: Ацетат пленкасы болмаса, киноны көре алмайтынымызды бәрі білуі керек. Әрине, басқа да қолданулар бар. Және сіз оларды күмәнсіз білесіз. Бірақ, ең бастысы, достар, «Өнеркәсіптің наны» - сірке қышқылы. CH 3 COOH CH3COOH Мыс ацетатының сулы ерітіндісі
Лимон қышқылы COOH HOOC – CH 2 – C – CH 2 – COOH OH Қымыздық қышқылы HOOC –– COOH Құмырсқа қышқылы H –– COOH Ацетилсалицил қышқылы COOH OCOCH 3 Тартар қышқылы HOOC – CH - CH –– COOH OH OH Сүт қышқылы CH 3 - CH –– COOH OH Алма қышқылы HOOC – CH - CH 2 –– COOH OH янтар қышқылы HOOC – CH 2 - CH 2 –– COOH Бензой қышқылы COOH аскорбин қышқылы HO OH H =O HOH 2 C-NONS O Сірке қышқылы H 3 C – – COOH карбон қышқылдары қышқылдықты жоғарылату ретімен
Қорытынды 1. Карбон қышқылдары – молекулаларында көмірсутек радикалымен байланысқан карбоксил тобы – СООН болатын органикалық қосылыстар. 2.Карбон қышқылдары: негізділігі бойынша (моно, екі және көп негізді) көмірсутек радикалы бойынша (қаныққан, қанықпаған және ароматты) С атомдарының мөлшері бойынша (төменгі және жоғары) 3. Карбон қышқылының атауы мынадан тұрады: алканның аты + аналық қышқыл. 4. Карбон қышқылының молекулалық массасы артқан сайын қышқылдың ерігіштігі мен күші төмендейді. 5. Бейорганикалық қышқылдар сияқты еритін карбон қышқылдары да сулы ерітіндіде диссоциацияланып, сутегі иондарын түзеді және индикатор түсін өзгертеді. Олар металдармен (Н-ге дейін), негіздік және амфотерлі оксидтермен және гидроксидтермен, әлсіз қышқылдардың тұздарымен әрекеттесіп, тұздар түзеді. 6 Табиғатта кең таралған және адамдар үшін үлкен практикалық маңызы бар.
Үйге тапсырма § 14, No6 жаттығу No9 жаттығу Королева Клеопатра сарай дәрігерінің кеңесі бойынша зергерлерге белгілі ең үлкен інжу-маржанды сірке суында ерітіп, содан кейін алынған ерітіндіні біраз уақыт қабылдады. Клеопатра қандай реакция жасады? Ол қандай байланыс жасады? 3. Жоғары карбон қышқылдары туралы есеп дайындаңыз
назарларыңызға рахмет
Карбон қышқылдары
Слайдтар: 41 Сөздер: 1295 Дыбыстар: 24 Әсерлер: 62Карбон қышқылдары. Барлық карбон қышқылдарының функционалдық тобы бар. Карбон қышқылдары қалай аталады? Өзін-өзі бақылау тапсырмасы. Карбон қышқылдарының номенклатурасы. Табиғаттағы карбон қышқылдары. Карбон қышқылдарының жалпы формуласы. Карбоксил тобының құрылысы. Карбон қышқылдарының физикалық қасиеттері. Қаныққан карбон қышқылдарының физикалық қасиеттері. Карбон қышқылдарының химиялық қасиеттері. Галогендермен әрекеттесу. Карбон қышқылдарын алу. Карбон қышқылының молекулалары димерлерді түзеді. Карбон қышқылдарын анықтауды қайталаңыз. Номенклатура күрделі эфирлер. Табиғаттағы эфирлер. Мыс ацетаты. - Қышқылдар 1.ppt
Карбон қышқылдарының әрекеттесуі
Слайд: 14 Сөз: 359 Дыбыс: 0 Әсер: 0Карбон қышқылдары. Қаныққан бір негізді карбон қышқылдарының құрамы O R – C OH жалпы формуласына сәйкес келеді. Классификация. Қышқылдарға мысалдар. Изомерия. Құрылым. Физикалық және химиялық қасиеттері. Төменгі карбон қышқылдары суда жақсы еритін өткір иісі бар сұйықтықтар. CH3COOH + SOCl2 CH3COCl + HCl + SO2. Алу әдістері. 4. Күрделі эфирлердің гидролизі: 5. Қышқыл ангидридтерінің гидролизі: алудың ерекше әдістері. Жеке қышқылдар үшін арнайы дайындау әдістері бар: Карбон қышқылдарын қолдану. Желім. Гербицидтер. Консервант, дәмдеуіш. Парфюмерия, косметика. - карбон қышқылдары.ppt
Карбон қышқылдарының қасиеттері
Слайдтар: 21 Сөздер: 424 Дыбыстар: 0 Әсерлер: 96Карбон қышқылдары. Органикалық химия 11-сынып. – COOH карбоксил тобы. Метандиой қышқылы (дикарбон қышқылы). 2-гидроксипропанетр қышқылы (2-гидрокси-1,2,3-пропанетрикарбон қышқылы). Физикалық қасиеттері. Молекуланың поляризациясы. Сутектік байланыстардың түзілу мүмкіндігі. Жоғары қайнау нүктелері. Сірке қышқылының димері. Суда ерігіштігі. Карбоксил тобының құрылысы. Радикалдар. Нуклеофильдер. Электрофильдер. Химиялық қасиеттері. Олар қышқылдардың жалпы қасиеттерін көрсетеді. Карбон қышқылы. Магний карбоксилаты. Этан қышқылы. Магний этанаты. Кальций этаты. Натрий метан. - карбон қышқылдары 1.ppt
Табиғаттағы карбон қышқылдары
Слайд: 20 Сөз: 379 Дыбыс: 0 Әсер: 0Карбон қышқылдары. Кейбір қарапайым қышқылдардың формулалары мен атаулары. Қышқыл қалдықтарының формулалары мен атаулары. Төменгі карбон қышқылдары. - өткір иісі бар түссіз сұйықтықтар. Молярлық масса ұлғайған сайын қайнау температурасы артады. ...Табиғаттағы карбон қышқылдары: C2H5COOH – ағаш шайыры. C3H7COOH – сары май. C4H9COOH – валериандық шөптің тамыры. C6H5COOH – қалампыр майы. Ең қарапайым карбон қышқылдары. Назар аударыңыз... HCOOH қышқылы альдегидтер сияқты «күміс айна» реакциясына түседі: Ал суды кетіретін заттардың әсерінен ыдырайды: Карбон қышқылдарын алу. - карбон қышқылдары 2.ppt
Карбон қышқылы
Слайд: 9 Сөз: 193 Дыбыс: 0 Әсер: 0Тұсаукесер. Карбон қышқылдары. Сабақтың мақсаты. Халықаралық және тривиальды номенклатуралардың негіздерін, карбон қышқылдарын пайдалануды қарастырыңыз. Карбоксил тобының құрылымын талдаңыз және карбон қышқылдарының химиялық әрекетін болжаңыз. Карбон қышқылдарының классификациясы. Карбоксил топтарының саны бойынша. Шексіз. Хош иісті. Бір негізді. Екі негізді. Көп негізді. Шектеу. Көмірсутек радикалының түріне қарай. Шектеу қатарындағы бір негізді қышқылдардың жалпы формуласы. CnH2n+1COOH мұндағы n нөл болуы мүмкін. Ең қарапайым карбон қышқылдары. Кейбір карбон қышқылдарының формулалары мен атаулары. - карбон қышқылдары 3.ppt
Көмірқышқылдары
Слайд: 14 Сөз: 889 Дыбыс: 0 Әсер: 0Карбон қышқылдары. Құрылым. Молекуласында бір карбоксил тобы бар органикалық қышқылдар бір негізді. Құрамында екі карбоксил тобы бар карбон қышқылдары екі негізді деп аталады. Қымыздық қышқылы. Қаныққан (немесе қаныққан) карбон қышқылдарының құрамында көмірсутек радикалында α-байланыстар болмайды. Мысалы, бензой қышқылы: Номенклатурасы және изомериясы. Көміртек атомдарының нөмірленуі карбоксил тобынан басталады. Метан (құмырсқа) қышқылы. Этандион (қымыздық) қышқылы. Қаныққан бір негізді карбон қышқылдарының физикалық қасиеттері. Химиялық қасиеттері. - карбон қышқылдары 4.ppt
Қанықпаған карбон қышқылдары
Слайдтар: 11 Сөздер: 305 Дыбыстар: 0 Әсерлер: 37Қанықпаған карбон қышқылдары. Физикалық қасиеттері. Изомерия. Алу әдістері. Химиялық қасиеттері. Биологиялық құрылымы. Қолдану. Акрил қышқылы. Метакрил қышқылы. CH2=CH-coon. CH2=c-coon. CH3. Олеин қышқылы. CH3 – (CH2)7-CH=CH-(CH2)7 -coon. Линол қышқылы. CH3-(CH2)4-CH=CH-CH2-CH=CH-(CH2)7-coon. Линолен қышқылы. CH3-SN2-CH=CH-CH2-CH=CH-CH2-CH=CH-(CH2)7-coon. Қанықпаған карбон қышқылдарының изомериясы. Көміртек тізбегі. Қосарлы байланыс позициялары. Геометриялық (цис-транс изомериясы). Олеин қышқылының геометриялық изомерлері. Азот оксидтері. Элаид қышқылы. - карбон қышқылдары 5.ppt
Сірке және стеарин қышқылдары
Слайд: 14 Сөз: 236 Дыбыс: 0 Әсер: 09-сынып 6-сабақ.Карбон қышқылдары. Сабақ жоспары. Карбон қышқылдары туралы түсінік. Сірке қышқылы. Стеарин қышқылы. Сұрақтар мен жаттығулар. 1. Карбон қышқылдары туралы түсінік. Карбоксил тобының құрылымдық формуласы: O C O H. -Coon. Карбон қышқылы. Карбоксилат анионы. Карбон қышқылдарының арасында көптеген танымал «адамдар» бар. Қышқылдарда карбоксил топтары бар, бірақ мұндағы барлық қышқылдар күшті емес. 2. Сірке қышқылы. Сірке қышқылы CH3COOH органикалық қышқылдардың ең көнесі. Таза сірке қышқылы - өткір иісі бар түсті сұйықтық. Сірке қышқылы химия өнеркәсібінде көп мөлшерде қолданылады. - карбон қышқылдары 6.ppt
Карбон қышқылдарының химиясы
Слайд: 14 Сөз: 341 Дыбыс: 0 Әсер: 0Карбон қышқылдары. Дәріс. 1. Қышқылдарды анықтау. 2. Гомологиялық қатар. Ең қарапайым өкілдері қаныққан бір негізді карбон қышқылдары. Бір функционалды карбоксил тобын құрайтын карбонил және гидроксил топтары. Карбон қышқылдарының қасиеттері олардың қолжетімділігіне байланысты. Ауыстыру 2-ші көміртегі атомында жүреді және катализаторда жүреді. Бұл реакция аминқышқылдарын өндіру үшін аралық болып табылады. Қышқылдардың карбон тобы. Альдегидтер тобы. Олеин қышқылы. 9,10 – дибромостеар қышқылы. Олеин қышқылы жоғары қанықпаған карбон қышқылдарына жатады. - карбон қышқылдары chemistry.ppt
Карбон қышқылдарының кластары
Слайдтар: 33 Сөздер: 809 Дыбыстар: 0 Әсерлер: 13Құрамында оттегі бар органикалық қосылыстар. Карбон қышқылдары. Карбон қышқылдарын алу. Жалпы формула. Анықтама. Карбон қышқылдарының классификациясы. Көмірсутек радикалының табиғаты бойынша карбон қышқылдарының жіктелуі. Карбон қышқылдарының функционалдық топтар саны бойынша жіктелуі. Бір негізді карбон қышқылдарының өкілдері. Қышқылдардың гомологиялық қатары. Карбон қышқылдарының номенклатурасы. Карбон қышқылдарының изомериясы. Карбон қышқылдарының физикалық қасиеттері. Карбон қышқылдарының қолданылуы. Өндіріс органикалық қосылыстар. Метилбутан қышқылы. Функционалды топ. - карбон қышқылдарының кластары.ppt
Карбон қышқылдарының мысалдары
Слайдтар: 15 Сөздер: 563 Дыбыстар: 0 Әсерлер: 10Карбон қышқылдары. Құрылымын зерттеңіз. Бұл органикалық заттар. Валерий қышқылы. Көрсеткіш. Құмырсқа қышқылы. Карбон қышқылдарының классификациясы. Қымыздық қышқылы. Лимон қышқылы. Сірке қышқылы. Карбон қышқылдарының химиялық қасиеттері. Олар эфирлер түзеді. Стеарин қышқылы. Қышқылдар. - карбон қышқылдарының мысалдары.ppt
Карбон қышқылдарының қасиеттері
Слайд: 24 Сөз: 328 Дыбыс: 0 Әсер: 0Химия сабағын дамыту. Функционалдық топ туралы түсінік. Бәлкім, қолымнан келеді деп ойлайтын адам шығар. Органикалық заттардың жаңа класына сипаттама беріңіз. Қышқыл. Қышқылдық қасиеттері. Карбоксил тобы. Бір негізді карбон қышқылдары. Органикалық заттар. Сипаттама жоспары. Карбон қышқылдары. Классификация. Құрылымдық изомерия. Физикалық қасиеттері. Димер құрылымы. Электрондық ығысу. Химиялық қасиеттері. Сулы ерітіндідегі диссоциация. Қасиеттер. - карбон қышқылдарының қасиеттері.ppt
Карбон қышқылдары және олардың қасиеттері
Слайдтар: 28 Сөздер: 1463 Дыбыстар: 0 Әсерлер: 65Карбон қышқылдары. Қышқылдардың ашылуы. Органикалық қышқылдарға қатысты қызықты тарихи деректер. Құрамында құмырсқа қышқылы бар қалақай. Табиғаттағы карбон қышқылдары. Құмырсқа қышқылы алғаш рет 17 ғасырда бөлініп алынды. Сірке қышқылы табиғатта кең таралған. Органикалық заттар. R-COOH. Карбон қышқылдарының номенклатурасы. Классификация. Дикарбон қышқылдары. Карбон қышқылдарын атау алгоритмі. Карбон қышқылдарының формулаларын жазу алгоритмі. Заттың атын атаңыз. Этан қышқылы немесе сірке қышқылы. Хлорсірке қышқылы немесе хлорэтан қышқылы. Қай қышқыл күштірек? - Карбон қышқылдары және олардың қасиеттері.pptx
Карбон қышқылдарының химиялық қасиеттері
Слайдтар: 17 Сөздер: 666 Дыбыстар: 0 Әсерлер: 25Карбон қышқылдарының химиялық қасиеттері. Білімге жол. Химиялық қасиеттері. Функционалды топ. Карбон қышқылдарының формулалары. Карбон қышқылдарының атауы. Карбон қышқылдарының тривиальды атаулары. Карбоксил тобының құрылысы. Құмырсқа қышқылы. Салицил қышқылы. Қымыздық қышқылы. Бейорганикалық қышқылдардың химиялық қасиеттері. Карбон қышқылдарының жалпы қасиеттері. Карбон қышқылдары. Тапсырма. - карбон қышқылдарының химиялық қасиеттері.ppt
Карбон қышқылының туындылары
Слайдтар: 19 Сөздер: 412 Дыбыстар: 0 Әсерлер: 127Карбон қышқылдарының функционалды туындылары. Карбоксил. Кетон. Карбон қышқылдарын алмастыратын өнімдер. Күрделі эфирлер. Эстерификация. Метан (құмырсқа) қышқылы. Амидтер. Метанамид. Күрделі эфирлер мен амидтердің химиялық қасиеттері. Қышқылдық гидролиз. Қайтымды процесс. Катализатор. Амидтердің гидролизі. Нуклеофильді қалдыру. Күрделі эфирлердің гидролизі. Минералды қышқылдардың күрделі эфирлері. Күкірт қышқылының күрделі эфирлері. Фосфор қышқылының күрделі эфирлері. - карбон қышқылдарының туындылары.ppt
Қаныққан карбон қышқылдары
Слайд: 41 Сөз: 1517 Дыбыс: 24 Әсер: 62Бір негізді карбон қышқылдарының құрылысы. Карбон қышқылдары. Барлық карбон қышқылдарының функционалдық тобы бар. Өзін-өзі бақылау тапсырмасы. Тривиальды атаулар. Гомологиялық қатар. Физикалық қасиеттері. Карбон қышқылдарының химиялық қасиеттері. Негізгі оксидтермен әрекеттеседі. Осы қышқылдардың қайсысы күштірек? Карбон қышқылдарын алу. Этан. Анықтама. Органикалық заттар. Карбон қышқылының формуласын таңдаңыз. Карбон қышқылдарын анықтауды қайталаңыз. Теория. Күрделі эфирлердің номенклатурасы. Изобутилацетат. Карбон қышқылдарын атаңдар. Диметилгексан қышқылы. Мыс ацетаты. - Қаныққан карбон қышқылдары.ppt
Қаныққан бір негізді карбон қышқылдары
Слайдтар: 13 Сөздер: 764 Дыбыстар: 1 Әсерлер: 20Қаныққан карбон қышқылдарының құрылымы мен номенклатурасы. Қаныққан бір негізді карбон қышқылдары. Карбон қышқылдары. Изомерия түрлері. Көміртек атомы. Карбон қышқылдарын атаңдар. Тривиальды атаулар. Бір негізді карбон қышқылдары. Физикалық қасиеттері. Ашылу тарихы. Құмырсқа қышқылы. Газ тәрізді заттар. Органикалық заттар. - Бір негізді карбон қышқылдарын шектеңіз.ppt
Май қышқылы
Слайдтар: 44 Сөз: 2065 Дыбыстар: 0 Әсерлер: 0Полиқанықпаған май қышқылдары сигналдық молекулалар ретінде. 1. Липидомика және липидология. Классикалық парадигма: Постгеномдық дәуір парадигмасы: Липидомикаға қызығушылық мыналармен байланысты: 1. Жасушаларды зерттеуге жалпы көзқарастардың өзгеруі. Липидология. Ұлпалар мен жасушалар. Липидті сығындылар. Липидті профиль. Ферменттер, белоктар. Жүйені басқару. Липидомиктер. Липидомиктердің басқа «-омикалардың» арасында алатын орны. Жүйенің құрылысы. Болжам. Диагностика. Емдеу. 2. Сигналдық молекулалар ретінде арахидон қышқылы және басқа полиен май қышқылдары. n-6 линол (18:2n-6) г-линолендік (18:3n-6) дихомо-г - линолендік (18:3n-6) арахидондық (20:4n-6) докосатетраендік (22:4n-6) докозапентаендік (22:5n-6). - Май қышқылдары.ppt
Омега қышқылы
Слайд: 12 Сөз: 617 Дыбыс: 0 Әсер: 0OMEGA 3 және OMEGA 6 полиқанықпаған май қышқылдары (PUFA). Шырышты қабаттар мен тері эпителийінің құрылымы мен қызметі бұзылады. Терінің зақымдалуы да тән: дерматологиялық бұзылулар пайда болады, тері астындағы кенелермен инфекцияға бейімділік бар. OMEGA 3 тобына жататын эйкозапентаендік және докозагексаендік май қышқылдары ісіктердің өсуін баяулатады. PUFA-ларды жеткіліксіз қабылдау кезінде жануарлардың өсуі баяулайды, құнарлылығы төмендейді және физиологиялық күйі нашарлайды. Жақында OMEGA 3 және OMEGA 6 май қышқылдарының иммундық жүйенің модуляторы ретінде әсерін көрсететін зерттеулер жүргізілді. -


Тапсырмалар 1. Карбон қышқылдарының функционалдық тобын және жалпы формуласын табыңыз. 2. Анықтаманы тұжырымдаңыз. 3. Карбон қышқылдарының жіктелуін оқып үйрену. 4. Номенклатуралық дағдыларды меңгеру. 5. Ең маңызды карбон қышқылдарының физикалық және химиялық қасиеттерін қарастырыңыз. 6. Кейбір карбон қышқылдарының қолдану аймақтарын табыңыз.

Барлық карбон қышқылдарының функционалдық тобы бар Карбонил тобы O - C Гидроксил тобы OH Карбоксил тобы Жалпы формула R C O OH Немесе қаныққан бір негізді қышқылдар үшін O OH Cn H2n+1C? Карбон қышқылдары қалай аталады? Карбон қышқылдары – молекулаларында көмірсутек радикалымен байланысқан карбоксил тобы, COOH бар органикалық қосылыстар. ? Карбон қышқылдарының бұрын зерттелген альдегидтер класымен генетикалық байланысы қандай? R C O H + [O] R C O OH [O]= KMnO4, K2Cr2O7+ H2SO4 конц. Карбон қышқылдары – молекулаларында көмірсутек радикалымен байланысқан карбоксил тобы, COOH бар органикалық қосылыстар. R C

Карбон қышқылдарының жіктелуі Карбоксил топтарының санына байланысты Бір негізді Екі негізді (сірке) (оксалдық) O OH CH3C C - CO OH O O HO радикалының табиғатына байланысты Қаныққан (пропиондық) O CH3- CH2-C OH Қанықпаған (акрил) O CH2= CH-C OH Көп негізді (лимон) O H2C – C OH HC - C O OH O H2C - C OH Хош иісті (бензой) C O OH С атомдарының құрамы бойынша: C1C9 төмен, C10 және одан жоғары.

Ұсынылған қышқылдарды жіктеңіз 1) СН3 – СН2 – СН2 – СН2 COOH 1. Бір негізді, қаныққан, төменгі 2) HOOC CH2 CH2 COOH 2. Екі негізді, қаныққан, төменгі 3) COOH CH3 3. Бір негізді, қаныққан, төменгі 4) СН3 – ( CH2 )7 –CH = CH (CH2)7 COOH 4. Бір негізді, қанықпаған, жоғары 5) HOOC –CH2 CH – CH2 COOH COOH 5. Көп негізді, қаныққан, төменгі

КӨМІРБЕК ҚЫШҚЫЛДАРЫНЫҢ НОМЕНКЛАТУРАСЫ КӨМІРБЕК ҚЫШҚЫЛДАРЫНЫҢ НОМЕНКЛАТУРАСЫ СІЛТІ ҚЫШҚЫЛЫ + ОБ + АЗ ҚЫШҚЫЛЫ СІЛТІК МЕТАН ҚЫШҚЫЛЫ МЕТАН ҚЫШҚЫЛЫ (ҚҰМҚЫЗДЫҚ)

2 1 CH3 – COOH COOH CH3 – ЭТАН ҚЫШҚЫЛЫ (сірке Қышқылы)) 33 44 11 COOH CH3 – CH2 – CH2 COOH CH3 – CH2 – CH2 22 БУТАН ҚЫШҚЫЛЫ (БУТАН ҚЫШҚЫЛЫ)

44 22 55 11 COOH CH3 – CH2 – CH2 – CH2 – COOH CH3 – CH2 – CH2 – CH2 – 33 ПЕНТАН ҚЫШҚЫЛЫ ПЕНТАН (ВАЛЕРИЯН ҚЫШҚЫЛЫ) (ВАЛЕРИЯЛЫҚ ҚЫШҚЫЛЫ) 22 NOOS – NOOS 11 КООХНЕТАКДИКА – КООХАНИДАКДИКА (О. Қышқыл қышқылы)

Карбон қышқылдарының гомологиялық қатары Карбон қышқылдарының гомологиялық қатары Химиялық формула Қышқылдың жүйелі атауы Қышқылдың тривиальды атауы Қышқылдық қалдықтың аты Формат Ацетат Пропионат Бутират капронат HCOOH CH3COOH CH3CH2COOH CH3CH2CH2COOH CH3CHCO2 (Meth2CH2COOHCHCO2) Бутан қалам тановая гексан құмырсқа сірке қышқылы пропион майы нейлон валериан валеринаты CH3(CH2)8 – COOH Декан каприк CH3(CH2)14 – COOH CH3(CH2)16 COOH гексадекан октадекан пальмитикалық пальмитат стеарин стеараты

Карбон қышқылдарын атау алгоритмі: 1. Көміртек атомдарының негізгі тізбегін тауып, оны карбоксил тобынан бастап нөмірлеңдер. 2. Орынбасарлардың орнын және олардың атын (аттарын) көрсетеміз. 3. Тізбектегі көміртегі атомдарының санын білдіретін түбірден кейін «ой қышқылы» жұрнағы келеді. 4. Егер бірнеше карбоксил топтары болса, онда «ova» алдында сан қойылады (ди, үш...) Мысалы: 4 CH3 3 CH 2 CH2 1 COOH CH3 3 метилбутан + ova = 3метилбутан қышқылы

ЗАТТАРҒА АТ БЕРІҢІЗ ЗАТТАРҒА ХАЛЫҚАРАЛЫҚ НОМЕНКЛАТУРА СӘЙКЕС АТ БЕРІҢІЗ (2 – МЕТИЛПРОПАН (2 – метилпропан қышқылы) Қышқылы) СН3 – СН – COOH 1.1. CH3 – CH – COOH CH3CH3 2. CH3 – CH2 – CH – CH – COOH 2. CH3 – CH2 – CH – CH – COOH CH3CH3 CH3CH3 (2, 3 – DIMETHYL PENTA PENTA (2, 3 – DIMETHILNNOVAICID) CH3 – CH = CH – CH – COOH 3. CH3 – CH = CH – CH – COOH CH3CH3 4. HOOC – CH2 – CH – COOH 4. HOOC – CH2 – CH – COOH CC22NNH55 (2 – МЕТИЛПЕНТ (2 – МЕТИЛ). ) Қышқыл) ПЕНТЕНЕН – 3– 3 – ОВА – ОВА (2 – ЭТИЛБУТАН (2 – ЭТИЛБУТАНДИОЙ ҚЫЗЫЛ) Қышқылы)

Карбон қышқылдарының формулаларын жазу алгоритмі: 1. Құрамында карбоксил тобы бар көміртек қаңқасын жазып алатын сөздің түбірін таңдаңыз. 2. Көміртек атомдарын карбоксил тобынан бастап нөмірлейміз. 3. Орынбасарларды нөмірлеуге сәйкес көрсетеміз. 4. Жетіспейтін сутегі атомдарын қосу керек (көміртек төрт валентті). 5. Формуланың дұрыс жазылғанын тексеріңіз. Мысалы: 4 3 2 1 C C C COOH 2метилбутан қышқылы. 4 3 2 1 C C C COOH 4 3 2 1 CH3 CH2 CH COOH CH3 CH3

ФИЗИКАЛЫҚ ҚАСИЕТТЕР ФИЗИКАЛЫҚ ҚАСИЕТТЕР CC11 – – CC33 Өзіне тән өткір иісі бар сұйықтықтар, өткір иісі бар, суда жақсы еритін сұйықтықтар Суда жақсы еритін CC44 – C – C99 Тұтқыр майлы Тұтқыр майлы сұйықтықтары бар, иісі нашар, иісі нашар. , суда нашар ериді CC1010 және одан да көп Қатты заттар, Қатты заттар, иіссіз, иіссіз, ерімейді суда суда ерімейді

Сірке қышқылының физикалық қасиеттері: Физикалық күйі сұйық Түсі түссіз мөлдір сұйықтық Иісі өткір сірке қышқылы Суда ерігіштігі жақсы Қайнау температурасы 118 º С Балқу температурасы 17 º С

Карбон қышқылдарының физикалық қасиеттерінің молекула құрылысына тәуелділігі: Төменгі карбон қышқылдары сұйық; жоғары – қатты заттар қышқылдың салыстырмалы молекулалық салмағы неғұрлым көп болса, оның иісі де аз болады. Қышқылдың салыстырмалы молекулалық массасы артқан сайын ерігіштігі төмендейді, альдегидтердің гомологиялық қатары екі газ тәрізді заттардан басталады (бөлме температурасында), ал карбон қышқылдары арасында газдар болмайды. Бұл немен байланысты?

Карбон қышқылдарының химиялық қасиеттері Карбон қышқылдарының химиялық қасиеттері I. Бейорганикалық қышқылдармен ортақ диссоциацияланады: 1. Су ерітінділерінде еритін карбон қышқылдары CH3 – COOH CH3 – COO + H + Орта қышқылды ма? Қышқыл ортада индикаторлардың түсі қалай өзгереді? 2. Сутегіге дейінгі электрохимиялық кернеу қатарындағы металдармен әрекеттесу: Лакмус (күлгін) - қызыл түске боялады Метил-апельсин - қызғылт түске боялады Фенофталейн - түсін өзгертпейді 2CH3 - COOH + Mg Сірке қышқылы 2CH3 COOH + Zn Сірке қышқылы (CH3 -COO) 2Mg Магний ацетаты ( CH3 – COO)2Zn Мырыш ацетаты + H2 + H2 Металл карбон қышқылы ерітіндісімен әрекеттескенде сутегі мен тұз I түзіледі. Бейорганикалық қышқылдармен жиі кездеседі

3. Негізгі оксидтермен әрекеттесу: 2 CH3 – COOH + CuO Сірке қышқылы (CH3 – COO) 2Сu Мыс ацетаты t + H2O 4. Металл гидроксидтерімен әрекеттесу (бейтараптандыру реакциясы) CH3 – COOH + HO –Na Сірке қышқылы 2CH3 – COOH + Cu (OH)2 Сірке қышқылы CH3COONa Натрий ацетаты + H2O (CH3COO)2Cu Мыс ацетаты + H2O 5. Әлсіз және көбірек ұшқыш қышқылдардың тұздарымен әрекеттесу (мысалы, көміртегі, кремний, күкіртсутек, стеарин, пальмитин...) 2CH3– COOH Сірке қышқылы + Na2CO3 натрий карбонаты 2CH3COONa Натрий ацетаты + H2CO3 CO2 H2O

Құмырсқа қышқылының ерекше қасиеттері «Күміс айна» реакциясы O + Ag2O t 2Ag + H2CO3 H C OH Құмырсқа қышқылы Күміс оксиді күміс CO2 H2O

Табиғатта пайда болуы және карбон қышқылдарының қолданылуы Құмырсқа қышқылы (метан қышқылы) - Химиялық формуласы CH2O2, немесе HCOOH. Құмырсқа қышқылын 1670 жылы ағылшын табиғат зерттеушісі Джон Рэй ашқан. Құмырсқа қышқылы қалақайдың ең жақсы түктерінде, ара уында, қарағай инесінде де болады және әртүрлі жемістерде, ұлпаларда, органдарда, жануарлар мен адам секрецияларында аз мөлшерде кездеседі.


Сұрақ: Неліктен құмырсқа шаққан жерді немесе қалақай шаққанда сумен сулауға болмайды? Бұл тек ауырсынудың күшеюіне әкеледі. Жараланған жер аммиакпен суланған болса, ауырсыну неге басылады? Бұл жағдайда тағы не қолдануға болады? Құмырсқа қышқылын суда еріткен кезде электролиттік диссоциация процесі жүреді: HCOOH HCOO + H Нәтижесінде қоршаған ортаның қышқылдығы артып, терінің коррозия процесі күшейеді. Ауырсынуды азайту үшін қышқылды бейтараптандыру керек, ол үшін аммиак ерітіндісі сияқты сілтілі реакциясы бар ерітінділерді пайдалану керек. HCOOH + NH4OH HCOONH4 + H2O немесе HCOOH + NaHCO3 HCOONa + CO2 + H2O

Сірке қышқылы (этан қышқылы) Бұл адам алған және қолданған бірінші қышқыл. 4 мың жылдан астам уақыт бұрын Ежелгі Египетте «туылған». 17-18 ғасырлар тоғысында Ресейде ол «қышқыл ылғал» деп аталды. Біз оны бірінші рет шарап ашыту кезінде алғанбыз. Латынша атауы - Acetum acidum, сондықтан тұздардың атауы - ацетаттар. Мұзды сірке қышқылы 16,8 ºС төмен температурада қатып, мұз тәрізді болады. Асханалық сірке суы 6% немесе 9% қышқыл ерітіндісі. Сірке қышқылы жануарлардың секрецияларында (зәрде, өтте, нәжісте), өсімдіктерде (әсіресе жасыл жапырақтар), қышқыл сүт пен ірімшікте болады; шарап пен сыраны ашыту, шіру, қышқылдау және көптеген органикалық заттардың тотығуы кезінде түзіледі;

Сірке қышқылын қолдану Сірке қышқылын қолдану Сірке қышқылының судағы ерітінділері тамақ өнеркәсібінде (тағамдық қоспа Е 260) және тұрмыстық ас әзірлеуде, сонымен қатар консервілеуде кеңінен қолданылады; өндірісінде: препараттар, НР, аспирин; жасанды талшықтар, мысалы, жібек ацетаты; индиго бояғыштары, жанбайтын пленка, органикалық шыны; лак еріткіштері; өсімдіктерді қорғаудың химиялық құралдары, өсімдіктердің өсу стимуляторлары; Натрий ацетаты CH3COONa трансфузияға арналған қанға арналған консервант ретінде қолданылады; Калий ацетаты CH3COOK – диуретик ретінде; Зәрдегі қантты анықтауға арналған қорғасын ацетаты (CH3COO)2 Pb; Темір (III) (CH3COO)3Fe, алюминий (CH3COO)3Al және хром (III) (CH3COO)3Cr ацетаттары тоқыма өнеркәсібінде морданды бояу үшін қолданылады; Мыс (II) ацетаты (CH3COO)2Cu өсімдік зиянкестерімен күресуге арналған препаратқа кіреді, Париж жасыл деп аталатын; Сірке қышқылының сулы ерітінділері тамақ өнеркәсібінде (Е 260 тағамдық қоспасы) және тұрмыстық аспаздық, сонымен қатар консервілеуде кеңінен қолданылады; өндірісінде: препараттар, НР, аспирин; жасанды талшықтар, мысалы, ацетатты жібек, жанбайтын пленка, лак еріткіштері, CH3COONa қан құюға арналған консервант ретінде қолданылады; зәрдегі қантты анықтауға арналған диуретик қорғасын ацетаты (CH3COO)2 Pb; Мыс ацетаты (II) ( CH3COO)2Cu өсімдік зиянкестерімен күресуге арналған препараттың бөлігі болып табылады, Париж жасыл деп аталатын;

Сірке қышқылын қолдану Косметологияда алкогольді сірке суын қолдану белгілі. Атап айтқанда, пермь және тұрақты бояудан кейін шашқа жұмсақтық пен жылтыр беру. Ол үшін шашыңызды спирттік сірке суын (1 литр суға 34 ас қасық сірке суы) қосып жылы сумен шаю ұсынылады. Халықтық медицинада сірке суын спецификалық емес антипиретик ретінде қолданады. лосьондарды қолдану арқылы бас ауруы үшін. компресстерді қолдану арқылы жәндіктердің шағуы үшін. Тот басқан гайканы бұрап алу қажет болса, кешке сірке қышқылына малынған шүберек қоюға болатынын білесіз бе? Таңертең бұл гайканы бұрап алу әлдеқайда оңай болады. Тәулік ішінде организмде 400 г сірке қышқылы түзіледі? Бұл парфюмерия өнімдерін өндіруде таптырмас 8 литр кәдімгі сірке суын жасауға жеткілікті болады.

N N S C 3 O O Барлық қышқылдардың, Ол, әрине, прима. Барлық жерде көрінетін және көрінбейтін түрде көрсетіңіз. Ол жануарлар мен өсімдіктерде бар, Техника мен медицина онымен мәңгі. Оның ұрпақтары - бұл өте қажет «жігіттер». Белгілі аспирин, жақсы джентльмен сияқты, науқастың қызуын төмендетеді және денсаулығын қалпына келтіреді. Бұл мыс ацетаты. Өсімдіктерге дос, ағайын, Дұшпанды өлтіреді. Қышқылдың әлі де біраз пайдасы бар - ол бізді ацетатты жібекпен киеді. Ал тұшпараны жақсы көретін адам сірке суын бұрыннан біледі. Кино туралы да сұрақ бар: Ацетат пленкасы болмаса, киноны көре алмайтынымызды бәрі білуі керек. Әрине, басқа да қолданулар бар. Және сіз оларды күмәнсіз білесіз. Бірақ, ең бастысы, достар, «Өнеркәсіптің наны» - сірке қышқылы. Мыс ацетаты CH3COOH сулы ерітіндісі
Қорытынды 1.Карбон қышқылдары – молекулаларында көмірсутек радикалымен байланысқан карбоксил тобы – СООН болатын органикалық қосылыстар. 2.Карбон қышқылдары: негізділігі бойынша (бір, екі және көп негізді) көмірсутек радикалы бойынша (қаныққан, қанықпаған және ароматты) С атомдарының құрамы бойынша (төменгі және жоғары) 3. Карбон қышқылының атауы атаудан тұрады. алкан + аналық қышқыл. 4. Карбон қышқылының молекулалық массасы артқан сайын қышқылдың ерігіштігі мен күші төмендейді. 5. Бейорганикалық қышқылдар сияқты еритін карбон қышқылдары да сулы ерітіндіде диссоциацияланып, сутегі иондарын түзеді және индикатор түсін өзгертеді. Олар металдармен (Н-ге дейін), негіздік және амфотерлі оксидтермен және гидроксидтермен, әлсіз қышқылдардың тұздарымен әрекеттесіп, тұздар түзеді. 6 Табиғатта кең таралған және адамдар үшін үлкен практикалық маңызы бар.

Үйге тапсырма 1. 2. §14, жаттығулар No 6 жаттығу No 9 Клеопатра патшайым сарай дәрігерінің кеңесімен зергерлерге белгілі ең үлкен інжу-маржанды сірке суына ерітіп, содан кейін алынған ерітіндіні біраз уақыт бойына қабылдады. Клеопатра қандай реакция жасады? Ол қандай байланыс жасады? 3. Жоғары карбон қышқылдары туралы есеп дайындаңыз

«Математика – табиғат кітабы жазылған тіл»
ГАЛИЛЕЙ ГАЛИЛИЯ - ИТАЛИЯ МАТЕМАТИК, ФИЗИК, АСТРОНОМ.


Білімді жаңарту
Альдегидтер – молекулаларында көмірсутек радикалымен байланысқан функционалды атомдар тобы – COH бар органикалық заттар.
Карбонил - - С = О;
Альдегидтік - - С = О
1. Альдегидтерге қандай қосылыстар жатады?
2. Қандай функционалдық топ карбонил, қайсысы альдегид деп аталады? Олардың арасындағы айырмашылық неде?
3. Альдегидтерге қандай реакциялар ең тән?
4. Құрамында оттегі бар қосылыстарға жататын органикалық қосылыстардың негізгі кластарын көрсетіңіз.
Қосылу және тотығу реакциялары.
Спирттер, альдегидтер, кетондар, карбон қышқылдары, көмірсулар.


Сабақтың мақсаттары
Тәрбиелік:
Студенттерді карбон қышқылдары туралы түсінік және олардың жіктелуімен таныстыру; құмырсқа және сірке қышқылдарын мысалға ала отырып, карбон қышқылдарының қасиеттерін (жану, эфирдену); қасиеттеріне қарай карбон қышқылдарын қолдану.
Тәрбиелік:
Химияға деген оң көзқарасты тәрбиелеу.
Дамытушылық: тривиальды және халықаралық номенклатураны пайдалана отырып, зерттелетін заттарды атай білуді дамыту; карбон қышқылдарының түсу реакцияларының түрлерін анықтау; карбон қышқылдарының құрылымы мен қасиеттерін сипаттау; карбон қышқылдарының реакциялық қабілетінің олардың молекулаларының құрылымына тәуелділігін түсіндіру; сірке қышқылының тұздарын алу үшін химиялық тәжірибе жасау; алған білімдері мен дағдыларын пайдаланады практикалық іс-шаралар(зертханада және үйде заттармен қауіпсіз жұмыс жасау); берілген концентрациядағы ерітінділерді дайындау мүмкіндігі.

Карбон қышқылдары (құрылымы)
Карбоксил
топ
көмірсу онил тобы
гидр оксил топ




Классификация
Радикалдың табиғаты бойынша
Карбоксил топтарының саны бойынша – бір-, екі-, үш-негізгі
Төмендегі қышқылдар қай класқа жатады?
CH 3 – C = O
O = C – C = O
БІРАҚ ОЛ
CH 2 = CH – C = O
- C = O

жүйелі және тривиальды номенклатура
N-COOH - метан ов ая (құмырсқа)
CH 3 -COOH – этан ов ая (сірке суы)
NOOS-COON – этан дио вая (оксал)
NOOS-SN 2 -С.Н 2 -COOH –бутан диов ал мен
(кәріптас)
МЕН 6 Н 5 COOH - бензой
МЕН 17 Н 35 COOH – стеарин
МЕН 17 Н 33 COOH - олеин

сауалнама
- Заттарды атаңыз:
CH 2 - CH - CH – КОУН
CH 3 CH 3 CH 3
CH 3
CH 3 - C – CH 2 – КОУН
CH 3
- 2 метилбутан қышқылы
- 2,2 диметилпропан қышқылы
- 3,3 дихлорогексан қышқылы

Физикалық қасиеттері
- МЕН 1 -МЕН 3 тән өткір иісі бар сұйықтықтар
- МЕН 4 -МЕН 9 жағымсыз иісі бар тұтқыр майлы сұйықтықтар
- c C 10 ерімейтін қатты заттар
- Карбон қышқылдары молекулааралық сутектік байланыстардың болуына байланысты жоғары қайнау температурасына ие және негізінен димер түрінде болады.
- Салыстырмалы молекулалық массаның жоғарылауымен қаныққан бір негізді қышқылдардың қайнау температурасы артады

N–S
Құмырсқа қышқылы
- Құмырсқалардың улы бездерінде, қалақайда, шырша инелерінде болады.
- Барлық карбон қышқылдарынан 10 есе күшті.
- Оны 1831 жылы Т.Пелуз циан қышқылынан алған.
Қолданылған:
- былғарыны бояуға және илеуге арналған мордант ретінде
- медицинада
- көкөністерді консервілеу кезінде
- нейлон, нейлон, поливинил үшін еріткіш ретінде

Құмырсқа қышқылының қасиеттері мен қолданылуы
- Өткір иісі бар түссіз сұйықтық, суда жақсы ериді .
- Ол қышқылдарға да, альдегидтерге де тән қасиеттерді көрсете алады.

CH 3 -МЕН
Сірке қышқылы
Кейбір өсімдіктерде, терде, зәрде, өтте кездеседі. Адам ағзасы күніне 0,5 кг осы қышқылды бөледі.
- Ежелден белгілі.
- IN таза пішін 1700 жылы бөлінген
- 1845 жылы Г.Кольбе оны синтетикалық жолмен алды.
- Ол синтетикалық жолмен де түзілуі мүмкін (бактериялардың әсерінен шараптың қышуы).

Химиялық қасиеттері
Белсенді металдармен әрекеттесу.
2CH 3 COOH + Mg = (CH 3 COO) 2 Mg+H 2
Сілтілермен әрекеттесу.
CH 3 COOH + NaOH = CH 3 COONa + H 2 О
Негізгі оксидтермен әрекеттесу.
2CH 3 COOH + CaO = (CH 3 COO) 2 Ca+H 2 О
Тұздармен әрекеттесу.
2CH 3 COOH+Na 2 CO 3 = 2CH 3 COONa + H 2 O+CO 2
Спирттермен әрекеттесу
CH 3 COOH + HOC 2 Х 5 = CH 3 -CO-O-C 2 Х 5 +H 2 О
этилацетат
эфир
Табиғатта күрделі эфирлер гүлдерде, жемістерде, жидектерде кездеседі. Олар жеміс сулары мен парфюмерия өндірісінде қолданылады.

Сірке қышқылының қасиеттері мен қолданылуы
Түссіз сұйықтық, өзіне тән иіс, суда ериді, көптеген органикалық заттар үшін жақсы еріткіш, теріге тиіп кетсе қауіпті.

Карбон қышқылдарын алу
- Бастапқы спирттер мен альдегидтердің тотығуы (катализатордағы оттегі және KMnO 4 ; Қ 2 Cr 2 О 7 ):
R-CH 2 OH → RCOH → RCOOH
- Метанның каталитикалық тотығуы:
2CH 4 + 3O 2 → 2H–COOH + 2H 2 О
- Бутанның каталитикалық тотығуы:
2CH 3 –Ч 2 –Ч 2 –Ч 3 +5O 2 → 4CH 3 COOH + 2H 2 О
- Хош иісті қышқылдар бензол гомологтарының тотығуы арқылы синтезделеді: KMnO ерітінділерін тотықтырғыш ретінде қолдануға болады. 4 немесе К 2 Cr 2 О 7 қышқыл ортада:
C 6 Х 5 CH 3 МЕН 6 Н 5 COOH+H 2 О
(5С 6 Х 5 CH 3 + 6кмнО 4 +9 сағ 2 SO 4 → 5С 6 Х 5 COOH+3K 2 SO 4 + 6MnSO 4 +14 сағ 2 О)

қолдану
- Құмырсқа қышқылы– медицинада, ара шаруашылығында, органикалық синтезде, еріткіштер мен консерванттар өндірісінде; күшті қалпына келтіретін агент ретінде.
- Сірке қышқылы– тамақ және химия өнеркәсібінде (ацетатты талшық, органикалық шыны, пленка алынатын целлюлоза ацетаты өндірісі; бояғыштарды, дәрілік заттарды және күрделі эфирлерді синтездеу үшін).
- Бутир қышқылы– хош иістендіргіш қоспаларды, пластификаторларды және флотациялық реагенттерді өндіру үшін.
- Қымыздық қышқылы– металлургия өнеркәсібінде (қақтан тазарту).
- Стеарикалық C17H35COOH және пальмиттік қышқыл C 15 H 31 COOH – металл өңдеуде беттік белсенді заттар, майлау материалдары ретінде.

Бақылау сұрақтары
- Қалақай мен медузаның шағу жасушаларының шағу әсерін қандай зат тудырады:
а) құмырсқа қышқылы, б) құмырсқа альдегиді
2. Қалақайдың бөлінуінен пайда болған күйік ауруын қалай жеңілдетуге болады?
а) сумен шаю, б) әлсіз сілті ерітіндісімен шаю,
в) сірке қышқылының әлсіз ерітіндісімен шаю.
3. Құрылымдық формулақұмырсқа қышқылын осылайша HO-SON деп жазуға болады. Демек, бұл қышқыл қос функциялы зат болады. Оны қалай атауға болады:
а) спирт, ә) альдегид спирті, б) қышқыл
4. Гомологтық қатардағы карбон қышқылдарының физикалық қасиеттерінің өзгеруін мысалға ала отырып, сандық қатынастың сапалық қатынасқа ауысуын қарастыруға бола ма?

5. Ұсынылған формулалардан карбон қышқылдарының формулаларын жазып, оларды атаңыз:
CH 3 , CH 3 COOH, C 2 Н 5 О, СН 3 ҰЙҚЫ, С 2 Н 4 , МЕН 15 Н 31 COOH, C 6 Н 6 , МЕН 5 Н 11 COOH, C 3 Н 7 UNS
6. Сірке қышқылы қандай заттармен әрекеттеседі?
а) мырыш, натрий оксиді, магний гидроксиді, натрий карбонаты, спирт (этил)
б) мырыш, натрий оксиді, магний гидроксиді, натрий карбонаты, метан
Реакция теңдеулерін жазыңыз.

ӨЗАРА БІЛІМДІ ТЕКСЕРУ
1) а; 2) b; 3) b;
4) мүмкін, физикалық және химиялық қасиеттеріне негізделген;
5) CH 3 COOH, C 15 Н 31 COOH, C 5 Н 11 COOH, C 3 Н 7 COOH; 6) а.
2CH 3 COOH + Zn = (CH 3 SOO) 2 Zn + H 2
2CH 3 COOH + MgO = (CH 3 SOO) 2 Mg + H 2 ТУРАЛЫ
2CH 3 COOH + Mg(OH) 2 = (CH 3 SOO) 2 Mg + 2H 2 ТУРАЛЫ
2CH 3 COOH + Na 2 CO 3 = 2CH 3 COONa + H 2 CO 3
CH 3 COOH + C 2 Н 5 ОЛ = CH 3 COO C 2 Н 5 + Н 2 ТУРАЛЫ


назарларыңызға рахмет
Үйге тапсырма: 153 - 157 бет
Химия, техникалық мамандықтарға арналған оқулық, М, «Академия», 2011 ж.
Карбон қышқылдарының жеке түрлеріне презентациялар дайындаңыз (тартар, сүт, алма, лимон және т.б.).
Жұмыс дәптері 21-бет.
Дайындалу үшін практикалық жұмыс«Сірке қышқылы туралы ілімдер және онымен тәжірибелер»