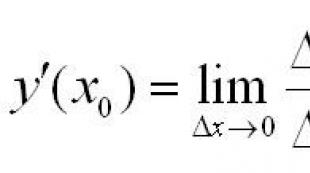ქიმიური მეცნიერების რევოლუცია. "ქიმიური რევოლუცია. ქიმიური განტოლებების ჩაწერის საფუძვლები
ჯოზეფ პრისტლიმ, პროტესტანტმა მღვდელმა, რომელიც გატაცებული იყო ქიმიით, დიდ წარმატებას მიაღწია გაზების გამოყოფაში და მათი თვისებების შესწავლაში. ლიდსთან (ინგლისი), სადაც ის მსახურობდა, იყო ლუდსახარში, საიდანაც შესაძლებელი იყო მიღება დიდი რაოდენობით„შეკრული ჰაერი“ (ახლა ვიცით, რომ ეს იყო ნახშირორჟანგი) ექსპერიმენტების ჩასატარებლად. პრისტლიმ აღმოაჩინა, რომ გაზები შეიძლება დაითხოვოს წყალში და შეეცადა მათი შეგროვება არა წყალზე, არამედ ვერცხლისწყალზე. ასე რომ, მან შეძლო აზოტის ოქსიდის, ამიაკის, წყალბადის ქლორიდის, გოგირდის დიოქსიდის შეგროვება და შესწავლა (რა თქმა უნდა, ეს მათი თანამედროვე სახელებია). 1774 წელს პრისტლიმ გააკეთა თავისი ყველაზე მნიშვნელოვანი აღმოჩენა: მან გამოყო გაზი, რომელშიც ნივთიერებები განსაკუთრებით მკვეთრად იწვის. როგორც ფლოგისტონის თეორიის მომხრე, მან ამ გაზს "დეფლოგისტირებული ჰაერი" უწოდა. პრისტლის მიერ აღმოჩენილი გაზი, როგორც ჩანს, იყო "ფლოგისტიკური ჰაერის" (აზოტის) ანტიპოდი, რომელიც იზოლირებული იყო 1772 წელს ინგლისელი ქიმიკოსის დანიელ რეზერფორდის (1749-1819) მიერ. "ფლოგისტირებულ ჰაერში" თაგვები დაიღუპნენ, მაგრამ "დეფლოგისტირებულ" ჰაერში ისინი ძალიან აქტიურები იყვნენ. (აღსანიშნავია, რომ პრისტლის მიერ იზოლირებული გაზის თვისებები აღწერილი იყო შვედმა ქიმიკოსმა კარლ ვილჰელმ შელემ ჯერ კიდევ 1771 წელს, მაგრამ მისი გზავნილი, გამომცემლის დაუდევრობის გამო, მხოლოდ 1777 წელს გამოჩნდა.) დიდი ფრანგი. ქიმიკოსმა ანტუან ლორან ლავუაზიემ მაშინვე შეაფასა პრისტლის აღმოჩენის მნიშვნელობა. 1775 წელს მან მოამზადა სტატია, რომელშიც ის ამტკიცებდა, რომ ჰაერი არ არის მარტივი ნივთიერება, არამედ ორი აირის ნაზავი, მათგან ერთ-ერთია პრისტლის „დეფლოგისტირებული ჰაერი“, რომელიც ერწყმის წვას ან დაჟანგვას, გადადის მადნებიდან ნახშირზე და. აუცილებელია სიცოცხლისთვის. ლავუაზიემ მას უწოდა ჟანგბადი, ჟანგბადი, ე.ი. "მჟავას წარმომქმნელი" ელემენტარული ელემენტების თეორიას მეორე დარტყმა მიაყენა მას შემდეგ, რაც გაირკვა, რომ წყალი ასევე არ არის მარტივი ნივთიერება, არამედ ორი აირის: ჟანგბადისა და წყალბადის კომბინაციის პროდუქტი. ყველა ამ აღმოჩენამ და თეორიამ, რომელმაც გააუქმა იდუმალი "ელემენტები", გამოიწვია ქიმიის რაციონალიზაცია. წინა პლანზე გამოვიდა მხოლოდ ის ნივთიერებები, რომელთა აწონვა ან ოდენობის სხვაგვარად გაზომვა შესაძლებელია. XVIII საუკუნის 80-იან წლებში. ლავუაზიემ სხვა ფრანგ ქიმიკოსებთან - ანტუან ფრანსუა დე ფურკრუასთან (1755-1809), გიტონ დე მორვოსთან (1737-1816) და კლოდ ლუი ბერტოლესთან თანამშრომლობით - შეიმუშავა ქიმიური ნომენკლატურის ლოგიკური სისტემა; მასში აღწერილია 30-ზე მეტი მარტივი ნივთიერებებიმათი თვისებების მითითებით. ეს ნაშრომი ქიმიური ნომენკლატურის მეთოდი გამოიცა 1787 წელს.
რევოლუცია ქიმიკოსთა თეორიულ შეხედულებებში, რომელიც მოხდა მე -18 საუკუნის ბოლოს. ექსპერიმენტული მასალის სწრაფი დაგროვების შედეგად ფლოგისტონის თეორიის დომინირების ქვეშ (თუმცა მისგან დამოუკიდებლად), მას ჩვეულებრივ „ქიმიურ რევოლუციას“ უწოდებენ.
ინფორმაცია ქიმიის შესახებ
უილშტატერი, რიჩარდ
გერმანელი ქიმიკოსი რიჩარდ მარტინ ვილშტატერი დაიბადა კარლსრუეში, ტექსტილის ვაჭრის, მაქს ვილშტატერისა და სოფია (ულმან) ვილშტატერის ვაჟი. მან დაამთავრა სკოლა კარლსრუეში, ხოლო ნამდვილი გიმნაზია ნიურნბერგში, სადაც თავი ისეთი უნარიანი გამოავლინა...
ტისელიუსი, არნე ვილჰელმ კაურინი
შვედი ბიოქიმიკოსი არნე ვილჰელმ კაურინ ტისელიუსი (ტისელიუსი) დაიბადა სტოკჰოლმში, სადაზღვევო კომპანიის თანამშრომლის ჰანს აბრაამ ჯეისონ ტისელიუსისა და ნორვეგიელი მღვდლის, როუზ (კაურინ) ტისელიუსის ქალიშვილი. როდესაც 1906 წელს მამა...
Pt - პლატინა
PLATINUM (ლათ. Platinum), Pt, პერიოდული სისტემის VIII ჯგუფის ქიმიური ელემენტი, ატომური ნომერი 78, ატომური წონა 195,08, მიეკუთვნება პლატინის ლითონებს. თვისებები: სიმკვრივე 21,45 გ/სმ3, დნობის წერტილი 1769 °C. დასახელება: ესპანურიდან...
მას შემდეგ, რაც კაცობრიობა გამოჩნდა ამ პლანეტაზე, მას ეწეოდა შედარებით მშვიდი და სტაბილური ცხოვრების წესი, მოიხმარდა ერთიდაიგივე საკვებს, იღებდა წყალს ერთი და იმავე წყაროდან და სუნთქავდა იმავე ჰაერს. ბოლო დრომდე იყო მყიფე ბალანსი ჩვენსა და დანარჩენ ბუნებას შორის და ყველა სახის ცვლილებასთან ერთად გარემოანუ კლიმატის, ძალთა ბალანსი კვლავ გათანაბრდა ევოლუციის შეუჩერებელი პროგრესის წყალობით.
გონებრივი შესაძლებლობების არსებობისა და ჩვენი სხეულის გარკვეული გამძლეობის გამო, ადამიანებს მოსწონთ ბიოლოგიური სახეობები, განუვითარდათ ბუნებაში ჩარევისა და გარემოს შეცვლის უნარი. იარაღების შექმნა, ცეცხლის აღმოჩენა, ცხოველების მოშინაურება, ველური მცენარეების მოშენება, პირველი დასახლებების ჩამოყალიბება - ეს ყველაფერი იყო პირველი ნაბიჯები პროგრესისა და ცივილიზაციის გზაზე.
ეს მნიშვნელოვანი იყო ადამიანებისთვის, მაგრამ ეს ყველაფერი სუსტი მცდელობები იყო, რადგან ადამიანს არ შეეძლო დიდი ზიანის მიყენება, რადგან ადამიანთა მცირე მოსახლეობა ჯერ კიდევ მთლიანად იყო დამოკიდებული ბუნების ძალებზე და კანკალებდა მისი ოდნავი ახირებების დროს. დროთა განმავლობაში, ხალხის მზარდი კონცენტრაცია, მათი შემოსევები გახდა არა მხოლოდ უფრო მუდმივი, არამედ უფრო მუდმივი, ამ შემოსევების ბუნება კიდევ უფრო მიზანმიმართული გახდა. ამან განაპირობა ის, რომ ბოლოს და ბოლოს, გასული საუკუნის მეორე ნახევარში, ადამიანების უნარი პროცესების დაჩქარებისას იმდენად შეიცვალა, რომ „ჩვენი განვითარების სისწრაფე“ დაიწყო ჩვენთვის საფრთხე.
მახსენდება ძმები ვაჩოვსკის ჩანაფიქრი - მატრიცა, სადაც, ბედის ირონიით, ადამიანების მიერ შექმნილმა მანქანებმა დაიწყეს ადამიანების ბიოლოგიურად სასარგებლო საწვავის გამოყენება. დღევანდელი რეალობა იწვევს აზრებს, რომლებიც ასე ფერადად არის ასახული ზემოხსენებულ ბლოკბასტერში: ხალხი დიდი ხანია დახვეწილია მრავალი მექანიზმის, მანქანისა და ნივთიერების გამოგონებაში, რაც ამ ყველაფერს ამართლებს საკუთარი ცხოვრების „გაუმჯობესების“, ანუ ცივილიზების სურვილით.

მახსენდება ფილმი „მატრიცა“.
მეტი სიცხადისთვის მივმართოთ ქიმიური „გამოგონებების“ ისტორიას და, როგორც უკვე ითქვა, ციფრებში გადავხედოთ გასული საუკუნის მეორე ნახევარს. გრაფიკი ნათლად აჩვენებს გამოგონების რაოდენობის ზრდას ქიმიური ნივთიერებებიმეოცე საუკუნის მეორე ნახევარში. როგორც ხედავთ, გასული საუკუნის 50-იან წლებში დაიწყო ქიმიური მრეწველობის ნამდვილი ბუმი და 1975 წლისთვის სტატისტიკამ დაფიქსირდა 1 000 000 სინთეზური ქიმიური მასალა. ქიმიკოსთა შემდგომი „წარმატებები“ სხვადასხვა ქვეყანაში ხასიათდებოდა ყოველწლიურად დაახლოებით 1000 ახალი ქიმიური ნივთიერების დამატებით. გასული ათასწლეულის ბოლოს კაცობრიობა „გამოყენებაში“ იყო, ე.ი. იყო 60000-ზე მეტი ხელოვნურად წარმოებული ქიმიკატი ფართოდ გავრცელებული.

გრაფიკი, რომელიც აჩვენებს ქიმიკატების რაოდენობის ზრდას გასული საუკუნის განმავლობაში
Ყველაზე დიდი რიცხვიამ ტიპის „გამოგონებები“ ეხება კაცობრიობის სიცოცხლის დამხმარე ჯაჭვის ყველაზე სუსტ რგოლებს, კერძოდ:
ხშირად გამოყენებული მასალების წარმოება
* იზოლატორები
* საფარები
ყველაზე ხშირად მოხმარებული პროდუქტების წარმოება და მოხმარება
* საკვები დანამატები
* ნივთიერებები, რომლებიც გამოიყენება გადამუშავებასა და შესანახად
* მედიკამენტებში გამოყენებული ნივთიერებები
საერთო და ხელმისაწვდომი ენერგიის წყაროებისა და მედიის გამოყენება
* საჰაერო

ქიმიკატების ფართო სპექტრი ჩვენი ცხოვრების ნაწილი გახდა.
ჩვენს მიერ შექმნილი ქიმიკატების ეს ციკლი უკვე ჩვენი ცხოვრების ნაწილია; და ჩვენ, როგორც ნებისმიერმა სახეობამ, უნდა გამოვიყენოთ იგი, შევეგუოთ მას, ან, რაც ყველაზე ნაკლებად, მოვერიდოთ მას, რომ გადარჩეს. ამ კონცეფციის გაგება შეიძლება, თუ მივიღებთ ამ უწყვეტ პროცესში ჩვენივე მონაწილეობის, დიახ, მონაწილეობის ფაქტს - ერთის მხრივ, ჩვენ ვართ მწარმოებლები, მეორე მხრივ, ჩვენ ვართ ამ ციკლის პროდუქტი. მაშასადამე, ჩვენი განვითარების ან ჩვენი ცოდნის ნებისმიერი შემობრუნება ჩვენზეა დამოკიდებული.
ზოგჯერ ჩვენი ექსპერიმენტები სარგებლობდა, ისევე როგორც პენიცილინის შემთხვევაში, რომელმაც მილიონზე მეტი სიცოცხლე გადაარჩინა ომებსა და მშვიდობიან პერიოდში. და არის ისეთებიც, რომელთა დავიწყებაც თავად მათ აღმომჩენებსაც კი სურთ - მიზანშეწონილია გავიხსენოთ მასობრივი განადგურების ერთ-ერთი უძლიერესი იარაღი, სარინის გაზი (რომელიც საბედისწერო შემთხვევით აღმოაჩინეს გერმანელმა ქიმიკოსებმა, რომლებიც ცდილობდნენ პესტიციდების გაძლიერებას. ეფექტური, მეორე მსოფლიო ომის წინა დღეს). მესამე აღმოჩენების ბუნება ჩვენთვისაც არ არის ნათელი, ისევე როგორც ჩვენთვის, რადგან ისინი უბრალოდ ცვლიან საკუთარ თავს: ალბათ არ არის საჭირო ნარკოტიკული საშუალებების ადამიანის სხეულზე ზემოქმედების მაგალითების მოყვანა. მიუხედავად იმისა, რომ აფთიაქის ბიზნესის გარიჟრაჟზე ძველ სამყაროში, შემდეგ კი მსოფლიოს სხვა ნაწილებში, მათ ემსახურებოდნენ როგორც ხალხს სჭირდებაწამლები.
როგორც ჩანს, თუ რაიმე ნივთიერება გამოიგონეს ხალხის სასარგებლოდ, მაშინ რატომ ჩნდება ისეთი ფაქტები, რომლებზეც ეჭვიც კი არ გვეპარებოდა? პრაქტიკაში, ყველაფერი საკმაოდ მარტივია - ხელოვნური ნივთიერებების საშიშროება სწორედ იმაში მდგომარეობს, რომ ჩვენ არაფერი ვიცით რაიმე სანდო სიზუსტით მათი ეფექტის შესახებ, რასთანაც ისინი შედიან კონტაქტში მთელი მათი უკონტროლო არსებობის მანძილზე.
ამის ჩვენება შეიძლება ელემენტარული მაგალითით: ჩვენ დიდი ხანია ვიცით, როგორც გვეჩვენება, ყველაფერი ჟანგბადის შესახებ. ჟანგბადი ძალიან მნიშვნელოვანია ჩვენი სხეულისთვის, მაგრამ სუფთა ჟანგბადს შეუძლია მოგვკლას. ვინაიდან ბუნებაში ჟანგბადი არ არის მინარევების გარეშე, ჩვენ არ შეგვიძლია მისი ამ ფორმით მოხმარება. როგორც ხედავთ, ჩვენ ვმონაწილეობთ ცხოვრების ჯაჭვებში ზუსტად ისე, როგორც ბუნებამ გვასწავლა; და ნებისმიერი გადახრა (და აქ ჩვენ შევეცადეთ გაგვეუმჯობესებინა საჭირო ნივთიერება) ფატალური აღმოჩნდება. აქ მხოლოდ ერთი დასკვნაა: რაშიც შეგვიძლია აბსოლუტურად დარწმუნებული ვიყოთ ნებისმიერი ნივთიერებით, არის ის, რომ არ ვიცით რამდენ ხანს შეიძლება არ გამოვლინდეს მისი პოტენციურად მავნე ზემოქმედება.
რევოლუციის ერთ-ერთი არსებითი ატრიბუტი, რომელსაც დღესაც მზარდი განგაშით ვაკვირდებით, არის ინფორმაციის თავისუფლების გამოუცხადებელი აკრძალვა გამოგონილ პროდუქტებთან, ინგრედიენტებთან, კომპოზიციებთან და მათ ეტიკეტებთან დაკავშირებით. მიუხედავად იმისა, რომ სულ უფრო მეტი ქვეყანა აწესებს სავალდებულო მოთხოვნებს საკვების, მედიკამენტების, ტანსაცმლის და ა.შ. შემადგენლობის შესახებ ინფორმაციის მიწოდებისთვის, ყოველდღიურ ცხოვრებაში მაინც თითქმის შეუძლებელია იმის დადგენა, თუ რა, მაგალითად, სარეცხი ფხვნილი, საღებავი, პლასტმასის პროდუქტი და ა.შ. შედგება არაფრისგან! ამ მხრივ ყველაზე პროვოკაციული არის იმ პირების დამალვა, რომლებიც უშუალოდ მონაწილეობენ ამ საიდუმლო რეჟიმის დამყარებაში.
არასაჭირო ქიმიკატების სიჭარბე უკვე იმდენად აშკარა გახდა, რომ არავის აღელვებს ახალი მასალის, პოლიმერის ან შემცვლელის გამოგონება. ამის მთავარი დადასტურებაა ხალხის მზარდი სურვილი ეკოლოგიურად სუფთა პროდუქტების მიმართ. „ჯოჯოხეთის გზა მოკირწყლულია კეთილი ზრახვებით“, შეიძლება ითქვას იმ გზაზე, რომელიც ყველა ადამიანმა უნდა გაიაროს, რათა თავიდან აიცილოს „ქიმიური რევოლუციის გამარჯვება“.
მეცნიერული მიღწევების ბოლოდროინდელი ტენდენციები მიუთითებს ბიოლოგიის, გენეტიკასა და ყველაფერზე მწვანეზე უფრო დიდ ცვლაზე. დიდი ალბათობით, ადამიანებს ექნებათ თვალები „გახსნილი“ ბუნების უსაზღვრო შესაძლებლობებზე ქიმიისა და ბირთვული ენერგიის მიღმა და მივლენ იმ დასკვნამდე, რომ თუ რაიმეს მიწოდება არ არის განახლებადი, მაშინ, ალბათ, აზრი არ აქვს ხანგრძლივი- ვადის გეგმები ამ სასრული ელემენტისთვის.
თუ მოგეწონათ ეს მასალა, მაშინ გთავაზობთ ჩვენს საიტზე საუკეთესო მასალების არჩევანს ჩვენი მკითხველების მიხედვით. თქვენ შეგიძლიათ იპოვოთ საუკეთესო მასალების არჩევანი ახალი ადამიანის, ახალი ეკონომიკის, მომავლისა და განათლების შესახებ, სადაც ეს თქვენთვის ყველაზე მოსახერხებელია.ანტიკურობის ქიმია.
ქიმია, მეცნიერება ნივთიერებების შემადგენლობისა და მათი გარდაქმნების შესახებ, იწყება ადამიანის მიერ ცეცხლის უნარის აღმოჩენით, შეცვალოს ბუნებრივი მასალები. როგორც ჩანს, ხალხმა სპილენძისა და ბრინჯაოს დნობა, თიხის ნაწარმის დაწვა და მინის დამზადება ჯერ კიდევ ჩვენს წელთაღრიცხვამდე 4000 წელს იცოდა. VII საუკუნისთვის ძვ.წ. ეგვიპტე და მესოპოტამია გახდა საღებავის წარმოების ცენტრები; იქ მიიღო სუფთა ფორმაოქრო, ვერცხლი და სხვა ლითონები. დაახლოებით 1500 წლიდან 350 წლამდე. დისტილაციას იყენებდნენ საღებავების დასამზადებლად, ხოლო ლითონებს დნობდნენ მადნებიდან ნახშირთან შერევით და ჰაერის აფეთქებით წვის ნარევში. ბუნებრივი მასალის გარდაქმნის პროცედურებს მისტიკური მნიშვნელობა მიეცა.
ბერძნული ბუნებრივი ფილოსოფია.
ამ მითოლოგიურმა იდეებმა საბერძნეთში შეაღწია თალეს მილეტელის მეშვეობით, რომელმაც ფენომენებისა და საგნების მთელი მრავალფეროვნება ერთ ელემენტამდე - წყალამდე აამაღლა. თუმცა, ბერძენი ფილოსოფოსები არ აინტერესებდათ ნივთიერებების მიღების მეთოდებით და მათი პრაქტიკული გამოყენებით, არამედ ძირითადად სამყაროში მიმდინარე პროცესების არსით. ამგვარად, ძველი ბერძენი ფილოსოფოსი ანაქსიმენე ამტკიცებდა, რომ სამყაროს ფუნდამენტური პრინციპი ჰაერია: როდესაც იშვიათდება, ჰაერი იქცევა ცეცხლად და გასქელებით ხდება წყალი, შემდეგ მიწა და ბოლოს ქვა. ჰერაკლიტე ეფესელი ცდილობდა აეხსნა ბუნებრივი მოვლენები ცეცხლის, როგორც პირველადი ელემენტის პოსტულაციის გზით.
ოთხი ძირითადი ელემენტი.
ეს იდეები გაერთიანდა ემპედოკლეს ბუნებრივ ფილოსოფიაში აგრიგენტუმიდან, სამყაროს ოთხი პრინციპის თეორიის შემქმნელიდან. სხვადასხვა ვერსიით, მისი თეორია დომინირებდა ადამიანთა გონებაში ორი ათას წელზე მეტი ხნის განმავლობაში. ემპედოკლეს აზრით, ყველა მატერიალური ობიექტი წარმოიქმნება მარადიული და უცვლელი ელემენტების - წყლის, ჰაერის, მიწისა და ცეცხლის - სიყვარულის (მიზიდულობის) და სიძულვილის (მოგერიების) კოსმიური ძალების გავლენის ქვეშ. ემპედოკლეს ელემენტების თეორია მიიღო და განავითარა ჯერ პლატონმა, რომელმაც დააკონკრეტა, რომ სიკეთისა და ბოროტების არამატერიალურ ძალებს შეუძლიათ ამ ელემენტების ერთმანეთში გარდაქმნა, შემდეგ კი არისტოტელემ.
არისტოტელეს აზრით, ელემენტარული ელემენტები არა მატერიალური ნივთიერებებია, არამედ გარკვეული თვისებების მატარებლები არიან - სიცხე, სიცივე, სიმშრალე და ტენიანობა. ეს შეხედულება გადაკეთდა გალენის იდეაში ოთხი „წვენების“ შესახებ და დომინირებდა მეცნიერებაში მე-17 საუკუნემდე. კიდევ ერთი მნიშვნელოვანი საკითხი, რომელიც აწუხებდა ბერძენ ბუნებრივ ფილოსოფოსებს, იყო მატერიის გაყოფის საკითხი. კონცეფციის დამფუძნებლები, რომელმაც მოგვიანებით მიიღო სახელი "ატომისტური", იყვნენ ლეუკიპუსი, მისი სტუდენტი დემოკრიტე და ეპიკური. მათი სწავლებით, არსებობს მხოლოდ სიცარიელე და ატომები - განუყოფელი მატერიალური ელემენტები, მარადიული, ურღვევი, შეუღწევადი, განსხვავებული ფორმა, პოზიციით სიცარიელე და ზომა; მათი „მორევიდან“ ყველა სხეული იქმნება. ატომური თეორია დემოკრიტეს შემდეგ ორი ათასწლეულის განმავლობაში არაპოპულარული რჩებოდა, მაგრამ მთლიანად არ გაქრა. მისი ერთ-ერთი მიმდევარი იყო ძველი ბერძენი პოეტი ტიტუს ლუკრეციუს კარუსი, რომელმაც გამოკვეთა დემოკრიტეს და ეპიკურეს შეხედულებები ლექსში. საგნების ბუნების შესახებ (De Rerum Natura).
ალქიმია.
ალქიმია არის მატერიის გაუმჯობესების ხელოვნება ლითონების ოქროდ გარდაქმნისა და ადამიანის გაუმჯობესების გზით სიცოცხლის ელექსირის შექმნით. მათთვის ყველაზე მიმზიდველი მიზნის მისაღწევად - უთვალავი სიმდიდრის შექმნას - ალქიმიკოსებმა გადაჭრეს მრავალი პრაქტიკული პრობლემა, აღმოაჩინეს მრავალი ახალი პროცესი, დააკვირდნენ სხვადასხვა რეაქციას, ხელი შეუწყო ახალი მეცნიერების - ქიმიის ჩამოყალიბებას.
ელინისტური პერიოდი.
ეგვიპტე იყო ალქიმიის აკვანი. ეგვიპტელები ბრწყინვალედ გამოირჩეოდნენ გამოყენებითი ქიმიით, რომელიც, თუმცა, არ იყო იზოლირებული, როგორც დამოუკიდებელი ცოდნის სფერო, მაგრამ იყო მღვდლების "წმინდა საიდუმლო ხელოვნების" ნაწილი. ცოდნის ცალკე დარგად ალქიმია მე-2 და მე-3 საუკუნეების მიჯნაზე გამოჩნდა. ახ.წ ალექსანდრე მაკედონელის გარდაცვალების შემდეგ მისი იმპერია დაინგრა, მაგრამ ბერძნების გავლენა ახლო და ახლო აღმოსავლეთის უზარმაზარ ტერიტორიებზე გავრცელდა. ალქიმიამ განსაკუთრებით სწრაფ ყვავილობას მიაღწია ჩვენს წელთაღრიცხვამდე 100-300 წლებში. ალექსანდრიაში.
დაახლოებით 300 წ. ეგვიპტელმა ზოსიმამ დაწერა ენციკლოპედია - 28 წიგნი, რომელიც მოიცავს ყველა ცოდნას ალქიმიის შესახებ წინა 5-6 საუკუნეების განმავლობაში, კერძოდ, ინფორმაცია ნივთიერებების ურთიერთკონვერსიების (გადაქცევის) შესახებ.
ალქიმია არაბულ სამყაროში.
მე-7 საუკუნეში ეგვიპტის დაპყრობის შემდეგ არაბებმა მიიღეს ბერძნულ-აღმოსავლური კულტურა, რომელიც საუკუნეების განმავლობაში იყო დაცული ალექსანდრიული სკოლის მიერ. ძველი მმართველების მიბაძვით, ხალიფებმა დაიწყეს მეცნიერებათა მფარველობა, ხოლო VII–IX სს. გამოჩნდნენ პირველი ქიმიკოსები.
ყველაზე ნიჭიერი და ცნობილი არაბი ალქიმიკოსი იყო ჯაბირ იბნ ჰაიანი (მე-8 საუკუნის ბოლოს), რომელიც მოგვიანებით ევროპაში ცნობილი გახდა გებერის სახელით. ჯაბირი თვლიდა, რომ გოგირდი და ვერცხლისწყალი ორი საპირისპირო პრინციპია, საიდანაც წარმოიქმნება შვიდი სხვა ლითონი; ოქრო ყველაზე რთულია ფორმირება: ამისათვის საჭიროა სპეციალური ნივთიერება, რომელსაც ბერძნებმა უწოდეს ქსერიონი - "მშრალი", ხოლო არაბებმა შეცვალეს ალ-იქსირი (ასე გაჩნდა სიტყვა "ელიქსირი"). ელექსირს სხვა შესანიშნავი თვისებებიც უნდა ჰქონოდა: ყველა დაავადების განკურნება და უკვდავების მიცემა. სხვა არაბი ალქიმიკოსი, ალ-რაზი (დაახლოებით 865–925) (ევროპაში ცნობილი როგორც რაზესი) ასევე მედიცინას ეწეოდა. ამგვარად, მან აღწერა თაბაშირის მომზადების მეთოდი და მოტეხილობის ადგილზე სახვევის წასმის მეთოდი. თუმცა, ყველაზე ცნობილი ექიმი იყო ბუხარიანი იბნ სინა, ასევე ცნობილი როგორც ავიცენა. მისი ნაშრომები მრავალი საუკუნის განმავლობაში ემსახურებოდა ექიმებს სახელმძღვანელოდ.
ალქიმია დასავლეთ ევროპაში.
არაბების მეცნიერულმა შეხედულებებმა შუა საუკუნეების ევროპაში XII საუკუნეში შეაღწია. ჩრდილოეთ აფრიკის, სიცილიასა და ესპანეთის გავლით. არაბი ალქიმიკოსების ნაშრომები ითარგმნა ლათინურად, შემდეგ კი სხვა ევროპულ ენებზე. თავდაპირველად, ევროპაში ალქიმია ეყრდნობოდა ისეთი მნათობთა მოღვაწეობას, როგორიცაა ჯაბირი, მაგრამ სამი საუკუნის შემდეგ განახლდა ინტერესი არისტოტელეს სწავლებების მიმართ, განსაკუთრებით გერმანელი ფილოსოფოსისა და დომინიკელი თეოლოგის ნაშრომების მიმართ, რომელიც მოგვიანებით გახდა ეპისკოპოსი და პროფესორი. პარიზის უნივერსიტეტში ალბერტუს მაგნუსმა და მისმა სტუდენტმა თომა აკვინელმა. დარწმუნებული იყო ბერძნული და არაბული მეცნიერების ქრისტიანულ დოქტრინასთან თავსებადობაში, ალბერტუს მაგნუსმა ხელი შეუწყო მათ დანერგვას სქოლასტიკურ კურსებში. 1250 წელს არისტოტელეს ფილოსოფია სწავლებაში შევიდა პარიზის უნივერსიტეტში. ალქიმიური პრობლემებით ასევე დაინტერესებული იყო ინგლისელი ფილოსოფოსი და ნატურალისტი, ფრანცისკანელი ბერი როჯერ ბეკონი, რომელიც ელოდა შემდგომ მრავალ აღმოჩენას; მან შეისწავლა მარილის და მრავალი სხვა ნივთიერების თვისებები და იპოვა შავი დენთის დამზადების მეთოდი. სხვა ევროპელი ალქიმიკოსები არიან არნალდო და ვილანოვა (1235–1313), რაიმონდ ლული (1235–1313) და ბასილ ვალენტიუსი (15–16 საუკუნეების გერმანელი ბერი).
ალქიმიის მიღწევები.
ხელოსნობისა და ვაჭრობის განვითარება, ქალაქების აღზევება დასავლეთ ევროპაში XII–XIII საუკუნეებში. თან ახლავს მეცნიერების განვითარება და მრეწველობის გაჩენა. ალქიმიკოსის რეცეპტები გამოიყენებოდა ტექნოლოგიურ პროცესებში, როგორიცაა ლითონის დამუშავება. ამ წლების განმავლობაში დაიწყო ახალი ნივთიერებების მოპოვებისა და იდენტიფიცირების გზების სისტემატური ძიება. ჩნდება ალკოჰოლის წარმოებისა და დისტილაციის პროცესის გაუმჯობესების რეცეპტები. ყველაზე მნიშვნელოვანი მიღწევა იყო ძლიერი მჟავების - გოგირდის და აზოტის აღმოჩენა. ახლა ევროპელმა ქიმიკოსებმა შეძლეს მრავალი ახალი რეაქციის განხორციელება და ისეთი ნივთიერებების მიღება, როგორიცაა აზოტის მჟავას მარილები, ვიტრიოლი, ალუმი, გოგირდის და მარილმჟავას მარილები. ალქიმიკოსების მომსახურებით, რომლებიც ხშირად გამოცდილი ექიმები იყვნენ, იყენებდნენ უმაღლესი თავადაზნაურები. ასევე ითვლებოდა, რომ ალქიმიკოსებს გააჩნდათ ჩვეულებრივი ლითონების ოქროდ გადაქცევის საიდუმლო.

მე-14 საუკუნის ბოლოს. ალქიმიკოსების ინტერესმა გარკვეული ნივთიერებების სხვად გადაქცევით ადგილი დაუთმო ინტერესს სპილენძის, სპილენძის, ძმრის, ზეითუნის ზეთისა და სხვადასხვა მედიკამენტების წარმოებით. მე-15-16 საუკუნეებში. ალქიმიკოსთა გამოცდილება სულ უფრო მეტად გამოიყენებოდა სამთო და მედიცინაში.
თანამედროვე ქიმიის დასაწყისი
შუა საუკუნეების დასასრული აღინიშნა ოკულტიზმიდან თანდათანობით უკან დახევით, ალქიმიისადმი ინტერესის დაქვეითებით და ბუნების სტრუქტურის მექანიკური შეხედულების გავრცელებით.
იატროქიმია.
პარაცელსუსს (1493–1541) სრულიად განსხვავებული შეხედულებები ჰქონდა ალქიმიის მიზნებზე. მის მიერ არჩეული ამ სახელით ("ცელსუსზე ზემდგომი") ისტორიაში შევიდა შვეიცარიელი ექიმი ფილიპ ფონ ჰოჰენჰაიმი. პარაცელსუსი, ისევე როგორც ავიცენა, თვლიდა, რომ ალქიმიის მთავარი ამოცანა იყო არა ოქროს მოპოვების გზების ძიება, არამედ მედიკამენტების წარმოება. მან ალქიმიური ტრადიციიდან ისესხა დოქტრინა, რომ არსებობს მატერიის სამი ძირითადი ნაწილი - ვერცხლისწყალი, გოგირდი, მარილი, რომლებიც შეესაბამება აქროლადობის, აალებადი და სიხისტის თვისებებს. ეს სამი ელემენტი ქმნის მაკროკოსმოსის (სამყაროს) საფუძველს და ასოცირდება მიკროსამყაროსთან (ადამიანთან), რომელიც ჩამოყალიბებულია სულით, სულით და სხეულით. დაავადების გამომწვევი მიზეზების დადგენაზე გადასვლისას, პარაცელსუსი ამტკიცებდა, რომ ცხელება და ჭირი წარმოიქმნება ორგანიზმში გოგირდის ჭარბი რაოდენობით, ვერცხლისწყლის ჭარბი რაოდენობით დამბლა ხდება და ა.შ. პრინციპი, რომელსაც ყველა იატროქიმიკოსი იცავდა, იყო ის, რომ მედიცინა ქიმიის საკითხია და ყველაფერი დამოკიდებულია ექიმის უნარზე, სუფთა პრინციპების გამოყოფა უწმინდური ნივთიერებებისგან. ამ სქემის ფარგლებში, სხეულის ყველა ფუნქცია დაყვანილი იყო ქიმიურ პროცესებამდე და ალქიმიკოსის ამოცანა იყო სამედიცინო მიზნებისთვის ქიმიური ნივთიერებების მოძიება და მომზადება.
იატროქიმიური მიმართულების მთავარი წარმომადგენლები იყვნენ პროფესიით ექიმი იან ჰელმონტი (1577–1644); ფრენსის სილვიუსი (1614–1672), რომელიც დიდი პოპულარობით სარგებლობდა, როგორც ექიმი და აღმოფხვრა „სულიერი“ პრინციპები იატროქიმიური სწავლებიდან; ანდრეას ლიებავიუსი (დაახლოებით 1550–1616), ექიმი როტენბურგიდან. მათმა კვლევამ დიდი წვლილი შეიტანა ქიმიის, როგორც დამოუკიდებელი მეცნიერების ჩამოყალიბებაში.
მექანიკური ფილოსოფია.
იატროქიმიის გავლენის შემცირებით, ბუნების ფილოსოფოსები კვლავ მიმართავენ ძველთა სწავლებებს ბუნების შესახებ. წინა პლანზე მე-17 საუკუნეში. გაჩნდა ატომისტური (კორპუსკულარული) შეხედულებები. ერთ-ერთი ყველაზე გამოჩენილი მეცნიერი - კორპუსკულარული თეორიის ავტორი - იყო ფილოსოფოსი და მათემატიკოსი რენე დეკარტი მსჯელობა მეთოდის შესახებ. დეკარტს სჯეროდა, რომ ყველა სხეული „შედგება სხვადასხვა ფორმისა და ზომის მრავალრიცხოვანი მცირე ნაწილაკებისგან, ... რომლებიც ისე ზუსტად არ ერგებიან ერთმანეთს, რომ მათ ირგვლივ უფსკრული არ არის; ეს ხარვეზები არ არის ცარიელი, არამედ ივსება... იშვიათი ნივთიერებით“. დეკარტი თავის „პატარა ნაწილაკებს“ არ თვლიდა ატომებად, ე.ი. განუყოფელი; იდგა მატერიის უსასრულო გაყოფის თვალსაზრისზე და უარყო სიცარიელის არსებობა. დეკარტის ერთ-ერთი ყველაზე ცნობილი ოპონენტი იყო ფრანგი ფიზიკოსი და ფილოსოფოსი პიერ გასენდი. გასენდის ატომიზმი არსებითად იყო ეპიკურუსის სწავლებების ხელახალი მოთხრობა, თუმცა, ამ უკანასკნელისგან განსხვავებით, გასენდი აღიარებდა ღმერთის მიერ ატომების შექმნას; მას სჯეროდა, რომ ღმერთმა შექმნა განუყოფელი და შეუღწევადი ატომების გარკვეული რაოდენობა, რომელთაგანაც ყველა სხეული შედგება; ატომებს შორის უნდა იყოს აბსოლუტური სიცარიელე. ქიმიის განვითარებაში XVII საუკუნეში. განსაკუთრებული როლი ეკუთვნის ირლანდიელ მეცნიერს რობერტ ბოილს. ბოილმა არ მიიღო ძველი ფილოსოფოსების განცხადებები, რომლებიც თვლიდნენ, რომ სამყაროს ელემენტები შეიძლება სპეკულაციური გზით დადგინდეს; ეს ასახულია მისი წიგნის სათაურში სკეპტიკოსი ქიმიკოსი. განსაზღვრის ექსპერიმენტული მიდგომის მომხრეა ქიმიური ელემენტები(რაც საბოლოოდ იქნა მიღებული), მან არ იცოდა რეალური ელემენტების არსებობის შესახებ, თუმცა ერთ-ერთი მათგანი - ფოსფორი - თავადაც თითქმის აღმოაჩინა. ბოილს, როგორც წესი, მიეწერება ქიმიაში ტერმინი „ანალიზის“ დანერგვა. თვისებრივ ანალიზზე ექსპერიმენტებში მან გამოიყენა სხვადასხვა ინდიკატორი და გააცნო ქიმიური აფინურობის ცნება. გალილეო გალილეის ევანგელისტა ტორიჩელის, ისევე როგორც ოტო გერიკეს ნამუშევრებზე დაყრდნობით, რომელმაც აჩვენა „მაგდებურგის ნახევარსფეროები“ 1654 წელს, ბოილმა აღწერა მის მიერ შემუშავებული ჰაერის ტუმბო და ექსპერიმენტები U- ფორმის მილის გამოყენებით ჰაერის ელასტიურობის დასადგენად. ამ ექსპერიმენტების შედეგად ჩამოყალიბდა ჰაერის მოცულობასა და წნევას შორის უკუპროპორციულობის ცნობილი კანონი. 1668 წელს ბოილი გახდა ლონდონის ახლად ორგანიზებული სამეფო საზოგადოების აქტიური წევრი, ხოლო 1680 წელს აირჩიეს მის პრეზიდენტად.
ტექნიკური ქიმია.
მეცნიერულმა მიღწევებმა და აღმოჩენებმა არ შეიძლება გავლენა მოახდინოს ტექნიკურ ქიმიაზე, რომლის ელემენტებიც გვხვდება მე-15-მე-17 საუკუნეებში. მე-15 საუკუნის შუა ხანებში. განვითარდა აფეთქების გაყალბების ტექნოლოგია. სამხედრო ინდუსტრიის საჭიროებებმა სტიმული მისცა მუშაობას დენთის წარმოების ტექნოლოგიის გასაუმჯობესებლად. მე-16 საუკუნის განმავლობაში. ოქროს წარმოება გაორმაგდა და ვერცხლის წარმოება ცხრაჯერ გაიზარდა. ქვეყნდება ფუნდამენტური სამუშაოები ლითონებისა და სხვადასხვა მასალის წარმოებაზე, რომლებიც გამოიყენება მშენებლობაში, მინის წარმოებაში, ქსოვილის შეღებვაში, საკვების შენახვასა და ტყავის გარუჯვაში. ალკოჰოლური სასმელების მოხმარების გაფართოებასთან ერთად იხვეწება დისტილაციის მეთოდები და მუშავდება ახალი დისტილაციის აპარატები. გამოჩნდა მრავალი საწარმოო ლაბორატორია, პირველ რიგში მეტალურგიული. იმდროინდელ ქიმიურ ტექნოლოგებს შორის შეიძლება აღინიშნოს ვანოციო ბირინგუციო (1480–1539), რომლის კლასიკური ნაშრომი. შესახებ პიროტექნიკადაიბეჭდა ვენეციაში 1540 წელს და შეიცავდა 10 წიგნს, რომლებიც ეხებოდა მაღაროებს, მინერალების გამოცდას, ლითონების მომზადებას, დისტილაციას, ომის ხელოვნებას და ფეიერვერკებს. კიდევ ერთი ცნობილი ტრაქტატი სამთო და მეტალურგიის შესახებ, დაწერა გეორგ აგრიკოლამ (1494–1555). ასევე უნდა აღინიშნოს იოჰან გლაუბერი (1604–1670), ჰოლანდიელი ქიმიკოსი, რომელმაც შექმნა გლაუბერის მარილი.
ᲛᲔᲗᲕᲠᲐᲛᲔᲢᲔ ᲡᲐᲣᲙᲣᲜᲔ
ქიმია, როგორც სამეცნიერო დისციპლინა.
1670-დან 1800 წლამდე ქიმიამ მიიღო ოფიციალური სტატუსი წამყვანი უნივერსიტეტების სასწავლო გეგმებში, ნატურფილოსოფიასა და მედიცინასთან ერთად. 1675 წელს გამოჩნდა ნიკოლას ლემერის (1645–1715) სახელმძღვანელო. ქიმიის კურსი, რომელმაც უზარმაზარი პოპულარობა მოიპოვა, გამოიცა მისი 13 ფრანგული გამოცემა, გარდა ამისა, ითარგმნა ლათინურ და ბევრ სხვა ევროპულ ენაზე. მე-18 საუკუნეში სამეცნიერო ქიმიური საზოგადოებები და დიდი რაოდენობით სამეცნიერო ინსტიტუტები; მათ მიერ ჩატარებული კვლევები მჭიდრო კავშირშია საზოგადოების სოციალურ და ეკონომიკურ საჭიროებებთან. გამოჩნდნენ პრაქტიკოსი ქიმიკოსები, რომლებიც დაკავებულნი იყვნენ ინსტრუმენტების დამზადებით და მრეწველობისთვის ნივთიერებების წარმოებით.
ფლოგისტონის თეორია.
XVII საუკუნის მეორე ნახევრის ქიმიკოსთა ნაშრომებში. დიდი ყურადღება დაეთმო წვის პროცესის ინტერპრეტაციებს. ძველი ბერძნების აზრით, ყველაფერი, რისი დაწვა შეიძლება, შეიცავს ცეცხლის ელემენტს, რომელიც გამოიყოფა შესაფერის პირობებში. 1669 წელს გერმანელმა ქიმიკოსმა იოჰან იოახიმ ბეხერმა სცადა აალებადი ახსნა-განმარტება. მან თქვა, რომ მყარი ნივთიერებები შედგება სამი ტიპის „დედამიწისგან“ და ერთ-ერთი ტიპი, რომელსაც მან „ცხიმიანი მიწა“ უწოდა, მიიჩნიეს „აალებადობის პრინციპად“.
ბეჩერის მიმდევარმა, გერმანელმა ქიმიკოსმა და ექიმმა გეორგ ერნსტ შტალმა, „ცხიმიანი მიწის“ ცნება გარდაქმნა ფლოგისტონის განზოგადებულ დოქტრინაში - „აალებადობის დასაწყისი“. სტალის აზრით, ფლოგისტონი არის გარკვეული ნივთიერება, რომელიც შეიცავს ყველა წვად ნივთიერებას და გამოიყოფა წვის დროს. სტალი ამტკიცებდა, რომ ლითონების დაჟანგვა ხის დაწვის მსგავსია. ლითონები შეიცავს ფლოგისტონს, მაგრამ ჟანგი (მასშტაბი) აღარ შეიცავს ფლოგისტონს. ამითაც მისაღებ ახსნას აძლევდა მადნების ლითონებად გადაქცევის პროცესს: მადანი, რომელშიც ფლოგისტონის შემცველობა უმნიშვნელოა, თბება ფლოგისტონით მდიდარ ნახშირზე და ეს უკანასკნელი იქცევა მადნად. ქვანახშირი იქცევა ნაცრად, ხოლო მადანი ფლოგისტონით მდიდარ ლითონად. 1780 წლისთვის ფლოგისტონის თეორია თითქმის ყველგან მიიღეს ქიმიკოსებმა, თუმცა მან არ უპასუხა ძალიან მნიშვნელოვან კითხვას: რატომ მძიმდება რკინა ჟანგის დროს, თუმცა მისგან აორთქლდება ფლოგისტონი? მე -18 საუკუნის ქიმიკოსები ეს წინააღმდეგობა არც ისე მნიშვნელოვანი ჩანდა; მთავარი, მათი აზრით, იყო ნივთიერებების გარეგნობის ცვლილების მიზეზების ახსნა.
მე-18 საუკუნეში ბევრი ქიმიკოსი იყო, რომელთა სამეცნიერო საქმიანობა არ ჯდება მეცნიერების განვითარების ეტაპებისა და მიმართულებების განხილვის ჩვეულ სქემებში და მათ შორის განსაკუთრებული ადგილი უკავია რუს ენციკლოპედისტ მეცნიერს, პოეტს და განმანათლებლობის ჩემპიონს მიხეილ ვასილიევიჩ ლომონოსოვს (1711-1711). 1765). თავისი აღმოჩენებით ლომონოსოვმა გაამდიდრა ცოდნის თითქმის ყველა სფერო და მისი ბევრი იდეა ას წელზე მეტი უსწრებდა იმდროინდელ მეცნიერებას. 1756 წელს ლომონოსოვმა ჩაატარა ცნობილი ექსპერიმენტები დახურულ ჭურჭელში ლითონების დაწვაზე, რამაც წარმოადგინა ქიმიური რეაქციების დროს ნივთიერების შენარჩუნებისა და წვის პროცესებში ჰაერის როლის უდავო მტკიცებულება: ლავუაზიემდეც კი მან ახსნა წონის დაფიქსირებული მატება ლითონების წვის დროს. მათი ჰაერთან შერწყმით. კალორიის შესახებ გავრცელებული იდეებისგან განსხვავებით, ის ამტკიცებდა, რომ თერმული ფენომენები გამოწვეულია მატერიალური ნაწილაკების მექანიკური მოძრაობით. მან აირების ელასტიურობა ნაწილაკების მოძრაობით ახსნა. ლომონოსოვმა განასხვავა "კორპუსკულის" (მოლეკულა) და "ელემენტის" (ატომი) ცნებები, რომლებმაც ზოგადი აღიარება მხოლოდ მე -19 საუკუნის შუა ხანებში მიიღო. ლომონოსოვმა ჩამოაყალიბა მატერიისა და მოძრაობის კონსერვაციის პრინციპი, გამორიცხა ფლოგისტონი ქიმიური აგენტების რიცხვიდან, საფუძველი ჩაუყარა ფიზიკურ ქიმიას, შექმნა ქიმიური ლაბორატორია პეტერბურგის მეცნიერებათა აკადემიაში 1748 წელს, რომელშიც არა მარტო სამეცნიერო ნაშრომები, არამედ პრაქტიკული მეცადინეობები სტუდენტებისთვის. მან ჩაატარა ვრცელი კვლევები ქიმიასთან დაკავშირებული ცოდნის სფეროებში - ფიზიკა, გეოლოგია და ა.შ.
პნევმატური ქიმია.
ფლოგისტონის თეორიის ნაკლოვანებები ყველაზე მკაფიოდ წარმოიშვა ე.წ. პნევმატური ქიმია. ამ ტენდენციის ყველაზე დიდი წარმომადგენელი იყო რ. ბოილი: მან არა მხოლოდ აღმოაჩინა გაზის კანონი, რომელიც ახლა მის სახელს ატარებს, არამედ დააპროექტა მოწყობილობები ჰაერის შეგროვებისთვის. ქიმიკოსებს ახლა აქვთ სასიცოცხლო საშუალებები სხვადასხვა „ჰაერების“ იზოლირებისთვის, იდენტიფიცირებისთვის და შესასწავლად. მნიშვნელოვანი ნაბიჯი იყო მე-18 საუკუნის დასაწყისში ინგლისელი ქიმიკოსის სტივენ ჰეილსის (1677–1761) მიერ „პნევმატური აბაზანის“ გამოგონება. - მოწყობილობა, რომელიც გამოიყოფა გაზების დასაჭერად, როდესაც ნივთიერების გაცხელება ხდება წყლის ჭურჭელში, თავდაყირა ჩაშვებული წყლის აბაზანაში. მოგვიანებით ჰეილსმა და ჰენრი კავენდიშმა დაადგინეს გარკვეული გაზების („ჰაერების“) არსებობა, რომლებიც თავიანთი თვისებებით განსხვავდება ჩვეულებრივი ჰაერისგან. 1766 წელს კავენდიშმა სისტემატურად შეისწავლა მჟავების რეაქციის შედეგად წარმოქმნილი აირი გარკვეულ ლითონებთან, რომელსაც მოგვიანებით წყალბადი უწოდეს. გაზების შესწავლაში დიდი წვლილი შეიტანა შოტლანდიელმა ქიმიკოსმა ჯოზეფ ბლეკმა. ბლეკმა აღმოაჩინა, რომ მინერალური კალციუმის კარბონატი იშლება გაცხელებისას, გამოყოფს გაზს და წარმოქმნის კირს (კალციუმის ოქსიდი). გამოთავისუფლებული აირი (ნახშირორჟანგი - შავი მას "შეკრულ ჰაერს" უწოდებდა) შეიძლება ცაცხვთან ერთად კალციუმის კარბონატის წარმოქმნით. სხვა საკითხებთან ერთად, ამ აღმოჩენამ დაადგინა ობლიგაციების განუყოფლობა მყარ და აირისებრ ნივთიერებებს შორის.
ქიმიური რევოლუცია.
ჯოზეფ პრისტლიმ, პროტესტანტმა მღვდელმა, რომელიც გატაცებული იყო ქიმიით, დიდ წარმატებას მიაღწია გაზების გამოყოფაში და მათი თვისებების შესწავლაში. ლიდსთან (ინგლისი), სადაც ის მსახურობდა, იყო ლუდსახარში, საიდანაც დიდი რაოდენობით „შეკრული ჰაერი“ (ახლა ვიცით, რომ ეს იყო ნახშირორჟანგი) ექსპერიმენტებისთვის შეიძლებოდა მიეღო. პრისტლიმ აღმოაჩინა, რომ გაზები შეიძლება დაითხოვოს წყალში და შეეცადა მათი შეგროვება არა წყალზე, არამედ ვერცხლისწყალზე. ასე რომ, მან შეძლო აზოტის ოქსიდის, ამიაკის, წყალბადის ქლორიდის, გოგირდის დიოქსიდის შეგროვება და შესწავლა (რა თქმა უნდა, ეს მათი თანამედროვე სახელებია). 1774 წელს პრისტლიმ გააკეთა თავისი ყველაზე მნიშვნელოვანი აღმოჩენა: მან გამოყო გაზი, რომელშიც ნივთიერებები განსაკუთრებით მკვეთრად იწვის. როგორც ფლოგისტონის თეორიის მომხრე, მან ამ გაზს "დეფლოგისტირებული ჰაერი" უწოდა. პრისტლის მიერ აღმოჩენილი გაზი, როგორც ჩანს, იყო "ფლოგისტირებული ჰაერის" (აზოტის) ანტითეზა, რომელიც იზოლირებული იყო 1772 წელს ინგლისელი ქიმიკოსის დანიელ რეზერფორდის (1749-1819) მიერ. "ფლოგისტირებულ ჰაერში" თაგვები დაიღუპნენ, მაგრამ "დეფლოგისტირებულ" ჰაერში ისინი ძალიან აქტიურები იყვნენ. (აღსანიშნავია, რომ პრისტლის მიერ იზოლირებული გაზის თვისებები აღწერილი იყო შვედმა ქიმიკოსმა კარლ ვილჰელმ შელემ ჯერ კიდევ 1771 წელს, მაგრამ მისი გზავნილი, გამომცემლის დაუდევრობის გამო, მხოლოდ 1777 წელს გამოჩნდა.) დიდი ფრანგი. ქიმიკოსმა ანტუან ლორან ლავუაზიემ მაშინვე შეაფასა პრისტლის აღმოჩენის მნიშვნელობა. 1775 წელს მან მოამზადა სტატია, რომელშიც ის ამტკიცებდა, რომ ჰაერი არ არის მარტივი ნივთიერება, არამედ ორი აირის ნაზავი, მათგან ერთ-ერთია პრისტლის „დეფლოგისტირებული ჰაერი“, რომელიც ერწყმის წვას ან დაჟანგვას, გადადის მადნებიდან ნახშირზე და. აუცილებელია სიცოცხლისთვის. ლავუაზიემ დაუძახა ჟანგბადი, ჟანგბადი, ე.ი. "მჟავას წარმომქმნელი" ელემენტარული ელემენტების თეორიას მეორე დარტყმა მიაყენა მას შემდეგ, რაც გაირკვა, რომ წყალი ასევე არ არის მარტივი ნივთიერება, არამედ ორი აირის: ჟანგბადისა და წყალბადის კომბინაციის პროდუქტი. ყველა ამ აღმოჩენამ და თეორიამ, რომელმაც გააუქმა იდუმალი "ელემენტები", გამოიწვია ქიმიის რაციონალიზაცია. წინა პლანზე გამოვიდა მხოლოდ ის ნივთიერებები, რომელთა აწონვა ან ოდენობის სხვაგვარად გაზომვა შესაძლებელია. XVIII საუკუნის 80-იან წლებში. ლავუაზიემ სხვა ფრანგ ქიმიკოსებთან ანტუან ფრანსუა დე ფურკრუასთან (1755–1809), გიტონ დე მორვოსთან (1737–1816) და კლოდ ლუი ბერტოლესთან თანამშრომლობით შეიმუშავა ქიმიური ნომენკლატურის ლოგიკური სისტემა; მასში აღწერილია 30-ზე მეტი მარტივი ნივთიერება, რაც მიუთითებს მათ თვისებებზე. Ეს სამუშაო ქიმიური ნომენკლატურის მეთოდი, გამოიცა 1787 წელს.
რევოლუცია ქიმიკოსთა თეორიულ შეხედულებებში, რომელიც მოხდა მე -18 საუკუნის ბოლოს. ექსპერიმენტული მასალის სწრაფი დაგროვების შედეგად ფლოგისტონის თეორიის დომინირების ქვეშ (თუმცა მისგან დამოუკიდებლად), მას ჩვეულებრივ „ქიმიურ რევოლუციას“ უწოდებენ.
ᲛᲔᲪᲮᲠᲐᲛᲔᲢᲔ ᲡᲐᲣᲙᲣᲜᲔ
ნივთიერებების შემადგენლობა და მათი კლასიფიკაცია.
ლავუაზიეს წარმატებებმა აჩვენა, რომ რაოდენობრივი მეთოდების გამოყენებამ შეიძლება დაგვეხმაროს ნივთიერებების ქიმიური შემადგენლობის დადგენაში და მათი ასოციაციის კანონების გარკვევაში.
ატომური თეორია.
ფიზიკური ქიმიის დაბადება.
მე-19 საუკუნის ბოლოსთვის. გაჩნდა პირველი ნაშრომები, რომლებშიც სისტემატურად იყო შესწავლილი სხვადასხვა ნივთიერების ფიზიკური თვისებები (დუღილისა და დნობის წერტილები, ხსნადობა, მოლეკულური წონა). ასეთი კვლევა დაიწყეს გეი-ლუსაკმა და ვანატ ჰოფმა, რომლებმაც აჩვენეს, რომ მარილების ხსნადობა დამოკიდებულია ტემპერატურასა და წნევაზე. 1867 წელს ნორვეგიელმა ქიმიკოსებმა პიტერ ვააგემ (1833–1900) და კატო მაქსიმილიან გულდბერგმა (1836–1902) ჩამოაყალიბეს მასის მოქმედების კანონი, რომლის მიხედვითაც რეაქციების სიჩქარე დამოკიდებულია რეაქტორების კონცენტრაციაზე. მათემატიკურმა აპარატმა, რომელიც მათ გამოიყენეს, შესაძლებელი გახადა იპოვონ ძალიან მნიშვნელოვანი რაოდენობა, რომელიც ახასიათებს ნებისმიერ ქიმიურ რეაქციას - სიჩქარის მუდმივობას.
ქიმიური თერმოდინამიკა.
იმავდროულად, ქიმიკოსებმა მიმართეს ფიზიკური ქიმიის ცენტრალურ საკითხს - სითბოს გავლენას ქიმიური რეაქციები. მე-19 საუკუნის შუა ხანებისთვის. ფიზიკოსებმა უილიამ ტომსონმა (ლორდ კელვინი), ლუდვიგ ბოლცმანმა და ჯეიმს მაქსველმა განავითარეს ახალი შეხედულებები სითბოს ბუნებაზე. უარყვეს ლავუაზიეს კალორიული თეორია, ისინი წარმოადგენდნენ სითბოს, როგორც მოძრაობის შედეგს. მათი იდეები შეიმუშავა რუდოლფ კლაუზიუსმა. მან შეიმუშავა კინეტიკური თეორია, რომლის მიხედვითაც ისეთი რაოდენობები, როგორიცაა მოცულობა, წნევა, ტემპერატურა, სიბლანტე და რეაქციის სიჩქარე, შეიძლება ჩაითვალოს მოლეკულების უწყვეტი მოძრაობისა და მათი შეჯახების იდეის საფუძველზე. ტომსონთან (1850) ერთდროულად კლასიუსმა მისცა თერმოდინამიკის მეორე კანონის პირველი ფორმულირება, შემოიღო ცნებები ენტროპია (1865), იდეალური გაზი და მოლეკულების საშუალო თავისუფალი გზა.
ქიმიური რეაქციებისადმი თერმოდინამიკური მიდგომა გამოიყენა თავის ნაშრომებში ავგუსტ ფრიდრიხ გორსტმანმა (1842–1929), რომელიც კლაუსიუსის იდეებზე დაყრდნობით ცდილობდა აეხსნა მარილების დისოციაცია ხსნარში. 1874–1878 წლებში ამერიკელმა ქიმიკოსმა ჯოსია უილარდ გიბსმა ჩაატარა ქიმიური რეაქციების თერმოდინამიკის სისტემატური შესწავლა. მან შემოიტანა თავისუფალი ენერგიისა და ქიმიური პოტენციალის კონცეფცია, ახსნა მასის მოქმედების კანონის არსი და გამოიყენა თერმოდინამიკური პრინციპები სხვადასხვა ტემპერატურაზე, წნევასა და კონცენტრაციაზე სხვადასხვა ფაზებს შორის წონასწორობის შესასწავლად (ფაზის წესი). გიბსის ნაშრომმა საფუძველი ჩაუყარა თანამედროვე ქიმიურ თერმოდინამიკას. შვედმა ქიმიკოსმა სვანტე ავგუსტ არენიუსმა შექმნა იონური დისოციაციის თეორია, რომელიც ხსნის ბევრ ელექტროქიმიურ მოვლენას და გააცნო აქტივაციის ენერგიის კონცეფცია. მან ასევე შეიმუშავა გაზომვის ელექტროქიმიური მეთოდი მოლეკულური წონაგახსნილი ნივთიერებები.
მთავარი მეცნიერი, რომლის წყალობითაც ფიზიკური ქიმია ცოდნის დამოუკიდებელ სფეროდ იქნა აღიარებული, იყო გერმანელი ქიმიკოსი ვილჰელმ ოსტვალდი, რომელმაც გამოიყენა გიბსის კონცეფციები კატალიზის შესწავლაში. 1886 წელს მან დაწერა პირველი სახელმძღვანელო ფიზიკური ქიმიის შესახებ, ხოლო 1887 წელს დააარსა (ვანტ ჰოფთან ერთად) ჟურნალი Physical Chemistry (Zeitschrift für physikalische Chemie).
მეოცე საუკუნე
ახალი სტრუქტურული თეორია.
ატომებისა და მოლეკულების სტრუქტურის შესახებ ფიზიკური თეორიების განვითარებით, ხელახლა განიხილეს ისეთი ძველი ცნებები, როგორიცაა ქიმიური მიახლოება და ტრანსმუტაცია. გაჩნდა ახალი იდეები მატერიის სტრუქტურის შესახებ.
ატომის მოდელი.
1896 წელს ანტუან ანრი ბეკერელმა (1852-1908) აღმოაჩინა რადიოაქტიურობის ფენომენი, აღმოაჩინა ურანის მარილებიდან სუბატომური ნაწილაკების სპონტანური ემისია, ხოლო ორი წლის შემდეგ, მეუღლეებმა პიერ კიურიმ და მარი სკლოდოვსკა-კურიმ გამოყო ორი რადიოაქტიური ელემენტი პოლონი და რადიუმი: . მომდევნო წლებში აღმოაჩინეს, რომ რადიოაქტიური ნივთიერებები ასხივებენ სამი სახის გამოსხივებას: ა- ნაწილაკები, ბ-ნაწილაკები და გ- სხივები. ფრედერიკ სოდის აღმოჩენასთან ერთად, რომელმაც აჩვენა, რომ რადიოაქტიური დაშლის დროს ხდება ზოგიერთი ნივთიერების სხვებად გარდაქმნა, ამ ყველაფერმა ახალი მნიშვნელობა მისცა იმას, რასაც ძველები ტრანსმუტაციას უწოდებდნენ.
1897 წელს ჯოზეფ ჯონ ტომსონმა აღმოაჩინა ელექტრონი, რომლის მუხტი მაღალი სიზუსტით გაზომა 1909 წელს რობერტ მილიკანის მიერ. 1911 წელს ერნსტ რეზერფორდმა, ტომსონის ელექტრონის კონცეფციაზე დაყრდნობით, შემოგვთავაზა ატომის მოდელი: ატომის ცენტრში არის დადებითად დამუხტული ბირთვი და მის გარშემო ბრუნავენ უარყოფითად დამუხტული ელექტრონები. 1913 წელს ნილს ბორმა კვანტური მექანიკის პრინციპების გამოყენებით აჩვენა, რომ ელექტრონები შეიძლება განთავსდეს არა რომელიმე, არამედ მკაცრად განსაზღვრულ ორბიტებში. ატომის რაზერფორდ-ბორის პლანეტარული კვანტური მოდელი აიძულა მეცნიერები მიეღოთ ახალი მიდგომა ქიმიური ნაერთების სტრუქტურისა და თვისებების ასახსნელად. ამის შემოთავაზება გერმანელმა ფიზიკოსმა ვალტერ კოსელმა (1888–1956 წწ). ქიმიური თვისებებიატომი განისაზღვრება მის გარე გარსში ელექტრონების რაოდენობით, ხოლო ქიმიური ბმების წარმოქმნა განისაზღვრება ძირითადად ელექტროსტატიკური ურთიერთქმედების ძალებით. ამერიკელმა მეცნიერებმა გილბერტ ნიუტონ ლუისმა და ირვინგ ლანგმუირმა ჩამოაყალიბეს ქიმიური კავშირის ელექტრონული თეორია. ამ იდეების შესაბამისად, არაორგანული მარილების მოლეკულები სტაბილიზირებულია ელექტროსტატიკური ურთიერთქმედებით მათ შემადგენელ იონებს შორის, რომლებიც წარმოიქმნება ელექტრონების ერთი ელემენტიდან მეორეზე გადაცემის დროს. იონური ბმა), და მოლეკულები ორგანული ნაერთები– ელექტრონების გაზიარების გამო (კოვალენტური ბმა). ეს იდეები საფუძვლად უდევს ქიმიური კავშირის თანამედროვე კონცეფციებს.
კვლევის ახალი მეთოდები.
მატერიის სტრუქტურის შესახებ ყველა ახალი იდეა ჩამოყალიბდა მხოლოდ მე-20 საუკუნის განვითარების შედეგად. ექსპერიმენტული ტექნიკა და ახალი კვლევის მეთოდების გაჩენა. 1895 წელს ვილჰელმ კონრად რენტგენის მიერ რენტგენის სხივების აღმოჩენამ საფუძველი ჩაუყარა რენტგენის კრისტალოგრაფიის მეთოდის შემდგომ შექმნას, რაც შესაძლებელს ხდის მოლეკულების სტრუქტურის დადგენას დიფრაქციის ნიმუშიდან. რენტგენიკრისტალებზე. ამ მეთოდის გამოყენებით მოხდა რთული ორგანული ნაერთების სტრუქტურის გაშიფვრა - ინსულინი, დეზოქსირიბონუკლეინის მჟავა (დნმ), ჰემოგლობინი და ა.შ. ატომური თეორიის შექმნასთან ერთად გამოჩნდა ახალი ძლიერი სპექტროსკოპიული მეთოდები, რომლებიც გვაწვდიან ინფორმაციას ატომებისა და მოლეკულების სტრუქტურის შესახებ. რადიოიზოტოპური ტრასერების გამოყენებით შესწავლილია სხვადასხვა ბიოლოგიური პროცესი, აგრეთვე ქიმიური რეაქციების მექანიზმი; რადიაციული მეთოდები ფართოდ გამოიყენება მედიცინაშიც.
ბიოქიმია.
ეს სამეცნიერო დისციპლინა ეხება ქიმიური თვისებების შესწავლას ბიოლოგიური ნივთიერებებიპირველი იყო ორგანული ქიმიის ერთ-ერთი განშტოება. იგი დამოუკიდებელი რეგიონი გახდა XIX საუკუნის ბოლო ათწლეულში. მცენარეული და ცხოველური წარმოშობის ნივთიერებების ქიმიური თვისებების შესწავლის შედეგად. ერთ-ერთი პირველი ბიოქიმიკოსი იყო გერმანელი მეცნიერი ემილ ფიშერი. მან მოახდინა ისეთი ნივთიერებების სინთეზირება, როგორიცაა კოფეინი, ფენობარბიტალი, გლუკოზა და მრავალი ნახშირწყალბადი და დიდი წვლილი შეიტანა ფერმენტების მეცნიერებაში - ცილის კატალიზატორები, რომლებიც პირველად იზოლირებული იქნა 1878 წელს. ბიოქიმიის, როგორც მეცნიერების ჩამოყალიბებას ხელი შეუწყო ახალი ანალიტიკური მეთოდების შექმნით. . 1923 წელს შვედმა ქიმიკოსმა თეოდორ სვედბერგმა დააპროექტა ულტრაცენტრიფუგა და შეიმუშავა დალექვის მეთოდი მაკრომოლეკულების, ძირითადად ცილების, მოლეკულური წონის დასადგენად. სვედბერგის ასისტენტმა არნე ტისელიუსმა (1902–1971) იმავე წელს შექმნა ელექტროფორეზის მეთოდი, უფრო მოწინავე მეთოდი გიგანტური მოლეკულების განცალკევების მიზნით, რომელიც დაფუძნებულია ელექტრულ ველში დამუხტული მოლეკულების მიგრაციის სიჩქარის განსხვავებაზე. მე-20 საუკუნის დასაწყისში. რუსმა ქიმიკოსმა მიხაილ სემენოვიჩ ცვეტმა (1872–1919) აღწერა მცენარეული პიგმენტების გამოყოფის მეთოდი მათი ნარევის ადსორბენტით სავსე მილში გავლის გზით. მეთოდს ქრომატოგრაფია ეწოდა. 1944 წელს ინგლისელმა ქიმიკოსებმა არჩერ მარტინმა და რიჩარდ სინგმა შემოგვთავაზეს მეთოდის ახალი ვერსია: მათ შეცვალეს მილი ადსორბენტით ფილტრის ქაღალდით. ასე გაჩნდა ქაღალდის ქრომატოგრაფია - ერთ-ერთი ყველაზე გავრცელებული ანალიტიკური მეთოდი ქიმიაში, ბიოლოგიასა და მედიცინაში, რომლის დახმარებითაც 1940-იანი წლების ბოლოს და 1950-იანი წლების დასაწყისში შესაძლებელი გახდა სხვადასხვა ცილების დაშლის შედეგად წარმოქმნილი ამინომჟავების ნარევების ანალიზი. განსაზღვრეთ ცილების შემადგენლობა. მტკივნეული კვლევის შედეგად დადგინდა ინსულინის მოლეკულაში ამინომჟავების რიგი (ფრედერიკ სანგერი) და 1964 წლისთვის ეს ცილა სინთეზირებული იყო. დღეისათვის ბიოქიმიური სინთეზის მეთოდებით მიიღება მრავალი ჰორმონი, წამალი და ვიტამინი.

სამრეწველო ქიმია.
ალბათ ყველაზე მნიშვნელოვანი ეტაპი თანამედროვე ქიმიის განვითარებაში იყო მე-19 საუკუნეში შემოქმედება. სხვადასხვა კვლევითი ცენტრები, გარდა ფუნდამენტური, გამოყენებითი კვლევებისა. მე-20 საუკუნის დასაწყისში. არაერთმა ინდუსტრიულმა კორპორაციამ შექმნა პირველი სამრეწველო კვლევითი ლაბორატორიები. აშშ-ში 1903 წელს დაარსდა დუპონის ქიმიური ლაბორატორია, ხოლო 1925 წელს დაარსდა Bell-ის ლაბორატორია. 1940-იან წლებში პენიცილინის, შემდეგ კი სხვა ანტიბიოტიკების აღმოჩენისა და სინთეზის შემდეგ, გაჩნდა დიდი ფარმაცევტული კომპანიები, დაკომპლექტებული პროფესიონალი ქიმიკოსებით. მაკრომოლეკულური ნაერთების ქიმიის დარგში მუშაობას დიდი პრაქტიკული მნიშვნელობა ჰქონდა. მისი ერთ-ერთი დამფუძნებელი იყო გერმანელი ქიმიკოსი ჰერმან შტაუდინგერი (1881–1965), რომელმაც შეიმუშავა პოლიმერების სტრუქტურის თეორია. ხაზოვანი პოლიმერების წარმოების მეთოდების ინტენსიურმა ძიებამ გამოიწვია 1953 წელს პოლიეთილენის (Karl Ziegler) სინთეზი, შემდეგ კი სასურველი თვისებების მქონე სხვა პოლიმერები. დღესდღეობით პოლიმერული წარმოება ქიმიური მრეწველობის უდიდესი დარგია.
ქიმიის ყველა მიღწევა არ ყოფილა ადამიანისთვის სასარგებლო. მე-19 საუკუნეში საღებავების, საპნისა და ქსოვილების წარმოებაში გამოიყენებოდა მარილმჟავა და გოგირდი, რაც დიდ საფრთხეს უქმნიდა გარემოს. მე-20 საუკუნეში მრავალი ორგანული და არაორგანული მასალის წარმოება გაიზარდა გამოყენებული ნივთიერებების გადამუშავების გამო, ასევე ქიმიური ნარჩენების გადამუშავებით, რომლებიც საფრთხეს უქმნის ადამიანის ჯანმრთელობას და გარემოს.
ლიტერატურა:
ფიგუროვსკი ნ.ა. ნარკვევი ქიმიის ზოგადი ისტორიის შესახებ. მ., 1969 წ
ჯუა მ. ქიმიის ისტორია. მ., 1975 წ
აზიმოვი ა. ქიმიის მოკლე ისტორია. მ., 1983 წ
სლაიდი 2
ლავუაზიეს მეთოდი
გლობალური ცვლილებები ქიმიურ ფენომენებზე შეხედულებებში, რაც გამოწვეულია ფრანგი მეცნიერის ა.ლ. ლავუაზიეს ტრადიციულად ქიმიურ რევოლუციას უწოდებენ.
სლაიდი 3
ქიმიური რევოლუციის შედეგები
1. ფლოგისტონის თეორიის ჩანაცვლება წვის ჟანგბადის კონცეფციით; 2. ქიმიური შემადგენლობის მიღებული სისტემის გადასინჯვა; 3. ქიმიური ელემენტის ცნების გადახედვა; 4. იდეების ჩამოყალიბება ნივთიერებების თვისებების დამოკიდებულების შესახებ მათ ხარისხობრივ და რაოდენობრივ შემადგენლობაზე.
სლაიდი 4
ა.ლავუაზიემ თავის კვლევას საფუძველი ჩაუყარა ფიზიკურ-ქიმიურ მიდგომაზე, რომელიც გამოირჩეოდა ექსპერიმენტული მეთოდებისა და იმდროინდელი ფიზიკის თეორიული ცნებების თანმიმდევრული გამოყენებით. იმდროინდელ ფიზიკის თეორიულ შეხედულებებს შორის ცენტრალური როლი ითამაშა ი.ნიუტონის დოქტრინამ მიზიდულობის ძალის შესახებ. ამ მიზიდულობის საზომი არის სხეულის წონა, I. ნიუტონის პოზიციის მიხედვით წონის პროპორციულობასთან დაკავშირებით, შეიძლება განისაზღვროს ფიზიკური მეთოდებით (აწონით). ამ შეხედულებების შედეგი იყო წონის აღქმა, როგორც მატერიალური ნაწილაკების ყველაზე მნიშვნელოვანი თვისება. ანტუან ლორან ლავუაზიე 1743-1794 წწ
სლაიდი 5
ა. ლავუაზიემ დაიწყო სისტემურად ზუსტი აწონვის გამოყენება ქიმიურ რეაქციებში ნივთიერებების რაოდენობის დასადგენად. მრავალი მისი წინამორბედისგან განსხვავებით, ა.ლავუაზიემ აწონა ქიმიურ პროცესში ჩართული ყველა ნივთიერება (მათ შორის აირისებრი), ურთიერთმოქმედი ნივთიერებების მთლიანი წონის შენარჩუნების ზოგადი პრინციპის საფუძველზე. ანუ მისი რაოდენობრივი მეთოდი ემყარებოდა მატერიის კონსერვაციის აქსიომას - კლასიკური საბუნებისმეტყველო მეცნიერების ფუნდამენტურ პოზიციას, რომელიც გამოხატული იყო ძველ დროში. ა.ლავუაზიემ განსაზღვრა არა მარტო წონა, არამედ სხვა ფიზიკური მახასიათებლებისაწყისი მასალები და რეაქციის პროდუქტები (სიმკვრივე, ტემპერატურა და ა.შ.). სამომავლოდ რაოდენობრივი პარამეტრების გაზომვით შესაძლებელი გახდა უკვე ხარისხობრივად შესწავლილი ქიმიური გარდაქმნების დეტალური მექანიზმის გარკვევა.
სლაიდი 6
მან აწონილი რაოდენობა ვერცხლისწყალში მოათავსა, რომლის გრძელი მოხრილი კისერი დაუკავშირდა თხევად ვერცხლისწყალზე გადაბრუნებულ ზარს. ექსპერიმენტამდე იზომებოდა არა მხოლოდ ჰაერის მოცულობა ვერცხლისწყლის ზემოთ რეტორტში და ზარში, არამედ განისაზღვრა მთელი აპარატის წონა. რეტორტი შემდეგ თბებოდა 12 დღის განმავლობაში ვერცხლისწყლის თითქმის დუღილის წერტილამდე. თანდათანობით, ვერცხლისწყლის ზედაპირი რეტორტში წითელი ქერცლებით დაიფარა. როდესაც ამ ფანტელების (ვერცხლისწყლის ოქსიდის) რაოდენობამ ზრდა შეწყვიტა, ექსპერიმენტი შეჩერდა. მოწყობილობის გაგრილების შემდეგ გაკეთდა წარმოქმნილი პროდუქტების რაოდენობის ზუსტი დათვლა. გაირკვა, რომ: მთელი მოწყობილობის საერთო წონა არ შეცვლილა, ჰაერის მოცულობა შემცირდა, აღებული ჰაერის წონა შემცირდა ისევე, როგორც გაიზარდა ვერცხლისწყლის წონა (ოქსიდის წარმოქმნის გამო).
სლაიდი 7
სურათის დასასრულებლად საჭირო იყო მხოლოდ მიღებული ვერცხლისწყლის ოქსიდის შეგროვება, მისი დაშლა პრისტლის მეთოდის შესაბამისად და მიღებული ჟანგბადის რაოდენობის გაზომვა. როგორც მოსალოდნელი იყო, ასეთი ექსპერიმენტის გამეორებამ ლავუაზიეს ჟანგბადის იგივე რაოდენობა (შესაძლო შეცდომის ფარგლებში) მისცა, რაც ჰაერიდან ვერცხლისწყლით შეიწოვებოდა. ჟანგბადის მიღება ვერცხლისწყლის ოქსიდიდან (რეტორტი ა) პრისტლის მეთოდით. ვერცხლისწყალი გროვდება სფერულ ჭურჭელში b და ჟანგბადი გადის გაზის გამომავალი მილით c ცილინდრში d, სადაც ის გროვდება თხევადი ვერცხლისწყლის ზემოთ.
სლაიდი 8
ა.ლავუაზიემ ფოსფორიანი თეფში წყალში მცურავ კორპის სადგამზე მოათავსა, ფოსფორი ცხელი მავთულით დადგა და სწრაფად დააფარა მინის ზარი. სქელმა თეთრმა კვამლმა შეავსო სივრცე შიგნით. მალე ფოსფორი გაქრა, წყალმა დაიწყო ამოსვლა და ზარის შევსება. გარკვეული პერიოდის შემდეგ წყლის ამოსვლა შეწყდა. - როგორც ჩანს, ფოსფორი არ მიმიღია. მთელი ჰაერი ვერ აკავშირებდა მას. ჩვენ უნდა გავიმეოროთ ექსპერიმენტი. მაგრამ მეორე ექსპერიმენტმა ორმაგი რაოდენობით ფოსფორით მსგავსი შედეგი გამოიღო: წყალი იმავე დონემდე ავიდა. მეათეჯერ ჩატარებულმა ექსპერიმენტმაც კი იგივე შედეგი აჩვენა. - ფოსფორი ერწყმის ჰაერის მხოლოდ მეხუთედს. ჰაერი მართლაც რთული ნარევია?
სლაიდი 9
ლავუაზიემ ასევე შეისწავლა გოგირდის წვა. წვის დროს ის ასევე შერწყმულია ჰაერის მხოლოდ მეხუთედთან. ამის შემდეგ მეცნიერმა ლითონების წვის შესწავლა დაიწყო. გახანგრძლივებული კალცინაციით ლითონები გადაიქცევა ლითონის ნაცრად, მაგრამ ნახშირთან შერევისას და მაღალ ტემპერატურაზე გაცხელებისას ფერფლი კვლავ მეტალად გადაიქცევა. ამასთან, ამ პროცესმა წარმოქმნა გაზი, რომელსაც ქიმიკოსებმა უწოდეს "შემკავშირებელი ჰაერი" (ნახშირორჟანგი). ლავუაზიეს კარგად ესმოდა, რომ წვა აირებთან იყო დაკავშირებული, მაგრამ საბოლოო დასკვნის გაკეთება მაინც ვერ შეძლო. ამრიგად გაჩნდა გაზების შესწავლის საჭიროება. რა არის "შემაკავშირებელი ჰაერი"? შეიცავს კირქვას? როგორ წარმოიქმნება კირქვის გაცხელებისას და გადაქცევის დროს? ლავუაზიეს მიერ გამოყენებული მოწყობილობები
სლაიდი 10
ჰაერი ყოველთვის შეიწოვება წვის დროს? თუ ეს ასეა, რომელი ნივთიერებაა ამ შემთხვევაში უფრო რთული - ლითონი თუ ლითონის ნაცარი? ა. ლავუაზიე ცხადი იყო, რომ ჰაერი შედგება ორი ნაწილისაგან - ერთი მათგანი ხელს უწყობს წვას (ის ერწყმის ლითონებს კალცინაციისას), მეორე არ უწყობს ხელს წვას და მასში ცოცხალი ორგანიზმები იღუპებიან. წვის დროს სხეულები შთანთქავენ ჰაერის ამ აქტიურ ნაწილს, რომელსაც მან "კარგი ჰაერი" უწოდა. ეს ასევე ხსნის იმ ფაქტს, რომ მიღებული პროდუქტი უფრო მძიმეა ვიდრე ორიგინალი. მეცნიერი მივიდა დასკვნამდე, რომ წვა არ არის დაშლის პროცესი, არამედ ჰაერის ნაწილთან კავშირი. უფრო მეტიც, ჰაერის ეს ნაწილი არ ასრულებს ფლოგისტონის გამხსნელის მექანიკურ ფუნქციას, მაგრამ მონაწილეობს წვის პროცესის ქიმიაში, რაც იწვევს ახალ ნაერთებს. მეტალის ვერცხლისწყალი და ვერცხლისწყლის(II) ოქსიდი მეტალის სპილენძი და სპილენძის(II) ოქსიდი
სლაიდი 11
1775 წლის დასაწყისში ა. ლავუაზიე გახდა დენთის და მარილის ოფისის დირექტორი. ამასთან დაკავშირებით მან დაიწყო დენთის დასამზადებლად გამოყენებული მასალების კვლევა. ლავუაზიემ დაამტკიცა, რომ მარილი და აზოტის მჟავა შეიცავს „კარგ ჰაერს“; გოგირდი და ფოსფორი წვის დროს ერწყმის ამ ტიპის ჰაერს და მიღებულ ნივთიერებებს აქვთ მჟავების თვისებები. - ალბათ ყველა მჟავა შეიცავს ამ გაზს? - არაერთხელ დაუსვა საკუთარ თავს კითხვა. ლავუაზიემ ახალ გაზს ჟანგბადი უწოდა. ვერცხლისწყლის ოქსიდის დაშლაზე დაკვირვება რეტორტში
სლაიდი 12
წვის ჟანგბადის თეორიის ძირითადი პრინციპები ჩამოყალიბდა 1777 წელს. ამ თეორიის თანახმად, წვა შეიძლება მოხდეს მხოლოდ ჟანგბადის თანდასწრებით, რომელიც წარმოქმნის შუქს და ცეცხლს. დამწვარი ნივთიერების წონა იზრდება ზუსტად შეწოვილი ჰაერის რაოდენობით. როდესაც ლითონები იწვის, მეტალის ცაცხვი წარმოიქმნება ჟანგბადთან შერწყმის შედეგად. არალითონური ნივთიერებების – მჟავების სროლისას (ამ დროს ასე ეძახდნენ მჟავა ანჰიდრიდებს).
სლაიდი 13
ნახშირორჟანგის შემადგენლობის განსაზღვრა
ა. ლავუაზიემ აჩვენა, რომ ნახშირორჟანგი წარმოიქმნება ნახშირის წვის დროს და ასევე გამოიყოფა მრავალი ბუნებრივი (ორგანული) სხეულის წვის დროს. ამან ა. ლავუაზიეს შესაძლებლობა მისცა შემოგვეთავაზებინა მოსახერხებელი მეთოდი ორგანული ნივთიერებების ხარისხობრივი და რაოდენობრივი შემადგენლობის დასადგენად. ნახშირორჟანგის შემადგენლობის განსაზღვრამ ა. ლავუაზიეს საშუალება მისცა გამოეხატა სუნთქვის ქიმიის სწორი გაგება (ჟანგბადის შეწოვა და ნახშირორჟანგის გამოყოფა), რომლის ახლო ანალოგია წვის პროცესებთან უკვე არაერთხელ აღინიშნა (ჯ. Mayow, G. Boerhaave, J. Priestley და სხვ.) ქიმიური მოწყობილობა გაზებთან ექსპერიმენტებისთვის. A.L. Lavoisier-ის წიგნიდან "ანტიფლოგისტონის ქიმიის საფუძვლები". გამოცემა 1792 წ
სლაიდი 14
ნახშირორჟანგის წარმოქმნის მეთოდებისა და თვისებების შესწავლამ ა. ლავუაზიეს საშუალება მისცა გაეფართოებინა წვის ჟანგბადის თეორია და აეხსნა მრავალი ქიმიური პროცესი ნივთიერებების დაჟანგვა-აღდგენის თვალსაზრისით. ანუ წვის პროცესების შესწავლიდან მეცნიერი გადავიდა ზოგადად ჟანგვის რეაქციების შესწავლაზე. მაგალითად, ა. ლავუაზიემ შეისწავლა რეაქციები: 2Fe2O3 + 3C = 3CO2 + 4Fe 2Fe + 3H2O = Fe2O3 + 3H2 წითელი რკინის მადანი (ჰემატიტი) Fe2Oz ქვანახშირი.
სლაიდი 15
წყლის შემადგენლობის დადგენა
და მაინც ვერ იპოვა პასუხი ერთ კითხვაზე; ეს ეხებოდა „აალებადი ჰაერის“ წვას, რომელიც მიიღება მჟავაში ლითონების გახსნით და ადვილად იწვებოდა. ახალი თეორიის მიხედვით, პროდუქცია უფრო მძიმე უნდა ყოფილიყო, ლავუაზიეს აზრით, მათი სრულად დაჭერა შეუძლებელი იყო, წონა კი ყოველთვის ნაკლები იყო. აქ სხვა სირთულე იყო. მჟავების თეორიის თანახმად, „აალებადი ჰაერი“ (წყალბადი) ჟანგბადთან შერწყმის შემდეგ უნდა: წარმოქმნას მჟავა, მაგრამ მისი მიღება შეუძლებელი იყო.
სლაიდი 16
ლავუაზიემ გადაწყვიტა განეხილა ეს რთული პრობლემა ინგლისიდან ჩამოსულ ფიზიკოს და ქიმიკოს ჩარლზ ბლაგდენთან, რომელსაც მან დეტალურად უამბო თავისი წარუმატებელი ექსპერიმენტების შესახებ. - ჩემმა მეგობარმა ჰენრი კავენდიშმა დაამტკიცა, რომ თუ დახურულ ჭურჭელში ჩვეულებრივ ჰაერს "აალებადი ჰაერი" შეურევთ და ნარევს ცეცხლზე დააყენებთ, ჭურჭლის კედლებზე წარმოიქმნება პატარა წვეთები - "აალებადი ჰაერის" წვის პროდუქტი. კავენდიშმა დაადგინა, რომ ეს იყო წყლის წვეთები. - საოცარი აღმოჩენა. ეს ნიშნავს, რომ წყალი არ არის ელემენტი, არამედ რთული ნივთიერება. მსურს დაუყოვნებლივ გავიმეორო ეს ექსპერიმენტები და თავად ვნახოთ. G. Cavendish-ის მოწყობილობა წყალბადის წარმოებისა და შეგროვებისთვის
სლაიდი 17
ა.ლავუაზიემ ჩაატარა ექსპერიმენტი აალებადი ჰაერიდან და ჟანგბადიდან წყლის სინთეზზე გ.კავენდიშისა და ჯ. ვატის მსგავსი ექსპერიმენტების შემდეგ (ა. ლავუაზიეს პარალელურად მსგავსი ექსპერიმენტები ჩაატარა გ.მონჯმა), მაგრამ ამ მეცნიერებისგან განსხვავებით, ა. ლავუაზიემ ეს სინთეზი განმარტა ჟანგბადის თეორიის პოზიციიდან და აჩვენა, რომ „წვადი ჰაერი“ (რომელსაც მან შესთავაზა სახელი „წყალბადის“ დარქმევა) და ჟანგბადი ელემენტებია და წყალი მათი ნაერთია. (ექსპერიმენტის დროს წყლის შემადგენლობის დადგენა წყალბადისა და ჟანგბადის ნარევის ელექტრული ნაპერწკალით აალებით)
სლაიდი 18
ექსპერიმენტების შედეგად ა.ლავუაზიე მივიდა დასკვნამდე, რომ ნივთიერებათა წონის შენარჩუნების კანონი უნივერსალური კანონია. ჟანგვის თეორია ასევე ზოგადია და არ არსებობს გამონაკლისი. წყალი, მჟავები და ლითონის ოქსიდები რთული ნივთიერებებია, ხოლო ლითონები, გოგირდი და ფოსფორი მარტივი ნივთიერებებია. ამან მთლიანად შეცვალა შეხედულებები ქიმიური ნაერთების შემადგენლობის მთელ სისტემაზე. ფლოგისტონი არ არსებობს, ჰაერი კი აირების ნაზავია. ა. ლავუაზიემ ეს აზრები გამოუცხადა აკადემიკოსებს, რომლებსაც მან აჩვენა თავისი ექსპერიმენტები. თუმცა, მათ უმეტესობას არ სურდა ლავუაზიეს შემოქმედების აღიარება, მას ბრალი დასდეს პრისტლისა და კავენდიშის კვლევებიდან. აკადემიკოსებმა არაერთხელ განაცხადეს, რომ მათ იციან მსგავსი ექსპერიმენტები წყლის დაშლის შესახებ, რაც გულისხმობს გასპარ მონჯს. ლავუაზიეს პრიორიტეტი არ იქნა აღიარებული. კვლევებში ძალების გაერთიანების ნაცვლად, მეცნიერები კამათობდნენ იმაზე, თუ ვინ აღმოაჩინა ეს ფენომენი.
სლაიდი 19
სამეცნიერო სამყაროში მხარდაჭერა რომ არ ჰპოვა, ლავუაზიემ მაინც განაგრძო მოღვაწეობა. ახლა ის თანამშრომლობდა ცნობილ ფიზიკოსთან და მათემატიკოსთან პიერ სიმონ ლაპლასთან. მათ მოახერხეს სპეციალური აპარატის აგება, რომლითაც შესაძლებელი იყო ნივთიერებების წვის შედეგად გამოთავისუფლებული სითბოს გაზომვა. ეს იყო ეგრეთ წოდებული ყინულის კალორიმეტრი. მკვლევარებმა ასევე ჩაატარეს ცოცხალი ორგანიზმების გამოსხივებული სითბოს დეტალური შესწავლა. ამოსუნთქული ნახშირორჟანგის რაოდენობისა და ორგანიზმის მიერ გამომუშავებული სითბოს გაზომვით დაამტკიცეს, რომ საკვები ორგანიზმში განსაკუთრებული გზით „იწვის“. ამ წვის შედეგად წარმოქმნილი სითბო ემსახურება სხეულის ნორმალური ტემპერატურის შენარჩუნებას. ლავუაზიე-ლაპლასის ყინულის კალორიმეტრმა მე-18 საუკუნეში შესაძლებელი გახადა მრავალი ადამიანის სითბოს სიმძლავრის გაზომვა. მყარიდა სითხეები, ასევე სხვადასხვა საწვავის წვის სითბო და ცოცხალი ორგანიზმების მიერ გამოთავისუფლებული სითბო. მაგალითად, შიდა პალატაში ცხოველის (ან სხვა საგნის) მიერ გამოყოფილი სითბო იხარჯებოდა შიდა „ყინულის ქურთუკში“ ყინულის დნობაზე. გარე ემსახურებოდა შიდა ნაწილის ტემპერატურის მუდმივ შენარჩუნებას. გამოთავისუფლებული სითბო იზომებოდა დნობის წყლის აწონვით, რომელიც ჭურჭელში ჩადიოდა.
სლაიდი 20
ლაპლასი დარწმუნებული იყო ლავუაზიეს შეხედულებების სისწორეში და პირველმა მიიღო მისი თეორია. 1785 წელს კლოდ ლუი ბერტოლე, რომელიც იმ დროს გახდა ძალიან ცნობილი, გამოვიდა ლავუაზიეს თეორიის მხარდასაჭერად. ცოტა მოგვიანებით, ლავუაზიეს მხარი დაუჭირეს მაშინდელმა ყველაზე გამოჩენილმა ქიმიკოსებმა ანტუან ფურკრუამ და გიტონ დე მორვომ. ლაპლას პიერ-სიმონი 1749 -1827 ფრანგი მათემატიკოსი, მექანიკოსი, ფიზიკოსი და ასტრონომი FourcroyAntoine-François (1755-1809) ფრანგი ქიმიკოსი და პოლიტიკური მოღვაწე
სლაიდი 21
"ელემენტის" კონცეფციის გადახედვა
მეთოდოლოგიურად, ქიმიაში რევოლუციის მნიშვნელოვანი შედეგი, რომელიც წარმოიქმნა ა.ლ. ლავუაზიეს, მოხდა ცვლილება „ქიმიური ელემენტის“ კონცეფციის შინაარსში. ელემენტების განხილვა დაიწყო არა როგორც მისი დაშლის პროდუქტები, რომლებიც ადრე არსებობდა ობიექტში, არამედ როგორც საბოლოო ზღვარი, რომლითაც შესაძლებელია ნივთიერებების დაშლა პრინციპში. ელემენტები დაიწყო ფიქრი, როგორც მატერიალური, ანალიტიკურად განსაზღვრული შემადგენლობის ფრაგმენტები, განუყოფელი თვისობრივად ახალ წარმონაქმნებში და შენახული რთული სხეულების ნებისმიერი ქიმიური გარდაქმნის პროცესში, რომელსაც ისინი ქმნიან.
სლაიდი 22
ანალიზის წონის მეთოდის გამოყენების წყალობით, ა. ლავუაზიეს ნაშრომებში ჩამოყალიბდა იდეები ელემენტების შეზღუდული ნაკრებისა და მათი ხარისხობრივი ჰეტეროგენურობის შესახებ. ამან გამოიწვია ქიმიური ნივთიერებების მრავალფეროვნების ახსნის მიდგომა, როგორც მრავალფეროვანი ხარისხობრივი და რაოდენობრივი ელემენტარული შემადგენლობის შედეგი. ითვლებოდა, რომ თითოეულ თვისობრივად განსაზღვრულ ნივთიერებას ყოველთვის აქვს ზუსტად განსაზღვრული და უნიკალური რაოდენობრივი შემადგენლობა. ცვლადი შემადგენლობის მქონე ნაერთები (ბერთოლიდები) და იზომერიზმის ფენომენი იმ დროისთვის ცნობილი არ იყო. ა.ლავუაზიეს მოწყობილობა ორგანული ნივთიერებების ელემენტარული ანალიზისთვის
სლაიდი 23
მჟავიანობის პრობლემა
მე-18 საუკუნეში მეცნიერმა ქიმიკოსებმა აჩვენეს ინტერესი მჟავიანობის პრობლემისადმი არანაკლებ წვის პრობლემის მიმართ, რადგან ორივე ეს პრობლემა შეესაბამებოდა იმდროინდელი ანალიტიკური კვლევის ორ ძირითად მიმართულებას (დაშლა „მშრალი გზა“ - ცეცხლის დახმარებით და "სველი გზა" - მჟავების დახმარებით). A. Lavoisier-ის შრომების გამოქვეყნებამდე ითვლებოდა, რომ ყველა მჟავა შეიცავს თავის შემადგენლობაში გარკვეულ ერთპირველ მჟავას, რომელიც მთელ ნაერთს აძლევს მჟავიანობის ხარისხს. ა. ლავუაზიემ, გოგირდის, ფოსფორისა და აზოტის მჟავების (თანამედროვე კონცეფციებში - SO3, P2O5, N2O5) დაშლის ექსპერიმენტებზე დაყრდნობით, მჟავიანობის თვისება დაუკავშირა ამ ნაერთებში ჟანგბადის არსებობას (აქედან გამომდინარე, სახელწოდება ჟანგბადი - ოქსიგენიუმი - მჟავა წარმომქმნელი, მჟავე პრინციპი). მჟავები, ა. ლავუაზიეს აზრით, განსხვავდებიან ერთმანეთისგან, რადგან ისინი დაკავშირებულია ჟანგბადთან, მჟავას რადიკალთან. ჟანგბადი ითვლებოდა მჟავების აუცილებელ ელემენტად და, გარკვეული პერიოდის განმავლობაში, მურაბის (ჰიდროქლორინის) მჟავაც კი წარმოდგენილი იყო ჟანგბადთან ერთად მურაბის რადიკალის ნაერთად, ხოლო ქლორი ითვლებოდა მურაბის მჟავას ოქსიდად.
სლაიდი 24
ქიმიური ელემენტების პირველი კლასიფიკაცია და ახალი ნომენკლატურა
გიტონ დე მორვო პირველად შეხვდა ლავუაზიეს წვის თეორიის შესახებ: ”არ ვიცი, რამდენად გაინტერესებთ, მაგრამ ქიმიური ნაერთების სახელები სრული ქაოსია”. - სრულიად გეთანხმები. - ამჟამად გამოსაცემად მზადდება მეთოდოლოგიური ენციკლოპედიის ქიმიური განყოფილება. და რადგან, ჯერ კიდევ არსებული სახელების გამოყენებით, შეუძლებელია ყველა კითხვაზე ამომწურავი პასუხის გაცემა, დავიწყე ქიმიური ნაერთების ახალი ნომენკლატურის შედგენა. რა თქმა უნდა, მჭირდება წამყვანი ქიმიკოსების დახმარება. გიტონ დე მორვო ლუი ბერნარდი (1737-1816) ფრანგი ქიმიკოსი და პოლიტიკოსი.
სლაიდი 25
წვის თეორიაზე და ამ პროცესში ჟანგბადის როლზე დაყრდნობით, შემიძლია რამდენიმე ვარაუდის გაკეთება. ავიღოთ ლითონის ნაცარი - ლითონის ნაერთი ჟანგბადთან. მოდით ვუწოდოთ ელემენტების კომბინაცია ჟანგბადის ოქსიდებთან. მაშინ თუთიის ნაცარი იქნება თუთიის ოქსიდი, რკინის ნაცარი იქნება რკინის ოქსიდი და ა.შ. რა არის "შემაკავშირებელი ჰაერი"? მე უკვე დავამტკიცე, რომ ეს არის ნახშირბადის და ჟანგბადის ნაერთი. ამიტომ მას ნახშირბადის მონოქსიდი უნდა ეწოდოს. 1787 წელს გიტონ დე მორვომ გამოაქვეყნა "ქიმიური ნომენკლატურის მეთოდი", რომლის შექმნაში მონაწილეობა მიიღეს ლავუაზიემ, ფურკრუამ და ბერტოლეტმა. ლავუაზიეს უბრალო მყარი ცხრილი
სლაიდი 26
კონვერტაცია ქიმიური ენაეს იყო ქიმიის გლობალური ცვლილებების შედეგი და მიზნად ისახავდა თითოეულ ნივთიერებას მიენიჭებინა სახელი, რომელიც დაახასიათებდა მის შემადგენლობას და ქიმიურ თვისებებს (ამ მომენტამდე, ერთ ნივთიერებას შეიძლება ჰქონოდა მრავალი სახელი, რომელსაც ხშირად შემთხვევით ეძახდნენ). ახალ ნომენკლატურაში თითოეული ნივთიერება განიხილებოდა მისი ზოგადი (მაგალითად, მჟავა) და სპეციფიკური თვისებების (მაგალითად, გოგირდის, აზოტის, ფოსფორის მჟავის) თვალსაზრისით. სპეციფიკური თვისებები განისაზღვრა ელემენტარული შემადგენლობის მონაცემების საფუძველზე. ნომენკლატურამ მნიშვნელოვნად შეუწყო ხელი ქიმიური ინფორმაციის გაცვლას მისი ძირითადი პრინციპები, ზოგადად, დღემდეა შემონახული. ა.ლ. ლავუაზიე
სლაიდი 27
ლავუაზიე იმ დროს მუშაობდა თავის ერთ-ერთ უდიდეს ქმნილებაზე - ქიმიის სახელმძღვანელოზე, რომლის შედგენის აუცილებლობა დიდი ხნის წინ იყო გადასული. საჭირო იყო ბუნებაში არსებული ფენომენების ახლებურად ახსნა, თანამედროვე თეორიების საფუძვლების მკაფიოდ ჩამოყალიბება. ახალი მიღწევები ქიმიაში არ იყო ასახული კრისტოფლ გლაზერისა და ნიკოლას ლემერის ძველ სახელმძღვანელოებში. 1788 წლის ბოლოს სახელმძღვანელო მზად იყო. ხელნაწერის მომზადების დიდი დამსახურება ეკუთვნოდა მადამ ლავუაზიეს, რომელმაც მხატვრულად შექმნა სახელმძღვანელოს მესამე ნაწილი.
სლაიდი 28
ა.ლავუაზიეს სახელმძღვანელოს პირველი ნაწილი მოიცავდა წვის ჟანგბადის თეორიის პრეზენტაციას, აირების ფორმირებისა და დაშლის ექსპერიმენტების აღწერას, მარტივი ნივთიერებების წვას, მჟავების წარმოქმნას, ატმოსფეროს შემადგენლობის აღწერას და წყალი და ახალი ნომენკლატურა. მეორე ნაწილი მოიცავდა „მარტივი სხეულების ცხრილს“, რომელიც პრაქტიკულად ქიმიური ელემენტების პირველი კლასიფიკაცია იყო (სულ წარმოდგენილი იყო 33 ელემენტი). ცხრილი შეიცავდა როგორც რეალურ ელემენტებს, ასევე ზოგიერთ ნაერთს (მაგალითად, ტუტე ლითონის ოქსიდებს), რომელთა დაშლა იმ დროს არ შეიძლებოდა (მაგრამ, როგორც ა. ლავუაზიემ აღნიშნა, შემდგომში შეიძლებოდა დაშლა). ცხრილში ორი პრინციპი ჩანს ელემენტების სახით - კალორიული და წყალბადი, რომლებსაც წონა არ აქვთ, მაგრამ მათი გარეგნობა მუდმივად დაკავშირებულია ქიმიურ პროცესებთან. ა. ლავუაზიეს სახელმძღვანელოს სათაური
სლაიდი 29
სითბოს და სინათლის ელემენტების მიკუთვნება იმდროინდელ ფიზიკაში კალორიების თეორიის გავრცელების შედეგი იყო. ამ თეორიაში სიცხე განიხილებოდა, როგორც ატმოსფეროს სახეობა, რომელიც გარს აკრავს ყველა სხეულის ნაწილაკს და არის ნაწილაკების ერთმანეთისგან მოგერიების მიზეზი. ლავუაზიე მიდრეკილი იყო აეხსნა სითბოს შთანთქმის ფენომენი ქიმიურ რეაქციებში, აგრეთვე ნივთიერებების მყარიდან თხევადში და თხევადიდან აირისებურ მდგომარეობაში გადასვლისას, კალორიულობის მატერიასთან შერწყმის შედეგად. მას სჯეროდა, რომ ნივთიერების მყარი, თხევადი და აირისებრი მდგომარეობა დამოკიდებულია მასში შემავალ სითბოს რაოდენობაზე, განსხვავებით ადრინდელი იდეებისგან აირების შესახებ, რომლებიც აბსოლუტურად არ კონდენსირებადია სითხეებში, "არააორთქლებადი" სითხეები და მუდმივი მყარი.
სლაიდი 30
ლავუაზიე წერდა, რომ მყარ მდგომარეობაში მიზიდულობის ძალები ნაწილაკებს შორის, რომლებიც ქმნიან სხეულს, აღემატება მოგერიების ძალებს, თხევად მდგომარეობაში ისინი გასწორებულია, ხოლო აირის მდგომარეობაში, კალორიის გავლენის ქვეშ, ჭარბობს მოგერიების ძალები. მიზიდულობის ძალებზე. ყველა მატერიალური მაკრო ნივთიერების უნარის არსებობის იდეა აგრეგაციის სხვადასხვა მდგომარეობაში გახდა ქიმიური რევოლუციის კიდევ ერთი მნიშვნელოვანი ასპექტი.
სლაიდი 31
ქიმიური განტოლებების ჩაწერის საფუძვლები
ქიმიურ რეაქციებში ელემენტების კონსერვაციის კანონისა და ნივთიერებათა მასის შენარჩუნების კანონის ექსპერიმენტულმა დასაბუთებამ საშუალება მისცა ა.ლავუაზიეს შემოეტანა ქიმიური განტოლებების შედგენა, ე.ი. ქიმიური გარდაქმნების მატერიალური ნაშთები. ა.ლავუაზიე წერდა: „აუცილებელია ვივარაუდოთ ტოლობის ან განტოლების არსებობა შესასწავლი ორგანოების პრინციპებსა (ელემენტებს) და ამ უკანასკნელისგან ანალიზით მიღებულს შორის“. ქაღალდის (ა) და სპილენძის (ბ) რეაქცია ჟანგბადთან
სლაიდი 32
მიხაილ ვასილიევიჩ ლომონოსოვი 1711-1765 უნდა აღინიშნოს, რომ ა.ლავუაზიეს მოღვაწეობამდე დიდი ხნით ადრე მატერიის აგებულების შესახებ ორიგინალური შეხედულებები გამოთქვა რუსმა მეცნიერმა მ.ვ. ლომონოსოვი. წიგნში "მათემატიკური ქიმიის ელემენტები" მან დაწერა, რომ ყველა სხეული შედგება სხეულებისგან, რომლებიც თავის მხრივ შეიცავს ელემენტთა გარკვეულ რაოდენობას. კორპუსები ერთგვაროვანია, თუ ისინი შედგებიან ერთი და იგივე ელემენტების ერთი და იგივე რაოდენობისგან, რომლებიც ერთმანეთთან დაკავშირებულია იმავე გზით. კორპუსკულები ჰეტეროგენულია, თუ მათი ელემენტები არ არის იდენტური და ურთიერთდაკავშირებულია სხვადასხვა გზითან შიგნით სხვადასხვა ნომრები. სხეულების უსასრულო მრავალფეროვნება ამაზეა დამოკიდებული.
სლაიდი 33
სხეულები მარტივია, როდესაც ისინი შედგება ერთგვაროვანი კორპუსკულებისგან და შერეულია, როდესაც ისინი შედგება რამდენიმე განსხვავებული კორპუსკულისგან. სხეულების თვისებები არ არის შემთხვევითი, ისინი დამოკიდებულია მათი შემადგენელი კორპუსების თვისებებზე. განვიხილოთ პირველი - სითბო. რას წარმოადგენს ის? უწონო სითხე, რომელსაც შეუძლია მიედინება ერთი სხეულიდან მეორეში? არა. გალილეოს ასევე სჯეროდა, რომ სხეულები მოძრაობდნენ. ჩემი აზრით, ეს არის კორპუსკულების პირველი და მთავარი თვისება. მაგრამ მოძრაობა ქმნის სითბოს. ყველამ იცის, რომ როდესაც ბორბალი ბრუნავს, მისი ღერძი თბება. სხეულის სხეულები მოძრაობენ, ბრუნავენ საკუთარი ღერძის გარშემო, იბნევიან ერთმანეთს და ქმნიან სითბოს...
სლაიდი 34
ეილერისადმი მიწერილ წერილში მიხაილ ვასილიევიჩმა გამოაქვეყნა თავისი შეხედულებები ბუნებაში გარდაქმნების შესახებ: „ბუნებაში მომხდარი ყველა ცვლილება ხდება ისე, რომ თუ რაღაცას ემატება, ის სხვას ართმევს. ამგვარად, იმდენი მატერია ემატება ერთ სხეულს, იგივე რაოდენობა იკარგება მეორისგან, რამდენ საათს ვატარებ ძილში, იგივე რაოდენობას ვიღებ სიფხიზლისგან და ა.შ. ვინაიდან ეს ბუნების უნივერსალური კანონია, ის ასევე მოქმედებს. მოძრაობის წესებს: სხეული, რომელიც თავისი ბიძგით აღაგზნებს სხვას გადაადგილებისკენ, კარგავს იმდენს თავისი მოძრაობიდან, რამდენსაც გადასცემს სხვას, მოძრაობს...“ - აზრები, რომლებიც ლომონოსოვამდე არავის გამოუთქვამს.
სლაიდი 35
რატომ გახსნა ბოილმა ჭურჭელი გათბობის შემდეგ? ასეთ შემთხვევაში, გემებიდან შეიძლება რაღაც აორთქლდეს და მათი წონა შეიცვალოს. აუცილებელია ექსპერიმენტების გამეორება, მაგრამ ყველა დაკვირვება და გაზომვა ჩაატარეთ დახურულ ჭურჭელში. მასში ჰაერია. ლომონოსოვმა მოამზადა სპეციალური ჭურჭელი, ჩაასხა მასში ტყვიის შიგთავსი, შემდეგ ცეცხლს ააფეთქა და ჭურჭლის ყელი გაახურა, სანამ მინა არ დარბილდებოდა. სამაგრის გამოყენებით დალუქა ჭიქა და ჭურჭელი მაშინვე ცეცხლზე დადო. ახლა ის სრულიად დარწმუნებული იყო, რომ ჭურჭელში არაფერი მოხვდებოდა და ვერაფერი გაექცევა. ბოლოჯერ ადიდდა ბუზი და ახლა ცისფერი ალი ნახშირის წითელ გროვაში გაქრა. ლომონოსოვმა ჭურჭელი ფრთხილად დადო მაგიდაზე და დაიწყო შემდეგის მომზადება. ექსპერიმენტის არაერთხელ გამეორება მოუხდა არა მარტო ტყვიის, არამედ სხვა ლითონების: რკინის, სპილენძის...
სლაიდი 36
ლომონოსოვმა აწონა გაცივებული ჭურჭელი, მოათავსა ნახშირზე დიდ ღუმელში და ცეცხლის დანთება დაიწყო. თავიდან ბუზი ნელა მუშაობდა, მაგრამ თანდათან ჰაერის ნაკადი გაძლიერდა და მასთან ერთად მოლურჯო ალი გაჩნდა. ჭურჭლის კედლები გაწითლდა და ტყვიის ნარჩენები დნება. ცქრიალა მოვერცხლისფრო-თეთრი წვეთები სწრაფად დაიფარა მონაცრისფრო-მოყვითალო საფარით. წითელი სპილენძის ნარჩენები გადაიქცა შავ-ყავისფერ ფხვნილად. რკინის ჩირქები გაშავდა. მაინტერესებს „კალორიული“ ხომ არ შევიდა ჭურჭელში? შერწყმულია ლითონებთან? თუ ასეა, მაშინ გემის წონა უნდა გაიზარდოს. მაგრამ სასწორმა აჩვენა, რომ ყველა ჭურჭლის წონა უცვლელი დარჩა!
სლაიდი 37
რაც შეეხება ლითონის ნაცარს? მისი წონა უნდა შევადაროთ ლითონის წონას. მეორე დღეს მკვლევარმა გაიმეორა ექსპერიმენტები. მან ჭურჭლის დალუქვამდე აწონა ლითონის ნაყარი. კალცინაციის შემდეგ მან ისევ აწონა ჭურჭელი, შემდეგ გახსნა და მიღებული ლითონის ნაცარი აწონა. ნაცარი უფრო მძიმე იყო, ვიდრე ადრე აღებული ლითონი! - ეს ექსპერიმენტები უარყოფს რობერტ ბოილის აზრს. ლითონები არ ერწყმის "კალორიას": ხომ არ იცვლება ხომალდის წონა. ეს უდაოა. და მაინც ნაცარი უფრო მძიმეა. - ისევ გაიფიქრა ლომონოსოვმა. თუმცა ჭურჭელში ჰაერის გარკვეული რაოდენობა იყო... იქნებ ლითონები ჰაერის კორპუსებს ერწყმის? ვინაიდან ჭურჭელში ლითონის ფერფლი უფრო მძიმე გახდა, ეს ნიშნავს, რომ ჭურჭელში ჰაერი წონაში იმავე რაოდენობით შემცირდა. გარე ჰაერის მიწოდების გარეშე ლითონის წონა უცვლელი დარჩება! ეკატერინე II-ის ვიზიტი ლომონოსოვის ლაბორატორიაში
სლაიდი 38
ცხოვრობდა ეპოქაში, როდესაც ქიმია ახლახან ჩნდებოდა, როგორც მეცნიერება, ლომონოსოვმა შეძლო, ფლოგისტონის თეორიის არასწორი იდეების მიუხედავად, მიაღწია ისეთ განზოგადებებს, რომლებიც დღესაც ქმნიან ფიზიკურ და ქიმიურ მეცნიერებას. მან პირველმა ჩამოაყალიბა მატერიისა და ენერგიის შენარჩუნების კანონი, პირველმა მიუთითა გზა, რომელსაც მრავალი მეცნიერი გაჰყვა.
ყველა სლაიდის ნახვა
ქიმიური რევოლუცია
საფრანგეთის ბურჟუაზიული რევოლუცია და მეცნიერება
რევოლუცია ქიმიაში, რომელიც დაკავშირებულია ფლოგისტონის თეორიის დამხობასთან, დაემთხვა საფრანგეთის ბურჟუაზიულ რევოლუციას. ეს ფაქტი, რა თქმა უნდა, შემთხვევით არ შეიძლება ჩაითვალოს. ქიმიური რევოლუცია მეტწილად საზოგადოების ფსიქიკურ ცხოვრებაში სოციალურ-ეკონომიკური ცვლილებებისა და ძვრების შედეგი იყო. ფ. ენგელსი ამ ფენომენებს შემდეგი სიტყვებით ახასიათებდა: „დიდი ხალხი, ვინც საფრანგეთში მოახლოებული რევოლუციისთვის თავი გაანათა, თავად იქცეოდნენ უკიდურესად რევოლუციურად. ისინი არ ცნობდნენ რაიმე სახის გარე ხელისუფლებას. რელიგია, ბუნების, საზოგადოების, პოლიტიკური სისტემის გაგება - ეს ყველაფერი ყველაზე დაუნდობელ კრიტიკას ექვემდებარებოდა; ყველაფერი უნდა გამოსულიყო გონების სასამართლოს წინაშე და ან გაემართლებინა თავისი არსებობა, ან მიატოვა იგი... საზოგადოების და სახელმწიფოს ყველა წინა ფორმა, ყველა ტრადიციული იდეა აღიარებული იყო არაგონივრულად და გადაყრილი, როგორც ძველი ნაგავი; სამყარო აქამდე მხოლოდ ცრურწმენებით ხელმძღვანელობდა და მთელი წარსული მხოლოდ სინანულისა და ზიზღის ღირსია“.
ქიმიური რევოლუცია ასევე იყო მეცნიერების ღრმა ცვლილებების ნაწილი, პირველ რიგში ქიმიასა და ფიზიკაში.
არაერთი ფრანგი მეცნიერი უშუალო მონაწილეობას იღებდა რევოლუციის დროს სოციალურ და პოლიტიკურ საქმიანობაში (გ. მონჟი, ლ. კარნო, ფ. ფურკრუა და სხვ.). მათი წინადადებით ქვეყანაში განათლების სრული რეფორმა განხორციელდა. რევოლუციამდელი საფრანგეთის უნივერსიტეტები მთლიანად კათოლიკური სასულიერო პირების გავლენის ქვეშ იყო, ისინი ასწავლიდნენ მოძველებული სისტემით. არ არსებობდა კავშირი უნივერსიტეტებსა და ქვეყნის ინდუსტრიას შორის. პარიზის მეცნიერებათა აკადემია და სხვა სამეცნიერო დაწესებულებებიც ფაქტობრივად განქორწინებული იყო ცხოვრებისგან. მეცნიერთა წინადადებების შედეგად 1793 წელს კონვენციამ დაამტკიცა უმაღლესი განათლების ორგანიზების ახალი სისტემა. 1794 წელს დაარსდა ნორმალური სკოლა სწავლების ხელოვნების შესასწავლად და გაიხსნა პოლიტექნიკური სკოლა სამოქალაქო ინჟინრების მოსამზადებლად. გაჩნდა სხვა სპეციალური საგანმანათლებლო დაწესებულებებიც. ძველი სამეფო ბოტანიკური ბაღი გადაკეთდა ბუნების ისტორიის მუზეუმად. დაარსდა მეცნიერებათა და ხელოსნობის ეროვნული კონსერვატორია (საცავი). ყველა ეს ღონისძიება მიზნად ისახავდა მეცნიერებისა და განათლების მიახლოებას ცხოვრებისა და წარმოების მოთხოვნებთან.
ბურჟუაზიული რევოლუციის ეპოქა საფრანგეთში მეცნიერების აყვავებით გამოირჩეოდა. მე-18 საუკუნის ბოლოს. დაწინაურდა საფრანგეთში
ბევრი ნიჭიერი მეცნიერი (J. Lagrange, G. Monge, N. Carnot, P. Laplace) და გამოჩენილი ქიმიკოსებისა და ბიოლოგების გალაქტიკა.
A. L. LAVOISIER
საფრანგეთის ბურჟუაზიული რევოლუციის ეპოქაში ქიმიის განვითარებაში ყველაზე გამორჩეული როლი ეკუთვნოდა A.L. Lavoisier-ს. ამ მეცნიერის გამორჩეული სამეცნიერო მოღვაწეობა შერწყმული იყო მსხვილი ბურჟუაზიისთვის დამახასიათებელ ბუნდოვან ფინანსურ ოპერაციებთან. ა.ლავუაზიეს სოციალურ-პოლიტიკურ შეხედულებებს არ შეიძლება ვუწოდოთ მოწინავე და მის ინოვაციურ სამეცნიერო მოღვაწეობასთან შესაბამისობაში.
ანტუან ლორან ლავუაზიე დაიბადა 1743 წლის 26 აგვისტოს. მან მიიღო სამართლის ხარისხი, მაგრამ დაინტერესებული იყო საბუნებისმეტყველო მეცნიერებებით, განსაკუთრებით ქიმიით, ასევე სწავლობდა ლიტერატურას. უნივერსიტეტის დამთავრების შემდეგ ა. ლავუაზიემ მიატოვა იურიდიული კარიერა და ყურადღება გაამახვილა საბუნებისმეტყველო დარგში მუშაობაზე. მან ჩაატარა რამდენიმე მინერალოგიური ექსკურსია, რომლის დროსაც დაინტერესდა მთელი რიგი მინერალებისა და სასმელი წყლის ქიმიური შემადგენლობით.
1764 წელს ა.ლავუაზიემ მონაწილეობა მიიღო პარიზის აკადემიის მიერ გამოცხადებულ კონკურსში ქუჩის განათების საუკეთესო მეთოდისთვის. ახალი ტიპის ნათურების შემუშავებისას მან გამოიჩინა დიდი გამძლეობა და მიიღო ოქროს მედალი. 1768 წელს ა.ლავუაზიე აირჩიეს მეცნიერებათა აკადემიის ადიუენტად და ამავე დროს გახდა მოსახლეობისგან გადასახადების აღების აქციონერი. უზარმაზარი მოგების მიღებით, ფერმის აქციონერები გარშემორტყმული იყვნენ ხალხის საერთო სიძულვილით. 1771 წელს იგი დაქორწინდა მდიდარი საგადასახადო ფერმერის, ანა მარია პოლცის ქალიშვილზე.
1775 წელს ა.ლავუაზიე დაინიშნა საფრანგეთში დენთის და მარილების ბიზნესის მენეჯერად. ის არსენალში გადავიდა და საკუთარი ხარჯებით კეთილმოწყობილი ლაბორატორია მოაწყო. აქ 15 წლის განმავლობაში ატარებდა ინტენსიურ ექსპერიმენტულ კვლევებს და მუდმივად მონაწილეობდა სხვადასხვა სამეცნიერო კომისიებში.
1789 წელს დაწყებულმა რევოლუციამ ა. ლავუაზიე ჩამოაშორა
სამეცნიერო მუშაობა ქიმიაში. რევოლუციის პირველ წლებში იგი დაინიშნა ეკონომიკური პრობლემები, იყო წონითა და ზომების კომისიის წევრი, ეროვნული ხაზინის კომისარი და ა.შ. მალევე დაიწყო ნეგატიური დამოკიდებულება რევოლუციის მიმართ.
1792 წელს, როიალისტებთან კავშირების გამო, გაათავისუფლეს დენთის ბიზნესის მენეჯერის თანამდებობიდან. 1792 წლის მარტში ეროვნული კრების დადგენილებით გაუქმდა მიწათმოქმედება. 1793 წლის აგვისტოში მეცნიერებათა აკადემია დაიხურა და იმავე წლის ოქტომბერში კონვენციამ გადაწყვიტა ყოფილი საგადასახადო ფერმერების დაპატიმრება. გამოძიების შემდეგ რევოლუციურმა ტრიბუნალმა 28 ყოფილ საგადასახადო ფერმერს, მათ შორის ა. ლავუაზიეს სიკვდილი მიუსაჯა. 1794 წლის 8 მაისს ლავუაზიეს გილიოტინა მოახდინეს.
ზოგიერთი მეცნიერი (ჯ. პრისტლი, ს. ბლაგდენი, ჯ. ვატი და სხვ.) კამათობდა მისი რიგი ძირითადი აღმოჩენების პრიორიტეტულობაზე. თუმცა უნდა აღინიშნოს, რომ ლავუაზიეს სახელის ირგვლივ მიმდინარე დებატებს ბურჟუაზიულ-ნაციონალისტური ელფერი აქვს.
წვის ჟანგბადის თეორია
ა. ლავუაზიეს ერთ-ერთი პირველი პუბლიკაცია იყო მემუარები „წყლის ბუნების შესახებ“ (1769 წ.). ნაშრომი მიეძღვნა წყლის მიწად გადაქცევის შესაძლებლობის საკითხს. 101 დღის განმავლობაში ა. ლავუაზიე აცხელებდა წყალს მინის პელიკანის ჭურჭელში და აღმოაჩინა (K. Scheele-ის მსგავსად) წყალში ნაცრისფერი მიწის ფოთლების წარმოქმნა. კ.შელესგან განსხვავებით ა.ლავუაზიემ არ ჩაატარა ამ დედამიწის ქიმიური ანალიზი, მაგრამ ჭურჭლისა და გამხმარი ფოთლების აწონვით დაადგინა, რომ ისინი მინის დაშლის შედეგად იყო მიღებული.
ამგვარად გადაჭრა კითხვა, რომელიც იმ დროს მეცნიერებს აწუხებდათ, ა. ლავუაზიემ გამოაქვეყნა კვლევა „ჰაერის ბუნების შესახებ“. შეისწავლა და გააანალიზა მონაცემები ჰაერის შეწოვის შესახებ სხვადასხვა ქიმიურ პროცესებში, მან შეადგინა ვრცელი კვლევის გეგმა: ”ოპერაციები, რომელთა მეშვეობითაც, - წერდა იგი, - შესაძლებელია ჰაერის შებოჭვის მიღწევა, არის: მცენარეების ზრდა, ცხოველი. სუნთქვა, ზოგიერთ შემთხვევაში - გამოწვა და ბოლოს, ზოგიერთი (სხვა) ქიმიური რეაქცია. მე დავთანხმდი, რომ ამ ექსპერიმენტებით უნდა დამეწყო“.
1772 წლის მეორე ნახევარში ა. ლავუაზიე უკვე დაკავებული იყო სხვადასხვა ნივთიერების, უპირველეს ყოვლისა, ფოსფორის წვის ექსპერიმენტებით. მან აღმოაჩინა, რომ ფოსფორის სრული წვისთვის საჭიროა დიდი რაოდენობით ჰაერი. ფლოგისტური იყო ის ახსნაც, რომელიც მან ამ ფაქტს მისცა. თუმცა, მან მალევე წარუდგინა მოგონება მეცნიერებათა აკადემიას, სადაც წერდა: „... აღმოვაჩინე, რომ წვის დროს გოგირდი საერთოდ არ იკლებს წონას, პირიქით, მატულობს, ანუ 1 ფუნტი გოგირდიდან შეგიძლიათ. მიიღეთ 1 ფუნტზე საგრძნობლად მეტი ვიტრიოლი... იგივე შეიძლება ითქვას ფოსფორზე;
ეს ზრდა ხდება ჰაერის უზარმაზარი რაოდენობის გამო, რომელიც შეკრულია წვის დროს“1. გარდა ამისა, ა. ლავუაზიე ვარაუდობს, რომ ლითონების მასის მატება კალცინაციის დროს აიხსნება აგრეთვე ჰაერის შეწოვით.
მომდევნო წელს ა. ლავუაზიემ დაიწყო ლითონების კალცინაციის კვლევა. ის ასევე იუწყება წვის პროცესებში ჰაერის შთანთქმის შემდგომ ექსპერიმენტებზე და საუბრობს (ჯერ არა კატეგორიული ფორმით) ჰაერში შემავალი ნივთიერების შესახებ და ასოცირდება წვის პროცესში ნივთიერებების წვასთან. ა. ლავუაზიემ ლითონების კალცირებაზე ექსპერიმენტების აღწერისას დაადასტურა ამ პროცესის დროს ჰაერის შთანთქმის ფაქტი.
წვის პროცესების და სხვადასხვა ნივთიერებებზე მაღალი ტემპერატურის ზემოქმედების ყოვლისმომცველი შესწავლისთვის ა.ლავუაზიემ ააგო დიდი ცეცხლგამჩენი მანქანა ორი დიდი ლინზათი, რომლის დახმარებითაც წვავდა ბრილიანტს. ყველა ამ კვლევის შედეგები სრულიად ეწინააღმდეგებოდა ფლოგისტონის თეორიას. ა. ლავუაზიე თავისი დასკვნების ჩამოყალიბებაში უკიდურესად ფრთხილად უნდა ყოფილიყო. მაგრამ მან განაგრძო გეგმის მიხედვით მუშაობა, სულ უფრო და უფრო რწმუნდებოდა ფლოგისტონის თეორიის სრულ უსაფუძვლობაში. 1774 წელს ა.ლავუაზიემ ამ თეორიაზე პირდაპირი შეტევა წამოიწყო. სხვადასხვა ნივთიერების დაწვაზე მისი ექსპერიმენტების შედეგების გაანალიზებით, ის მალე მივიდა დასკვნამდე, რომ ჰაერი არ არის მარტივი სხეული, როგორც მე-18 საუკუნის მეცნიერები ფიქრობდნენ, არამედ სხვადასხვა თვისებების მქონე აირების ნარევი. ნარევის ერთი ნაწილი მხარს უჭერს წვას. გამოცდილი გზაა. ლავუაზიემ უარყო ვარაუდი, რომ ეს არის ბლექის „ფიქსირებული ჰაერი“, პირიქით, იგი ამტკიცებდა, რომ ეს ნაწილი „სუნთქვისთვის ყველაზე კომფორტულია“.
ამ დროს (70-იანი წლები) ჟანგბადის აღმოჩენა "ჰაერში" იყო და გარდაუვალი გახდა. მართლაც, კ.შეილმა აღმოაჩინა ჟანგბადი 1772 წელს, ჯ.პრისტლიმ კი 1774 წელს. ა. ლავუაზიე მაშინვე არ მივიდა ჟანგბადის აღმოჩენამდე. სწავლობდა ლითონების კალცინაციას "ცაცხვის" წარმოქმნით, მას სჯეროდა, რომ ჰაერის "ყველაზე სუნთქვადი" ნაწილი შეიძლება მიღებულ იქნას მეტალის "ცაცხვისგან", ანუ ნებისმიერი ლითონის ოქსიდებისგან. თუმცა მისი მცდელობები წარუმატებელი აღმოჩნდა და მხოლოდ 1774 წლის ნოემბერში (ჯ. პრისტლისთან შეხვედრის შემდეგ) გადავიდა ვერცხლისწყლის ოქსიდის ექსპერიმენტებზე.
ა.ლავუაზიემ ეს ექსპერიმენტები ორი გზით ჩაატარა. მან ვერცხლისწყლის ოქსიდი ქვანახშირით გაათბო და მიიღო ბლეკის „ფიქსირებული ჰაერი“, ასევე უბრალოდ გააცხელა ვერცხლისწყლის ოქსიდი. მიღებული გაზი, მისი აზრით, ჰაერის ყველაზე სუფთა ნაწილი იყო. A. Lavoisier ასევე მივიდა იმ დასკვნამდე, რომ "ფიქსირებული ჰაერი" არის "სუფთა" ჰაერის ნახშირის კომბინაცია. აკადემიაში წარდგენილ მოხსენებაში მან უწოდა „ყველაზე სუფთა
ჰაერის ნაწილი“ ასევე არის „ძალიან სუნთქვადი“ ან „მაცოცხლებელი ჰაერი“.
მნიშვნელოვანი დასკვნები ჩამოაყალიბა ა. ლავუაზიემ თავის მემუარებში „ექსპერიმენტები ცხოველების სუნთქვაზე“: 1. სუნთქვისას ურთიერთქმედება ხდება მხოლოდ სუფთა „სუნთქვისთვის ყველაზე შესაფერის“ ნაწილთან. ატმოსფერული ჰაერი. დანარჩენი ჰაერი მხოლოდ ინერტული საშუალებაა, რომელიც არ იცვლება სუნთქვის დროს. 2. ლითონების კალციაციის შემდეგ რეტორში დარჩენილი გაფუჭებული ჰაერის თვისებები არაფრით განსხვავდება იმ ჰაერის თვისებებისგან, რომელშიც ცხოველი გარკვეული პერიოდის განმავლობაში იმყოფებოდა.
1777 წლიდან ა. ლავუაზიე ღიად დაუპირისპირდა ფლოგისტონის თეორიას. თავის ერთ-ერთ მემუარში ის წერდა: „ქიმიკოსებმა ფლოგისტონის ბუნდოვანი პრინციპი შექმნეს, რომელიც ზუსტად არ არის განსაზღვრული და, შესაბამისად, შესაფერისია ნებისმიერი ახსნა-განმარტებისთვის, რომლებშიც მათ სურთ მისი დანერგვა. ხან ეს დასაწყისი მნიშვნელოვანია, ხან – არა; ხან თავისუფალი ცეცხლია, ხან - ცეცხლი შერწყმული მიწის ელემენტთან; ხან გადის სისხლძარღვების ფორებში, ხან გაუვალია მისთვის. იგი განმარტავს ერთდროულად ტუტეობას და ნეიტრალიტეტს, გამჭვირვალობას და გამჭვირვალობას, ფერს და ფერის ნაკლებობას; ეს არის ნამდვილი პროტეუსი, რომელიც ყოველ წამს იცვლის თავის გარეგნობას“.
საინტერესოა, რომ ა. ლავუაზიეს ეს სიტყვები მოგვაგონებს მ.ვ. ლომონოსოვის ფორმულირებებს, რომელიც წერდა 1744 წელს „ცეცხლოვანი მატერიის“ შესახებ, რომელიც ან ხვდება სხეულების ფორებში, „თითქოს იზიდავს რაიმე სახის სასიყვარულო წამალს. , შემდეგ ძალადობრივად ტოვებს მათ, თითქოს საშინელებათაა დაპყრობილი“1 2.
თავის მემუარებში „ზოგადად წვის შესახებ“ (1777) ა. ლავუაზიემ წვის ფენომენების შემდეგი აღწერა: „1. ნებისმიერი წვის დროს გამოიყოფა "ცეცხლოვანი მატერია" ან სინათლე. 2. სხეულებს შეუძლიათ დაწვა მხოლოდ ძალიან ცოტა ტიპის ჰაერში, უფრო სწორად, წვა შეიძლება მოხდეს მხოლოდ ერთ ტიპის ჰაერში, რომელსაც პრისტლიმ უწოდა ფლოგისტონი და რომელსაც მე დავარქმევ „სუფთა“ ჰაერს. სხეულები, რომლებსაც წვადს ვუწოდებთ, არა მხოლოდ არ იწვებიან სიცარიელეში ან სხვა ჰაერში, არამედ ისე სწრაფად გამოდიან, თითქოს წყალში ჩაეფლონ... 3. ნებისმიერი წვის დროს ხდება „სუფთა“ ნგრევა ან დაშლა. » ჰაერი და დამწვარი სხეულის წონა იზრდება ზუსტად შეწოვილი ჰაერის რაოდენობით. 4. ნებისმიერი წვის დროს დამწვარი სხეული მჟავად იქცევა... ასე რომ, თუ გოგირდს ზარის ქვეშ დაწვავთ, მაშინ წვის პროდუქტი გოგირდმჟავა იქნება... „3.
ამ უკანასკნელ პოზიციაზე დაყრდნობით ა. ლავუაზიე ქმნის მჟავების თეორიას, რომლებიც წარმოიქმნება მჟავების შერწყმისას.
დაწყებული აალებადი ნივთიერებებით. ამასთან დაკავშირებით მან ამ მჟავაწარმომქმნელ პრინციპს უწოდა სახელი „ჟანგბადი“ (მჟავას წარმომქმნელი, ანუ ჟანგბადი). ა.ლავუაზიეს მჟავების თეორია არათანმიმდევრული აღმოჩნდა ბევრ ცნობილ ფაქტთან. Ისე, მარილმჟავაიქმნება ჟანგბადის მონაწილეობის გარეშე. ა.ლავუაზიე ამ შემთხვევაში იძულებული გახდა მიემართა ფანტაზიით ამ მჟავის შემადგენლობის ასახსნელად. მან აღიარა, რომ მარილმჟავა შეიცავს სპეციალურ მარტივ სხეულს - მურიუმს - რომელიც მჟავაში ჟანგვის მდგომარეობაშია. ამიტომ, ბოლო დრომდე, ჰიდროქლორინის მჟავას ფარმაცევტები ეძახდნენ მურინის მჟავას.
წყალბადის წვის დროს წყლის წარმოქმნის ფაქტი ასევე ეწინააღმდეგებოდა ლავუაზიეს მჟავების თეორიას. რამდენიმე წლის განმავლობაში ლავუაზიე წარუმატებლად ცდილობდა წყალში მჟავას კვალის აღმოჩენას. ამავდროულად, მან დაადგინა წყალბადისა და ჟანგბადის მოცულობითი თანაფარდობა წყალში (12:22.9, ანუ თითქმის 1:2). თუმცა მან ამ შედეგს არანაირ მნიშვნელობას არ ანიჭებდა. წყლის დაშლის დროს ის წყალზე მოქმედებდა რკინის ჩირქებით და წყალბადს იღებდა. ეს კვლევები იყო საბოლოო ექსპერიმენტების დაგეგმილი სერია, რომელიც შექმნილია ფლოგისტონის თეორიის დასამხობად.
აღვნიშნოთ, რომ ზოგიერთი მეცნიერის მიერ ა.ლავუაზიეს აღმოჩენების პრიორიტეტულობის შესახებ პრეტენზია უსაფუძვლო აღმოჩნდა. მართლაც, ჟანგბადის აღმოჩენა არსებითად ეკუთვნის A. Lavoisier-ს და არა K. Sheele-ს და J. Priestley-ს, რომლებიც დარჩნენ, ფ. ენგელსის სიტყვებით, „ფლოგისტიკური კატეგორიების ტყვედ“ და ვერ გაიგეს, რა აღმოაჩინეს მათ. . "და მაშინაც კი, თუ" წერდა ენგელსი, "ა ლავუაზიემ არ მისცა ჟანგბადის აღწერა, როგორც მოგვიანებით ამტკიცებდა, სხვებთან ერთად და მათგან დამოუკიდებლად, მაინც, არსებითად, მან აღმოაჩინა ჟანგბადი და არა ის ორი. მხოლოდ აღწერეს, არც კი იცოდნენ, რას აღწერდნენ"
COURSE OF CHEMISTRY LAVOISIER
წვის და სუნთქვის ანტიფლოგისტური ჟანგბადის თეორიის საფუძვლების შემუშავების პროცესში ა. ლავუაზიეს არ აკლდა თავისი ახალი შეხედულებების კრიტიკოსები. ამ კრიტიკასთან დაკავშირებით მას მოუწია ახალი ექსპერიმენტების ჩატარება, ახალი განზოგადებების გამოხატვა და ეტაპობრივად დაამტკიცა წამოყენებული წინააღმდეგობების შეუსაბამობა. ამავდროულად, მან გადაჭრა სხვადასხვა საკითხები, რომლებიც უშუალოდ არ იყო დაკავშირებული კვლევის დაგეგმილ გეგმასთან. ამრიგად, მას მოუწია უარყო გ.კავენდიშის ახსნა მეტალზე განზავებული მჟავების მოქმედებით წყალბადის წარმოქმნის მექანიზმის შესახებ. ა.ლავუაზიემ აღნიშნა, რომ წყალბადი ამ შემთხვევაში გამოიყოფა არა ლითონის დაშლის, არამედ მჟავას განზავებული წყლის დაშლის შედეგად (იმ დროს მჟავა ოქსიდები ითვლებოდა მჟავებად).
საკითხებს შორის, რამაც გამოიწვია კამათი წვის ფენომენების ახსნაში, იყო საკითხი სითბოს ბუნების შესახებ. ა.ლავუაზიემ კარგად იცოდა სითბოს კინეტიკური თეორია, მაგრამ ის არ იყო ატომისტი და ამიტომ დარჩა კალორიული მატერიის პოზიციაზე, განსხვავებით მ.ვ. ამავდროულად, ის ერთ-ერთ ელემენტარულ სითხედ თვლიდა კალორიულობას და, ამრიგად, ამ საკითხში მისი პოზიცია ემთხვეოდა მართლმადიდებლური ფლოგისტიკის პოზიციას.
ა. ლავუაზიეს მიენიჭება რეაქციების თერმული ეფექტების პიონერი. პ.ლაპლასთან ერთად მან დააპროექტა კალორიმეტრი და 15 წლის განმავლობაში მუშაობდა თერმული ეფექტების განსაზღვრაზე, რითაც საფუძველი ჩაუყარა თერმოქიმიას. ორგანული ნივთიერებების შემადგენლობის თავისებურებების დადგენისთვის ა. ლავუაზიესაც იმსახურებს. ანალიზის საფუძველზე მან აღმოაჩინა, რომ ორგანული ნივთიერებებიშედგება ნახშირბადის, წყალბადისა და ჟანგბადისგან. შემდეგ ამ მარტივ სხეულებს დაემატა აზოტი და ფოსფორი.
ლავუაზიე ქიმიის ერთ-ერთ უმნიშვნელოვანეს პრინციპად მატერიის ურღვევობის პრინციპად მიიჩნევდა. ცნობილია, რომ ფლოგისტიკოსები უგულებელყოფდნენ ამ პრინციპს, მაგალითად, ლითონების მასის npnf კალციფიკაციის ახსნისას. ამ პრინციპის ჩამოყალიბების შემდეგ, ა. ლავუაზიემ იგი აჩვენა ყურძნის წვენის დუღილის შედეგად ალკოჰოლის წარმოქმნის მაგალითით:
ყურძნის წვენი = ნახშირმჟავა + ალკოჰოლი.
დაახლოებით 1785 წელს ა. ლავუაზიეს გაუჩნდა იდეა, სისტემატურად წარმოედგინა მის მიერ აღმოჩენილი ახალი ფაქტები და სხვადასხვა ფენომენის ახსნა ჟანგბადის თეორიის თვალსაზრისით მოკლე „ქიმიის ელემენტარულ კურსში“. ამ კურსის მომზადებისას მას მოუწია შემდგომი გამოკვლევა და გადაჭრა რამდენიმე ფუნდამენტური საკითხი, რომლებიც დაკავშირებულია პრინციპების, ანუ მარტივი ნივთიერებების დოქტრინის შემუშავებასთან, ქიმიური ნომენკლატურის შექმნასთან და ქიმიაში ახალი ამოცანების ჩამოყალიბებასთან. წარმოიშვა ჟანგბადის თეორიის საფუძველზე.
კურსის „წინასწარ დისკურსში“ ა. ლავუაზიე საუბრობს მარტივ სხეულებზე: „ასე რომ, ქიმია მიდის თავისი მიზნისკენ, სრულყოფილებისკენ, სხეულების გაყოფის, დაყოფისა და შემდგომი დაყოფისკენ და ჩვენ არ ვიცით რა არის მისი წარმატების ზღვარი. იქნება. ამიტომ ჩვენ არ შეგვიძლია იმის მტკიცება, რომ ის, რაც დღეს მარტივია აღიარებული, მართლაც მარტივია. ჩვენ მხოლოდ შეგვიძლია ვთქვათ, რომ ესა თუ ის ნივთიერება ქიმიური ანალიზით მხოლოდ გაყოფის ზღვარია და ჩვენი ცოდნის დღევანდელი მდგომარეობით მისი შემდგომი გაყოფა შეუძლებელია“.
ელემენტებზე საუბრისას, ა. ლავუაზიე არ იძლევა ამ ცნების ცალსახად განმარტებას: „ასე რომ, მე ვიტყვი, რომ თუ ელემენტების სახელი აღნიშნავს მარტივ ან განუყოფელ მოლეკულებს, რომლებიც ქმნიან სხეულებს, მაშინ ჩვენ, ალბათ, არ ვიცით ისინი; თუ, პირიქით, ელემენტების სახელს ან პრინციპებს ვუკავშირებთ ანალიზით მიღწეული საბოლოო ლიმიტის იდეას, მაშინ ყველა ნივთიერება, რომლის დაშლა ჯერ კიდევ ვერანაირად ვერ მოვახერხეთ, ჩვენთვის ელემენტებია.”2
ეს განმარტება არსებითად ემთხვევა ბოილის.
კიდევ ერთი კითხვა, რომელიც წარმოიშვა ა.ლავუაზიეს წინაშე „ქიმიის დაწყებით კურსზე“ მუშაობისას, იყო ქიმიური ნომენკლატურის შემუშავება. ალქიმიურ პერიოდში, როდესაც სიმბოლიზმი და ნივთიერების ჩვეულებრივი სახელების დაშიფვრის სურვილი იყო გავრცელებული, ბევრმა ნივთიერებამ მიიღო შემთხვევითი და ხშირად განსხვავებული სახელები სხვადასხვა ავტორებისგან. ახლად აღმოჩენილ ნივთიერებებზე შემთხვევითი სახელების მინიჭების ტრადიცია მომავალშიც გაგრძელდა. ასეთ პირობებში ქიმიური ნომენკლატურის სისტემის შექმნა არ შეიძლებოდა.
მე-18 საუკუნეში ქიმიკოსები და ლოგისტიკოსებიც კი გრძნობდნენ გადაუდებელ საჭიროებას, შეექმნათ ქიმიური ნომენკლატურის სისტემა, რადგან ცნობილი ნივთიერებების რაოდენობა სწრაფად გაიზარდა საუკუნის მეორე ნახევარში. ერთ-ერთმა გამოჩენილმა ფლოგისტიკოსმა ქიმიკოსმა გიტონ დე მორვომ (გვ. 68) დაიწყო ქიმიური ნომენკლატურის სისტემის შემუშავება ფლოგისტონის თეორიაზე დაფუძნებული ჯერ კიდევ 1782 წელს. იგივე პრობლემით დაკავებული ა. ლავუაზიე ცდილობდა დე მორვოს თავის მხარეს მოეზიდა, რაც მან მიაღწია 1786 წელს. ცოტა ადრე, იმ დროის ერთ-ერთი ყველაზე ცნობილი ქიმიკოსი, კ. ლ. ბერტოლე, შეუერთდა ა. ლავუაზიეს (გვ. 68). ) , ხოლო მის შემდეგ - A. Fourcroix.
ამ მეცნიერებთან ალიანსით ა. ლავუაზიემ მოაწყო პარიზის აკადემიის ნომენკლატურის კომისია, რომელმაც მუშაობა დაიწყო 1786 წელს. ერთი წლის შემდეგ გამოქვეყნდა შემუშავებული ნომენკლატურა. მას საფუძვლად დაედო მარტივი სხეულების სახელები, რომელთა სია (და კლასიფიკაცია) თავად ა.ლავუაზიემ შეადგინა. ახალ სახელწოდებებს შორის კომისიამ დაამტკიცა ჟანგბადის (ჟანგბადის), წყალბადის (წყალბადის) და აზოტის სახელები. საერთაშორისო „ნიტროგენიუმისგან“ განსხვავებული გვარი შემოგვთავაზა ა. ლავუაზიემ და მიიღო, მიუხედავად იმისა, რომ
„ქიმიის დაწყებითი კურსის“ შესავალში ა. ლავუაზიე წერდა: „სხეულების შემადგენელი და ელემენტარული ნაწილების შესახებ თავის არარსებობა ქიმიის საწყის კურსში აუცილებლად გამოიწვევს გაოცებას, მაგრამ თავს უფლებას მივცემ აღვნიშნო, რომ. სურვილი, რომ ბუნების ყველა სხეული შედგებოდეს მხოლოდ სამი ან ოთხი ელემენტისგან, მოდის ბერძენი ფილოსოფოსებისგან ჩვენამდე გადმოცემული ცრურწმენებიდან.
სხეულების ელემენტარული კომპონენტების საკითხის გადასაჭრელად ა.ლავუაზიეს არ გააჩნდა საჭირო ფაქტობრივი მონაცემები და იძულებული გახდა დაეყრდნო ძირითადად საკუთარი კვლევის შედეგებს. ალბათ ამიტომაა მისი შეხედულებები ბუნდოვანი და არათანმიმდევრული.
კომისიის წევრებმა ის წარუმატებლად მიიჩნიეს და შესთავაზეს სახელწოდება „აზოტი“. "აზოტი", "ტუტე". სიტყვა „აზოტი“, ა. ლავუაზიეს წინადადებით, ითარგმნება სიტყვით „უსიცოცხლო“. თუმცა ეს თარგმანი არასწორია. სინამდვილეში, სიტყვა "აზოტი", რომელიც არ არსებობს ბერძენი, აღებულია ალქიმიური ლექსიკონიდან, სადაც ის ნიშნავდა „ფილოსოფიურ ვერცხლისწყალს“.
მარტივი სხეულების წარმოებულებად დადგინდა რთული ნივთიერებების (მჟავები, ტუტეები, მარილები და სხვ.) სახელები. მჟავების და მარილების სახელები შეიცვალა (დაბოლოებით) მჟავა წარმომქმნელი ელემენტის (სულფატი, სულფიტი, სულფიდი და ა.შ.) დაჟანგვის ხარისხის მიხედვით. აზოტის მჟავას მარილებს, ელემენტის სახელის საწინააღმდეგოდ, ნიტრატები ეწოდა.
ახალ ნომენკლატურასთან დაკავშირებით A. Lavoisier-ის „დაწყებითი კურსი“ შეიცავს მჟავების, მარილების და სხვა ნაერთების კლასიფიკაციის ცხრილებს მჟავაწარმომქმნელი ელემენტების ჟანგვის მდგომარეობების მიხედვით. "ქიმიური ნომენკლატურის" დანართში მოცემულია ქიმიკოსების P. A. Ade (1763-1834) და J. A. Gassenfratz (1755-1827) მიერ შემოთავაზებული მარტივი სხეულების სიმბოლოები, რომლებიც, თუმცა, არ მიიღეს აღიარება.
რაც შეეხება უმარტივეს სხეულებს, „დაწყებით კურსში“ ა. ლავუაზიემ ჩამოაყალიბა მათი სია და გამოყო შემდეგი ოთხი ჯგუფი:
1. მარტივი ნივთიერებები, წარმოდგენილი ბუნების სამივე სამეფოში, რომლებიც შეიძლება მივიჩნიოთ სხეულების ელემენტებად: მსუბუქი, კალორიული, ჟანგბადი, აზოტი და წყალბადი.
2. მარტივი არალითონური ნივთიერებები, რომლებიც იჟანგება და წარმოქმნის მჟავებს: გოგირდი, ფოსფორი, ქვანახშირი, მურაბის მჟავას რადიკალი, ჰიდროფთორმჟავას რადიკალი, ბორის მჟავას რადიკალი.
3. მარტივი მეტალის ნივთიერებები, რომლებიც იჟანგება და წარმოქმნის მჟავებს: ანტიმონი, ვერცხლი, დარიშხანი, ბისმუტი, კობალტი, სპილენძი, კალა, რკინა, მანგანუმი, ვერცხლისწყალი, მოლიბდენი, ნიკელი, ოქრო, პლატინი, ტყვია, ვოლფრამი, თუთია.
4. მარტივი ნივთიერებები, მარილწარმომქმნელი და მიწიერი: ცაცხვი, მაგნეზია, ბარიტი, ალუმინი, სილიციუმი.
ამ ცხრილის ჩანაწერში ა. ლავუაზიემ აღნიშნა, რომ მას არ შეუტანია „მუდმივი“ (კაუსტიკური) ტუტე მარტივი ნივთიერებების ჩამონათვალში, ვინაიდან ამ ნივთიერებებს, როგორც ჩანს, რთული შემადგენლობა აქვთ.
ა.ლავუაზიეს ცხრილი შეიცავს 23 მარტივ სხეულს, 3 რადიკალს, 2 მჟავას, 5 მიწას და 2 უწონო სითხეს. ცხრილის სახელში
აშკარა შეუსაბამობებია. უწონო სითხეების შემოტანის გარდა, მასში „დედამიწები“ ჩნდებიან როგორც მარტივი ნივთიერებები და, ბოლოს და ბოლოს, ლითონები კლასიფიცირდება მჟავების ზოგადი თეორიის შესაბამისად, როგორც მჟავა წარმომქმნელი ელემენტები. ეს ცხრილი იყო პირველი მცდელობა მეცნიერების ისტორიაში მარტივი სხეულების კლასიფიკაციისთვის.
ა. ლავუაზიეს „ქიმიის ელემენტარული კურსი“ მისი მეუღლის (მ. ლავუაზიეს) ლამაზად შესრულებული ილუსტრაციებით გამოჩნდა 1789 წელს, საფრანგეთის ბურჟუაზიული რევოლუციის დაწყების თითქმის ერთდროულად. ამ კურსის გამოჩენამ ფაქტიურად აღნიშნა ქიმიური რევოლუცია, როგორც თავად ა. ლავუაზიემ აღნიშნა კურსში. მართალია, ახალი ქიმიის ჯერ კიდევ ბევრი მოწინააღმდეგე იყო, მაგალითად ჯ.პრისტლი, რომელიც აქტიურად ემხრობოდა ფლოგისტონის თეორიას. მაგრამ ოპონენტების რაოდენობა სწრაფად შემცირდა. ამგვარად, ინგლისელმა ფლოგისტიკოსმა რ.კირვანმა (1733-1812) 1787 წელს გამოსცა წიგნი „ნარკვევები ფლოგისტონის შესახებ და მჟავების კონსტიტუცია“. ა. R. Kirwan ითარგმნა ფრანგულად და გამოქვეყნდა კომენტარებით თითოეულ თავში დაწერილი A. Lavoisier, C. Berthollet, G. de Morveau, A. Fourque-foy და G. Monge ამ კომენტარებში, ყველა ძირითადი დებულება დამანგრეველი კრიტიკა საბოლოოდ იძულებული გახდა ეღიარებინა თავისი შეხედულებების შეცდომა და შეუერთდა ჟანგბადის თეორიას 1796 წელს. ჟანგბადის თეორია და აგებულია მის საფუძველზე ახალი ქიმიამნიშვნელოვანი გამარჯვება მოიპოვა. და მაინც არ შეიძლება ითქვას, რომ „ქიმიური რევოლუცია“ დასრულდა, როგორც თავად ა. ლავუაზიე ფიქრობდა, „ქიმიის დაწყებითი კურსის“ გამოშვებით. ახალი შეხედულებები შეიმუშავეს და საკმაოდ სრული დასრულება მიიღეს მომდევნო მე-4 თაობის ქიმიკოსებმა მხოლოდ ქიმიაში ატომიზმის დანერგვის შემდეგ.