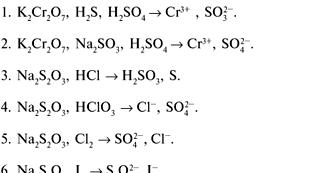როგორ აღმოაჩინეს ქიმიური ელემენტი ფოსფორი. შარდით გამდიდრება (ფოსფორის აღმოჩენის ისტორიის შესახებ). რას ჰგავს აპატიტი?
შავი ფოსფორის სტრუქტურა
სამასზე მეტი წელი გვაშორებს იმ მომენტს, როდესაც ჰამბურგელმა ალქიმიკოსმა გენინგ ბრენდმა აღმოაჩინა ახალი ელემენტი - . სხვა ალქიმიკოსების მსგავსად, ბრენდი ცდილობდა ეპოვა სიცოცხლის ელექსირი ანუ ფილოსოფიური ქვა, რომლის დახმარებით მოხუცები ახალგაზრდები ხდებიან, ავადმყოფები გამოჯანმრთელდებიან და უღირსნი იქცევიან... ბრენდს ხელმძღვანელობდა არა ხალხის კეთილდღეობა, არამედ პირადი ინტერესი. ამას მოწმობს ფაქტები ამ ალქიმიკოსის მიერ გაკეთებული ერთადერთი რეალური აღმოჩენის ისტორიიდან.
ერთ-ერთი ექსპერიმენტის დროს მან აორთქლდა შარდი, ნარჩენი ნახშირთან და ქვიშაში შეურია და განაგრძო აორთქლება. მალე რეტორტში წარმოიქმნა ნივთიერება, რომელიც სიბნელეში ანათებდა. მართალია, kaltes Feuer (ცივი ცეცხლი), ან "ჩემი ცეცხლი", როგორც მას ბრენდმა უწოდა, არ გარდაიქმნა ან შეცვალა მოხუცების გარეგნობა, მაგრამ ის ფაქტი, რომ მიღებული ნივთიერება ანათებდა გათბობის გარეშე, უჩვეულო და ახალი იყო.
ბრენდი სწრაფად ისარგებლა ამ ახალი საკუთრებით. მან დაიწყო სხვადასხვა პრივილეგირებული პირების ჩვენება, მათგან საჩუქრების და ფულის მიღება. ფოსფორის მოპოვების საიდუმლოს შენახვა ადვილი არ იყო და ბრენდმა ის მალე მიჰყიდა დრეზდენელ ქიმიკოს ი.კრაფტს. ფოსფორის დემონსტრატორთა რიცხვი გაიზარდა, როდესაც მისი წარმოების რეცეპტი ცნობილი გახდა ი.კუნკელი და კ.კირჩმეიერი. 1680 წელს, მიუხედავად მისი წინამორბედებისა, ახალი ელემენტი მიიღო ცნობილმა ინგლისელმა ფიზიკოსმა და ქიმიკოსმა რობერტ ბოილმა. მაგრამ ბოილი მალე გარდაიცვალა და მისმა სტუდენტმა ა. განკვვიცმა უღალატა წმინდა მეცნიერებას და კვლავ გააცოცხლა "ფოსფორის სპეკულაცია". მხოლოდ 1743 წელს იპოვა ა. მარკგრაფმა ფოსფორის წარმოების უფრო მოწინავე მეთოდი და გამოაქვეყნა თავისი მონაცემები საჯარო ინფორმაციისთვის. ამ მოვლენამ დაასრულა ბრენდის ბიზნესი და გახდა ფოსფორისა და მისი ნაერთების სერიოზული შესწავლის დასაწყისი.
ფოსფორის ისტორიის პირველ, ორმოცდაათწლიან ეტაპზე, ბოილის აღმოჩენის გარდა, მხოლოდ ერთი მოვლენა იყო აღსანიშნავი მეცნიერების ისტორიით: 1715 წელს გენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში. მარკგრეივის ექსპერიმენტების შემდეგ, ელემენტის ისტორია, რომელმაც მრავალი წლის შემდეგ შეიძინა ნომერი 15, გახდა მრავალი დიდი აღმოჩენის ისტორია.
ყველაფერი ფოსფორის შესახებ
1769 წელს იუ განმა დაამტკიცა, რომ ძვლები შეიცავს უამრავ ფოსფორს. იგივე დაადასტურა ორი წლის შემდეგ ცნობილმა შვედმა ქიმიკოსმა კ.შელემ, რომელმაც შემოგვთავაზა ძვლების გამოწვის დროს წარმოქმნილი ფერფლიდან ფოსფორის მიღების მეთოდი.
რამდენიმე წლის შემდეგ J.L.Prust-მა და M.Klaproth-მა, სხვადასხვა ბუნებრივი ნაერთების შესწავლით, დაამტკიცეს, რომ ის ფართოდ არის გავრცელებული დედამიწის ქერქში, ძირითადად კალციუმის ფოსფატის სახით.
მან დიდ წარმატებას მიაღწია ფოსფორის თვისებების შესწავლაში მე-18 საუკუნის 70-იანი წლების დასაწყისში. დიდი ფრანგი ქიმიკოსი ანტუან ლორანი. ფოსფორის დაწვით სხვა ნივთიერებებთან ჰაერის დახურულ მოცულობაში, მან დაამტკიცა, რომ ფოსფორი დამოუკიდებელი ელემენტია, ხოლო ჰაერს აქვს რთული შემადგენლობა და შედგება მინიმუმ ორი კომპონენტისგან - ჟანგბადისა და აზოტისგან. ”ამ გზით, მან პირველად დააყენა ფეხზე მთელი ქიმია, რომელიც თავის ფლოგისტიკური ფორმით იდგა თავზე.” ასე წერდა ფ.ენგელსი ნაწარმოების შესახებ კა-პიტალას მეორე ტომის წინასიტყვაობაში“.
1709 წელს დონდონალდმა დაამტკიცა, რომ ფოსფორის ნაერთები აუცილებელია მცენარეების ნორმალური განვითარებისთვის.
1839 წელს სხვა ინგლისელმა, ლაუსმა, პირველმა მიიღო სუპერფოსფატი - ფოსფორიანი სასუქი, რომელიც ადვილად ასათვისებელია.მცენარეები.
1847 წელს გერმანელმა ქიმიკოსმა შროტერმა, ჰაერის წვდომის გარეშე გათბობით, შეიმუშავა მე-15 ელემენტის ახალი სახეობა (ალოტროპული მოდიფიკაცია) - და უკვე მე-20 საუკუნეში, 1934 წელს, ამერიკელმა ფიზიკოსმა პ. ბრაჯენმა, შეისწავლა მაღალის ეფექტი. ზეწოლა სხვადასხვა, გამოთავისუფლებულ მსგავს შავ ფოსფორზე. ეს არის მთავარი ეტაპები No15 ელემენტის ისტორიაში. ახლა მოდით მივყვეთ რა მოჰყვა თითოეულ ამ აღმოჩენას.
„1715 წელს გენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში... 1769 წელს ჰანმა დაამტკიცა, რომ ძვლები შეიცავს უამრავ ფოსფორს“
ფოსფორი არის აზოტის ანალოგი
მიუხედავად იმისა, რომ ფიზიკური და ქიმიური თვისებებიეს ელემენტები ძალიან განსხვავებულია, მათ აქვთ. და ზოგადად, კერძოდ, ის არის, რომ ორივე ეს ელემენტი აბსოლუტურად აუცილებელია ცხოველებისა და მცენარეებისთვის. აკადემიკოსმა A.E. Fersman-მა ფოსფორს უწოდა "სიცოცხლისა და აზროვნების ელემენტი", მაგრამ ეს განმარტება ძნელად შეიძლება კლასიფიცირდეს როგორც ლიტერატურული გაზვიადება. ფოსფორი გვხვდება მწვანე მცენარეების ფაქტიურად ყველა ორგანოში: ღეროებში, ფესვებში, ფოთლებში, მაგრამ ყველაზე მეტად ხილსა და თესლში. მცენარეები აგროვებენ ფოსფორს და აწვდიან მას ცხოველებს.
ცხოველებში ფოსფორი ძირითადად კონცენტრირებულია ჩონჩხში, კუნთებსა და ნერვულ ქსოვილში.
ადამიანის საკვებ პროდუქტებს შორის ფოსფორით განსაკუთრებით მდიდარია ქათმის კვერცხის გული.
ადამიანის ორგანიზმი შეიცავს საშუალოდ დაახლოებით 1,5 კგ No15 ელემენტს. აქედან 1,4 კგ არის ძვლებში, დაახლოებით 130 გ კუნთებში და 12 გ ნერვებში და ტვინში. ჩვენს ორგანიზმში მიმდინარე თითქმის ყველა უმნიშვნელოვანესი ფიზიოლოგიური პროცესი დაკავშირებულია ფოსფორორგანული ნივთიერებების გარდაქმნასთან. ფოსფორი არის ძვლებში ძირითადად კალციუმის ფოსფატის სახით. კბილის მინანქარი ასევე ფოსფორის ნაერთია, რომელიც შემადგენლობითა და კრისტალური სტრუქტურით შეესაბამება ყველაზე მნიშვნელოვან ფოსფორის მინერალს, აპატიტს Ca5(P04)3(F, Cl).
ბუნებრივია, როგორც ნებისმიერი სასიცოცხლო ელემენტი, ფოსფორი ბუნებაში ციკლს გადის. მცენარეები მას ნიადაგიდან იღებენ, მცენარეებიდან კი ეს ელემენტი ხვდება ადამიანისა და ცხოველის სხეულში. ფოსფორი მიწაში ბრუნდება ექსკრემენტებით და როცა გვამები ლპება. ფოსფორობაქტერიები ორგანულ ფოსფორს არაორგანულ ნაერთებად გარდაქმნის.
თუმცა, დროის ერთეულში, ნიადაგიდან გაცილებით მეტი ფოსფორი გამოიყოფა, ვიდრე მიწაში შედის. მსოფლიო მოსავალი ყოველწლიურად 3 მილიონ ტონაზე მეტ ფოსფორს აშორებს მინდვრებიდან.
ბუნებრივია, მდგრადი მოსავლიანობის მისაღებად, ეს ფოსფორი უნდა დაბრუნდეს ნიადაგში და ამიტომ გასაკვირი არ არის, რომ ფოსფატის ქანების მსოფლიო წარმოება ახლა მნიშვნელოვნად აღემატება 100 მილიონ ტონას წელიწადში.
პრუსტმა და კლაპროტმა დაამტკიცეს, რომ ფოსფორი ფართოდ არის გავრცელებული დედამიწის ქერქში, ძირითადად კალციუმის ფოსფატის სახით.
დედამიწის ქერქში ფოსფორი მხოლოდ ნაერთების სახით გვხვდება. ეს არის ძირითადად ორთოფოსფორის მჟავას ცუდად ხსნადი მარილები; კატიონი ყველაზე ხშირად არის კალციუმის იონი.
ფოსფორი შეადგენს წონის 0,08%-ს დედამიწის ქერქი. გავრცელების თვალსაზრისით, იგი მე-13 ადგილზეა ყველა ელემენტს შორის. ფოსფორს შეიცავს მინიმუმ 190 მინერალი, რომელთაგან ყველაზე მნიშვნელოვანია: ფტორპატიტი Ca5(P04)3F, ჰიდროქსილაპატიტი Ca5(P04)3OH, ფოსფორიტი Cae(P04)2 მინარევებით.
ფოსფორი იყოფა პირველად და მეორად. პირველებს შორის განსაკუთრებით გავრცელებულია აპატიტები, რომლებიც ხშირად გვხვდება ცეცხლოვანი წარმოშობის ქანებს შორის. ისინი ჩამოყალიბდნენ დედამიწის ქერქის წარმოქმნის დროს.
აპატიტებისაგან განსხვავებით, ფოსფორიტები გვხვდება დანალექი წარმოშობის ქანებს შორის, რომლებიც წარმოიქმნება ცოცხალი არსებების სიკვდილის შედეგად. ეს მეორეხარისხოვანია.
ფოსფორი მეტეორიტებში გვხვდება რკინის, კობალტის და ნიკელის ფოსფიდების სახით. რა თქმა უნდა, ეს საერთო ელემენტი ასევე გვხვდება ზღვის წყალში (6 10-6%).
„ლავუაზიემ დაამტკიცა, რომ ფოსფორი დამოუკიდებელია ქიმიური ელემენტი…»
ფოსფორი არის საშუალო აქტივობის არალითონი (რასაც ადრე მეტალოიდს ეძახდნენ). ფოსფორის ატომის გარე ორბიტა შეიცავს ხუთ ელექტრონს, რომელთაგან სამი დაუწყვილებელია. აქედან გამომდინარე, მას შეუძლია გამოავლინოს 3-, 3+ და 5+ ვალენტობა.
იმისთვის, რომ ფოსფორმა გამოავლინოს 5+, საჭიროა გარკვეული გავლენა ატომზე, რომელიც გადააქცევს ბოლო ორბიტის ორ დაწყვილებულ ელექტრონს დაუწყვილებად.
ფოსფორს ხშირად უწოდებენ მრავალმხრივ ელემენტს. მართლაც, სხვადასხვა პირობებში ის განსხვავებულად იქცევა, ავლენს ან ჟანგვის ან შემცირების თვისებებს. ფოსფორის მრავალფეროვნება ასევე მოიცავს მის უნარს არსებობდეს რამდენიმე ალოტროპულ მოდიფიკაციაში.
შესაძლოა, No15 ელემენტის ყველაზე ცნობილი მოდიფიკაცია არის რბილი, ცვილისებრი, თეთრი ან ყვითელი ფოსფორი. სწორედ ბრენდმა აღმოაჩინა იგი და მისი თვისებების წყალობით ელემენტმა მიიღო სახელი: ბერძნულად "ფოსფორი" ნიშნავს მანათობელ, მანათობელ. თეთრი ფოსფორის მოლეკულა შედგება ოთხი ატომისგან, რომლებიც განლაგებულია ტეტრაედრის სახით. სიმკვრივე 1,83, დნობის წერტილი 44,1° C. შხამიანი, ადვილად იჟანგება. ხსნადი ნახშირბადის დისულფიდში, თხევად ამიაკში და SO2-ში, ბენზოლში, ეთერში. წყალში თითქმის არ იხსნება.
როდესაც თბება ჰაერზე წვდომის გარეშე 250°C-ზე ზემოთ, ის წითლდება. ეს უკვე პოლიმერია, მაგრამ არა ძალიან მოწესრიგებული სტრუქტურა. წითელი ფოსფორის რეაქტიულობა მნიშვნელოვნად ნაკლებია, ვიდრე თეთრი ფოსფორის. ის არ ანათებს სიბნელეში, არ იხსნება ნახშირბადის დისულფიდში და არ არის შხამიანი. მისი სიმკვრივე გაცილებით დიდია, სტრუქტურა წვრილკრისტალურია.
შავი ფოსფორის სტრუქტურა
სამასზე მეტი წელი გვაშორებს იმ მომენტს, როდესაც ჰამბურგელმა ალქიმიკოსმა გენინგ ბრენდმა აღმოაჩინა ახალი ელემენტი - . სხვა ალქიმიკოსების მსგავსად, ბრენდი ცდილობდა ეპოვა სიცოცხლის ელექსირი ანუ ფილოსოფიური ქვა, რომლის დახმარებით მოხუცები ახალგაზრდები ხდებიან, ავადმყოფები გამოჯანმრთელდებიან და უღირსნი იქცევიან... ბრენდს ხელმძღვანელობდა არა ხალხის კეთილდღეობა, არამედ პირადი ინტერესი. ამას მოწმობს ფაქტები ამ ალქიმიკოსის მიერ გაკეთებული ერთადერთი რეალური აღმოჩენის ისტორიიდან.
ერთ-ერთი ექსპერიმენტის დროს მან აორთქლდა შარდი, ნარჩენი ნახშირთან და ქვიშაში შეურია და განაგრძო აორთქლება. მალე რეტორტში წარმოიქმნა ნივთიერება, რომელიც სიბნელეში ანათებდა. მართალია, kaltes Feuer (ცივი ცეცხლი), ან "ჩემი ცეცხლი", როგორც მას ბრენდმა უწოდა, არ გარდაიქმნა ან შეცვალა მოხუცების გარეგნობა, მაგრამ ის ფაქტი, რომ მიღებული ნივთიერება ანათებდა გათბობის გარეშე, უჩვეულო და ახალი იყო.
ბრენდი სწრაფად ისარგებლა ამ ახალი საკუთრებით. მან დაიწყო სხვადასხვა პრივილეგირებული პირების ჩვენება, მათგან საჩუქრების და ფულის მიღება. ფოსფორის მოპოვების საიდუმლოს შენახვა ადვილი არ იყო და ბრენდმა ის მალე მიჰყიდა დრეზდენელ ქიმიკოს ი.კრაფტს. ფოსფორის დემონსტრატორთა რიცხვი გაიზარდა, როდესაც მისი წარმოების რეცეპტი ცნობილი გახდა ი.კუნკელი და კ.კირჩმეიერი. 1680 წელს, მიუხედავად მისი წინამორბედებისა, ახალი ელემენტი მიიღო ცნობილმა ინგლისელმა ფიზიკოსმა და ქიმიკოსმა რობერტ ბოილმა. მაგრამ ბოილი მალე გარდაიცვალა და მისმა სტუდენტმა ა. განკვვიცმა უღალატა წმინდა მეცნიერებას და კვლავ გააცოცხლა "ფოსფორის სპეკულაცია". მხოლოდ 1743 წელს იპოვა ა. მარკგრაფმა ფოსფორის წარმოების უფრო მოწინავე მეთოდი და გამოაქვეყნა თავისი მონაცემები საჯარო ინფორმაციისთვის. ამ მოვლენამ დაასრულა ბრენდის ბიზნესი და გახდა ფოსფორისა და მისი ნაერთების სერიოზული შესწავლის დასაწყისი.
ფოსფორის ისტორიის პირველ, ორმოცდაათწლიან ეტაპზე, ბოილის აღმოჩენის გარდა, მხოლოდ ერთი მოვლენა იყო აღსანიშნავი მეცნიერების ისტორიით: 1715 წელს გენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში. მარკგრეივის ექსპერიმენტების შემდეგ, ელემენტის ისტორია, რომელმაც მრავალი წლის შემდეგ შეიძინა ნომერი 15, გახდა მრავალი დიდი აღმოჩენის ისტორია.
ყველაფერი ფოსფორის შესახებ
1769 წელს იუ განმა დაამტკიცა, რომ ძვლები შეიცავს უამრავ ფოსფორს. იგივე დაადასტურა ორი წლის შემდეგ ცნობილმა შვედმა ქიმიკოსმა კ.შელემ, რომელმაც შემოგვთავაზა ძვლების გამოწვის დროს წარმოქმნილი ფერფლიდან ფოსფორის მიღების მეთოდი.
რამდენიმე წლის შემდეგ J.L.Prust-მა და M.Klaproth-მა, სხვადასხვა ბუნებრივი ნაერთების შესწავლით, დაამტკიცეს, რომ ის ფართოდ არის გავრცელებული დედამიწის ქერქში, ძირითადად კალციუმის ფოსფატის სახით.
მან დიდ წარმატებას მიაღწია ფოსფორის თვისებების შესწავლაში მე-18 საუკუნის 70-იანი წლების დასაწყისში. დიდი ფრანგი ქიმიკოსი ანტუან ლორანი. ფოსფორის დაწვით სხვა ნივთიერებებთან ჰაერის დახურულ მოცულობაში, მან დაამტკიცა, რომ ფოსფორი დამოუკიდებელი ელემენტია, ხოლო ჰაერს აქვს რთული შემადგენლობა და შედგება მინიმუმ ორი კომპონენტისგან - ჟანგბადისა და აზოტისგან. ”ამ გზით, მან პირველად დააყენა ფეხზე მთელი ქიმია, რომელიც თავის ფლოგისტიკური ფორმით იდგა თავზე.” ასე წერდა ფ.ენგელსი ნაწარმოების შესახებ კა-პიტალას მეორე ტომის წინასიტყვაობაში“.
1709 წელს დონდონალდმა დაამტკიცა, რომ ფოსფორის ნაერთები აუცილებელია მცენარეების ნორმალური განვითარებისთვის.
1839 წელს სხვა ინგლისელმა, ლაუსმა, პირველმა მიიღო სუპერფოსფატი - ფოსფორიანი სასუქი, რომელიც ადვილად ასათვისებელია.მცენარეები.
1847 წელს გერმანელმა ქიმიკოსმა შროტერმა, ჰაერის წვდომის გარეშე გათბობით, შეიმუშავა მე-15 ელემენტის ახალი სახეობა (ალოტროპული მოდიფიკაცია) - და უკვე მე-20 საუკუნეში, 1934 წელს, ამერიკელმა ფიზიკოსმა პ. ბრაჯენმა, შეისწავლა მაღალის ეფექტი. ზეწოლა სხვადასხვა, გამოთავისუფლებულ მსგავს შავ ფოსფორზე. ეს არის მთავარი ეტაპები No15 ელემენტის ისტორიაში. ახლა მოდით მივყვეთ რა მოჰყვა თითოეულ ამ აღმოჩენას.
„1715 წელს გენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში... 1769 წელს ჰანმა დაამტკიცა, რომ ძვლები შეიცავს უამრავ ფოსფორს“
ფოსფორი არის აზოტის ანალოგი
მიუხედავად იმისა, რომ ამ ელემენტების ფიზიკური და ქიმიური თვისებები მნიშვნელოვნად განსხვავდება, მათ აქვთ. და ზოგადად, კერძოდ, ის არის, რომ ორივე ეს ელემენტი აბსოლუტურად აუცილებელია ცხოველებისა და მცენარეებისთვის. აკადემიკოსმა A.E. Fersman-მა ფოსფორს უწოდა "სიცოცხლისა და აზროვნების ელემენტი", მაგრამ ეს განმარტება ძნელად შეიძლება კლასიფიცირდეს როგორც ლიტერატურული გაზვიადება. ფოსფორი გვხვდება მწვანე მცენარეების ფაქტიურად ყველა ორგანოში: ღეროებში, ფესვებში, ფოთლებში, მაგრამ ყველაზე მეტად ხილსა და თესლში. მცენარეები აგროვებენ ფოსფორს და აწვდიან მას ცხოველებს.
ცხოველებში ფოსფორი ძირითადად კონცენტრირებულია ჩონჩხში, კუნთებსა და ნერვულ ქსოვილში.
ადამიანის საკვებ პროდუქტებს შორის ფოსფორით განსაკუთრებით მდიდარია ქათმის კვერცხის გული.
ადამიანის ორგანიზმი შეიცავს საშუალოდ დაახლოებით 1,5 კგ No15 ელემენტს. აქედან 1,4 კგ არის ძვლებში, დაახლოებით 130 გ კუნთებში და 12 გ ნერვებში და ტვინში. ჩვენს ორგანიზმში მიმდინარე თითქმის ყველა უმნიშვნელოვანესი ფიზიოლოგიური პროცესი დაკავშირებულია ფოსფორორგანული ნივთიერებების გარდაქმნასთან. ფოსფორი არის ძვლებში ძირითადად კალციუმის ფოსფატის სახით. კბილის მინანქარი ასევე ფოსფორის ნაერთია, რომელიც შემადგენლობითა და კრისტალური სტრუქტურით შეესაბამება ყველაზე მნიშვნელოვან ფოსფორის მინერალს, აპატიტს Ca5(P04)3(F, Cl).
ბუნებრივია, როგორც ნებისმიერი სასიცოცხლო ელემენტი, ფოსფორი ბუნებაში ციკლს გადის. მცენარეები მას ნიადაგიდან იღებენ, მცენარეებიდან კი ეს ელემენტი ხვდება ადამიანისა და ცხოველის სხეულში. ფოსფორი მიწაში ბრუნდება ექსკრემენტებით და როცა გვამები ლპება. ფოსფორობაქტერიები ორგანულ ფოსფორს არაორგანულ ნაერთებად გარდაქმნის.
თუმცა, დროის ერთეულში, ნიადაგიდან გაცილებით მეტი ფოსფორი გამოიყოფა, ვიდრე მიწაში შედის. მსოფლიო მოსავალი ყოველწლიურად 3 მილიონ ტონაზე მეტ ფოსფორს აშორებს მინდვრებიდან.
ბუნებრივია, მდგრადი მოსავლიანობის მისაღებად, ეს ფოსფორი უნდა დაბრუნდეს ნიადაგში და ამიტომ გასაკვირი არ არის, რომ ფოსფატის ქანების მსოფლიო წარმოება ახლა მნიშვნელოვნად აღემატება 100 მილიონ ტონას წელიწადში.
პრუსტმა და კლაპროტმა დაამტკიცეს, რომ ფოსფორი ფართოდ არის გავრცელებული დედამიწის ქერქში, ძირითადად კალციუმის ფოსფატის სახით.
დედამიწის ქერქში ფოსფორი მხოლოდ ნაერთების სახით გვხვდება. ეს არის ძირითადად ორთოფოსფორის მჟავას ცუდად ხსნადი მარილები; კატიონი ყველაზე ხშირად არის კალციუმის იონი.
ფოსფორი დედამიწის ქერქის წონის 0,08%-ს შეადგენს. გავრცელების თვალსაზრისით, იგი მე-13 ადგილზეა ყველა ელემენტს შორის. ფოსფორს შეიცავს მინიმუმ 190 მინერალი, რომელთაგან ყველაზე მნიშვნელოვანია: ფტორპატიტი Ca5(P04)3F, ჰიდროქსილაპატიტი Ca5(P04)3OH, ფოსფორიტი Cae(P04)2 მინარევებით.
ფოსფორი იყოფა პირველად და მეორად. პირველებს შორის განსაკუთრებით გავრცელებულია აპატიტები, რომლებიც ხშირად გვხვდება ცეცხლოვანი წარმოშობის ქანებს შორის. ისინი ჩამოყალიბდნენ დედამიწის ქერქის წარმოქმნის დროს.
აპატიტებისაგან განსხვავებით, ფოსფორიტები გვხვდება დანალექი წარმოშობის ქანებს შორის, რომლებიც წარმოიქმნება ცოცხალი არსებების სიკვდილის შედეგად. ეს მეორეხარისხოვანია.
ფოსფორი მეტეორიტებში გვხვდება რკინის, კობალტის და ნიკელის ფოსფიდების სახით. რა თქმა უნდა, ეს საერთო ელემენტი ასევე გვხვდება ზღვის წყალში (6 10-6%).
„ლავუაზიემ დაამტკიცა, რომ ფოსფორი დამოუკიდებელი ქიმიური ელემენტია...“
ფოსფორი არის საშუალო აქტივობის არალითონი (რასაც ადრე მეტალოიდს ეძახდნენ). ფოსფორის ატომის გარე ორბიტა შეიცავს ხუთ ელექტრონს, რომელთაგან სამი დაუწყვილებელია. აქედან გამომდინარე, მას შეუძლია გამოავლინოს 3-, 3+ და 5+ ვალენტობა.
იმისთვის, რომ ფოსფორმა გამოავლინოს 5+, საჭიროა გარკვეული გავლენა ატომზე, რომელიც გადააქცევს ბოლო ორბიტის ორ დაწყვილებულ ელექტრონს დაუწყვილებად.
ფოსფორს ხშირად უწოდებენ მრავალმხრივ ელემენტს. მართლაც, სხვადასხვა პირობებში ის განსხვავებულად იქცევა, ავლენს ან ჟანგვის ან შემცირების თვისებებს. ფოსფორის მრავალფეროვნება ასევე მოიცავს მის უნარს არსებობდეს რამდენიმე ალოტროპულ მოდიფიკაციაში.
შესაძლოა, No15 ელემენტის ყველაზე ცნობილი მოდიფიკაცია არის რბილი, ცვილისებრი, თეთრი ან ყვითელი ფოსფორი. სწორედ ბრენდმა აღმოაჩინა იგი და მისი თვისებების წყალობით ელემენტმა მიიღო სახელი: ბერძნულად "ფოსფორი" ნიშნავს მანათობელ, მანათობელ. თეთრი ფოსფორის მოლეკულა შედგება ოთხი ატომისგან, რომლებიც განლაგებულია ტეტრაედრის სახით. სიმკვრივე 1,83, დნობის წერტილი 44,1° C. შხამიანი, ადვილად იჟანგება. ხსნადი ნახშირბადის დისულფიდში, თხევად ამიაკში და SO2-ში, ბენზოლში, ეთერში. წყალში თითქმის არ იხსნება.
როდესაც თბება ჰაერზე წვდომის გარეშე 250°C-ზე ზემოთ, ის წითლდება. ეს უკვე პოლიმერია, მაგრამ არა ძალიან მოწესრიგებული სტრუქტურა. წითელი ფოსფორის რეაქტიულობა მნიშვნელოვნად ნაკლებია, ვიდრე თეთრი ფოსფორის. ის არ ანათებს სიბნელეში, არ იხსნება ნახშირბადის დისულფიდში და არ არის შხამიანი. მისი სიმკვრივე გაცილებით დიდია, სტრუქტურა წვრილკრისტალურია.
ფოსფორის აღმოჩენის თარიღად, ჩვეულებრივ, 1669 წელია მიჩნეული, მაგრამ არსებობს გარკვეული მინიშნებები, რომ ის ადრე იყო ცნობილი. მაგალითად, გეფერი იუწყება, რომ პარიზის ბიბლიოთეკაში შენახული კოლექციიდან ალქიმიურ ხელნაწერში ნათქვამია, რომ დაახლოებით მე-12 საუკუნეში. ერთმა ალჩიდმა ბეხილმა თიხისა და ცაცხვით შარდის გამოხდით მიიღო ნივთიერება, რომელსაც „ესკარბუკული“ უწოდა. ალბათ ეს იყო ფოსფორი, რომელიც იყო ალქიმიკოსების დიდი საიდუმლო. ნებისმიერ შემთხვევაში, ცნობილია, რომ ფილოსოფიური ქვის ძიებაში ალქიმიკოსები ყველა სახის მასალას ახორციელებდნენ დისტილაციისა და სხვა ოპერაციების, მათ შორის შარდის, ექსკრეციის, ძვლების და ა.შ. ფოსფორები. მე-17 საუკუნეში ცნობილი იყო ბოლონიის ფოსფორი - ბოლონიის მახლობლად მთებში ნაპოვნი ქვა; ქვანახშირზე სროლის შემდეგ ქვამ ბზინვის უნარი შეიძინა. ასევე აღწერილია „ბალდუინის ფოსფორი“, რომელიც მომზადებულია ვოლოსტი ოსტატის ალდუინის მიერ ცარცისა და აზოტის მჟავის კალცინირებული ნარევიდან. ასეთი ნივთიერებების სიკაშკაშე იწვევდა უკიდურეს გაოცებას და ითვლებოდა სასწაულად.
1669 წელს ჰამბურგელი მოყვარული ალქიმიკოსი ბრენდი, გაკოტრებული ვაჭარი, რომელიც ოცნებობდა ალქიმიის დახმარებით გაეუმჯობესებინა თავისი საქმეები, დაამუშავა მრავალფეროვანი პროდუქტი. იმის თეორიით, რომ ფიზიოლოგიური პროდუქტები შესაძლოა შეიცავდეს „პირველ მატერიას“, რომელიც ფილოსოფიური ქვის საფუძველად ითვლება, ბრენდი დაინტერესდა ადამიანის შარდით.
მან დაახლოებით ერთი ტონა შარდი შეაგროვა ჯარისკაცების ყაზარმებიდან და აორთქლდა სიროფიანი სითხის შესაქმნელად. მან კვლავ გამოხდა ეს სითხე და მიიღო მძიმე წითელი „შარდის ზეთი“. ამ ზეთის ხელახლა გამოხდის შემდეგ, მან აღმოაჩინა რეტორტის ბოლოში „მკვდარი თავის“ ნაშთები (Caput mortuum), რომელიც ერთი შეხედვით არაფრისთვის გამოუსადეგარი იყო. თუმცა, ამ ნარჩენების კალცირება დიდი დრო, მან შეამჩნია, რომ რეზერვში თეთრი მტვერი გაჩნდა, რომელიც ნელ-ნელა ძირს იდგა და აშკარად ანათებდა. ბრენდმა გადაწყვიტა, რომ მან მოახერხა ელემენტარული ცეცხლის ამოღება "ზეთოვანი სიკვდილის თავიდან" და მან კიდევ უფრო დიდი მონდომებით განაგრძო ექსპერიმენტები. მან, რა თქმა უნდა, ვერ შეძლო ამ "ცეცხლის" ოქროდ გადაქცევა, მაგრამ ფოსფორის აღმოჩენა (ბერძნულიდან - მსუბუქი და "გამტარი", ანუ სინათლის მომტანი) მაინც მკაცრ საიდუმლოდ შეინახა. თუმცა, გარკვეულმა კუნკელმა, რომელიც იმ დროს ალქიმიკოსად და საქსონიის კურფიურსტის საიდუმლო მსახურობდა, შეიტყო ბრენდის საიდუმლოს შესახებ. კუნკელმა ჰამბურგში მიმავალ კოლეგას კრაფტს სთხოვა, რომ ბრენდისგან ფოსფორის შესახებ რაიმე ინფორმაცია გაეგო. თუმცა კრაფტმა თავად გადაწყვიტა გამოეყენებინა ბრენდის საიდუმლო. მან საიდუმლო მისგან 200 ტალერად იყიდა და საკმარისი რაოდენობის ფოსფორის გამომუშავებით გაემგზავრა ევროპაში, სადაც დიდი წარმატებააჩვენა ფოსფორის ბზინვარება დიდგვაროვანი ხალხის წინაშე. კერძოდ, ინგლისში მან ფოსფორი აჩვენა მეფე ჩარლზ II-ს და მეცნიერ ბოილს. იმავდროულად, კუნკელმა თავად მოახერხა ფოსფორის მომზადება ბრენდის მეთოდთან ახლოს და ამ უკანასკნელისგან განსხვავებით, ფართოდ აქვეყნებდა ფოსფორის რეკლამას, მაგრამ დუმდა მისი წარმოების საიდუმლოების შესახებ. 1680 წელს, მიუხედავად მისი წინამორბედებისა, ახალი ელემენტი მიიღო ცნობილმა ინგლისელმა ფიზიკოსმა და ქიმიკოსმა რობერტ ბოილმა, რომელმაც, კუნკელის მსგავსად, გამოაქვეყნა მონაცემები ფოსფორის თვისებების შესახებ, მაგრამ მისი მომზადების მეთოდი დახურულ შეფუთვაში მოახსენა მხოლოდ ლონდონის სამეფო საზოგადოება (ეს შეტყობინება გამოქვეყნდა მხოლოდ 12 წლის შემდეგ, ბოილის გარდაცვალების შემდეგ) და ბოისის სტუდენტმა ა. განკვვიცმა უღალატა წმინდა მეცნიერებას და კვლავ გააცოცხლა „ფოსფორის სპეკულაცია“ ამ ნივთიერების წარმოებისთვის ფართო საწარმოო საქმიანობის სახით: 50 წლის განმავლობაში იგი ფართოდ ვაჭრობდა ფოსფორს ძალიან მაღალ ფასად. მაგალითად, ჰოლანდიაში უნცია (31,1 გ) ფოსფორი იმ დროს ღირდა 16 დუკატი. ყველაზე ფანტასტიკური ვარაუდები გაკეთდა ფოსფორის ბუნებასთან დაკავშირებით. მე-18 საუკუნეში ბევრი გამოჩენილი მეცნიერი სწავლობდა ფოსფორს და მათ შორის მარგგრაფი, რომელმაც გააუმჯობესა შარდიდან ფოსფორის მიღების მეთოდი ამ უკანასკნელს ტყვიის ქლორიდის დამატებით (1743).
1777 წელს შეელმა დაადგინა ფოსფორის არსებობა ცხოველების ძვლებში და რქებში ცაცხვთან დაკავშირებული ფოსფორის მჟავის სახით. თუმცა ზოგიერთი ავტორი ამ აღმოჩენას სხვა შვედ ქიმიკოსს, ჰანს მიაწერს, მაგრამ სწორედ შელემ შეიმუშავა ძვლებიდან ფოსფორის მიღების მეთოდი. ლავუაზიემ ფოსფორი ელემენტარულ ნივთიერებად აღიარა ჟანგბადში ფოსფორის წვის შესახებ მისი ცნობილი ექსპერიმენტების საფუძველზე. მარტივი სხეულების ცხრილში ლავუაზიემ ფოსფორი მოათავსა უბრალო სხეულების მეორე ჯგუფში, არალითონური, დამჟანგველი და წარმომქმნელი მჟავები. მე-19 საუკუნიდან ფოსფორი ფართოდ გამოიყენება ძირითადად ნიადაგის გასანაყოფიერებლად გამოყენებული მარილების სახით.
ასე რომ, სამასზე მეტი წელი გვაშორებს იმ მომენტს, როდესაც ჰამბურგელმა ალქიმიკოსმა გენინგ ბრენდმა აღმოაჩინა ახალი ელემენტი - ფოსფორი. სხვა ალქიმიკოსების მსგავსად, ბრენდიც ცდილობდა ეპოვა სიცოცხლის ელექსირი ან ფილოსოფიური ქვა, რომლის დახმარებით მოხუცები უფრო ახალგაზრდულად გამოიყურებიან, ავადმყოფები გამოჯანმრთელდებიან და ძირეული ლითონები ოქროდ იქცევა. ბრენდს ხელმძღვანელობდა არა ხალხის კეთილდღეობა, არამედ პირადი ინტერესი. ამას მოწმობს ფაქტები მის მიერ გაკეთებული ერთადერთი რეალური აღმოჩენის ისტორიიდან. ფოსფორის ისტორიის პირველ, ორმოცდაათწლიან ეტაპზე, ბოილის აღმოჩენის გარდა, მეცნიერების ისტორიით აღინიშნა მხოლოდ ერთი მოვლენა: 1715 წელს გენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში. მარკგრეივის ექსპერიმენტების შემდეგ, ელემენტის ისტორია, რომელმაც მრავალი წლის შემდეგ შეიძინა ნომერი 15, გახდა მრავალი დიდი აღმოჩენის ისტორია.
ფოსფორთან დაკავშირებული აღმოჩენების ქრონოლოგია
1715 წელსგენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში...
1743 წელსგერმანელი ქიმიკოსი, პეტერბურგის მეცნიერებათა აკადემიის საპატიო წევრი ა. მარგგრაფი განვითარდა ახალი გზაფოსფორის მიღება.

1769 წელსიუ.განმა დაამტკიცა, რომ ძვლები შეიცავს უამრავ ფოსფორს. იგივე დაადასტურა ორი წლის შემდეგ შვედმა ქიმიკოსმა კ.შელემ, რომელმაც შემოგვთავაზა ძვლების გამოწვის დროს წარმოქმნილი ფერფლიდან ფოსფორის მიღების მეთოდი. რამდენიმე წლის შემდეგ ჯ.ლ.პრუსტმა და მ.კლაპროტმა სხვადასხვა ბუნებრივი ნაერთების შესწავლით დაამტკიცეს, რომ ფოსფორი ფართოდ არის გავრცელებული დედამიწის ქერქში, ძირითადად კალციუმის ფოსფატის სახით.
1797 წრუსეთში A.A. Musin-Pushkin-მა მიიღო ფოსფორის ალოტროპული სახეობა - იისფერი ფოსფორი. თუმცა ლიტერატურაში ფოსფორის აღმოჩენა შეცდომით მიეწერება ი.ჰიტორფს, რომელმაც ა.ა.მუსინ-პუშკინის მეთოდით იგი მხოლოდ 1853 წელს მოიპოვა.

1799 წელსდონდონალდმა დაამტკიცა, რომ ფოსფორის ნაერთები აუცილებელია მცენარეების ნორმალური განვითარებისთვის.
1839 წელსკიდევ ერთი ინგლისელი, Laws, იყო პირველი, ვინც მიიღო სუპერფოსფატი - ფოსფორის სასუქი, რომელიც ადვილად შეიწოვება მცენარეთა მიერ.
1842 წელსინგლისმა მოაწყო სუპერფოსფატის პირველი ინდუსტრიული წარმოება მსოფლიოში. რუსეთში ასეთი წარმოება გამოჩნდა 1868 და 1871 წლებში.

1848 წელსავსტრიელმა ქიმიკოსმა ა.შროტერმა აღმოაჩინა ფოსფორის ალოტროპული მოდიფიკაცია - წითელი ფოსფორი. მან ეს ფოსფორი მიიღო თეთრი ფოსფორის გაცხელებით 250 გრადუსამდე ტემპერატურაზე CO (ნახშირბადის მონოქსიდი ორი) ატმოსფეროში. საინტერესოა, რომ ა.შროტერმა პირველმა აღნიშნა

ასანთის წარმოებაში წითელი ფოსფორის გამოყენების შესაძლებლობა.
1926 წელსფერსმანმა და მისმა კოლეგებმა კოლას ნახევარკუნძულზე აპატიტის უზარმაზარი მარაგი აღმოაჩინეს.
1934 წელს, ამერიკელი ფიზიკოსი პ. ბრიჯმანი, რომელიც სწავლობს მაღალი წნევის გავლენას სხვადასხვა ნივთიერებები, იზოლირებული გრაფიტისმაგვარი შავი ფოსფორი.
ფოსფორი არის ცხოვრების მნიშვნელოვანი კომპონენტი და უსულო ბუნება. ის გვხვდება დედამიწის სიღრმეში, წყალში და ჩვენს სხეულებში და აკადემიკოსმა ფერსმანმა მას მეტსახელად "სიცოცხლისა და აზროვნების ელემენტი" უწოდა. მიუხედავად მისი სარგებლობისა, თეთრი ფოსფორი შეიძლება იყოს უკიდურესად საშიში და შხამიანი. მოდით უფრო დეტალურად ვისაუბროთ მის მახასიათებლებზე.
ელემენტის გახსნა
ფოსფორის აღმოჩენის ისტორია ალქიმიით დაიწყო. მე-15 საუკუნიდან მოყოლებული ევროპელი მეცნიერები ცდილობდნენ იპოვონ ფილოსოფიური ქვა ან „დიდი ელექსირი“, რომლითაც მათ შეუძლიათ ნებისმიერი ლითონი ოქროდ აქციონ.
მე-17 საუკუნეში ალქიმიკოსმა ჰენიგ ბრენდმა გადაწყვიტა, რომ "ჯადოსნური რეაგენტის" გზა შარდში გადიოდა. ის ყვითელია, რაც ნიშნავს, რომ შეიცავს ოქროს ან რაღაცნაირად უკავშირდება მას. მეცნიერი საგულდაგულოდ აგროვებდა მასალას, იცავდა და შემდეგ გამოხდიდა. ოქროს ნაცვლად მან მიიღო თეთრი ნივთიერება, რომელიც სიბნელეში ანათებდა და კარგად იწვოდა.
ბრენდმა აღმოჩენას "ცივი ცეცხლი" უწოდა. მოგვიანებით, ირლანდიელმა ალქიმიკოსმა რობერტ ბოილმა და გერმანელმა ანდრეას მაგგრაფმა გაუჩნდა იდეა ფოსფორის მსგავსი გზით მოპოვების შესახებ. ამ უკანასკნელმა შარდში ნახშირი, ქვიშა და მინერალური ფოსგენიტიც დაამატა. მოგვიანებით, ნივთიერებას დაარქვეს ფოსფორი მირაბილისი, რაც ითარგმნა როგორც "სინათლის სასწაულებრივი მატარებელი".
მანათობელი ელემენტი
ფოსფორის აღმოჩენა ნამდვილი სენსაცია გახდა ალქიმიკოსებს შორის. ზოგი დროდადრო ცდილობდა ბრენდისგან ნივთიერების მოპოვების საიდუმლოს ყიდვას, ზოგიც დამოუკიდებლად ცდილობდა იქ მისვლას. მე-18 საუკუნეში დადასტურდა, რომ ელემენტს შეიცავდა ორგანიზმების ძვლის ნაშთები და მალე გაიხსნა მისი წარმოებისთვის რამდენიმე ქარხანა.
ფრანგმა ფიზიკოსმა ლავუაზიემ დაამტკიცა, რომ ფოსფორი არის მარტივი ნივთიერება. პერიოდულ სისტემაში არის ნომერი 15. აზოტთან, ანტიმონთან, დარიშხანთან და ბისმუტთან ერთად იგი მიეკუთვნება პნიკტიდების ჯგუფს და ხასიათდება როგორც არალითონი.

ელემენტი ბუნებაში საკმაოდ გავრცელებულია. პროცენტული თვალსაზრისით, ის დედამიწის ქერქის მასით მე-13 ადგილს იკავებს. ფოსფორი აქტიურად ურთიერთქმედებს ჟანგბადთან და არ გვხვდება თავისუფალი სახით. ის არსებობს მრავალ მინერალში (190-ზე მეტი), როგორიცაა ფოსფორიტები, აპატიტები და ა.შ.
თეთრი ფოსფორი
ფოსფორი არსებობს რამდენიმე ფორმით ან ალოტროპად. ისინი ერთმანეთისგან განსხვავდებიან სიმკვრივით, ფერითა და ქიმიური თვისებებით. ჩვეულებრივ არსებობს ოთხი ძირითადი ფორმა: თეთრი, შავი, წითელი და მეტალის ფოსფორი. სხვა მოდიფიკაციები მხოლოდ ზემოაღნიშნულის ნაზავია.

თეთრი ფოსფორი ძალიან არასტაბილურია. ნორმალური განათების პირობებში ის სწრაფად წითლდება, მაგრამ მაღალი წნევა შავდება. მისი ატომები განლაგებულია ტეტრაედრის სახით. მას აქვს კრისტალური მოლეკულური ბადე, მოლეკულური ფორმულით P4.
მე ასევე ხაზს ვუსვამ ყვითელ ფოსფორს. ეს არ არის ნივთიერების მორიგი მოდიფიკაცია, არამედ არარაფინირებული თეთრი ფოსფორის სახელი. მას შეიძლება ჰქონდეს ღია ან მუქი ყავისფერი ელფერი და ხასიათდება ძლიერი ტოქსიკურობით.
თეთრი ფოსფორის თვისებები
ნივთიერების კონსისტენცია და გარეგნობა ცვილს წააგავს. ნივრის სუნი აქვს და შეხებით ცხიმიანია. ფოსფორი რბილია (იჭრება დანით დიდი ძალისხმევის გარეშე) და დეფორმირებადია. გაწმენდის შემდეგ ხდება უფერული. მისი გამჭვირვალე კრისტალები მზეზე ირიბად ანათებს და ალმასს ჰგავს.
ის დნება 44 გრადუსზე. ნივთიერების აქტივობა თავს იჩენს ოთახის ტემპერატურაზეც კი. ფოსფორის მთავარი მახასიათებელია ქიმილუმინესცენტური ან ბზინვის უნარი. ჰაერში იჟანგება, ის ასხივებს თეთრ-მწვანე შუქს და დროთა განმავლობაში სპონტანურად ანთებს.

ნივთიერება პრაქტიკულად არ იხსნება წყალში, მაგრამ შეიძლება დაიწვას მასში ჟანგბადთან ხანგრძლივი კონტაქტით. ის კარგად იხსნება ორგანულ გამხსნელებში, როგორიცაა ნახშირბადის დისულფიდი, თხევადი პარაფინი და ბენზოლი.
ფოსფორის გამოყენება
ადამიანმა ფოსფორი „მოათვინიერა“ როგორც მშვიდობიანი, ასევე სამხედრო მიზნებისთვის. ნივთიერება გამოიყენება ფოსფორმჟავას წარმოებისთვის, რომელიც გამოიყენება სასუქებისთვის. ადრე მას ფართოდ იყენებდნენ მატყლის შესაღებად და ფოტომგრძნობიარე ემულსიების დასამზადებლად.
თეთრი ფოსფორი ფართოდ არ გამოიყენება. მისი მთავარი ღირებულება არის აალებადი. ამრიგად, ნივთიერება გამოიყენება ცეცხლგამჩენი საბრძოლო მასალისთვის. ამ ტიპის იარაღი აქტუალური იყო ორივე მსოფლიო ომის დროს. იგი გამოიყენეს ღაზას ომში 2009 წელს, ასევე ერაყში 2016 წელს.

წითელი ფოსფორი უფრო ფართოდ გამოიყენება. გამოიყენება საწვავის, საპოხი მასალების, ასაფეთქებელი ნივთიერებების და ასანთის თავების დასამზადებლად. სხვადასხვა ფოსფორის ნაერთები გამოიყენება მრეწველობაში წყლის დამარბილებლებში და ემატება პასივაციურ აგენტებს ლითონის კოროზიისგან დასაცავად.
შინაარსი სხეულში და გავლენა ადამიანებზე
ფოსფორი ჩვენთვის ერთ-ერთი სასიცოცხლო ელემენტია. კალციუმის ნაერთების სახით ის იმყოფება კბილებსა და ჩონჩხში, რაც ძვლებს აძლევს სიმტკიცეს და სიმტკიცეს. ელემენტი იმყოფება ATP და დნმ ნაერთებში. ის აუცილებელია ტვინის ფუნქციონირებისთვის. ნერვულ უჯრედებში ყოფნა ხელს უწყობს ნერვული იმპულსების გადაცემას.
ფოსფორი გვხვდება კუნთოვან ქსოვილში. ის მონაწილეობს ორგანიზმში შემავალი ცილების, ცხიმებისა და ნახშირწყლების ენერგიის გარდაქმნის პროცესში. ელემენტი ინარჩუნებს მჟავა-ტუტოვანი ბალანსს უჯრედებში და ხდება მათი დაყოფა. ის ხელს უწყობს მეტაბოლიზმს და აუცილებელია სხეულის ზრდისა და აღდგენის დროს.
თუმცა, ფოსფორი შეიძლება საშიში იყოს. თავად თეთრი ფოსფორი ძალიან ტოქსიკურია. 50 მილიგრამზე მეტი დოზები ფატალურია. ფოსფორით მოწამვლას თან ახლავს ღებინება, თავის ტკივილი და კუჭის ტკივილი. ნივთიერების კონტაქტი კანთან იწვევს დამწვრობას, რომელიც ძალიან ნელა და მტკივნეულად კურნავს.
ჭარბი ფოსფორი ორგანიზმში იწვევს მტვრევად ძვლებს, გულ-სისხლძარღვთა დაავადებებს, სისხლდენას და ანემიას. ღვიძლი და საჭმლის მომნელებელი სისტემა ასევე განიცდის ფოსფორის გადაჭარბებულ გაჯერებას.
„...დიახ! ეს იყო ძაღლი, უზარმაზარი, შავი ფერის. მაგრამ არცერთ ჩვენგანს, მოკვდავებს, არ უნახავს ასეთი ძაღლი. ღია პირიდან ალი აფეთქდა, თვალები ნაპერწკლებს აფრქვევდა და მბჟუტავი ცეცხლი აფრქვევდა მის მუწუკსა და ზურგზე. არავის ციებ-ცხელებულ ტვინში ვერ გაჩნდა ხილვა, რომელიც უფრო საშინელი, ამაზრზენი იყო, ვიდრე ეს ჯოჯოხეთური არსება, რომელიც ნისლიდან გადმოგვხტა... საშინელი ძაღლი, ახალგაზრდა ლომის ზომა. მისი უზარმაზარი პირი ჯერ კიდევ მოლურჯო ალივით ანათებდა, ღრმად ჩამწკრივებული ველური თვალები ცეცხლოვანი წრეებით იყო გარშემორტყმული.
ამ მანათობელ თავს შევეხე და ხელი მოვშორე და დავინახე, რომ ჩემი თითებიც სიბნელეში ანათებდნენ. ფოსფორი, მე ვთქვი“.
Ისწავლა? არტურ კონან დოილი. "Ბასკერვილების ძაღლი."
ეს არის საზიზღარი ამბავი, რომელშიც მონაწილეობდა მე-15 ელემენტი.
კიდევ ერთი ცუდი ამბავი
სამასზე მეტი წელი გვაშორებს იმ მომენტს, როდესაც ჰამბურგელმა ალქიმიკოსმა გენინგ ბრენდმა აღმოაჩინა ახალი ელემენტი - ფოსფორი. სხვა ალქიმიკოსების მსგავსად, ბრენდიც ცდილობდა ეპოვა სიცოცხლის ელექსირი ან ფილოსოფიური ქვა, რომლის დახმარებით მოხუცები უფრო ახალგაზრდულად გამოიყურებიან, ავადმყოფები გამოჯანმრთელდებიან და ძირეული ლითონები ოქროდ იქცევა. ბრენდს ხელმძღვანელობდა არა ხალხის კეთილდღეობა, არამედ პირადი ინტერესი. ამას მოწმობს ფაქტები მის მიერ გაკეთებული ერთადერთი რეალური აღმოჩენის ისტორიიდან.
ერთ-ერთი ექსპერიმენტის დროს მან აორთქლდა შარდი, ნარჩენი ნახშირთან და ქვიშაში შეურია და განაგრძო აორთქლება. მალე რეტორტში წარმოიქმნა ნივთიერება, რომელიც სიბნელეში ანათებდა. მართალია, kaltes Feuer (ცივი ცეცხლი), ან "ჩემი ცეცხლი", როგორც მას ბრენდმა უწოდა, არ აქცევდა ტყვიას ოქროდ და არ ცვლიდა მოხუცების გარეგნობას, მაგრამ ის ფაქტი, რომ მიღებული ნივთიერება ანათებდა გაცხელების გარეშე, უჩვეულო და ახალი იყო. .
ბრენდმა სწრაფად ისარგებლა ახალი ნივთიერების ამ თვისებით. მან დაიწყო ფოსფორის ჩვენება სხვადასხვა პრივილეგირებულ პირებს, მათგან საჩუქრებს და ფულს იღებდა. ფოსფორის მოპოვების საიდუმლოს შენახვა ადვილი არ იყო და ბრენდმა ის მალე მიჰყიდა დრეზდენელ ქიმიკოს ი.კრაფს. ფოსფორის დემონსტრატორთა რიცხვი გაიზარდა, როდესაც მისი წარმოების რეცეპტი ცნობილი გახდა ი.კუნკელი და კ.კირჩმეიერი. 1680 წელს, მიუხედავად მისი წინამორბედებისა, ახალი ელემენტი მიიღო ცნობილმა ინგლისელმა ფიზიკოსმა და ქიმიკოსმა რობერტ ბოილმა. მაგრამ ბოილი მალე გარდაიცვალა და მისმა სტუდენტმა ა. განკვვიცმა უღალატა წმინდა მეცნიერებას და კვლავ გააცოცხლა "ფოსფორის სპეკულაცია". მხოლოდ 1743 წელს იპოვა ა. მარკგრაფმა ფოსფორის წარმოების უფრო მოწინავე მეთოდი და გამოაქვეყნა თავისი მონაცემები საჯარო ინფორმაციისთვის. ამ მოვლენამ დაასრულა ბრენდის ბიზნესი და გახდა ფოსფორისა და მისი ნაერთების სერიოზული შესწავლის დასაწყისი.
ფოსფორის ისტორიის პირველ, ორმოცდაათწლიან ეტაპზე, ბოილის აღმოჩენის გარდა, მეცნიერების ისტორიით აღინიშნა მხოლოდ ერთი მოვლენა: 1715 წელს გენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში. მარკგრეივის ექსპერიმენტების შემდეგ, ელემენტის ისტორია, რომელმაც მრავალი წლის შემდეგ შეიძინა ნომერი 15, გახდა მრავალი დიდი აღმოჩენის ისტორია.
ამ აღმოჩენების ქრონოლოგია
1769 წელს იუ განმა დაამტკიცა, რომ ძვლები შეიცავს უამრავ ფოსფორს. იგივე დაადასტურა ორი წლის შემდეგ ცნობილმა შვედმა ქიმიკოსმა კ.შელემ, რომელმაც შემოგვთავაზა ძვლების გამოწვის დროს წარმოქმნილი ფერფლისგან ფოსფორის წარმოების მეთოდი.
რამდენიმე წლის შემდეგ ჯ.ლ. პრუსტმა და მ.კლაპროტმა სხვადასხვა ბუნებრივი ნაერთების შესწავლით დაამტკიცეს, რომ ფოსფორი ფართოდ არის გავრცელებული დედამიწის ქერქში, ძირითადად კალციუმის ფოსფატის სახით.
მან დიდ წარმატებას მიაღწია ფოსფორის თვისებების შესწავლაში მე-18 საუკუნის 70-იანი წლების დასაწყისში. დიდი ფრანგი ქიმიკოსი ანტუან ლორან ლავუაზიე. ფოსფორის დაწვით სხვა ნივთიერებებთან ჰაერის დახურულ მოცულობაში, ლავუაზიემ დაამტკიცა, რომ ფოსფორი დამოუკიდებელი ელემენტია, ხოლო ჰაერს აქვს რთული შემადგენლობა და შედგება მინიმუმ ორი კომპონენტისგან - ჟანგბადისა და აზოტისგან. ”ამ გზით, მან პირველად დააყენა ფეხზე მთელი ქიმია, რომელიც თავის ფლოგისტიკური ფორმით იდგა თავზე.” ასე წერდა ფ. ენგელსი ლავუაზიეს შემოქმედების შესახებ კაპიტალის მეორე ტომის წინასიტყვაობაში.
1799 წელს დონდონალდმა დაამტკიცა, რომ ფოსფორის ნაერთები აუცილებელია მცენარეების ნორმალური განვითარებისთვის.
1839 წელს კიდევ ერთმა ინგლისელმა, ლაუსმა, პირველმა მიიღო სუპერფოსფატი - ფოსფორიანი სასუქი, რომელიც ადვილად შეიწოვება მცენარეთა მიერ.
1847 წელს გერმანელმა ქიმიკოსმა შროტერმა თეთრი ფოსფორის ჰაერის წვდომის გარეშე გაცხელებით მიიღო მე-15 ელემენტის ახალი ჯიში (ალოტროპული მოდიფიკაცია) - წითელი ფოსფორი, ხოლო უკვე მე-20 საუკუნეში, 1934 წელს, ამერიკელი ფიზიკოსი პ.ბრიჯმანი სწავლობდა. მაღალი წნევის გავლენა სხვადასხვა ნივთიერებებზე, იზოლირებული შავი ფოსფორი, გრაფიტის მსგავსი. ეს არის მთავარი ეტაპები No15 ელემენტის ისტორიაში. ახლა ვნახოთ, რა მოჰყვა თითოეულ ამ აღმოჩენას.
„1715 წელს გენსინგმა დაადგინა ფოსფორის არსებობა ტვინის ქსოვილში... 1769 წელს ჰანმა დაამტკიცა, რომ ძვლები შეიცავს უამრავ ფოსფორს“.
ფოსფორი არის აზოტის ანალოგი. მიუხედავად იმისა, რომ ამ ელემენტების ფიზიკური და ქიმიური თვისებები ძალიან განსხვავებულია, მათ ასევე აქვთ რაღაც საერთო, კერძოდ ის ფაქტი, რომ ორივე ეს ელემენტი აბსოლუტურად აუცილებელია ცხოველებისა და მცენარეებისთვის. აკადემიკოსი ა.ე. ფერსმანმა ფოსფორს უწოდა "სიცოცხლისა და აზროვნების ელემენტი" და ეს განმარტება ძნელად შეიძლება კლასიფიცირდეს როგორც ლიტერატურული გაზვიადება. ფოსფორი გვხვდება მწვანე მცენარეების ფაქტიურად ყველა ორგანოში: ღეროებში, ფესვებში, ფოთლებში, მაგრამ ყველაზე მეტად ხილსა და თესლში. მცენარეები აგროვებენ ფოსფორს და აწვდიან მას ცხოველებს.
ცხოველებში ფოსფორი ძირითადად კონცენტრირებულია ჩონჩხში, კუნთებსა და ნერვულ ქსოვილში.
ადამიანის საკვებ პროდუქტებს შორის ფოსფორით განსაკუთრებით მდიდარია ქათმის კვერცხის გული.
ადამიანის ორგანიზმი შეიცავს საშუალოდ დაახლოებით 1,5 კგ No15 ელემენტს. აქედან 1,4 კგ ძვლებშია, დაახლოებით 130 გ კუნთებში და 12 გ ნერვებში და ტვინში. ჩვენს ორგანიზმში მიმდინარე თითქმის ყველა უმნიშვნელოვანესი ფიზიოლოგიური პროცესი დაკავშირებულია ფოსფორორგანული ნივთიერებების გარდაქმნასთან. ფოსფორი არის ძვლებში ძირითადად კალციუმის ფოსფატის სახით. კბილის მინანქარი ასევე ფოსფორის ნაერთია, რომელიც შემადგენლობითა და კრისტალური სტრუქტურით შეესაბამება ყველაზე მნიშვნელოვან ფოსფორის მინერალს, აპატიტს Ca 5 (PO 4) 3 (F, Cl).
ბუნებრივია, როგორც ნებისმიერი სასიცოცხლო ელემენტი, ფოსფორი ბუნებაში ციკლს გადის. მცენარეები მას ნიადაგიდან იღებენ, მცენარეებიდან კი ეს ელემენტი ხვდება ადამიანისა და ცხოველის სხეულში. ფოსფორი მიწაში ბრუნდება ექსკრემენტებით და როცა გვამები ლპება. ფოსფორობაქტერიები ორგანულ ფოსფორს არაორგანულ ნაერთებად გარდაქმნის.
თუმცა, დროის ერთეულში, ნიადაგიდან გაცილებით მეტი ფოსფორი გამოიყოფა, ვიდრე მიწაში შედის. მსოფლიო მოსავალი ყოველწლიურად 3 მილიონ ტონაზე მეტ ფოსფორს აშორებს მინდვრებიდან.
ბუნებრივია, მდგრადი მოსავლიანობის მისაღებად, ეს ფოსფორი უნდა დაბრუნდეს ნიადაგში და ამიტომ გასაკვირი არ არის, რომ ფოსფატის ქანების მსოფლიო წარმოება ახლა წელიწადში 100 მილიონ ტონაზე მეტს შეადგენს.
პრუსტმა და კლაპროტმა დაამტკიცეს, რომ ფოსფორი ფართოდ არის გავრცელებული დედამიწის ქერქში, ძირითადად კალციუმის ფოსფატის სახით.
დედამიწის ქერქში ფოსფორი მხოლოდ ნაერთების სახით გვხვდება. ეს არის ძირითადად ორთოფოსფორის მჟავას ცუდად ხსნადი მარილები; კატიონი ყველაზე ხშირად არის არაკალციუმი.
ფოსფორი დედამიწის ქერქის წონის 0,08%-ს შეადგენს. გავრცელების თვალსაზრისით, იგი მე-13 ადგილზეა ყველა ელემენტს შორის. ფოსფორს შეიცავს მინიმუმ 190 მინერალი, რომელთაგან ყველაზე მნიშვნელოვანია: ფტორპატიტი - Ca 5 (PO 4) 3 F, ჰიდროქსიაპატიტი Ca 5 (PO 4) 3 OH, ფოსფორიტი Ca 3 (PO 4) 2 მინარევებით.
ნაკლებად გავრცელებულია ვივიანიტი Fe 3 (PO 4) 2 8H 2 O, მონაზიტი (Ce, La)PO 4, ამბლიგონიტი LaAl(PO 4)F, ტრიფილიტი Li(Fe, Mn)PO 4 და კიდევ უფრო იშვიათად ქსენოტიმი YPO 4 და ტორბერნიტი. Cu (UO 2) 2 [PO 4 ] 2 12H 2 O.
ფოსფორის მინერალები იყოფა პირველად და მეორად. პირველებს შორის განსაკუთრებით გავრცელებულია აპატიტები, რომლებიც ხშირად გვხვდება ცეცხლოვანი წარმოშობის ქანებს შორის. ეს მინერალები წარმოიქმნება დედამიწის ქერქის წარმოქმნის დროს.
აპატიტებისაგან განსხვავებით, ფოსფორიტები გვხვდება დანალექი წარმოშობის ქანებს შორის, რომლებიც წარმოიქმნება ცოცხალი არსებების სიკვდილის შედეგად. ეს არის მეორადი მინერალები.
ფოსფორი მეტეორიტებში გვხვდება რკინის, კობალტის და ნიკელის ფოსფიდების სახით. რა თქმა უნდა, ეს საერთო ელემენტი ასევე გვხვდება ზღვის წყალში (6·10–6%).
„ლავუაზიემ დაამტკიცა, რომ ფოსფორი დამოუკიდებელი ქიმიური ელემენტია...“
ფოსფორი არის საშუალო აქტივობის არალითონი (რასაც ადრე მეტალოიდს ეძახდნენ). ფოსფორის ატომის გარე ორბიტა შეიცავს ხუთ ელექტრონს, რომელთაგან სამი დაუწყვილებელია. აქედან გამომდინარე, მას შეუძლია გამოავლინოს 3–, 3+ და 5+ ვალენტობა.
იმისთვის, რომ ფოსფორმა გამოავლინოს 5+ ვალენტობა, აუცილებელია ატომზე გარკვეული გავლენა, რაც ბოლო ორბიტის ორ დაწყვილებულ ელექტრონს დაუწყვილებად გადააქცევს.
ფოსფორს ხშირად უწოდებენ მრავალმხრივ ელემენტს. მართლაც, სხვადასხვა პირობებში ის განსხვავებულად იქცევა, ავლენს ან ჟანგვის ან შემცირების თვისებებს. ფოსფორის მრავალფეროვნება ასევე მოიცავს მის უნარს არსებობდეს რამდენიმე ალოტროპულ მოდიფიკაციაში.
შესაძლოა, No15 ელემენტის ყველაზე ცნობილი მოდიფიკაცია არის რბილი, ცვილისებრი, თეთრი ან ყვითელი ფოსფორი. სწორედ ბრენდმა აღმოაჩინა იგი და მისი თვისებების წყალობით ელემენტმა მიიღო სახელი: ბერძნულად "ფოსფორი" ნიშნავს მანათობელ, მანათობელ. თეთრი ფოსფორის მოლეკულა შედგება ოთხი ატომისგან, რომლებიც განლაგებულია ტეტრაედრის სახით. სიმკვრივე 1.83, დნობის წერტილი 44.1°C. თეთრი ფოსფორი შხამიანია და ადვილად იჟანგება. ხსნადი ნახშირბადის დისულფიდში, თხევად ამიაკში და SO 2-ში, ბენზოლში, ეთერში. წყალში თითქმის არ იხსნება.
როდესაც თბება ჰაერზე წვდომის გარეშე 250°C-ზე ზემოთ, თეთრი ფოსფორი წითლად იქცევა. ეს უკვე პოლიმერია, მაგრამ არა ძალიან მოწესრიგებული სტრუქტურა. წითელი ფოსფორის რეაქტიულობა მნიშვნელოვნად ნაკლებია, ვიდრე თეთრი ფოსფორის. ის არ ანათებს სიბნელეში, არ იხსნება ნახშირბადის დისულფიდში და არ არის შხამიანი (ყოველთვის შეიცავს მცირე რაოდენობით თეთრ ფოსფორს, რის შედეგადაც ის შეიძლება იყოს შხამიანი.). მისი სიმკვრივე გაცილებით დიდია, სტრუქტურა წვრილკრისტალურია.
ნაკლებად ცნობილია ფოსფორის სხვა, კიდევ უფრო მაღალმოლეკულური მოდიფიკაციები - იისფერი, ყავისფერი და შავი, რომლებიც ერთმანეთისგან განსხვავდებიან მოლეკულური წონით და მაკრომოლეკულების რიგითობის ხარისხით. შავი ფოსფორი, რომელიც პირველად მიიღო P. Bridgman-მა მაღალი წნევის პირობებში (200 ათასი ატმოსფერო 200°C ტემპერატურაზე), უფრო მოგვაგონებს გრაფიტს, ვიდრე თეთრი ან წითელი ფოსფორი. ეს ცვლილებები ლაბორატორიული ეგზოტიკურია და თეთრი და წითელი ფოსფორისგან განსხვავებით პრაქტიკული გამოყენებაჯერ არ უპოვია.
სხვათა შორის, ელემენტარული ფოსფორის გამოყენების შესახებ; მისი ძირითადი მომხმარებლები არიან ასანთის წარმოება, მეტალურგია და ქიმიური წარმოება. ახლო წარსულში მიღებული ელემენტარული ფოსფორის ნაწილი იხარჯებოდა სამხედრო საწარმოებში.
მეტალურგები, როგორც წესი, ცდილობენ მოიცილონ ლითონში არსებული ფოსფორის მინარევები - ეს აუარესებს მექანიკურ თვისებებს, მაგრამ ზოგჯერ ფოსფორი შეგნებულად შეჰყავთ შენადნობებში. ეს კეთდება მაშინ, როდესაც საჭიროა ლითონის ოდნავ გაფართოება გამაგრებისას და ზუსტად მიიღოს ფორმის მონახაზი. ფოსფორი ასევე ფართოდ გამოიყენება ქიმიაში. მისი ნაწილი გამოიყენება ფოსფორის ქლორიდების მოსამზადებლად, რომელიც საჭიროა გარკვეული ორგანული პრეპარატების სინთეზისთვის; ელემენტარული ფოსფორის წარმოების ეტაპი ასევე წარმოდგენილია კონცენტრირებული ფოსფორის სასუქების წარმოების ზოგიერთ ტექნოლოგიურ სქემაში.
ახლა მისი კავშირების შესახებ.
ფოსფორის ანჰიდრიდი P 2 O 5 არის შესანიშნავი გამწმენდი, რომელიც ხარბად შთანთქავს წყალს ჰაერიდან და სხვა ნივთიერებებიდან. P 2 O 5 შემცველობა არის ყველა ფოსფატური სასუქის ღირებულების მთავარი კრიტერიუმი.
ფოსფორის მჟავები, ძირითადად ფოსფორის მჟავა H 3 PO 4 , გამოიყენება ძირითად ქიმიურ მრეწველობაში. ფოსფორის მჟავების მარილები, პირველ რიგში, არის ფოსფორის სასუქები (მათ შესახებ სპეციალური განხილვა) და ტუტე ლითონის ფოსფატები, რომლებიც აუცილებელია სარეცხი საშუალებების წარმოებისთვის.
ფოსფორის ჰალოიდები (ძირითადად ქლორიდები PCl 3 და PCl 5) გამოიყენება ორგანული სინთეზის ინდუსტრიაში.
წყალბადის ფოსფორის ნაერთებიდან ყველაზე ცნობილია ფოსფინი PH 3 - უაღრესად მომწამვლელი უფერო აირი ნივრის სუნით.
ფოსფორის ნაერთებს შორის განსაკუთრებული ადგილი უკავია ფოსფორორგანულ ნაერთებს. უმეტესობას აქვს ბიოლოგიური აქტივობა. ამიტომ, ფოსფორორგანული ნაერთები გამოიყენება როგორც წამალი, ზოგი კი მავნებლების კონტროლის საშუალებად.
ნივთიერებების დამოუკიდებელი კლასი შედგებოდა ფოსფონიტრილის ქლორიდებისგან - ფოსფორის ნაერთები აზოტით და ქლორით. ფოსფონიტრილის ქლორიდის მონომერს შეუძლია პოლიმერიზაცია. ზრდასთან ერთად მოლეკულური წონაიცვლება ამ კლასის ნივთიერებების თვისებები, კერძოდ, შესამჩნევად მცირდება მათი ხსნადობა ორგანულ სითხეებში. როდესაც პოლიმერის მოლეკულური წონა რამდენიმე ათასს აღწევს, მიიღება რეზინის მსგავსი ნივთიერება - ჯერჯერობით ერთადერთი რეზინა, რომელიც ნახშირბადს საერთოდ არ შეიცავს. მოლეკულური წონის შემდგომი ზრდა იწვევს პლასტმასის მსგავსი მყარი ნივთიერებების წარმოქმნას. "ნახშირბადო რეზინას" აქვს მნიშვნელოვანი სითბოს წინააღმდეგობა: ის იწყებს ნგრევას მხოლოდ 350°C ტემპერატურაზე.
”1839 წელს ინგლისელმა კანონებმა პირველმა მიიღო სუპერფოსფატი - ფოსფორიანი სასუქი, რომელიც ადვილად შეიწოვება მცენარეებით.”
იმისათვის, რომ მცენარეებმა აითვისონ ფოსფორი, ის უნდა იყოს ხსნად ნაერთში. ამ ნაერთების მისაღებად კალციუმის ფოსფატს და გოგირდის მჟავას ურევენ ისეთი პროპორციებით, რომ ფოსფატის თითო გრამ მოლეკულაზე მჟავას ორი გრამი მოლეკულაა. ურთიერთქმედების შედეგად წარმოიქმნება სულფატი და ხსნადი კალციუმის დიჰიდროფოსფატი: Ca 3 (PO 4) 2 + 2H 2 SO 4 → 2CaSO 4 + Ca (H 2 PO 4) 2. ამ ორი მარილის ნარევი ცნობილია როგორც სუპერფოსფატი. ამ ნარევში, კალციუმის სულფატი აგროქიმიის თვალსაზრისით არის ბალასტი, მაგრამ ჩვეულებრივ არ არის გამოყოფილი, რადგან ეს ოპერაცია ძვირია და მნიშვნელოვნად ზრდის სასუქის ღირებულებას. მარტივი სუპერფოსფატი შეიცავს მხოლოდ 14...20% P 2 O 5.
უფრო კონცენტრირებული ფოსფორის სასუქი არის ორმაგი სუპერფოსფატი. იგი მიიღება კალციუმის ფოსფატის ფოსფორის მჟავასთან რეაქციით:
Ca 3 (PO 4) 2 + 4H 3 PO 4 → 3Ca (H 2 PO 4) 2.
ორმაგი სუპერფოსფატი შეიცავს 40...50% P 2 O 5. სინამდვილეში, უფრო სწორი იქნება, რომ მას სამმაგი ვუწოდოთ: ის სამჯერ უფრო მდიდარია ფოსფორით, ვიდრე უბრალო სუპერფოსფატი.
ზოგჯერ CaHPO 4 2H 2 O ნალექი გამოიყენება ფოსფორის სასუქად, რომელიც მიიღება ფოსფორის მჟავას ჰიდროქსიდთან ან კალციუმის კარბონატთან რეაქციით:
Ca(OH) 2 + H 3 PO 4 → CaHPO 4 2H 2 O.
2CaCO 3 + 2H 3 PO 4 → 2CaHPO 4 2H 2 O + 2CO 2.
ეს სასუქი შეიცავს 30...35% P 2 O 5.
ფოსფორის ნედლეულის შესწავლილი მარაგით როგორც ჩვენს ქვეყანაში, ისე მთელ მსოფლიოში, მდგომარეობა მთლად ხელსაყრელი არ არის. აკადემიკოსი ს.ი. ვოლფკოვიჩი მენდელეევის IX კონგრესის ტრიბუნიდან გენერალურ და გამოყენებითი ქიმიაგანაცხადა:
”თუ აზოტის ინდუსტრიის ნედლეულის ბაზა - ჰაერის ოკეანე, წყალი და ბუნებრივი აირი - არ ზღუდავს ახალი მშენებლობის მასშტაბებს, ხოლო კალიუმის მარილების საბადოები, რომლებიც დღემდე გამოკვლეულია, უზრუნველყოფს კალიუმის სასუქების წარმოების განვითარებას ათასწლეულის განმავლობაში, მაშინ შიდა ფოსფორის ნედლეულის მარაგი, რომელიც დღემდე შესწავლილია სასუქის წარმოების დაგეგმილი დიდი მოცულობით, მხოლოდ რამდენიმე ათწლეულის განმავლობაში გაგრძელდება“.
ეს სულაც არ ნიშნავს, რომ კაცობრიობას შიმშილი ემუქრება და მოსავალი წლიდან წლამდე მცირდება. არის რეზერვები. ბევრი დამატებითი ფოსფორის მიღება შესაძლებელია მინერალური ნედლეულის კომპლექსური დამუშავების, ქვედა ზღვის ნალექისა და უფრო დეტალური გეოლოგიური გამოკვლევით. შესაბამისად, პესიმიზმის განსაკუთრებული საფუძველი არ გვაქვს, მით უმეტეს, რომ ფოსფორის მადნების რეგისტრირებული მარაგებით სსრკ მსოფლიოში პირველ ადგილზეა. ჩვენ გვაქვს აპატიტის უდიდესი საბადოები კოლას ნახევარკუნძულზე და ფოსფორიტები სამხრეთ ყაზახეთში და სხვა რიგ ადგილებში.
მაგრამ ახლა საჭიროა ახალი საბადოების ძიება და ღარიბი მადნებიდან ფოსფატური სასუქების წარმოების მეთოდების შემუშავება. ეს აუცილებელია მომავლისთვის, რადგან ფოსფორი - "სიცოცხლისა და აზროვნების ელემენტი" - ყოველთვის საჭირო იქნება კაცობრიობისთვის.
ფოსფორის იზოტოპები
ბუნებრივი ფოსფორი, ელემენტების დიდი უმრავლესობისგან განსხვავებით, შედგება მხოლოდ ერთი იზოტოპისგან 31 P. 15 ელემენტის რამდენიმე ხანმოკლე რადიოაქტიური იზოტოპი სინთეზირებულია ბირთვულ რეაქციებში. ერთ-ერთი მათგანი, ფოსფორი-30, ხელოვნურად მიღებული პირველი იზოტოპი აღმოჩნდა. ეს მიიღეს 1934 წელს ფრედერიკ და ირინე ჯოლიო-კიურიების მიერ ალუმინის ალფა ნაწილაკებით დასხივებით. ფოსფორ-30-ის ნახევარგამოყოფის პერიოდი 2,55 წუთია და მისი დაშლისას გამოყოფს პოზიტრონებს („დადებითი ელექტრონები“). ამჟამად ცნობილია ფოსფორის ექვსი რადიოაქტიური იზოტოპი. მათგან ყველაზე ხანგრძლივ, 33 P, ნახევარგამოყოფის პერიოდი 25 დღეა. ფოსფორის იზოტოპები ძირითადად გამოიყენება ბიოლოგიურ კვლევებში.
სუპერფოსფატების ინდუსტრიის დასაწყისი
მსოფლიოში პირველი სუპერფოსფატის ინდუსტრიული წარმოება მოეწყო 1842 წელს ინგლისში. რუსეთში მსგავსი საწარმოები გამოჩნდა 1868 და 1871 წლებში. რევოლუციამდე ჩვენს ქვეყანაში მხოლოდ ექვსი სუპერფოსფატის ქარხანა აშენდა, მათი მთლიანი პროდუქტიულობა წელიწადში 50 ათას ტონას არ აღემატებოდა. პირველი მსოფლიო ომის დროს საგარეო ინტერვენცია და სამოქალაქო ომიექვსი ქარხნიდან ოთხი ჩაიშალა და 1918 წელს ჩვენს ქვეყანაში მხოლოდ 2,8 ათასი ტონა სუპერფოსფატი იწარმოებოდა. და მხოლოდ 20 წლის შემდეგ, 1938 წელს, ფოსფატური სასუქების წარმოებისთვის საბჭოთა კავშირიპირველი ადგილი ევროპაში და მეორე მსოფლიოში. ახლა ჩვენი ქვეყნის წილი ფოსფატური ქანების და ფოსფატური სასუქების მსოფლიო წარმოებაში დაახლოებით მეოთხედია.
ჩვენება დ.ნ. პრიანიშნიკოვი
„...რაც არ უნდა სწორად იყოს შენახული და გამოყენებული სასუქი, ის ვერ დააბრუნებს ნიადაგს იმას, რაც თავად არ შეიცავს, ე.ი. მეურნეობიდან გასხვისებული ფოსფორის დიდი წილი გაყიდულ მარცვლეულში, ცხოველის ძვლებში, რძეში და ა.შ. ამრიგად, ნიადაგი თანდათან, მაგრამ სტაბილურად კარგავს თავის ფოსფორს (ან თუნდაც მის შესათვისებელ ნაწილს) და გარკვეული ზღვრის მიღმა, ფოსფორი ხვდება იმ „მინიმალურ ფაქტორში“, რომელიც ყველაზე მეტად აკლია კარგი მოსავლის მისაღებად, როგორც ეს იყო საკმაოდ სწორად. აღნიშნა ლიბიგმა“. (სტატიიდან „ჩვენი სოფლის მეურნეობისთვის ფოსფატების მნიშვნელობისა და ფოსფორიტების პირდაპირი გამოყენების შესაძლებლობის გაფართოების შესახებ“, 1924 წ.).
არქტიკის აპატიობა
1926 წელს ა.ე. ფერსმანმა და მისმა თანამშრომლებმა კოლას ნახევარკუნძულზე აპატიტის უზარმაზარი მარაგი აღმოაჩინეს. მრავალი წლის შემდეგ, აკადემიკოსმა ა.ე. ფერსმანი წერდა ამ საბადოს შესახებ: „...ცქრიალა აპატიტი ნაცრისფერი ნეფელინით ქმნის უწყვეტ კედელს 100 მ სიგრძის ხიბინის ტუნდრას, გადაჭიმულია 25 კმ-ზე, ირგვლივ რგოლის სახით. კვლევამ აჩვენა, რომ აპატიტის საბადო ღრმად ხვდება ოკეანის ზედაპირის ქვემოთაც და დაახლოებით ორი მილიარდი ტონა ამ ძვირფასი მინერალები დაგროვდა აქ, ხიბინის მთებში, რომელიც მსოფლიოს ნებისმიერ წერტილში არ არის მსგავსი. („გასართობი მინერალოგია“, 1937 წ.) ამ საბადოს ბაზაზე აშენდა აპატიტის სამთო-ქიმიური ქარხანა. ᲡᲛ. კიროვი. ომამდე ცოტა ხნით ადრე აღმოაჩინეს ფოსფორის ნედლეულის კიდევ ერთი ძალიან დიდი საბადო - ყარა-ტაუს ფოსფორიტები ყაზახეთში. ფოსფორიტები ასევე გვხვდება ჩვენი ქვეყნის სხვა რეგიონებში, კერძოდ მოსკოვის რეგიონში. მაგრამ ფოსფატური სასუქების წარმოებისთვის საუკეთესო ნედლეული მაინც მოდის აპატიტის "ხიბინის ტუნდრას სარტყელიდან".
რას ჰგავს აპატიტი?
მოდით კვლავ მივმართოთ „გასართობ მინერალოგიას“. ”აპატიტი არის კალციუმის ფოსფატი, მაგრამ მისი გარეგნობა იმდენად მრავალფეროვანი და უცნაურია, რომ ტყუილად არ ეძახდნენ ძველ მინერალოგებს მას აპატიტი, რაც ბერძნულად ნიშნავს ”მატყუარას”: ან ეს არის გამჭვირვალე კრისტალები, რომლებიც წვრილად მოგვაგონებს ბერილს ან თუნდაც კვარცს, ან ისინი მკვრივი მასებია, მარტივი კირქვისგან არ განსხვავდებიან, მერე რადიალური სფეროებია, ან კლდე მარცვლოვანი და მბზინავია, როგორც მსხვილმარცვლოვანი მარმარილო.”
ვინ არის პირველი?
ფრანგი ისტორიკოსი ფ. გეფერი ამტკიცებს, რომ საყოველთაოდ მიღებული აზრი იმის შესახებ, რომ ფოსფორი პირველად ალქიმიკოსმა გ.ბრანდმა 1669 წელს მიიღო, არასწორია. მისი თქმით, ფოსფორის მოპოვება ჯერ კიდევ მე-12 საუკუნეში შეძლეს. არაბი ალქიმიკოსები და ფოსფორის მოპოვების მათი ტექნოლოგია იგივე იყო, რაც ბრენდის: შარდის აორთქლება და მშრალი ნარჩენების გაცხელება ნახშირით და ქვიშით. თუ ასეა, მაშინ კაცობრიობა თითქმის 800 წელია იცნობს No15 ელემენტს.
წითელი და იასამნისფერი
ფოსფორის ყველაზე ცნობილი მოდიფიკაციებია თეთრი და წითელი, რომლებიც ორივე გამოიყენება ინდუსტრიაში. No15 ელემენტის სხვა ჯიშები - იისფერი, ყავისფერი, შავი ფოსფორი - მხოლოდ ლაბორატორიებში გვხვდება. მაგრამ იისფერი ფოსფორი ხალხისთვის უფრო ადრე გახდა ცნობილი, ვიდრე წითელი ფოსფორი. რუსი მეცნიერი ა.ა. მუსინ-პუშკინმა ის პირველად 1797 წელს მიიღო. ზოგიერთ წიგნში შეგიძლიათ იხილოთ განცხადება, რომ წითელი და იისფერი ფოსფორი ერთი და იგივეა. მაგრამ ეს ჯიშები განსხვავდება არა მხოლოდ ფერით. იისფერი ფოსფორის კრისტალები უფრო დიდია. წითელი ფოსფორი მიიღება თეთრი ფოსფორის გაცხელებით დახურულ მოცულობაში უკვე 250°C, ხოლო იისფერი მხოლოდ 500°C-ზე.
"ნათელი ბერი"
აკადემიკოს ს.ი.-ს მოგონებებიდან. ვოლფკოვიჩი: „ფოსფორი იწარმოებოდა მოხოვაიას ქუჩაზე მოსკოვის უნივერსიტეტში დამონტაჟებულ ელექტროღუმელში. ვინაიდან ეს ექსპერიმენტები იმ დროს პირველად ჩატარდა ჩვენს ქვეყანაში, მე არ მივიღე სიფრთხილის ზომები, რაც აუცილებელია აირისებრ ფოსფორთან მუშაობისას - მომწამვლელ, თვითგამწვავ და მოლურჯო ელემენტთან მუშაობისას. ელექტროღუმელში მუშაობის მრავალი საათის განმავლობაში გამოთავისუფლებული ფოსფორის გაზის ნაწილი იმდენად გაჯერდა ჩემს ტანსაცმელს და ფეხსაცმელსაც კი, რომ როცა უნივერსიტეტიდან ღამით დავდიოდი მოსკოვის ბნელ, მაშინდელი განათებულ ქუჩებში, ჩემი ტანსაცმელი მოლურჯო ელვარებას ასხივებდა. და ჩემი ფეხსაცმლის ქვემოდან (მათი ხახუნისას) ტროტუარზე) ნაპერწკლები მოდიოდა.
ყოველთვის, როცა ჩემს უკან ბრბო იკრიბებოდა, რომელთა შორის, ჩემი ახსნა-განმარტების მიუხედავად, ბევრი იყო, ვინც ჩემში ხედავდა სხვა სამყაროს „ახლად გამოჩენილ“ წარმომადგენელს. მალე, მოხოვაიას რაიონის მცხოვრებთა შორის და მთელ მოსკოვში, ფანტასტიკური ისტორიები "ნათელი ბერის" შესახებ დაიწყო პირიდან პირში გადაცემა...
სასწაულები სასწაულების გარეშე
ეკლესიამ არაერთხელ გამოიყენა თეთრი ფოსფორი მორწმუნეების მოსატყუებლად. ცნობილია მინიმუმ ორი სახის "სასწაული", რომელშიც ეს ნივთიერება მონაწილეობს. სასწაული პირველი: სანთელი, რომელიც თავისით ანათებს. ეს კეთდება ასე: ნახშირბადის დისულფიდში ნახშირბადის ფოსფორის ხსნარი გამოიყენება ფითილზე, გამხსნელი საკმაოდ სწრაფად აორთქლდება, ხოლო ფითილზე დარჩენილი ფოსფორის მარცვლები იჟანგება ატმოსფერული ჟანგბადით და სპონტანურად აალდება. მეორე სასწაული: კედლებზე მოციმციმე „ღვთაებრივი“ წარწერები. იგივე ხსნარი, იგივე რეაქციები. თუ ხსნარი საკმარისად გაჯერებულია, წარწერები ჯერ ანათებს, შემდეგ ციმციმებს და ქრება.
ორგანოფოსფორი და სიცოცხლე
მრავალი ტომი დაიწერა ფოსფორორგანული ნაერთების როლზე სხეულის ყველაზე მნიშვნელოვან ბიოქიმიურ რეაქციებში. ბიოქიმიის ნებისმიერ სახელმძღვანელოში ეს ნივთიერებები არა მხოლოდ არაერთხელ არის ნახსენები, არამედ დეტალურად არის აღწერილი. ფოსფორორგანული ნაერთების გარეშე ტვინის ქსოვილში ნახშირწყლების ცვლის პროცესი ვერ მოხდებოდა. ფოსფორის შემცველი ფერმენტი ფოსფორილაზა ხელს უწყობს არა მხოლოდ დაშლას, არამედ ტვინში პოლისაქარიდების სინთეზსაც. თავის ტვინის ქსოვილში ნახშირწყლების დაჟანგვის პროცესში მნიშვნელოვან როლს თამაშობს დიფოსფო-პირიდინის ნუკლეოტიდი და არაორგანული ფოსფატი. კიდევ ერთი მნიშვნელოვანი პროცესი - კუნთების შეკუმშვა მხარს უჭერს ადენოზინფოსფატებთან დაკავშირებული რეაქციების დროს გამოთავისუფლებულ ენერგიას. როდესაც კუნთი იკუმშება, ადენოზინის ტრიფოსფატის (ATP) მოლეკულა იშლება ადენოზინის დიფოსფატად და არაორგანულ ფოსფორის მჟავად. ეს გამოყოფს უამრავ ენერგიას (8...11 კკალ/მოლი). ამ ნივთიერებების უმნიშვნელოვანეს როლზე მეტყველებს ის ფაქტი, რომ ატფ-ის მუდმივი დონე ყოველთვის შენარჩუნებულია კუნთოვან ქსოვილში.