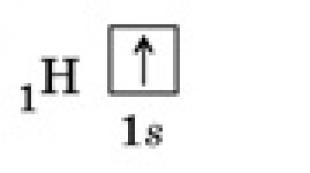
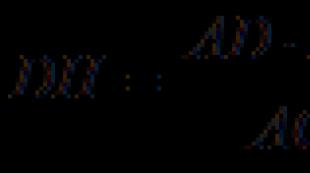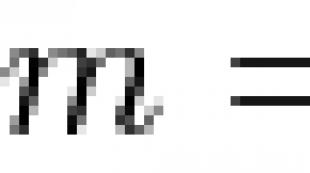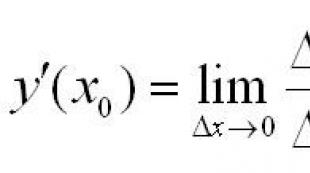ქიმიის ძირითადი ცნებები და კანონები. ჰემოგლობინის მოლური მასა ჰემოგლობინის მოლეკულური წონა
15. მოცემულ ტემპერატურაზე 0,2 მოლ/ლ კონცენტრაციის სურფაქტანტის ხსნარიდან შეიწოვება 2 96 10 3 მოლ/გ ნივთიერება ზოგიერთი ადსორბენტით. განისაზღვროს ადსორბციის უნარი (მოლ/გ), თუ მუდმივია a 0,07 მოლ/ლ.
[ადსორბენტის მოცულობა 4 00 10 3 მოლ/გ]
16. ფროუნდლიხის განტოლების გამოყენებით გამოთვალეთ ძმარმჟავას წონასწორული კონცენტრაცია ხსნარში, თუ 1 გ ნახშირი.
17. აცეტონის წყალში გახსნისას განსაზღვრეთ ადსორბციის ტიპი, თუ წყალში აცეტონის კონცენტრაცია არის 29 გ/ლ, ზედაპირი.
ხსნარის დაძაბულობა - 59 4 |
3 ნ/მ, ზედაპირული დაჭიმულობა |
||||||
წყალი - 73 49 10 |
3 ნ/მ, ტ |
||||||
[ადსორბცია დადებითი, |
6 მოლი მ2] |
||||||
18. იზობუტირმჟავას ხსნარის კონცენტრაციის 0,125-დან 0,250 მოლ/ლ-მდე მატებით, მისი ზედაპირული დაძაბულობა მცირდება 55,1-დან 47,9 მნ/მ-მდე, ხოლო იზოვალერინის მჟავას ხსნარის - 43,2-დან 35,0 მნნ/მ-მდე. შეადარეთ ნივთიერებების ადსორბციული მნიშვნელობები მოცემულ კონცენტრაციის დიაპაზონში 293 K.
19. დაადგინეთ, იზრდება თუ მცირდება წყალხსნარებიდან ზედაპირული ადსორბციის რაოდენობა კონცენტრაციის მატებასთან ერთად (T 298 K), თუ ცნობილია შემდეგი ექსპერიმენტული მონაცემები:
[ადსორბცია იზრდება 2 12 10 6-დან 9 09 10 6 მოლმ2-მდე ხსნარში სურფაქტანტის კონცენტრაციის გაზრდით]
20. რამდენჯერ შეიცვლება ბუტირის მჟავას ადსორბცია წყალხსნარიდან კონცენტრაციის მატებასთან ერთად ექსპერიმენტული მონაცემების მიხედვით (T 288 K):
c 102, |
|||||
3, ნ/მ |

21. კალციუმის ქლორიდის და გოგირდმჟავას 1%-იანი ხსნარის შერეული თანაბარი მოცულობები (სიმკვრივეების ტოლი 1 გ/მლ). დაწერეთ მიცელების ფორმულები მიღებული კალციუმის სულფატის სოლის.
[გრანულები უარყოფითად არის დამუხტული]
22. რა მოცულობის ვერცხლის ნიტრატის ხსნარი 0,001 მოლ/ლ კონცენტრაციით უნდა დაემატოს 10 მლ ნატრიუმის ქლორიდის ხსნარს cNaCl 0,002 მოლ/ლ, რომ მივიღოთ ხსნარი, რომლის გრანულები დადებითად დამუხტულია? დაწერეთ სოლის მიკელის აგებულების დიაგრამა.
[გრანულები დადებითად არის დამუხტული, AgNO 3 ხსნარის მოცულობა უნდა იყოს 0,02 ლ-ზე მეტი]
23. ამონიუმის სულფიდის რა მინიმალური მოცულობა 0,001 მოლ/ლ კონცენტრაციით უნდა დაემატოს 15 მლ მანგანუმის(II) ქლორიდის 0,003 მოლ/ლ კონცენტრაციით ხსნარის მისაღებად უარყოფითად დამუხტული ნაწილაკებით?
24. პრუსიული ლურჯი Fe 4 Fe CN 6 3 გრანულა ანოდში გადადის ელექტრულ ველში. რა ნივთიერება ემსახურება როგორც სტაბილიზატორი? დაწერეთ მიკელის ფორმულა.
[სტაბილიზატორი - K4 Fe CN 6 ]
25. 100 მლ 0,03% NaCl ხსნარს (1 გ/მლ) ემატება 250 მლ 0,001 Mr AgNO 3 ხსნარი. დაწერეთ ლუმიცელის სოლის ფორმულა. ქვემოთ ჩამოთვლილთაგან რომელი ელექტროლიტი გამოიწვევს ამ სოლის კოაგულაციას ყველაზე დაბალი კოაგულაციის ზღურბლით: KCl, Ba NO 3 2,
K2 CrO 4 , MgSO 4 , AlCl3 ?
[გრანულები უარყოფითად არის დამუხტული, შესაბამისად, კოაგულანტი იონები არის კათიონები. ყველაზე დაბალი კოაგულაციის ბარიერი AlCl3-ისთვის]
26. K2 SiO 3-ისა და HCl-ის ხსნარების რეაქციის შედეგად მიიღეს სილიციუმის მჟავა სოლი. დაწერეთ სოლის მიცელის ფორმულა და დაადგინეთ, ელექტროლიტებიდან რომელი იყო ჭარბი, თუ კონტრიონები ელექტრულ ველში გადადიან კათოდში?
[ჭარბი K2 SiO 3]

27. რა მოცულობის 0,001 M FeCl 3 ხსნარი უნდა დაემატოს 0,03 ლ 0,002 M AgNO 3 ხსნარს, რათა ვერცხლის ქლორიდის ზოლის ნაწილაკები ელექტრულ ველში მოძრაობდეს ანოდისკენ? დაწერეთ მიცელეზოლის ფორმულა.
[FeCl 3-ის მოცულობა უნდა იყოს 0,02 ლ-ზე მეტი]
28. რკინის(III) ჰიდროქსიდის ჰიდროზოლის კოაგულაციის ზღურბლები ნატრიუმის სულფატთან და კალიუმის ქლორიდთან არის შესაბამისად 0,32 და 20,50 მმოლ/ლ. დაადგინეთ კოლოიდური სოლის ნაწილაკების მუხტის ნიშანი. გამოთვალეთ ამ ელექტროლიტების კოაგულაციის უნარი და შეადარეთ მათი თანაფარდობა გამოთვლილ შულზე-ჰარდის წესთან.
29. ელექტროლიტების შედედების უნარი გარკვეულ სოლთან მიმართებაში მცირდება თანმიმდევრობით: NH 4 3 PO 4 NH 4 2 SO 4 NH 4 NO3. რა არის კოლოიდური ნაწილაკების მუხტის ნიშანი? მოიყვანეთ ელექტროლიტების მაგალითები, რომელთა კოაგულაციის უნარი დაახლოებით ზემოაღნიშნულის ტოლი იქნება.
[sol ნაწილაკები დადებითად არის დამუხტული, იონების კოაგულაციის უნარი თითქმის არ მცირდება: PO 3 4 SO 2 4 NO 3 ]
30. მაგნიუმის სულფატთან სოლის კოაგულაციის ზღურბლი ნიტრატომბარიუმზე ნაკლებია. როგორ არის დამუხტული სოლის ნაწილაკები? რა შეგვიძლია ვთქვათ იმავე სოლის ჰეკოაგულაციაზე კალიუმის ფოსფატით?
31. 1,5ლ მოცულობით ოქროს სულფიდის ზოლის შედედება მოხდა 570მლ ნატრიუმის ქლორიდის ხსნარის დამატებით 0,2მოლ/ლ კონცენტრაციით. გამოთვალეთ ნატრიუმის იონური ხსნარის კოაგულაციის ბარიერი.
32. სოლის ჰიდროქსიდის და რკინის ფოსფატის იონების შედედების ზღვარი არის 0,37 მმოლ/ლ. რა მოცულობის ნატრიუმის ფოსფატის 5%-იანი ხსნარი (105 გ/მლ) არის საჭირო 750 მლ ხსნარის შესადედებლად?
[Na 3 PO 4 ხსნარის მოცულობა არის 0,87 მლ]
33. 2 ლიტრიანი ალუმინის ჰიდროქსიდის ხსნარის გამჭვირვალე კოაგულაცია მოხდა, როდესაც დაემატა 10,6 მლ ხსნარი K4 Fe CN 6 კონცენტრაციით 0,01 მოლ/ლ. გამოთვალეთ ჰექსაციანოფერატის იონების მიერ ხსნარის შედედების ბარიერი; დაწერეთ ალუმინის ჰიდროქსიდის მიცელების ფორმულა.
34. ოქროს სულფიდური ზოლის კალციუმის იონებით შედედების ზღვარი არის 0,69 მმოლ/ლ. რა მოცულობის ხსნარი კალციუმის ქლორიდის კონცენტრაციით 0,5 მოლ/ლ არის საჭირო 100 მლ ხსნარის შედედებისთვის?
[CaCl2 ხსნარის მოცულობა არის 0 15 10 3 ლ]
35. დაადგინეთ სოლის კოლოიდური ნაწილაკების მუხტის ნიშანი, თუ ელექტროლიტებით მისი შედედებისას მიიღება შემდეგი შედედების ზღურბლები (მმოლ/ლ): c pc KNO3 300; c pc MgCl2 320; c PC Na3 PO4 0 6.
[დადებითი]
36. რომელ ელექტროლიტს, Na2 SO4 ან MgCl2, ექნება უფრო დიდი შედედების უნარი ვერცხლის იოდიდის ხსნარისთვის, რომელიც მიიღება კალიუმის იოდიდის 0,01 მოლ/ლ ხსნარის თანაბარი მოცულობის შერევით და ვერცხლის ნიტრატის 0,015 მოლ/ლ ხსნარით. ლ?
[Na2 SO4-ის კოაგულაციის უნარი უფრო დიდია]
37. 10 მლ AgI უარყოფითად დამუხტული ხსნარის შედედება, 1,5 მლ ხსნარი KNO3 კონცენტრაციით 1 მოლ/ლ ან 0,5 მლ ხსნარი Ca NO3 2 კონცენტრაციით 0,1 მოლ/ლ ან 0,2 მლ. საჭიროა ხსნარი Al NO3 კონცენტრაციით 0,01 მოლ/ლ. მართალია თუ არა წესი c p 1 z 6?
[წესი შესრულებულია დაახლოებით]
38. დაწერეთ KAuO2-ით სტაბილიზირებული ოქროს ხსნარის მიცელის ფორმულა. რომელ ელექტროლიტს - NaCl, BaCl2, FeCl3 - ექნება კოაგულაციის უფრო დაბალი ზღურბლი?
[კოაგულაციის ბარიერი უფრო დაბალია FeCl3-ის შემთხვევაში]
39. ზეითუნის ზეთის სიმკვრივე 22 Æ C-ზე არის 960 კგ მ3, ხოლო წყლის სიმკვრივე ამ ტემპერატურაზე 996 კგ მ3. ზეითუნის ზეთი ვისკომეტრში გადის 21 წუთში 15,6 წამში და იგივე მოცულობის წყალი
წყალი 22 H2 O 9 58 10 4 N s m2. |
||
[ზეითუნის ზეთის სიბლანტე 841 3 |
10 4 N s m2 ] |
|
40. ნავთის სიბლანტე 20-ზე |
Æ C უდრის 1 8-ს |
10 3 Pa s, და vis- |
წყლის ძვალი იმავე პირობებში - 1 005 10 |
3 Pa s (N s m2). |
|
განსაზღვრეთ ნავთის სიმკვრივე, თუ ცნობილია, რომ ვისკომეტრიდან ნავთის გადინების დროა 53 წმ, ხოლო წყლის იგივე მოცულობა 24 წმ. წყლის სიმკვრივეა 998 კგ მ3.
[ნავთობის სიმკვრივეა 809 4 კგ მ3]
41. რომელ ელექტროდზე გადაადგილდება ცილის ნაწილაკები pI 4 0) ელექტროფორეზის დროს აცეტატის ბუფერში მომზადებული 100 მლ ხსნარისგან ნატრიუმის აცეტატის კონცენტრაციით 0,1 მოლ/ლ და 25 მლ ძმარმჟავას კონცენტრაციით 0,2 მოლი. /ლ?
[ამ ბუფერულ ხსნარში ცილა უარყოფითად არის დამუხტული და ელექტროფორეზის დროს გადადის ანოდში]
42. ხსნარი შეიცავს ცილების ნარევს: გლობულინი (pI 7), ალბუმინი (pI 4 9) და კოლაგენი (pI 4 0). რა pH მნიშვნელობით შეიძლება ამ ცილების გამოყოფა ელექტროფორეტულად?
[ცილები შეიძლება გამოიყოს ელექტროფორეზულად pH 4-9-ზე]
43. რომელ ელექტროდზე გადაინაცვლებს ცილის ნაწილაკები ელექტროფორეზის დროს, თუ მისი pI არის 4 და pH 5?
[ცილის ნაწილაკები გადავა ანოდისკენ]
44. ჰემოგლობინი pI 6 68 მოთავსებულია ბუფერულ ხსნარში წყალბადის იონის კონცენტრაციით 1 5 10 6 მოლ/ლ. ელექტროფორეზის დროს ჰემოგლობინის მოლეკულების მოძრაობის მიმართულების განსაზღვრა. ცნობილია, რომ სისხლის წითელ უჯრედებში pH არის 7 25. რა მუხტი აქვთ ჰემოგლობინის მოლეკულებს ამ pH მნიშვნელობისას.
[ჰემოგლობინის მოლეკულები გადაინაცვლებს კათოდისკენ; pH 7 25 ჰემოგლობინის მოლეკულებს აქვთ უარყოფითი მუხტი]
45. 1 კგ მ3 მასური კონცენტრაციის ცილის წყალხსნარის ოსმოსური წნევა ფიზიოლოგიურ ტემპერატურაზე არის 292,7 Pa. განსაზღვრეთ ცილის მოლეკულური მასა საშუალო მოლური მასისგან (ცილის მოლეკულა არის იზოდიამეტრული).
[ფარდობითი მოლეკულური წონა არის 87,940]
46. გამოთვალეთ საშუალო ოსმოსური წნევა 25 ცენტაციაზე - 4176 კგ მ3;
პოლისტიროლის მოლური მასა, თუ Æ C უდრის 120,9 Pa, ხოლო მასა კონ- 1 Pa m6 kg2.
47. შეიწოვება თუ არა ჟელატინი (pI 4 7) აცეტატის ბუფერში კომპონენტების თანაბარი შემცველობით 0 Æ C ტემპერატურაზე? როგორ ამოვიცნოთ ჟელატინის შეშუპების პროცესი? Განმარტე შენი პასუხი.
[შეშუპება მინიმალურია იზოელექტრული წერტილის მახლობლად]
48. 200 გ მასის რეზინის შეშუპებისას შეიწოვება 964 მლ ქლოროფორმი (1 9 გ მლ). გამოთვალეთ რეზინის შეშუპების ხარისხი და მიღებული ჟელეს პროცენტული შემადგენლობა.
[ 915 8%; რეზინი 9 84%; ქლოროფორმი 90 16%]
49. გამოთვალეთ პოლიმერის საშუალო მოლური მასა, თუ მისი დამახასიათებელი სიბლანტეა 0 126 მ3 კგ, მუდმივი K 5 10 5, 0 67.
50. პოლიმერის რა მასა უნდა მივიღოთ ხსნარის მოსამზადებლად, რომლის მოლური კონცენტრაცია ტოლია 0,0025 მოლ/კგ.
თუ გამხსნელის მასა არის 1,5 კგ? მონომერის მოლური მასა არის 100 გ/მოლი. პოლიმერიზაციის ხარისხი - 100.
51. რა pH მნიშვნელობით უნდა გამოიყოს ორი ფერმენტი 5 და 3 იზოელექტრული წერტილებით ელექტროფორეზით? როგორ არის დამუხტული ფერმენტის ნაწილაკები pH 4.6 ხსნარებში?
და 7.9?
[უნდა გამოიყოს pH 4-ზე; დამუხტავს pH 4 6 " " და " ", pH 7 9 " " და " "]
52. განსაზღვრეთ პოლიმეთილმეთაკრილატის მოლური მასა ვისკომეტრიული მეთოდის შემდეგი მონაცემების გამოყენებით:
კონცენტრაცია |
||||||
ხსნარი, კგ მ3 |
||||||
შემცირებული სიბლანტე |
||||||
სპირალის ხსნარი |
||||||
ბენზოლში |
მუდმივები: კ
105 ] |
53. ზოგიერთი BMC-ის მოლური მასა არის 600000 ხსნარის მოლური კონცენტრაცია, თუ ნივთიერების მასური კონცენტრაციაა 6 გ/ლ? როგორია ასეთი ხსნარის ოსმოსური წნევა 27-ზეÆ C?
54. 1 ლიტრი ხსნარი შეიცავს 5 გ ამილოზას. ასეთი ხსნარის ოსმოსური წნევა 27-ზეÆ C უდრის 0,15 მმ Hg. Ხელოვნება. გამოთვალეთ ამილოზის მოლური მასა.
55. მემბრანის ერთ მხარეს მოთავსებულია ცილის ხსნარი PrtCl კონცენტრაციით 0,1 მოლ/ლ, ხოლო მეორე მხარეს ნატრიუმის ქლორიდის კონცენტრაციით 0,2 მოლ/ლ. გამოთვალეთ ქლორიდიების კონცენტრაცია მემბრანის ორივე მხარეს წონასწორობის დამყარებისას.
56. ჟელატინის ოქროს რაოდენობის დასადგენად, 0,1 მლ 1% ჟელატინის ხსნარი დაემატა 9,9 მლ წითელი ოქროს ხსნარს. შემდეგ ჩატარდა თავდაპირველი ხსნარის 10 თანმიმდევრული განზავების სერია 1 მლ თითოეულ სინჯარაში 10%
ნატრიუმის ქლორიდის ხსნარი. პირველ ხუთ საცდელ მილში ცვლილებები არ დაფიქსირებულა, მაგრამ სინჯებში 6-10 ხსნარმა შეიძინა ლურჯი ელფერი. რა არის ოქროს რიცხვი?
57. განსაზღვრეთ ოსმოსური წნევა 293 K ჟელატინის წყალხსნარში, რომლის მასური კონცენტრაციაა 2 5 კგ მ. 3 .
ჟელატინის მოლური მასა არის 104600, ხოლო კოეფიციენტი
0 69 Pa m6 |
კგ 2. |
58. პოლიაკრილონიტრილის მოლეკულური წონა სხვადასხვა კონცენტრაციით დიფენილფორმამიდის ხსნარში არის 75000 და 39100 293 K-ზე, ხოლო შინაგანი სიბლანტე არის შესაბამისად 0,299 და 0,110. განსაზღვრეთ კოეფიციენტები და K მარკ–ჰაუვინკის განტოლებაში.
59. ჩირქოვანი მენინგიტის დიაგნოსტიკისას დგინდება ცერებროსპინალური სითხის ცილების დამცავი რაოდენობა. გამოთვალეთ ეს რიცხვი, თუ ცნობილია, რომ 20 მლ AgBr ხსნარის კოაგულაციის თავიდან ასაცილებლად 2 მლ ხსნარის ზემოქმედებით NaNO მასის წილით. 3 საჭიროა 10% ამ ხსნარში 3 მლ ცერებროსპინალური სითხის დამატება, რომელიც შეიცავს 2 გ ცილას 1 ლიტრში.
60. 26 გ/ლ ჰემოგლობინის შემცველი ხსნარის ოსმოსური წნევა იზოეკლექტიკურ მდგომარეობაში ტოლია 0,0117 გ/ლ ნატრიუმის ქლორიდის შემცველი ხსნარის ოსმოსური წნევა. აიღეთ ხსნარების სიმკვრივე 1 გ/მლ, ტემპერატურა 25Æ C, ვან'ტ ჰოფის კანონიდან გადახრა შეიძლება უგულებელყო. გამოთვალეთ ჰემოგლობინის მოლეკულური (მოლური) მასა.
აპლიკაცია
1. ძირითადი ფიზიკური მუდმივები
ავოგადროს მუდმივი, N A 6 02 1023 mol 1. უნივერსალური აირის მუდმივი, R 8 31 J mol
ბოლცმანის მუდმივი, k R N A 1 38 10 23 J K. გაზის ნორმალური მოლური მოცულობა, V 0 22 4 ლ მოლი. პლანკის მუდმივი, h 6 63 10 34 J s.
2. ფაქტორები და პრეფერენციები ათწილადის მრავალჯერადი და ჩარჩო ერთეულების და მათი აღნიშვნების ფორმირებისთვის
ფაქტორი, |
ფაქტორი, |
||||||
რომელზედაც |
რომელზედაც |
||||||
მრავლდება |
მრავლდება |
||||||
მთავარი |
მთავარი |
||||||
1012 |
|||||||
| მეტრი | |||||||
კილოგრამი |
|||||||
ელექტრული დენის სიძლიერე |
|||||||
თერმოდინამიკური ტემპერატურა |
|||||||
ნივთიერების რაოდენობა |
|||||||
მიღებული რაოდენობები |
სივრცე და დრო |
||||||
კვადრატული მეტრის |
|||||||
კუბური მეტრი |
|||||||
სიჩქარე |
მეტრი წამში |
||||||
მექანიკური წარმოებულები |
და თერმული რაოდენობით |
||||||
სიმჭიდროვე |
კილოგრამი თითო |
კგ მ3 |
|||||
კუბური მეტრი |
|||||||
ძალა, წონა |
|||||||
წნევა |
|||||||
ენერგია, სამუშაო, სითბოს რაოდენობა, |
|||||||
თერმოდინამიკური პოტენციალი |
|||||||
ენტროპია |
ჯული კელვინზე |
||||||
ელექტრული წარმოებულები |
და მაგნიტური სიდიდეები |
||||||
ელექტროენერგიის რაოდენობა |
|||||||
თერმოდინამიკური პოტენციალი |
|||||||
ელექტრული ძაბვა |
|||||||
ელექტრო პოტენციალი, |
|||||||
ელექტრომამოძრავებელი ძალა |
|||||||
ელექტრული წინააღმდეგობა |
|||||||
ცილები არის ნივთიერებების ყველაზე მნიშვნელოვანი კლასი, რომლებიც ქმნიან ცოცხალ ორგანიზმებს. ბევრი ცილა ფუნქციონირებს როგორც კატალიზატორი. ჰემოგლობინი ასევე ატარებს ჟანგბადს ფილტვებიდან ქსოვილებში.
25-1. ჰემოგლობინის მოლური მასაა გ/მოლი. ჰემოგლობინის საშუალო შემცველობა სისხლის წითელ უჯრედებში არის 15 გ/100 მლ. განსაზღვრეთ ჰემოგლობინის (M) მოლური კონცენტრაცია სისხლში.
25-3. ჰენრის კანონი შემდეგია:
ხსნადობა = კნაწილობრივი წნევა ( კГ – ჰენრის მუდმივი)
ჰენრის მუდმივი ჟანგბადისთვის არის 1,3 x 10 –3 მოლ/ლ/ატმ. გამოთვალეთ საშუალო მანძილი ორ ჟანგბადის მოლეკულას შორის წყალში ჰაერთან წონასწორობაში.
25-4. ჰემოგლობინის მოლეკულას შეუძლია დააკავშიროს ჟანგბადის ოთხამდე მოლეკულა. შეაფასეთ საშუალო მანძილი ჟანგბადის ორ მოლეკულას შორის ჟანგბადით გაჯერებულ სისხლში. შეადარეთ შედეგი 25-2 და 25-3 კითხვებზე პასუხებს. გამოიტანეთ დასკვნა ჰემოგლობინის ეფექტურობის შესახებ ჟანგბადის კონცენტრაციისა და ქსოვილებში მიტანის თვალსაზრისით, სადაც ჟანგბადის ნაწილობრივი წნევა დაბალია.
25-6. რამდენ განსხვავებულ ამინომჟავას შეიცავს ჰემოგლობინის მოლეკულა?
25-7. ტრიფსინი ჰიდროლიზებს პეპტიდურ ობლიგაციებს, რომლებიც წარმოიქმნება ლიზინისა და არგინინის კარბოქსილის ჯგუფების მიერ. მაგალითად, ქვემოთ მოცემული პეპტიდი
ტრიპსინის მოქმედების შემდეგ ის იშლება შემდეგ პეპტიდებად:
ჰემოგლობინს ექვემდებარებოდა დისულფიდური ბმების შემცირება და ალკილირება, შემდეგ კი სრული ჰიდროლიზი ტრიფსინის მოქმედებით. რამდენი ამინომჟავის ნარჩენისაგან შედგება (საშუალოდ) ჰიდროლიზის პროდუქტები?
ჰემოგლობინის მოლური მასა
ჰემოგლობი i n (Hb) (დან ჰემო. და ლათ. გლობუსი - ბურთი), წითელი რკინის შემცველი პიგმენტი ადამიანის, ხერხემლიანების და ზოგიერთი უხერხემლოების სისხლში; ორგანიზმში ის ასრულებს ჟანგბადის (O 2) ტრანსპორტირების ფუნქციას სასუნთქი ორგანოებიდან ქსოვილებში; ასევე მნიშვნელოვან როლს ასრულებს ნახშირორჟანგის ქსოვილებიდან სასუნთქ ორგანოებში გადატანაში. უხერხემლოების უმეტესობაში გლიცერინი თავისუფლად იხსნება სისხლში; ხერხემლიანებში და ზოგიერთ უხერხემლოში ის გვხვდება სისხლის წითელ უჯრედებში - ერითროციტებში, რაც შეადგენს მათი მშრალი ნარჩენების 94%-მდე. ერითროციტებში შემავალი აირის მოლური მასა დაახლოებით, პლაზმაში გახსნილი - მდე. ქიმიური ბუნების მიხედვით, გ. რთული ცილაა - ქრომოპროტეინი , რომელიც შედგება ცილოვანი გლობინისა და რკინის პორფირინის - ჰემისგან. მაღალ ცხოველებსა და ადამიანებში სისხლი შედგება 4 მონომერული ქვედანაყოფისგან, რომელთა მოლური მასა დაახლოებით 17000-ია; ორი მონომერი თითოეული შეიცავს 141 ამინომჟავის ნარჩენს ( ა-ჯაჭვი), დანარჩენი ორი - თითო 146 ნარჩენი ( ბ- ჯაჭვები).
ამ პოლიპეპტიდების სივრცითი სტრუქტურები დიდწილად მსგავსია. ისინი ქმნიან დამახასიათებელ „ჰიდროფობიურ ჯიბეებს“, რომლებშიც განლაგებულია ჰემის მოლეკულები (თითოეული ქვეგანყოფილებისთვის). ჰემში შემავალი რკინის ატომის 6 საკოორდინაციო ბმადან 4 მიმართულია პიროლის რგოლების აზოტისკენ; მე-5 უკავშირდება ჰისტიდინის იმიდაზოლის რგოლის აზოტს, რომელიც ეკუთვნის პოლიპეპტიდებს და მდებარეობს 87-ე ადგილზე. ა-ჯაჭვში და 92-ე ადგილზეა ბ-ჯაჭვები; მე-6 ბმა მიმართულია წყლის მოლეკულასთან ან სხვა ჯგუფთან (ლიგანდებთან), მათ შორის ჟანგბადთან. ქვედანაყოფები თავისუფლად არის დაკავშირებული ერთმანეთთან წყალბადის, მარილისა და სხვა არაკოვალენტური ბმებით და ადვილად იშლება ამიდების გავლენის ქვეშ და მარილის გაზრდილი კონცენტრაციით ძირითადად სიმეტრიული დიმერების წარმოქმნით. ბ) და ნაწილობრივ ა-და ბ- მონომერები. გაზის მოლეკულის სივრცითი სტრუქტურა შეისწავლა რენტგენის დიფრაქციული ანალიზით (M. Peruts, 1959).
ამინომჟავების თანმიმდევრობა ა-და ბ-გ-ის ჯაჭვები მთელ რიგ უმაღლეს ცხოველებსა და ადამიანებში სრულიად გამორკვეულია. ჰემის მოლეკულაში, რომელიც აწყობილია ტეტრამერში, ჰემის ოთხივე ნარჩენი განლაგებულია ზედაპირზე და O 2-თან რეაქციები ადვილად ხელმისაწვდომია. O 2-ის დამატება უზრუნველყოფილია ჰემში Fe 2+ ატომის შემცველობით. ეს რეაქცია შექცევადია და დამოკიდებულია O 2-ის ნაწილობრივ წნევაზე (დაძაბულობაზე). ფილტვების კაპილარებში, სადაც O 2 ძაბვა არის დაახლოებით 100 მმ Hg. Ხელოვნება., G. აერთიანებს O 2-ს (ჟანგბადის პროცესი), გადაიქცევა ჟანგბადიან G. - ჟანგბადიან ჰემოგლობინში. ქსოვილის კაპილარებში, სადაც O 2 დაძაბულობა მნიშვნელოვნად დაბალია (დაახ. 40 მმ Hg. Ხელოვნება.), ხდება ოქსიჰემოგლობინის დისოციაცია ჰემოგლობინში და O 2; ეს უკანასკნელი შედის ორგანოებისა და ქსოვილების უჯრედებში, სადაც O 2-ის ნაწილობრივი წნევა კიდევ უფრო დაბალია (5-20 მმ Hg. სმ.); უჯრედების სიღრმეში ის თითქმის ნულამდე ეცემა. O 2-ის დამატება ჰემოგლობინში და ოქსიჰემოგლობინის დისოციაცია ჰემოგლობინში და O 2 თან ახლავს ჰემოგლობინის მოლეკულის კონფორმაციულ (სივრცულ) ცვლილებებს, აგრეთვე მის შექცევად დაშლას დიმერებად და მონომერებად, რასაც მოჰყვება აგრეგაცია ტეტრამერებად.
აირის თვისებები იცვლება O 2-თან ურთიერთობისას და სხვა თვისებები: ჟანგბადით გაჯერებული აირი 70-ჯერ უფრო ძლიერი მჟავაა, ვიდრე აირი. დამახასიათებელია შთანთქმის ზოლები სპექტრის ხილულ ნაწილში: G. აქვს ერთი მაქსიმუმი (554-ზე მმკ), ჟანგბადით გაჯერებულ გაზს აქვს ორი მაქსიმუმი 578 და 540 მმკ. G. შეუძლია უშუალოდ დააკავშიროს CO 2 (CO 2-ის რეაქციის შედეგად NH 2 - გლობინის ჯგუფებთან); ამ შემთხვევაში წარმოიქმნება კარბჰემოგლობინი - არასტაბილური ნაერთი, რომელიც ადვილად იშლება ფილტვების კაპილარებში ჰემოგლობინში და CO 2-ში.
ადამიანის სისხლში გ-ის რაოდენობა საშუალოდ 13-16-ია G%(ან 78%-96% სალის მიხედვით); ქალებში გ. ოდნავ ნაკლებია, ვიდრე მამაკაცებში. გ.-ის თვისებები იცვლება ონტოგენეზის დროს. ამიტომ განასხვავებენ ემბრიონულ გ-ს, ნაყოფის გ-ს (ნაყოფი) - HbF და ზრდასრულ გ-ს - HbA. ნაყოფის უჯრედებში ჟანგბადისადმი მიდრეკილება უფრო მაღალია, ვიდრე მოზრდილებში, რასაც აქვს მნიშვნელოვანი ფიზიოლოგიური მნიშვნელობა და უზრუნველყოფს ნაყოფის ორგანიზმის უფრო მეტ წინააღმდეგობას O2 დეფიციტის მიმართ. სისხლში გ.-ის ოდენობის განსაზღვრა მნიშვნელოვანია ნორმალურ პირობებში სისხლის რესპირატორული ფუნქციის დასახასიათებლად და მრავალფეროვანი დაავადებების, განსაკუთრებით სისხლის დაავადებების დროს. გ-ის რაოდენობა განისაზღვრება სპეციალური მოწყობილობებით - ჰემომეტრებით.
ზოგიერთი დაავადების, აგრეთვე სისხლის თანდაყოლილი ანომალიების დროს (იხ. ჰემოგლობინოპათიები ერითროციტებში ჩნდება პათოლოგიური (პათოლოგიური) სისხლის უჯრედები, რომლებიც განსხვავდება ნორმალურისგან ამინომჟავის ნარჩენების ჩანაცვლებით ( - ან ბ- ჯაჭვები. გამოვლენილია პათოლოგიური გ.-ის 50-ზე მეტი სახეობა, ამრიგად, ნამგლისებრუჯრედოვანი ანემიის დროს აღმოჩნდა გ ბ- ჯაჭვები, რომელთა გლუტამინის მჟავა, რომელიც მდებარეობს N-ბოლოდან მე-6 ადგილზე, შეიცვალა ვალინით. სისხლის წითელი უჯრედების ანომალიები ასოცირდება ჰემოგლობინის F ან H შემცველობასთან თალასემია , მეტემოგლობინემია . ზოგიერთი პათოლოგიური კუჭ-ნაწლავის ტრაქტის რესპირატორული ფუნქცია მკვეთრად დაქვეითებულია, რაც იწვევს სხვადასხვა პათოლოგიურ მდგომარეობას ( ანემია და ა.შ.). გ-ის თვისებები შეიძლება შეიცვალოს სხეულის მოწამვლისას, მაგალითად, ნახშირბადის მონოქსიდით, რომელიც იწვევს წარმოქმნას. კარბოქსიჰემოგლობინი , ან შხამები, რომლებიც გარდაქმნის Fe 2+ ჰემს Fe 3+-ად მეტემოგლობინის წარმოქმნით. ამ G. წარმოებულებს არ შეუძლიათ ჟანგბადის გადატანა. G. სხვადასხვა ცხოველებს აქვთ სახეობრივი სპეციფიკა, მოლეკულის ცილოვანი ნაწილის უნიკალური სტრუქტურის გამო. ფორმირების წყაროა სისხლის წითელი უჯრედების განადგურების დროს გამოთავისუფლებული გ ნაღვლის პიგმენტები.
კუნთოვანი ქსოვილი შეიცავს კუნთს G. - მიოგლობინი , მოლური მასის, შემადგენლობისა და თვისებების მიხედვით ახლოსაა გ.ქვეერთეულებთან (მონომერები). გ.-ს ანალოგები აღმოჩენილია ზოგიერთ მცენარეში (მაგ. ლეგემოგლობინი გვხვდება პარკოსან კვანძებში).
ნათ.: Korzhuev P. A., ჰემოგლობინი, მ., 1964; Gaurowitz F., ქიმია და ცილების ფუნქციები, ტრანს. ინგლისურიდან, 2nd ed., M., 1965, გვ. 303-23; ინგრამ ვ., მაკრომოლეკულების ბიოსინთეზი, ტრანს. ინგლისურიდან, მ., 1966, გვ. 188-97; Rapoport S. M., სამედიცინო ბიოქიმია, თარგმანი. გერმანულიდან, მ., 1966; Perutz M., Hemoglobin molecule, კრებულში: Molecules and Cell, M., 1966; ცუკერკანდლ ე. ჰემოგლობინის ევოლუცია, იქვე; Fanelli A. R., Antonini E., Caputo A., Hemoglobin and myoglobin, “Advances in Protein Chemistry”, 1964, ვ. 19, გვ. 73-222; Antonini E., Brunori M., Hemoglobin, “Annual Review of Biochemistry”, 1970, ვ. 39, გვ. 977-1042 წწ.
G. V. Andreenko, S. E. Severin.
გამოთვალეთ ერთი ჰემოგლობინის მოლეკულის მასა: გრამებში და ატომური მასის ერთეულებში.
გამოთვალეთ ერთი ჰემოგლობინის მოლეკულის მასა (მოლეკულური ფორმულა C 2954 H 4516 N 780 O 806 S 12 Fe 4):
ა) გრამებში; ბ) ატომური მასის ერთეულებში.
მოდით დავწეროთ პრობლემის მოკლე განცხადება და მისი გადასაჭრელად საჭირო დამატებითი მონაცემები.
ა) ჰემოგლობინის მოლეკულის მასის გამოსათვლელად, თქვენ უნდა იცოდეთ მისი მოლური მასა:
M (ჰემოგლობინი) = 2954·12 + 4516·1 + 780·14 + + 806·16 + 12·32 + 4·56 =( გ/მოლ)
შემდგომი მსჯელობა შეიძლება განხორციელდეს ორი გზით.
მეთოდი 1: ნივთიერების რაოდენობით.
ნივთიერების რაოდენობა არის მოსახერხებელი უნივერსალური რაოდენობა, რომელიც საშუალებას გვაძლევს დავაკავშიროთ ატომების ან მოლეკულების რაოდენობა, ნივთიერების მასა და მოცულობა.
სადაც m არის მასა, M არის მოლური მასა, N არის ატომების ან მოლეკულების რაოდენობა, N A = 6.02 10 23 მოლი - 1- ავოგადროს მუდმივი.
ამ ფორმულების გაერთიანებით ჩვენ შეგვიძლია გამოვხატოთ მასა მოლეკულების რაოდენობის მიხედვით:
მიღებული ფორმულის ჩანაცვლება N = 1, M = გ/მოლ, N A = 6.02·10 23 მოლი - 1, ჩვენ ვიპოვეთ
მეთოდი 2: პროპორციების გამოყენება.
ჰემოგლობინის 6,02 10 23 მოლეკულის მასა არის გ;
ხოლო ჰემოგლობინის 1 მოლეკულის მასა არის m გ.
ბ) მოლეკულის აბსოლუტური მასა უდრის ფარდობით მოლეკულურ მასას გამრავლებული 1 ა-ზე. ჭამე.
ფარდობითი მოლეკულური მასა რიცხობრივად უდრის მოლურ მასას.
პასუხი:ჰემოგლობინის ერთი მოლეკულის მასა არის:
ა) 1,07·10 –19 გ; ბ) ა. ჭამე.
პროექტი სტუდენტებისგან სტუდენტებისთვის! უნივერსიტეტში ჩაბარებას 50%-ით ვამარტივებთ. ჩვენ ვზოგავთ დროს სწავლაზე 40%-ით. გაზარდე სიხარული 200%-ით!
ქიმიკოსის სახელმძღვანელო 21
ქიმია და ქიმიური ტექნოლოგია
ჰემოგლობინის მოლეკულური წონა
რკინა ფუნქციონირებს როგორც ელექტრონის პირველადი გადამზიდავი ბიოლოგიურ დაჟანგვა-აღდგენით რეაქციებში. რკინის იონები, როგორც Fe+, ასევე Fe+, იმყოფება ადამიანის სხეულში და მოქმედებენ როგორც ელექტრონის მატარებლები, მუდმივად იცვლება ერთი დაჟანგვის მდგომარეობიდან მეორეში. ეს შეიძლება იყოს ილუსტრირებული ციტოქრომების მაგალითის გამოყენებით. რკინის იონები ასევე ემსახურება მოლეკულური ჟანგბადის ტრანსპორტირებას და შენახვას - ფუნქცია, რომელიც აუცილებელია ყველა ხერხემლიანის სიცოცხლისთვის. ამ სისტემაში მუშაობს მხოლოდ Re(P). მეტაბოლური პროცესების ჟანგბადის მოთხოვნილების დასაკმაყოფილებლად, ცხოველთა უმეტესობას აქვს სითხე, რომელიც ცირკულირებს მთელ სხეულში და გადასცემს ჟანგბადს, შთანთქავს მას გარე წყაროდან, ქსოვილების მიტოქონდრიაში. აქ საჭიროა რესპირატორული ჯაჭვის შუამავლობა ოქსიდაციური ფოსფორილირებისა და ატფ-ის გამომუშავებისთვის. თუმცა, წყალში ჟანგბადის ხსნადობა ძალიან დაბალია ცოცხალ არსებებში სუნთქვის მხარდასაჭერად. ამიტომ, სისხლი ჩვეულებრივ შეიცავს ცილებს, რომლებიც შექცევადად აკავშირებენ ჟანგბადს. ეს ცილის მოლეკულები ხელს უწყობენ ჟანგბადის შეღწევას კუნთებში (ქსოვილებში) და ასევე შეუძლიათ ჟანგბადის შესანახად.
მეორეს მხრივ, TMV-ის მოლეკულური წონა დაახლოებით 40 მილიონი იყო და თავიდან ჩანდა, რომ TMV-ის სტრუქტურის გაგება განუზომლად უფრო რთული იქნებოდა, ვიდრე მიოგლობინისა და ჰემოგლობინის გაცილებით მცირე მოლეკულების სტრუქტურა, რაც ჯონ კენდრიუ. და მაქს პერუცი მრავალი წლის განმავლობაში იბრძოდნენ, მაგრამ არასოდეს მიუღიათ ბიოლოგის ინტერესის შედეგი.
ჰემოგლობინი
ჰემოგლობინი (Hb) (დან ჰემო. და ლათ. გლობუსი - ბურთი), ადამიანის, ხერხემლიანების და ზოგიერთი უხერხემლოების წითელი რკინის შემცველი სისხლის პიგმენტი
ჰემოგლობინის და მისი ნაერთების შთანთქმის სპექტრები: 1 - ჰემოგლობინი; 2 - ოქსიჰემოგლობინი; 3 - კარბოქსიჰემოგლობინი; 4 - მეტემოგლობინი: B, C, D, E, F, G - მზის სპექტრის ფრაუნჰოფერის ძირითადი ხაზები, ტალღების სიგრძე მითითებულია რიცხვებით.
ადამიანის ოქსიჰემოგლობინის დისოციაციის მრუდი.
ჰემოგლობინი
ცილის მოლეკულის ფორმის მიხედვით განასხვავებენ ფიბრილურ და გლობულურ ცილებს, რომლებიც შედგება კომპლექსური ცილებისგან, რომლებიც ამინომჟავების გარდა შეიცავს ნახშირწყლებს, ნუკლეინის მჟავებს და ა.შ. გლობინი და რკინის პორფირინი - ჰემი. მაღალ ცხოველებსა და ადამიანებში სისხლი შედგება 4 მონომერული ქვედანაყოფისგან, რომელთა მოლური მასა დაახლოებით 17000-ია; ორი მონომერი შეიცავს 141 ამინომჟავის ნარჩენებს (?-ჯაჭვი), დანარჩენი ორი - 146 ნარჩენი (?-ჯაჭვი).
ამ პოლიპეპტიდების სივრცითი სტრუქტურები დიდწილად მსგავსია. ისინი ქმნიან დამახასიათებელ „ჰიდროფობიურ ჯიბეებს“, რომლებშიც განლაგებულია ჰემის მოლეკულები (თითოეული ქვეგანყოფილებისთვის). ჰემში შემავალი რკინის ატომის 6 საკოორდინაციო ბმადან 4 მიმართულია პიროლის რგოლების აზოტისკენ; მე-5 დაკავშირებულია ჰისტიდინის იმიდაზოლური რგოლის აზოტთან, რომელიც ეკუთვნის პოლიპეპტიდებს და მდებარეობს α-ჯაჭვში 87-ე და β-ჯაჭვის 92-ე ადგილზე; მე-6 ბმა მიმართულია წყლის მოლეკულაზე ან სხვა ჯგუფებზე (ლიგანდებზე), მათ შორის ჟანგბადზე. ქვედანაყოფები ერთმანეთთან თავისუფლად არის დაკავშირებული წყალბადის, მარილისა და სხვა არაკოვალენტური ბმებით და ადვილად იშლება ამიდების გავლენით და მარილის გაზრდილი კონცენტრაციით, რათა წარმოქმნან ძირითადად სიმეტრიული დიმერები (??) და ნაწილობრივ?- და?- მონომერები. ჰემოგლობინის მოლეკულის სივრცითი სტრუქტურა შეისწავლა რენტგენის დიფრაქციული ანალიზით 1959 წელს ინგლისელმა ბიოქიმიკოსმა მაქს ფერდინანდ პერუცმა.
ამინომჟავების განლაგების თანმიმდევრობა ჰემოგლობინის α- და β-ჯაჭვებში უმაღლეს ცხოველებში და ადამიანებში სრულად არის განმარტებული. ჰემის მოლეკულაში, რომელიც აწყობილია ტეტრამერში, ჰემის ოთხივე ნარჩენი განლაგებულია ზედაპირზე და O 2-თან რეაქციები ადვილად ხელმისაწვდომია. O 2-ის დამატება უზრუნველყოფილია ჰემში Fe 2+ ატომის შემცველობით. ეს რეაქცია შექცევადია და დამოკიდებულია O 2-ის ნაწილობრივ წნევაზე (დაძაბულობაზე). კაპილარებში კაპილარები არის ყველაზე პატარა გემები, რომლებიც შეაღწევენ ორგანოებსა და ქსოვილებში. ისინი აკავშირებენ არტერიოლებს ვენულებთან (ყველაზე პატარა ვენებთან) და ხურავენ სისხლის მიმოქცევას; მათი კედლების მეშვეობით ხდება ნივთიერებების გაცვლა სისხლსა და ქსოვილებს შორის (სისხლის კაპილარები). ლიმფური კაპილარები ქმნიან ლიმფურ გემებს, ხელს უწყობენ ქსოვილებიდან სითხის გადინებას და ორგანიზმიდან უცხო ნაწილაკებს და პათოგენურ ბაქტერიებს აშორებენ. ფილტვებში, სადაც O 2 დაძაბულობა არის დაახლოებით 100 მმ Hg. Art., G. აერთიანებს O 2-ს (ჟანგბადის პროცესი Oxygenation - გაჯერება ჟანგბადით.), გარდაიქმნება ჟანგბადიან G. - oxygenated ჰემოგლობინში. ქსოვილის კაპილარებში, სადაც O 2 დაძაბულობა გაცილებით დაბალია (დაახლოებით 40 მმ Hg), ოქსიჰემოგლობინი იშლება ჰემოგლობინად და ჟანგბად O 2; ეს უკანასკნელი შედის ორგანოებისა და ქსოვილების უჯრედებში, სადაც O 2-ის ნაწილობრივი წნევა კიდევ უფრო დაბალია (5-20 მმ Hg); უჯრედების სიღრმეში ის თითქმის ნულამდე ეცემა. O 2-ის დამატება ჰემოგლობინში და ოქსიჰემოგლობინის დისოციაცია ჰემოგლობინში და O 2 თან ახლავს ჰემოგლობინის მოლეკულის კონფორმაციულ (სივრცულ) ცვლილებებს, აგრეთვე მის შექცევად დაშლას დიმერებად და მონომერებად, რასაც მოჰყვება აგრეგაცია ტეტრამერებად.
ჰემოგლობინის სხვა თვისებები ასევე იცვლება ჟანგბადთან O 2-თან ურთიერთობისას: ჟანგბადით გაჯერებული ჰემოგლობინი 70-ჯერ უფრო ძლიერი მჟავაა, ვიდრე ჰემოგლობინი. დამახასიათებელი შთანთქმის ზოლები არის სპექტრის ხილულ ნაწილში: გეოგლობინს აქვს ერთი მაქსიმუმი (554 მმკკ-ზე), ხოლო ჟანგბადით გაჯერებულ გაზს აქვს ორი მაქსიმუმი 578 და 540 მმკ-ზე. G. შეუძლია პირდაპირ დაამატოთ ნახშირორჟანგი (ნახშირორჟანგი) CO 2 (CO 2-ის რეაქციის შედეგად NH2- გლობინის ჯგუფებთან); ამ შემთხვევაში წარმოიქმნება კარბჰემოგლობინი - არასტაბილური ნაერთი, რომელიც ადვილად იშლება ფილტვების კაპილარებში ჰემოგლობინში და CO 2-ში.
ბრინჯი. 1. ჰემოგლობინის და მისი ნაერთების შთანთქმის სპექტრები: 1 - ჰემოგლობინი; 2 - ოქსიჰემოგლობინი; 3 - კარბოქსიჰემოგლობინი; 4 - მეტემოგლობინი: B, C, D, E, F, G - მზის სპექტრის ფრაუნჰოფერის ძირითადი ხაზები, ტალღების სიგრძე მითითებულია რიცხვებით.
ადამიანის სისხლში ჰემოგლობინის რაოდენობა საშუალოდ არის % (ანუ 78% - 96% სალის მიხედვით); ქალებში გ. ოდნავ ნაკლებია, ვიდრე მამაკაცებში. გ.-ის თვისებები იცვლება ონტოგენეზის დროს. ამიტომ განასხვავებენ ემბრიონულ გ-ს, ნაყოფის გ-ს (ნაყოფი) - HbF და ზრდასრულ გ-ს - HbA. ნაყოფის უჯრედებში ჟანგბადისადმი მიდრეკილება უფრო მაღალია, ვიდრე მოზრდილებში, რომელსაც აქვს მნიშვნელოვანი ფიზიოლოგიური ფიზიოლოგიური, ფიზიოლოგიური მდგომარეობა - ე.ი. ერთი, რომელშიც არ არის გადახრები სისტემებისა და ორგანოების ნორმალური ფუნქციონირებისგან. მნიშვნელობა აქვს და უზრუნველყოფს ნაყოფის სხეულის უფრო მეტ წინააღმდეგობას O 2 დეფიციტის მიმართ. სისხლში გ.-ის ოდენობის განსაზღვრა მნიშვნელოვანია ნორმალურ პირობებში სისხლის რესპირატორული ფუნქციის დასახასიათებლად და მრავალფეროვანი დაავადებების, განსაკუთრებით სისხლის დაავადებების დროს. გ-ის რაოდენობა განისაზღვრება სპეციალური მოწყობილობებით - ჰემომეტრებით.
ზოგიერთი დაავადების, ასევე თანდაყოლილი ანომალიების დროს ანომალია არის სხეულის სტრუქტურული ან ფუნქციური დარღვევა, რომელიც გამოწვეულია ემბრიონის განვითარების დარღვევით. მკვეთრად გამოხატულ ანომალიებს მალფორმაციები ან დეფორმაციები ეწოდება. სისხლის წითელ უჯრედებში სისხლი ჩნდება პათოლოგიური (პათოლოგიური) G., რომელიც განსხვავდება ნორმალურისგან ამინომჟავის ნარჩენების ჩანაცვლებით (- ან?-ჯაჭვებში. გამოვლენილია პათოლოგიური გ.-ის 50-ზე მეტი სახეობა. ამრიგად, ნამგლისებრუჯრედოვანი ანემია, რომლის β-ჯაჭვებში აღმოჩენილია გლუტამინის მჟავა, რომელიც დგას N-ბოლოდან მე-6 ადგილზე, ჩანაცვლებული ერითროციტების ანომალიებით, რომლებიც დაკავშირებულია ჰემოგლობინის F ან H შემცველობასთან თალასემია (ბერძნულიდან th?lassa - ზღვა და h?ima - სისხლი) არის ხმელთაშუა ზღვის დაავადება, მემკვიდრეობითი ჰემოლიზური ანემია, რომელიც პირველად გამოვლინდა (1925) ხმელთაშუა ზღვის რეგიონებში, გამოწვეულია ჰემოგლობინის სინთეზის დარღვევით. ზოგიერთი პათოლოგიური ჰემოგლობინის რესპირატორული ფუნქცია ძლიერ დარღვეულია, რაც იწვევს სხვადასხვა პათოლოგიურ მდგომარეობას (ანემია და ა.შ.), როდესაც ორგანიზმი მოწამლულია , ან შხამები, რომლებიც გარდაქმნის Fe 2+ ჰემს Fe 3+-ად მეტემოგლობინის წარმოქმნით. ამ G. წარმოებულებს არ შეუძლიათ ჟანგბადის გადატანა. G. სხვადასხვა ცხოველებს აქვთ სახეობრივი სპეციფიკა, მოლეკულის ცილოვანი ნაწილის უნიკალური სტრუქტურის გამო. სისხლის წითელი უჯრედების განადგურების დროს გამოთავისუფლებული გ. ნაღვლის პიგმენტების წარმოქმნის წყაროა.
კუნთოვანი ქსოვილი შეიცავს კუნთების ჰემოგლობინს - მიოგლობინი მიოგლობინი არის გლობულური ცილა, რომელიც ინახავს ჟანგბადს კუნთებში. , მოლური მასის, შემადგენლობისა და თვისებების მიხედვით ახლოსაა გ.ქვეერთეულებთან (მონომერები). გ-ის ანალოგები აღმოჩენილია ზოგიერთ მცენარეში (მაგალითად, ლეგჰემოგლობინი გვხვდება პარკოსან კვანძებში).
ბრინჯი. 2. ადამიანის ოქსიჰემოგლობინის დისოციაციის მრუდი.
ჰემოგლობინის შესახებ დამატებითი დეტალების შესწავლა შესაძლებელია ლიტერატურაში: Korzhuev P. A., Hemoglobin, M., 1964; Gaurowitz F., ქიმია და ცილების ფუნქციები, ტრანს. ინგლისურიდან, 2nd ed., M., 1965, გვ. 303 - 23; ინგრამ ვ., მაკრომოლეკულების ბიოსინთეზი, ტრანს. ინგლისურიდან, მ., 1966, გვ. 188 - 97; Rapoport S. M., სამედიცინო ბიოქიმია, თარგმანი. გერმანულიდან, მ., 1966; Perutz M., Hemoglobin molecule, კრებულში: Molecules and Cell, M., 1966; ცუკერკანდლ ე. ევოლუცია ევოლუცია (ბიოლოგიაში) არის ცოცხალი ბუნების შეუქცევადი ისტორიული განვითარება. განისაზღვრება ორგანიზმების ცვალებადობით, მემკვიდრეობითობით და ბუნებრივი გადარჩევით. მას თან ახლავს მათი ადაპტაცია არსებობის პირობებთან, სახეობათა ჩამოყალიბება და გადაშენება, ბიოგეოცენოზისა და მთლიანად ბიოსფეროს ტრანსფორმაცია. ჰემოგლობინი, იქვე; Fanelli A. R., Antonini E., Caputo A., Hemoglobin and myoglobin, “Advances in Protein Chemistry”, 1964, ვ. 19, გვ. 73 - 222; Antonini E., Brunori M., Hemoglobin, “Annual Review of Biochemistry”, 1970, ვ. 39, გვ. 977 - 1042. (G. V. Andreenko, S. E. Severin)
იპოვე სხვა საინტერესო:
- ინფორმაციის გამოყენებამდე გაიარეთ კონსულტაცია ექიმთან! მარკ ტვენი: ფრთხილად იყავით ჯანმრთელობის შესახებ წიგნების კითხვისას. შეიძლება მოკვდე ბეჭდვითი შეცდომით.
კომენტარები სტატიაზე
სისხლის შემადგენლობის გასაუმჯობესებლად და ჰემოგლობინის ასამაღლებლად მოამზადეთ ეს ფაფა.
შეურიეთ 1 ჭიქა წიწიბურა და 1 ჭიქა კეფირი და გააჩერეთ 12 საათი. დაამატეთ თაფლი გემოვნებით.
მიირთვით ეს ფაფა საუზმეზე ან საღამოს. სხვა მარცვლეულებთან შედარებით, წიწიბურა შეიცავს ცოტა ნახშირწყლებს, ამიტომ ძალიან სასარგებლოა ჭარბწონიანთა და დიაბეტით დაავადებულთათვის.
ჰემოგლობინის ასამაღლებლად: 300გრ უმი სტაფილო და ჭარხალი გახეხეთ მსხვილ სახეხზე, დაუმატეთ 300გრ თაფლი. აურიეთ და შედგით მაცივარში.
მიიღეთ 1 ს.კ. 1-ჯერ დღეში, დილით უზმოზე 30 წუთის განმავლობაში. ჭამის წინ.
ერთ კვირაში ჰემოგლობინი ნორმალურად გაიზრდება (შეიძლება გაორმაგდეს!).
როგორ გავზარდოთ ჰემოგლობინი ხორცის გარეშე
ჰემოგლობინის დონე ასევე შეიძლება გაიზარდოს შემდეგი პროდუქტებით:
ქატო, ხორბლის ფაფა, გარგარი, გარგრის ჩირი, შავი შოკოლადი, მწვანე ვაშლი, მარცვლეულის პური, წითელი ყურძენი, ჭარხალი, პარკოსნები, ნუში, ბროწეული, ქლიავის წვენი, ქლიავი, ქიშმიში, ბარდა, ტომატის წვენი, ბრიუსელის კომბოსტო, ბროკოლი, არაქისის კარაქი, შვრიის ფაფა, ანანასი (ახალი და დაკონსერვებული).
ყველა ეს საკვები მდიდარია რკინით, რომელიც ზრდის ჰემოგლობინს. და ჩამოთვლილი პროდუქტებიდან ბევრი რკინის შემცველობით შედარებულია ხორცთან.
ჰემოგლობინის გაზრდის სპეციალური რეცეპტები
ქვემოთ მოყვანილი რეცეპტებიდან აირჩიეთ ის, რაც ყველაზე მეტად მოგწონთ და შეეცადეთ გამოიყენოთ იგი მუდმივად, როგორც „ვიტამინური დანამატი“ ორგანიზმისთვის.
1) გახეხეთ ერთი ჭიქა ნიგოზი და ერთი ჭიქა უმი წიწიბურა, დაუმატეთ ერთი ჭიქა თაფლი, ყველაფერი აურიეთ, მიირთვით თითო სუფრის კოვზი ყოველდღე.
2) ნიგოზი, გარგრის ჩირი, თაფლი, ქიშმიში - ყველაფერი 1:1 თანაფარდობით - დაფქვით და კარგად აურიეთ, მიირთვით 1-3 სუფრის კოვზი დღეში (ერთ-ერთი საუკეთესო რეცეპტი არა მხოლოდ ჰემოგლობინის ასამაღლებლად, არამედ ორგანიზმის მიწოდებისთვის. საჭირო ვიტამინები).
3) გახეხეთ 1 ჭიქა ქლიავი, გარგარი ჩირი, ნიგოზი, ქიშმიში, დაუმატეთ თაფლი, დაუმატეთ 1-2 ლიმონი კანით (ლიმონის ნაცვლად შეიძლება ალოეს წვენი დაუმატოთ), მიირთვით დღეში 1-3 სუფრის კოვზი.
4) 100 მლ ახლად გამოწურული ჭარხლის წვენი, 100 მლ სტაფილოს წვენი, აურიეთ და დალიეთ (ამაღლებს ჰემოგლობინს ფაქტიურად 2 დღეში).
5) 1/2 ჭიქა ვაშლის წვენი, 1/4 ჭიქა ჭარხლის წვენი და 1/4 ჭიქა სტაფილოს წვენი, აურიეთ და დალიეთ 1-2-ჯერ დღეში.
6) 1/2 ჭიქა ახლად გამოწურული ვაშლის წვენი, 1/2 ჭიქა ხელნაკეთი მოცვის წვენი, 1 სუფრის კოვზი ახლად გამოწურული ჭარხლის წვენი, აურიეთ და დალიეთ.
7) ნედლი წიწიბურა 1/2 ჭიქა, გარეცხეთ, დაასხით 1 ჭიქა კეფირი და დატოვეთ ღამით, დილით ფაფა მზად არის, შეგიძლიათ მიირთვათ.
8) 1/2 ჭიქა მშრალი წითელი ღვინო კარგი ხარისხისაორთქლებულია წყლის აბაზანაში 5-7 წუთის განმავლობაში; 1/4 ჭიქა მოხარშული ჭინჭარი, 1 სუფრის კოვზი გამდნარი კარაქი, დალიეთ თბილი.
ჰემოგლობინის მოლური მასა
ჰემოგლობინი, Hb ( ჰემოგლობინი; ბერძენი ჰაიმა სისხლი + ლათ. globus ball), არის ჰემოპროტეინი, რთული ცილა, რომელიც მიეკუთვნება ჰემის შემცველ ქრომოპროტეინებს; ახორციელებს ჟანგბადის გადატანას ფილტვებიდან ქსოვილებში და მონაწილეობს ნახშირორჟანგის ქსოვილებიდან სასუნთქ ორგანოებში გადატანაში. გ. გვხვდება ყველა ხერხემლიანი და ზოგიერთი უხერხემლო ცხოველის (ჭიები, მოლუსკები, ფეხსახსრიანები, ექინოდერმები) ერითროციტებში, აგრეთვე ზოგიერთი პარკოსანთა ფესვის კვანძებში. მოლ. ადამიანის სისხლის წითელი უჯრედების წონა (მასა) უდრის; ერთი ერითროციტი შეიცავს დაახლ. G. G.-ის 400 მილიონი მოლეკულა ძალიან ხსნადია წყალში, უხსნადი ალკოჰოლში, ქლოროფორმში და ეთერში და კარგად კრისტალიზდება (გ. კრისტალების ფორმა განსხვავდება ცხოველიდან ცხოველამდე).
გ-ის შემადგენლობაში შედის მარტივი ცილა - გლობინი და რკინის შემცველი პროთეზირების (არაცილოვანი) ჯგუფი - ჰემი (შესაბამისად, მოლეკულის წონით 96 და 4%). 2.0-ზე დაბალ pH-ზე ჰემის მოლეკულა იყოფა ჰემად და გლობინად.
ჰემე (C 34 H 32 O 4 N 4) არის რკინის პროტოპორფირინი - პროტოპორფირინ IX-ის რთული ნაერთი ორვალენტიანი რკინით. რკინა განლაგებულია პროტოპორფირინის ბირთვის ცენტრში და დაკავშირებულია პიროლის ბირთვების ოთხ აზოტის ატომთან (ნახ. 1): ორი საკოორდინაციო ბმა და ორი წყალბადის შემცვლელი ბმა.
ვინაიდან რკინის საკოორდინაციო რიცხვია 6, ორი ვალენტობა რჩება გამოუყენებელი, ერთი მათგანი რეალიზდება, როდესაც ჰემი უკავშირდება გლობინს, ხოლო მეორეს უერთდება ჟანგბადი ან სხვა ლიგანდები - CO, F +, აზიდები, წყალი (ნახ. 2). და ა.შ.
პროტოპორფინ IX-ის კომპლექსს Fe 3+-თან ერთად ჰემატინი ეწოდება. ჰემატინის მარილმჟავას მარილი (ქლორემინი, ჰემინი) ადვილად გამოიყოფა შიგნით. კრისტალური ფორმა (ე.წ. Teichmann კრისტალები). ჰემს აქვს უნარი შექმნას რთული ნაერთები აზოტოვან ნაერთებთან (ამიაკი, პირიდინი, ჰიდრაზინი, ამინები, ამინომჟავები, ცილები და ა.შ.), რითაც გადაიქცევა ჰემოქრომოგენებად (იხ.). ვინაიდან ჰემი ყველა ცხოველურ სახეობაში ერთნაირია, ჰემოგლობინის თვისებებში განსხვავებები განპირობებულია ჰემოგლობინის მოლეკულის ცილოვანი ნაწილის - გლობინის სტრუქტურული მახასიათებლებით.
გლობინი
გლობინი არის ალბუმინის ტიპის ცილა, რომელიც შეიცავს ოთხ პოლიპეპტიდურ ჯაჭვს თავის მოლეკულაში: ორი ალფა ჯაჭვი (თითოეული შეიცავს 141 ამინომჟავის ნარჩენს) და ორი ბეტა ჯაჭვი, რომელიც შეიცავს 146 ამინომჟავის ნარჩენებს. ამრიგად, G. მოლეკულის ცილოვანი კომპონენტი აგებულია სხვადასხვა ამინომჟავების 574 ნარჩენებისგან. პირველადი სტრუქტურა, ანუ ამინომჟავების გენეტიკურად განსაზღვრული თანმიმდევრობა გლობინის პოლიპეპტიდურ ჯაჭვებში ადამიანებში და რიგ ცხოველებში, სრულად არის შესწავლილი. ადამიანის გლობინის გამორჩეული თვისებაა მის შემადგენლობაში ამინომჟავების იზოლეიცინის და ცისტინის არარსებობა. N-ტერმინალური ნარჩენები ალფა და ბეტა ჯაჭვებში არის ვალინის ნარჩენები. ალფა ჯაჭვების C-ტერმინალური ნარჩენები წარმოდგენილია არგინინის ნარჩენებით, ხოლო ბეტა ჯაჭვები წარმოდგენილია ჰისტიდინის ნარჩენებით. თითოეულ ჯაჭვში ბოლო პოზიცია უკავია ტიროზინის ნარჩენებს.
კრისტალების რენტგენის სტრუქტურულმა ანალიზმა შესაძლებელი გახადა მისი მოლეკულის სივრცითი სტრუქტურის ძირითადი მახასიათებლების იდენტიფიცირება [M. აღმოჩნდა, რომ ალფა და ბეტა ჯაჭვები შეიცავს სხვადასხვა სიგრძის ხვეული სეგმენტებს, რომლებიც აგებულია ალფა სპირალის პრინციპით (მეორადი სტრუქტურა); ალფა ჯაჭვს აქვს 7, ხოლო ბეტა ჯაჭვს აქვს 8 ხვეული სეგმენტი, რომლებიც დაკავშირებულია არასპირალური სექციებით. ხვეული სეგმენტები, დაწყებული N-ბოლოდან, აღინიშნება ლათინური ანბანის ასოებით (A, B, C, D, E, F, G, H), ხოლო ხვეულების ბრუნვის არასპირალისებურ მონაკვეთებს ან კუთხეებს აქვთ შესაბამისი აღნიშვნა (AB, BC, CD, DE და ა.შ.). გლობინის ჯაჭვის ამინის (N) ან კარბოქსილის (C) ბოლოში არასპირალური რეგიონები აღინიშნება NA ან HC, შესაბამისად. ამინომჟავების ნარჩენები დანომრილია თითოეულ სეგმენტში და გარდა ამისა, ამ ნარჩენის ნუმერაცია ჯაჭვის N-ბოლოდან მოცემულია ფრჩხილებში.
სპირალური და არასპირალური სექციები სივრცეში განლაგებულია გარკვეულწილად, რაც განსაზღვრავს მესამეული სტრუქტურაგლობინის ჯაჭვები. ეს უკანასკნელი თითქმის იდენტურია გ-ის ალფა და ბეტა ჯაჭვებში, მიუხედავად მათი პირველადი სტრუქტურის მნიშვნელოვანი განსხვავებებისა. ეს გამოწვეულია ამინომჟავების პოლარული და ჰიდროფობიური ჯგუფების სპეციფიკური განლაგებით, რაც იწვევს არაპოლარული ჯგუფების დაგროვებას გლობულის შიდა ნაწილში ჰიდროფობიური ბირთვის წარმოქმნით. ცილის პოლარული ჯგუფები აწყდებიან წყლის გარემოს და მასთან კონტაქტში არიან. თითოეული გლობინის ჯაჭვის შიგნით, ზედაპირის მახლობლად, არის ჰიდროფობიური ღრუ ("ჰემის ჯიბე"), რომელშიც ჰემი მდებარეობს, ისეა ორიენტირებული, რომ მისი არაპოლარული შემცვლელები მიმართულია მოლეკულის შიგნიდან და ხდება ჰიდროფობიური ბირთვის ნაწილი. შედეგი არის დაახლ. 60 არაპოლარული კონტაქტი ჰემს და გლობინს შორის და ჰემის ერთი ან ორი პოლარული (იონური) კონტაქტი ალფა და ბეტა ჯაჭვებთან, რომლებიც მოიცავს ჰემის პროპიონის მჟავას ნარჩენებს, რომლებიც გამოდიან ჰიდროფობიური „ჯიბიდან“. ჰემის მდებარეობა გლობინის ჰიდროფობიურ ღრუში იძლევა ჟანგბადის შექცევად დამატების შესაძლებლობას ჰემის Fe 2+-ში ამ უკანასკნელის Fe 3+-მდე დაჟანგვის გარეშე და დამახასიათებელია ცხოველთა სხვადასხვა სახეობის ჰემოგლობინებისთვის. ამას ადასტურებს გ-ის უკიდურესი მგრძნობელობა ჰემის მახლობლად არაპოლარული კონტაქტების ნებისმიერი ცვლილების მიმართ. ამრიგად, ჰემატოფირინში ჰემატოფირინით ჰემატოპორფირინით ჩანაცვლება იწვევს ჰემის თვისებების მკვეთრ დარღვევას.
ჰიდროფობიურ ღრუში ჰემის მიმდებარე ზოგიერთი ამინომჟავის ნარჩენები შედის უცვლელ ამინომჟავებს შორის, ე. დიდი მნიშვნელობაგამოყოფილია სამი: ჰისტიდინის ნარჩენები, ე.წ. პროქსიმალური ჰისტიდინები (87-ე პოზიცია a- და 92-ე პოზიცია P-ჯაჭვებში), დისტალური ჰისტიდინები (58-ე პოზიცია a- და 63-ე პოზიციაზე (5-ჯაჭვებში), ასევე ვალინის ნარჩენი E-11 (62-ე პოზიცია ალფაში ჯაჭვი და 67-ე პოზიცია ბეტა ჯაჭვში).
კავშირი ე.წ პროქსიმალური ჰისტიდინი და ჰემის რკინა ერთადერთი ქიმიური ნივთიერებაა. მათ შორის კავშირი (რეალიზებულია ჰემის Fe 2+ ატომის მეხუთე საკოორდინაციო ბმა) და პირდაპირ გავლენას ახდენს ჰემში ჟანგბადის დამატებაზე. "დისტალური" ჰისტიდინი პირდაპირ არ არის დაკავშირებული ჰემთან და არ მონაწილეობს ჟანგბადის ფიქსაციაში. მისი მნიშვნელობა არის Fe 2+ ატომის სტაბილიზაცია შეუქცევადი დაჟანგვის წინააღმდეგ (როგორც ჩანს, წყალბადის ბმის წარმოქმნის გამო ჟანგბადსა და აზოტს შორის). ვალინის ნარჩენი (E-11) არის ჰემების ჟანგბადის დამატების სიჩქარის ერთგვარი რეგულატორი: ბეტა ჯაჭვებში ის სტერილურად არის განლაგებული ისე, რომ იკავებს ადგილს, სადაც ჟანგბადი უნდა შეერთდეს, რის შედეგადაც ჟანგბადი იწყება ფლაკონის ჯაჭვებით. .
ცილოვანი ნაწილი და მოლეკულის პროთეზირების ჯგუფი ერთმანეთზე ძლიერ გავლენას ახდენს. გლობინი ცვლის ჰემის ბევრ თვისებას, აძლევს მას ჟანგბადის შებოჭვის უნარს. ჰემი უზრუნველყოფს გლობინის წინააღმდეგობას მოქმედება, გათბობა, მონელება ფერმენტებით და განსაზღვრავს გ-ის კრისტალიზაციის თვისებების მახასიათებლებს.
პოლიპეპტიდური ჯაჭვები მათზე დამაგრებული ჰემის მოლეკულებით ქმნიან ოთხ ძირითად ნაწილს - ჰემის მოლეკულის ქვეერთეულებს ერთმანეთთან დაკავშირების (დაყრის) ბუნება და მათი მდებარეობა სივრცეში განისაზღვრება ჰემის მეოთხეული სტრუქტურის მახასიათებლებით: a- და. P- ჯაჭვები განლაგებულია ტეტრაედრის კუთხეებში სიმეტრიის ღერძის გარშემო, უფრო მეტიც, ალფა ჯაჭვები დევს p-ჯაჭვების თავზე და თითქოს მათ შორისაა ჩაჭიმული და ოთხივე ჰემი ერთმანეთისგან შორს არის (ნახ. 3). მთლიანობაში, წარმოიქმნება ტეტრამერული სფეროიდური ნაწილაკი, რომლის ზომებია 6,4 X 5,5 X 5,0 ნმ. მეოთხეული სტრუქტურა სტაბილიზირებულია მარილის ბმებით α-α და β-β ჯაჭვებს შორის და ორი ტიპის კონტაქტებით α და β ჯაჭვებს შორის (α1-β1 და α2-β2). α1-β1 კონტაქტები ყველაზე ფართოა, მოიცავს 34 ამინომჟავის ნარჩენს და ურთიერთქმედების უმეტესობა არაპოლარულია. α1-β2 კონტაქტი შედგება 19 ამინომჟავის ნარჩენებისგან, ბმების უმეტესობა ასევე არაპოლარულია, წყალბადის რამდენიმე ბმის გამოკლებით. ამ კონტაქტში მდებარე ყველა ნარჩენი ერთნაირია ყველა შესწავლილ ცხოველურ სახეობაში, ხოლო α1-β1 კონტაქტებში ნარჩენების 1/3 განსხვავდება.
ადამიანის ჯირკვალი ჰეტეროგენულია, რაც განპირობებულია მის შემადგენლობაში შემავალი პოლიპეპტიდური ჯაჭვების სხვაობით. ამრიგად, ზრდასრული ადამიანის სისხლში გლუკოზა, რომელიც შეადგენს სისხლში გლუკოზის (HbA) 95-98%-ს, შეიცავს ორ α- და ორ β-ჯაჭვს; G.-ის მცირე ფრაქცია (HbA2), რომელიც აღწევს მაქსიმალურ შემცველობას 2,0-2,5%, შეიცავს ორ α- და ორ σ-ჯაჭვს; ნაყოფის ჰემოგლობინი (HbF), ან ნაყოფის ჰემოგლობინი, რომელიც შეადგენს 0,1-2%-ს ზრდასრული ადამიანის სისხლში, შედგება ორი α- და ორი γ-ჯაჭვისგან.
ნაყოფის G. იცვლება HbA-ით დაბადებიდან პირველ თვეებში. ახასიათებს მნიშვნელოვანი წინააღმდეგობა თერმული დენატურაციის მიმართ, რასაც ეფუძნება სისხლში მისი შემცველობის განსაზღვრის მეთოდები.
პოლიპეპტიდური ჯაჭვების შემადგენლობიდან გამომდინარე, G.-ის ჩამოთვლილი ტიპები შემდეგია: HbA - როგორც Hbα2β2, HbA2 - როგორც Hbα2σ2 და HbF - როგორც Hbα2γ. თანდაყოლილი ანომალიებითა და ჰემატოპოეტური აპარატის დაავადებებით ჩნდება ჰემატოპოეზის პათოლოგიური ტიპები, მაგალითად, ნამგლისებრუჯრედოვანი ანემიით (იხ.), თალასემიით (იხ.), არაფერმენტული წარმოშობის თანდაყოლილი მეტემოგლობინემიით (იხ. მეტემოგლობინემია) და ა.შ. ყველაზე გავრცელებული ჩანაცვლება. ერთი ამინომჟავა ერთ წყვილ პოლიპეპტიდურ ჯაჭვში.
ჰემის რკინის ატომის ვალენტურობიდან და ჰემის მოლეკულაში ლიგანდის ტიპებიდან გამომდინარე, ეს უკანასკნელი შეიძლება იყოს რამდენიმე ფორმით. შემცირებულ წყალბადს (დეოქსი-Hb) აქვს Fe 2+ თავისუფალი მეექვსე ვალენტობით, როდესაც მას ემატება O 2, წარმოიქმნება წყალბადის ჟანგბადიანი ფორმა (HbO 2). როდესაც HbO 2 ექვემდებარება უამრავ ჟანგვის აგენტს (კალიუმის ფერიციანიდი, ნიტრიტები, ქინონები და ა. გარემოს pH მნიშვნელობიდან გამომდინარე, არსებობს მეტემოგლობინის მჟავე და ტუტე ფორმები, რომლებიც შეიცავს H 2 O ან OH ჯგუფს, როგორც მეექვსე ლიგანდს. ჯანმრთელი ადამიანების სისხლში მეტემოგლობინის კონცენტრაცია არის 0,83+0,42%.
მეტემოგლობინს აქვს უნარი მყარად შეაერთოს წყალბადის ფტორი, ჰიდროციანმჟავა და სხვა ნივთიერებები. ეს თვისება გამოიყენება თაფლში. ჰიდროციანით მოწამლული ადამიანების გადარჩენის პრაქტიკა. G.-ის სხვადასხვა წარმოებულები განსხვავდება შთანთქმის სპექტრით (ცხრილი).
ტალღის სიგრძე (მაქსიმალური შთანთქმის დროს), ნმ
მილიეკვივალენტური სინათლის შთანთქმის კოეფიციენტი, E
მეტემოგლობინი (met-Hb; pH 7.0-7.4)
ჰემოგლობინის ფუნქციური თვისებები. გაზის მთავარი ბიოლის როლი არის მონაწილეობა გაზის გაცვლაში სხეულსა და გარე გარემოს შორის. G. უზრუნველყოფს სისხლით ჟანგბადის გადატანას ფილტვებიდან ქსოვილებში და ნახშირორჟანგის გადატანას ქსოვილებიდან ფილტვებში (იხ. გაზის გაცვლა). არანაკლებ მნიშვნელოვანია ბუფერული თვისებებიგ., აყალიბებს ძლიერ ჰემოგლობინს და ოქსიჰემოგლობინის ბუფერულ სისტემებს სისხლში, რაც ხელს უწყობს ორგანიზმში მჟავა-ტუტოვანი ბალანსის შენარჩუნებას (იხ. ბუფერული სისტემებიმჟავა-ტუტოვანი ბალანსი).
HbO 2-ის ჟანგბადის მოცულობა არის 1,39 მლ O 2 1 გ HbO 2-ზე. G.-ს ჟანგბადის შებოჭვისა და გამოთავისუფლების უნარი აისახება მისი ჟანგბადის დისოციაციის მრუდით (ODC), რომელიც ახასიათებს G.-ის ჟანგბადით გაჯერების პროცენტს O 2 (pO 2) ნაწილობრივი წნევის მიხედვით.
ჟანგბადის ტეტრამერულ მოლეკულებს აქვთ S- ფორმის CDK, რაც მიუთითებს იმაზე, რომ ჟანგბადი უზრუნველყოფს ჟანგბადის ოპტიმალურ შეკავშირებას ფილტვებში შედარებით დაბალი პარციული წნევის დროს და გამოყოფს ქსოვილებში ჟანგბადის შედარებით მაღალი ნაწილობრივი წნევის დროს (ნახ. 4). ქსოვილებში ჟანგბადის მაქსიმალური მიწოდება შერწყმულია სისხლში მაღალი ნაწილობრივი წნევის შენარჩუნებასთან, რაც უზრუნველყოფს ჟანგბადის ღრმად შეღწევას ქსოვილებში. ჟანგბადის ნაწილობრივი წნევის მნიშვნელობა მმ Hg-ში. ხელოვნება, როდესაც გაზის 50% ჟანგბადია, არის გაზის ჟანგბადისადმი მიდრეკილების საზომი და დასახელებულია P50.
ჟანგბადის დამატება გ-ის ოთხ ჰემს თანმიმდევრულად ხდება. G.-ს CDK-ის S- ფორმის ბუნება მიუთითებს იმაზე, რომ პირველი ჟანგბადის მოლეკულა გაერთიანებულია G.-სთან ძალიან ნელა, ანუ მისი აფინურობა G.-ს მიმართ დაბალია, ვინაიდან აუცილებელია მარილის კონტაქტების გაწყვეტა დეოქსიჰემოგლობინის მოლეკულაში. თუმცა, პირველი ჟანგბადის მოლეკულის დამატება ზრდის მის მიმართ დარჩენილი სამი ჰემის აფინურობას და ჰემის შემდგომი ჟანგბადი გაცილებით სწრაფად ხდება (მეოთხე ჰემის ჟანგბადი 500-ჯერ უფრო სწრაფად ხდება, ვიდრე პირველი). შესაბამისად, ჟანგბადის დამაკავშირებელ ცენტრებს შორის არის თანამშრომლობითი ურთიერთქმედება. ნახშირბადის მონოქსიდის (CO) რეაქციის ნიმუშები იგივეა, რაც ჟანგბადს, მაგრამ ნახშირბადის მონოქსიდის მიდრეკილება CO-ს მიმართ თითქმის 300-ჯერ მეტია, ვიდრე O2-ის მიმართ, რაც ნახშირბადის მონოქსიდს უაღრესად ტოქსიკურს ხდის. ამრიგად, ჰაერში CO კონცენტრაციის ტოლი 0,1%, სისხლის გაზის ნახევარზე მეტი ასოცირდება არა ჟანგბადთან, არამედ ნახშირბადის მონოქსიდთან. ამ შემთხვევაში წარმოიქმნება კარბოქსიჰემოგლობინი, რომელსაც არ შეუძლია ჟანგბადის ტრანსპორტირება.
ჰემოგლობინის ჟანგბადის პროცესის რეგულატორები. ჟანგბადის და დეოქსიგენაციის პროცესებზე დიდ გავლენას ახდენს წყალბადის იონები, ორგანული ფოსფატები, არაორგანული მარილები, ტემპერატურა, ნახშირორჟანგი და სხვა ნივთიერებები, რომლებიც აკონტროლებენ წყალბადის აფინურობას ჟანგბადთან ფიზიოლის შესაბამისად. სხეულის მოთხოვნები. ჟანგბადის ჟანგბადისადმი მიდრეკილების დამოკიდებულებას გარემოს pH მნიშვნელობაზე ეწოდება ბორის ეფექტს (იხ. ვერიგოს ეფექტი). არსებობს "მაწონი" (pH<6) и «щелочной» эффект Бора (pH>6). უდიდესი ფიზიოლი. მთავარია ბორის "ტუტე" ეფექტი. მისი მოლეკულური მექანიზმი განპირობებულია ჰემოგლობინის მოლეკულაში დადებითად დამუხტული ფუნქციური ჯგუფების არსებობით, რომელთა დისოციაციის მუდმივები გაცილებით მაღალია დეოქსიჰემოგლობინში, ჰემოგლობინის მოლეკულის შიგნით მეზობელი ცილოვანი ჯაჭვების უარყოფითად დამუხტულ ჯგუფებს შორის მარილის ხიდების ფორმირების გამო. ოქსიგენაციის დროს ჰემოგლობინის მოლეკულაში მომხდარი კონფორმაციული ცვლილებების გამო, ნადგურდება მარილის ხიდები, იცვლება უარყოფითად დამუხტული ჯგუფების pH და გამოიყოფა ხსნარში. შესაბამისად, ოქსიგენაცია იწვევს პროტონის (H +) გაყოფას აირის მოლეკულიდან და, პირიქით, pH მნიშვნელობის ცვლილება, ანუ გარემოში H + იონების არაპირდაპირი კონცენტრაცია გავლენას ახდენს ჟანგბადის დამატებაზე გაზში. ამრიგად, H + ხდება ლიგანდი, რომელიც უპირატესად აკავშირებს დეოქსიჰემოგლობინს და ამით ამცირებს მის კავშირს ჟანგბადთან, ანუ pH-ის ცვლილება მჟავე მხარეს იწვევს CDC-ის მარჯვნივ გადასვლას. ჟანგბადის პროცესი ენდოთერმულია და ტემპერატურის მატება ხელს უწყობს ჟანგბადის გაყოფას G მოლეკულიდან, შესაბამისად, ორგანოების გაზრდილი აქტივობა და სისხლის ტემპერატურის მატება გამოიწვევს CDC-ის მარჯვნივ გადასვლას და ჟანგბადის მიწოდებას. ქსოვილებში გაიზრდება.
ჟანგბადის პროცესის უნიკალურ რეგულირებას ახორციელებენ ერითროციტებში ლოკალიზებული ორგანული ფოსფატები. კერძოდ, 2,3-დიფოსფოგლიცერატი (DPG) მნიშვნელოვნად ამცირებს G.-ის აფინურობას ჟანგბადთან, რაც ხელს უწყობს O 2-ის მოცილებას ოქსიჰემოგლობინიდან. DPG-ის გავლენა გ.-ზე იზრდება pH-ის მნიშვნელობის შემცირებით (ფიზიოლის, რეგიონის ფარგლებში), ამიტომ მისი გავლენა გ.-ს CDK-ზე უფრო მეტად ვლინდება დაბალი pH-ის მნიშვნელობებზე. DPG უერთდება უპირატესად დეოქსიჰემოგლობინს 1:1 მოლური თანაფარდობით, შედის მისი მოლეკულის შიდა ღრუში და ქმნის 4 მარილის ხიდს ბეტა ჯაჭვების ვალინის ნარჩენების ორი ალფა-NH 2 ჯგუფთან და, როგორც ჩანს, ჰისტიდინების ორი იმიდაზოლური ჯგუფით. 21 (143) ბეტა ჯაჭვი. DPG-ის გავლენა მცირდება ტემპერატურის მატებასთან ერთად, ანუ DPG-ის G მოლეკულასთან შეკავშირების პროცესი ეგზოთერმულია. ეს იწვევს იმ ფაქტს, რომ DPG-ის თანდასწრებით, ჟანგბადის პროცესის დამოკიდებულება ტემპერატურაზე დიდწილად ქრება. შესაბამისად, სისხლის მიერ ჟანგბადის ნორმალური გამოყოფა შესაძლებელი ხდება ტემპერატურის ფართო დიაპაზონში. ანალოგიურ ეფექტს, თუმცა ნაკლებად, ახორციელებს ATP, პირიდოქსალ ფოსფატი და სხვა ორგანული ფოსფატები. ამრიგად, ორგანული ფოსფატების კონცენტრაცია ერითროციტებში მნიშვნელოვან გავლენას ახდენს რესპირატორული ფუნქციაგ., სწრაფად ადაპტირდება სხვადასხვა ფიზიოლთან და პატოლთან, პირობებთან, რომლებიც დაკავშირებულია ჟანგბადის დაქვეითებასთან * (ატმოსფეროში ჟანგბადის შემცველობის ცვლილება, სისხლის დაკარგვა, ჟანგბადის ტრანსპორტირების რეგულირება დედიდან ნაყოფამდე პლაცენტის მეშვეობით და ა.შ.). ამრიგად, ანემიისა და ჰიპოქსიის დროს, ერითროციტებში DPG-ის შემცველობა იზრდება, რაც CDC-ს მარჯვნივ გადააქვს და იწვევს ჟანგბადის უფრო მეტ გამოყოფას ქსოვილებში. ბევრი ნეიტრალური მარილი (აცეტატები, ფოსფატები, კალიუმის და ნატრიუმის ქლორიდები) ასევე ამცირებს გ.-ის მიდრეკილებას ჟანგბადთან. ეს ეფექტი დამოკიდებულია ნივთიერების ბუნებაზე და ორგანული ფოსფატების ეფექტის მსგავსია. მარილის მაღალი კონცენტრაციის თანდასწრებით, G.-ს მიდრეკილება ჟანგბადთან აღწევს მინიმუმს - იგივე ზომით სხვადასხვა მარილებისა და DPG-ისთვის, ანუ მარილები და DPG ერთმანეთს ეჯიბრებიან G მოლეკულაზე ერთიდაიგივე შეკავშირების ცენტრებისთვის. ასე რომ, მაგალითად, DPG-ის ეფექტი ჟანგბადისადმი კავშირზე ქრება 0,5 M ნატრიუმის ქლორიდის თანდასწრებით.
ჯერ კიდევ 1904 წელს, ჩრ. აჩვენა გ.-ს ჟანგბადისადმი მიდრეკილების დაქვეითება სისხლში ნახშირორჟანგის ნაწილობრივი წნევის მატებით.
ნახშირორჟანგის შემცველობის ზრდა, პირველ რიგში, იწვევს გარემოს pH-ის ცვლილებას, მაგრამ P50 მნიშვნელობა მცირდება იმაზე მეტად, ვიდრე მოსალოდნელია მნიშვნელობის ასეთი შემცირებით.
pH მნიშვნელობები. ეს გამოწვეულია ნახშირორჟანგის სპეციფიური ურთიერთობით ალფა ჯაჭვების დაუმუხტავ ალფა-NH2 ჯგუფებთან და, შესაძლოა, აირის ბეტა ჯაჭვებთან, კარბამატების (კარბჰემოგლობინის) წარმოქმნით შემდეგი სქემის მიხედვით:
დეოქსიჰემოგლობინი აკავშირებს უფრო მეტ ნახშირორჟანგს, ვიდრე HbO2. ერითროციტებში DPG-ის არსებობა კონკურენტულად აფერხებს კარბამატების წარმოქმნას. კარბამატის მექანიზმის დახმარებით ჯანმრთელი ადამიანების ორგანიზმიდან 15%-მდე გამოიყოფა ნახშირორჟანგი დასვენების დროს. სისხლის ბუფერული სიმძლავრის 70%-ზე მეტი უზრუნველყოფილია მასში არსებული გაზით, რაც ასევე იწვევს გაზის მნიშვნელოვან არაპირდაპირ მონაწილეობას ნახშირორჟანგის გადაცემაში. როდესაც სისხლი მიედინება ქსოვილებში, HbO 2 გარდაიქმნება დეოქსიჰემოგლობინში, აკავშირებს H+ იონებს და ამით H 2 CO 3-ს გარდაქმნის HCO 3-ად. ამრიგად, გ.-ს პირდაპირი და არაპირდაპირი მონაწილეობით ქსოვილებიდან სისხლში შემომავალი ნახშირორჟანგის 90%-ზე მეტი იკვრება და გადადის ფილტვებში.
მნიშვნელოვანია, რომ CDC ცვლის ყველა ეს რეგულატორი (H + , DPG, CO 2) ურთიერთდაკავშირებულია, რასაც დიდი მნიშვნელობა აქვს რიგ განვითარებად პათოლოგიურ პირობებში. ამრიგად, ერითროციტებში DPG-ის კონცენტრაციის ზრდა მათი მეტაბოლიზმის კომპლექსური ცვლილებების შედეგია, რომლის დროსაც pH მნიშვნელობის მატება მთავარი პირობაა. აციდოზისა და ალკალოზის დროს, ასევე H+-სა და DPG-ს შორის ურთიერთობის გამო, P50-ის მნიშვნელობა ტოლდება.
ჰემოგლობინის მეტაბოლიზმი
G.-ს ბიოსინთეზი ხდება ერითროციტების ახალგაზრდა ფორმებში (ერითრობლასტები, ნორმობლასტები, რეტიკულოციტები), სადაც გლიცინის შემადგენლობაში შემავალი რკინის ატომები და სუქცინის მჟავა მონაწილეობენ პორფირინის რგოლის ფორმირებით. ამინოლევულინის მჟავა. ამ უკანასკნელის ორი მოლეკულა გარდაიქმნება პიროლის წარმოებულად - პორფირინის წინამორბედად. გლობინი წარმოიქმნება ამინომჟავებისგან, ანუ ცილის სინთეზის ჩვეულებრივი გზით. გ-ის დაშლა იწყება ერითროციტებში, სრულდება მათი სასიცოცხლო ციკლი. ჰემი იჟანგება ალფა-მეთინის ხიდის მეშვეობით, არღვევს კავშირს პიროლის შესაბამის რგოლებს შორის.
მიღებულ G. წარმოებულს ეწოდება ვერდოგლობინი (მწვანე პიგმენტი). ის ძალიან არასტაბილურია და ადვილად იშლება რკინის იონად (Fe 3+), დენატურირებულ გლობინად და ბილივერდინად.
გ-ის კატაბოლიზმში დიდი მნიშვნელობა აქვს ჰაპტოგლობინ-ჰემოგლობინის კომპლექსს (Hp-Hb). ერითროციტიდან სისხლში გამოსვლისას G. შეუქცევადად უერთდება ჰაპტოგლობინს (იხ.) Hp-Hb კომპლექსში. პლაზმაში Hp-ის მთელი რაოდენობის ამოწურვის შემდეგ გ. შეიწოვება თირკმელების პროქსიმალური მილაკებით. გლობინის ძირითადი ნაწილი თირკმელებში იშლება 1 საათის განმავლობაში.
ჰემის კატაბოლიზმი Hp-Hb კომპლექსში ხორციელდება ღვიძლის, ძვლის ტვინის და ელენთის რეტიკულოენდოთელური უჯრედებით ნაღვლის პიგმენტების წარმოქმნით (იხ.). ამ პროცესში გამოთავისუფლებული რკინა ძალიან სწრაფად ხვდება მეტაბოლურ აუზში და გამოიყენება ახალი რკინის მოლეკულების სინთეზში.
ჰემოგლობინის კონცენტრაციის განსაზღვრის მეთოდები. სოლებში, პრაქტიკაში, G. ჩვეულებრივ განისაზღვრება კოლორიმეტრული მეთოდით Sali ჰემომეტრის გამოყენებით, G.-დან წარმოქმნილი ჰემინის რაოდენობის გაზომვის საფუძველზე (იხ. ჰემოგლობინომეტრია). თუმცა, სისხლში ბილირუბინისა და მეტემოგლობინის შემცველობიდან გამომდინარე, ასევე პატოლის ზოგიერთ პირობებში მეთოდის ცდომილება აღწევს +30%-ს. სპექტროფოტომეტრიული კვლევის მეთოდები უფრო ზუსტია (იხ. სპექტროფოტომეტრია).
სისხლში მთლიანი ჰემოგლობინის დასადგენად გამოიყენება ციანმეტემოგლობინის მეთოდი, რომელიც ეფუძნება ჰემოგლობინის ყველა წარმოებულს (დეოქსი-Hb, HbO 2, HbCO, met-Hb და ა. ხსნარი 540 ნმ. ამავე მიზნით გამოიყენება პირიდინ-ჰემოქრომოგენული მეთოდი. HbO 2-ის კონცენტრაცია ჩვეულებრივ განისაზღვრება სინათლის შთანთქმით 542 ნმ ან გაზომეტრიული მეთოდით (შეკრული ჟანგბადის რაოდენობით).
ჰემოგლობინი კლინიკურ პრაქტიკაში
გ-ის რაოდენობრივი შემცველობისა და თვისებრივი შემადგენლობის განსაზღვრა გამოიყენება სხვა ჰემატოლთან ერთად. ინდიკატორები (ჰემატოკრიტი, სისხლის წითელი უჯრედების რაოდენობა, მათი მორფოლოგია და ა.შ.) რიგი პათოლოგიების დიაგნოსტიკისთვის, სისხლის წითელი მდგომარეობების (ანემია, ერითრემია და მეორადი ერითროციტოზი, სისხლის დაკარგვის ხარისხის შეფასება, სისხლის გასქელება დეჰიდრატაციის დროს. სხეული და დამწვრობა და ა.შ.), თერაპიის დროს ჰემო-ტრანსფუზიის ეფექტურობის შესაფასებლად და ა.შ.
ჩვეულებრივ, სისხლში გ-ს შემცველობა საშუალოდ 14,5 + 0,06 გ% შეადგენს მამაკაცებს (ვარიაციები 13,0-16,0 გ%) და ქალებში 12,9 + 0,07 გ% (12,0- 14,0 გ%), L. E. Yarustovskaya et al. (1969); რყევები დამოკიდებულია სხეულის ასაკზე და კონსტიტუციურ მახასიათებლებზე, ფიზიკურზე. აქტივობა, დიეტა, კლიმატი, ჟანგბადის ნაწილობრივი წნევა გარემომცველ ჰაერში. გ-ის კონცენტრაცია სისხლში არის ფარდობითი მნიშვნელობა, რაც დამოკიდებულია არა მხოლოდ სისხლში მთლიანი გ-ის აბსოლუტურ რაოდენობაზე, არამედ პლაზმის მოცულობაზეც. პლაზმის მოცულობის მატებამ G.-ს მუდმივი რაოდენობით სისხლში შეიძლება დაუფასებელი მაჩვენებლების მიცემა გ.-ს განსაზღვრისას და ანემიის იმიტაცია.
გ-ის შემცველობის უფრო სრულყოფილი შეფასებისთვის გამოიყენება აგრეთვე არაპირდაპირი მაჩვენებლები: ფერის ინდიკატორის განსაზღვრა, გ-ის საშუალო შემცველობა სისხლის ერთ წითელ უჯრედში, უჯრედული გ-ის საშუალო კონცენტრაცია ჰემატოკრიტის ინდექსთან მიმართებაში და ა.შ.
წარმოიქმნება ანემიის მძიმე ფორმების დროს, სისხლში გ.-ს კონცენტრაციის დაქვეითება გარკვეულ კრიტიკულ მნიშვნელობამდე - 2-3 გ% და ქვემოთ (ჰემოგლობინოპენია, ოლიგოქრომია) - ჩვეულებრივ იწვევს სიკვდილს, თუმცა, ქრონიკული ანემიის ზოგიერთი ტიპით. ცალკეული პაციენტები, კომპენსატორული მექანიზმების განვითარების გამო, ეგუებიან ასეთ კონცენტრაციას.
პატოლში პირობები, გ-ის შემცველობა და სისხლის წითელი უჯრედების რაოდენობა ყოველთვის არ იცვლება პარალელურად, რაც აისახება ანემიის კლასიფიკაციაში (გამოყოფენ ანემიის ნორმალურ, ჰიპო- და ჰიპერქრომიულ ფორმებს); ერითრემიას და მეორად ერითროციტოზს ახასიათებს G.-ს მომატებული კონცენტრაცია (ჰიპერქრომია) და ერთდროულად სისხლის წითელი უჯრედების რაოდენობის მატება.
სისხლში თითქმის მთელი გლუკოზა გვხვდება სისხლის წითელ უჯრედებში; მისი ნაწილი არის პლაზმაში Hp-Hb კომპლექსის სახით. თავისუფალი პლაზმური გლუკოზა ჩვეულებრივ შეადგენს 0,02-2,5 მგ% (გ.ვ. დერვიზისა და ნ.კ. ბიალკოს მიხედვით). პლაზმაში თავისუფალი ჰემოლიზის შემცველობა იზრდება ზოგიერთი ჰემოლიზური ანემიის დროს, რომელიც ვლინდება უპირატესად ინტრავასკულარული ჰემოლიზით (იხ. ჰემოგლობინემია).
რამდენიმე ნორმალური ტიპის ჰემოგლობინის არსებობის გამო, აგრეთვე სისხლში სხვადასხვა წარმოშობის პათოლოგიური ჰემოგლობინის ზოგიერთი დაავადების გამოჩენის გამო (იხ. ჰემოგლობინოპათია), დიდი ყურადღება ეთმობა ერითროციტებში ჰემოგლობინის ხარისხობრივი შემადგენლობის განსაზღვრას („ჰემოგლობინის ფორმულა ”). ამრიგად, G. ტიპის HbF და HbA2 გაზრდილი რაოდენობით გამოვლენა ჩვეულებრივ დამახასიათებელია ბეტა თალასემიის ზოგიერთი ფორმისთვის.
HbF შემცველობის მატება ასევე აღინიშნა სხვა ჰემატოლთან ერთად. დაავადებები (მწვავე ლეიკემია, აპლასტიკური ანემია, პაროქსიზმული ღამის ჰემოგლობინურია და ა.შ.), ასევე ინფექციური ჰეპატიტი, ნაყოფის ჰემოგლობინის ასიმპტომური მემკვიდრეობითი მდგრადობა და ორსულობა. სისხლში HbA2 ფრაქციის კონცენტრაცია იზრდება გარკვეული არასტაბილური გაზებისა და ინტოქსიკაციების არსებობისას და მცირდება რკინადეფიციტური ანემიის დროს.
ადამიანის ონტოგენეზში არის ცვლილება სხვადასხვა სახისნაყოფში გამოვლენილია ნორმალური ჰემოგლობინი P (პრიმიტიული) (18 კვირამდე); მისი ჯიშები იგივეა, რაც Hb Gower1 და Hb Gower2.
პირველადი ჰემატოპოეზის უპირატესობა შეესაბამება ვიტელინური ჰემატოპოეზის პერიოდს, ხოლო შემდგომში ღვიძლის ჰემატოპოეზის პერიოდში HbF სინთეზირდება უპირატესად.
"ზრდასრული" HbA-ს სინთეზი მკვეთრად ძლიერდება ძვლის ტვინის ჰემატოპოეზის პერიოდში; HbF შემცველობა ახალშობილ ბავშვში შეადგენს G.-ს მთლიანი რაოდენობის 70-90%-მდე (დარჩენილი 10-30% მოდის HbA ფრაქციაზე). სიცოცხლის პირველი წლის ბოლოს HbF კონცენტრაცია ჩვეულებრივ მცირდება 1-2%-მდე და შესაბამისად იზრდება HbA შემცველობა.
ცნობილია, რომ წმ. გ-ის 200 პათოლოგიური (პათოლოგიური ან უჩვეულო) ვარიანტი, რომელთა გაჩენა გამოწვეულია გლობინის პოლიპეპტიდური ჯაჭვების წარმოქმნის სხვადასხვა მემკვიდრეობითი დეფექტებით.
აღმოჩენა L. Pauling, Itano (N. A. Itano) და სხვ. 1949 წელს პატოლმა, ჰემოგლობინმა S (ინგლ. sickle cell sickle cell) საფუძველი ჩაუყარა მოლეკულური დაავადებების შესწავლას. სისხლის წითელ უჯრედებში პათოლოგიური სისხლის უჯრედების არსებობა ჩვეულებრივ (მაგრამ არა ყოველთვის) იწვევს მემკვიდრეობითი ჰემოლიზური ანემიის სინდრომის განვითარებას (იხ.).
ჰემოგლობინის აღწერილი ვარიანტების უმეტესობა უნდა ჩაითვალოს არა პათოლოგიურ, არამედ G.S თაფლის საკმაოდ იშვიათ უჩვეულო ფორმებად. ჰემოგლობინებს S, C, D, E, Bart, H, M და არასტაბილური ჰემოგლობინის დიდ ჯგუფს (დაახლოებით 60) აქვს გარკვეული მნიშვნელობა. , მოლეკულა ხდება არასტაბილური ჟანგვის აგენტების მოქმედების, გათბობისა და რიგი სხვა ფაქტორების მიმართ. GM-ჯგუფები წარმოიქმნება ამინომჟავების ჩანაცვლების შედეგად პოლიპეპტიდურ ჯაჭვებში ჰემე-გლობინის კონტაქტების არეში, რაც იწვევს არა მხოლოდ მოლეკულის არასტაბილურობას, არამედ მეტემოგლობინის წარმოქმნისადმი მიდრეკილებას. M-ჰემოგლობინოპათია ხშირად არის მემკვიდრეობითი მეტემოგლობინემიის მიზეზი (იხ.).
გ.-ს კლასიფიკაცია თავდაპირველად ეფუძნებოდა მათ გამოსახვას ლათინური ანბანის ასოებით გახსნის თანმიმდევრობით; გამონაკლისი კეთდება ნორმალური "ზრდასრული" G.-სთვის, რომელიც მითითებულია ასო A და ნაყოფის G. (HbF). ასო S მიუთითებს არანორმალური ნამგლისებრუჯრედოვანი G. (სინონიმი HbB). ამრიგად, ლათინური ანბანის ასოები A-დან S-მდე ითვლებოდა G-ის საყოველთაოდ მიღებულ აღნიშვნებში X International Hematol-ში მიღებულის მიხედვით. კონგრესი (სტოკჰოლმი, 1964) გ. ნომენკლატურა ამიერიდან არ არის რეკომენდებული ანბანის დარჩენილი ასოების გამოყენება ახალი ვარიანტების აღსანიშნავად.
ახლა მიღებულია გ.-ს ახლად აღმოჩენილი ფორმების დასახელება აღმოჩენის ადგილის მიხედვით, ქალაქის (რეგიონის), საავადმყოფოს ან ლაბორატორიის სახელის გამოყენებით, სადაც პირველად აღმოაჩინეს ახალი გ. და ამინომჟავების ჩანაცვლების ბუნება დაზარალებულ წრეში. მაგალითად, Hb Koln (alpha 2 beta 2 98 val->met) ნიშნავს, რომ ჰემოგლობინის კოლნში იყო ჩანაცვლება ამინომჟავის ვალინის ერთ-ერთი ბეტა პოლიპეპტიდური ჯაჭვის 98-ე პოზიციაზე მეთიონინით.
გ-ის ყველა ჯიში განსხვავდება ერთმანეთისგან ფიზიკური და ქიმიური მახასიათებლებით. და ფიზიკური თვისებები და ზოგიერთი ასევე ფუნქციური თვისებებით, რომლებზეც დაფუძნებულია კლინიკაში გ.-ის სხვადასხვა ვარიანტების გამოვლენის მეთოდები. აღმოჩენილია არანორმალური გაზების ახალი კლასი ჟანგბადთან შეცვლილი აფინურობით. გ.-ს აკრეფა ხორციელდება ელექტროფორეზისა და რიგი სხვა ლაბორატორიული მეთოდების გამოყენებით (ტესტები ტუტე რეზისტენტობისა და თერმული დენატურაციის, სპექტროფოტომეტრია და სხვ.).
ელექტროფორეზული მობილურობიდან გამომდინარე, გ. იყოფა სწრაფ, ნელა და ნორმალურად (იგივე მობილურობით, რაც HbA). თუმცა, ამინომჟავის ნარჩენების ჩანაცვლება ყოველთვის არ იწვევს მოლეკულის მუხტის ცვლილებას, ამიტომ ზოგიერთი ვარიანტის აღმოჩენა ელექტროფორეზის გამოყენებით შეუძლებელია.
ჰემოგლობინი სასამართლო მედიცინაში
G. და მისი წარმოებულები სასამართლო მედიცინაში განსაზღვრულია სისხლის არსებობის დადგენა ფიზიკურ მტკიცებულებებზე ან ნებისმიერ სითხეში მოწამვლის დიაგნოსტიკის დროს, რომლებიც იწვევენ გ.-ში ცვლილებებს, განასხვავებენ ნაყოფის ან ახალშობილის კუთვნილ სისხლს ზრდასრული ადამიანის სისხლისაგან. . არსებობს მტკიცებულება მემკვიდრეობითი ნიშნების გამოყენების შესახებ სადავო მამობის, მშობიარობისა და ბავშვების გამოცვლის გამოკვლევისას, აგრეთვე სისხლის ინდივიდუალიზაციის მიზნით ფიზიკურ მტკიცებულებებზე.
ცხოველების იმუნიზაციით ადამიანის ჰემოგლობინით, მიიღეს ჰემოგლობინის გამომწვევი შრატები. ამ შრატების დახმარებით ადამიანის სისხლის არსებობა შეიძლება დადგინდეს გ-ზე გამოკვლეულ ლაქაში.
ლაქებში სისხლის არსებობის დასადგენად გამოიყენება მიკროსპექტრული ანალიზი და მიკროკრისტალური რეაქციები. პირველ შემთხვევაში ჰემოქრომოგენი გარდაიქმნება ტუტე და შემამცირებელი საშუალება ჰემოქრომოგენად, რომელსაც აქვს დამახასიათებელი შთანთქმის სპექტრი (იხ. ჰემოქრომოგენი), ან ჰემოქრომოგენზე მოქმედებს კონცენტრირებული გოგირდის მჟავა, რაც იწვევს ჰემატოპორფირინის წარმოქმნას ტიპიური შთანთქმის სპექტრი სპექტრის ხილულ ნაწილში.
მიკროკრისტალური რეაქციებიდან სისხლის არსებობის დასადგენად, ყველაზე ხშირად გამოიყენება ტესტები, რომლებიც დაფუძნებულია ჰემოქრომოგენისა და ჰემინის ჰიდროქლორიდის კრისტალების წარმოებაზე. ჰემინის კრისტალების მისაღებად ქსოვილიდან გ.-ზე გამოკვლეული ლაქით, აიღეთ ძაფი და დადეთ მინის სლაიდზე, დაამატეთ ნატრიუმის ქლორიდის რამდენიმე კრისტალი და რამდენიმე წვეთი კონცენტრირებული ძმარმჟავა (ტეიხმანის რეაგენტი). გაცხელებისას (სისხლის თანდასწრებით) გ-დან წარმოიქმნება ჰემინის ჰიდროქლორიდის კრისტალები (ტეიხმანის კრისტალები) - ყავისფერი ირიბი პარალელოგრამები, ზოგჯერ რეაქციები გამოიყენება გ-დან იოდის ჰემინის კრისტალების მისაღებად - პატარა შავი კრისტალები ფორმის. რომბისებრი პრიზმები.
გარკვეული მოწამვლის დროს სისხლში სპექტროსკოპიულად ვლინდება გ-ის წარმოებულები. მაგალითად, ნახშირბადის მონოქსიდით მოწამვლის შემთხვევაში, მსხვერპლთა სისხლში აღმოჩენილია კარბოქსიჰემოგლობინი მეტემოგლობინის წარმომქმნელი ნივთიერებებით მოწამვლისას;
ჩვილების მკვლელობის შემთხვევაში შესაძლოა საჭირო გახდეს ახალშობილის ან ნაყოფის სისხლის არსებობის დადგენა სხვადასხვა ფიზიკურ მტკიცებულებებზე. ვინაიდან ნაყოფისა და ახალშობილის სისხლში HbA-ის მაღალი შემცველობაა, ხოლო ზრდასრული ადამიანის სისხლში HbA, ისინი გამოირჩევიან ფიზიკური და ქიმიური თვისებებით. თვისებები, ახალშობილის (ნაყოფის) და ზრდასრული ადამიანის გ. ადვილად დიფერენცირებულია.
პრაქტიკაში ყველაზე ხშირად გამოიყენება ტუტე დენატურაცია, ვინაიდან ნაყოფის ჯირკვალი უფრო მდგრადია ტუტეების მოქმედების მიმართ, ვიდრე ზრდასრული ჯირკვალი. გ-ის ცვლილებები განისაზღვრება სპექტროსკოპიულად, სპექტროფოტომეტრიულად ან ფოტომეტრიულად.
პოლიპეპტიდური ჯაჭვების სინთეზი ხორციელდება სტრუქტურული და (შესაძლოა) მარეგულირებელი გენების კონტროლით. სტრუქტურული გენები განსაზღვრავს პოლიპეპტიდური ჯაჭვების ამინომჟავების სპეციფიკურ თანმიმდევრობას, ხოლო მარეგულირებელი გენები განსაზღვრავს მათი სინთეზის სიჩქარეს (იხ. გენი).
ადამიანებში არსებული 6 ტიპის ნორმალური გ ჯაჭვები (Hbα, Hbβ, Hbγ, Hbδ, Hbε, Hbζ) შესაბამისად კოდირებულია 6 გენის ლოკუსით (α, β, γ, δ, ε, ζ). ითვლება, რომ α ჯაჭვებისთვის შეიძლება არსებობდეს ორი ადგილი. გარდა ამისა, აღმოაჩინეს 5 სხვადასხვა γ-ჯაჭვი, რომლებიც დაშიფრულია სხვადასხვა ლოკებით. ამრიგად, საერთო ჯამში, ადამიანს შეიძლება ჰქონდეს 7-დან 10 წყვილამდე სტრუქტურული გენი, რომლებიც აკონტროლებენ გ-ის სინთეზს.
განვითარების ეტაპების შესწავლამ აჩვენა, რომ ადამიანებში არსებობს სხვადასხვა გ-ების სინთეზის მკაფიო და კარგად დაბალანსებული გენეტიკური რეგულირება საშვილოსნო სიცოცხლის პირველ ნახევარში ადამიანებში, გლ. arr. α, γ, ζ, ε-ჯაჭვების ლოკუსები (ეს უკანასკნელი მხოლოდ მცირე ხნით, ემბრიონის სიცოცხლის ადრეულ პერიოდში). დაბადების შემდეგ, გამა ჯაჭვის ლოკუსის გამორთვასთან ერთად, აქტიურდება β და δ ჯაჭვის ლოკუსები. ამ გადართვის შედეგად ნაყოფის ჰემოგლობინი (HbF) იცვლება ზრდასრული ჰემოგლობინებით - HbA HbA2-ის მცირე ფრაქციით.
რჩება გაურკვეველი კითხვები: გენის ლოკუსების მდებარეობა, რომლებიც განსაზღვრავენ G.-ს სინთეზს ქრომოსომებზე, მათ კავშირში, გ.-ს სტრუქტურული გენების სპეციფიური აქტივაციისა და რეპრესიის დამოკიდებულება, რომელიც დაკავშირებულია ონტოგენეზის პერიოდებთან მარეგულირებელი გენების მოქმედებაზე. ჰუმორული ფაქტორების (მაგალითად, ჰორმონების) გავლენა და ა.შ.
გლობინის ჯაჭვების სინთეზი უჯრედში ცილის სინთეზის განსაკუთრებული მაგალითია.
მიუხედავად იმისა, რომ ჯერ კიდევ ბევრი რამ არის გაურკვეველი G. სინთეზის რეგულირებაში, ძირითადი მექანიზმები, როგორც ჩანს, არის ის, რაც აკონტროლებს mRNA (მესენჯერი RNA) დნმ-დან ტრანსკრიფციის სიჩქარეს. გლობინის სინთეზზე სპეციალურად პასუხისმგებელი დნმ-ის ზუსტი დახასიათება არ არის მიღებული. თუმცა, 1972 წელს რამდენიმე ლაბორატორიამ ერთდროულად მოახერხა გენის სინთეზირება, რომელიც არეგულირებს G-ის სინთეზს. ეს გაკეთდა ფერმენტის საპირისპირო ტრანსკრიპტაზას გამოყენებით (იხ. გენეტიკური ინჟინერია).
G. მოლეკულის ჰემის ნაწილი ცალკე სინთეზირებულია სერიის გამოყენებით ფერმენტული რეაქციებიდაწყებული აქტიური სუქცინატით (საქცინის მჟავით) კრებსის ციკლიდან და დამთავრებული რთული პროტოპორფირინის რგოლით, ცენტრში რკინის ატომით.
ცილის სინთეზის პროცესში გლობინის ჯაჭვები იღებენ თავის დამახასიათებელ კონფიგურაციას და ჰემი „იდება“ სპეციალურ ჯიბეში. შემდეგი, დასრულებული ჯაჭვების კომბინაცია ხდება ტეტრამერის წარმოქმნით.
სპეციფიკური დნმ-ის სინთეზი ხდება ერითროციტების წინამორბედებში მხოლოდ ორთოქრომული ნორმობლასტის სტადიამდე. ამ პერიოდის განმავლობაში იქმნება გლობინის პოლიპეპტიდური ჯაჭვების საბოლოო ნაკრები, იგი შერწყმულია ჰემთან და წარმოიქმნება ყველა სახის რნმ და საჭირო ფერმენტები.
გ.-ს სინთეზის მემკვიდრეობითი დარღვევები იყოფა ორ დიდ ჯგუფად:
1) ე.წ ჰემოგლობინის პირველადი სტრუქტურის სტრუქტურული ვარიანტები ან ანომალიები - „ხარისხობრივი“ ჰემოგლობინოპათიები, როგორიცაა Hb, S, C, D, E, M, ისევე როგორც არასტაბილური ჰემოგლობინით გამოწვეული დაავადებები და ჰემოგლობინოპათიები O 2-ის მიმართ გაზრდილი აფინურობით (იხ. ჰემოგლობინოპათიები),
2) პირობები, რომლებიც წარმოიქმნება გლობინის ერთ-ერთი პოლიპეპტიდური ჯაჭვის სინთეზის სიჩქარის დარღვევის შედეგად - "რაოდენობრივი" ჰემოგლობინოპათია ან თალასემია (იხ.).
სტრუქტურული ვარიანტებით, G მოლეკულის სტაბილურობა და ფუნქცია შეიძლება შეიცვალოს თალასემიის დროს, გლობინის სტრუქტურა შეიძლება იყოს ნორმალური. ვინაიდან გენეტიკური დეფექტების ორივე ტიპი ხშირია ადამიანთა მრავალ პოპულაციაში, ხშირად შეინიშნება ინდივიდები, რომლებიც ერთდროულად ჰეტეროზიგოტები არიან G.-ს სტრუქტურული ვარიანტისთვის და თალასემიისთვის. სხვადასხვა გენების კომბინაცია ქმნის ჰემოგლობინოპათიების ძალიან რთულ სპექტრს. ზოგიერთ შემთხვევაში, მუტაციამ შეიძლება გავლენა მოახდინოს G.-ს სინთეზის გადართვის მექანიზმებზე, რაც იწვევს, მაგალითად, ნაყოფის G.-ს სინთეზის გაგრძელებას მოზრდილებში. ამ პირობებს ერთობლივად უწოდებენ ნაყოფის ჰემოგლობინის მემკვიდრეობითი მდგრადობას.
შერწყმის ვარიანტებს მიეკუთვნება Hb Lepore, ანტი-ლეპური და კენიური მუტანტები. სავარაუდოა, რომ G.-ის ეს სტრუქტურული ანომალიები წარმოიშვა მჭიდროდ დაკავშირებულ G გენებს შორის არათანაბარი არაჰომოლოგური გადაკვეთის შედეგად, რის შედეგადაც, მაგალითად, Hb Lepore-ში α-ჯაჭვები ნორმალურია და სხვა პოლიპეპტიდური ჯაჭვები. შეიცავს δ- თანმიმდევრობის ნაწილს და β- მიმდევრობის პოლიპეპტიდურ ჯაჭვების ნაწილს.
ვინაიდან მუტაციები შეიძლება მოხდეს ნებისმიერ გენში, რომელიც განსაზღვრავს გენების სინთეზს, შეიძლება წარმოიშვას რამდენიმე სიტუაცია, როდესაც ინდივიდები იქნებიან ჰომოზიგოტები, ჰეტეროზიგოტები ან ორმაგი ჰეტეროზიგოტები პათოლოგიური გენების ალელებისთვის ერთ ან მეტ ლოკზე.
ცნობილია გ-ის 200-ზე მეტი სტრუქტურული ვარიანტი, მათგან 120-ზე მეტი დახასიათებულია და ხშირ შემთხვევაში შესაძლებელი გახდა გ-ის სტრუქტურული ცვლილების დაკავშირება მის ანომალიურ ფუნქციასთან. წერტილის მუტაციის შედეგად გ-ის ახალი ვარიანტის გაჩენის უმარტივესი მექანიზმი (გენეტიკურ კოდში ერთი ბაზის ჩანაცვლება) შეიძლება აჩვენოს HbS-ის (სქემის) მაგალითით.
ამინომჟავის ჩანაცვლების გავლენა ფიზიკურ-ქიმიურზე. G. მოლეკულის თვისებები, სტაბილურობა და ფუნქცია დამოკიდებულია ამინომჟავის ტიპზე, რომელმაც შეცვალა წინა და მის პოზიციაზე მოლეკულაში. მთელი რიგი მუტაციები (მაგრამ არა ყველა) მნიშვნელოვნად ცვლის ჰემოგლობინის მოლეკულის ფუნქციას და სტაბილურობას (HbM, არასტაბილური ჰემოგლობინი, ჰემოგლობინი შეცვლილი აფინურობით O 2-ის მიმართ) ან მის კონფიგურაციას და ფიზიკურ-ქიმიურ რიგს. თვისებები (HbS და HbC).
ჰემოგლობინი არასტაბილურია
არასტაბილური ჰემოგლობინი არის არანორმალური ჰემოგლობინის ჯგუფი, რომელიც განსაკუთრებით მგრძნობიარეა ჟანგვის აგენტების, სითბოს და რიგი სხვა ფაქტორების მოქმედების მიმართ, რაც აიხსნება მათ მოლეკულებში ზოგიერთი ამინომჟავის ნარჩენების გენეტიკურად განსაზღვრული ჩანაცვლებით სხვებით; ასეთი ჰემოგლობინის გადატანა ხშირად ვლინდება ჰემოგლობინოპათიის სახით (იხ.).
ადამიანების ერითროციტებში, რომლებიც არასტაბილური გ-ის მატარებლები არიან, ე.წ. ჰაინცის სხეულები, რომლებიც წარმოადგენენ არასტაბილური სისხლის უჯრედების დენატურირებული მოლეკულების აკუმულაციას (თანდაყოლილი ჰემოლიზური ანემია ჰაინცის სხეულებით). 1952 წელს I.A. Cathie ვარაუდობს, რომ ეს დაავადება მემკვიდრეობითი იყო. Frick (P. Frick), Gitzig (W. H. Hitzig) და Vetke (K. Betke) 1962 წელს პირველად Hb Zurich-ის მაგალითის გამოყენებით დაამტკიცეს, რომ ჰემოლიზური ანემია ჰაინცის სხეულებთან დაკავშირებულია არასტაბილური ჰემოგლობინის არსებობასთან. კარელმა (R. W. Carrell) და გ. ლემანმა 1969 წელს შემოგვთავაზეს ახალი სახელი ასეთი ჰემოგლობინოპათიებისთვის - ჰემოლიზური ანემია, რომელიც გამოწვეულია არასტაბილური გ.
ჰემის მოლეკულების არასტაბილურობა შეიძლება გამოწვეული იყოს ჰემთან კონტაქტში ამინომჟავების ნარჩენების ჩანაცვლებით; არაპოლარული ამინომჟავის ნარჩენის შეცვლა პოლარულით; მოლეკულის მეორადი სტრუქტურის დარღვევა, რომელიც გამოწვეულია ნებისმიერი ამინომჟავის ნარჩენის პროლინის ნარჩენით ჩანაცვლებით; ამინომჟავების ნარჩენების ჩანაცვლება α1β1- და α2β2-კონტაქტების არეში, რამაც შეიძლება გამოიწვიოს ჰემოგლობინის მოლეკულის დაშლა მონომერებად და დიმერებად; ზოგიერთი ამინომჟავის ნარჩენების წაშლა (დაკარგვა); ქვედანაყოფის გახანგრძლივება, მაგალითად, ორ არასტაბილურ ჰემოგლობინს - Hb Cranston-ს და Hb Tak-ს აქვს წაგრძელებული ბეტა ჯაჭვები ნორმალურ ჰემოგლობინთან შედარებით, მათ C-ბოლოზე მიმაგრებული ჰიდროფობიური სეგმენტის გამო.
არასტაბილური აირების კლასიფიკაცია, შემოთავაზებული J.V. Dacie-ს მიერ და შეცვლილია Yu N. Tokarev-ისა და V.M. Belostotsky-ის მიერ, ეფუძნება მოლეკულაში მომხდარი ცვლილებების ბუნებას, რაც აირს არასტაბილურს ხდის.
აღწერილია დაახლ. 90 არასტაბილური G. და G. მოლეკულის ბეტა ჯაჭვებში ამინომჟავების ნარჩენების ჩანაცვლებითი ვარიანტები გვხვდება დაახლოებით 4-ჯერ უფრო ხშირად, ვიდრე ალფა ჯაჭვებში ასეთი ნარჩენების ჩანაცვლებით.
არასტაბილური გ-ის მატარებელი მემკვიდრეობით მიიღება აუტოსომური დომინანტური გზით, ხოლო მატარებლები არიან ჰეტეროზიგოტები. ზოგ შემთხვევაში არასტაბილური გ-ის გადაზიდვის გაჩენა სპონტანური მუტაციის შედეგია. გ-ის სტაბილურობის დაქვეითება იწვევს არა მხოლოდ მის ადვილ ნალექს, არამედ ზოგიერთ შემთხვევაში ჰემის დაკარგვას. ამინომჟავების ნარჩენების ჩანაცვლებამ ჰემოგლობინის მოლეკულის a- და (3-ჯაჭვები) შეხების წერტილებში შეიძლება გავლენა მოახდინოს მოლეკულის ჟანგბადისადმი მიდრეკილებაზე, ჰემების ურთიერთქმედებასა და ტეტრამერებს, დიმერებს და ჰემოგლობინის მონომერებს შორის ბალანსს. ადამიანები ჰეტეროზიგოტები არასტაბილური ჰემოგლობინის გენების მიმართ, როგორც ნორმალური, ასევე არანორმალური, არასტაბილური G., თუმცა, ეს უკანასკნელი სწრაფად დენატურდება და ხდება ფუნქციურად არააქტიური.
მძიმე ჰემოლიზური ანემია ჩვეულებრივ აღინიშნება პაციენტებში, რომლებიც არიან არასტაბილური გ-ის მატარებლები მოლეკულური არასტაბილურობის მაღალი ხარისხით.
სხვა არასტაბილური გ.სოლის ტარებისას, გამოვლინებები ჩვეულებრივ ზომიერი სიმძიმის ან სრულიად უმნიშვნელოა. ზოგიერთ შემთხვევაში (Hb Riverdale-Bronx, Hb Zurich და სხვ.) არასტაბილური გ.-ის გადატანა ვლინდება ჰემოლიზური კრიზების სახით გარკვეული მედიკამენტების მიღების (სულფონამიდები, ანალგეტიკები და სხვ.) ან ინფექციების ზემოქმედების შემდეგ. ზოგიერთ პაციენტს, მაგალითად, Hb Hammersmith-ის, Hb Bristol-ის, Hb Sydney-ის და ა.შ. მატარებლებს, აღენიშნებათ კანის ციანოზი, რომელიც გამოწვეულია მეტ- და სულფჰემოგლობინის ფორმირებით. არასტაბილური გ.-ს ტარებით გამოწვეული ჰემოგლობინოპათიები უნდა განვასხვავოთ სხვა ეტიოლოგიის ჰემოლიზური და ჰიპოქრომული ანემიებისაგან და, უპირველეს ყოვლისა, რკინის დეფიციტით და ჰემოლიზური ანემიებით, რომლებიც დაკავშირებულია პენტოზა-ფოსფატის ციკლის ფერმენტების გენეტიკურად განსაზღვრულ დეფიციტთან, გლიკოლიზთან და ა.შ.
ადამიანების უმეტესობას, რომლებიც არიან არასტაბილური გ-ის მატარებლები, არ საჭიროებს სპეციალურ მკურნალობას. ჰემოლიზისთვის სასარგებლოა აღდგენითი თერაპია. არასტაბილური გ.-ის ყველა მატარებელს რეკომენდირებულია თავი შეიკავოს ჰემოლიზის პროვოცირების ჟანგვითი პრეპარატებისგან (სულფონამიდები, სულფონები, ანალგეტიკები და სხვ.). სისხლის გადასხმა ნაჩვენებია მხოლოდ ღრმა ანემიის განვითარებით. მძიმე ჰემოლიზის შემთხვევაში ელენთის მიერ სისხლის წითელი უჯრედების გაზრდილი სეკვესტრით და ჰიპერსპლენიზმით, ნაჩვენებია სპლენექტომია (იხ.). თუმცა, სპლენექტომია ბავშვებში (6 წლამდე) ჩვეულებრივ არ ტარდება სეპტიცემიის განვითარების რისკის გამო.
არასტაბილური ჰემოგლობინის იდენტიფიცირების მეთოდები
ჰემოგლობინის თერმოლაციის შესწავლა ყველაზე მნიშვნელოვანი ტესტია მისი არასტაბილურობის დასადგენად. იგი შემოგვთავაზეს A. G. Grimes და A. Meisler-მა 1962 წელს და Dacey-მ 1964 წელს და შედგება 0.1 M ფოსფატით ან Tris-HCl ბუფერით განზავებული ჰემოლიზატების ინკუბაციისგან, pH 7.4, 50-60°-ზე ერთი საათის განმავლობაში. ამ შემთხვევაში, არასტაბილური გლიკოზიდები დენატურირებული და ნალექი ხდება, ხოლო ხსნარში დარჩენილი თერმოსტაბილური ჰიდროქსიდის რაოდენობა განისაზღვრება სპექტროფოტომეტრიულად 541 ნმ და გამოითვლება ფორმულის გამოყენებით:
/ * 100 = = თერმოსტაბილური ჰემოგლობინი (პროცენტი),
სადაც E არის ჩაქრობის მნიშვნელობა 541 ნმ ტალღის სიგრძეზე.
თერმოსტაბილური გ-ის ფარდობითი შემცველობა უდრის 100%-ს - თერმოსტაბილური გ-ის რაოდენობას (პროცენტებში).
კარელმა და ქეიმ (R. Kau) 1972 წელს შემოგვთავაზეს ჰემოლიზატების ინკუბაცია 17% იზოპროპანოლ-ტრის ბუფერის ნარევში, pH 7.4 37°-ზე 30 წუთის განმავლობაში.
ერითროციტების ჰემოლიზი შეიძლება გამოიწვიოს წყალმა, რადგან ამ მიზნით ნახშირბადის ტეტრაქლორიდის ან ქლოროფორმის გამოყენება იწვევს არასტაბილური სისხლის უჯრედების ნაწილობრივ დენატურაციას და მიღებული მონაცემების დამახინჯებას.
არასტაბილური გ.-ს განსაზღვრის ყველაზე გავრცელებული მეთოდია ჰისტოქიმიური, ჰაინცის სხეულების იდენტიფიცირების მეთოდი. ამ შემთხვევაში სისხლის წითელი უჯრედები შეღებილია ბროლის იისფერით, მეთილის იისფერით ან გამოიყენება რეაქცია აცეტილფენილჰიდრაზინით. სისხლი წინასწარ ინახება 24 საათის განმავლობაში 37° ტემპერატურაზე. გასათვალისწინებელია, რომ ჰაინცის სხეულები ასევე გვხვდება სხვა ჰემოლიზური ანემიების, თალასემიის, მეტემოგლობინის ფორმირების აგენტებით მოწამვლისა და ზოგიერთი ფერმენტის დროს.
ჰემოლიზატების ელექტროფორეზული გამოყოფა ქაღალდზე ან ცელულოზის აცეტატზე ხშირად არ იძლევა შედეგს, რადგან ბევრ არასტაბილურ ჰემოლიზატში მოლეკულაში ამინომჟავების ნარჩენების ჩანაცვლება არ ცვლის მოლეკულის ელექტროფორეზულ თვისებებს. ამ მხრივ უფრო ინფორმაციულია ელექტროფორეზი პოლიაკრილამიდის და სახამებლის გელებში (იხ. ელექტროფორეზი) ან იზოელექტრული ფოკუსირება.
ბევრ პაციენტში, რომლებიც არიან არასტაბილური გ.-ის მატარებლები, შარდი მუდმივად ან ზოგჯერ იძენს მუქ ფერს დიპიროლის წარმოქმნის გამო, რაც საკმაოდ ზუსტ ნიშანს წარმოადგენს ერითროციტებში არასტაბილური გ.-ს არსებობის შესახებ.
ბიბლიოგრაფია: Vladimirov G. E. and Panteleeva N. S. Functional biochemistry, L., 1965; და r და L. I. ჰემოგლობინები და მათი თვისებები, M., 1975, ბიბლიოგრ.; Korzhuev P. A. Hemoglobin, M., 1964, ბიბლიოგრ.; კუშაკოვსკი M. S. ჰემოგლობინის დაზიანების კლინიკური ფორმები, L., 1968; Peru TC M. Hemoglobin molecule, წიგნში: Molecules and Cell, ed. G. M. Frank, მთარგმნ. ინგლისურიდან, გვ. 7, მ., 1966; თ უ-მ და ნ შესახებ ა.კ.-ში მატერიალური მტკიცებულების სასამართლო სამედიცინო ექსპერტიზის საფუძვლები, მ., 1975 წ., ბიბლიოგრ. Uspenskaya V.D. ჰაპტოგლობინის სინთეზისა და კატაბოლიზმის ადგილის შესახებ და მისი როლი ჰემოგლობინის მეტაბოლიზმში, Vopr. თაფლი. ქიმია, ტ. 16, №3, გვ. 227, 1970, ბიბლიოგრ.; ჰარის გ. ადამიანის ბიოქიმიური გენეტიკის საფუძვლები, ტრანს. ინგლისურიდან, გვ. 15, მ., 1973; Sharonov Yu. და Sharonova N. A. ჰემოგლობინის სტრუქტურა და ფუნქციები, მოლეკულური ბიოლ. 145, 1975, ბიბლიოგრ.; C h a g a c h e S. ჰემოგლობინები შეცვლილი ჟანგბადის აფინურობით, Clin. ჰემატ., ვ. 3, გვ. 357, 1974, ბიბლიოგრ.; Giblett E. R. გენეტიკური მარკერები ადამიანის სისხლში, ფილადელფია, 1969; ჰემოგლობინის და წითელი უჯრედების სტრუქტურა და ფუნქცია, ed. G. J. Brewer, N. Y.-L., 1972; HuehnsE. R. ჰემოგლობინის ალფა-ჯაჭვის სინთეზის გენეტიკური კონტროლი, ჰემატოლოგია, ვ. 8, გვ. 61, 1974, ბიბლიოგრ.; Leh-mannH. ა. Hunt s m a n R. G. Man's hemoglobins, ფილადელფია, 1974; P e-r u t z M. F. The croonian lecture, 1968, The hemoglobin molecule, Proc, roy, Soc. ვ., ვ. 173, გვ. 113, 1969; P e rut z M. F* a. Lehmann H. ადამიანის ჰემოგლობინის მოლეკულური პათოლოგია, ბუნება (ლონდონი), ვ. 219, გვ. 902, 1968; RoughtonF. J. ზოგიერთი ბოლოდროინდელი ნაშრომი ჟანგბადის, ნახშირორჟანგის და ჰემოგლობინის ურთიერთქმედების შესახებ, Biochem. ჯ., ვ. 117, გვ. 801, 1970; ს ტ ა მ ა-ტოიანნოპონლოს გ ა. NuteP. E. ჰემოგლობინის გენეტიკური კონტროლი, კლინ. ჰემატ., ვ. 3, გვ. 251, 1974, ბიბლიოგრ.; Van Assendelft O. W. ჰემოგლობინის წარმოებულების სპექტროფოტომეტრია, Assen, 1970; Weatherall D. J. მოლეკულური საფუძველი ჰემოგლობინის ზოგიერთი დარღვევისთვის, ბრიტანული, მედ. ჯ., ვ. 4, გვ. 451, 516, 1974; ამინდი D. J. a. Clegg J. B. თალასემიის მოლეკულური საფუძველი, ბრიტ. J. Haemat., v. 31, მიწოდება, გვ. 133, 1975; Wintro-b e M. M. კლინიკური ჰემატოლოგია, ფილადელფია, 1974 წ.
ჰემოგლობინი არასტაბილურია- დიდკოვსკი N.A. et al. Hemoglobin Volga ft 27 (B9) alanine->aspartic acid (ახალი არანორმალური ჰემოგლობინი მძიმე არასტაბილურობით), პრობლემები, ჰემატოლი და გადინება, სისხლი, ტ. 30, 1977, ბიბლიოგრ.; I d e l l-s o n L. I., Didkovsky N. A. and Ermilchenko G. V. Hemolytic anemias, M., 1975, bibliogr.; In u n n H. F., დაივიწყე B. G. a. R a n n e y H. M. Human hemoglobins, Philadelphia, 1977, ბიბლიოგრ.; ლემანი ჰ.ა. K y-n o h P. A. ადამიანის ჰემოგლობინის ვარიანტები და მათი მახასიათებლები, ამსტერდამი, 1976 წ.
ა.პ. ანდრეევა; იუ ნ.ტოკარევი (ძვირფასი ქვები და გენი), ა.კ.ტუმანოვი (სასამართლო); იუ ნ.ტოკარევი, ვ.მ.ბელოსტოსკი.
ქიმიის ძირითადი ცნებები და კანონები.
მოლური მასა, ნივთიერების რაოდენობა, ავოგადროს მუდმივი.
გაზის მოლური მოცულობა.
I. ნივთიერების სტრუქტურული ერთეულის მასის გამოთვლა.
განსაზღვრეთ წყალბადის ატომების რაოდენობა 9 გ წყლის ნიმუშში.
M(H2O) = 18 გ\მოლ
n(H2O) = 9/18= 0,5 მოლი
ფორმულიდან გამომდინარეობს, რომ 1 მოლი H2O შეიცავს 2 მოლ წყალბადის ატომს, ე.ი. n(H) = 2×0,5 მოლი = 1 მოლი.
განსაზღვრეთ წყალბადის ატომების რაოდენობა ამონიუმის წყალბადოფოსფატის 26,4 გ ნიმუშში.
M(NH4)2HPO4 = 132 გ\მოლ
n((NH4)2HPO4) = 26.4/132= 0.2 მოლი
n(H) =0.2×9= 1.8 მოლი
პასუხი: 1,8 მოლი
ნარევი შედგება ეთანოლის C2H5OH მასით 46 გ და წყლის მასის 72 გ. განსაზღვრეთ ნარევში ჟანგბადის ატომების რაოდენობა.
n(C2H5OH) = 46/46 = 0.1 მოლი n(O) =0.1×1= 0.1 მოლი
n(H2O) =72/18 = 0.4 მოლი n(O) =0.4×1= 0.4 მოლი n(O) =0.1+0.4=0.5 მოლი
ნარევი შედგება ძმარმჟავას CH3COOH მასით 6 გ და ჭიანჭველა მჟავა HCOOH წონით 9.2 გ. განსაზღვრეთ ნარევში ჟანგბადის ატომების რაოდენობა.
n(CH3COOH) =6 /60 = 0,1 მოლი n(O) =0,1×2= 0,2 მოლი
n(HCOOH) =9,2/46 = 0,2 მოლი n(O) =0,2×2= 0,4 მოლი n(O) =0,2+0,4=0,6 მოლი
განსაზღვრეთ წყლის ნიმუშის მასა, რომელიც შეიცავს 12,04 1022 წყლის მოლეკულას.
n(H2O) = NNA= 12.04∙10226.02∙1023=0.2 მოლი
m(H2O) = 0,2×18= 3,6 გ
განსაზღვრეთ სპილენძის სულფატის ნიმუშის მასა, რომელიც შეიცავს 6,021022 სპილენძის ატომს.
პასუხი: 16
გამოთვალეთ ამონიუმის სულფატის ნიმუშის მასა, რომელიც შეიცავს 3,011022 წყალბადის ატომს.
n(H) =NNA=3.0110226.02∙1023=0.05 მოლი
ნაერთში არის 8 ჟანგბადის ატომი
n(NH4)2SO4 = 0.05 /8 = 0.00625 მოლი
მ = 0,00625 × 132 გ\მოლი = 0,825 გ.
განსაზღვრეთ მაგნიუმის წყალბადის სულფატის ნიმუშის მასა, თუ ცნობილია, რომ იგი შეიცავს 3,6121023 ჟანგბადის ატომს.
n(O) =NNA = 3.612×10236.02×1023=0.6 მოლი
n Mg(HSO4)2 = 0.6/8= 0.075 მოლი
მ = 0,075×218= 16,35 გ
განსაზღვრეთ ნატრიუმის სულფატის ხსნარის მასა წყალში, რომელიც შეიცავს 30,1 1022 ნატრიუმის ატომს და 6,021024 წყალბადის ატომს.
n (Na) =NNA =30.1∙10226.02∙1023=0.5 მოლი
ფორმულა შეიცავს 2 ნატრიუმის ატომს, შესაბამისად: n(Na2SO4) = 0.5/2 = 0.25 მოლი
მ ნივთიერება (Na2SO4) = 0,25 × 142 გ\მოლი = 35,5 გ
n(H) =NNA= 6.02∙10246.02∙1023=10 მოლი
n(H2O) = 10/2=5 მოლი
m(H2O) =5×18=90 გ
m ხსნარი = m ნივთიერება (Na2 SO4) + m (H2O) = 35,5 + 90 = 125,5 გ.
განსაზღვრეთ ეთანოლის C2H5OH ხსნარის მასა წყალში, რომელიც შეიცავს 12,04 1022 ნახშირბადის ატომს და 24,08 1022 ჟანგბადის ატომს.
n (C) =NNA= 12.04∙10226.02∙1023=0.2 მოლი
n (C2H5OH) = 0,2/2 = 0,1 მოლი
m(C2H5OH) = 0.1 ×46 = 4.6 გ
n(O) =NNA =2.405∙10236.02∙1023=0.4 მოლი
n(H2O) =0.4/1=0.4 მოლი
m(H2O) =0,4×18= 7,2 გ
msolution = m ნივთიერება + m(H2O) = 4,6 + 7,2 = 11,8 გ
გამოთვალეთ ერთი ნატრიუმის ატომის მასა.
ma= M (Na) / NA = 23/ 6.021023 = 3.8210-23 გ.
იპოვეთ კალციუმის სამი ატომის მასა.
ma=3 M (Ca) / NA = (3×40) / 6.021023 = 19.910-23 გ
გამოთვალეთ 7 წყლის მოლეკულის მასა.
ma=7 M (H2O) / NA = (7×18) / 6.021023 = 20.910-23 გ
განსაზღვრეთ ერთი SO3 მოლეკულის მასა
ma= M (SO3) / NA = 80 /6.021023 = 13.3 10-23 გ
გამოთვალეთ სილიციუმის(IV) ოქსიდის ხუთი ფორმულის ერთეულის მასა (გრებში).
mfe=5×Mr×u=5×60×1,66∙10-27=4,98∙10-22 გ.
გამოთვალეთ მასა:
ნატრიუმის ატომი (გ)
ma= M (Na) / NA = 23/ 6.021023 = 3.8210-23 გ
ma=ArNa×u=23×1,6610-27 = 3,8210-23 გ
თეთრი ფოსფორის P4 (კგ) ხუთი მოლეკულა
პასუხი: 1,02910-24 კგ
რომბის გოგირდის ათი მოლეკულა S8 (გ)
პასუხი: 4,2510-21 გ
ოზონის სამი მოლეკულა O3 (ამუში)
ma=3×16×3×a.u.m=144a.u.m.
ფულერენის მოლეკულები C60 (მგ)
მმ = Mr(C60)×u = 1195,210-27 = 1,19510-24 კგ = 1,19510-21 გ = 1,195 10-18 მგ
კოფეინის სამი მოლეკულა С8Н10O2N4(კგ)
პასუხი: 9,6610-25 კგ
ამონიუმის კატიონი (გ)
ma=Mr(NH4+)×u = 18×1,6610-27 = 2,9910-23 გ
ანიონი SO42-(გ)
პასუხი: 1,5910-22 გ.
ჰემოგლობინის მოლეკულები С2954H4516N780O806S12Fe4 (მგ)
პასუხი: 1,0710-16 მგ
ნატრიუმის ქლორიდის ფორმულის ერთეული (გ)
კალიუმის ჰიდროქსიდის ექვსი ფორმულის ერთეული (კგ)
ბარიუმის ოქსიდის სამი ფორმულის ერთეული (გ)
გოგირდის მოლეკულის მასა უდრის რვა ჟანგბადის ატომის მასას. რამდენი გოგირდის ატომია მის მოლეკულაში?
maO=(8×16)×1.6610-27=2.12∙10-26 გ
მოდით წარმოვიდგინოთ მოლეკულის შემადგენლობა, როგორც Sx
X = ატომის მმოლეკულები = 2,12∙10-26Ar∙u = 2,12∙10-2632×1,66∙10-27 = 4 ატომი
რამდენჯერ არის საქაროზის მოლეკულის C12H22O11 მასა მეტი თეთრი ფოსფორის P4 მოლეკულის მასაზე (პასუხი: 2,76-ჯერ)
მეთანის CH4-ისა და ჟანგბადის ნიმუშები შეიცავს მოლეკულების ერთსა და იმავე რაოდენობას. იპოვეთ ჟანგბადის მასის შეფარდება მეთანის მასასთან (პასუხი: 2)
მაგნიუმის ნიმუშს აქვს სამჯერ მეტი ნახშირბადის ატომების რაოდენობა ალმასში. გამოთვალეთ მაგნიუმის ნიმუშის მასის თანაფარდობა ალმასის ნიმუშის მასასთან (პასუხი: 6)
II. გამოთვლები ნივთიერების ქიმიური რაოდენობის ცნების გამოყენებით.
გამოთვალეთ ქიმიური რაოდენობა:
წყალბადი 3,01 1024 H2 მოლეკულის შემცველ ნაწილში
n (H2) =NNA=3.01∙10246.02∙1023=5 მოლი
აზოტი 5,6 დმ3 პორციაში (პასუხი: 0,25 მოლი)
ნატრიუმის სულფატი 14,2 გ მასის ნიმუშში (პასუხი: 0,1 მოლი)
ნივთიერების მოლეკულის მასა არის 1,0610-22 გ გამოთვალეთ ნივთიერების მოლური მასა.
M= ma×NA=1.06∙10-22×6.02∙1023=64 გ\მოლი
განსაზღვრეთ მოლეკულების რაოდენობა ნივთიერებების მითითებულ ნაწილებში:
3.25 მოლი O2 (პასუხი: 1.961024)
11,5 მოლი H2 (პასუხი: 6,921024)
40 მოლი NH3 (პასუხი: 2.411025)
0.0125 მოლი H2O (პასუხი: 7.521021)
გამოთვალეთ ქიმიური რაოდენობა ნივთიერებების მითითებულ ნაწილებში:
3.921023 O2 მოლეკულები (პასუხი: 0.651 მოლი)
14,7 1024 არგონის ატომები (პასუხი: 24,4 მოლი)
2.451023 ფორმულის ერთეული Na3PO4 (პასუხი: 0.407 მოლი)
17.34 1024 H2SO4 მოლეკულები (პასუხი: 28.8 მოლი)
გამოთვალეთ ქიმიური რაოდენობა ნივთიერებების მითითებულ ნაწილებზე:
5,6 დმ3 ჰელიუმი (პასუხი: 0,25 მოლი)
1.12 dm3SO2 (პასუხი: 0.05 მოლი)
5 მ3 NH3 (პასუხი: 2.23102 მოლი)
300 სმ3 HCl (პასუხი: 1.3410-2 მოლი)
განსაზღვრეთ ნივთიერებების მითითებული ნაწილების მოცულობა:
3.2 მოლი H2S (დმ3) (პასუხი: 71.7 დმ3)
0,05 მოლი CH4 (სმ3) (პასუხი: 1120 სმ3)
300 მოლი O2 (მ3) (პასუხი: 6,72 მ3)
1,14 მოლი არგონი (დმ3) (პასუხი: 25,5 დმ3)
გამოთვალეთ აზოტის ნაწილის მოცულობა (დმ3), რომელიც შეიცავს 1,12 1023 მოლეკულას.
n(H2) =NNA= 1.12∙10236.02∙1023=0.18 მოლი
V (H2) = 0,18×22,4 = 4 დმ3
გამოთვალეთ ჟანგბადის 2 კგ ნაწილის მოცულობა (პასუხი: 1400 დმ3)
გამოთვალეთ მოლეკულების რაოდენობა ამიაკის პორციაში 3,45 დმ3 მოცულობით (პასუხი: 9,271022)
გამოთვალეთ ამიაკის ნაწილის მასა, რომელიც შეიცავს 5,43 1024 მოლეკულას. (პასუხი: 153 გ).
გარდა იმისა, რომ დასამახსოვრებელია, .com დომენები უნიკალურია: ეს არის ერთ-ერთი და ერთადერთი .com სახელი. სხვა გაფართოებები, როგორც წესი, უბრალოდ მიჰყავს ტრაფიკი მათი .com კოლეგებისკენ. Premium .com დომენის შეფასების შესახებ მეტის გასაგებად, უყურეთ ქვემოთ მოცემულ ვიდეოს:
ტურბოდამუხტეთ თქვენი ვებ გვერდი. უყურეთ ჩვენს ვიდეოს, რომ გაიგოთ როგორ.
გააუმჯობესეთ თქვენი ვებ-ყოფნა
მიაქციეთ ყურადღება ინტერნეტში დიდი დომენის სახელით
ინტერნეტში რეგისტრირებული ყველა დომენის 73% არის .coms. მიზეზი მარტივია: .com არის ადგილი, სადაც ხდება ვებ ტრაფიკის უმეტესი ნაწილი. Premium .com-ის ფლობა გაძლევთ დიდ სარგებელს, მათ შორის უკეთესი SEO, სახელის ამოცნობა და თქვენი საიტის ავტორიტეტის გრძნობის უზრუნველყოფა.
აი რას ამბობენ სხვები
2005 წლიდან ჩვენ დავეხმარეთ ათასობით ადამიანს, მიიღონ სრულყოფილი დომენის სახელი
- ტელეფონით ველაპარაკე რაიანს და ის დამეხმარა ყველა კითხვაში! შესანიშნავი მომხმარებლის მომსახურება და ადვილად ხელმისაწვდომი. პროცესი მარტივი და შედარებით სწრაფი იყო, მხოლოდ სამი სამუშაო დღის განმავლობაში მიმდინარეობდა. უაღრესად გირჩევთ მათ, ვინც განიხილავს დომენის შეძენას largedomains.com-დან. ჩაერთვება მესამე მხარე სახელად namebright.com, მაგრამ დამატებითი გადასახადი არ არის და ისინი ხელს უწყობენ დომენების გადაცემას სევერებიდან. Გაუმარჯოს - სემი ლამი, 14/10/2019
- გულწრფელად რომ გითხრათ, სანამ დომენს ვიყიდიდი HugeDomains.com-დან, ძალიან შემეშინდა, რადგან წავიკითხე უარყოფითი მიმოხილვა ზოგიერთ ვებსაიტზე.. მაგრამ გადავწყვიტე გამომეყენებინა შანსი. შეძენის შემდეგ გამიკვირდა, წარმოუდგენელი იყო, რომ ჩემი დომენის სახელის შეძენა წარმატებული იყო და საუკეთესო ნაწილი იყო ის, რომ მე გადავეცი სხვა რეგისტრატორს და ისევ hugggggeeeee სიურპრიზი, რადგან ჩემი დომენის სახელი გადაიცემა 30 წუთში.. შეძენიდან გადაცემამდე გატარებული მთლიანი დრო იყო ნაკლები 2 საათი.... ძალიან დიდი მადლობა HugeDomain.com-სა და NameBright.com-ს - სანდიპ რაჯპუტი, 14/10/2019
- სწრაფი და შეუფერხებელი გარიგება და გადაცემა. შეგიძლიათ გირჩიოთ! - ტომი, 12/10/2019
- მეტი