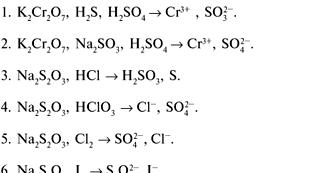តារាងរូបមន្តគីមីវិទ្យា និងឈ្មោះរបស់វា។ រូបមន្តគីមីនៃសារធាតុ។ ឧទាហរណ៍នៃការដោះស្រាយបញ្ហា
២.១. ភាសាគីមីនិងផ្នែករបស់វា។
មនុស្សជាតិប្រើភាសាផ្សេងៗគ្នាជាច្រើន។ លើកលែងតែ ភាសាធម្មជាតិ(ជប៉ុន អង់គ្លេស រុស្សី - សរុបជាង ២,៥ពាន់នាក់) ក៏មានដែរ។ ភាសាសិប្បនិម្មិតឧទាហរណ៍ Esperanto ។ ក្នុងចំណោមភាសាសិប្បនិម្មិតមាន ភាសាផ្សេងៗ វិទ្យាសាស្ត្រ. ដូច្នេះនៅក្នុងគីមីវិទ្យាពួកគេប្រើរបស់ពួកគេផ្ទាល់។ ភាសាគីមី.
ភាសាគីមី- ប្រព័ន្ធនៃនិមិត្តសញ្ញា និងគំនិតដែលបានរចនាឡើងសម្រាប់ការកត់ត្រា និងការបញ្ជូនព័ត៌មានគីមីដោយសង្ខេប សង្ខេប និងមើលឃើញ។
សារដែលសរសេរជាភាសាធម្មជាតិភាគច្រើនត្រូវបានបែងចែកទៅជាប្រយោគ ប្រយោគទៅជាពាក្យ និងពាក្យទៅជាអក្សរ។ ប្រសិនបើយើងហៅប្រយោគ ពាក្យ និងអក្សរជាផ្នែកនៃភាសា នោះយើងអាចសម្គាល់ផ្នែកស្រដៀងគ្នាជាភាសាគីមី (តារាងទី 2)។
តារាង 2 ។ផ្នែក ភាសាគីមី
វាមិនអាចទៅរួចទេក្នុងការធ្វើជាម្ចាស់ភាសាណាមួយភ្លាមៗ នេះក៏អនុវត្តចំពោះភាសាគីមីផងដែរ។ ដូច្នេះហើយ សម្រាប់ពេលនេះ អ្នកនឹងស្គាល់តែមូលដ្ឋានគ្រឹះនៃភាសានេះប៉ុណ្ណោះ៖ រៀន "អក្សរ" មួយចំនួន រៀនយល់ពីអត្ថន័យនៃ "ពាក្យ" និង "ប្រយោគ"។ នៅចុងបញ្ចប់នៃជំពូកនេះ អ្នកនឹងត្រូវបានណែនាំ ឈ្មោះសារធាតុគីមីគឺជាផ្នែកសំខាន់មួយនៃភាសាគីមី។ នៅពេលអ្នកសិក្សាគីមីវិទ្យា ចំណេះដឹងរបស់អ្នកអំពីភាសាគីមីនឹងពង្រីក និងស៊ីជម្រៅ។
ភាសាគីមី។
1. តើអ្នកដឹងភាសាសិប្បនិម្មិតអ្វីខ្លះ (ក្រៅពីអ្វីដែលបានរៀបរាប់នៅក្នុងអត្ថបទនៃសៀវភៅសិក្សា)?
២.តើភាសាធម្មជាតិខុសពីភាសាសិប្បនិមិត្តយ៉ាងណា?
3. តើអ្នកគិតថាវាអាចទៅរួចទេក្នុងការពិពណ៌នាអំពីបាតុភូតគីមីដោយមិនប្រើភាសាគីមី? បើមិនដូច្នេះទេ? បើដូច្នេះ តើអ្វីទៅជាគុណសម្បត្តិ និងគុណវិបត្តិនៃការពិពណ៌នាបែបនេះ?
២.២. និមិត្តសញ្ញាធាតុគីមី
និមិត្តសញ្ញាសម្រាប់ធាតុគីមី តំណាងឱ្យធាតុខ្លួនវា ឬអាតូមមួយនៃធាតុនោះ។
និមិត្តសញ្ញានីមួយៗគឺជាឈ្មោះអក្សរកាត់ឡាតាំងនៃធាតុគីមី ដែលមានអក្សរមួយ ឬពីរនៃអក្ខរក្រមឡាតាំង (សម្រាប់អក្ខរក្រមឡាតាំង សូមមើលឧបសម្ព័ន្ធទី 1)។ និមិត្តសញ្ញាត្រូវបានសរសេរដោយអក្សរធំ។ និមិត្តសញ្ញា ក៏ដូចជាឈ្មោះរុស្ស៊ី និងឡាតាំងនៃធាតុមួយចំនួនត្រូវបានផ្តល់ឱ្យក្នុងតារាងទី 3 ។ ព័ត៌មានអំពីប្រភពដើមនៃឈ្មោះឡាតាំងក៏ត្រូវបានផ្តល់ឱ្យនៅទីនោះផងដែរ។ ក្បួនទូទៅមិនមានការបញ្ចេញសំឡេងនៃនិមិត្តសញ្ញាទេ ដូច្នេះតារាងទី 3 ក៏បង្ហាញ "ការអាន" នៃនិមិត្តសញ្ញា នោះគឺជារបៀបដែលនិមិត្តសញ្ញានេះត្រូវបានអាននៅក្នុងរូបមន្តគីមី។
វាមិនអាចទៅរួចទេក្នុងការជំនួសឈ្មោះរបស់ធាតុដោយនិមិត្តសញ្ញានៅក្នុងការនិយាយផ្ទាល់មាត់ ប៉ុន្តែនៅក្នុងអត្ថបទដែលសរសេរដោយដៃ ឬបោះពុម្ព វាត្រូវបានអនុញ្ញាត ប៉ុន្តែមិនត្រូវបានណែនាំទេ បច្ចុប្បន្ន 110 ធាតុគីមីមាន 109 ឈ្មោះ និងនិមិត្តសញ្ញាដែលត្រូវបានអនុម័តដោយសហភាពអន្តរជាតិនៃគីមីវិទ្យាបរិសុទ្ធ និងអនុវត្ត (IUPAC)។
តារាងទី 3 ផ្តល់ព័ត៌មានអំពីធាតុ 33 ប៉ុណ្ណោះ។ ទាំងនេះគឺជាធាតុដែលអ្នកនឹងជួបប្រទះដំបូងនៅពេលសិក្សាគីមីវិទ្យា។ ឈ្មោះរុស្ស៊ី (តាមលំដាប់អក្ខរក្រម) និងនិមិត្តសញ្ញានៃធាតុទាំងអស់ត្រូវបានផ្តល់ឱ្យនៅក្នុងឧបសម្ព័ន្ធទី 2 ។
តារាងទី 3 ។ឈ្មោះ និងនិមិត្តសញ្ញានៃធាតុគីមីមួយចំនួន
ឈ្មោះ |
||||
ឡាតាំង |
ការសរសេរ |
|||
| - | ការសរសេរ |
ប្រភពដើម |
- | - |
| អាសូត | នអ៊ីដ្រូសែន | មកពីភាសាក្រិច "ផ្តល់កំណើតឱ្យអំបិល" | "en" | |
| អាលុយមីញ៉ូម | អាល់អ៊ុយមីញ៉ូម | ពីឡាតាំង។ "អាលុម" | "អាលុយមីញ៉ូម" | |
| អាហ្គុន | អាហ្គុន | មកពីភាសាក្រិច "អសកម្ម" | "អាហ្គុន" | |
| បារីយ៉ូម | បារីម | មកពីភាសាក្រិច "ធ្ងន់" | "បារីយ៉ូម" | |
| បូ | ខ orum | ពីភាសាអារ៉ាប់ "រ៉ែពណ៌ស" | "បូរុន" | |
| ប្រូមីន | Brអ៊ុំ | មកពីភាសាក្រិច "ក្លិន" | "ប្រូមីន" | |
| អ៊ីដ្រូសែន | ហអ៊ីដ្រូសែន | មកពីភាសាក្រិច "ផ្តល់កំណើតឱ្យទឹក" | "ផេះ" | |
| អេលីយ៉ូម | គាត់ lium | មកពីភាសាក្រិច "ព្រះអាទិត្យ" | "អេលីយ៉ូម" | |
| ជាតិដែក | ហ្វេរុម | ពីឡាតាំង។ "ដាវ" | "ferrum" | |
| មាស | អ rum | ពីឡាតាំង។ "ដុត" | "អូរ៉ុម" | |
| អ៊ីយ៉ូត | ខ្ញុំអូដុម | មកពីភាសាក្រិច "វីយូឡុង" | "អ៊ីយ៉ូត" | |
| ប៉ូតាស្យូម | ខេអាលយូម | ពីភាសាអារ៉ាប់ "លី" | "ប៉ូតាស្យូម" | |
| កាល់ស្យូម | Caជាតិកាល់ស្យូម | ពីឡាតាំង។ "ថ្មកំបោរ" | "កាល់ស្យូម" | |
| អុកស៊ីហ្សែន | អូ xygenium | មកពីភាសាក្រិច "ការបង្កើតអាស៊ីត" | "អូ" | |
| ស៊ីលីកុន | ស៊ីលីស្យូម | ពីឡាតាំង។ "flint" | "ស៊ីលីស្យូម" | |
| គ្រីបតុន | Kr ypton | មកពីភាសាក្រិច "លាក់" | "គ្រីបតុន" | |
| ម៉ាញ៉េស្យូម | មក gនីស្យូម | ពីឈ្មោះ ឧបទ្វីប Magnesia | "ម៉ាញេស្យូម" | |
| ម៉ង់ហ្គាណែស | មក ន ganum | មកពីភាសាក្រិច "សម្អាត" | "ម៉ង់ហ្គាណែស" | |
| ស្ពាន់ | គព្រំ | មកពីភាសាក្រិច ឈ្មោះ អូ ស៊ីប | "ពែង" | |
| សូដ្យូម | ណាជ័យជំនះ | មកពីភាសាអារ៉ាប់ "សាប៊ូបោកខោអាវ" | "សូដ្យូម" | |
| អ៊ីយូន | ណនៅលើ | មកពីភាសាក្រិច "ថ្មី" | "អ៊ីយូតា" | |
| នីកែល | នី ccolum | ពីគាត់។ "ផ្លូវនីកូឡាស្ពាន់" | "នីកែល" | |
| បារត | ហអ៊ីដ្រារ g yrum | ឡាត "ប្រាក់រាវ" | "hydrargyrum" | |
| នាំមុខ | ទំ lum ខអ៊ុំ | ពីឡាតាំង។ ឈ្មោះនៃលោហៈធាតុដែក និងសំណប៉ាហាំង។ | "បំពង់ទឹក" | |
| ស្ពាន់ធ័រ | ស ulfur | មកពីសំស្ក្រឹត "ម្សៅដែលអាចឆេះបាន" | "es" | |
| ប្រាក់ | ក r g entum | មកពីភាសាក្រិច "ពន្លឺ" | "អាហ្សង់ទីន" | |
| កាបូន | គ arboneum | ពីឡាតាំង។ "ធ្យូងថ្ម" | "tse" | |
| ផូស្វ័រ | ទំ hosphorus | មកពីភាសាក្រិច "អ្នកនាំពន្លឺ" | "peh" | |
| ហ្វ្លុយអូរីន | ចលូរ៉ុម | ពីឡាតាំង។ កិរិយាស័ព្ទ "ហូរ" | "ហ្វ្លុយអូរីន" | |
| ក្លរីន | Cl orum | មកពីភាសាក្រិច "បៃតង" | "ក្លរីន" | |
| ក្រូមីញ៉ូម | គ h rអូមីញ៉ូម | មកពីភាសាក្រិច "លាបពណ៌" | "ក្រូម" | |
| សេស្យូម | គអេ សអ៊ីយ៉ូម | ពីឡាតាំង។ "មេឃខៀវ" | "ស៊ីស្យូម" | |
| ស័ង្កសី | Zខ្ញុំ ន cum | ពីគាត់។ "សំណប៉ាហាំង" | "ស័ង្កសី" | |
២.៣. រូបមន្តគីមី
ដើម្បីកំណត់សារធាតុគីមីដែលពួកគេប្រើ រូបមន្តគីមី.
ចំពោះសារធាតុម៉ូលេគុល រូបមន្តគីមីអាចសម្គាល់ម៉ូលេគុលមួយនៃសារធាតុនេះ។
ព័ត៌មានអំពីសារធាតុអាចខុសគ្នា ដូច្នេះមានភាពខុសគ្នា។ ប្រភេទនៃរូបមន្តគីមី.
ដោយផ្អែកលើភាពពេញលេញនៃព័ត៌មាន រូបមន្តគីមីត្រូវបានបែងចែកជាបួនប្រភេទសំខាន់ៗ៖ ប្រូតូហ្សូ,
ម៉ូលេគុល, រចនាសម្ព័ន្ធនិង លំហ.
Subscripts នៅក្នុងរូបមន្តសាមញ្ញបំផុតមិនមានការបែងចែកទូទៅទេ។
លិបិក្រម "1" មិនត្រូវបានប្រើក្នុងរូបមន្តទេ។
ឧទាហរណ៍នៃរូបមន្តសាមញ្ញបំផុត៖ ទឹក - H 2 O, អុកស៊ីសែន - O, ស្ពាន់ធ័រ - S, ផូស្វ័រអុកស៊ីដ - P 2 O 5, butane - C 2 H 5, អាស៊ីតផូស្វ័រ - H 3 PO 4, សូដ្យូមក្លរួ (អំបិលតុ) - NaCl
រូបមន្តសាមញ្ញបំផុតនៃទឹក (H 2 O) បង្ហាញថាសមាសធាតុទឹករួមបញ្ចូលធាតុ អ៊ីដ្រូសែន(H) និងធាតុ អុកស៊ីសែន(O) ហើយនៅក្នុងផ្នែកណាមួយ (ផ្នែកមួយគឺជាផ្នែកនៃអ្វីមួយដែលអាចបែងចែកដោយមិនបាត់បង់លក្ខណៈសម្បត្តិរបស់វា។) នៃទឹក ចំនួនអាតូមអ៊ីដ្រូសែនគឺពីរដងនៃចំនួនអាតូមអុកស៊ីសែន។
ចំនួនភាគល្អិតរួមទាំង ចំនួនអាតូមតំណាងដោយអក្សរឡាតាំង ន. កំណត់ចំនួនអាតូមអ៊ីដ្រូសែន - ន H និងចំនួនអាតូមអុកស៊ីសែនគឺ នអូ យើងអាចសរសេរវាបាន
ឬ ន H: ន O=2:1។
រូបមន្តសាមញ្ញបំផុតនៃអាស៊ីតផូស្វ័រ (H 3 PO 4) បង្ហាញថាអាស៊ីតផូស្វ័រមានអាតូម អ៊ីដ្រូសែន, អាតូម ផូស្វ័រនិងអាតូម អុកស៊ីសែនហើយសមាមាត្រនៃចំនួនអាតូមនៃធាតុទាំងនេះនៅក្នុងផ្នែកណាមួយនៃអាស៊ីតផូស្វ័រគឺ 3: 1: 4 នោះគឺ
NH៖ នទំ៖ ន O=3:1:4។

រូបមន្តសាមញ្ញបំផុតអាចត្រូវបានចងក្រងសម្រាប់បុគ្គលណាមួយ។ សារធាតុគីមី, និងសម្រាប់ សារធាតុម៉ូលេគុលលើសពីនេះទៀតអាចត្រូវបានចងក្រង រូបមន្តម៉ូលេគុល.
ឧទាហរណ៍នៃរូបមន្តម៉ូលេគុល៖ ទឹក - H 2 O, អុកស៊ីសែន - O 2, ស្ពាន់ធ័រ - S 8, ផូស្វ័រអុកស៊ីដ - P 4 O 10, butane - C 4 H 10, អាស៊ីតផូស្វ័រ - H 3 PO 4 ។
សារធាតុដែលមិនមែនជាម៉ូលេគុល មិនមានរូបមន្តម៉ូលេគុលទេ។
លំដាប់នៃការសរសេរនិមិត្តសញ្ញាធាតុនៅក្នុងរូបមន្តសាមញ្ញ និងម៉ូលេគុលត្រូវបានកំណត់ដោយច្បាប់នៃភាសាគីមី ដែលអ្នកនឹងស្គាល់នៅពេលអ្នកសិក្សាគីមីវិទ្យា។ ព័ត៌មានដែលបង្ហាញដោយរូបមន្តទាំងនេះមិនត្រូវបានប៉ះពាល់ដោយលំដាប់នៃនិមិត្តសញ្ញាទេ។
ក្នុងចំណោមសញ្ញាដែលឆ្លុះបញ្ចាំងពីរចនាសម្ព័ន្ធនៃសារធាតុ យើងនឹងប្រើសម្រាប់ពេលនេះប៉ុណ្ណោះ។ valence stroke("សញ្ញា") ។ សញ្ញានេះបង្ហាញពីវត្តមានរវាងអាតូមនៃអ្វីដែលគេហៅថា សម្ព័ន្ធកូវ៉ាឡង់(តើការតភ្ជាប់ប្រភេទនេះជាអ្វី និងលក្ខណៈពិសេសរបស់វា អ្នកនឹងដឹងក្នុងពេលឆាប់ៗនេះ)។

នៅក្នុងម៉ូលេគុលទឹក អាតូមអុកស៊ីហ្សែនមួយត្រូវបានតភ្ជាប់ដោយចំណងសាមញ្ញ (តែមួយ) ទៅនឹងអាតូមអ៊ីដ្រូសែនពីរ ប៉ុន្តែអាតូមអ៊ីដ្រូសែនមិនភ្ជាប់គ្នាទៅវិញទៅមកទេ។ នេះគឺជាអ្វីដែលរូបមន្តរចនាសម្ព័ន្ធនៃទឹកបង្ហាញយ៉ាងច្បាស់។ ![]()
ឧទាហរណ៍មួយទៀត៖ ម៉ូលេគុលស្ពាន់ធ័រ S8 ។ នៅក្នុងម៉ូលេគុលនេះ អាតូមស្ពាន់ធ័រ 8 បង្កើតជារង្វង់ដែលមានសមាជិកប្រាំបី ដែលអាតូមស្ពាន់ធ័រនីមួយៗត្រូវបានភ្ជាប់ទៅអាតូមពីរផ្សេងទៀតដោយចំណងសាមញ្ញ។ ប្រៀបធៀបរូបមន្តរចនាសម្ព័ន្ធនៃស្ពាន់ធ័រជាមួយនឹងគំរូបីវិមាត្រនៃម៉ូលេគុលរបស់វាដែលបានបង្ហាញក្នុងរូបភព។ 3. សូមចំណាំថារូបមន្តរចនាសម្ព័ន្ធនៃស្ពាន់ធ័រមិនបង្ហាញពីរូបរាងនៃម៉ូលេគុលរបស់វាទេ ប៉ុន្តែបង្ហាញតែលំដាប់នៃការតភ្ជាប់អាតូមដោយចំណង covalent ។

រូបមន្តរចនាសម្ព័ន្ធនៃអាស៊ីត phosphoric បង្ហាញថានៅក្នុងម៉ូលេគុលនៃសារធាតុនេះ អាតូមអុកស៊ីសែនមួយក្នុងចំនោមអាតូមអុកស៊ីហ៊្សែនទាំងបួនត្រូវបានតភ្ជាប់ទៅអាតូមផូស្វ័រដោយចំណងទ្វេរដង ហើយអាតូមផូស្វ័រត្រូវបានភ្ជាប់ទៅអាតូមអុកស៊ីសែនបីទៀតដោយចំណងតែមួយ។ . អាតូមអុកស៊ីហ្សែនទាំងបីនេះ នីមួយៗក៏ត្រូវបានភ្ជាប់ដោយចំណងសាមញ្ញទៅនឹងអាតូមអ៊ីដ្រូសែនមួយក្នុងចំណោមអាតូមអ៊ីដ្រូសែនទាំងបីដែលមាននៅក្នុងម៉ូលេគុល។
ប្រៀបធៀបគំរូបីវិមាត្រខាងក្រោមនៃម៉ូលេគុលមេតានជាមួយនឹងរូបមន្តលំហ រចនាសម្ព័ន្ធ និងម៉ូលេគុលរបស់វា៖
|
|
|
នៅក្នុងរូបមន្តលំហនៃមេតាន ការវាយលុករាងជាក្រូចឆ្មារ ដូចជានៅក្នុងទស្សនៈ បង្ហាញថាអាតូមអ៊ីដ្រូសែនមួយណាគឺ "នៅជិតយើង" ហើយមួយណាទៀត "ពីយើង" ។
ជួនកាលរូបមន្តលំហបង្ហាញពីប្រវែងចំណង និងមុំរវាងចំណងនៅក្នុងម៉ូលេគុល ដូចដែលបានបង្ហាញក្នុងឧទាហរណ៍នៃម៉ូលេគុលទឹក។

សារធាតុដែលមិនមែនជាម៉ូលេគុលមិនមានម៉ូលេគុលទេ។ សម្រាប់ភាពងាយស្រួលនៃការអនុវត្តការគណនាគីមីនៅក្នុងសារធាតុដែលមិនមែនជាម៉ូលេគុលអ្វីដែលគេហៅថា ឯកតារូបមន្ត.
ឧទាហរណ៍នៃសមាសភាពនៃឯកតារូបមន្តនៃសារធាតុមួយចំនួន៖ 1) ស៊ីលីកុនឌីអុកស៊ីត (ខ្សាច់រ៉ែថ្មខៀវ) SiO 2 - ឯកតារូបមន្តមានអាតូមស៊ីលីកុនមួយ និងអាតូមអុកស៊ីសែនពីរ។ 2) សូដ្យូមក្លរួ (អំបិលតុ) NaCl - ឯកតារូបមន្តមានអាតូមសូដ្យូមមួយ និងអាតូមក្លរីនមួយ; 3) ជាតិដែក Fe - ឯកតារូបមន្តមានអាតូមដែកមួយ ដូចទៅនឹងម៉ូលេគុល ឯកតារូបមន្តគឺជាផ្នែកតូចបំផុតនៃសារធាតុដែលរក្សាលក្ខណៈសម្បត្តិគីមីរបស់វា។
តារាងទី 4
ព័ត៌មានបញ្ជូនដោយប្រភេទផ្សេងៗនៃរូបមន្ត
ប្រភេទរូបមន្ត |
ព័ត៌មានបញ្ជូនដោយរូបមន្ត។ |
|
| សាមញ្ញបំផុត។ ម៉ូលេគុល រចនាសម្ព័ន្ធ លំហ |
|
|
ឥឡូវនេះ ចូរយើងពិចារណា ដោយប្រើឧទាហរណ៍ តើព័ត៌មានប្រភេទណាខ្លះនៃរូបមន្តផ្តល់ឱ្យយើង។
1. សារធាតុ៖ អាស៊ីតអាសេទិច. រូបមន្តសាមញ្ញបំផុតគឺ CH 2 O រូបមន្តម៉ូលេគុលគឺ C 2 H 4 O 2 រូបមន្តរចនាសម្ព័ន្ធ

រូបមន្តសាមញ្ញបំផុត។ប្រាប់យើងថា
1) អាស៊ីតអាសេទិកមានកាបូនអ៊ីដ្រូសែននិងអុកស៊ីសែន;
2) នៅក្នុងសារធាតុនេះ ចំនួនអាតូមកាបូនទាក់ទងទៅនឹងចំនួនអាតូមអ៊ីដ្រូសែន និងចំនួនអាតូមអុកស៊ីសែន ដូចជា 1: 2: 1 នោះគឺ ន H: នគ៖ ន O = 1:2:1 ។
រូបមន្តម៉ូលេគុលបន្ថែមថា
3) នៅក្នុងម៉ូលេគុលនៃអាស៊ីតអាសេទិកមានអាតូមកាបូន 2 អាតូមអ៊ីដ្រូសែន 4 និងអាតូមអុកស៊ីសែន 2 ។
រូបមន្តរចនាសម្ព័ន្ធបន្ថែមថា
4, 5) ក្នុងម៉ូលេគុលអាតូមកាបូនពីរត្រូវបានតភ្ជាប់ទៅគ្នាទៅវិញទៅមកដោយចំណងសាមញ្ញ; មួយក្នុងចំនោមពួកវាលើសពីនេះទៀតត្រូវបានភ្ជាប់ទៅនឹងអាតូមអ៊ីដ្រូសែនបី ដែលនីមួយៗមានចំណងតែមួយ និងមួយទៀតទៅអាតូមអុកស៊ីសែនពីរ ដែលមួយមានចំណងទ្វេ និងមួយទៀតមានចំណងតែមួយ។ អាតូមអុកស៊ីសែនចុងក្រោយត្រូវបានភ្ជាប់ដោយចំណងសាមញ្ញទៅនឹងអាតូមអ៊ីដ្រូសែនទីបួន។
2. សារធាតុ៖ សូដ្យូមក្លរួ.
រូបមន្តសាមញ្ញបំផុតគឺ NaCl ។
1) សូដ្យូមក្លរួមានសូដ្យូមនិងក្លរីន។
2) នៅក្នុងសារធាតុនេះចំនួនអាតូមសូដ្យូមគឺស្មើនឹងចំនួនអាតូមក្លរីន។
3. សារធាតុ៖ ជាតិដែក.
រូបមន្តសាមញ្ញបំផុតគឺ Fe ។
១) សារធាតុនេះមានជាតិដែកតែប៉ុណ្ណោះ ពោលគឺវាជាសារធាតុសាមញ្ញ។
៤.សារធាតុ៖ អាស៊ីត trimetapphosphoric . រូបមន្តសាមញ្ញបំផុតគឺ HPO 3 រូបមន្តម៉ូលេគុលគឺ H 3 P 3 O 9 រូបមន្តរចនាសម្ព័ន្ធ

1) អាស៊ីត Trimetaphosphoric មានអ៊ីដ្រូសែន ផូស្វ័រ និងអុកស៊ីសែន។
2) ន H: នទំ៖ ន O = 1:1:3 ។
3) ម៉ូលេគុលមានអាតូមអ៊ីដ្រូសែនបី អាតូមផូស្វ័របី និងអាតូមអុកស៊ីសែនប្រាំបួន។
4, 5) អាតូមផូស្វ័របី និងអាតូមអុកស៊ីសែនបី ឆ្លាស់គ្នាបង្កើតជាវដ្ដដែលមានសមាជិកប្រាំមួយ។ ការតភ្ជាប់ទាំងអស់នៅក្នុងវដ្តគឺសាមញ្ញ។ អាតូមផូស្វ័រនីមួយៗក៏ត្រូវបានភ្ជាប់ជាមួយអាតូមអុកស៊ីហ្សែនពីរទៀតដែរ ដែលមួយមានចំណងទ្វេ និងមួយទៀតមានចំណងតែមួយ។ អាតូមអុកស៊ីសែនទាំងបីដែលតភ្ជាប់ដោយចំណងសាមញ្ញទៅនឹងអាតូមផូស្វ័រក៏ត្រូវបានភ្ជាប់ដោយចំណងសាមញ្ញទៅនឹងអាតូមអ៊ីដ្រូសែនផងដែរ។
| អាស៊ីតផូស្វ័រ - H 3 PO 4(ឈ្មោះផ្សេងទៀតគឺអាស៊ីត orthophosphoric) គឺជាសារធាតុថ្លា គ្មានពណ៌ និងគ្រីស្តាល់នៃរចនាសម្ព័ន្ធម៉ូលេគុលដែលរលាយនៅសីតុណ្ហភាព 42 អង្សាសេ។ សារធាតុនេះរលាយក្នុងទឹកបានយ៉ាងល្អ ហើយថែមទាំងស្រូបយកចំហាយទឹកពីខ្យល់ (hygroscopic)។ អាស៊ីតផូស្វ័រត្រូវបានផលិតនៅក្នុង បរិមាណដ៏ច្រើន។ហើយត្រូវបានគេប្រើជាចម្បងក្នុងការផលិតជីផូស្វាត ក៏ដូចជានៅក្នុងឧស្សាហកម្មគីមី ក្នុងការផលិតឈើគូស និងសូម្បីតែក្នុងការសាងសង់។ លើសពីនេះទៀតអាស៊ីត phosphoric ត្រូវបានគេប្រើនៅក្នុងការផលិតស៊ីម៉ងត៍នៅក្នុងបច្ចេកវិទ្យាធ្មេញហើយត្រូវបានរួមបញ្ចូលនៅក្នុងថ្នាំជាច្រើន។ អាស៊ីតនេះមានតម្លៃថោកណាស់ ដូច្នេះហើយនៅក្នុងប្រទេសមួយចំនួនដូចជាសហរដ្ឋអាមេរិក អាស៊ីតផូស្វ័រសុទ្ធដែលពនឺខ្លាំងជាមួយនឹងទឹកត្រូវបានបន្ថែមទៅក្នុងភេសជ្ជៈស្រស់ដើម្បីជំនួសអាស៊ីតនៃក្រូចឆ្មាដែលមានតំលៃថ្លៃ។ |
| មេតាន - CH ៤.ប្រសិនបើអ្នកមានចង្រ្កានហ្គាសនៅផ្ទះ នោះអ្នកជួបប្រទះសារធាតុនេះជារៀងរាល់ថ្ងៃ៖ ឧស្ម័នធម្មជាតិដែលឆេះនៅក្នុងឡដុតចង្ក្រានរបស់អ្នកមាន 95% នៃមេតាន។ មេតានគឺជាឧស្ម័នគ្មានពណ៌ និងគ្មានក្លិន ជាមួយនឹងចំណុចរំពុះនៃ -161 o C. នៅពេលដែលលាយជាមួយខ្យល់ វាគឺជាការផ្ទុះ ដែលពន្យល់ពីការផ្ទុះ និងភ្លើងដែលជួនកាលកើតឡើងនៅក្នុងអណ្តូងរ៉ែធ្យូងថ្ម (ឈ្មោះផ្សេងទៀតសម្រាប់មេតានគឺ firedamp) ។ ឈ្មោះទីបីសម្រាប់មេតាន - ឧស្ម័នវាលភក់ - គឺដោយសារតែការពិតដែលថាពពុះនៃឧស្ម័នពិសេសនេះកើនឡើងពីបាតនៃវាលភក់ដែលជាកន្លែងដែលវាត្រូវបានបង្កើតឡើងជាលទ្ធផលនៃសកម្មភាពនៃបាក់តេរីមួយចំនួន។ នៅក្នុងឧស្សាហកម្ម មេតានត្រូវបានប្រើប្រាស់ជាឥន្ធនៈ និងវត្ថុធាតុដើមសម្រាប់ផលិតសារធាតុផ្សេងទៀត មេតានគឺសាមញ្ញបំផុត។ អ៊ីដ្រូកាបូន. ថ្នាក់នៃសារធាតុនេះក៏រួមបញ្ចូលផងដែរ អេតាន (C 2 H 6), propane (C 3 H 8), អេទីឡែន (C 2 H 4), អាសេទីល (C 2 H 2) និងសារធាតុជាច្រើនទៀត។ |
តារាងទី 5.ឧទាហរណ៍នៃប្រភេទផ្សេងគ្នានៃរូបមន្តសម្រាប់សារធាតុមួយចំនួន-
វិទ្យាសាស្ត្រនីមួយៗមានប្រព័ន្ធកំណត់សំគាល់ផ្ទាល់ខ្លួន។ គីមីវិទ្យាមិនមានករណីលើកលែងក្នុងរឿងនេះទេ។ អ្នកដឹងរួចហើយថានិមិត្តសញ្ញាដែលមកពីឈ្មោះឡាតាំងនៃធាតុត្រូវបានប្រើដើម្បីកំណត់ធាតុគីមី។ ធាតុគីមីមានសមត្ថភាពបង្កើតបានទាំងសារធាតុសាមញ្ញ និងស្មុគស្មាញ ដែលសមាសភាពអាចបង្ហាញបាន។ រូបមន្តគីមី។
ដើម្បីសរសេររូបមន្តគីមីនៃសារធាតុសាមញ្ញ អ្នកត្រូវសរសេរនិមិត្តសញ្ញានៃធាតុគីមីដែលបង្កើតជាសារធាតុសាមញ្ញ ហើយសរសេរលេខនៅខាងស្តាំខាងក្រោមបង្ហាញពីចំនួនអាតូមរបស់វា។ តួលេខនេះត្រូវបានគេហៅថា សន្ទស្សន៍។
ឧទាហរណ៍រូបមន្តគីមីនៃអុកស៊ីសែនគឺ O2.លេខ 2 បន្ទាប់ពីនិមិត្តសញ្ញាអុកស៊ីហ៊្សែនគឺជាសន្ទស្សន៍ដែលបង្ហាញថាម៉ូលេគុលអុកស៊ីសែនមានអាតូមពីរនៃធាតុអុកស៊ីសែន។
សន្ទស្សន៍ - លេខបង្ហាញពីចំនួនអាតូមនៃប្រភេទជាក់លាក់មួយនៅក្នុងរូបមន្តគីមី ដើម្បីសរសេររូបមន្តគីមីនៃសារធាតុស្មុគ្រស្មាញ អ្នកត្រូវដឹងថាតើអាតូមនៃធាតុណាដែលវាមាន (សមាសភាពគុណភាព) និងចំនួនអាតូមនៃធាតុនីមួយៗ (សមាសធាតុបរិមាណ)។
ឧទាហរណ៍រូបមន្តគីមីនៃសូដាដុតនំគឺ NaHCO3 ។ សមាសភាពនៃសារធាតុនេះរួមមានអាតូមនៃសូដ្យូមអ៊ីដ្រូសែនកាបូនអុកស៊ីដ - នេះគឺជាសមាសភាពគុណភាពរបស់វា។ មានអាតូមសូដ្យូម អ៊ីដ្រូសែន និងកាបូននីមួយៗ ហើយអាតូមអុកស៊ីសែនបី។ នេះគឺជាសមាសធាតុបរិមាណនៃសូដា
- សមាសភាពដែលមានគុណភាពខ្ពស់។សារធាតុបង្ហាញថាអាតូមនៃធាតុណាមួយត្រូវបានរួមបញ្ចូលនៅក្នុងសមាសភាពរបស់វា។
- សមាសភាពបរិមាណសារធាតុបង្ហាញចំនួនអាតូមដែលបង្កើតវា។
រូបមន្តគីមី- ការកត់ត្រាធម្មតានៃសមាសធាតុនៃសារធាតុដោយប្រើនិមិត្តសញ្ញាគីមី និងសន្ទស្សន៍
សូមចំណាំថា ប្រសិនបើរូបមន្តគីមីមានអាតូមតែមួយនៃប្រភេទមួយ នោះលេខរង 1 មិនត្រូវបានប្រើទេ។ ឧទាហរណ៍រូបមន្ត កាបូនឌីអុកស៊ីតសរសេរដូចនេះ - CO2 មិនមែន C1O2 ទេ។
របៀបយល់ឱ្យបានត្រឹមត្រូវតើមានរូបមន្តគីមីទេ?
នៅពេលសរសេររូបមន្តគីមី អ្នកតែងតែជួបលេខដែលសរសេរមុនរូបមន្តគីមី។
ឧទាហរណ៍, 2Na ឬ 5O2 ។តើលេខទាំងនេះមានន័យដូចម្តេច ហើយតើវាសម្រាប់អ្វី? លេខដែលសរសេរមុនរូបមន្តគីមីត្រូវបានគេហៅថា មេគុណ។
មេគុណបង្ហាញពីចំនួនភាគល្អិតសរុបនៃសារធាតុមួយ៖ អាតូម ម៉ូលេគុល អ៊ីយ៉ុង។
មេគុណ -លេខដែលបង្ហាញពីចំនួនសរុបនៃភាគល្អិត។
មេគុណត្រូវបានសរសេរមុនរូបមន្តគីមីនៃសារធាតុនៃម៉ូលេគុលអុកស៊ីសែន។សូមចំណាំថា ម៉ូលេគុលមិនអាចមានអាតូមតែមួយទេ ចំនួនអាតូមអប្បបរមានៅក្នុងម៉ូលេគុលគឺ ពីរ។
- ដូច្នេះធាតុចូលគឺ៖ 2H, 4Pឈរសម្រាប់អាតូមអ៊ីដ្រូសែនពីរ និងអាតូមផូស្វ័របួនរៀងគ្នា។
- កត់ត្រា 2H2តំណាងឱ្យម៉ូលេគុលអ៊ីដ្រូសែនពីរដែលមានអាតូមពីរនៃធាតុអ៊ីដ្រូសែន។
- កត់ត្រា 4S8- បង្ហាញពីម៉ូលេគុលស្ពាន់ធ័រចំនួនបួន ដែលនីមួយៗមានអាតូមចំនួនប្រាំបីនៃធាតុស្ពាន់ធ័រ។
- ប្រព័ន្ធសម្គាល់ស្រដៀងគ្នាសម្រាប់ចំនួនភាគល្អិតត្រូវបានប្រើសម្រាប់អ៊ីយ៉ុង។ កត់ត្រា 5K+តំណាងឱ្យ ប៉ូតាស្យូមអ៊ីយ៉ុងប្រាំ.
គួរកត់សម្គាល់ថាអ៊ីយ៉ុងអាចត្រូវបានបង្កើតឡើងមិនត្រឹមតែដោយអាតូមនៃធាតុមួយប៉ុណ្ណោះទេ។
- អ៊ីយ៉ុងដែលបង្កើតឡើងដោយអាតូមនៃធាតុគីមីមួយត្រូវបានគេហៅថាសាមញ្ញ: លី+, N3− ។
- អ៊ីយ៉ុងដែលបង្កើតឡើងដោយធាតុគីមីជាច្រើនត្រូវបានគេហៅថាស្មុគស្មាញ៖ OH⎺, SO4 2−។ចំណាំថាបន្ទុកនៃអ៊ីយ៉ុងត្រូវបានចង្អុលបង្ហាញដោយអក្សរធំ។
តើការចូលមានន័យយ៉ាងណា? 2NaCl?
ប្រសិនបើចម្លើយចំពោះសំណួរនេះគឺជាម៉ូលេគុលពីរនៃអំបិលតុ នោះចម្លើយគឺមិនត្រឹមត្រូវទេ។ អំបិលតុ ឬសូដ្យូមក្លរួ មានបន្ទះគ្រីស្តាល់អ៊ីយ៉ុង ពោលគឺវាជាសមាសធាតុអ៊ីយ៉ុង និងមានអ៊ីយ៉ុង Na+ និង Cl⎺. គូនៃអ៊ីយ៉ុងទាំងនេះត្រូវបានគេហៅថា ឯកតារូបមន្តនៃសារធាតុមួយ។ដូច្នេះសញ្ញាណ 2NaCl មានន័យថា ឯកតារូបមន្តពីរសូដ្យូមក្លរួ។ ពាក្យ ឯកតារូបមន្ត ក៏ត្រូវបានប្រើប្រាស់សម្រាប់សារធាតុនៃរចនាសម្ព័ន្ធអាតូមផងដែរ។
ឯកតារូបមន្ត- ភាគល្អិតតូចបំផុតនៃសារធាតុនៃរចនាសម្ព័ន្ធមិនមែនម៉ូលេគុលសមាសធាតុអ៊ីយ៉ុងគឺគ្រាន់តែជាអព្យាក្រឹតអគ្គិសនីដូចម៉ូលេគុលដែរ។ នេះមានន័យថាបន្ទុកវិជ្ជមាននៃ cations មានតុល្យភាពទាំងស្រុងដោយបន្ទុកអវិជ្ជមាននៃ anions ។ ឧទាហរណ៍ តើអ្វីជាឯកតារូបមន្តនៃសារធាតុដែលមានអ៊ីយ៉ុង Ag+ និង PO4 3−?ជាក់ស្តែងដើម្បីទូទាត់សងសម្រាប់បន្ទុកអវិជ្ជមាននៃអ៊ីយ៉ុង (បន្ទុក -3) វាចាំបាច់ត្រូវមានបន្ទុក +3 ។ ដោយពិចារណាលើការពិតដែលថា cation ប្រាក់មានបន្ទុក +1 បន្ទាប់មក cations បីគឺត្រូវការ។ នេះមានន័យថាឯកតារូបមន្ត (រូបមន្ត) នៃសារធាតុដែលបានផ្តល់ឱ្យគឺ Ag3PO4 ។
ដូច្នេះ ដោយប្រើនិមិត្តសញ្ញានៃធាតុគីមី សន្ទស្សន៍ និងមេគុណ វាអាចបង្កើតរូបមន្តគីមីនៃសារធាតុយ៉ាងច្បាស់លាស់ ដែលនឹងផ្តល់ព័ត៌មានអំពីសមាសភាពគុណភាព និងបរិមាណនៃសារធាតុ។
ជាចុងក្រោយ សូមមើលពីរបៀបបញ្ចេញរូបមន្តគីមីអោយបានត្រឹមត្រូវ។ ឧទាហរណ៍កត់ត្រា 3Ca2+បញ្ចេញសំឡេង៖ "កាល់ស្យូមអ៊ីយ៉ុងបីពីរបូក"ឬ "អ៊ីយ៉ុងកាល់ស្យូមបីជាមួយបន្ទុកពីរបូក" ។ កត់ត្រា 4HClបាននិយាយថា "ម៉ូលេគុលចំនួនបួននៃក្លរីនផេះ" ។ កត់ត្រា 2NaCl, បញ្ចេញសំឡេងដូច "ឯកតារូបមន្តពីរនៃក្លរួសូដ្យូម។"
ច្បាប់នៃភាពស្ថិតស្ថេរនៃធាតុផ្សំនៃរូបធាតុ
សមាសធាតុគីមីដូចគ្នាអាចទទួលបាន វិធីផ្សេងគ្នា. ឧទាហរណ៍កាបូនឌីអុកស៊ីត ឧស្ម័នកាបូនិកវាត្រូវបានបង្កើតឡើងដោយឥន្ធនៈដែលឆេះ: ធ្យូងថ្មឧស្ម័នធម្មជាតិ។ ផ្លែឈើមានជាតិគ្លុយកូសច្រើន។ ក្នុងអំឡុងពេលនៃការរក្សាទុករយៈពេលវែង ផ្លែឈើចាប់ផ្តើមកាន់តែយ៉ាប់យ៉ឺន ហើយដំណើរការដែលគេហៅថាការ fermentation ជាតិស្ករចាប់ផ្តើម ដែលនាំឱ្យការបញ្ចេញកាបូនឌីអុកស៊ីត។
កាបូនឌីអុកស៊ីតក៏ត្រូវបានបង្កើតឡើងនៅពេលដែលថ្មដូចជាដីស ថ្មម៉ាប និងថ្មកំបោរត្រូវបានកំដៅ។ ប្រតិកម្មគីមីខុសគ្នាទាំងស្រុង ប៉ុន្តែសារធាតុដែលបានបង្កើតឡើងជាលទ្ធផលនៃការកើតឡើងរបស់វាមានសមាសភាពគុណភាព និងបរិមាណដូចគ្នា - ឧស្ម័ន CO2 ។
គំរូនេះអនុវត្តជាចម្បងចំពោះសារធាតុនៃរចនាសម្ព័ន្ធម៉ូលេគុល។ នៅក្នុងករណីនៃសារធាតុនៃរចនាសម្ព័ន្ធដែលមិនមែនជាម៉ូលេគុលអាចមានករណីនៅពេលដែលសមាសភាពនៃសារធាតុអាស្រ័យលើវិធីសាស្រ្តនៃការរៀបចំរបស់វា។
ច្បាប់នៃភាពស្ថិតស្ថេរនៃសមាសធាតុនៃសារធាតុនៃរចនាសម្ព័ន្ធម៉ូលេគុល៖ សមាសធាតុនៃសារធាតុស្មុគស្មាញគឺតែងតែដូចគ្នា ហើយមិនអាស្រ័យលើវិធីសាស្រ្តនៃការរៀបចំរបស់វានោះទេ។
សេចក្តីសង្ខេបនៃអត្ថបទលើប្រធានបទ រូបមន្តគីមីសារធាតុ:
- សន្ទស្សន៍ - លេខបង្ហាញពីចំនួនអាតូមនៃប្រភេទជាក់លាក់មួយនៅក្នុងរូបមន្តគីមី
- សមាសភាពគុណភាពនៃសារធាតុបង្ហាញថាអាតូមនៃធាតុណាត្រូវបានបញ្ចូលក្នុងសមាសភាពរបស់វា។
- សមាសភាពបរិមាណនៃសារធាតុបង្ហាញពីចំនួនអាតូមដែលត្រូវបានរួមបញ្ចូលនៅក្នុងសមាសភាពរបស់វា។
- រូបមន្តគីមី - ការកត់ត្រាសាមញ្ញនៃសមាសធាតុនៃសារធាតុដោយប្រើនិមិត្តសញ្ញាគីមីនិងសន្ទស្សន៍ (បើចាំបាច់)
- មេគុណគឺជាលេខដែលបង្ហាញពីចំនួនសរុបនៃភាគល្អិត។ មេគុណត្រូវបានសរសេរមុនរូបមន្តគីមីនៃសារធាតុ
- ឯកតារូបមន្ត - ភាគល្អិតតូចបំផុតនៃសារធាតុនៃរចនាសម្ព័ន្ធអាតូមិច ឬអ៊ីយ៉ុង
ការចាត់ថ្នាក់នៃសារធាតុអសរីរាង្គ និងនាមនាមរបស់ពួកវាគឺផ្អែកលើលក្ខណៈសាមញ្ញបំផុត និងថេរបំផុតតាមពេលវេលា - សមាសធាតុគីមីដែលបង្ហាញពីអាតូមនៃធាតុដែលបង្កើតជាសារធាតុដែលបានផ្តល់ឱ្យក្នុងសមាមាត្រលេខរបស់វា។ ប្រសិនបើសារធាតុមួយត្រូវបានបង្កើតឡើងពីអាតូមនៃធាតុគីមីមួយ ពោលគឺឧ។ គឺជាទម្រង់នៃអត្ថិភាពនៃធាតុនេះក្នុងទម្រង់សេរី បន្ទាប់មកវាត្រូវបានគេហៅថាសាមញ្ញ សារធាតុ; ប្រសិនបើសារធាតុត្រូវបានបង្កើតឡើងដោយអាតូមពីរឬ ច្រើនទៀតធាតុបន្ទាប់មកវាត្រូវបានគេហៅថា សារធាតុស្មុគស្មាញ. សារធាតុសាមញ្ញទាំងអស់ (លើកលែងតែសារធាតុ monatomic) និងសារធាតុស្មុគស្មាញទាំងអស់ត្រូវបានគេហៅថាជាធម្មតា សមាសធាតុគីមីចាប់តាំងពីពួកវាមានអាតូមមួយ ឬ ធាតុផ្សេងគ្នាភ្ជាប់គ្នាទៅវិញទៅមកដោយចំណងគីមី។
នាមត្រកូលនៃសារធាតុអសរីរាង្គមានរូបមន្ត និងឈ្មោះ។ រូបមន្តគីមី - ការពិពណ៌នាអំពីសមាសធាតុនៃសារធាតុដោយប្រើនិមិត្តសញ្ញានៃធាតុគីមី សន្ទស្សន៍លេខ និងសញ្ញាមួយចំនួនទៀត។ ឈ្មោះគីមី - រូបភាពនៃសមាសភាពនៃសារធាតុដោយប្រើពាក្យឬក្រុមនៃពាក្យ។ ការស្ថាបនារូបមន្តគីមីនិងឈ្មោះត្រូវបានកំណត់ដោយប្រព័ន្ធ ច្បាប់នាមត្រកូល.
និមិត្តសញ្ញា និងឈ្មោះនៃធាតុគីមីត្រូវបានផ្តល់ឱ្យនៅក្នុងតារាងតាមកាលកំណត់នៃធាតុដោយ D.I. ម៉ែនដេឡេវ។ ធាតុត្រូវបានបែងចែកជាធម្មតា លោហធាតុ និង មិនមែនលោហធាតុ . មិនមែនលោហធាតុរួមមានធាតុទាំងអស់នៃក្រុម VIIIA (ឧស្ម័នដ៏ថ្លៃថ្នូ) និងក្រុម VIIA (ហាឡូហ្សែន) ធាតុនៃក្រុម VIA (លើកលែងតែប៉ូឡូញ៉ូម) ធាតុអាសូត ផូស្វ័រ អាសេនិច (ក្រុម VA); កាបូន, ស៊ីលីកុន (ក្រុម IVA); boron (ក្រុម IIA) ក៏ដូចជាអ៊ីដ្រូសែន។ ធាតុដែលនៅសល់ត្រូវបានចាត់ថ្នាក់ជាលោហធាតុ។
នៅពេលចងក្រងឈ្មោះនៃសារធាតុ ជាធម្មតាឈ្មោះរបស់ធាតុរុស្ស៊ីត្រូវបានគេប្រើឧទាហរណ៍ ឌីអុកស៊ីហ្សែន ស៊ីណូឌីហ្វ្លុយអូរី ប៉ូតាស្យូមសេលេណេត។ ជាប្រពៃណី សម្រាប់ធាតុមួយចំនួន ឫសនៃឈ្មោះឡាតាំងរបស់ពួកគេត្រូវបានបញ្ចូលទៅក្នុងពាក្យដេរីវេ៖
ឧទាហរណ៍: កាបូន, ម៉ង់ហ្គាណែ, អុកស៊ីដ, ស៊ុលហ្វីត, ស៊ីលីកេត។
ចំណងជើង សារធាតុសាមញ្ញ មានពាក្យមួយ - ឈ្មោះនៃធាតុគីមីដែលមានបុព្វបទលេខឧទាហរណ៍៖
ខាងក្រោមនេះត្រូវបានប្រើ បុព្វបទលេខ:
ចំនួនមិនកំណត់ត្រូវបានចង្អុលបង្ហាញដោយបុព្វបទលេខ ន- ប៉ូលី។
សម្រាប់សារធាតុសាមញ្ញមួយចំនួនពួកគេក៏ប្រើផងដែរ។ ពិសេសឈ្មោះដូចជា O 3 - អូហ្សូន P 4 - ផូស្វ័រពណ៌ស។
រូបមន្តគីមី សារធាតុស្មុគស្មាញបង្កើតឡើងដោយការចាត់តាំង electropositive(លក្ខខណ្ឌ និង cations ពិត) និង អេឡិចត្រូនិកសមាសធាតុ (អ៊ីយ៉ុងតាមលក្ខខណ្ឌ និងពិត) ឧទាហរណ៍ CuSO 4 (នៅទីនេះ Cu 2+ គឺជា cation ពិតប្រាកដ SO 4 2 - គឺជា anion ពិតប្រាកដ) និង PCl 3 (នៅទីនេះ P + III គឺជា cation តាមលក្ខខណ្ឌ Cl -I គឺជា anion តាមលក្ខខណ្ឌ) ។
ចំណងជើង សារធាតុស្មុគស្មាញផ្សំឡើងតាមរូបមន្តគីមីពីស្តាំទៅឆ្វេង។ ពួកវាត្រូវបានបង្កើតឡើងដោយពាក្យពីរ - ឈ្មោះនៃសមាសធាតុអេឡិចត្រុង (ក្នុងករណីតែងតាំង) និងសមាសធាតុអេឡិចត្រូនិច (នៅក្នុង ករណីហ្សែន), ឧទាហរណ៍:
CuSO 4 - ស្ពាន់ (II) ស៊ុលហ្វាត
PCl 3 - ផូស្វ័រ trichloride
LaCl 3 - lanthanum (III) ក្លរ
CO - កាបូនម៉ូណូអុកស៊ីត
ចំនួននៃសមាសធាតុ electropositive និង electronegative នៅក្នុងឈ្មោះត្រូវបានចង្អុលបង្ហាញដោយបុព្វបទលេខដែលបានផ្តល់ឱ្យខាងលើ (វិធីសាស្ត្រសកល) ឬដោយរដ្ឋអុកស៊ីតកម្ម (ប្រសិនបើពួកគេអាចត្រូវបានកំណត់ដោយរូបមន្ត) ដោយប្រើលេខរ៉ូម៉ាំងក្នុងវង់ក្រចក (សញ្ញាបូកត្រូវបានលុបចោល) ។ ក្នុងករណីខ្លះការចោទប្រកាន់នៃអ៊ីយ៉ុងត្រូវបានផ្តល់ឱ្យ (សម្រាប់ cations និង anions នៃសមាសភាពស្មុគស្មាញ) ដោយប្រើលេខអារ៉ាប់ដែលមានសញ្ញាដែលត្រូវគ្នា។
ឈ្មោះពិសេសខាងក្រោមត្រូវបានប្រើសម្រាប់ cations និង anions ទូទៅ៖
|
H 2 F + - fluoronium |
C 2 2 - - អាសេទីលលីន |
|
H 3 O + - អុកស៊ីតូនីញ៉ូម |
CN - - ស៊ីយ៉ាន |
|
H 3 S + - ស៊ុលហ្វាន |
CNO - - បំពេញ |
|
NH 4 + - អាម៉ូញ៉ូម |
HF 2 - - hydrodifluoride |
|
N 2 H 5 + - hydrazinium (1+) |
ហូ 2 - អ៊ីដ្រូភឺរអុកស៊ីត |
|
N 2 H 6 + - hydrazinium (2+) |
HS - - អ៊ីដ្រូស៊ុលហ្វីត |
|
NH 3 OH + - hydroxylamine |
N 3 - - អាហ្សីត |
|
NO+ - nitrosyl |
NCS - - thiocyanate |
|
NO 2 + - nitroyl |
O 2 2 - - peroxide |
|
O 2 + - dioxygenyl |
O 2 - - superoxide |
|
PH 4 + - ផូស្វ័រ |
អូ 3 - - អូហ្សូន |
|
វីអូ 2+ - vanadyl |
OCN - - cyanate |
|
UO 2+ - អ៊ុយរ៉ានីល។ |
អូ - - អ៊ីដ្រូសែន |
សម្រាប់ចំនួនតិចតួចនៃសារធាតុល្បីវាក៏ត្រូវបានគេប្រើផងដែរ។ ពិសេសចំណងជើង៖
1. អាស៊ីត និងអ៊ីដ្រូសែនមូលដ្ឋាន។ អំបិល
អ៊ីដ្រូសែនគឺជាប្រភេទសារធាតុស្មុគស្មាញដែលមានអាតូមនៃធាតុមួយចំនួន E (លើកលែងតែហ្វ្លុយអូរីន និងអុកស៊ីហ៊្សែន) និងក្រុមអ៊ីដ្រូស៊ីល OH; រូបមន្តទូទៅនៃអ៊ីដ្រូសែនអ៊ីដ្រូសែន E(OH) ន, កន្លែងណា ន= 1÷6 ។ ទម្រង់អ៊ីដ្រូសែន E(OH) នហៅ អ័រថូ- រាង; នៅ ន> 2 អ៊ីដ្រូសែនក៏អាចត្រូវបានរកឃើញនៅក្នុង មេតា-ទម្រង់ ដែលរួមមាន បន្ថែមលើអាតូម E និងក្រុម OH អាតូមអុកស៊ីសែន O ឧទាហរណ៍ E(OH) 3 និង EO(OH) E(OH) 4 និង E(OH) 6 និង EO 2 (OH) 2 .
អ៊ីដ្រូសែនត្រូវបានបែងចែកជាពីរក្រុមដែលមានលក្ខណៈសម្បត្តិគីមីផ្ទុយគ្នា៖ អ៊ីដ្រូសែនអាស៊ីត និងអ៊ីដ្រូសែនមូលដ្ឋាន។
អ៊ីដ្រូសែនអាស៊ីតមានអាតូមអ៊ីដ្រូសែន ដែលអាចត្រូវបានជំនួសដោយអាតូមដែកដែលស្ថិតនៅក្រោមច្បាប់នៃ stoichiometric valence ។ អាស៊ីតអ៊ីដ្រូសែនភាគច្រើនត្រូវបានរកឃើញនៅក្នុង មេតា-ទម្រង់ ហើយអាតូមអ៊ីដ្រូសែននៅក្នុងរូបមន្តនៃអ៊ីដ្រូសែនអាសុីតត្រូវបានផ្តល់កន្លែងដំបូង ឧទាហរណ៍ H 2 SO 4 HNO 3 និង H 2 CO 3 ហើយមិនមែន SO 2 (OH) 2 ទេ NO 2 (OH) និង CO ( អូ) ២. រូបមន្តទូទៅនៃអាស៊ីតអ៊ីដ្រូសែនគឺ H X EO នៅដែលជាកន្លែងដែលសមាសធាតុអេឡិចត្រូនិ EO y x - ហៅថាសំណល់អាស៊ីត។ ប្រសិនបើមិនមែនអាតូមអ៊ីដ្រូសែនទាំងអស់ត្រូវបានជំនួសដោយលោហៈទេ នោះពួកវានៅតែជាផ្នែកមួយនៃសំណល់អាស៊ីត។
ឈ្មោះនៃអាស៊ីតអ៊ីដ្រូសែនទូទៅមានពាក្យពីរយ៉ាង៖ ឈ្មោះត្រឹមត្រូវដែលមានការបញ្ចប់ “អា” និងពាក្យក្រុម “អាស៊ីត”។ នេះគឺជារូបមន្ត និងឈ្មោះត្រឹមត្រូវនៃអាស៊ីត hydroxides ទូទៅ និងសំណល់អាស៊ីតរបស់វា (សញ្ញាចុចមានន័យថាអ៊ីដ្រូសែនមិនត្រូវបានគេស្គាល់ក្នុងទម្រង់សេរី ឬក្នុងដំណោះស្រាយទឹកអាស៊ីត):
|
អាស៊ីត hydroxide |
សំណល់អាស៊ីត |
|
HAsO 2 - មេតាអាសេនិច |
AsO 2 - - metaarsenite |
|
H 3 AsO 3 - orthoarsenic |
AsO 3 3 - - orthoarsenite |
|
H 3 AsO 4 - អាសេនិច |
AsO 4 3 - arsenate |
|
B 4 O 7 2 - - tetraborate |
|
|
ВiО 3 - - ប៊ីស្មុត |
|
|
HBrO - bromide |
BroO - - hypobromite |
|
HBrO 3 - brominated |
ប្រូអូ ៣ - ប្រូមេត |
|
H 2 CO 3 - ធ្យូងថ្ម |
CO 3 2 - - កាបូន |
|
HClO - hypochlorous |
ClO- - hypochlorite |
|
HClO 2 - ក្លរួ |
ClO2- - ក្លរីត |
|
HClO 3 - ក្លរ |
ClO3- - ក្លរ |
|
HClO 4 - ក្លរីន |
ClO4 - - perchlorate |
|
H 2 CrO 4 - chrome |
CrO 4 2 - - ក្រូម |
|
НCrO 4 - - hydrochromate |
|
|
H 2 Cr 2 O 7 - dichromic |
Cr 2 O 7 2 - - dichromate |
|
FeO 4 2 - - ferrate |
|
|
HIO 3 - អ៊ីយ៉ូត |
អាយអូ ៣ - - អ៊ីយ៉ូត |
|
HIO 4 - មេទីយ៉ូឌីន |
អាយអូ ៤ - - metaperiodate |
|
H 5 IO 6 - អ័រតូយ៉ូឌីន |
អាយអូ ៦៥ - - orthoperiodate |
|
HMnO 4 - ម៉ង់ហ្គាណែស |
MnO4- - permanganate |
|
MnO 4 2 - - ម៉ង់ហ្គាណេត |
|
|
ម.ក ៤២ - - ម៉ូលីបដេត |
|
|
HNO 2 - អាសូត |
លេខ 2 - - នីទ្រីត |
|
HNO 3 - អាសូត |
លេខ ៣ - - នីត្រាត |
|
HPO 3 - metaphosphoric |
PO 3 - - មេតាផូស្វាត |
|
H 3 PO 4 - orthophosphoric |
PO 43 - - អ័រថូផូស្វាត |
|
НPO 4 2 - - hydroorthophosphate |
|
|
H 2 PO 4 - - dihydroothophosphate |
|
|
H 4 P 2 O 7 - diphosphoric |
ទំ ២ ឱ ៧ ៤ - - ឌីផូស្វាត |
|
ReO 4 - - perrhenate |
|
|
SO 3 2 - - ស៊ុលហ្វីត |
|
|
HSO 3 - - អ៊ីដ្រូស៊ុលហ្វីត |
|
|
H 2 SO 4 - ស្ពាន់ធ័រ |
SO 4 2 - - ស៊ុលហ្វាត |
|
HSO 4 - - អ៊ីដ្រូសែនស៊ុលហ្វាត |
|
|
H 2 S 2 O 7 - disulfur |
ស ២ អូ ៧ ២ - - disulfate |
|
H 2 S 2 O 6 (O 2) - peroxodisulfur |
ស ២ អូ ៦ (អូ ២) ២ - - peroxodisulfate |
|
H 2 SO 3 S - thiosulfur |
SO 3 S 2 - - thiosulfate |
|
H 2 SeO 3 - សេលេញ៉ូម |
SeO 3 2 - - សេលេនីត |
|
H 2 SeO 4 - សេលេញ៉ូម |
SeO 4 2 - - សេលេណេត |
|
H 2 SiO 3 - មេតាស៊ីលីកុន |
SiO 3 2 - - មេតាស៊ីលីត |
|
H 4 SiO 4 - orthosilicon |
ស៊ីអូ ៤ ៤ - - orthosilicate |
|
H 2 TeO 3 - telluric |
TeO 3 2 - - tellurite |
|
H 2 TeO 4 - metatelluric |
TeO 4 2 - - metatellurate |
|
H 6 TeO 6 - orthotelluric |
TeO 6 6 - - orthotellurate |
|
វីអូ ៣ - - មេតាវ៉ាណាដេត |
|
|
វីអូ ៤៣ - - អ័រថូវ៉ាណាដេត |
|
|
WO 4 3 - - tungstate |
អាស៊ីត hydroxides មិនសូវសាមញ្ញត្រូវបានគេដាក់ឈ្មោះយោងទៅតាមច្បាប់នាមត្រកូលសម្រាប់សមាសធាតុស្មុគស្មាញឧទាហរណ៍៖
ឈ្មោះសំណល់អាស៊ីតត្រូវបានប្រើដើម្បីបង្កើតឈ្មោះអំបិល។
អ៊ីដ្រូសែនជាមូលដ្ឋានមានអ៊ីយ៉ុងអ៊ីដ្រូអុកស៊ីត ដែលអាចត្រូវបានជំនួសដោយសំណល់អាស៊ីតដែលស្ថិតនៅក្រោមច្បាប់នៃ stoichiometric valence ។ អ៊ីដ្រូសែនមូលដ្ឋានទាំងអស់ត្រូវបានរកឃើញនៅក្នុង អ័រថូ- រាង; រូបមន្តទូទៅរបស់ពួកគេគឺ M (OH) ន, កន្លែងណា ន= 1.2 (តិចជាញឹកញាប់ 3.4) និង M ន+ ជាសារធាតុដែក។ ឧទាហរណ៍នៃរូបមន្ត និងឈ្មោះនៃអ៊ីដ្រូសែនមូលដ្ឋាន៖
ទ្រព្យសម្បត្តិគីមីដ៏សំខាន់បំផុតនៃអ៊ីដ្រូអុកស៊ីតជាមូលដ្ឋាន និងអាស៊ីតគឺអន្តរកម្មរបស់វាជាមួយគ្នាដើម្បីបង្កើតជាអំបិល ( ប្រតិកម្មនៃការបង្កើតអំបិល), ឧទាហរណ៍:
Ca(OH) 2 + H 2 SO 4 = CaSO 4 + 2H 2 O
Ca(OH) 2 + 2H 2 SO 4 = Ca(HSO 4) 2 + 2H 2 O
2Ca(OH)2 + H2SO4 = Ca2SO4(OH)2 + 2H2O
អំបិលគឺជាប្រភេទសារធាតុស្មុគ្រស្មាញដែលមានផ្ទុកសារធាតុ M cations ន+ និងសំណល់អាស៊ីត*។
អំបិលជាមួយរូបមន្តទូទៅ M X(EO នៅ)នហៅ មធ្យម អំបិល និងអំបិលដែលមានអាតូមអ៊ីដ្រូសែនដែលមិនអាចជំនួសបាន - ជូរអំបិល។ ពេលខ្លះអំបិលក៏មានអ៊ីយ៉ុងអ៊ីដ្រូសែន និង/ឬអុកស៊ីតកម្មផងដែរ។ អំបិលបែបនេះត្រូវបានគេហៅថា មេអំបិល។ នេះជាឧទាហរណ៍ និងឈ្មោះអំបិល៖
|
កាល់ស្យូម orthophosphate |
|
|
កាល់ស្យូម dihydrogen orthophosphate |
|
|
កាល់ស្យូមអ៊ីដ្រូសែនផូស្វាត |
|
|
ស្ពាន់ (II) កាបូន |
|
|
Cu 2 CO 3 (OH) ២ |
Dicopper dihydroxide កាបូន |
|
លែនថុន (III) នីត្រាត |
|
|
ទីតានីញ៉ូមអុកស៊ីដឌីនីត្រាត |
អាស៊ីត និងអំបិលមូលដ្ឋានអាចត្រូវបានបំប្លែងទៅជាអំបិលកណ្តាលដោយប្រតិកម្មជាមួយនឹងអ៊ីដ្រូអុកស៊ីតជាមូលដ្ឋាន និងអាស៊ីតសមស្រប ឧទាហរណ៍៖
Ca(HSO 4) 2 + Ca(OH) = CaSO 4 + 2H 2 O
Ca 2 SO 4 (OH) 2 + H 2 SO 4 = Ca 2 SO 4 + 2H 2 O
វាក៏មានអំបិលដែលមាន cations ពីរផ្សេងគ្នាផងដែរ: ពួកគេត្រូវបានគេហៅថាជាញឹកញាប់ អំបិលពីរដង, ឧទាហរណ៍:
2. អាស៊ីតនិងអុកស៊ីដមូលដ្ឋាន
អុកស៊ីដ អ៊ី Xអំពី នៅ- ផលិតផលនៃការខះជាតិទឹកពេញលេញនៃអ៊ីដ្រូសែន៖
អាស៊ីតអ៊ីដ្រូសែន (H 2 SO 4, H 2 CO 3) អាសុីតអុកស៊ីតឆ្លើយ(SO 3, CO 2) និងអ៊ីដ្រូសែនមូលដ្ឋាន (NaOH, Ca(OH) 2) - មូលដ្ឋានអុកស៊ីដ(Na 2 O, CaO) និងស្ថានភាពអុកស៊ីតកម្មនៃធាតុ E មិនផ្លាស់ប្តូរនៅពេលផ្លាស់ប្តូរពីអ៊ីដ្រូសែនទៅជាអុកស៊ីដ។ ឧទាហរណ៍នៃរូបមន្ត និងឈ្មោះអុកស៊ីដ៖
អុកស៊ីដអាស៊ីត និងមូលដ្ឋានរក្សាលក្ខណៈសម្បត្តិបង្កើតអំបិលនៃអ៊ីដ្រូអុកស៊ីតដែលត្រូវគ្នា នៅពេលមានអន្តរកម្មជាមួយអ៊ីដ្រូសែនដែលមានលក្ខណៈសម្បត្តិផ្ទុយគ្នា ឬជាមួយគ្នាទៅវិញទៅមក៖
N 2 O 5 + 2NaOH = 2NaNO 3 + H 2 O
3CaO + 2H3PO4 = Ca3(PO4)2 + 3H2O
ឡា 2 O 3 + 3SO 3 = ឡា 2 (SO 4) ៣
3. អុកស៊ីដ amphoteric និង hydroxides
អំភ្លីអ៊ីដ្រូសែន និងអុកស៊ីដ - ទ្រព្យសម្បត្តិគីមីដែលមាននៅក្នុងការបង្កើតអំបិលពីរជួរ ឧទាហរណ៍សម្រាប់អាលុយមីញ៉ូមអ៊ីដ្រូសែន និងអុកស៊ីដអាលុយមីញ៉ូម៖
(a) 2Al(OH) 3 + 3SO 3 = Al 2 (SO 4) 3 + 3H 2 O
Al 2 O 3 + 3H 2 SO 4 = Al 2 (SO 4) 3 + 3H 2 O
(b) 2Al(OH) 3 + Na 2 O = 2NaAlO 2 + 3H 2 O
Al 2 O 3 + 2NaOH = 2NaAlO 2 + H 2 O
ដូច្នេះអាលុយមីញ៉ូអ៊ីដ្រូសែននិងអុកស៊ីដនៅក្នុងប្រតិកម្ម (ក) បង្ហាញលក្ខណៈសម្បត្តិ មេអ៊ីដ្រូសែន និងអុកស៊ីដ, ឧ។ ប្រតិកម្មជាមួយអាស៊ីតអ៊ីដ្រូសែន និងអុកស៊ីដ បង្កើតជាអំបិលដែលត្រូវគ្នា - អាលុយមីញ៉ូស៊ុលហ្វាត Al 2 (SO 4) 3 ខណៈពេលដែលមានប្រតិកម្ម (ខ) ពួកគេក៏បង្ហាញលក្ខណៈសម្បត្តិផងដែរ។ អាសុីតអ៊ីដ្រូសែន និងអុកស៊ីដ, ឧ។ ប្រតិកម្មជាមួយអ៊ីដ្រូអុកស៊ីត និងអុកស៊ីដមូលដ្ឋាន បង្កើតជាអំបិល - សូដ្យូម ឌីយ៉ូអូអាលូមីត (III) NaAlO ២. ក្នុងករណីទី 1 ធាតុអាលុយមីញ៉ូមបង្ហាញពីទ្រព្យសម្បត្តិនៃលោហៈហើយជាផ្នែកមួយនៃសមាសធាតុអេឡិចត្រូប៉ូស៊ីត (Al 3+) នៅក្នុងទីពីរ - ទ្រព្យសម្បត្តិនៃលោហៈមិនមែនលោហៈនិងជាផ្នែកមួយនៃសមាសធាតុអេឡិចត្រូនិនៃរូបមន្តអំបិល ( អាឡូ 2 -) ។
ប្រសិនបើប្រតិកម្មទាំងនេះកើតឡើងនៅក្នុងដំណោះស្រាយ aqueous នោះសមាសភាពនៃអំបិលលទ្ធផលបានផ្លាស់ប្តូរ ប៉ុន្តែវត្តមានរបស់អាលុយមីញ៉ូមនៅក្នុង cation និង anion នៅតែមាន:
2Al(OH) 3 + 3H 2 SO 4 = 2 (SO 4) 3
Al(OH) 3 + NaOH = Na
នៅទីនេះ អ៊ីយ៉ុងស្មុគស្មាញ 3+ - hexaaqualuminium(III) cation, - - tetrahydroxoaluminate(III) ion ត្រូវបានបន្លិចក្នុងតង្កៀបការ៉េ។
ធាតុដែលបង្ហាញលក្ខណៈសម្បត្តិលោហធាតុ និងមិនមែនលោហធាតុនៅក្នុងសមាសធាតុត្រូវបានគេហៅថា amphoteric ទាំងនេះរួមបញ្ចូលធាតុនៃក្រុម A តារាងតាមកាលកំណត់- Be, Al, Ga, Ge, Sn, Pb, Sb, Bi, Po ជាដើម ក៏ដូចជាធាតុក្រុម B ភាគច្រើនផងដែរ - Cr, Mn, Fe, Zn, Cd, Au ជាដើម។ អុកស៊ីដ Amphoteric ត្រូវបានគេហៅផងដែរថា ក៏ដូចជារបស់សំខាន់ៗឧទាហរណ៍៖
Amphoteric hydroxides (ប្រសិនបើស្ថានភាពអុកស៊ីតកម្មនៃធាតុលើសពី + II) អាចត្រូវបានរកឃើញនៅក្នុង អ័រថូ- ឬ (និង) មេតា- ទម្រង់។ នេះគឺជាឧទាហរណ៍នៃ amphoteric hydroxides:
អុកស៊ីដ amphoteric មិនតែងតែត្រូវគ្នាទៅនឹង hydroxides amphoteric ទេ ចាប់តាំងពីពេលដែលព្យាយាមទទួលបានចុងក្រោយ អុកស៊ីដ hydrated ត្រូវបានបង្កើតឡើង ឧទាហរណ៍៖
ប្រសិនបើធាតុ amphoteric នៅក្នុងសមាសធាតុមានស្ថានភាពអុកស៊ីតកម្មជាច្រើននោះ amphotericity នៃអុកស៊ីដ និងអ៊ីដ្រូសែនដែលត្រូវគ្នា (ហើយជាលទ្ធផល amphotericity នៃធាតុខ្លួនវា) នឹងត្រូវបានបង្ហាញខុសគ្នា។ សម្រាប់រដ្ឋអុកស៊ីតកម្មទាប អ៊ីដ្រូអុកស៊ីត និងអុកស៊ីដមានគុណសម្បត្តិជាមូលដ្ឋាន ហើយធាតុខ្លួនវាមានលក្ខណៈសម្បត្តិលោហធាតុ ដូច្នេះវាត្រូវបានរួមបញ្ចូលស្ទើរតែជានិច្ចនៅក្នុងសមាសភាពនៃ cations ។ ចំពោះរដ្ឋអុកស៊ីតកម្មខ្ពស់ ផ្ទុយទៅវិញ អ៊ីដ្រូអុកស៊ីត និងអុកស៊ីដមានគុណសម្បត្តិអាស៊ីតខ្លាំង ហើយធាតុខ្លួនវាមានលក្ខណៈសម្បត្តិមិនមែនលោហធាតុ ដូច្នេះវាត្រូវបានរួមបញ្ចូលស្ទើរតែជានិច្ចនៅក្នុងសមាសភាពនៃ anions ។ ដូច្នេះម៉ង់ហ្គាណែស (II) អុកស៊ីដនិងអ៊ីដ្រូសែនមានលក្ខណៈសម្បត្តិជាមូលដ្ឋានលេចធ្លោហើយម៉ង់ហ្គាណែសខ្លួនឯងគឺជាផ្នែកមួយនៃ cations នៃប្រភេទ 2+ ខណៈពេលដែលម៉ង់ហ្គាណែស (VII) អុកស៊ីដនិងអ៊ីដ្រូសែនមានលក្ខណៈសម្បត្តិអាស៊ីតលេចធ្លោហើយម៉ង់ហ្គាណែសខ្លួនវាគឺជាផ្នែកមួយនៃ MnO 4 - ប្រភេទ anion ។ Amphoteric hydroxides ដែលមានលក្ខណៈលេចធ្លោខ្ពស់នៃលក្ខណៈសម្បត្តិអាស៊ីតត្រូវបានផ្តល់រូបមន្តនិងឈ្មោះដោយផ្អែកលើគំរូនៃ hydroxides អាស៊ីតឧទាហរណ៍ HMn VII O 4 - អាស៊ីតម៉ង់ហ្គាណែស។
ដូច្នេះការបែងចែកធាតុទៅជាលោហធាតុ និងមិនមែនលោហធាតុគឺមានលក្ខខណ្ឌ។ រវាងធាតុ (Na, K, Ca, Ba ។ ធាតុដែលមានលក្ខណៈសម្បត្តិ amphoteric ។
4. សមាសធាតុគោលពីរ
ប្រភេទដ៏ធំទូលាយនៃសារធាតុស្មុគស្មាញអសរីរាង្គគឺជាសមាសធាតុគោលពីរ។ ទាំងនេះរួមបញ្ចូលជាដំបូង សមាសធាតុធាតុពីរទាំងអស់ (លើកលែងតែអុកស៊ីដមូលដ្ឋាន អាសុីត និងអាមផូទីក) ឧទាហរណ៍ H 2 O, KBr, H 2 S, Cs 2 (S 2), N 2 O, NH 3, HN 3, CaC 2, SiH 4 ។ សមាសធាតុ electropositive និង electronegative នៃរូបមន្តនៃសមាសធាតុទាំងនេះរួមមានអាតូមបុគ្គល ឬក្រុមដែលជាប់ទាក់ទងគ្នានៃអាតូមនៃធាតុដូចគ្នា។
សារធាតុពហុធាតុ នៅក្នុងរូបមន្តដែលសមាសធាតុមួយមានអាតូមមិនទាក់ទងនៃធាតុជាច្រើន ក៏ដូចជាក្រុមធាតុតែមួយ ឬពហុធាតុនៃអាតូម (លើកលែងតែអ៊ីដ្រូសែន និងអំបិល) ត្រូវបានចាត់ទុកថាជាសមាសធាតុគោលពីរ ឧទាហរណ៍ CSO, IO 2 F 3, SBrO 2 F, CrO (O 2) 2, PSI 3, (CaTi)O 3, (FeCu)S 2, Hg(CN) 2, (PF 3) 2 O, VCl 2 (NH 2) ។ ដូច្នេះ CSO អាចត្រូវបានតំណាងថាជាសមាសធាតុ CS 2 ដែលអាតូមស្ពាន់ធ័រមួយត្រូវបានជំនួសដោយអាតូមអុកស៊ីសែន។
ឈ្មោះនៃសមាសធាតុគោលពីរត្រូវបានបង្កើតឡើងដោយយោងទៅតាមច្បាប់នាមនាមធម្មតា ឧទាហរណ៍៖
|
នៃ 2 - difluoride អុកស៊ីសែន |
K 2 O 2 - ប៉ូតាស្យូម peroxide |
|
HgCl 2 - ក្លរួបារត (II) |
Na 2 S - សូដ្យូមស៊ុលហ្វីត |
|
Hg 2 Cl 2 - dimercury dichloride |
Mg 3 N 2 - ម៉ាញ៉េស្យូមនីត្រាត |
|
SBr 2 O - ស្ពាន់ធ័រអុកស៊ីដឌីប្រូម |
NH 4 Br - អាម៉ូញ៉ូម bromide |
|
N 2 O - អុកស៊ីដឌីនីត្រូសែន |
Pb(N 3) 2 - នាំមុខ (II) azide |
|
NO 2 - អាសូតឌីអុកស៊ីត |
CaC 2 - កាល់ស្យូម acetylenide |
សម្រាប់សមាសធាតុគោលពីរមួយចំនួន ឈ្មោះពិសេសត្រូវបានប្រើប្រាស់ ដែលជាបញ្ជីដែលត្រូវបានផ្តល់ឱ្យមុន។
លក្ខណៈសម្បត្តិគីមីនៃសមាសធាតុគោលពីរគឺមានភាពចម្រុះណាស់ ដូច្នេះពួកវាត្រូវបានបែងចែកជាក្រុមជាញឹកញាប់ដោយឈ្មោះរបស់ anions i.e. halides, chalcogenides, nitrides, carbides, hydrides ជាដើម ត្រូវបានចាត់ទុកថាដាច់ដោយឡែកពីគ្នា ក្នុងចំណោមសមាសធាតុគោលពីរ ក៏មានសារធាតុដែលមានលក្ខណៈមួយចំនួននៃប្រភេទផ្សេងទៀតនៃសារធាតុអសរីរាង្គផងដែរ។ ដូច្នេះសមាសធាតុ CO, NO, NO 2, និង (Fe II Fe 2 III) O 4 ដែលជាឈ្មោះដែលត្រូវបានសាងសង់ដោយប្រើពាក្យ អុកស៊ីដ មិនអាចត្រូវបានគេចាត់ថ្នាក់ជាអុកស៊ីដ (អាស៊ីត មូលដ្ឋាន អំពែរ) ទេ។ កាបូនម៉ូណូអុកស៊ីត CO, អាសូតម៉ូណូអុកស៊ីត NO និងអាសូតឌីអុកស៊ីត NO 2 មិនមានអ៊ីដ្រូអុកស៊ីតអាស៊ីតដែលត្រូវគ្នាទេ (ទោះបីជាអុកស៊ីដទាំងនេះត្រូវបានបង្កើតឡើងដោយមិនមែនលោហធាតុ C និង N) ហើយក៏មិនបង្កើតជាអំបិលដែល anions នឹងរួមបញ្ចូលអាតូម C II, N II និង N ដែរ។ IV. អុកស៊ីដទ្វេដង (Fe II Fe 2 III) O 4 - diiron (III) - ជាតិដែក (II) អុកស៊ីដទោះបីជាវាមានអាតូមនៃធាតុ amphoteric - ជាតិដែកនៅក្នុងសមាសធាតុអេឡិចត្រុងប៉ុន្តែនៅក្នុងពីរ កម្រិតខុសគ្នាអុកស៊ីតកម្ម ជាលទ្ធផលដែលនៅពេលធ្វើអន្តរកម្មជាមួយអាស៊ីតអ៊ីដ្រូសែន វាមិនមែនជាអំបិលមួយទេ ប៉ុន្តែជាអំបិលពីរផ្សេងគ្នា។
សមាសធាតុគោលពីរដូចជា AgF, KBr, Na 2 S, Ba(HS) 2, NaCN, NH 4 Cl, និង Pb(N 3) 2 ត្រូវបានបង្កើតឡើង ដូចជាអំបិល ពី cations និង anions ពិតប្រាកដ ដែលជាមូលហេតុដែលពួកគេត្រូវបានគេហៅថា ដូចអំបិល សមាសធាតុគោលពីរ (ឬធម្មតាអំបិល) ។ ពួកវាអាចត្រូវបានចាត់ទុកថាជាផលិតផលនៃការជំនួសអាតូមអ៊ីដ្រូសែននៅក្នុងសមាសធាតុ HF, HCl, HBr, H 2 S, HCN និង HN 3 ។ ក្រោយមកទៀតនៅក្នុងដំណោះស្រាយ aqueous មានមុខងារជាអាស៊ីត ហើយដូច្នេះដំណោះស្រាយរបស់ពួកគេត្រូវបានគេហៅថាអាស៊ីត ឧទាហរណ៍ HF (aqua) - អាស៊ីត hydrofluoric, H 2 S (aqua) - អាស៊ីត hydrosulfide ។ ទោះជាយ៉ាងណាក៏ដោយ ពួកវាមិនមែនជារបស់ប្រភេទអាស៊ីតអ៊ីដ្រូសែនទេ ហើយនិស្សន្ទវត្ថុរបស់វាមិនមែនជារបស់អំបិលក្នុងចំណាត់ថ្នាក់នៃសារធាតុអសរីរាង្គនោះទេ។
ភារកិច្ចសំខាន់បំផុតមួយនៅក្នុងគីមីវិទ្យាគឺសមាសភាពត្រឹមត្រូវនៃរូបមន្តគីមី។ រូបមន្តគីមីគឺជាការតំណាងជាលាយលក្ខណ៍អក្សរនៃសមាសភាពនៃសារធាតុគីមីដោយប្រើការកំណត់ និងសន្ទស្សន៍ធាតុឡាតាំង។ ដើម្បីចងក្រងរូបមន្តឱ្យបានត្រឹមត្រូវ យើងពិតជាត្រូវការតារាងតាមកាលកំណត់ និងចំណេះដឹងអំពីច្បាប់សាមញ្ញ។ ពួកវាសាមញ្ញណាស់ ហើយសូម្បីតែកូនក្មេងក៏អាចចងចាំវាបានដែរ។
របៀបធ្វើរូបមន្តគីមី
គំនិតសំខាន់នៅពេលគូររូបមន្តគីមីគឺ "ភាពស្មោះត្រង់" ។ Valency គឺជាទ្រព្យសម្បត្តិនៃធាតុមួយដើម្បីផ្ទុកចំនួនអាតូមជាក់លាក់នៅក្នុងសមាសធាតុមួយ។ valence នៃធាតុគីមីអាចត្រូវបានមើលក្នុងតារាងកាលកំណត់ ហើយអ្នកក៏ត្រូវចងចាំ និងអាចអនុវត្តច្បាប់ទូទៅសាមញ្ញផងដែរ។
- valence នៃលោហៈគឺតែងតែស្មើនឹងលេខក្រុម ដោយផ្តល់ថាវាស្ថិតនៅក្នុងក្រុមរងសំខាន់។ ឧទាហរណ៍ ប៉ូតាស្យូមមាន valency 1 ហើយកាល់ស្យូមមាន valency 2។
- មិនមែនលោហធាតុមានភាពស្មុគស្មាញបន្តិច។ មិនមែនលោហធាតុអាចមាន valency ខ្ពស់ជាង និងទាបជាង។ valence ខ្ពស់បំផុតគឺស្មើនឹងលេខក្រុម។ តម្លៃទាបបំផុតអាចត្រូវបានកំណត់ដោយដកលេខក្រុមរបស់ធាតុចេញពីប្រាំបី។ នៅពេលផ្សំជាមួយលោហធាតុ លោហធាតុមិនមែនលោហធាតុតែងតែមាន valency ទាបបំផុត។ អុកស៊ីសែនតែងតែមាន valence 2 ។
- នៅក្នុងសមាសធាតុដែលមិនមែនជាលោហធាតុពីរ ធាតុគីមីដែលស្ថិតនៅខាងស្តាំ និងខ្ពស់ជាងនៅក្នុងតារាងតាមកាលកំណត់មាន valence ទាបបំផុត។ ទោះយ៉ាងណាក៏ដោយ ហ្វ្លុយអូរីន តែងតែមានចន្លោះ 1 ។
- រឿងមួយទៀត ច្បាប់សំខាន់ពេលកំណត់ហាងឆេង! ចំនួនសរុប valencies នៃធាតុមួយត្រូវតែស្មើនឹងចំនួនសរុបនៃ valencies នៃធាតុមួយផ្សេងទៀតជានិច្ច!
ចូរយើងបង្រួបបង្រួមចំណេះដឹងដែលទទួលបានដោយប្រើឧទាហរណ៍នៃសមាសធាតុនៃលីចូម និងអាសូត។ លោហធាតុលីចូមមាន valence 1. អាសូតមិនមែនលោហធាតុស្ថិតនៅក្នុងក្រុម 5 ហើយមាន valence ខ្ពស់ជាង 5 និង valence ទាបជាង 3. ដូចដែលយើងដឹងរួចមកហើយថា នៅក្នុងសមាសធាតុជាមួយលោហធាតុ មិនមែនលោហធាតុតែងតែមានកម្រិតទាបជាង។ valence ដូច្នេះអាសូតក្នុងករណីនេះនឹងមាន valence បី។ យើងរៀបចំមេគុណ និងទទួលបានរូបមន្តដែលត្រូវការ៖ Li 3 N ។
ដូច្នេះ សាមញ្ញណាស់ យើងបានរៀនពីរបៀបផ្សំរូបមន្តគីមី! ហើយសម្រាប់ការទន្ទេញចាំបានប្រសើរជាងមុននៃក្បួនដោះស្រាយសម្រាប់ការតែងរូបមន្ត យើងបានរៀបចំតំណាងក្រាហ្វិករបស់វា។
មេរៀននេះត្រូវបានឧទ្ទិសដល់ការរៀនច្បាប់នៃការគូរ និងអានរូបមន្តគីមីនៃសារធាតុ។ អ្នកនឹងរៀនអំពីព័ត៌មានដែលរូបមន្តគីមីនៃសារធាតុផ្តល់ និងរបៀបបង្កើតរូបមន្តគីមីដោយផ្អែកលើទិន្នន័យស្តីពីប្រភាគធំនៃធាតុគីមី។
ប្រធានបទ៖ គំនិតគីមីដំបូង
មេរៀន៖ រូបមន្តគីមីនៃសារធាតុមួយ។
រូបមន្តគីមីត្រូវបានប្រើដើម្បីកំណត់សារធាតុ។
រូបមន្តគីមី
គឺជាសញ្ញាណធម្មតានៃសមាសធាតុនៃសារធាតុដែលប្រើ សញ្ញាគីមីនិង សន្ទស្សន៍.
ការប្រើប្រាស់សន្ទស្សន៍ Y.Ya. Berzelius បានស្នើឱ្យកំណត់ចំនួនអាតូមនៃធាតុគីមីនៅក្នុងម៉ូលេគុលនៃសារធាតុមួយ។ ឧទាហរណ៍៖ ម៉ូលេគុលទឹកមានអាតូមអ៊ីដ្រូសែនពីរ និងអាតូមអុកស៊ីសែនមួយ - H 2 O (2 - សន្ទស្សន៍) ។ កាបូនឌីអុកស៊ីតមានអាតូមកាបូនមួយ និងអាតូមអុកស៊ីសែនពីរ - CO 2 ។ លិបិក្រមស្មើនឹងមួយមិនត្រូវបានសរសេរទេ។
លេខមុនរូបមន្តនៃសារធាតុត្រូវបានគេហៅថា មេគុណនិងបង្ហាញពីចំនួនម៉ូលេគុលនៃសារធាតុដែលបានផ្តល់ឱ្យ។ ឧទាហរណ៍ 4H 2 O - 4 ម៉ូលេគុលទឹក។ ម៉ូលេគុលទឹក 4 មានអាតូមអ៊ីដ្រូសែន 8 និងអាតូមអុកស៊ីសែន 4 ។
ការប្រើប្រាស់កាបូនឌីអុកស៊ីត CO 2 ជាឧទាហរណ៍ សូមឲ្យយើងពិចារណាអំពីព័ត៌មានអំពីសារធាតុដែលអាចទទួលបានពីរូបមន្តគីមីរបស់វា។
តារាងទី 1 ។
ដោយផ្អែកលើរូបមន្តគីមី អ្នកអាចគណនាប្រភាគធំនៃធាតុគីមីនៅក្នុងសារធាតុមួយ នេះនឹងត្រូវបានពិភាក្សានៅក្នុងសម្ភារៈនៃមេរៀនបន្ទាប់។
រូបមន្តគីមីត្រូវបានទាញយកដោយផ្អែកលើទិន្នន័យដែលទទួលបានដោយពិសោធន៍។ ប្រសិនបើធាតុនៅក្នុងសារធាតុមួយ និងសារធាតុដែលទាក់ទងត្រូវបានគេស្គាល់ នោះគេអាចរកឃើញចំនួនអាតូមនៃធាតុនីមួយៗនៅក្នុងម៉ូលេគុល។
ឧទាហរណ៍។គេស្គាល់ថាជាសាច់ញាតិ ម៉ាស់ម៉ូលេគុលកាបូនឌីអុកស៊ីតគឺ 44. ប្រភាគម៉ាសនៃអុកស៊ីសែននៅក្នុងសារធាតុនេះគឺ 0.727 (72.7%) នៅសល់គឺកាបូន។ ចូរយើងបង្កើតរូបមន្តគីមីនៃកាបូនឌីអុកស៊ីត។ ដើម្បីធ្វើដូចនេះអ្នកត្រូវការ:
1. កំណត់ម៉ាស់ក្នុងមួយចំណែកនៃអាតូមអុកស៊ីសែននៅក្នុងម៉ូលេគុល៖
44*0.727=32 (ឯកតាដែលទាក់ទង);
2. កំណត់ចំនួនអាតូមអុកស៊ីសែន ដោយដឹងថាម៉ាស់អាតូមដែលទាក់ទងនៃអុកស៊ីសែនគឺ 16៖
3. កំណត់ម៉ាស់ក្នុងមួយចំណែកនៃអាតូមកាបូន៖
44-32=12 (ឯកតាទាក់ទង);
4. កំណត់ចំនួនអាតូមកាបូន ដោយដឹងថាម៉ាស់អាតូមដែលទាក់ទងនៃកាបូនគឺ 12៖
5. បង្កើតរូបមន្តសម្រាប់កាបូនឌីអុកស៊ីត: CO 2 ។
1. បណ្តុំបញ្ហា និងលំហាត់គីមីវិទ្យា ថ្នាក់ទី៨៖ ដល់សៀវភៅសិក្សាដោយ P.A. Orzhekovsky និងអ្នកផ្សេងទៀត "គីមីវិទ្យាថ្នាក់ទី 8" / P.A. Orzhekovsky, N.A. Titov, F.F. ហេហ្គែល។ - M.: AST: Astrel, 2006. (ទំព័រ 26-28)
2. Ushakova O.V. សៀវភៅការងារគីមីវិទ្យា៖ ថ្នាក់ទី ៨ ដល់សៀវភៅសិក្សាដោយ P.A. Orzhekovsky និងអ្នកដទៃ។ ថ្នាក់ទី ៨” / O.V. Ushakova, P.I. Bespalov, P.A. អ័រហ្សេកូវស្គី; ក្រោម។ ed ។ សាស្រ្តាចារ្យ P.A. Orzhekovsky - M.: AST: Astrel: Profizdat, 2006. (ទំព័រ 32-34)
៣.គីមីវិទ្យា៖ ថ្នាក់ទី៨៖ សៀវភៅសិក្សា។ សម្រាប់ការអប់រំទូទៅ ស្ថាប័ន / P.A. Orzhekovsky, L.M. Meshcheryakova, L.S. ផុនតាក់។ M.: AST: Astrel, 2005.(§14)
4. គីមីវិទ្យា៖ inorg ។ គីមីវិទ្យា៖ សៀវភៅសិក្សា។ សម្រាប់ថ្នាក់ទី ៨ ។ ការអប់រំទូទៅ ស្ថាប័ន / G.E. Rudzitis, Fyu Feldman ។ - អិមៈ ការអប់រំ, OJSC “សៀវភៅសិក្សាទីក្រុងម៉ូស្គូ”, ឆ្នាំ ២០០៩។ (§១០)
5. សព្វវចនាធិប្បាយសម្រាប់កុមារ។ ភាគ 17. គីមីវិទ្យា / ជំពូក។ ed.V.A. Volodin, Ved ។ វិទ្យាសាស្ត្រ ed ។ I. លីសុន។ - អិមៈ Avanta+ ឆ្នាំ ២០០៣។
ធនធានគេហទំព័របន្ថែម
1. ការប្រមូលផ្តុំបង្រួបបង្រួមនៃធនធានអប់រំឌីជីថល () ។
2. កំណែអេឡិចត្រូនិចទស្សនាវដ្តី "គីមីវិទ្យានិងជីវិត" () ។
កិច្ចការផ្ទះ
1. p.77 លេខ 3ពីសៀវភៅសិក្សា "គីមីវិទ្យា៖ ថ្នាក់ទី ៨" (P.A. Orzhekovsky, L.M. Meshcheryakova, L.S. Pontak. M.: AST: Astrel, 2005) ។
2. ជាមួយ។ ៣២-៣៤ លេខ ៣,៤,៦,៧ពី សៀវភៅការងារគីមីវិទ្យា៖ ថ្នាក់ទី ៨៖ ដល់សៀវភៅសិក្សា P.A. Orzhekovsky និងអ្នកដទៃ។ ថ្នាក់ទី ៨” / O.V. Ushakova, P.I. Bespalov, P.A. អ័រហ្សេកូវស្គី; ក្រោម។ ed ។ សាស្រ្តាចារ្យ P.A. Orzhekovsky - M.: AST: Astrel: Profizdat, 2006 ។