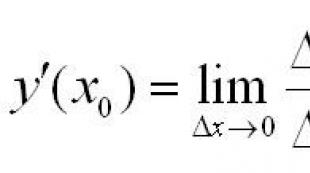Halogenų fizinės ir cheminės savybės. Halogenai ir jų junginiai. Halogeniniai junginiai ir jų vaidmuo žmogaus organizme
Halogenai– VII grupės elementai – fluoras, chloras, bromas, jodas, astatinas (astatinas dėl radioaktyvumo mažai ištirtas). Halogenai yra skirtingi nemetalai. Tik jodas retais atvejais pasižymi kai kuriomis savybėmis, panašiomis į metalus.
Nesužadintoje būsenoje halogeno atomai turi bendrą elektroninę konfigūraciją: ns2np5. Tai reiškia, kad halogenai turi 7 valentinius elektronus, išskyrus fluorą.
Fizinės halogenų savybės: F2 – bespalvės, sunkiai suskystintos dujos; Cl2 yra gelsvai žalios, lengvai suskystintos dujos, turinčios aštrų dusinantį kvapą; Br2 – raudonai rudas skystis; I2 yra violetinė kristalinė medžiaga.

Vandeniniai vandenilio halogenidų tirpalai sudaro rūgštis. HF – vandenilio fluoridas (fluoridas); HCl – druskos (druska); НBr – vandenilio bromidas; HI – vandenilio jodidas. Rūgščių stiprumas mažėja iš viršaus į apačią. Vandenilio fluorido rūgštis yra silpniausia halogenintų rūgščių serijoje, o vandenilio jodo rūgštis yra stipriausia. Tai paaiškinama tuo, kad Hg surišimo energija mažėja iš viršaus. NG molekulės stiprumas mažėja ta pačia kryptimi, o tai susiję su tarpbranduolinio atstumo padidėjimu. Mažėja ir mažai tirpių druskų tirpumas vandenyje:
Iš kairės į dešinę mažėja halogenidų tirpumas. AgF gerai tirpsta vandenyje. Visi laisvos būsenos halogenai yra oksidatoriai. Jų, kaip oksidatorių, stiprumas sumažėja nuo fluoro iki jodo. Kristalinėje, skystoje ir dujinėje būsenose visi halogenai egzistuoja atskirų molekulių pavidalu. Atominiai spinduliai didėja ta pačia kryptimi, todėl padidėja lydymosi ir virimo taškai. Fluoras geriau skaidosi į atomus nei jodas. Judant žemyn halogeno pogrupiu, elektrodų potencialai mažėja. Fluoras turi didžiausią elektrodo potencialą. Fluoras yra stipriausias oksidatorius. Bet koks aukštesnis laisvas halogenas išstums žemesnįjį, kuris tirpale yra neigiamo vieno krūvio jono būsenoje.
20. Chloras. Vandenilio chloridas ir druskos rūgštis
Chloras (Cl) - stovi 3 periode, periodinės sistemos pagrindinio pogrupio VII grupėje, eilės numeris 17, atominė masė 35,453; reiškia halogenus.
Fizinės savybės: geltonai žalios aitraus kvapo dujos. Tankis 3,214 g/l; lydymosi temperatūra -101 °C; virimo temperatūra -33,97 °C, Įprastoje temperatūroje lengvai suskystėja esant 0,6 MPa slėgiui. Ištirpęs vandenyje, susidaro gelsvas chloro vanduo. Jis gerai tirpsta organiniuose tirpikliuose, ypač heksane (C6H14) ir anglies tetrachloride.
Cheminės chloro savybės: elektroninė konfigūracija: 1s22s22p63s22p5. Išoriniame lygyje yra 7 elektronai. Norėdami užbaigti lygį, jums reikia 1 elektrono, kurį priima chloras, kurio oksidacijos būsena yra -1. Taip pat yra teigiamų chloro oksidacijos būsenų iki + 7. Žinomi šie chloro oksidai: Cl2O, ClO2, Cl2O6 ir Cl2O7. Jie visi yra nestabilūs. Chloras yra stiprus oksidatorius. Jis tiesiogiai reaguoja su metalais ir nemetalais:
Reaguoja su vandeniliu. Normaliomis sąlygomis reakcija vyksta lėtai, stipriai kaitinant ar apšviečiant - sprogus, pagal grandinės mechanizmą:
![]()
Chloras sąveikauja su šarminiais tirpalais, sudarydamas druskas - hipochloritus ir chloridus:
Kai chloras patenka į šarminį tirpalą, susidaro chlorido ir hipochlorito tirpalų mišinys:
Chloras yra reduktorius: Cl2 + 3F2 = 2ClF3.
Sąveika su vandeniu:
Chloras tiesiogiai nereaguoja su anglimi, azotu ir deguonimi.
Kvitas: 2NaCl + F2 = 2NaF + Cl2.
Elektrolizė: 2NaCl + 2H2O = Cl2 + H2 + 2NaOH.
Rasti gamtoje: yra šiuose mineraluose: halitas (akmens druska), silvitas, bischofitas; jūros vandenyje yra natrio, kalio, magnio ir kitų elementų chloridų.
Vandenilio chloridas HCl. Fizinės savybės: bespalvės dujos, sunkesnės už orą, gerai tirpios vandenyje, sudarydamos druskos rūgštį.
Kvitas: laboratorijoje:
Pramonėje: vandenilis deginamas chloro sraute. Tada vandenilio chloridas ištirpinamas vandenyje, kad susidarytų druskos rūgštis (žr. aukščiau).
Cheminės savybės: druskos rūgštis yra stipri, vienabazė, sąveikauja su metalais įtampos serijoje iki vandenilio: Zn + 2HCl = ZnCl2 + H2.
Kaip reduktorius, jis reaguoja su daugelio metalų oksidais ir hidroksidais.
Elementų chemija
VIIA pogrupio nemetalai
VIIA pogrupio elementai yra tipiški nemetalai su aukštu
elektronegatyvumas, jie turi grupės pavadinimą - „halogenai“.
Pagrindinės paskaitoje nagrinėjamos problemos
Bendrosios VIIA pogrupio nemetalų charakteristikos. Elektroninė sandara, svarbiausios atomų charakteristikos. Būdingiausias ste-
oksidacijos baudos. Halogenų chemijos ypatybės.
Paprastos medžiagos.
Natūralūs junginiai.
Halogeniniai junginiai
Hidrohalogeninės rūgštys ir jų druskos. Druska ir vandenilio fluorido rūgštis
laiko tarpsniai, kvitas ir paraiška.
Halogenidų kompleksai.
Dvejetainiai halogenų deguonies junginiai. Nestabilumas apytiksl.
Paprastų medžiagų redoksinės savybės ir
vienybės. Disproporcingumo reakcijos. Latimerų diagramos.
Vykdytojas: |
Renginio Nr. |
||||||||||||||||

VIIA pogrupio elementų chemija
bendrosios charakteristikos
Manganas |
||||||||
Techneciumas |
||||||||
VIIA-grupę sudaro p-elementai: fluoras F, chloras
Cl, bromas Br, jodas I ir astatinas At.
Bendroji valentinių elektronų formulė yra ns 2 np 5.
Visi VIIA grupės elementai yra tipiški nemetalai.
Kaip matyti iš paskirstymo |
|||||||
valentiniai elektronai |
|||||||
pagal atomų orbitales |
trūksta tik vieno elektrono |
||||||
stabiliam aštuonių elektronų apvalkalo susidarymui
dėžės, todėl ir turi yra stipri tendencija
elektrono pridėjimas.
Visi elementai lengvai sudaro paprastą vieną įkrovimą
ny anijonai G – .
Paprastų anijonų pavidalu VIIA grupės elementai randami natūraliame vandenyje ir natūralių druskų kristaluose, pavyzdžiui, halitas NaCl, silvitas KCl, fluoritas
CaF2.
Bendras elementų grupės pavadinimas VIIA-
„halogenų“ grupė, t.
yra tipinė druska (CaF2, NaCl, MgBr2, KI), kuri
kurią galima gauti tiesioginės sąveikos būdu
metalo sąveika su halogenu. Laisvieji halogenai gaunami iš natūralių druskų, todėl pavadinimas „halogenai“ taip pat verčiamas kaip „gimę iš druskų“.
Vykdytojas: |
Renginio Nr. |
||||||||||||||||

Mažiausia oksidacijos būsena (–1) yra stabiliausia
visiems halogenams.
Pateikiamos kai kurios VIIA grupės elementų atomų charakteristikos
Svarbiausios VIIA grupės elementų atomų charakteristikos
giminaitis- |
Giminingumas |
||||||
elektrinis |
|||||||
neigiamas |
jonizacija, |
||||||
ness (pagal |
|||||||
apklausa) |
|||||||
skaičiaus padidėjimas |
|||||||
elektroniniai sluoksniai; |
|||||||
dydžio padidėjimas |
|||||||
elektros sumažinimas |
|||||||
trigubas negatyvumas |
Halogenai turi didelį elektronų afinitetą (didžiausias at
Cl) ir labai didelė jonizacijos energija (maksimali esant F) ir didžiausia
galimas elektronegatyvumas kiekviename periode. Daugiausia yra fluoro
visų cheminių elementų elektronneigiamas.
Vieno nesuporuoto elektrono buvimas halogeno atomuose lemia
reiškia atomų susijungimą paprastose medžiagose į dviatomes molekules Г2.
Paprastoms medžiagoms, halogenams, būdingiausi oksidatoriai
savybės, kurios yra stipriausios F2 ir susilpnėja pereinant prie I2.
Halogenai pasižymi didžiausiu reaktyvumu iš visų nemetalinių elementų. Fluoras net tarp halogenų išsiskiria
pasižymi itin dideliu aktyvumu.
Stipriausiai nuo kito skiriasi antrojo laikotarpio elementas fluoras
kiti pogrupio elementai. Tai yra bendras visų nemetalų modelis.
Vykdytojas: |
Renginio Nr. |
||||||||||||||||
Fluoras, kaip labiausiai elektroneigiamas elementas, nerodo sekso
nuolatinės oksidacijos būsenos. Bet kokiu ryšiu, įskaitant su ki-
deguonies, fluoras yra oksidacijos būsenoje (-1).
Visi kiti halogenai pasižymi teigiamu oksidacijos laipsniu
leniya iki maksimumo +7.
Būdingiausios halogenų oksidacijos būsenos:
F: -1, 0;
Cl, Br, I: -1, 0, +1, +3, +5, +7.
Cl turi žinomų oksidų, kuriuose jis randamas oksidacijos būsenose: +4 ir +6.
Svarbiausi halogenų junginiai teigiamos būsenos,
Oksidacijos pasekmės yra deguonies turinčios rūgštys ir jų druskos.
Visi halogeniniai junginiai, esantys teigiamos oksidacijos būsenos, yra
yra stiprūs oksidatoriai.
baisus oksidacijos laipsnis. Disproporcingumą skatina šarminė aplinka.
Paprastų medžiagų ir deguonies junginių praktinis pritaikymas
Halogenų redukciją daugiausia lemia jų oksidacinis poveikis.
Paprasčiausios medžiagos, Cl2, randa plačiausią praktinį pritaikymą.
ir F2. Daugiausia chloro ir fluoro sunaudojama pramonėje
organinė sintezė: gaminant plastikus, šaltnešius, tirpiklius,
pesticidai, vaistai. Nemažai chloro ir jodo sunaudojama metalams gauti ir jų valymui. Taip pat naudojamas chloras
celiuliozės balinimui, geriamojo vandens dezinfekcijai ir gamyboje
baliklio ir druskos rūgšties vanduo. Sprogmenų gamyboje naudojamos okso rūgščių druskos.
Vykdytojas: |
Renginio Nr. |
||||||||||||||||

Rūgštys - druskos ir išlydytos rūgštys - yra plačiai naudojamos praktikoje.
Fluoras ir chloras priklauso dvidešimt labiausiai paplitusių elementų
ten bromo ir jodo gamtoje žymiai mažiau. Visi halogenai gamtoje randami oksidacijos būsenose(-1). Tik jodas yra druskos KIO3 pavidalu,
kuri yra įtraukta į Čilės salietrą (KNO3) kaip priemaiša.
Astatinas yra dirbtinai pagamintas radioaktyvus elementas (gamtoje jo nėra). At nestabilumas atsispindi pavadinime, kuris kilęs iš graikų kalbos. „astatos“ – „nestabilus“. Astatinas yra patogus spinduliuotės šaltinis vėžio navikų radioterapijai.
Paprastos medžiagos
Paprastas halogenų medžiagas sudaro dviatomės molekulės G2.
Paprastose medžiagose, pereinant iš F2 į I2, padidėjus elektronų skaičiui
sosto sluoksniai ir didėja atomų poliarizacija, didėja
tarpmolekulinė sąveika, dėl kurios pasikeičia bendras
stovi standartinėmis sąlygomis.
Fluoras (normaliomis sąlygomis) yra geltonos dujos, prie –181o C virsta
skysta būsena.
Chloras yra geltonai žalios dujos, kurios –34o C temperatūroje virsta skysčiais.
Su juo siejamas pavadinimas Cl, kilęs iš graikų „chloros“ – „geltonas-
žalias". Staigus Cl2 virimo temperatūros padidėjimas, palyginti su F2,
rodo padidėjusią tarpmolekulinę sąveiką.
Bromas yra tamsiai raudonas, labai lakus skystis, verda 58,8o C temperatūroje.
elemento pavadinimas siejamas su aštriu nemaloniu dujų kvapu ir yra kilęs iš
„bromos“ – „dvokiantis“.
Jodas – tamsiai violetiniai kristalai su silpnu „metaliniu“
gumulėlių, kurie kaitinant lengvai sublimuojasi, sudarydami violetinius garus;
su greitu aušinimu |
garai iki 114o C |
susidaro skystis. Temperatūra |
|||||||||||||||||
Vykdytojas: |
Renginio Nr. |
||||||||||||||||||
Jodo virimo temperatūra yra 183 ° C. Jo pavadinimas kilęs nuo jodo garų spalvos -
"jodos" - "violetinė".
Visos paprastos medžiagos turi aštrų kvapą ir yra nuodingos.
Įkvėpus jų garų, dirginama gleivinė ir kvėpavimo organai, o esant didelei koncentracijai – uždusimas. Pirmojo pasaulinio karo metais chloras buvo naudojamas kaip nuodinga medžiaga.
Fluoro dujos ir skystas bromas sukelia odos nudegimus. Darbas su ha-
logens, reikia imtis atsargumo priemonių.
Kadangi paprastas halogenų medžiagas sudaro nepolinės molekulės
vėsina, gerai tirpsta nepoliniuose organiniuose tirpikliuose:
alkoholis, benzenas, anglies tetrachloridas ir kt. Chloras, bromas ir jodas mažai tirpsta vandenyje, jų vandeniniai tirpalai vadinami chloro, bromo ir jodo vandeniu. Br2 tirpsta geriau nei kiti, bromo koncentracija sat.
Tirpalas pasiekia 0,2 mol/l, o chloras – 0,1 mol/l.
Fluoras skaido vandenį:
2F2 + 2H2 O = O2 + 4HF
Halogenai pasižymi dideliu oksidaciniu aktyvumu ir perėjimu
į halogenidų anijonus.
Г2 + 2e– 2Г–
Fluoras turi ypač didelį oksidacinį aktyvumą. Fluoras oksiduoja tauriuosius metalus (Au, Pt).
Pt + 3F2 = PtF6
Jis netgi sąveikauja su kai kuriomis inertinėmis dujomis (kriptonu,
ksenonas ir radonas), pavyzdžiui,
Xe + 2F2 = XeF4
F2 atmosferoje dega daug labai stabilių junginių, pvz.
vanduo, kvarcas (SiO2).
SiO2 + 2F2 = SiF4 + O2
Vykdytojas: |
Renginio Nr. |
||||||||||||||||

Reakcijose su fluoru, net tokie stiprūs oksidatoriai kaip azotas ir siera
niko rūgštis, veikia kaip reduktorius, o fluoras oksiduoja įvestą medžiagą
kurių sudėtyje yra O(–2).
2HNO3 + 4F2 = 2NF3 + 2HF + 3O2 H2SO4 + 4F2 = SF6 + 2HF + 2O2
Didelis F2 reaktyvumas sukelia sunkumų pasirenkant
konstrukcinės medžiagos darbui su juo. Paprastai šiems tikslams naudojame
Yra nikelio ir vario, kurie oksiduodami savo paviršiuje sudaro tankias apsaugines fluoridų plėveles. Pavadinimas F atsirado dėl jo agresyvaus veikimo.
Aš valgau, jis kilęs iš graikų kalbos. „fluoros“ – „destruktyvus“.
Serijose F2, Cl2, Br2, I2 oksidacijos gebėjimas susilpnėja dėl padidėjimo
didinant atomų dydį ir mažinant elektronegatyvumą.
Vandeniniuose tirpaluose medžiagos oksidacinės ir redukcinės savybės
Medžiagos paprastai apibūdinamos naudojant elektrodų potencialus. Lentelėje pateikti standartiniai elektrodų potencialai (Eo, V) redukcijos pusinėms reakcijoms
halogenų susidarymas. Palyginimui, Eo vertė ki-
anglis yra labiausiai paplitęs oksidatorius.
Paprastų halogeninių medžiagų standartiniai elektrodų potencialai
Eo, B, už reakciją |
|||||||||||||
O2 + 4e– + 4H+ 2H2 O |
|||||||||||||
Eo, V |
|||||||||||||
elektrodui |
|||||||||||||
2Г– +2е – = Г2 |
|||||||||||||
Sumažėjęs oksidacinis aktyvumas
Kaip matyti iš lentelės, F2 yra daug stipresnis oksidatorius,
nei O2, todėl F2 vandeniniuose tirpaluose neegzistuoja , oksiduoja vandenį,
atsigauna į F–. Sprendžiant pagal Eо reikšmę, Cl2 oksidacinis gebėjimas
Vykdytojas: |
Renginio Nr. |
||||||||||||||||
taip pat didesnis nei O2. Iš tiesų, ilgai laikant chloro vandenį, jis suyra, išsiskiriant deguoniui ir susidaro HCl. Tačiau reakcija yra lėta (Cl2 molekulė yra pastebimai stipresnė nei F2 molekulė ir
aktyvacijos energija reakcijai su chloru yra didesnė), dispro-
porcijavimas:
Cl2 + H2 O HCl + HOCl
Vandenyje jis nepasiekia galo (K = 3,9 . 10–4), todėl vandeniniuose tirpaluose Cl2 yra. Br2 ir I2 pasižymi dar didesniu stabilumu vandenyje.
Disproporcija yra labai būdinga oksidacija.
halogenų redukcijos reakcija. Stiprinimo neproporcingumas
liejasi šarminėje aplinkoje.
Dėl Cl2 disproporcijos šarme susidaro anijonai
Cl– ir ClO–. Disproporcingumo konstanta lygi 7,5. 1015 m.
Cl2 + 2NaOH = NaCl + NaClO + H2O
Kai jodas yra neproporcingas šarmams, susidaro I– ir IO3–. Ana-
Logiškai mąstant, Br2 neproporcuoja jodo. Produkto pakeitimas yra neproporcingas
tauta yra dėl to, kad Br ir I anijonai GO– ir GO2– yra nestabilūs.
Chloro disproporcijos reakcija naudojama pramonėje
gebėjimas gauti stiprų ir greitai veikiantį hipochlorito oksidatorių,
balinamosios kalkės, bertoleto druska.
3Cl2 + 6 KOH = 5KCl + KClO3 + 3H2O
Vykdytojas: |
Renginio Nr. |
||||||||||||||||
Halogenų sąveika su metalais
Halogenai intensyviai reaguoja su daugeliu metalų, pavyzdžiui:
Mg + Cl2 = MgCl2 Ti + 2I2 TiI4
Na + halogenidai, kuriuose metalas turi žemą oksidacijos laipsnį (+1, +2),
– Tai į druskas panašūs junginiai, kuriuose vyrauja joninės jungtys. Kaip
štai, joniniai halogenidai yra kietos medžiagos, kurių lydymosi temperatūra yra aukšta
Metalų halogenidai, kuriuose metalas turi aukštą oksidacijos laipsnį
Tai junginiai, kuriuose vyrauja kovalentiniai ryšiai.
Daugelis jų yra dujos, skysčiai arba įprastomis sąlygomis tirpios kietosios medžiagos. Pavyzdžiui, WF6 yra dujos, MoF6 yra skystis,
TiCl4 yra skystas.
Halogenų sąveika su nemetalais
Halogenai tiesiogiai sąveikauja su daugeliu nemetalų:
vandenilis, fosforas, siera ir kt. Pavyzdžiui:
H2 + Cl2 = 2HCl 2P + 3Br2 = 2PBr3 S + 3F2 = SF6
Nemetalų halogenidų jungtis daugiausia yra kovalentinė.
Paprastai šie junginiai turi žemą lydymosi ir virimo temperatūrą.
Pereinant iš fluoro į jodą, didėja kovalentinis halogenidų pobūdis.
Tipiškų nemetalų kovalentiniai halogenidai yra rūgštiniai junginiai; sąveikaudami su vandeniu jie hidrolizuojasi ir susidaro rūgštys. Pavyzdžiui:
PBr3 + 3H2O = 3HBr + H3PO3
PI3 + 3H2 O = 3HI + H3 PO3
PCl5 + 4H2O = 5HCl + H3PO4
Vykdytojas: |
Renginio Nr. |
||||||||||||||||

Pirmosios dvi reakcijos naudojamos bromo ir vandenilio jodido gamybai.
triukšmo rūgštis.
Interhalidai. Halogenai, jungdamiesi vienas su kitu, sudaro interg-
veda. Šiuose junginiuose lengvesnis ir elektronegatyvesnis halogenas yra (–1) oksidacijos būsenos, o sunkesnis – teigiamos.
oksidacijos baudos.
Dėl tiesioginės halogenų sąveikos kaitinant gaunami: ClF, BrF, BrCl, ICl. Taip pat yra sudėtingesnių interhalogenidų:
ClF3, BrF3, BrF5, IF5, IF7, ICl3.
Visi interhalogenidai normaliomis sąlygomis yra skystos medžiagos, kurių virimo temperatūra žema. Interhalogenidai pasižymi dideliu oksidaciniu aktyvumu
veikla. Pavyzdžiui, ClF3 garuose dega tokios chemiškai stabilios medžiagos kaip SiO2, Al2 O3, MgO ir kt.
2Al2 O3 + 4ClF3 = 4 AlF3 + 3O2 + 2Cl2
Fluoride ClF 3 yra agresyvus fluorinantis reagentas, kuris veikia greitai
kiemas F2. Jis naudojamas organinėje sintezėje ir apsauginėms plėvelėms gauti ant nikelio įrangos, skirtos darbui su fluoru, paviršiaus.
Vandenyje interhalogenidai hidrolizuojasi, sudarydami rūgštis. Pavyzdžiui,
ClF5 + 3H2O = HClO3 + 5HF
Halogenai gamtoje. Paprastų medžiagų gavimas
Pramonėje halogenai gaunami iš jų natūralių junginių. Visi
laisvųjų halogenų gavimo procesai yra pagrįsti halogeno oksidacija
Nid jonai.
2Г – Г2 + 2e–
Nemaža dalis halogenų natūraliuose vandenyse randama anijonų pavidalu: Cl–, F–, Br–, I–. Jūros vandenyje gali būti iki 2,5 % NaCl.
Bromas ir jodas gaunami iš naftos gręžinių vandens ir jūros vandens.
Vykdytojas: |
Renginio Nr. |
||||||||||||||||
Halogenai fluoras F, chloras C1, bromas Br, jodas I yra VILA grupės elementai. Elektroninė halogeno atomų valentinio apvalkalo konfigūracija pagrindinėje būsenoje ns 2 np 5 . Penkių elektronų buvimas išorinėje p orbitoje, įskaitant vieną nesuporuotą, yra didelio halogenų elektronų giminingumo priežastis. Pridėjus elektroną, susidaro halogenidų anijonai (F-, Cl-, Br-, I-) su stabiliu artimiausių tauriųjų dujų 8 elektronų apvalkalu. Halogenai yra skirtingi nemetalai.
Labiausiai elektronegatyvus elementas, fluoras, junginiuose turi tik vieną oksidacijos būseną - 1, nes jis visada yra elektronų akceptorius. Kiti junginiuose esantys halogenai gali turėti oksidacijos laipsnius nuo -1 iki +7. Halogenų teigiamas oksidacijos būsenas lemia jų valentinių elektronų perėjimas į išorinio lygmens laisvąsias d-orbitales (2.1.3 skyrius), kai susidaro ryšiai su elektronegatyvesniais elementais.
Halogeno molekulės yra dviatomės: F 2, C1 2, Br 2, I 2. Standartinėmis sąlygomis fluoras ir chloras yra dujos, bromas – lakus skystis (Tbp = 59 °C), o jodas – kietas, tačiau lengvai sublimuojasi (virsta į dujinę būseną, apeidamas skystą).
Redokso savybės. Halogenai yra stiprūs oksidatoriai, reaguojantys su beveik visais metalais ir daugeliu nemetalų:
Fluoras pasižymi ypač dideliu cheminiu aktyvumu, kuris kaitinant reaguoja net su inercinėmis dujomis ksenonu, kriptonu ir radonu:
![]()
Cheminis halogenų aktyvumas mažėja nuo fluoro iki jodo, nes didėjant atominiam spinduliui mažėja halogenų gebėjimas prijungti elektronus:

Aktyvesnis halogenas visada išstumia mažiau aktyvųjį iš jo junginių su metalais. Taigi fluoras išstumia visus kitus halogenus iš jų halogenidų, o bromas iš jodidų išstumia tik jodą:
Skirtingos halogenų oksidacinės savybės pasireiškia ir jų poveikiu organizmui. Dujinis chloras ir fluoras dėl savo labai stiprių oksiduojančių savybių yra galingos toksinės medžiagos, stipriai pažeidžiančios plaučius bei akių, nosies ir gerklų gleivines. Jodas yra švelnesnis oksidatorius, pasižymintis antiseptinėmis savybėmis, todėl plačiai naudojamas medicinoje.
Halogenų redoksinių savybių skirtumai atsiranda ir jiems sąveikaujant su vandeniu. Fluoras oksiduoja vandenį, o reduktorius yra vandens molekulės deguonies atomas:
Kitų halogenų sąveiką su vandeniu lydi jų atomų redokso dismutacija. Taigi, chlorui reaguojant su vandeniu, vienas iš chloro molekulės atomų, gaudamas elektroną iš kito atomo, redukuojasi, o kitas chloro atomas, atiduodamas elektroną, oksiduojasi. Tai sukuria chloro vanduo, kurių sudėtyje yra vandenilio chlorido (vandenilio chlorido rūgšties) ir hipochlorinės (hipochlorinės) rūgšties:
Reakcija yra grįžtama, o jos pusiausvyra stipriai pasislenka į kairę. Hipochloro rūgštis yra nestabili ir lengvai suyra, ypač šviesoje, susidarant labai stipriam oksiduojančiam agentui - atominiam deguoniui:
Taigi chloro vandenyje skirtingomis koncentracijomis yra trys oksidatoriai, turintys skirtingą oksidacinį gebėjimą: molekulinis chloras, hipochlorinė rūgštis ir atominis deguonis, kurių suma dažnai vadinama "aktyvus chloras".
Susidaręs atominis deguonis balina dažus ir naikina mikrobus, o tai paaiškina chloro vandens balinimą ir baktericidinį poveikį.
Hipochloro rūgštis yra stipresnis oksidatorius nei chloro dujos. Jis reaguoja su organiniais junginiais RH ir kaip oksidatorius, ir kaip chlorinimo reagentas:
Todėl geriant vandenį, kuriame priemaišų yra organinių medžiagų, jie gali virsti toksiškesniais organiniais chloro junginiais RC1. Į tai tikrai reikėtų atsižvelgti kuriant vandens valymo metodus ir juos taikant.
Kai į chloro vandenį pridedama šarmo, pusiausvyra pasislenka į dešinę dėl hipochloro ir druskos rūgščių neutralizavimo:
Gautas druskų mišinio tirpalas, vadinamas Javelinis vanduo, naudojamas kaip balinimo ir dezinfekavimo priemonė. Šios savybės atsiranda dėl to, kad kalio hipochloritas, veikiamas CO2 + H 2 0 ir dėl hidrolizės, virsta nestabilia hipochlorine rūgštimi, sudarydama atominį deguonį. Dėl to Javel vanduo sunaikina dažus ir naikina mikrobus.
Dujiniam chlorui veikiant šlapias gesintas kalkes Ca(OH) 2, gaunamas druskų CaCl 2 ir Ca(0C1) 2 mišinys, vadinamas baliklis:
Kalkių chloridas gali būti laikomas mišria druskos ir hipochloro rūgščių CaCl(OCl) kalcio druska. Drėgname ore baliklis, sąveikaudamas su vandeniu ir anglies dioksidu, palaipsniui išskiria hipochloro rūgštį, kuri suteikia balinimo, dezinfekavimo ir degazavimo savybes:
Kai baliklis yra veikiamas druskos rūgšties, išsiskiria laisvas chloras:
Kaitinant, hipochloro rūgštis skyla dėl redokso disproporcijos ir susidaro druskos ir perchloro rūgštys:
![]()
Kai chloras praleidžiamas per karštą šarmo tirpalą, pvz., KOH, susidaro kalio chloridas ir kalio chloratas KClO 3 (Bertholet druska):
Deguonies turinčių chloro rūgščių anijonų oksidacinis gebėjimas vandeniniuose tirpaluose serijoje СlO - - СlO4(-) mažėja, nepaisant padidėjusio chloro oksidacijos laipsnio juose:
![]()
Tai paaiškinama padidėjusiu anijonų stabilumu šioje serijoje dėl padidėjusio jų neigiamo krūvio delokalizacijos. Tuo pačiu metu LiC10 4 ir KClO 4 perchloratai sausoje būsenoje aukštoje temperatūroje yra stiprūs oksidatoriai ir naudojami įvairių biomedžiagų mineralizacijai, nustatant juose esančius neorganinius komponentus.
Halogenų anijonai (išskyrus F-) gali atiduoti elektronus, todėl jie yra reduktorius. Didėjant jų spinduliui, halogenidų anijonų redukcinis gebėjimas didėja nuo chlorido anijono iki jodido anijono:

Taigi, vandenilio jodo rūgštis oksiduojasi atmosferos deguonimi jau esant normaliai temperatūrai:
![]()
Vandenilio chlorido rūgšties deguonis neoksiduoja, todėl chlorido anijonas yra stabilus organizmo sąlygomis, o tai labai svarbu fiziologijos ir medicinos požiūriu.
Rūgščių-šarmų savybės. Vandenilio halogenidai HF, HC1, HBr, HI dėl savo molekulių poliškumo labai gerai tirpsta vandenyje. Šiuo atveju vyksta molekulių hidratacija, dėl kurios jos atsiskiria su hidratuotų protonų ir halogenidų anijonų susidarymu. Rūgščių stiprumas serijose HF, HC1, HBr, HI didėja dėl anijonų spindulio ir poliarizacijos padidėjimo nuo F- iki I-.
Vandenilio chlorido rūgštis, kaip skrandžio sulčių sudedamoji dalis, vaidina svarbų vaidmenį virškinimo procese. Daugiausia dėl druskos rūgšties, kurios masės dalis skrandžio sultyse yra 0,3 %, jos pH palaikomas intervale nuo 1 iki 3. Druskos rūgštis skatina pepsino fermento perėjimą į aktyvią formą, kuri užtikrina baltymų virškinimą. dėl hidrolizinio peptidinių jungčių skilimo, susidarant įvairioms aminorūgštims:
Skyriuje buvo aptartas druskos rūgšties ir kitų rūgščių kiekio nustatymas skrandžio sultyse. 8.3.3.
Chloro rūgščių, kurių sudėtyje yra deguonies, serijoje, didėjant jo oksidacijos laipsniui, rūgščių stiprumas didėja.

Taip yra dėl padidėjusio O-H jungties poliškumo dėl jo elektronų tankio poslinkio link chloro atomo, taip pat dėl padidėjusio anijonų stabilumo.
Kompleksinės savybės. Halogenų anijonai linkę sudaryti kompleksus kaip ligandai. Halogenidų kompleksų stabilumas paprastai mažėja F- > Cl- > Br- > > I- tvarka. Būtent kompleksavimo procesas paaiškina toksinį fluoro anijonų poveikį, kurie, sudarydami fluoro kompleksus su metalų katijonais, įtrauktais į aktyvius fermentų centrus, slopina jų aktyvumą.
Jodo molekulė pasižymi įdomiomis kompleksą formuojančiomis savybėmis. Taigi molekulinio jodo tirpumas vandenyje smarkiai padidėja esant kalio jodidui, kuris yra susijęs su kompleksinio anijono susidarymu.
Mažas šio sudėtingo jono stabilumas užtikrina molekulinio jodo buvimą tirpale. Todėl medicinoje kaip baktericidinis agentas naudojamas vandeninis jodo tirpalas, pridedant KI. Be to, molekulinis jodas sudaro inkliuzinius kompleksus su krakmolu (22.3 skirsnis) ir polivinilo alkoholiu (mėlynas jodas).Šiuose kompleksuose jodo molekulės arba jų junginiai su jodido anijonais užpildo kanalus, suformuotus atitinkamų polihidroksipolimerų spiralinės struktūros. Inkliuziniai kompleksai nėra labai stabilūs ir gali palaipsniui išskirti molekulinį jodą. Todėl toks vaistas kaip mėlynasis jodas yra veiksminga, bet švelni, ilgai veikianti baktericidinė priemonė.
Biologinis halogenų ir jų junginių vaidmuo ir panaudojimas medicinoje.Įvairių junginių pavidalo halogenai yra gyvų audinių dalis. Organizme visų halogenų oksidacijos būsena yra 1. Tuo pačiu metu chloras ir bromas egzistuoja hidratuotų Cl- ir Br- anijonų pavidalu, o fluoras ir jodas yra vandenyje netirpių biosubstratų dalis:
Fluoro junginiai yra kaulinio audinio, nagų ir dantų sudedamosios dalys. Biologinis fluoro poveikis pirmiausia siejamas su dantų ligų problema. Fluoro anijonas, pakeičiantis hidroksido joną hidroksiapatite, sudaro apsauginį emalio sluoksnį iš kieto fluorapatito:
Geriamojo vandens fluoravimas iki 1 mg/l fluoro jonų koncentracijos ir natrio fluorido pridėjimas į dantų pastą ženkliai sumažina gyventojų dantų ėduonį. Tuo pačiu metu, kai fluoro anijono koncentracija geriamajame vandenyje yra didesnė nei 1,2 mg/l, didėja kaulų ir dantų emalio trapumas, atsiranda bendras organizmo išsekimas, vadinamasis. fluorozė.
Chloridų anijonai užtikrina jonų srautus per ląstelių membranas, dalyvauja palaikant osmosinę homeostazę, sukuria palankią aplinką skrandžio sulčių protolitinių fermentų veikimui ir aktyvavimui.
Bromido anijonai žmogaus organizme yra lokalizuoti daugiausia hipofizėje ir kitose endokrininėse liaukose. Buvo nustatytas dinaminis ryšys tarp bromido ir chlorido anijonų kiekio organizme. Taigi padidėjęs bromido anijonų kiekis kraujyje skatina greitą chlorido anijonų išsiskyrimą per inkstus. Bromidai daugiausia lokalizuoti tarpląsteliniame skystyje. Jie sustiprina slopinamuosius procesus smegenų žievės neuronuose, todėl kalio, natrio ir bromokamparo bromidai naudojami farmakologijoje.
Jodas ir jo junginiai veikia baltymų, riebalų ir hormonų sintezę. Daugiau nei pusė jodo kiekio skydliaukėje yra surištoje būsenoje skydliaukės hormonų pavidalu. Nepakankamai įsisavinus jodo organizme, išsivysto endeminis gūžys. Siekiant išvengti šios ligos, į valgomąją druską dedama NaI arba KI (1-2 g 1 kg NaCl). Taigi, visi halogenai yra būtini normaliam gyvų organizmų funkcionavimui.
13 skyrius
APIBRĖŽIMAS
Halogenai– VIIA grupės elementai – fluoras (F), chloras (Cl), bromas (Br) ir jodas (I).
Halogenų išorinio energijos lygio elektroninė konfigūracija ns 2 np 5. Kadangi halogenams iki energijos lygio pabaigos trūksta tik vieno elektrono, ORR jie dažniausiai pasižymi oksiduojančių medžiagų savybėmis. Halogenų oksidacijos būsenos: nuo „-1“ iki „+7“. Vienintelis halogenų grupės elementas, fluoras, turi tik vieną oksidacijos būseną „-1“ ir yra labiausiai elektronegatyvus elementas.
Halogeno molekulės yra dviatomės: F 2, Cl 2, Br 2, I 2. Didėjant cheminio elemento atomo branduolio krūviui, t.y. pereinant nuo fluoro prie jodo, halogenų oksidacinis gebėjimas mažėja, o tai patvirtina gebėjimas žemesnius halogenus išstumti aukštesniaisiais iš vandenilio halogeninių rūgščių ir jų druskų:
Br 2 + 2HI = I 2 + 2 HBr
Cl 2 + 2KBr = Br 2 + 2KCl
Halogenų fizinės savybės
Prie Nr. fluoras yra šviesiai geltonos dujos, turinčios aštrų kvapą. nuodingas. Chloras yra šviesiai žalios dujos, kaip ir fluoras, jis turi aštrų kvapą. Labai nuodingas. Esant aukštam slėgiui ir kambario temperatūrai, jis lengvai virsta skysta būsena. Bromas yra sunkus raudonai rudos spalvos skystis, turintis būdingą nemalonų aštrų kvapą. Skystas bromas, kaip ir jo garai, yra labai toksiški. Bromas blogai tirpsta vandenyje ir gerai nepoliniuose tirpikliuose. Jodas yra tamsiai pilka kieta medžiaga su metaliniu blizgesiu. Jodo garai yra purpuriniai. Jodas lengvai sublimuoja, t.y. iš kietos medžiagos virsta dujine būsena, apeinant skystąją būseną.
Halogenų gamyba
Halogenai gali būti gauti elektrolizuojant halogenidų tirpalus arba lydalus:
MgCl 2 = Mg + Cl 2 (lydas)
Dažniausiai halogenai gaunami vykstant vandenilio halogeninių rūgščių oksidacijos reakcijai:
MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2 O
K 2 Cr 2 O 7 + 14HCl = 3Cl 2 + 2KCl + 2CrCl 3 + 7H 2 O
2KMnO4 +16HCl = 2MnCl2 +5Cl2 +8H2O +2KCl
Cheminės halogenų savybės
Fluoras turi didžiausią cheminį aktyvumą. Dauguma cheminių elementų net kambario temperatūroje sąveikauja su fluoru, išskirdami didelį šilumos kiekį. Net vanduo dega fluoru:
2H 2 O + 2F 2 = 4HF + O 2
Laisvas chloras yra mažiau reaktyvus nei fluoras. Jis tiesiogiai nereaguoja su deguonimi, azotu ir tauriosiomis dujomis. Jis sąveikauja su visomis kitomis medžiagomis, tokiomis kaip fluoras:
2Fe + Cl2 = 2FeCl3
2P + 5Cl2 = 2PCl 5
Kai chloras sąveikauja su vandeniu šaltyje, įvyksta grįžtama reakcija:
Cl 2 + H 2 O↔HCl +HClO
Reakcijos produktų mišinys vadinamas chloro vandeniu.
Kai chloras sąveikauja su šarmais šaltyje, susidaro chloridų ir hipochloritų mišiniai:
Cl 2 + Ca(OH) 2 = Ca(Cl)OCl + H 2 O
Kai chloras ištirpsta karštame šarmo tirpale, įvyksta tokia reakcija:
3Cl 2 + 6KOH = 5KCl + KClO 3 + 3H 2 O
Bromas, kaip ir chloras, ištirpsta vandenyje ir, iš dalies su juo reaguodamas, sudaro vadinamąjį „brominį vandenį“, o jodas praktiškai netirpus vandenyje.
Jodas cheminiu aktyvumu labai skiriasi nuo kitų halogenų. Su daugeliu nemetalų jis nereaguoja, o su metalais reaguoja lėtai tik kaitinamas. Jodo sąveika su vandeniliu vyksta tik stipriai kaitinant, reakcija yra endoterminė ir labai grįžtama:
H 2 + I 2 = 2HI - 53 kJ.
Problemų sprendimo pavyzdžiai
1 PAVYZDYS
| Pratimas | Apskaičiuokite chloro tūrį (nr.), kuris sureagavo su kalio jodidu, jei susidarė 508 g jodo |
| Sprendimas | Parašykime reakcijos lygtį: Cl 2 + 2KI = I 2 + 2KCl Raskime susidariusio jodo kiekį: v(I 2)=m(I 2)/M(I 2) v(I 2)=508/254=2 mol Pagal reakcijos lygtį chloro medžiagos kiekis. Iš chemijos vadovėlio daugelis žmonių žino, kad halogenai apima cheminius Mendelejevo periodinės sistemos elementus iš 17 lentelės grupės. Iš graikų kalbos verčiama kaip gimimas, kilmė. Beveik visi jie yra labai aktyvūs, todėl smarkiai reaguoja su paprastomis medžiagomis, išskyrus keletą nemetalų. Kas yra halogenai ir kokios jų savybės? Susisiekus su Halogenų sąrašasDėl šios priežasties halogenai yra geri oksidatoriai, gamtoje jų galima rasti tik kai kuriuose junginiuose. Kuo didesnis atominis skaičius, tuo mažesnis šios grupės elementų cheminis aktyvumas. Halogenų grupę sudaro šie elementai:
Pastarasis buvo sukurtas Branduolinių tyrimų institute, kuris yra Dubnos mieste. Fluoras yra šviesiai geltonos spalvos nuodingos dujos. Chloras taip pat yra nuodingas. Tai dujos, turinčios gana aštrų ir nemalonų šviesiai žalios spalvos kvapą. Bromas yra rausvai rudos spalvos ir yra toksiškas skystis, galintis net paveikti uoslę. Jis labai lakus, todėl laikomas ampulėse. Jodas yra kristalinė, lengvai sublimuojama, tamsiai violetinė medžiaga. Astatinas yra radioaktyvus, krištolo spalva: juoda su mėlyna, pusinės eliminacijos laikas yra 8,1 valandos.
Fluoras sąveikauja su inertinėmis dujomis ir yra apšvitinamas (Xe + F 2 = XeF 2 + 152 kJ). Kaitinamas fluoras veikia kitus halogenus, juos oksiduodamas. Formulė galioja: Hal 2 + F 2 = 2HalF, kur Hal = Cl, Br, I, At, tuo atveju, kai chloro, bromo, jodo ir astatino HalF oksidacijos būsenos yra lygios + 1. Fluoras taip pat gana intensyviai sąveikauja su sudėtingomis medžiagomis. To pasekmė – vandens oksidacija. Tokiu atveju įvyksta sprogstamoji reakcija, kuri trumpai parašyta formule: 3F 2 + ZH 2 O = OF 2 + 4HF + H 2 O 2. ChlorasLaisvo chloro aktyvumas yra šiek tiek mažesnis nei fluoro, tačiau jis taip pat turi gerą gebėjimą reaguoti. Tai gali atsirasti sąveikaujant su daugeliu paprastų medžiagų, išskyrus retas išimtis deguonies, azoto ir inertinių dujų pavidalu. Jis gali smarkiai reaguoti su sudėtingomis medžiagomis, sukuriant pakeitimo reakcijas, angliavandenilių pridėjimo savybė taip pat būdinga chlorui. Kaitinant, iš junginių su vandeniliu ar metalais išstumiamas bromas arba jodas.
Cl2+ hν → 2Cl, Cl + H2 → HCl + H, H + Cl2 → HCl + Cl, Cl + H2 → HCl + H ir kt. Sužadinti fotonai sukelia Cl 2 molekulių skilimą į atomus ir įvyksta grandininė reakcija, dėl kurios atsiranda naujų dalelių, kurios inicijuoja kito etapo pradžią. Chemijos istorijoje šis reiškinys buvo tiriamas. Rusijos chemikas ir Nobelio premijos laureatas N. N. Semenovas. 1956 m. jis studijavo fotocheminę grandininę reakciją ir taip padarė didelį indėlį į mokslą. Chloras reaguoja su daugeliu sudėtingų medžiagų, tai yra pakeitimo ir pridėjimo reakcijos. Jis gerai tirpsta vandenyje. Cl 2 + H 2 O = HCl + HClO - 25 kJ. Su šarmais, kaitinant, chloras gali neproporcingas.
Bromas, jodas ir astatinasCheminis bromo aktyvumas yra šiek tiek mažesnis nei minėto fluoro ar chloro, tačiau jis taip pat yra gana didelis. Bromas dažnai naudojamas skystoje formoje. Jis, kaip ir chloras, labai gerai tirpsta vandenyje. Su juo įvyksta dalinė reakcija, leidžianti gauti „brominį vandenį“. Cheminis jodo aktyvumas pastebimai skiriasi nuo kitų šios serijos atstovų. Jis beveik nebendrauja su nemetalais, o su Su metalais reakcija vyksta labai lėtai ir tik kaitinant. Tokiu atveju įvyksta didelis šilumos sugertis (endoterminė reakcija), kuri yra labai grįžtama. Be to Jodas jokiu būdu negali būti ištirpintas vandenyje, to neįmanoma pasiekti net šildant, todėl gamtoje „jodo vandens“ nėra. Jodą galima ištirpinti tik jodido tirpale. Tokiu atveju susidaro kompleksiniai anijonai. Medicinoje šis junginys vadinamas Lugolio tirpalu. Astatinas reaguoja su metalais ir vandeniliu. Halogenų serijoje cheminis aktyvumas mažėja nuo fluoro iki astatino. Kiekvienas F - At serijos halogenas gali išstumti tolesnius elementus iš junginių su metalais arba vandeniliu. Astatinas yra pasyviausias iš šių elementų. Tačiau jam būdinga sąveika su metalais. TaikymasChemija yra tvirtai įsitvirtinusi mūsų gyvenime, skverbiasi į visas sritis. Žmogus išmoko naudoti halogenus, kaip ir jų junginius, savo naudai. Biologinė halogenų reikšmė neabejotina. Jų taikymo sritys yra skirtingos:
Chloras mūsų gyvenime buvo naudojamas plačiausiai. Jo taikymo sritis yra gana įvairi. Naudojimo pavyzdžiai:
Reikia atsiminti, kad halogenai yra labai toksiškos medžiagos. Ši savybė ypač ryški fluore. Halogenai gali sukelti asfiksiją, dirginti kvėpavimo takus ir pažeisti biologinius audinius. Chloro garai gali būti itin pavojingi, taip pat fluoro aerozolis, kuris turi silpną kvapą ir gali būti jaučiamas didelėmis koncentracijomis. Asmuo gali patirti uždusimo efektą. Dirbant su tokiomis jungtimis reikia imtis atsargumo priemonių. Halogenų gamybos metodai yra sudėtingi ir įvairūs. Pramonėje į tai kreipiamasi laikantis tam tikrų reikalavimų, kurių griežtai laikomasi. Plačiau apie temą |
 Didelis halogenų oksidacinis aktyvumas sumažėja nuo fluoro iki jodo. Aktyviausias iš jo brolių yra fluoras, kuris turi savybę reaguoti su bet kokiais metalais, sudarydamas druskas, kai kurie iš jų savaime užsiliepsnoja, išskirdami didžiulį šilumos kiekį. Be šildymo šis elementas reaguoja beveik su visais nemetalais, reakcijas lydi tam tikro šilumos kiekio išsiskyrimas (egzoterminis).
Didelis halogenų oksidacinis aktyvumas sumažėja nuo fluoro iki jodo. Aktyviausias iš jo brolių yra fluoras, kuris turi savybę reaguoti su bet kokiais metalais, sudarydamas druskas, kai kurie iš jų savaime užsiliepsnoja, išskirdami didžiulį šilumos kiekį. Be šildymo šis elementas reaguoja beveik su visais nemetalais, reakcijas lydi tam tikro šilumos kiekio išsiskyrimas (egzoterminis). Šis elementas turi savotišką ryšį su vandeniliu. Kambario temperatūroje ir be šviesos chloras niekaip nereaguoja į šias dujas, tačiau jas kaitinus arba nukreipus į šviesą, įvyks sprogi grandininė reakcija. Formulė pateikta žemiau:
Šis elementas turi savotišką ryšį su vandeniliu. Kambario temperatūroje ir be šviesos chloras niekaip nereaguoja į šias dujas, tačiau jas kaitinus arba nukreipus į šviesą, įvyks sprogi grandininė reakcija. Formulė pateikta žemiau: Iš natūralaus junginio kriolitas, kurio cheminė formulė yra tokia: Na3AlF6, gaunamas aliuminio. Gamyboje plačiai naudojami fluoro junginiai dantų pastos. Yra žinoma, kad fluoras padeda išvengti karieso. Naudojama alkoholinė jodo tinktūra žaizdų dezinfekcijai ir dezinfekcijai.
Iš natūralaus junginio kriolitas, kurio cheminė formulė yra tokia: Na3AlF6, gaunamas aliuminio. Gamyboje plačiai naudojami fluoro junginiai dantų pastos. Yra žinoma, kad fluoras padeda išvengti karieso. Naudojama alkoholinė jodo tinktūra žaizdų dezinfekcijai ir dezinfekcijai.