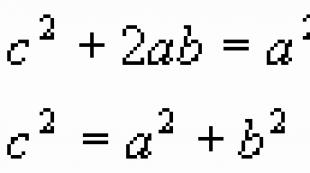екзогенен липиден транспорт. Катедра по биохимия. Фамилен дефицит на апопротеин SP
Транспортни форми на липиди
Транспорт и метаболитни трансформации на кръвни липиди
Новосинтезирани TAGs, фосфолипиди и други абсорбирани липиди напускат клетките на чревната лигавица, влизайки първо в лимфата, а с лимфния поток и в кръвта. Поради факта, че повечето липиди са неразтворими във водната среда, техният транспорт в лимфата, а след това и в кръвната плазма, се извършва в комбинация с протеини.
Мастните киселини в кръвта се свързват с албумин, а други липиди се транспортират като част от специални частици - липопротеини .
Електронната микроскопия на избраните видове липопротеинови частици показа, че те са сферични частици, чийто диаметър намалява с увеличаване на плътността (таблица 1). Липопротеините се състоят от ядро, което включва хидрофобни липиди - триацилглицериди, холестеролни естери и др., докато външната част, при контакт с кръвна плазма съдържа амфифиллипиди: фосфолипиди, свободен холестерол. Протеин Компоненти (апопротеини) с техните хидрофобни зониразположени във вътрешната част на липопротеиновите частици, а хидрофилни - предимно на повърхността.
Таблица 1. Характеристики на липопротеините.
| Имоти | VLDL | LPPP | LDL | HDL |
|
| Плътност g/l | < 0,95 | ||||
| Диаметър, nm | |||||
| Електрофоретична мобилност | Останете в началото | Плаващ β | |||
| Място на обучение | Тънко черво | VLDL катаболизъм | Катаболизъм на VLDL чрез LPPP | Черен дроб, тънки черва, катаболизъм на HM и VLDL |
|
| Главна функция | Транспорт на екзогенни TG | Транспорт на ендогенен TG | LDL прекурсор | Транспорт на холестерол | обратен транспорт на холестерола |
| съединение: |
|||||
| холестерол | |||||
| Фосфолипиди | |||||
| Апопротеини | A, B-48, C, E | B-100, S, E | Б-100, Е | А, В, Е |
|
Липопротеинови частици - макромолекулни комплекси, чиято вътрешна част съдържа неутрални липиди (TAGs и холестеролни естери), а повърхностният слой се състои от фосфолипиди и специфични липидни транспортни протеини, наречени аполипопротеини.
Липопротеините се класифицират въз основа на тяхната мобилност в електрическо поле (по време на електрофореза). По време на електрофорезата липопротеините се разделят на фракции, една от които остава в началото (хиломикрони), други мигрират към глобулиновите зони - β-LP, pre-β-LP, α-LP.
Според размера на хидратиращата обвивка те обикновено се разделят на 5 класа: хиломикрони, VLDL, LPP, LDL, HDL.
Според електрофоретичната подвижност VLDL съответстват на pre-β-LP, LDL - β-LP, HDL - α-LP и HM остават в началото.
Апопротеини са липопротеинови обвивни протеини, нековалентно свързани с фосфолипиди и холестерол. Апопротеините поддържат структурната цялост на липопротеините, участват в обменните процеси между липопротеините и са отговорни за взаимодействието на липопротеините с техните рецептори.
ApoLP насърчава образуването на LP мицели в ендоплазмения ретикулум на хепатоцитите, служат като лиганди за специфични рецептори на повърхността на плазмената мембрана на клетките и кофактори (активатори и инхибитори) на процеса на липолиза и метаболизма на LP в съдовото легло.
Получените хиломикрони първо се секретират в лимфните капиляри. След това през лимфната система съдове с лимфен ток, те влизат в кръвта. на площадав кръвта, апопротеиновият състав на хиломикроните се променя поради обмен с други видове липопротеинови частици (дали протеини с висока плътност - HDL) . По-специално, на чиломикроните получават апопротеин С, който по-късно е необходим за активиране на тяхната липолиза.
Трансформацията на хиломикроните в кръвната плазма се определя главно от действието на ензима - липопротеин липаза (LPL) . Този ензим принадлежи към семейството на липазата. Той се синтезира в клетките на мускулната и мастната тъкан, но функционира на външната повърхност на ендотелните клетки, вие облицоване на стените на съдовете отвътре. LPL катализира реакциятахидролиза на триацилглицериди в състава на хиломикрони с люспиредукция на радикалите на мастните киселини в позиции 1 и 3, както и в позиция 1 във фосфолипидите. 2-моноацилглицеридите, образувани в случай на разцепване на триацилглицериди, впоследствие спонтанно изомеризират, превръщайки се в 1- или 3-моноацилглицериди, и се подлагат на по-нататъшно разцепване с участието на същия LPL до глицерол и мастна киселина. Това се случва, докато количеството на триацилглицеридите в състава на липопротеиновите частици намалее до 20% от първоначалното съдържание.
Мастни киселини, освободени по време на храносмилането много са свързани с албумин от кръвна плазмаи в такъвплексусите се транспортират до клетките на органите и тъканите. клетки абсорбират мастните киселини и ги използват като енергиягенетично гориво или строителен материал (синтез на собствени липиди в клетките). Основните консуматори на мастни киселини са мастната и мускулната тъкан.
В резултат на действието на LPL, хиломикроните се унищожават и фрагменти от тези частици навлизат в черния дроб, където се подлагат на окончателно унищожаване. В черния дроб се разцепват както протеиновият компонент на хиломикроните (до аминокиселини), така и неразделените или частично разцепените триацилглицериди и други липиди. В този процес участват чернодробната липаза и други ензими.
В същото време черният дроб се развива интензивнолипиден синтез от оригиналните субстрати (оцетна киселина,глицерол, мастни киселини и др.). Транспортирането на новосинтезирани липиди от черния дроб до кръвта, а оттам до органите и тъканите, се осъществява от два други вида липопротеини. птици, които се образуват в черния дроб - липопротеините са много ниски плътност (VLDL) и липопротеини с висока плътност (HDL) . Принципите на подреждане на тези частици са подобни на тези на хиломикроните. Разликата е, че VLDL и дори повече HDL са по-малки от хиломикроните. Делът на протеиновия компонент в състава им е по-висок (съответно 10,4 и 48,8% от теглото на частицата), а съдържанието на триацилглицериди е по-ниско (съответно 31,4 и 1,8% от теглото). В резултат на това плътността на VLDL и HDL е по-висока от тази на хиломикроните.
Основният липиден компонент VLDL са триацилглицериди. Въпреки това, за разлика от хиломикроните, тези триацилглицериди се синтезират в чернодробните клетки. Затова те се наричат ендогенни, докато в състава на хиломикроните се наричат екзогенни (поглъщани с храна). VLDL сек се транспортират от черния дроб в кръвта. Има липиди, открити в технитесъстав, точно както беше в случая на хиломикроните, претърпяват LPL разцепване. Освободена мастнакиселините навлизат в клетките на органите и тъканите.
Трябва да се отбележи, че нивото на LPL в мускулната и мастната тъкан се колебае по такъв начин, че да осигури максимално снабдяване с мастни киселини на клетките на мастната тъкан за тяхното отлагане след хранене, а в периода между храненията до клетките на мускулната тъкан за поддържане техните функции. В същото време в мастната тъкан основният фактор, който увеличава синтеза на каталитично активни LPL е инсулин. Следователно, хиперинсулинемиякоето допринася за периода на усвояване на продуктите за храносмилане, ще бъде придружено от повишен прием на триацилглицеридни продукти на разцепване от хиломикрони и VLDL в мастната тъкан за съхранение.
Основният път за образуване на LDL- VLDLP липолиза с LPL. Появява се директно в кръвния поток. По време на тази реакция се образуват редица междинни съединения.канали или частици, съдържащи различни количества триа циглицериди. Те са наречени колективно липопротеин Ines със средна плътност (LPP) . По-нататъшна съдба LPPP могат да бъдат сгънати по два начина: те или влизат в черния дроб от кръвния поток, или претърпяват допълнителни трансформации (механизмът им не е добре разбран), трансформирайки се в LDL.
Основен липиден компонент на ядрото LDL са холестеролни естери. LDL е основното средство за доставяне на холестерол в клетките на органите и тъканите (фигура). Първо, LDL частицата взаимодейства с един от 15 000 рецептора, специфични за тези липопротеини на клетъчната повърхност. На следващия етап LDL частицата, свързана с рецептора, се абсорбира от клетката. В рамките на образуваните ендозоми липопротеините се отцепват от рецепторите.
Впоследствие LDL навлиза в лизозомите, където се разпадазалитане. Среща се в лизозомихидролиза на ef и rovcholesterol, включени в LDL . Като резултатобразува се свободен холестерол или неговите окислени форми. Свободният холестерол се използва за различни цели:живее като структурен компонент на клетъчните мембрани, субстрат за синтеза на стероидни хормони и жлъчни киселини. професионалист каналите на неговата окислителна трансформация имат регулаторнаторсионен ефект върху тялото.
Механизмите за управление координират използването вътрешно- и извънклетъчни източници на холестерол. Когато е достатъчноточното количество LDL, клетките на бозайниците предпочитат да използват LDL като източник на холестерол чрез рецептори. По това време вътреклетъчната система за синтез на холестерол е като че ли в резерв, не функционира с пълна сила.
Важна роля в насоченото доставяне на липопротеини до Пътят на техния метаболизъм принадлежи на апопротеините. Теудар взаимодействието на липопротеините с ензими и рецептори на клетъчната повърхност.
Обратно транспортиране на холестерола от периферните тъкани към черния дроб чрез HDL. Тези липопротеиновите частици отстраняват излишния свободен rified) холестерол от клетъчната повърхност.
HDL - това е цял клас липопротеинови частици, които ръжта значително се различават един от друг по липиди исъстав, размер и функция на апопротеин. Оформят се HDL в черния дроб. Оттам те се секретират в кръвния поток в „незряла" форма, т.е. имат дисковидна форма. Тази форма се дължи на липсата на ядро от неутрални липиди в тях. дов. Фосфосът е техният основен липиден компонент. pids.
Трансфер на свободен холестерол от клетките към HDLпоради разликата в концентрациите му върху повърхността на клетъчните мембрани и липопротеиновите частици. Следователно, той продължава, докато концентрацията на холестерол между донора (мембранна повърхност) и акцептора (HDL) се изравни. Поддържането на градиента на концентрацията се осигурява от постоянното превръщане на свободния холестерол в HDL , в холестеролни естери. Тази реакция катионът се катализира от ензим лецитин-холестерол транс ferase (LHAT) . Получените холестеролни естери са напълно хидрофобни съединения. (за разлика от свободния холестерол, който има хидроксилна група, която го прави хидрофилен). ПосредствомПоради своята хидрофобност, холестеролните естери губят способността си да дифундират и не могат да се върнат обратно в клетката. Те образуват хидрофобно ядро вътре в частиците, поради което HDL придобива сферична форма. В тази форма HDL с кръвния поток навлиза в черния дроб, където се унищожава.
Освободените холестеролни естери служат като начален субстрат за образуването на жлъчни киселини.
Образуването на липопротеини (LP) в организма е необходимост поради хидрофобността (неразтворимост) на липидите. Последните са облечени в протеинова обвивка, образувана от специални транспортни протеини - апопротеини, които осигуряват разтворимостта на липопротеините. В допълнение към хиломикроните (HM), в тялото на животните и хората се образуват липопротеини с много ниска плътност (VLDL), липопротеини със средна плътност (IDL), липопротеини с ниска плътност (LDL) и липопротеини с висока плътност (HDL). Фино разделяне на класове се постига чрез ултрацентрофугиране в градиент на плътност и зависи от съотношението на количеството протеини и липиди в частиците, т.к. липопротеините са супрамолекулни образувания, базирани на нековалентни връзки. В същото време HMs са разположени на повърхността на кръвния серум поради факта, че съдържат до 85% мазнини и е по-лек от водата, в долната част на центрофужната епруветка има HDL, съдържащи най-голямо количество протеини.
Друга класификация на LP се основава на електрофоретичната мобилност. По време на електрофореза в полиакриламиден гел XM, тъй като най-големите частици остават в началото, VLDL образуват пре-β - LP фракция, LDL и CDL - β - LP фракция, HDL - α - LP фракция.
Всички лекарства са изградени от хидрофобно ядро (мазнини, холестеролни естери) и хидрофилна обвивка, представена от протеини, както и фосфолипиди и холестерол. Техните хидрофилни групи са обърнати към водната фаза, докато хидрофобните части са обърнати към центъра, към сърцевината. Всеки тип LP се образува в различни тъкани и транспортира определени липиди. И така, XM транспортира мазнините, получени от храната, от червата до тъканите. HM е 84-96% съставен от екзогенни триацилглицериди. В отговор на натоварването с мазнини капилярните ендотелни клетки освобождават ензима липопротеин липаза (LPL) в кръвта, който хидролизира XM мастните молекули до глицерол и мастни киселини. Мастните киселини навлизат в различни тъкани, а разтворимият глицерол се транспортира до черния дроб, където може да се използва за синтез на мазнини. LPL е най-активен в капилярите на мастната тъкан, сърцето и белите дробове, което е свързано с активното отлагане на мазнини в адипоцитите и особеността на метаболизма в миокарда, който използва много мастни киселини за енергийни цели. В белите дробове мастните киселини се използват за синтезиране на повърхностно активно вещество и осигуряване на активността на макрофагите. Не случайно мазнината от язовец и мечка се използват в народната медицина за белодробни патологии, а северните народи, живеещи в сурови климатични условия, рядко се разболяват от бронхит и пневмония, консумирайки мазни храни.
От друга страна, високата LPL активност в капилярите на мастната тъкан допринася за затлъстяването. Има и доказателства, че по време на гладуване намалява, но активността на мускулната LPL се увеличава.
Остатъчните HM частици се улавят чрез ендоцитоза от хепатоцити, където се разцепват от лизозомни ензими до аминокиселини, мастни киселини, глицерол и холестерол. Една част от холестерола и други липиди се отделя директно в жлъчката, друга част се превръща в жлъчни киселини, а третата част се включва в VLDL. Последните съдържат 50-60% ендогенни триацилглицериди, поради което след отделянето им в кръвта те са подложени, подобно на НМ, на действието на липопротеин липаза. В резултат на това VLDL губят TAGs, които след това се използват от клетките на мастната и мускулната тъкан. В хода на катаболизма на VLDL относителният процент на холестерола и неговите естери (EF) нараства (особено при консумация на храна, богата на холестерол), а VLDL се превръща в LDLP, който при много бозайници, особено гризачи, се усвоява от черния дроб и напълно се разцепва в хепатоцитите. При хора, примати, птици, прасета голяма част от LDL в кръвта, която не се улавя от хепатоцитите, се превръща в LDL. Тази фракция е най-богата на холестерол и НМ и тъй като високият холестерол е един от първите рискови фактори за атеросклероза, LDL се нарича най-атерогенната LP фракция. LDL холестеролът се използва от надбъбречните жлези и половите жлези за синтезиране на стероидни хормони. LDL доставят холестерол на хепатоцитите, бъбречния епител, лимфоцитите, клетките на съдовата стена. Поради факта, че самите клетки са в състояние да синтезират холестерол от ацетилкоензим А (AcoA), съществуват физиологични механизми, които предпазват тъканта от излишък на CM: инхибиране на производството на собствен вътрешен холестерол и рецептори за LP апопротеини, т.к. всяка ендоцитоза е рецепторно-медиирана. HDL дренажната система е призната за основен стабилизатор на клетъчния холестерол.
HDL прекурсори се образуват в черния дроб и червата. Те съдържат висок процент протеини и фосфолипиди, имат много малък размер, свободно проникват през съдовата стена, свързвайки излишния ChM и го отстранявайки от тъканите, и сами стават зрели HDL. Част от ЕС преминава директно в плазмата от HDL към VLDL и LPPP. В крайна сметка всички LP се разцепват от лизозоми на хепатоцити. Така почти целият "допълнителен" холестерол навлиза в черния дроб и се отделя от него като част от жлъчката в червата, като се отстранява с изпражненията.
Липопротеините играят ключова роля в липидния транспорт и метаболизма. .
липопротеини- сферични структури, които се образуват поради комбинацията от холестерол, холестеролни естери и триглицериди на мастни киселини. Те образуват ядро, заобиколено от обвивка с дебелина 2 nm. Съставът на черупката включва фосфолипидни молекули, неестерифициран холестерол и специфични протеини - апопротеини, които винаги са на повърхността на липопротеините. Сега има 5 класа апопротеини - A, B, C, D, E.
Функции на апопротеините:
Допринесе за разтварянето на ECS и TG
Регулиране на реакциите на липидите с ензими
Свързват липопротеините с клетъчните рецептори
Определете функционалните свойства на лекарството.
Всички липопротеини са разделени на четири класа, които се различават по състава на ядрото, вида на апопротеините и функциите. Колкото по-високо е съдържанието на протеин в LP и по-ниско е съдържанието на триглицериди, толкова по-малък е размерът на частиците на LP и толкова по-висока е тяхната плътност.
Образува се в стената на тънките черва хиломикрони- големи сферични частици, 90 % съставен от триглицериди. Функцията на хиломикроните е транспортирането на хранителния холестерол и мастни киселини от червата до периферните тъкани (скелетни мускули, миокард, мастна тъкан, където се използват като енергиен субстрат) и черния дроб. Протеиновата обвивка на хиломикроните включва апопротеин В-48. Апопротеин В-48 се синтезира само в чревните клетки. При негово отсъствие хиломикроните не се образуват. Хиломикроните навлизат в кръвта през чревната лимфна система през гръдния лимфен канал. В кръвта хиломикроните взаимодействат с HDL и придобиват от тях апо C-II и апо Е, образувайки зрялформи. Протеин апо C-II е активатор на ензима липопротеин липаза, протеинът apoE е необходим за отстраняване на остатъчните хиломикрони от кръвта.
VLDL (липопротеини с много ниска плътност).Състои се от 60% мазнини и 18% фосфолипиди. Протеините и холестерола са приблизително равни.
Метаболизъм на VLDL
1. Първичните VLDL се образуват в черния дроб от хранителни мазнини, снабдени с хиломикрони и новосинтезирани мазнини от глюкоза. Съдържа само апоВ-100;
2. В кръвта първичните VLDL взаимодействат с HDL и придобиват apoC-II и apoE от тях, образувайки зрели форми.
3. Върху капилярния ендотел зрелите VLDL са изложени на липопротеин липаза с образуването на свободни мастни киселини. Мастните киселини се придвижват в клетките на органа или остават в кръвната плазма и в комбинация с албумин се пренасят с кръвта до други тъкани.
4. Остатъчен VLDL (наричан още липопротеин с междинна плътност, LDLP)
LDL (липопротеин с ниска плътност)са най-атерогенни
са основната транспортна форма на холестерола. Те съдържат около 6% TG, максималното количество холестерол (50%) и 22% протеин.
LDL частицата съдържа като протеинов компонент една молекула аполипопротеин В-100 (apoB-100), който стабилизира структурата на частицата и е лиганд за LDL рецептора. Размерите на LDL варират от 18 до 26 nm. .
LDL се образува от VLDL по време на хидролизата на последния от липопротеин липаза и чернодробна липаза. В същото време относителното съдържание на триглицериди в частицата намалява значително, докато холестеролът се увеличава. По този начин LDL е последната стъпка в обмена на ендогенни (синтезирани в черния дроб) липиди в тялото. Те пренасят холестерол в тялото, както и триглицериди, каротеноиди, витамин Е и някои други липофилни компоненти.
Нивото на LDL холестерола корелира с висок риск от развитие на атеросклероза и нейните прояви като инфаркт на миокарда, инсулт и HDL. Трябва да се отбележи, че малките LDL са по-атерогенни от по-големите.
Наследствена форма на заболяването високо ниво LDL е наследствена хиперхолестеролемия или хиперлипопротеинемия тип II.
Клетъчно усвояване на LDL
Ако клетката се нуждае от холестерол, тя синтезира LDL рецептори, които след синтеза се транспортират до клетъчната мембрана. LDL, циркулиращи в кръвта, се свързват с тези трансмембранни рецептори и се ендоцитират от клетката. След абсорбция, LDL се доставя до ендозомите, а след това до лизозомите, където холестеролните естери се хидролизират и холестеролът навлиза в клетката.
HDL (липопротеини с висока плътност) -произведени в чернодробните клетки. Това са най-малките липопротеини. – 7-14nm. Те се състоят от протеини (50%), 75% са апопротеин А.; 30% са фосфолипиди.
След като напуснат хепатоцита, те са дисковидни, но, циркулиращи в кръвта и усвоявайки холестерола, се превръщат в сферични структури. Функцията на HDL е да премахва излишния холестерол от клетките на периферните тъкани. Това се улеснява от чернодробния ензим - лецитин-холестерол-ацилтрансфераза, който се намира на повърхността на HDL, поради взаимодействието с апапротеин А .. Този ензим осигурява трансформацията на холестерола в неговите естери и транслацията в ядрото. Това е, което позволява на HDL да премахне излишния холестерол. Освен това HDL навлиза в черния дроб и излишният холестерол се отделя в жлъчката.
В кръвта се откриват липопротеини и хиломикрони с две липази, липопротеин липаза и изпечена триацилглицерол липаза.
Липопротеин липазата се намира на повърхността на ендотела на капилярите на мускулната и мастната тъкан. Тази липаза има афинитет към апопротеин-С и следователно се свързва с VLDL и хиломикроните. В ядрото мазнините се разграждат до мастни киселини, които влизат в клетките на мастната тъкан, там се преобразуват триглицеридите и се натрупват в резерв и в мускулни клетки, където се използват като енергиен субстрат. Останалите хиломикрони губят апопротеин С и се свързват с HDL.
Чернодробната триглицеридна липаза също разгражда мазнините в хиломикроните и VLDL, но продуктите на нейното разцепване се използват от миокардните клетки и скелетните мускули. Хиломикроните се превръщат в остатъци от хиломикрони, а VLDL в LDL.
Поддържането на метаболизма на холестерола се осъществява автоматично с участието на специфични липопротеинови рецептори, разположени върху мембраната на хепатоцитите. Синтезът на холестерол в хепатоцитите се определя от общия брой и натоварване на рецепторите за LDL и HDL. При ниско ниво на холестерол и малък брой рецептори синтезът на холестерол се активира в хепатоцитите. Взаимодействието на молекулния комплекс холестерол-LDL с нормалната експресия на LDL рецептора на клетъчната повърхност води до пиноцитоза на молекулярния комплекс. След пиноцитоза, комплексът се включва в лизозомите, където се освобождава свободен холестерол. Увеличаването на концентрацията на свободния холестерол в клетката намалява активността на ключовия ензим за вътреклетъчния синтез на холестерол, хидроксиметилглутарил-коензим А-редуктаза. С възрастта има ограничение на този рецепторен механизъм и повишеният прием на холестерол не е придружен от ограничаване на синтеза му в черния дроб. Освен това, при атерогенни условия, хепатоцитите преминават към нов тип екскреция на холестерол: в хепатоцитите се активира синтеза на апопротеин В и се засилва образуването и освобождаването на VLDL.
По този начин основната част от атерогенните липопротеини се образуват, метаболизират и екскретират от тялото от черния дроб, следователно нарушенията в регулирането на обмена на тези частици в черния дроб са отговорни за развитието на атеросклероза.
Основата на атеросклерозатанарушение на метаболизма на холестерола и преобладаване на атерогенни липопротеини (LDL, VLDL ). Сега е доказано, че изходната линия на атеросклерозата е оксидативната модификация на липопротеините, свързана с продължителен дисбаланс в организма между про- и антиоксидантите. Особено податливи на окислителна модификация на LDL, тъй като съдържат много линолова киселина.
Оказа се, че липопротеините имат собствена защита срещу оксидативен стрес под формата на молекули ά-TF, β-каротин и други, чието общо съдържание достига 14 nM/mg протеин в липопротеина. Но дори и при нормалния LDL е открито високо съдържание на хидропероксиди. Способността да окисляват LDL се увеличава, когато те попаднат в интимата на съдовете.
Освен това увреждането на ендотела е важен фактор за атеросклеротично съдово заболяване. Увреждането на ендотела насърчава навлизането на LDL в съдовата стена . Ендотелият обикновено се уврежда най-значително в главните съдове при повишен механичен стрес. LDL се изпращат към увредените зони, доставяйки енергиен субстрат за възстановяване, но в тези области влизат в контакт със свободни метали с променлива валентност, което води до тяхната окислителна модификация. Окисленият LDL става токсичен за ендотела. В допълнение към хиперлипидемията, други фактори също влияят на ендотела: артериална хипертония, хормонална дисфункция, промени в реологията на кръвта, тютюнопушене и диабет.
Механизъм на атерогенезата
1. Под влияние на модифицирани LDL ендотелиумът се уврежда и се променят повърхностните свойства на моноцитите и тромбоцитите, което повишава тяхната адхезивност.
2. Окисленият LDL проявява хемоатрактантни свойства.
3. След фиксиране върху ендотела моноцитът мигрира между ендотелните клетки към субендотелния слой и се превръща в макрофаг, който с участието на специални „почистващи“ рецептори започва да улавя липиди. Поемането на липиди също се осъществява по нерецепторни пътища. Това причинява образуването на пяна клетки.
4. Макрофагите произвеждат увреждащи вещества (левкотриени, интерлевкини), които от своя страна влияят неблагоприятно на съседните ендотелни клетки.
5. Активираните макрофаги произвеждат няколко растежни фактора, които имат митогенен ефект върху гладкомускулните клетки и предизвикват тяхната миграция към интимата, и стимулират миграцията на фибробластите, както и образуването на съединителна тъкан.
6. При увреждане на ендотела патогенно действие имат и тромбоцитите, които при контакт с ендотела предизвикват ретракция на клетките. След това тромбоцитите започват да взаимодействат с клетките на пяна и клетките на съединителната тъкан. Възможно е също така тромбоцитите да се агрегират и да образуват париетален тромб. Растежните фактори, освободени по време на активиране на тромбоцитите, причиняват пролиферация на гладкомускулните клетки. Пролифериращите клетки от своя страна произвеждат растежен фактор, водещ до прогресиране на лезията.
7. Ретракция на ендотелните клетки може да се случи поради натрупването на холестерол, липопротеини с ниска плътност в тях. Прекомерното им съдържание нарушава съвместимостта на клетките. Следователно, на места, които са най-изложени на притока на кръв (области на бифуркация, изпускане на съда), се получава отделяне на ендотелните клетки поради твърдост. Изменените ендотелни клетки също започват да произвеждат растежни фактори, под въздействието на които се образуват ивици и плаки.
Клетъчният състав на плаките се оказва подобен на състава на хроничното възпаление, възникващо в интимата на артериите. Понастоящем атеросклеротични лезии се разглеждат като полиетиологична реакция на съдовата стена, подобна на възпаление, което се появява в ранна детска възраст.
Масовите епидемиологични проучвания на населението на различни страни позволиха да се идентифицират редица фактори, които влияят на честотата на атеросклерозата - рискови фактори. Значението на възрастта, пола и семейната предразположеност не се поставя под въпрос. Сред другите фактори, основните са: хиперлипидемия, артериална хипертония, тютюнопушене, захарен диабет. Съществува връзка между тежестта на атеросклерозата и излагането на различни стресови фактори, депресия, липса на физическа активност, затлъстяване, хиперурикемия, консумация на силно кафе, чай.
От решаващо значение за появата и прогресията на атеросклерозата е съотношението на LP от различни класове: LDL, VLDL имат атерогенен, а HDL - антиатерогенен ефект. Най-висок риск от развитие на атеросклероза се наблюдава при лица с високо съдържание на LDL и VLDL и ниско - HDL.
Норми за холестерол
Нива на общия холестеролв кръвта - 3,0-6,0 mmol/l.
Нормисъдържание LDL холестерол: за мъже- 2,25-4,82 mmol / l, for Жени- 1,92-4,51 mmol / l.
Норминиво HDL холестерол:за мъже- 0,7-1,73 mmol/l, за Жени- 0,86-2,28 mmol/l
Механизъм на атерогенезата
(образуване на атеросклеротична плака)
Ситуационни задачи за самостоятелна работастуденти
Задача 1
Биохимично изследване на кръвта при пациент Х. показа, че стойността на коефициента на атерогенност на холестерола е 5 (норма ≤3). По думите на пациента преди време той е бил лекуван в клиниката по ендокринология от умерено тежък хипотиреоидизъм.
Тестови въпроси:
1. Пациентът е с висок риск от развитие на атеросклероза?
2. Какъв е механизмът на връзката между хиперхолестеролемия и хипотиреоидизъм? Обосновете отговора.
Задача 2
22-годишен мъж е приет в клиниката с оплаквания от болки в областта на сърцето. Пациентът съобщава, че е диагностициран с ангина пекторис преди 2 години. При прегледа се установяват атеросклеротични плаки в субепикардни коронарни артерии и големи мозъчни съдове. Съдържанието на холестерол в кръвта, LDL и LPPP в кръвната плазма надвишава горната граница на нормата няколко пъти. Пациентът е подложен на чернодробна биопсия, която разкрива намаляване на броя на рецепторите за LDL и LDL.
Тестови въпроси:
1. Има ли значение наследствеността при възникването и развитието на откритата патология?
2. Има ли връзка между намаляването на броя на LDL рецепторите и хиперхолестеремията?
3. Какви са превантивните мерки за тази патология?
Задача 3
Пациент К., на 58 г., страда от артериална хипертония. През последните 1,5 години тя започва да забелязва увеличаване на телесното тегло, втрисане в краката, изтръпване и болка в мускулите на прасеца при ходене и след това в покой (главно през нощта, в резултат на което сънят й е нарушен) . Преди 5 месеца се появи ерозия в долната трета на десния пищял, а след това и язва, безболезнена и неподлежаща на лечение. Има постоянно повишена (до 37,2-37,4 ° C) телесна температура. При назначаването при лекаря пациентът, освен изброените по-горе, има и оплаквания от сухота в устата, жажда, повишен прием на течности (4-5 литра на ден), често обилно уриниране. Обективно: кожата на краката е суха, бледа, студена на допир. Палпацията не определя пулсацията на артериите в подколенната ямка и на стъпалото. Кръвен тест повишени нива на холестерол, фибриноген, тромбоцити, GPC 180 mg%
Тестови въпроси:
1. Какви форми на патология, освен артериална хипертония, се доказват от наличните клинични и лабораторни данни? Обосновете отговора.
2. Какво може да причини тези форми на патология и каква е връзката им?
3. Какви са основните механизми на тяхното развитие, както и симптомите на пациента?
4. Има ли патогенетична връзка между установената от Вас форма на патология при пациента и развитието на язва на крака? Ако да, тогава назовете и опишете основните връзки на тази зависимост. Ако не, тогава обяснете механизма на развитие на язва в този случай?
Задача 4
Пациент М., 46 г., изследовател, се оплаква от загуба на паметта, виене на свят, болка в сърцето, задух при физическо натоварване. Смята се за болен от 3 години. Не се занимава с физически труд и физическо възпитание. Пуши много. Храни се добре, яде много месо и животински мазнини, а плодове и зеленчуци – недостатъчно. Обективно: среден ръст, хиперстеничен. Изглежда много по-възрастен от годините си. Кожата и мускулите са отпуснати. Границите на сърцето са разширени. Тоновете са приглушени. Пулс 86 в минута, ритмичен. AD 140/90 мм. rt. Изкуство. ЕКГ разкрива признаци на коронарна недостатъчност. Рентгеново се установява дилатация на аортната дъга. Съдържанието на холестерол и β-липопротеини рязко се повишава в кръвта. На пациента са предписани физиотерапевтични упражнения и диета, богата на зеленчуци и плодове, с намалено съдържание на калории и ограничаване на животинските мазнини. Освен това се препоръчва да се въвеждат поне 20 g натурално растително масло в дневната диета.
Тестови въпроси:
1. Какви са вероятните причини и последствия от хиперхолестеролемия при този пациент?
Тестови задачи за контрол на крайното ниво на знания на учениците
1. ХИПЕРХОЛЕСТЕРОЛЕМИЯТА СЕ СРЕЩА ПРИ СЛЕДНИТЕ ПАТОЛОГИЧНИ СЪСТОЯНИЯ (3):
1. надхепатална жълтеница
2. атеросклероза
3. диабет
4. остър гломерулонефрит
5. липоидна нефроза
2. ИЗБЕРЕТЕ РИСКОВИ ФАКТОРИ ЗА РАЗВИТИЕ НА АТЕРОСКЛЕРОЗА (3)
1. хипотония
2. хипертония
3. диабет
4. безвкусен диабет
5. затлъстяване
3. СЛЕДНИТЕ ЦИТОКИНИ УЧАСТВАТ В ОБРАЗУВАНЕТО НА АТЕРОМИТЕ (3):
1. интерферони
2. интерлевкин-3
3. интерлевкин-1
4. тумор некрозис фактор-α
5. растежен фактор на тромбоцитите
4. ПОСОЧЕТЕ НИВОТО НА ХОЛЕСТЕРОЛА В КРЪВНАТА ПЛАЗМА, ОТРАЗЯВАЩО ИЗХОД Й ОТ СЪДОВАТА СТЕНА (А) И ДЕПОЗИРАНЕ В ИНТИМАТА НА СЪДА (В)
1. 4,7 mmol/l
2. 5,2 mmol/l
3. 6,1 mmol/l
5. ИЗБЕРЕТЕ КОЕ СООТНОШЕНИЕ НА ЛИПОПРОТЕИНОВИТЕ ФРАКЦИИ В КРЪВНАТА ПЛАЗМА СЪСТОЯВА ОБРАЗУВАНЕТО НА АТЕРОСКЛЕРОТИЧНИ ПЛАКИ (2):
1. повишаване на съдържанието на LDL
2. Намаляване на LDL
3. увеличаване на съдържанието на HDL
4. Намаляване на HDL
5. Намаляване на VLDL
6. ПРИ ПОЯВАТА НА УСЛОЖНЕНИЯ НА АТЕРОСКЛЕРОЗАТА ВАЖНО Е СЪСТОЯНИЕТО НА „НЕСТАБИЛНОСТ” НА МЛАДИ ИЛИ „МЕКИ” АТЕРОСКЛЕРОТИЧНИ ПЛАКИ, ПРЕДПОСЛОЖЕНИ КЪМ РАЗДЪЛВАНЕ НА ЧЕРВИКАТА. ТОВА ВОДИ ДО СЛЕДНИТЕ НАРУШЕНИЯ (3):
1. болков синдром на мястото на разкъсване на плаката
2. повишават тромбогенния потенциал на кръвта
3. образуване на париетален тромб
4. нарушение на реологичните свойства на кръвта в системното кръвообращение
5. влошаване на локалните хемодинамични нарушения
7. ЕФЕКТЪТ НА ЛЕКАРСТВАТА ЗА ПРЕВЕНЦИЯ НА АТЕРОСКЛЕРОЗА МОЖЕ ДА СЕ СВЪРЗИ СЪС СЛЕДНИТЕ МЕХАНИЗМИ (2):
1. Понижени нива на LDL в кръвта
2. повишени нива на LDL в кръвта
3. повишаване на съдържанието на VLDL в кръвта
4. повишаване на HDL в кръвта
5. Понижени нива на HDL в кръвта
8. ПРИЧИНИ ЗА МОДИФИКАЦИЯ НА ЛИПОПРОТЕИНИ СА(2):
1. гликозилиране
2. разграждане на липидите под действието на триглицеридната липаза
3. естерификация на холестерола
4. Активиране на FRO
5. ресинтез на липопротеини от кетонни тела и протеини
9. "ПЯНА КЛЕТКИ" СЕ ОБРАЗУВА ПРИ НАТРУПВАНЕ НА ЛИПИД B(2):
1. макрофаги
2. лимфоцити
3. неутрофили
4. гладкомускулни клетки
5. ендотелни клетки
10. МАКРОФАГИТЕ АБОРБИРАТ ЛИПОПРОТЕИНИ С УЧАСТИЕ (2):
1. Рецептор за LDL
2. рецептор за HDL
3. рецептор за холестерол
4. рецептор за VLDL
5. Рецептор за фосфолипиди
11. ОСНОВНИТЕ КОМПОНЕНТИ НА ФИБРОЗНАТА ПЛАКА СА(1):
1. фибробласти
2. еозинофили
3. базофили
4. макрофаги
12. ИЗБЕРЕТЕ ПОСЛЕДОВАТЕЛНОСТ ОТ ПРОМЕНИ ПО ВРЕМЕ НА АТЕРОГЕНЕЗАТА (1):
1) миграция на макрофагите към фокуса на натрупване на липиди;
2) улавяне на липопротеини от макрофаги, трансформация в "пяна клетки"
3) освобождаване на растежни и хемотактични фактори за гладкомускулните клетки
4) увреждане на ендотела и натрупване на липопротеини в интимата на артериите
5) активиране на синтеза на колаген и еластин от гладкомускулните клетки
6) образуване на фиброзна капсула около огнището на натрупване на липиди
А - 4,3,1,2,5,6
Б - 4,2,3,1,5,6
Б - 2,4,5,1,3,6
13. ПЪРВИЧНИ АТЕРОСКЛЕРОТИЧНИ ИЗМЕНЕНИЯ В АРТЕРИИТЕ (ЛИПИДНИ ИНИЦИ) МОЖЕ ДА СЕ ПОЯВЯТ ЗА ПЪРВИ ПЪТ НА ВЪЗРАСТ (1):
1. до 10 години 2. 20–25 години 3. 30–35 години
4. 40–45 години 5. след 50 години
14. НАЙ-ЧЕСТИТЕ ПОСЛЕДСТВИЯ И УСЛОЖНЕНИЯ ОТ АТЕРОСКЛЕРОЗАТА СА (2):
1. артериална тромбоза
2. венозна тромбоза
3. недостатъчност на аортната клапа
5. сърдечна недостатъчност
15. МИНИМАЛНО УВЕЛИЧЕНИЕ НА КОЕФИЦИЕНТА НА ХОЛЕСТЕРОЛ НА АТЕРОГЕННОСТ, ПОКАЗВАЩО СИ РИСК ОТ АТЕРОСКЛЕРОЗА (1):
1. 1 2. 5 3. 4 4. 3 5. 2
16. ИЗБЕРЕТЕ ТВЪРДЕНИЯТА, ВЯРНИ ЗА ТРОМБОГЕННАТА ТЕОРИЯ (2):
1. Намалено производство на азотен оксид от ендотелиоцитите
2. намаляване на адхезивната способност на тромбоцитите
3. увеличаване на производството на азотен оксид от ендотелиоцитите
4. Засилване на агрегационната способност на тромбоцитите
5. увеличаване на производството на простациклин I2
От биологична гледна точка най-важните физикохимични свойства на липидите са противоположни по свойства на въглехидратите. Техните молекули са мастноразтворими, големи и имат относително ниско съдържание на кислородни атоми.
Липидите са бавен енергиен субстрат. Поради ниската си разтворимост във вода, те не могат да достигнат високи концентрации в кръвта и следователно не могат да бъдат енергиен субстрат за тъканите.
Много липиди. Първо, поради ниския брой кислородни атоми, свободната енергия на липидите е доста висока. Второ, поради тяхната хидрофобност, те могат да образуват големи капчици, които запълват почти цялата клетка.
Липидите са важен пластичен материал. Те могат да образуват хидрофобна обвивка, която ограничава клетката от околния воден разтвор. Поради тази причина те са в основата на биологичните мембрани.
Подкожната мастна тъкан е топлоизолатор. Отлагането на липиди е важна механична функция.
Основните липиди на човешкото тяло са холестерол, фосфолипиди, триглицериди.
Мастните киселини и триглицеридите функционират главно като енергийни субстрати. Холестеролът и фосфолипидите се използват за други цели - за образуване на биологично активни вещества и мембрани.
Употреба на триглицериди:
Отлагане в мастната тъкан, катаболизъм - изграждане на мембрани.
Източници на триглицериди:
Те идват с храната и се мобилизират от мастната тъкан.
Образуване от въглехидрати и протеини. При повишен прием на субстрати те се превръщат в триглицериди в черния дроб и се прехвърлят в мастната тъкан в кръвта, където остават.
Триглицеридите са основната форма на съхранение на липиди в мастната тъкан.
Мастните киселини са основният енергиен субстрат, доставян на клетките от мастната тъкан. Това се дължи на факта, че мастните киселини проникват по-добре през клетъчните мембрани.
По-бързите енергийни субстрати са кетонни тела. Кетонните тела се образуват в черния дроб. Кетонните тела могат да се използват от тъкани с бърз обмен. Но за да се окислят напълно кетонните тела, са необходими продукти на въглехидратно окисление. Следователно, при наличие на нарушения на въглехидратния катаболизъм, кетонните тела се натрупват в кръвта.
Мазнините са хидрофобни, така че има специални механизми за тяхното транспортиране в кръвта. Свободните (неестерифицирани) мастни киселини се пренасят в кръвта под формата на комплекси с албумини. Холестеролът, неговите естери, триацилглицероли, фосфолипиди се транспортират като част от липопротеините.
липопротеинипредставляват молекулярни комплекси, състоящи се от липиди и протеини.
Ориз. 10.2. Структурата на липопротеина
Има няколко класа липопротеини (LP), но всички те са обединени от следните характеристики: 1) повърхностният слой на липопротеините се състои от фосфолипиди, свободен холестерол и протеини; 2) всеки липопротеин съдържа специален набор от повърхностни протеини - аполипопротеини (apo), които се обозначават с букви от латинската азбука (A, B, C); 3) сърцевината (ядрото) на липопротеина се състои от хидрофобни триацилглицероли, холестеролни естери (фиг. 10.2).
аполипопротеиниизпълняват следните характеристики: 1) са структурни компоненти на липопротеините; 2) участват в разпознаването и взаимодействието с мембранните рецептори; 3) активират ензимите на метаболизма на липопротеините.
Липопротеините се разделят на 4 основни класа в зависимост от плътността (определена чрез ултрацентрофугиране) и електрофоретичната подвижност (Таблица 10.1).
Таблица 10.1.
Класификация на липопротеините по метод на разделяне
Основните параметри и състав на липопротеините са представени в табл. 10.2.
Хиломикрони(XM) - най-големите частици. HM се синтезират в чревната лигавица и участват в екзогенен транспорт на хранителни липиди до различни тъкани. Основните липиди са триацилглицероли.
VLDLсинтезирани в черния дроб. Основните липиди са триацилглицероли. Главна функция - транспорт на ендогенни липиди от черния дроб до периферните тъкани.
LDL се произвежда в кръвния потокот VLDL. Съдържа много холестерол(основен преносител на холестерол), който се транспортира в периферните тъкани.
HDLобразуват се в черния дроб, съдържат много фосфолипиди и протеини; в тези LPs компонентите на обвивката преобладават над ядрото.
Таблица 10.2
Състав на липопротеини
TG, триацилглицероли; PL, фосфолипиди. CS - холестерол
Има екзогенен (транспорт на хранителни липиди) и ендогенен (транспорт на липиди, синтезирани в тялото) транспорт.
екзогенен транспорт. Продуктите на храносмилането на липидите се абсорбират в клетките на чревната лигавица в състава на мицели. Мастни киселини с въглероден номер<12 всасываются в кровь и по воротной вене транспортируются в печень. Длинноцепочечные жирные кислоты (С >12) се реестерифицират в чревните клетки до триацилглицероли, които са сходни по състав с хранителните мазнини. Получените триацилглицероли заедно с фосфолипиди, холестерол и протеини (2%) образуват хиломикрони. Хиломикроните съдържат апопротеин В48 и апоА.
Ориз. 10.3. Екзогенен липиден транспорт (според Murray R. et al., 2004)
Хиломикроните навлизат в лимфата. В кръвта те се откриват с HDL частици, съдържащи apoE и apoC. Хиломикроните даряват apoA на HDL частици и в замяна придобиват apoE и apoC. Един от аполипопротеините от група С, apoCII, служи като активатор на ензима липопротеин липаза (LPL). Този ензим се синтезира и секретира от мастната и мускулната тъкан, клетките на млечните жлези. Секретираният ензим е прикрепен към плазмената мембрана на ендотелните клетки на капилярите на онези тъкани, където е синтезиран. ApoCII, разположен на повърхността на HM, активира LPL. Той хидролизира триацилглицероли в НМ до глицерол и мастни киселини. Тези мастни киселини или влизат в клетките на мастната и мускулната тъкан, или се комбинират с плазмените албумини. В резултат на действието на LPL хиломикроните рязко намаляват по размер и се наричат остатъци (остатъци). Остатъците от НМ се поемат от черния дроб от рецепторния път (фиг. 10.3).
ендогенен транспорт. В чернодробните клетки се ресинтезират триацилглицероли и фосфолипиди, които са характерни за този организъм. Те са включени в VLDL. Съставът на VLDL включва apoB100 и apoC. Това е основната транспортна форма на триацилглицероли. Друг клас липопротеини, образувани в черния дроб - HDL - включва холестерол, фосфолипиди, апоА. Тези частици са плоски и се наричат зараждащ се HDL. (В ядрото им няма хидрофобни молекули). Тези HDL играят важна роля в обратния транспорт на холестерола от клетките на периферната тъкан към черния дроб.
В капилярите на мастната и мускулната тъкан apoCII VLDL активира LPL, който катализира хидролизата на VLDL триацилглицероли и ги превръща в LDLP (липопротеини с междинна плътност). LPPP, под действието на циркулиращата чернодробна триацилглицерол липаза, синтезирана в черния дроб, губи друга част от триацилглицероли и се превръща в LDL. Холестеролът се превръща в основния липид на LDL, който, като част от LDL, се пренася в клетките на всички тъкани. Следователно LDL се образува директно в съдовото легло (фиг. 10.4).
Ориз. 10.4. Ендогенен липиден транспорт (според Murray R. et al., 2004)
И така, в резултат на екзогенен и ендогенен транспорт, мастни киселини и глицерол се освобождават в капилярите на мастната и мускулната тъкан. Мастните киселини се свързват с албумина и се транспортират до консуматорските тъкани.