Teadlased mikrobioloogid ja nende saavutused. Mikrobioloogia arengu abstraktne ajalugu. Mikrobioloogiateaduse tekkimine
Vene mikrobioloogia rajaja on L. Tsenkovski (1822-1887). Tema uurimisobjektid olid mikroskoopilised algloomad, vetikad ja seened. Ta avastas ja kirjeldas suure hulga algloomi, uuris nende morfoloogiat ja arengutsükleid. See võimaldas tal järeldada, et taimede ja loomade maailma vahel pole teravat piiri. Ta korraldas ka ühe esimese Pasteuri jaama Venemaal ja pakkus välja vaktsiini siberi katku vastu ("Tsenkovsky elusvaktsiin").
I. Mechnikovi (1845-1916) nimi on seotud mikrobioloogia uue suuna – immunoloogia – väljatöötamisega. Esimest korda teaduses töötas Mechnikov välja ja kinnitas eksperimentaalselt immuunsuse bioloogilise teooria, mis läks ajalukku Mechnikovi fagotsüütiteooriana. See teooria põhineb keha rakuliste kaitseseadmete ideel. Mechnikov tõestas loomkatsetes (dafnia, meritähe vastsed), et leukotsüütidel ja teistel mesodermaalse päritoluga rakkudel on võime püüda kinni ja seedida kehasse sisenevaid võõrosakesi (sh mikroobid). See nähtus, mida nimetatakse fagotsütoosiks, moodustas immuunsuse fagotsüütilise teooria aluse ja on saanud üldise tunnustuse. Arendades tõstatatud küsimusi, sõnastas Mechnikov üldise põletiku kui keha kaitsva reaktsiooni teooria ja lõi immunoloogias uue suuna - antigeeni spetsiifilisuse doktriini. Praegu muutub see üha olulisemaks seoses elundite ja kudede siirdamise probleemi arenemisega ning vähi immunoloogia uurimisega.
Mechnikovi olulisemad tööd meditsiinilise mikrobioloogia vallas hõlmavad koolera patogeneesi ja kooleralaadsete vibrioonide, süüfilise, tuberkuloosi ja retsidiveeruva palaviku bioloogia uuringuid. Mechnikov on mikroobse antagonismi doktriini rajaja, mis oli aluseks antibiootikumravi teaduse arengule. Mikroobse antagonismi ideed kasutas Mechnikov pikaealisuse probleemi väljatöötamisel. Uurides keha vananemise nähtust, jõudis Mechnikov järeldusele. Et selle kõige olulisem põhjus on keha krooniline mürgistus mädanevate bakterite poolt jämesooles toodetud lagunemissaadustega.
Praktilist huvi pakuvad Mechnikovi varajased tööd seene Isaria destructor kasutamisest põllukahjuri – teraviljamardika – tõrjumiseks. Need annavad põhjust pidada Mechnikovit põllumajandustaimede kahjurite tõrje bioloogilise meetodi rajajaks – meetod, mis leiab tänapäeval üha enam rakendust ja populaarsust. Seega I.I. Mechnikov, silmapaistev vene bioloog, kes ühendas endas eksperimenteerija, õpetaja ja teaduslike teadmiste propageerija omadused, oli suure vaimu ja tööga mees, kelle kõrgeimaks autasuks oli Nobeli preemia määramine 1909. aastal fagotsütoosi uurimise eest. Mikrobioloogia areng meie riigis on tihedalt seotud ka suurima teadlase, sõbra ja kolleegi I. Mechnikovi nimega N.F. Gamaleya (1859-1949). Gamaleya pühendas kogu oma elu nakkushaiguste uurimisele ja nende patogeenide vastu võitlemise meetmete väljatöötamisele. Gamaleya andis suure panuse tuberkuloosi, koolera ja marutaudi uurimisse, 1886. aastal korraldas ta koos I. Mechnikoviga Odessas esimese Pasteuri jaama ja juurutas marutaudivastase vaktsineerimise praktikasse. Ta avastas lindude vibrio – lindude kooleralaadse haiguse põhjustaja – ja nimetas selle Ilja Iljitši auks Mechnikovi vibrioks. Seejärel saadi inimese koolera vastane vaktsiin.
Gamaleya pööras suurt tähelepanu ka nakkushaiguste epidemioloogiale. Ta oli immunoloogia valdkonna suur spetsialist. Olles välja töötanud originaalse meetodi rõugevaktsiini valmistamiseks, pakkus ta kõigepealt välja idee eraldada bakteritest kõige täiuslikumad antigeenid ja kasutada neid niinimetatud keemiliste vaktsiinide valmistamiseks. Gamaleya oli esimene, kes jälgis ja kirjeldas bakterite spontaanse lüüsi nähtust tol ajal tundmatu aine – bakteriofaagi – mõjul. Seetõttu peetakse Gamaleyat mitte ainult meditsiinilise mikrobioloogia, vaid ka immunoloogia ja viroloogia üheks rajajaks.
S.N.Vinogradsky, V.L. Omeljanski, B.L. Isachenko, D.I. Ivanovski, G.A. Nadson, kes olid üldmikrobioloogia teatud suundade rajajad. Näiteks mulla mikroorganismide ökoloogia õpetuse loomine on lahutamatult seotud vene teadlase S. Vinogradski (1856-1953) nimega. Winogradsky andis suure panuse ka mikroobimaailma füsioloogilise mitmekesisuse tundmisse. Ta viis läbi klassikalisi töid väävlibakterite ja rauabakterite füsioloogia kohta, mille tulemusena avastati bakterites kemosüntees – 19. sajandi suurim avastus.
S. Winogradsky tõestas, et on baktereid, mis sünteesivad iseseisvalt orgaanilist ainet, kasutades selleks mineraalsete ühendite (vesiniksulfiid, ammoniaak) ja süsinikdioksiidi oksüdatsioonienergiat jne. See tähendab, et avastati uut tüüpi mikroorganismide toitumine - autotrofism.
Winogradsky pidev nõue oli uurida mikroorganisme nende looduslikus elupaigas või looduslikele võimalikult lähedastes tingimustes. Seda põhimõtet järgides töötas ta välja lihtsad ja originaalsed meetodid mulla mikroorganismide uurimiseks. Valikulise (selektiivse) söötme meetod on muutunud üldtunnustatud ja laialdaselt kasutatavaks, võimaldades isoleerida looduskeskkonnast mitmeid uusi mikroorganisme ja määrata nende rolli aineringes.
S. Winogradsky avaldas üle 300 teadusliku artikli mulla mikroorganismide ökoloogia ja füsioloogia kohta. Teda peetakse õigusega mullamikrobioloogia isaks. Vene mikrobioloogia ühe silmapaistva rajaja hulka peaks kuuluma ka S. Vinogradsky õpilane V.L. Omaljanski (1867-1928). Ta polnud mitte ainult tähelepanuväärne teadlane, vaid ka andekas õpetaja ja mikrobioloogia saavutuste populariseerija. V. Omeljanskil olid sarnaselt Pasteuriga sügavad teadmised keemia vallas, mis olid aluseks tema ja mikroorganismide ökoloogilisele uurimisele. V. Omeljanski teaduslike huvide ring on väga lai, kuid tema uurimistöö põhisuund on seotud looduses leiduvate ainete ringluse uurimisega, milles ta omistas olulise rolli mikroorganismidele. Orgaanilise aine lagunemisprotsesse uurides eraldas ta esimesena tselluloosi lagundavad bakterid, kirjeldas nende füsioloogiat ja protsessi enda keemiat.
Omeljansky uuris põhjalikult ja põhjalikult lämmastikuringes osalevaid mikroorganisme, eriti vabalt elavaid lämmastikufiksaatoreid ja nitrifikaatoreid. Üks Omeljanski viimastest teostest "Mikroorganismide roll kivimite ilmastikumõjus" kuulub uude uurimisvaldkonda. See töö pani aluse geoloogilisele mikrobioloogiale.
Omeljanski suur teene on esimese venekeelse õpiku "Mikrobioloogia põhialused" loomine, mis ilmus 1909. aastal ja läbis 9 väljaannet. Selles võttis Omeljansky kokku mikrobioloogiliste uuringute tulemused ja andis üldised diagrammid üksikute elementide, sealhulgas lämmastiku, süsiniku, väävli ja raua tsükli kohta. Aastakümneid on see õpik olnud spetsialistide teatmeteos.
Mikrobioloogia ökoloogilise suuna töötas edukalt välja B.L. Isachenko (1871-1948). Veemikrobioloogia valdkonna tööd on laialt tuntuks saanud. Ta oli esimene, kes uuris mikroorganismide levikut Põhja-Jäämeres ning tõi välja nende olulise rolli geoloogilistes protsessides ja ainete ringlemises veekogudes.
D.I. andis suure panuse kodumaise ja maailma mikrobioloogia arengusse. Ivanovski (1864-1920), kes avastas 1892. aastal taimeviirused ja pani sellega aluse uuele teadusele – viroloogiale. Inglise viroloog N. Pirie kirjutas Ivanovski uurimistöö tähtsust rõhutades: "Ivanovski avastuse tohutu tähtsus teoreetilisele loodusteadusele seisneb selles, et ta avastas valgukehade uue eksisteerimise vormi." Ivanovski ideed mängisid otsustavat rolli viroloogia hiilgavas edus, mille tulemusena avastati enamiku inimeste, loomade, taimede ja mikroorganismide viirushaiguste tekitajad. Ameerika viroloogi Stanley järelduse kohaselt tuleks Ivanovski nime viroloogias käsitleda samas valguses Pasteuri ja Kochi nimedega mikrobioloogias.
10. Sfäärilised kujundid(kokid) - sfäärilised bakterid suurusega 0,5 - 1,0 mikronit; Rakkude vastastikuse paigutuse järgi eristatakse mikrokokke, diplokokke, streptokokke, tetrakokke, sarkinaid ja stafülokokke.
Mikrokokid (lat. väikesed) - eraldi asetsevad rakud või "pakkide" kujul.
Diplokokid (lat. double) - on paigutatud paaridesse, kuna rakud pärast jagunemist ei eraldu.
Streptokokid (kreeka keelest streptos - ahel) on ümmargused või pikliku kujuga rakud, mis moodustavad ahela rakkude jagunemise tõttu samas tasapinnas ja säilitavad nendevahelise sideme jagunemiskohas.
Sartsiinid (ladina keelest sarcina - kimp, pall) - on paigutatud 8 või enama koki pakettidena, kuna need moodustuvad rakkude jagunemisel kolmel üksteisega risti asetseval tasapinnal.
Stafülokokid (kreeka keelest staphyle - viinamarjakobar) on kookid, mis paiknevad viinamarjakobarana erinevatel tasapindadel jagunemise tulemusena.
Vardakujulised bakterid erinevad suuruse, rakuotste kuju ja rakkude suhtelise paigutuse poolest. Raku pikkus varieerub vahemikus 1,0 kuni 8,0, paksus 0,5 kuni 2,0 µm. Vardad võivad olla korrapärase (Escherichia coli) või ebakorrapärase kujuga (korünebakterid), sealhulgas hargnevad, näiteks aktinomütseedid. Kergelt kõveraid vardaid nimetatakse vibriodeks (Vibrio cholerae). Enamik pulgakujulisi baktereid on paigutatud juhuslikult, kuna rakud liiguvad pärast jagunemist lahku.
Elementaarkehad sisenevad epiteelirakku endotsütoosi teel koos rakusisese vakuooli moodustumisega. Raku sees nad suurenevad ja muunduvad jagunevateks retikulaarseteks kehadeks, moodustades vakuoolides (sulgudes) klastreid. Elementaarkehad moodustuvad retikulaarsetest kehadest, mis lahkuvad rakkudest eksotsütoosi või rakulüüsi teel.
Mükoplasmad on väikesed bakterid (0,15–1,0 µm), mis on ümbritsetud tsütoplasmaatilise membraaniga ja ilma rakuseinata. Rakuseina puudumise tõttu on mükoplasmad osmootselt tundlikud. Neid on mitmesuguse kujuga: kookoidsed, niitjad, kolvikujulised. Need vormid on nähtavad mükoplasmade puhaste kultuuride faasikontrastmikroskoopia abil. Patogeensed mükoplasmad põhjustavad kroonilisi infektsioone – mükoplasmoosi.
Aktinomütseedid on hargnevad, filamentsed või pulgakujulised grampositiivsed bakterid. Nad said oma nime (kreeka keelest actis - ray, mykes - seen) tänu mõjutatud kudedes moodustumisele druseni - tihedalt põimunud niitide graanulite kujul, mis ulatuvad keskelt ja lõpevad kolvikujuliste paksenemistega. Aktinomütseedid võivad seeneniidistiku killustumise teel jaguneda rakkudeks, mis on sarnased pulgakujulistele ja kookoidbakteritele. Aktinomütseedi õhuhüüfidel võivad moodustuda eosed, mida kasutatakse paljunemiseks. Aktinomütseedi eosed ei ole tavaliselt kuumakindlad.
Ühise filogeneetilise haru aktinomütseetidega moodustavad nn nokardiformsed (nokardioformsed) aktinomütseedid - pulgakujuliste, ebakorrapärase kujuga bakterite kollektiivne rühm. Nende üksikud esindajad moodustavad hargnevaid vorme. Nende hulka kuuluvad bakterid perekondadest Corynebacterium, bdycobacterium, Hocardia jne.
Nocardi-sarnased aktinomütseedid eristuvad suhkrute arabinoosi, galaktoosi, aga ka mükoolhapete ja suurte rasvhapete sisalduse poolest rakuseinas. Mükoolhapped ja rakuseina lipiidid määravad bakterite, eelkõige mükobakterite tuberkuloosi ja leepra happeresistentsuse (Ziehl-Neelseni järgi värvides on need punased ning happeresistentsed bakterid ja koeelemendid, röga on sinised).
Keerdunud vormid on spiraalikujulised bakterid, näiteks spirilla, millel on korgitserikujuliste keerdunud rakkude välimus. Patogeense spirilla hulka kuulub tekitaja sodoku (rotihammustushaigus). Keeruliste hulka kuuluvad ka Campylobacter, Helicobacter, mille kõverad on nagu lendava kajaka tiib; bakterid nagu spiroheedid on samuti nende lähedal.
Spiroheedid on õhukesed, pikad, keerdunud (spiraalikujulised) bakterid, mis erinevad spirillust oma liikuvuse poolest rakkude paindemuutuste tõttu. Spiroheetidel on välismembraani rakusein, mis ümbritseb tsütoplasmaatilise membraaniga protoplasmilist silindrit. Rakuseina välismembraani all (periplasmas) on periplasmaatilised fibrillid (flagella), mis justkui keerdudes ümber spiroheedi protoplasmilise silindri, annavad sellele spiraalse kuju (spiroheedi esmased lokid). Fibrillid on kinnitatud raku otste külge ja suunatud üksteise poole. Fibrillide teine ots on vaba. Fibrillide arv ja paigutus on liikide lõikes erinev. Fibrillid osalevad spiroheetide liikumises, andes rakkudele pöörlemis-, painutus- ja translatsiooniliikumise. Sel juhul moodustavad spiroheedid silmuseid, lokke ja painutusi, mida nimetatakse sekundaarseteks lokideks.
Spirochetes ei taju värvaineid hästi. Neid värvitakse Romanovsky-Giemsa meetodil ehk hõbedamisel ning elaval kujul uuritakse ühekontrast- või tumedavälja mikroskoopiaga.
Leptospiral (perekond Leptospira) on madalad ja sagedased lokid - keerdunud köie kujul. Nende spiroheetide otsad on kõverad nagu konksud, mille otstes on paksendeid. Sekundaarseid lokke moodustades omandavad nad tähtede S või C kuju; on 2 aksiaalset keerme. Patogeenne esindaja L. küsitleb põhjustab leptospiroosi.
Bakterite keskmine suurus on 0,5-5 mikronit. Näiteks Escherichia coli mõõtmed on 0,3-1 x 1-6 mikronit, Staphylococcus aureus'e läbimõõt on 0,5-1 mikronit, Bacillus subtilis 0,75 x 2-3 mikronit. Suurim teadaolev bakter on Thiomargarita namibiensis, mille suurus ulatub 750 mikronini (0,75 mm). Teine on Epulopiscium fishelsoni, mille läbimõõt on 80 mikronit ja pikkus kuni 700 mikronit ning mis elab kirurgilise kala Acanthurus nigrofuscus seedetraktis. Achromatium oxaliferum ulatub mõõtmeteni 33 x 100 mikronit, Beggiatoa alba - 10 x 50 mikronit. Spirochetes võib kasvada kuni 250 µm pikkuseks ja paksusega 0,7 µm. Samal ajal hõlmavad bakterid kõige väiksemaid rakulise struktuuriga organisme. Mycoplasma mycoides on 0,1-0,25 mikroni suurune, mis on sarnane suurte viiruste, nagu tubaka mosaiik, lehmarõuged või gripp. Teoreetiliste arvutuste kohaselt muutub sfääriline rakk läbimõõduga alla 0,15-0,20 mikroni iseseisvaks paljunemiseks võimetuks, kuna see ei sisalda füüsiliselt piisavas koguses kõiki vajalikke biopolümeere ja struktuure.
Siiski on kirjeldatud nanobaktereid, mis on „vastuvõetavast“ suurusest väiksemad ja erinevad väga tavalistest bakteritest. Erinevalt viirustest on nad võimelised iseseisvalt kasvama ja paljunema (äärmiselt aeglane). Neid on seni vähe uuritud, nende eluslooduse seatakse kahtluse alla.
Raku raadiuse lineaarse suurenemisega suureneb selle pind proportsionaalselt raadiuse ruuduga ja ruumala proportsionaalselt kuubikuga, seetõttu on väikestes organismides pinna ja ruumala suhe suurem kui suuremates, mis tähendab esimeste jaoks aktiivsemat ainete vahetust keskkonnaga. Metaboolne aktiivsus, mõõdetuna erinevate näitajatega, biomassi ühiku kohta on väikevormidel suurem kui suurtel. Seetõttu annavad isegi mikroorganismide väikesed suurused bakteritele ja arheadele eeliseid kasvu ja paljunemise kiiruses võrreldes keerukamate eukarüootidega ning määravad nende olulise ökoloogilise rolli.
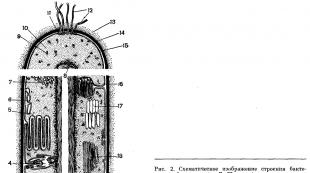
11. Bakteriraku ehituse üldskeem on näidatud joonisel 2. Bakteriraku sisemine korraldus on keeruline. Igal süstemaatilisel mikroorganismide rühmal on oma spetsiifilised struktuuriomadused.
Raku sein. Bakterirakk on kaetud tiheda membraaniga. Seda pinnakihti, mis asub väljaspool tsütoplasmamembraani, nimetatakse rakuseinaks (joonis 2, 14). Sein täidab kaitse- ja tugifunktsioone, samuti annab rakule püsiva iseloomuliku kuju (näiteks varda või kooki kuju) ning esindab raku välist skeletti. See tihe kest muudab bakterid taimerakkudega sarnaseks, mis eristab neid loomarakkudest, millel on pehme kest. Bakteriraku sees on osmootne rõhk mitu korda, mõnikord kümneid kordi kõrgem kui väliskeskkonnas. Seetõttu puruneks rakk kiiresti, kui seda ei kaitseks nii tihe, jäik struktuur nagu rakusein.
Rakuseina paksus on 0,01-0,04 mikronit. See moodustab 10–50% bakterite kuivmassist. Rakuseina moodustava materjali hulk muutub bakterite kasvu ajal ja tavaliselt suureneb koos vanusega.
Seinte peamiseks struktuurikomponendiks, nende jäiga struktuuri aluseks peaaegu kõigis seni uuritud bakterites, on mureiin (glükopeptiid, mukopeptiid). See on keerulise struktuuriga orgaaniline ühend, mis sisaldab lämmastikku kandvaid suhkruid - aminosuhkruid ja 4-5 aminohapet. Veelgi enam, rakuseina aminohapetel on ebatavaline kuju (D-stereoisomeerid), mida looduses leidub harva.
Rakuseina koostisosad, selle komponendid moodustavad keeruka tugeva struktuuri.
Kasutades 1884. aastal Christian Grami poolt esmakordselt välja pakutud värvimismeetodit, võib bakterid jagada kahte rühma: grampositiivsed ja gramnegatiivsed. Grampositiivsed organismid on võimelised siduma mõningaid aniliinvärve, näiteks kristallvioletset, ning säilitama pärast töötlemist joodi ja seejärel alkoholiga (või atsetooniga) joodi-värvi kompleksi. Samad bakterid, milles see kompleks etüülalkoholi mõjul hävib (rakud muutuvad värviliseks), liigitatakse gramnegatiivseteks.
Grampositiivsete ja gramnegatiivsete bakterite rakuseinte keemiline koostis on erinev.
Grampositiivsetel bakteritel on rakuseinte koostises lisaks mukopeptiididele polüsahhariidid (komplekssed kõrgmolekulaarsed suhkrud), teikhoiinhapped (koostise ja struktuuriga komplekssed ühendid, mis koosnevad suhkrutest, alkoholidest, aminohapetest ja fosforhappest ). Polüsahhariidid ja teikhoiinhapped on seotud seinakarkassiga – mureiiniga. Me ei tea veel, millise struktuuri need grampositiivsete bakterite rakuseina komponendid moodustavad. Kasutades õhukeste lõikude elektroonilisi fotosid (kihilisus), ei tuvastatud seintes grampositiivseid baktereid. Tõenäoliselt on kõik need ained omavahel väga tihedalt seotud.
Gramnegatiivsete bakterite seinad on keemilise koostisega keerulisemad, need sisaldavad märkimisväärses koguses valkude ja suhkrutega seotud lipiide (rasvu) kompleksseteks kompleksideks - lipoproteiinideks ja lipopolüsahhariidideks. Gramnegatiivsete bakterite rakuseintes on mureiini üldiselt vähem kui grampositiivsetes bakterites. Ka gramnegatiivsete bakterite seina struktuur on keerulisem. Elektronmikroskoobi abil leiti, et nende bakterite seinad on mitmekihilised (joonis 6).
Sisemine kiht koosneb mureiinist. Selle kohal on laiem kiht lõdvalt pakitud valgumolekule. See kiht on omakorda kaetud lipopolüsahhariidi kihiga. Ülemine kiht koosneb lipoproteiinidest.
Rakusein on läbilaskev: selle kaudu liiguvad toitained vabalt rakku ja ainevahetusproduktid väljuvad keskkonda. Suure molekulmassiga suured molekulid ei läbi kesta.
Kapsel. Paljude bakterite rakuseina ümbritseb pealt limaskesta kiht – kapsel (joon. 7). Kapsli paksus võib olla mitu korda suurem kui raku enda läbimõõt ja mõnikord on see nii õhuke, et seda on võimalik näha vaid läbi elektronmikroskoobi – mikrokapsli.
Kapsel ei ole raku oluline osa, see moodustub sõltuvalt tingimustest, milles bakterid satuvad. See toimib raku kaitsekattena ja osaleb vee ainevahetuses, kaitstes rakku kuivamise eest.
Kapslite keemiline koostis on enamasti polüsahhariidid. Mõnikord koosnevad need glükoproteiinidest (suhkrute ja valkude komplekssed kompleksid) ja polüpeptiididest (perekond Bacillus), harvadel juhtudel - kiudainetest (perekond Acetobacter).
Mõnede bakterite poolt substraati eritatavad limaained põhjustavad näiteks riknenud piima ja õlle limaskest konsistentsi.
Tsütoplasma. Kogu raku sisu, välja arvatud tuum ja rakuseina, nimetatakse tsütoplasmaks. Tsütoplasma (maatriksi) vedel, struktuurita faas sisaldab ribosoome, membraanisüsteeme, mitokondreid, plastiide ja muid struktuure, aga ka varutoitaineid. Tsütoplasma on äärmiselt keerulise peene struktuuriga (kihiline, teraline). Elektronmikroskoobi abil on avastatud palju huvitavaid detaile raku struktuurist.
Bakteriaalse protoplasti välimist lipoprotoidkihti, millel on erilised füüsikalised ja keemilised omadused, nimetatakse tsütoplasmaatiliseks membraaniks (joon. 2, 15).
Tsütoplasma sees on kõik elutähtsad struktuurid ja organellid.
Tsütoplasma membraanil on väga oluline roll – see reguleerib ainete sisenemist rakku ja ainevahetusproduktide väljumist väljapoole.
Läbi membraani saavad toitained rakku siseneda ensüümidega seotud aktiivse biokeemilise protsessi tulemusena. Lisaks toimub membraanis mõnede rakukomponentide süntees, peamiselt rakuseina ja kapsli komponendid. Lõpuks sisaldab tsütoplasmaatiline membraan kõige olulisemaid ensüüme (bioloogilised katalüsaatorid). Ensüümide järjestatud paigutus membraanidel võimaldab reguleerida nende aktiivsust ja vältida mõne ensüümi hävitamist teiste poolt. Membraaniga on seotud ribosoomid - struktuursed osakesed, millel sünteesitakse valku. Membraan koosneb lipoproteiinidest. See on piisavalt tugev ja suudab tagada raku ajutise eksisteerimise ilma kestata. Tsütoplasmaatiline membraan moodustab kuni 20% raku kuivmassist.
Plasmamembraani ja rakuseina vahel on ühendus desmooside - sildade kujul. Tsütoplasmaatiline membraan põhjustab sageli invaginatsioone – invaginatsioone rakku. Need invaginatsioonid moodustavad tsütoplasmas spetsiaalsed membraanstruktuurid, mida nimetatakse mesosoomideks. Teatud tüüpi mesosoomid on kehad, mis on tsütoplasmast eraldatud omaenda membraaniga. Nendesse membraanikottidesse on pakitud arvukalt vesiikuleid ja torukesi (joonis 2). Need struktuurid täidavad bakterites mitmesuguseid funktsioone. Mõned neist struktuuridest on mitokondrite analoogid. Teised täidavad endoplasmaatilise retikulumi või Golgi aparaadi funktsioone. Tsütoplasmaatilise membraani invagineerimisega moodustub ka bakterite fotosünteesiaparaat. Pärast tsütoplasma invagineerimist jätkab membraan kasvamist ja moodustab virnad (tabel 30), mida analoogselt taimede kloroplasti graanulitega nimetatakse tülakoidide virnadeks. Nendes membraanides, mis sageli täidavad suurema osa bakteriraku tsütoplasmast, paiknevad fotosünteesi protsessi teostavad pigmendid (bakterioklorofüll, karotenoidid) ja ensüümid (tsütokroomid).
Bakterite tsütoplasma sisaldab ribosoome, valke sünteesivaid osakesi läbimõõduga 200A. Neid on ühes puuris üle tuhande. Ribosoomid koosnevad RNA-st ja valgust. Bakterites paiknevad paljud ribosoomid vabalt tsütoplasmas, osa neist võib olla seotud membraanidega.
Ribosoomid on rakus valkude sünteesi keskused. Samal ajal ühenduvad nad sageli üksteisega, moodustades agregaate, mida nimetatakse polüribosoomideks või polüsoomideks.
Bakterirakkude tsütoplasma sisaldab sageli erineva kuju ja suurusega graanuleid. Kuid nende olemasolu ei saa pidada mingisuguseks püsivaks märgiks mikroorganismist, enamasti on see suuresti seotud keskkonna füüsikaliste ja keemiliste tingimustega. Paljud tsütoplasmaatilised inklusioonid koosnevad ühenditest, mis toimivad energia- ja süsinikuallikana. Need varuained tekivad siis, kui keha on varustatud piisavate toitainetega, ja vastupidi, kasutatakse siis, kui organism satub toitumise seisukohalt ebasoodsamatesse tingimustesse.
Paljudes bakterites koosnevad graanulid tärklisest või muudest polüsahhariididest – glükogeenist ja granuloosist. Mõnel bakteril on suhkrurikkas keskkonnas kasvatamisel rakus rasvapiisad. Teine laialt levinud granuleeritud inklusioonide tüüp on volutiin (metakromatiini graanulid). Need graanulid koosnevad polümetafosfaadist (fosforhappe jääke sisaldav varuaine). Polümetafosfaat on keha jaoks fosfaatrühmade ja energia allikas. Bakterid koguvad volutiini suurema tõenäosusega ebatavalistes toitumistingimustes, näiteks väävlivabas keskkonnas. Mõnede väävlibakterite tsütoplasmas on väävli tilgad.
Lisaks erinevatele struktuurikomponentidele koosneb tsütoplasma vedelast osast - lahustuvast fraktsioonist. See sisaldab valke, erinevaid ensüüme, t-RNA-d, mõningaid pigmente ja madala molekulmassiga ühendeid – suhkruid, aminohappeid.
Madala molekulmassiga ühendite esinemise tagajärjel tsütoplasmas tekib raku sisu ja väliskeskkonna osmootse rõhu erinevus ning see rõhk võib erinevate mikroorganismide puhul olla erinev. Suurimat osmootset rõhku täheldatakse grampositiivsetes bakterites - 30 atm, gramnegatiivsetes bakterites on see palju madalam - 4-8 atm.
Tuumaaparaat. Tuumaaine desoksüribonukleiinhape (DNA) paikneb raku keskosas.
Bakteritel ei ole sellist tuuma nagu kõrgematel organismidel (eukarüootidel), kuid neil on selle analoog - "tuumaekvivalent" - nukleoid (vt joonis 2, 8), mis on tuumaaine evolutsiooniliselt primitiivsem organiseerimisvorm. Mikroorganismid, millel puudub päristuum, kuid millel on selle analoog, liigitatakse prokarüootidena. Kõik bakterid on prokarüootid. Enamiku bakterite rakkudes on suurem osa DNA-st koondunud ühte või mitmesse kohta. Eukarüootsetes rakkudes paikneb DNA kindlas struktuuris – tuumas. Südamikku ümbritseb membraan.
Bakterites on DNA erinevalt tõelistest tuumadest vähem tihedalt kokku pakitud; Nukleoidil ei ole membraani, nukleooli ega kromosoomide komplekti. Bakteri DNA ei ole seotud peamiste valkude – histoonidega – ja paikneb nukleoidis fibrillide kimbu kujul.
Flagella. Mõnel bakteril on pinnal lisandistruktuurid; Kõige levinumad neist on flagellad - bakterite liikumisorganid.
Lipu kinnitatakse tsütoplasmaatilise membraani alla, kasutades kahte paari kettaid. Bakteritel võib olla üks, kaks või mitu flagellat. Nende asukoht on erinev: raku ühes otsas, kahes, kogu pinna ulatuses jne (joon. 9). Bakterite viburite läbimõõt on 0,01-0,03 mikronit, nende pikkus võib olla mitu korda suurem kui raku pikkus. Bakteriaalsed flagellad koosnevad valgust - flagelliinist - ja on keerdunud spiraalsed filamentid.
 23 Ensüümid või ensüümid (alates lat.fermentum, kreeka keel ζύμη, ἔνζυμον - juuretis) - tavaliselt valgumolekulid või RNA molekulid (ribosüümid) või nende kompleksid, mis kiirendavad (katalüüsivad) keemilisi reaktsioone elussüsteemides. Ensüümkatalüüsitud reaktsiooni reagente nimetatakse substraatideks ja saadud aineid toodeteks. Ensüümid on substraadispetsiifilised (ATPaas katalüüsib ainult ATP lagunemist ja fosforülaasi kinaas fosforüleerib ainult fosforülaasi). Ensüümi aktiivsust saab reguleerida aktivaatorite ja inhibiitoritega (aktivaatorid suurenevad, inhibiitorid vähenevad) Valgu ensüümid sünteesitakse ribosoomidel, RNA sünteesitakse tuumas.
23 Ensüümid või ensüümid (alates lat.fermentum, kreeka keel ζύμη, ἔνζυμον - juuretis) - tavaliselt valgumolekulid või RNA molekulid (ribosüümid) või nende kompleksid, mis kiirendavad (katalüüsivad) keemilisi reaktsioone elussüsteemides. Ensüümkatalüüsitud reaktsiooni reagente nimetatakse substraatideks ja saadud aineid toodeteks. Ensüümid on substraadispetsiifilised (ATPaas katalüüsib ainult ATP lagunemist ja fosforülaasi kinaas fosforüleerib ainult fosforülaasi). Ensüümi aktiivsust saab reguleerida aktivaatorite ja inhibiitoritega (aktivaatorid suurenevad, inhibiitorid vähenevad) Valgu ensüümid sünteesitakse ribosoomidel, RNA sünteesitakse tuumas.
Ensüümide funktsioonid
Ensüüme leidub kõigis elusrakkudes ja need aitavad muuta mõningaid aineid (substraate) teisteks (produktideks). Ensüümid toimivad katalüsaatoritena peaaegu kõigis elusorganismides toimuvates biokeemilistes reaktsioonides – need katalüüsivad enam kui 4000 erinevat biokeemilist reaktsiooni. Ensüümid mängivad olulist rolli kõigis eluprotsessides, suunates ja reguleerides organismi ainevahetust.
Nagu kõik katalüsaatorid, kiirendavad ensüümid nii edasi- kui ka vastupidiseid reaktsioone, vähendades protsessi aktiveerimisenergiat. Sel juhul ei nihku keemiline tasakaal ei ette ega taha. Ensüümide eripära võrreldes mittevalguliste katalüsaatoritega on nende kõrge spetsiifilisus – mõne substraadi seondumiskonstant valguga võib ulatuda 10–10 mol/l või alla selle. Iga ensüümi molekul on võimeline sooritama mitu tuhat kuni mitu miljonit "toimingut" sekundis. Näiteks ensüümi reniini üks molekul, mis sisaldub vasika mao limaskestas, tarretab temperatuuril 37 °C 10 minutiga umbes 10 6 molekuli piima kaseinogeeni. Pealegi on ensüümide efektiivsus palju suurem kui mittevalguliste katalüsaatorite efektiivsus – ensüümid kiirendavad reaktsioone miljoneid ja miljardeid kordi, mittevalgulised katalüsaatorid – sadu ja tuhandeid kordi. Vaata ka katalüütiliselt täiuslik ensüüm
ENSÜÜMIDE PÕHIOMADUSED
Ensüümidel, olles valgud, on mitmeid sellele orgaaniliste ühendite klassile iseloomulikke omadusi, mis erinevad anorgaaniliste katalüsaatorite omadustest.
Ensüümide termiline labiilsus. Keemiliste reaktsioonide kiirus sõltub temperatuurist, seega on ensüümkatalüüsitud reaktsioonid tundlikud ka temperatuurimuutuste suhtes. On kindlaks tehtud, et enamiku biokeemiliste reaktsioonide kiirus suureneb 2 korda, kui temperatuur tõuseb 10 ° C võrra, ja vastupidi, väheneb 2 korda, kui temperatuur langeb 10 ° C võrra. Seda indikaatorit nimetatakse temperatuurikoefitsiendiks. Kuid ensüümi valgulise olemuse tõttu vähendab termiline denatureerimine temperatuuri tõusuga ensüümi efektiivset kontsentratsiooni koos reaktsioonikiiruse vastava vähenemisega. Seega temperatuuril, mis ei ületa 45–50°C, suureneb reaktsioonikiirus vastavalt keemilise kineetika teooriale. Temperatuuridel üle 50°C hakkab reaktsioonikiirusele suurt mõju avaldama ensüümvalgu termiline denaturatsioon, mis viib ensümaatilise protsessi täieliku seiskumiseni (joonis 4.16).
Seega on termolabiilsus ehk tundlikkus kõrgendatud temperatuuri suhtes üks ensüümidele iseloomulikke omadusi, mis eristab neid järsult anorgaanilistest katalüsaatoritest. Viimase juuresolekul suureneb reaktsioonikiirus plahvatuslikult temperatuuri tõustes (vt kõverat “a” joonisel 4.16). Temperatuuril 100°C kaotavad peaaegu kõik ensüümid oma aktiivsuse (ainsaks erandiks on ilmselgelt üks lihaskoe ensüüm – müokinaas, mis talub kuumutamist kuni 100°C). Enamiku ensüümide toime optimaalne temperatuur soojaverelistel loomadel on 40°C; nendes tingimustes on reaktsioonikiirus maksimaalne tänu reageerivate molekulide kineetilise energia suurenemisele. Madalatel temperatuuridel (0°C ja alla selle) ensüümid reeglina ei hävine, kuigi nende aktiivsus langeb peaaegu nullini. Kõigil juhtudel on oluline sobiva temperatuuriga kokkupuute aeg. Praegu on otsese seose olemasolu pepsiini, trüpsiini ja paljude teiste ensüümide puhul tõestatud.

Riis. 4.17. Ensüümkatalüüsitud reaktsiooni kiiruse sõltuvus pH-st (nool näitab pH optimumi).
ensüümi inaktiveerimise kiiruse ja valgu denaturatsiooni astme vahel. Tuleb märkida, et ensüümide termolabiilsust mõjutavad kindlasti substraadi kontsentratsioon, keskkonna pH ja muud tegurid. Ensüümide aktiivsuse sõltuvus keskkonna pH-st. Ensüümid on tavaliselt kõige aktiivsemad kitsas vesinikioonide kontsentratsiooni tsoonis, mis loomsete kudede puhul vastab peamiselt evolutsiooni käigus välja kujunenud füsioloogilistele pH väärtustele 6,0–8,0. Graafiliselt joonistades on kellakujulisel kõveral konkreetne punkt, kus ensüümil on maksimaalne aktiivsus; seda punkti nimetatakse selle ensüümi toime jaoks keskkonna optimaalseks pH-ks (joonis 4.17). Ensüümi aktiivsuse sõltuvuse määramisel vesinikioonide kontsentratsioonist viiakse reaktsioon läbi keskkonna erinevatel pH väärtustel, tavaliselt optimaalsel temperatuuril ja substraadi piisavalt kõrge (küllastava) kontsentratsiooni juuresolekul. Tabelis Tabelis 4.3 on näidatud mitmete ensüümide optimaalsed pH väärtused. 
Tabeli andmetest. 4.3 on näha, et ensüümi toime pH optimum jääb füsioloogiliste väärtuste piiridesse. Erandiks on pepsiin, mille pH optimum on 2,0 (pH 6,0 juures ei ole see aktiivne ja stabiilne). Seda seletatakse esiteks ensüümmolekuli struktuurilise ülesehitusega ja teiseks asjaoluga, et pepsiin on vaba vesinikkloriidhapet sisaldava maomahla komponent, mis loob selle ensüümi toimimiseks optimaalse happelise keskkonna. Teisest küljest asub arginaasi pH optimum tugevalt aluselises tsoonis (umbes 10,0); Maksarakkudes sellist keskkonda ei ole, seetõttu ei toimi arginaas ilmselt oma optimaalses pH-tsoonis in vivo.
Kaasaegsete kontseptsioonide kohaselt mõjutab keskkonna pH muutuste mõju ensüümi molekulile happeliste ja aluseliste rühmade (eriti dikarboksüülaminohapete COOH-rühma, tsüsteiini SH-rühma) olekut ja ionisatsiooniastet. , histidiini imidasooli lämmastik, NH 2 rühma lüsiin jne). Järsku nihkega keskkonna optimaalsest pH-st võivad ensüümid läbi viia konformatsioonilisi muutusi, mille tulemuseks on aktiivsuse kadumine denaturatsiooni või ensüümmolekuli laengu muutumise tõttu. Söötme erinevatel pH väärtustel võib aktiivne kese olla osaliselt ioniseeritud või ioniseerimata kujul, mis mõjutab valgu tertsiaarset struktuuri ja vastavalt ka aktiivse ensüümi-substraadi kompleksi moodustumist. Lisaks on oluline substraatide ja kofaktorite ionisatsiooniseisund.
Ensüümi spetsiifilisus. Ensüümidel on kõrge toime spetsiifilisus. See omadus eristab neid sageli anorgaanilistest katalüsaatoritest. Seega võivad peeneks jahvatatud plaatina ja pallaadium katalüüsida (molekulaarse vesiniku osalusel) kümnete tuhandete erineva struktuuriga keemiliste ühendite redutseerimist. Ensüümi kõrge spetsiifilisuse määrab, nagu märgitud, ensüümi substraadi molekulide konformatsiooniline ja elektrostaatiline komplementaarsus ning aktiivse keskuse ainulaadne struktuurne korraldus, mis tagab "äratundmise", kõrge afiinsuse ja selektiivsuse ensüümi substraadi molekulide vahel. üks reaktsioon tuhandetest teistest elusolendites samaaegselt toimuvatest keemilistest reaktsioonidest.rakud.
Sõltuvalt toimemehhanismist eristatakse suhtelise (või rühma) ja absoluutse spetsiifilisusega ensüüme. Seega on mõnede hüdrolüütiliste ensüümide toimimiseks kõige olulisem keemilise sideme tüüp substraadi molekulis. Näiteks pepsiin lagundab samal määral loomset ja taimset päritolu valke, hoolimata sellest, et need valgud erinevad üksteisest oluliselt nii keemilise struktuuri ja aminohappe koostise kui ka füüsikalis-keemiliste omaduste poolest. Pepsiin aga ei lagunda ei süsivesikuid ega rasvu. Seda seletatakse asjaoluga, et pepsiini kasutuskoht, toimekoht on peptiid-CO-NH side. Lipaasi toimel, mis katalüüsib rasvade hüdrolüüsi glütserooliks ja rasvhapeteks, on sarnane koht esterside. Sarnase rühmaspetsiifilisusega on polüsahhariidides trüpsiin, kümotrüpsiin, peptidaasid, ensüümid, mis hüdrolüüsivad α-glükosiidsidemeid (kuid mitte tselluloosis sisalduvaid β-glükosiidsidemeid) jne. Tavaliselt osalevad need ensüümid seedimisprotsessis ja nende rühmaspetsiifilisus on tõenäolisemalt on kõigel teatud bioloogiline tähendus. Mõned intratsellulaarsed ensüümid on samuti suhtelise spetsiifilisusega, näiteks heksokinaas, mis katalüüsib peaaegu kõigi heksooside fosforüülimist ATP juuresolekul, kuigi samal ajal on rakkudes iga heksoosi jaoks spetsiifilised ensüümid, mis teostavad sama fosforüülimist (vt. 10. peatükk).
Toime absoluutne spetsiifilisus on ensüümi võime katalüüsida ainult ühe substraadi transformatsiooni. Kõik muudatused (modifikatsioonid) substraadi struktuuris muudavad selle ensüümi toimele kättesaamatuks. Sellised ensüümid on näiteks arginaas, mis lagundab arginiini looduslikes tingimustes (organismis), ureaas, mis katalüüsib uurea lagunemist jne.
Eksperimentaalselt on tõendeid nn stereokeemilise spetsiifilisuse olemasolu kohta, mis on tingitud keemiliste ainete optiliselt isomeersete L- ja D-vormide või geomeetriliste (cis- ja trans-) isomeeride olemasolust. Seega on teada L- ja D-aminohapete oksüdaasid, kuigi looduslikes valkudes leidub ainult L-aminohappeid. Iga tüüpi oksüdaasid toimivad ainult oma kindlale stereoisomeerile.
Stereokeemilise spetsiifilisuse selge näide on bakteriaalne aspartaatdekarboksülaas, mis katalüüsib CO 2 eemaldamist ainult L-asparagiinhappest, muutes selle L-alaniiniks. Stereospetsiifilisust näitavad ensüümid, mis katalüüsivad ja sünteetilisi reaktsioone. Seega sünteesitakse kõigis elusorganismides ammoniaagist ja α-ketoglutaraadist L-isomerglutamiinhapet, mis on osa looduslikest valkudest. Kui ühend eksisteerib cis- ja trans-isomeeride kujul, millel on kaksiksideme ümber erinevad aatomirühmade paigutused, siis reeglina saab ensüümi toime substraadina olla ainult üks neist geomeetrilistest isomeeridest. Näiteks fumaraas katalüüsib ainult fumaarhappe (trans-isomeeri) konversiooni, kuid ei mõjuta maleiinhapet (cis-isomeer):
Seega tagavad ensüümid oma toime kõrge spetsiifilisuse tõttu selle, et rakkude mikroruumis ja kogu organismis toimuvad suurel kiirusel ainult teatud keemilised reaktsioonid väga erinevatest võimalikest transformatsioonidest, reguleerides seeläbi ainevahetuse intensiivsust.
Ensüümide roll ainevahetuses.
Mikrobioloogia mängib inimkonna ajaloos olulist rolli. Selle teaduse päritolu ulatub 6. - 5. sajandisse eKr. e. Juba neil kaugetel aegadel hakkasid inimesed mõistma, et haigused ei teki niisama. Ja see juhtub mikroskoopiliste, silmale nähtamatute mikroorganismide tõttu. Kuidas teadus tekkis ja kujunes?
Mis on mikrobioloogia?
Mikrobioloogia on teadus, mis tegeleb erinevate mikroorganismide eluprotsesside uurimisega ja uurimisega, mida ilma eriaparatuurita näha ei ole. Neil võib olla erinevat päritolu: taimne, loomne. Üks fundamentaalteadusi on mikrobioloogia. Selle põhjalikuks uurimiseks kasutatakse paljusid teisi teadusi, nimelt:
- keemia;
- Füüsika;
- tsütoloogia;
- bioloogia jne.
Mikrobioloogiat on ainult kahte tüüpi: üldine, individuaalne. Üldmikrobioloogia tegeleb väikeste mikroorganismide ehituse ja eluprotsesside uurimisega erinevatel tasanditel. Ja individuaalne mikrobioloogia (või era) tegeleb üksikute mikroobitüüpide uurimisega.
19. sajandil aitasid edusammud meditsiini, eelkõige mikrobioloogia vallas kaasa immunoloogia kujunemisele, mida tänapäeval peetakse üldiseks bioloogiliseks distsipliiniks. Mikrobioloogia arengus võib eristada kolme peamist etappi:
- Paljastades tõsiasja, et looduses on tõesti väikseid mikroorganisme, mida ilma spetsiaalse varustuseta tuvastada ei saa.
- Liikide eristamine.
- Immuunsuse ja haiguste (nakkuslike) uurimine.
Mikrobioloogia põhiülesanne on mikroorganismide omaduste üksikasjalik uurimine. Selleks kasutatakse spetsiaalseid seadmeid, näiteks mikroskoope. Nende abiga saate näha väikeseid organisme ning määrata nende kuju ja asukohta. Meditsiinis tehakse katset, kui tervele loomale siirdatakse teadlikult väikseid mikroorganisme. See aitab rekonstrueerida ja uurida infektsiooni iga etappi.
Prantsuse maadeavastaja Louis Pasteur
27. detsembril 1822 sündis Ida-Prantsusmaal tulevane suur teadlane Louis Pasteur. Juba varases nooruses tundis ta huvi kunstivaldkonna vastu. Kuid hiljem tekkis tal huvi loodusteaduste vastu. Ta õppis Pariisis Ecole Superieure'is. Pärast õpingute lõpetamist oli tema saatus saada reaalainete õpetajaks.
19. sajandi 48. aastal tutvustas Louis omaenda teadusliku uurimistöö tulemusi. Just tema esitas tõendid selle kohta, et viinhape sisaldab kahte tüüpi kristalle, mis polariseerivad valgust täiesti erineval viisil. See märkimisväärne sündmus tähistas tema hiilgava edu algust teaduses.
Louis Pasteur on mikrobioloogia looja. Enne tema töö algust eeldasid teadlased, et pärm moodustas keemilise protsessi. Ja Louis Pasteur suutis pärast mitmete uuringute läbiviimist seda fakti tõestada. Ta avastas, et selliseid mikroorganisme on kahte tüüpi: ühed moodustavad alkoholi, teised aga hävitavad seda. Hiljem suutis ta välja selgitada, et aeglase kuumutamisega hävivad mittevajalikud bakterid, mis tõstis oluliselt alkoholi sisaldavate toodete kvaliteeti.
Teadlast huvitas ka hallituse teke toidule. Hiljem tõestas ta, et hallituse põhjuseks on keskkonnas leiduvad eosed. Mida vähem neid ruumis on, seda aeglasemalt toit rikneb.
Tema uurimistöö aitas päästa Prantsusmaa siiditööstust. Ja ka palju inimelusid, kuna just tema leiutas marutaudivaktsiini.
Saksa teadlane Robert Koch
Koch Robertit peetakse Passeri kaasaegseks. Tema sünd toimus detsembris 1843. 23-aastaselt lõpetas ta meditsiiniülikooli ja sai diplomi, mille järel töötas mitmes raviasutuses.
Tema märkimisväärne karjäär sai alguse tööst bakterioloogina. Ta uuris siberi katku haigetel loomadel. Tema uuringud näitasid, et nakatunud isikutel on palju võõraid mikroorganisme, mida tervetel loomadel ei ole. Need bakterid olid vardakujulised.
Hiljem hakkas Koch tuberkuloosi vastu huvi tundma. Esimesed uuringud viidi läbi tarbimisse surnud töötaja surnukehaga. Elundite üksikasjalik uurimine ei viinud patogeensete bakterite tuvastamiseni. Seejärel soovitas Koch, et proovid tuleks värvida. Ja tõepoolest, teadlane märkas kopsukudede vahel mingeid pulgakesi. Pärast töötas Robert Koch välja tuberkuloosivastase vaktsiini, kuid see ei suutnud haigust ravida, kuid see määras 100% kindlaks, kas patsient on nakatunud või mitte. See vaktsiin on kasutusel tänaseni.
Mikrobioloogiateaduse tekkimine
Inimene kohtas mikroorganismide elutähtsa aktiivsuse mõju palju varem kui nende ametlik avastus. Inimesed kääritasid teadlikult piima, kääritasid tainast ja veini. Isegi Vana-Kreeka teadlase töödes leiti ridu selle kohta, mida ta soovitab haiguste ja ohtlike patogeensete aurude vahelise seose kohta.
Anthony van Leeuwenhoek kinnitas neid oletusi enda leiutatud suurendusklaasi abil. Selle abiga sai Anthony ümbritsevaid objekte uurida. Selgus, et nendel objektidel, mis on palja silmaga nähtamatud, elavad väikesed organismid. Kuid ta ei suutnud kunagi tõestada nende osalemist inimeste nakatamises ohtlike haigustega.
Kodu ennetavat ravi haiguste ennetamiseks pakkusid hindud. 1771. aastal kasutas sõjaväearst Moskvas esmakordselt katku nakatunute asjade desinfitseerimist ning vaktsineeris ka nakatunutega kokku puutunuid.
Kõige põnevam lugu räägib rõugete vastu vaktsineerimise avastamisest. Seda kasutasid ka pärslased, türklased ja hiinlased. Juhtus nii: inimesele viidi sisse nõrgenenud baktereid, sest usuti, et nii läheb haigus kergemini. Inglise arst Edward Jenner märkis, et enamik inimesi, kes ei põe rõugeid, ei nakatunud nakatunud inimestega tihedas kontaktis. Seda asjaolu märgati lüpsjatel, kes puutusid kokku rõugetesse nakatunud lehmadega. Selle fakti uurimine kestis umbes 10 aastat. Selle tulemusena süstis teadlane haige lehma verd tervele poisile. Hiljem pookis Jenner noormehele haige inimese mikroobe. Nii avastati vaktsiin, tänu millele inimesed sellest kohutavast haigusest vabanesid.
Kodumaiste teadlaste uurimused
Kõige kuulsamad avastused mikrobioloogia vallas, mille on teinud teadlased üle kogu maailma, näitavad, et peaaegu igast haigusest on võimalik jagu saada. Kodumaised teadlased on teinud tohutu investeeringu kaasaegse teaduse kujunemisse. Peeter I tegi 1698. aastal tutvust Leeuwenhoekiga, kes omakorda näitas talle mikroskoobi tööd.
L.S. Tsenkovski avaldas oma teaduslikud uurimused, milles mikroorganismid liigitati taimset päritolu organismideks. Ta kasutas Pasteuri meetodeid ka võitluses siberi katkuga.
I.I. Mechnikov kujundas puutumatuse teooria. Ta esitas tugevaid argumente, et paljudel keharakkudel on kõik võimalused viirusbaktereid üksinda alla suruda. Tema uuringud said põletiku uurimise aluseks. Mechnikov uuris inimkeha ja püüdis mõista, miks see vananeb. Professor soovis leida meetodi, mis pikendaks eluiga. Ta uskus, et putrefaktiivsete mikroorganismide tegevuse käigus tekkivad toksilised elemendid mürgitavad inimkeha. Mechnikovi sõnul tuleks keha asustada kääritatud piima mikroorganismidega, mis suruvad alla kahjulikke mikroorganisme. Professor uskus, et nii saab eluiga oluliselt pikendada.
Mechnikov uuris suurt hulka tõsiseid haigusi: tuberkuloosi, kõhutüüfust, koolerat ja paljusid teisi.
Tehniline mikrobioloogia
Tehniline mikrobioloogia uurib baktereid, mida kasutatakse vitamiinide ja teatud ainete tootmisel. Peamiseks probleemiks selles valdkonnas peetakse teaduslike ja tehniliste tehnikate kasvu tootmises (eriti toiduainesektoris).
Tööstusliku mikrobioloogia valdamine suunab spetsialisti vajadusele järgida tootmises absoluutselt kõiki üldtunnustatud sanitaarstandardeid. Seda teadust uurides saate vältida paljude toodete riknemist. Teemat uurivad rohkem tulevased toiduainetööstuse eksperdid.
Uuenduslikud tehnoloogiad
Mikrobioloogia on uuenduslike tehnoloogiate alus. Mikroorganisme ja nende maailma pole veel täielikult uuritud. Enamik teadlasi on kindlad, et mikroorganismide abil on võimalik välja töötada tehnoloogiaid, millel pole analooge. Just biotehnoloogiast saab uusimate tehnoloogiliste avastuste aluseks.
Nafta- ja söemaardlate uurimisel kasutatakse baktereid. Pole saladus, et kütusevarud on juba lõppemas. Seetõttu soovitavad teadlased juba praegu kasutada mikrobioloogilisi meetodeid alkoholide ekstraheerimiseks taastuvatest allikatest.
Mikrobioloogilised tehnoloogiad aitavad ületada keskkonna- ja energiaprobleeme. Uskumatult võimaldab aga orgaaniliste jääkide mikrobioloogiline töötlemine nii keskkonda puhastada kui ka saada biogaasi, mis ei jää alla maagaasile. Seda tüüpi kütuse eraldamise meetod ei nõua suuri kulutusi. Tänapäeval on looduses ümbertöötlemiseks suur hulk kasutatud materjali.
Paljud kaasaegsed teadlased usuvad, et tulevikus on bioloogia see, mis võimaldab ületada paljud energia- ja keskkonnaprobleemid, millel on kõik võimalused võimalikult lühikese aja jooksul ilmneda.
Mikrobioloogia on läbinud pika arengutee, mis kestab hinnanguliselt mitu aastatuhandet. Juba V-IV aastatuhandel eKr. inimene nautis mikroorganismide tegevuse vilju, teadmata nende olemasolust. Veini valmistamine, leivaküpsetamine, juustu valmistamine, nahaparkimine pole midagi muud kui protsessid, mis toimuvad mikroorganismide osalusel. Siis, iidsetel aegadel, eeldasid teadlased ja mõtlejad, et paljud haigused on põhjustatud mõnest eluslooduse kõrvalisest nähtamatust põhjusest.
Järelikult tekkis mikrobioloogia ammu enne meie ajastut. Oma arengus läbis see mitu etappi, mitte niivõrd kronoloogiliselt seotud, kuivõrd põhisaavutuste ja avastuste poolt määratud.
Mikrobioloogia arengulugu võib jagada viieks etapiks: heuristiline, morfoloogiline, füsioloogiline, immunoloogiline ja molekulaargeneetiline.
Heuristiline periood (IV-IIV aastatuhat eKr – 16. sajand pKr) on seotud pigem tõe leidmise loogiliste ja metodoloogiliste meetoditega, s.o. heuristika kui mis tahes katsete ja tõenditega. Tolleaegsed mõtlejad (Hippokrates, Rooma kirjanik Varro jt) tegid oletusi nakkushaiguste, miasmide ja väikeste nähtamatute loomade olemuse kohta. Need ideed sõnastati sidusaks hüpoteesiks palju sajandeid hiljem Itaalia arsti D. Fracastoro (1478-1553) kirjutistes, kes väljendas ideed elada nakkushaigust põhjustavast nakkushaigusest. Pealegi on iga haigus põhjustatud tema enda nakkusest. Haiguste eest kaitsmiseks soovitati patsient isoleerida, panna karantiini, kanda maske ja ravida esemeid äädikaga.
Seega oli D. Fracastoro üks epidemioloogia ehk haiguste tekkepõhjuste, -tingimuste ja -mehhanismide ning nende ennetamise meetodite teaduse rajajaid.
Küll aga sai pärast mikroskoobi leiutamist võimalikuks tõestada nähtamatute patogeenide olemasolu. Mikroorganismide avastamisel kuulub prioriteet Hollandi amatöörlooduseteadlasele Antonio Leeuwenhoekile (1b32 - 1723). Linakaupmees A. Levenguk armastas klaasilihvimist ja viis selle kunsti täiuslikkuseni, konstrueerides mikroskoobi, mis võimaldas kõnealuseid esemeid 300 korda suurendada.
Mikroskoobi all erinevaid objekte (vihmavesi, leotised, hambakatt, veri, väljaheited, sperma) uurides jälgis A. Leeuwenhoek väikseimaid loomi, keda ta nimetas animalculideks. A. Leeuwenhoek andis oma tähelepanekutest regulaarselt aru Londoni Kuninglikule Seltsile ja 1695. aastal võttis ta need kokku raamatus “Anthony Leeuwenhoeki avastatud looduse saladused”.
Seega algab A. Leeuwenhoeki mikroskoobi leiutamisega mikrobioloogia arengu järgmine etapp, mida nimetatakse morfoloogiliseks.
A. Leeuwenhoeki avastus äratas spetsialistide tohutut tähelepanu ning tal oli palju õpilasi ja järgijaid. Ebaselgeks jäid aga küsimused mikroorganismide välimuse, nende elutingimuste, eesmärgi ja inimeste haiguste esinemises osalemise kohta. Need küsimused said hiljem paljude teadlaste uuringutes selged vastused.
Kuigi haiguste teket seostati nüüdseks avastatud mikroorganismidega, oli vaja otseseid tõendeid. Ja need sai vene epidemioloog D. Samoilovitš (1744 - 1805). Tõestamaks, et katku põhjustas spetsiaalne haigustekitaja, nakatas ta end katku põdeva inimese bubo eritistega ja haigestus katku. Õnneks jäi D. Samoilovitš ellu. Seejärel viisid vene arstid G. N. Minkh ja O. O. Mochutkovsky, I. I. Mechnikov jt läbi kangelaslikud eneseinfektsioonikatsed, et tõestada konkreetse mikroorganismi nakkavust.
Küsimus mikroorganismide ilmumise ja paljunemise meetodi kohta lahenes vaidluses tol ajal domineerinud spontaanse genereerimise teooriaga. Vaatamata sellele, et Itaalia teadlane L. Spallanzani 18. sajandi keskel. jälgis mikroskoobi all bakterite jagunemist, arvamust, et nad tekivad ise (tekivad mädanemisest, mustusest jne), ümber ei lükatud.
Seda tegi silmapaistev prantsuse teadlane Louis Pasteur (1822 - 1895), kes oma lihtsuses hiilgava vaimuka katsega näitas, et spontaanset põlvkonda pole olemas. L. Pasteur asetas kolbi steriilse puljongi, mis suhtles atmosfääriõhuga läbi kõvera S-kujulise toru. Sellises sisuliselt avatud kolvis püsis puljong pikemat aega seistes läbipaistev, sest toru kumerus ei lasknud mikroorganismidel koos õhust tulnud tolmuga kolbi tungida.
Mikrobioloogia kiire areng 19. sajandil. tõi kaasa paljude nakkushaiguste (siberi katk, katk, teetanus, difteeria, düsenteeria, koolera, tuberkuloos jne) tekitajate avastamise.
Lõpuks, 1892. aastal, avastas vene botaanik D. I. Ivanovski (1864. 1920) viirused – viiruste kuningriigi esindajad. Need elusolendid läbisid filtreid, mis säilitasid baktereid ja seetõttu nimetati neid filtreeritavateks viirusteks. Esiteks avastati viirus, mis põhjustab tubaka mosaiikina tuntud tubakahaigust, seejärel suu- ja sõrataudi viirus, kollapalavik ja paljud teised viirused. Viirusosakesi sai aga võimalik näha alles pärast elektronmikroskoobi leiutamist, kuna viirused pole valgusmikroskoobis nähtavad. Praeguseks kuulub viiruste kuningriiki (viirus) kuni 1000 patogeenset viirusliiki. Alles hiljuti avastati mitmeid uusi viiruseid, sealhulgas AIDSi põhjustav viirus.
Pole kahtlust, et uute viiruste ja bakterite avastamise periood jätkub. Uute mikroorganismide avastamisega kaasnes mitte ainult nende struktuuri, vaid ka elutegevuse uurimine. Seetõttu nimetatakse 19. sajandit, eriti selle teist poolt, mikrobioloogia arengus tavaliselt füsioloogiliseks perioodiks. Seda etappi seostatakse L. Pasteuri nimega, kellest sai meditsiinilise mikrobioloogia, aga ka immunoloogia ja biotehnoloogia rajaja.
Mitmekülgse haritud, geniaalne eksperimenteerija, Prantsuse Meditsiiniakadeemia liige L. Pasteur tegi mitmeid silmapaistvaid avastusi. Lühikese aja jooksul 1857–1885 tõestas ta, et käärimine (piimhape, alkohol, äädikhape) ei ole keemiline protsess, vaid seda põhjustavad mikroorganismid. Lükkas ümber spontaanse genereerimise teooria; avastas anaerobioosi fenomeni, s.o. mikroorganismide elamise võimalus hapniku puudumisel. pani aluse desinfitseerimisele, aseptikale ja antiseptikutele; avastas viisi, kuidas vaktsineerimisega kaitsta nakkushaiguste eest.
Paljud L. Pasteuri avastused tõid inimkonnale tohutult praktilist kasu. Kuumutamise (pastöriseerimise) abil võideti mikroorganismide põhjustatud õlle- ja veinihaigusi, piimhappetooteid; haavade mädaste tüsistuste vältimiseks võeti kasutusele antiseptikumid; L. Pasteuri põhimõtetele tuginedes on nakkushaiguste vastu võitlemiseks välja töötatud palju vaktsiine.
L. Pasteuri teoste tähendus ulatub aga palju kaugemale ainult nendest praktilistest saavutustest. L. Pasteur viis mikrobioloogia ja immunoloogia põhimõtteliselt uutele positsioonidele, näitas mikroorganismide rolli inimeste elus, majanduses, tööstuses, nakkuspatoloogias ning pani paika põhimõtted, mille järgi mikrobioloogia ja immunoloogia meie ajal arenevad.
L. Pasteur oli lisaks väljapaistev õppejõud ja teaduse organisaator. Pasteuri Instituut Pariisis, mis asutati 1888. aastal riiklike vahenditega, on siiani üks juhtivaid teadusasutusi maailmas. Pole juhus, et inimese immuunpuudulikkuse viiruse (HIV) avastas selle instituudi teadlane L. Montagnier (samal ajal ameeriklase R. Galloga).
Mikrobioloogia arengu füsioloogiline periood on seotud ka saksa teadlase Robert Kochi nimega, kes töötas välja meetodid bakterite puhaskultuuride saamiseks, bakterite värvimiseks mikroskoopia käigus ja mikrofotograafiaks. Tuntud on ka R. Kochi sõnastatud Kochi triaad, mida kasutatakse siiani haiguse tekitaja tuvastamiseks.
L. Pasteuri töö vaktsineerimise alal avas mikrobioloogia arengus uue etapi, mida õigustatult nimetatakse "immunoloogiliseks".
Mikroorganismide nõrgenemise (nõrgestamise) põhimõte vastuvõtliku looma läbimisel või mikroorganismide ebasoodsates tingimustes (temperatuuril, kuivatamisel) hoidmisel võimaldas L. Pasteuril hankida vaktsiine marutaudi, siberi katku ja kanakoolera vastu; seda põhimõtet kasutatakse vaktsiinide valmistamisel siiani. Järelikult on L. Pasteur teadusliku immunoloogia rajaja, kuigi enne teda oli tuntud Inglise arsti E. Jenneri välja töötatud meetod rõugete ennetamiseks lehmarõugetesse nakatades. Seda meetodit ei ole aga laiendatud teiste haiguste ennetamisele.
Pärast L. Pasteuri tööd ilmus palju uuringuid, mis püüdsid selgitada vaktsineerimisjärgse immuunsuse tekke põhjuseid ja mehhanisme. Selles mängisid silmapaistvat rolli I. I. Mechnikovi ja P. Ehrlichi teosed.
Saksa keemik P. Ehrlich esitas humoraalse (ladina huumor - vedel) puutumatuse teooria. Ta uskus, et immuunsus tekib veres mürki neutraliseerivate antikehade moodustumise tulemusena. Seda kinnitas antitoksiinide – toksiine neutraliseerivate antikehade – avastamine loomadel, kellele süstiti difteeria- või teetanusetoksiini (E. Bering, S. Kitazato). I. I. Mechnikovi (1845 - 1916) uuringud näitasid aga, et immuunsuse kujunemisel mängivad suurt rolli spetsiaalsed rakud, makro- ja mikrofaagid. Need rakud neelavad ja seedivad võõrosakesi, sealhulgas baktereid. I. I. Mechnikovi uuringud fagotsütoosi kohta tõestasid veenvalt, et lisaks humoraalsele on ka rakuline immuunsus. L. Pasteuri lähimat abilist ja järgijat I. I. Mechnikovit peetakse väärikalt üheks immunoloogia rajajaks. Tema töö tähistas immunokompetentsete rakkude kui immuunsüsteemi morfoloogilise aluse, selle ühtsuse ja bioloogilise olemuse uurimise algust. Immunoloogilist perioodi iseloomustab immuunsüsteemi peamiste reaktsioonide avastamine geneetiliselt võõrastele ainetele (antigeenidele): antikehade teke ja fagotsütoos/viivitatud tüüpi ülitundlikkus (DTH), vahetu tüüpi ülitundlikkus (IHT), tolerantsus, immunoloogiline mälu. HRT ja HNT on kaks reaktsiooni, mis on allergia (kreeka keelest allos – muu ja ergon – toime) aluseks, st haigused, mida iseloomustavad teatud kliinilised sümptomid, mis on tingitud ebatüüpilisest, väärastunud reaktsioonist antigeenile. Allergilised reaktsioonid võivad tekkida näiteks seerumipreparaatide, antibiootikumide, loomsete ja taimsete valkude, kodutolmu, kohevuse, villa jms suhtes.
1915. aastal jälgis vene arst M. Raisky esmakordselt immunoloogilise mälu nähtusi, s.o. antikehade kiire energeetiline tootmine sama antigeeni korduval manustamisel.
Seejärel seostas F. Vernet seda mälurakkude – T-lümfotsüütide – moodustumisega kehas pärast esmast kokkupuudet antigeeniga. Inglise teadlane P. Medawar ja Tšehhi teadlane M. Hasek avastasid 1953. aastal tolerantsuse, tolerantsuse, antigeeniresistentsuse, s.o. seisund, mille korral immuunsüsteem ei reageeri antigeenile. Tolerantsus omaantigeenide suhtes kujuneb välja embrüonaalsel perioodil ja seda saab kunstlikult luua antigeeni sissetoomisega embrüonaalsel perioodil või vahetult pärast lapse või looma sündi. Immunoloogilise tolerantsuse fenomeni kasutatakse kirurgias elundite ja kudede siirdamise probleemi lahendamiseks.
Samuti tuleb märkida, kui oluline on avastada sel perioodil inimeste ja loomade normaalsete elundite ja kudede antigeenid ning inimeste ja loomade individuaalsed antigeensed erinevused. Nende antigeensete erinevuste üldine tunnus on inimese individuaalsed veretüübid. Koduteadlane L.A. Zilber (1957) avastas pahaloomuliste kasvajate antigeenid, mis oli kasvajavastase immuunsuse uurimise algus.
Mikrobioloogia arengu immunoloogilisel perioodil loodi mitmeid immuunsuse teooriaid: P. Ehrlichi humoraalne teooria, I. I. Mechnikovi fagotsüütiteooria, N. Erne idiotüüpsete interaktsioonide teooria, hüpofüüsi-hüpotalamuse-neerupealiste teooria. P. F. Zdrodovsky immuunsuse reguleerimise teooria jne. Kuid kõige enam Austraalia immunoloogi F. Burneti (1899 - 1986) loodud kloonse valiku teooria jääb paljude immuunsuse nähtuste ja mehhanismide selgitamiseks vastuvõetavaks. Ameerika teadlane S. Tanegawa töötas välja selle teooria geneetilised aspektid.
Mikrobioloogia ja immunoloogia arenesid eriti kiiresti meie sajandi 50-60ndatel aastatel. Sellele aitasid kaasa järgmised põhjused:
· olulisemad avastused molekulaarbioloogia, geneetika, bioorgaanilise keemia vallas;
· uute teaduste, nagu geenitehnoloogia, biotehnoloogia, arvutiteadus, esilekerkimine;
· uute meetodite ja teadusaparatuuri loomine, mis võimaldavad tungida sügavamale eluslooduse saladustesse.
Nii algas 50ndatest alates mikrobioloogia ja immunoloogia arengus molekulaargeneetiline periood, mida iseloomustavad mitmed põhimõtteliselt olulised teadussaavutused ja avastused. Need sisaldavad:
· paljude viiruste ja bakterite molekulaarstruktuuri ja molekulaarbioloogilise korralduse dešifreerimine; kõige lihtsamate eluvormide, "nakkusliku valgu" priooni avastamine;
· mõne antigeeni keemilise struktuuri ja keemilise sünteesi dešifreerimine. Näiteks lüsosüümi keemiline süntees, AIDS-i viiruse peptiidid (R.V. Petrov, V.T. Ivanov jt);
· uute antigeenide, näiteks kasvajaantigeenide (LA Zilber jt), histocompatibility antigeenide (HLA süsteem) avastamine;
· antikehade-immunoglobuliinide struktuuri dešifreerimine;
· meetodi väljatöötamine looma- ja taimerakkude kultiveerimiseks ning tööstuslikuks kasvatamiseks viirusantigeenide saamiseks;
· rekombinantsete bakterite ja rekombinantsete viiruste tootmine. Viiruste ja bakterite üksikute geenide süntees. Bakterite ja viiruste rekombinantsete tüvede saamine, mis ühendavad vanemlike indiviidide omadusi või omandavad uusi omadusi;
· hübridoomide loomine immuunsete B-lümfotsüütide, antikehade tootjate ja vähirakkude liitmise teel monoklonaalsete antikehade tootmiseks
· immunomodulaatorite, immunotsütokiinide (interleukiinid, interferoonid, müelopeptiidid jt), endogeensete looduslike immuunsüsteemi regulaatorite avastamine ja nende kasutamine erinevate haiguste ennetamiseks ja raviks;
· vaktsiinide (B-hepatiidi vaktsiin, malaaria, HIV-antigeenid ja muud antigeenid), bioloogiliselt aktiivsete peptiidide (interferoonid, interleukiinid, kasvufaktorid jne) saamine biotehnoloogiliste meetodite ja geenitehnoloogia meetoditega;
· sünteetiliste vaktsiinide väljatöötamine, mis põhinevad looduslikel või sünteetilistel antigeenidel ja nende fragmentidel, samuti kunstlikul kandjal. adjuvant (assistent). immuunstimulaator;
· kaasasündinud ja omandatud immuunpuudulikkuse uurimine, nende roll immunopatoloogias ja immunokorrektiivne ravi väljatöötamine. Immuunpuudulikkust põhjustavate viiruste avastamine;
· põhimõtteliselt uute meetodite väljatöötamine nakkus- ja mittenakkushaiguste diagnoosimiseks (ensüümimmunoanalüüs, radioimmunoanalüüs, immunoblotanalüüs, nukleiinhapete hübridisatsioon). Nendel meetoditel põhinevate testsüsteemide loomine näidustuseks, mikroorganismide tuvastamiseks, nakkus- ja mittenakkushaiguste (kasvajad, kardiovaskulaarsed, autoimmuunsed, endokriinsed jne) diagnoosimiseks, samuti teatud seisundite (rasedus, vereülekanne) häirete tuvastamiseks , elundisiirdamine jne)
Immuunsuse teooriad. Immuunsuse teooriate väljatöötamine. Immuunsuse fagotsütaarne teooria. I. I. Mechnikov
Patogeensete mikroorganismide rolli tuvastamine nakkushaiguste tekkes ja immuunsuse kunstliku loomise võimalus on ajendanud uurima tegureid, mis kaitsevad organismi nakkusetekitajate eest.
Pasteur pakkus välja ammendatud jõu teooria; Selle teooria kohaselt tähistab “immuunsus” seisundit, milles inimkeha (toitekeskkonnana) ei toeta mikroobide arengut.
Autor sai aga kiiresti aru, et tema teooria ei suuda seletada mitmeid tähelepanekuid. Eelkõige näitas Pasteur, et kui nakatada kana siberi katkuga ja hoida ta jalgu külmas vees, tekib tal haigus (tavalistes tingimustes on kanad siberi katku suhtes immuunsed). Nähtuse areng tõi kaasa kehatemperatuuri languse 1-2 °C võrra ehk mingist toitainekeskkonna ammendumisest organismis ei saanud juttugi olla.
Immuunsuse fagotsütaarne teooria. I. I. Mechnikov
1883. aastal ilmus immuunsuse teooria, mis põhines Charles Darwini evolutsioonilistel õpetustel ja põhineb loomade seedimise uurimisel bioloogilise arengu erinevatel etappidel. Uue teooria autor I. I. Mechnikov avastas ainete intratsellulaarse seedimise sarnasuse amööbides, koelenteraatide endodermirakkudes ja mõnes mesenhümaalse päritoluga rakkudes (vere monotsüüdid, koe makrofaagid). Mechnikov tutvustas kreeka keelest terminit "fagotsüüdid". faagid, söövad, + kytos, rakk ja tegid hiljem ettepaneku jagada need mikrofaagideks ja makrofaagideks. Seda jagunemist soodustasid ka P. Ehrlichi saavutused, kes eristas värvimise teel mitut tüüpi leukotsüüte. Põletiku võrdleva patoloogia klassikalistes töödes tõestas I. I. Mechnikov fagotsüütrakkude rolli patogeenide kõrvaldamisel. 1901. aastal ilmus Pariisis tema monumentaalne lõputöö “Immunity in Infectious Diseases”.
Olulise panuse fagotsüütiteooria levitamisse andsid E. Roux ja I. I. Mechnikovi üliõpilased (A. M. Bezredka, I. G. Savtšenko, L. A. Tarasevitš, F. Ya. Chistovitš, V. I. Isaev).
I. I. Mechnikov (1845–1916)
Väljapaistev vene teadlane. 1882. aastal pidas Mechnikov Venemaa loodusteadlaste ja arstide kongressil oma kuulsa kõne “Keha kaitsemehhanismidest”, milles ta põhjendas sügavalt teaduslikult keha immuunsust nakkushaiguste suhtes. Seda teooriat nimetatakse immuunsuse fagotsüütiliseks teooriaks. Selle teooria kujunemise aluseks oli tema tähelepanekud rakusisese seedimise kohta erinevatel mereloomadel (meduusid, käsnad, molluskid jne). Mechnikov avastas nende loomade kehas spetsiaalsed "rändlevad" rakud, mis kohtuvad, püüavad kinni ja neelavad kõik kehasse sisenevad võõrkehad, sealhulgas mitmesugused mikroobid. Ta nimetas "rändavaid" rakke fagotsüütideks, st sööjarakkudeks.
Mechnikov rõhutas, et fagotsüüdid kaitsevad organismi ja nende tegevuse tulemusena kujuneb välja immuunsus nakkushaiguste vastu. Surematu õpetus keha immuunsusest ja selle bioloogiline immuunsusteooria avasid uue etapi meditsiini arengus. Selle avastuse eest 1908. aastal pälvis I. I. Mechnikov Nobeli preemia.
Charles Niccol nimetas Mechnikovi piltlikult "mikrobioloogia poeediks", kellele omistatakse mikroobse antagonismi doktriini väljatöötamist, millest sai teoreetiline alus antibiootikumide tootmisel, mida kasutatakse mitmete nakkushaiguste raviks. Mechnikovile kuuluvad ka originaalsed uuringud eksperimentaalse süüfilise ja koolera kohta.
Mechnikov uuris vanaduse põhjuseid. Uskudes, et "vanadus on haigus, mida tuleb ravida", tõi ta välja, et see tekib soolestiku mikrofloora esindajate jääkainetest põhjustatud kroonilise kehamürgistuse mõjul. Ta hõlmas selliste toodete hulka indooli, fenooli ja skatooli. Putrefaktiivsete bakterite väljatõrjumiseks pakkus Mechnikov välja dieedi, mis koosneks peamiselt köögiviljadest, puuviljadest ja hapupiimast, mis sisaldavad piimhappebaktereid, mis on putrefaktiivsete bakterite antagonistid.
I. I. Mechnikovi nimi on riiklikult tunnustatud. Nõukogude valitsus asutas kuldmedali ja Mechnikovi preemia, mis antakse parima töö eest bioloogias.
M. M. Terekhovski (1740-1796) teoseid on võimatu märkimata jätta. Alates 1770. aastast töötas Terekhovsky umbes viis aastat välismaal, Strasbourgi ülikoolis, mis oli kuulus oma meditsiinikooli poolest. Siin kaitses Terekhovsky doktoriväitekirja - oma peamist teaduslikku tööd. Doktoritöö kandis pealkirja "Linna ripslaste pimeduseriik". See seadis ülesandeks uurida mikroskoopiliste olendite olemust ja tekkeviise erinevates infusioonides. Suure hulga katsete põhjal jõudis teadlane järeldusele, et "loomad" on elusolendid. Nad surevad kõrgete temperatuuride, mürkide ja elektrivoolu tõttu. Kõige olulisem järeldus oli "loomade" spontaanse genereerimise võimatus, mis oli vastuolus paljude tolleaegsete teadlaste seisukohtadega. Terekhovsky kirjutas, et Harvey (1578-1651) tuntud seisukoht - "iga elusolend pärineb munast" - omandab aksioomi jõu.
Venemaale naastes töötas Terekhovsky meditsiinikoolides. 1782. aastal kinnitati ta Peterburi üldmaahaigla professori ja botaanikaaia (praegu NSV Liidu Teaduste Akadeemia Botaanikainstituut) direktori ametikohale.
1835. aastal avaldas K. Ehrenberg selleks ajaks kogutud faktide põhjal raamatu väga märgilise pealkirjaga: "Ripsilased kui täiuslikud organismid." Ta jagas madalamad olendid 22 klassi. Raamatuga oli kaasas ripslaste atlas, millest paljusid kirjeldati üksikasjalikult ja nimetati kahendnomenklatuuri järgi. Kolm klassi hõlmasid baktereid.
VENEMAA FÖDERATSIOONI HARIDUSMINISTEERIUM
TULA RIIKÜLIKOOL
Sanitaar-, hügieeni- ja ennetusdistsipliinide osakond
CHESTNOVA T.V., SMOLYANINOVA O.L.
MEDITSIINILINE MIKROBIOLOOGIA, VIRUSOLOOGIA
JA IMMUNOLOOGIA
(Õppe- ja praktiline käsiraamat meditsiiniülikoolide üliõpilastele).
TULA – 2008
UDK 576,8
Arvustajad:…………
Meditsiiniline mikrobioloogia, viroloogia ja immunoloogia: õppe- ja praktiline käsiraamat / Toim. M422 T.V. Tšestnovoy, O.L. Smolyaninova, –….., 2008. -….lk.
Õppe- ja praktilise käsiraamatu koostasid Tula osariigi ülikooli sanitaar-hügieeni- ja ennetusteaduste osakonna töötajad vastavalt ametlikult heaks kiidetud mikrobioloogia (bakterioloogia, viroloogia, mükoloogia, protozooloogia) ja immunoloogia õpetamise programmidele meditsiiniülikoolide üliõpilastele. kõik teaduskonnad.
Õppe- ja praktiline käsiraamat kirjeldab bakterioloogia laboratooriumi, toob välja mikroskoopilised uurimismeetodid, toitekeskkonna valmistamise põhitõed ning sisaldab teavet bakterite, seente, algloomade ja viiruste morfoloogia, süstemaatika ja füsioloogia kohta. Samuti on toodud erinevate patogeensete mikroorganismide, viiruste omadused ja nende laboriuuringute meetodid.
ÜLDMIKROBIOLOOGIA
Sissejuhatus…………………………………………………………………………………………………………
Mikrobioloogia arengu lühiajalugu…………………………………………………………
Teema 1. Mikroorganismide morfoloogia ja klassifikatsioon………………………………………..
1.1. Mikrobioloogilised laborid, nende varustus, põhilised ohutusabinõud ja tööreeglid neis…………………………………………………………………………………….
1.2. Mikroorganismide struktuur ja klassifikatsioon……………………………………………………………………
1.3. Bakterite (prokarüootide) struktuur ja klassifikatsioon……………………………………………………………….
1.4. Seente struktuur ja klassifikatsioon………………………………………………………………..
1.5. Algloomade struktuur ja klassifikatsioon……………………………………………………….
1.6. Viiruste struktuur ja klassifikatsioon…………………………………………………………………
Test teemal ……………………………………………………………………………………………..
Teema 2. Mikroskoopia………………………………………………………………………………..
2.1. Mikroskoobid, nende struktuur, mikroskoopia tüübid, mikroorganismide mikroskoopiatehnikad, mikroskoobi käsitsemise reeglid…………………………………………………………….
2.2. Mikroskoopiliste preparaatide valmistamise ja värvimise meetodid………………………..
Test teemal ………………………………………………………………………………………….
Teema 3. Mikroorganismide füsioloogia………………………………………………………………….
3.1. Bakterite kasv ja paljunemine. Paljunemisfaasid …………………………………………………………….
3.2 Toitesöötmed, nende klassifitseerimise põhimõtted, nõuded toitekeskkonnale, mikroorganismide kasvatamise meetodid…………………………………………….
3.3. Bakterite toitumine ……………………………………………………………………………….
3.4. Bakteriraku ainevahetus…………………………………………………………….
3.5. Plastivahetuse tüübid…………………………………………………………………………………………
3.6. Puhaskultuuride eraldamise põhimõtted ja meetodid. Bakteriaalsed ensüümid, nende identifitseerimine. Liigisisene identifitseerimine (epidemioloogiline märgistus)………………………………..
3.7. Seente, algloomade, viiruste ja nende kasvatamise füsioloogia tunnused………………
3.8. Bakteriofaagid, nende struktuur, klassifikatsioon ja kasutusala…………………………………………………………..
Test teemal ……………………………………………………………………………………………
Teema 4. Keskkonnatingimuste mõju mikroorganismidele………………………………………..
4.1. Füüsikaliste, keemiliste ja bioloogiliste tegurite mõju mikroorganismidele………….
4.2. Steriliseerimise, desinfitseerimise, aseptika ja antiseptikumide mõiste. Steriliseerimismeetodid, seadmed. Desinfitseerimise kvaliteedikontroll…………………………………………………………..
Teema 5. Inimkeha normaalne mikrofloora………………………………………………………………….
5.1. Normofloora, selle tähtsus mikroorganismide jaoks. Mööduva floora mõiste, düsbiootilised seisundid, nende hindamine, korrigeerimise meetodid……………………………………………………….
Teema 6. Mikroobide geneetika. ……………………………………………………………………………………………..
6.1. Bakteri genoomi struktuur. Fenotüübiline ja genotüübiline varieeruvus. Mutatsioonid. Muudatused……………………………………………………………………………………..
Mikroorganismide geneetilised rekombinatsioonid. Geenitehnoloogia alused, praktiline rakendamine……………………………………………………………………………………………………………….
Test teemal ……………………………………………………………………………………………..
Teema 7. Antimikroobsed ained……………………………………………………………………………….
7.1. Looduslikud ja sünteetilised antibiootikumid. Antibiootikumide klassifikatsioon keemilise struktuuri, mehhanismi, spektri ja toimetüübi järgi. Saadamise meetodid…………………………….
7.2. Bakterite ravimiresistentsus, selle ületamise viisid. Antibiootikumide suhtes tundlikkuse määramise meetodid…………………………………………………………………………………….
Teema 8. Nakatumise õpetus……………………………………………………………………………………..
8.1. Infektsiooni mõiste. Nakkusvormid ja nakkushaiguste perioodid. Patogeensus ja virulentsus. Patogeensuse tegurid. Bakteriaalsed toksiinid, nende olemus, omadused, tootmine……………………………………………………………………………………………….
8.2. Nakkusprotsessi epidemioloogilise seire kontseptsioon. Reservuaari mõiste, nakkusallikas, levikuteed ja -tegurid…………………………………………………………………
Test teemal ……………………………………………………………………………………………..
ÜLDIMMUNOLOOGIA………………………………………………………………………………………….
Teema 9. Immunoloogia…………………………………………………………………………………
9.1. Immuunsuse mõiste. Immuunsuse tüübid. Mittespetsiifilised kaitsefaktorid…………….
9.2. Immuunsüsteemi kesk- ja perifeersed organid. Immuunsüsteemi rakud. Immuunvastuse vormid …………………………………………………………………………………
9.3. Komplement, selle struktuur, funktsioonid, aktiveerimisviisid. Roll immuunsuses …………………….
9.4. Antigeenid, nende omadused ja liigid. Mikroorganismide antigeenid …………………………………….
9.5. Antikehad ja antikehade moodustumine. Immunoglobuliinide struktuur. Immunoglobuliinide klassid ja nende omadused …………………………………………………………………………………………………………
96. Seroloogilised reaktsioonid ja nende rakendamine……………………………………………………….
9.7. Immuunpuudulikkuse seisundid. Allergilised reaktsioonid. Immunoloogiline mälu. Immunoloogiline tolerantsus. Autoimmuunprotsessid ………………………………………………………………
9.8. Immunoprofülaktika, immunoteraapia………………………………………………………..
ERAMIKROBIOLOOGIA……………………………………………………………………………….
Teema 10. Sooleinfektsioonide patogeenid…………………………………………………………….
10.1. Salmonella………………………………………………………………………………………..
10.2. Shigella………………………………………………………………………………………….
10.3. Escherichia ………………………………………………………………………………………………………….
10.4. Vibrio cholerae……………………………………………………………………………….
10.5. Yersinia………………………………………………………………………………….
Teema 11. Toidu kaudu levivad toksilised infektsioonid. Toidu toksikoosid……………………………………………………………
11.1. PTI üldised omadused ja patogeenid……………………………………………………….
11.2. Botulism ………………………………………………………………………………………….
Teema 12. Mädaste-põletikuliste haiguste patogeenid……………………………………………………………
12.1. Patogeensed kokid (streptokokid, stafülokokid)………………………………………………………………….
12.2. Gramnegatiivsed bakterid (Haemophilus influenzae, Pseudomonas aeruginosa, Klebsiella, Proteus)…
12.3. Haava anaeroobsed klostriidide ja mitteklostriidide infektsioonid………………………
Teema 13. Õhu kaudu levivate bakteriaalsete infektsioonide patogeenid…………………………….
13.1. Korünebakterid……………………………………………………………………………………
13.2. Bordetella………………………………………………………………………………………………………………
13.3. Meningokokk……………………………………………………………………………………
13.4. Mükobakterid ………………………………………………………………………………….
13.5. Legionella……………………………………………………………………………………………..
Teema 14. Sugulisel teel levivate haiguste (STD) patogeenid…………………………
14.1. Klamüüdia ………………………………………………………………………………………….
14.2. Süüfilise põhjustaja …………………………………………………………………………………….
14.3. Gonokokid…………………………………………………………………………………….
Teema 15. Riketsiaalsete haiguste patogeenid…………………………………………………………………………………..
Teema 16. Bakteriaalsete zoonootiliste infektsioonide tekitajad………………………………….
16.1. Francisella………………………………………………………………………………………
16.2. Brucella ………………………………………………………………………………………….
16.3. Siberi katku põhjustaja……………………………………………………………………………………..
16.4. Katku tekitaja …………………………………………………………………………………
16.5. Leptospira ……………………………………………………………………………………….
Teema 17. Patogeensed algloomad…………………………………………………………………………………..
17.1. Plasmodium malaaria ………………………………………………………………………………….
17.2. Toksoplasma……………………………………………………………………………………….
17.3. Leishmania……………………………………………………………………………………….
17.4. Amööbiaasi põhjustaja ……………………………………………………………………….
17.5. Giardia……………………………………………………………………………………………………………
Teema 18. Patogeensete seente põhjustatud haigused…………………………………………………………..
ERAVIRUSOLOOGIA…………………………………………………………………………………………..
Teema 19. Ägedate hingamisteede viirusnakkuste patogeenid…………………………………………………………………………………………
19.1. Gripiviirused ……………………………………………………………………………….
19.2. Paragripp. PC viirused………………………………………………………………………………………………
19.3. Adenoviirused…………………………………………………………………………………………………………
19.4. Rinoviirused ……………………………………………………………………………………….
19.5. Reoviirused …………………………………………………………………………………….
Teema 20. Õhu kaudu levivate viirusnakkuste patogeenid……………………………………..
20.1. Leetrite ja mumpsi viirused…………………………………………………………………………………….
20.2. Herpesviirus ………………………………………………………………………………………
20.3. Punetiste viirus ……………………………………………………………………………………
Teema 21. Poksüviirused……………………………………………………………………………….
21.1. Rõugete tekitaja …………………………………………………………………………………….
Teema 22. Enteroviiruse infektsioonid………………………………………………………………..
22.1. Polioviirus…………………………………………………………………………………
22.2. ECHO viirused. Coxsackie viirused…………………………………………………………………………………
Teema 23. Retroviirused……………………………………………………………………………..
23.1. HIV-nakkuse põhjustaja ……………………………………………………………………………………….
Teema 24. Arboviirusnakkused……………………………………………………………………………………….
24.1. Rabdoviirused…………………………………………………………………………………….
24.2. Flaviviirused…………………………………………………………………………………………………………
24.3. Hantaviirused ……………………………………………………………………………………….
Teema 25. Viirusliku hepatiidi tekitajad……………………………………………………………………………………
25.1. A-hepatiidi viirus ……………………………………………………………………………….
25.2. B-hepatiidi viirus …………………………………………………………………………………….
25.3. C-hepatiidi viirus …………………………………………………………………………………….
ESIMENE OSA. ÜLDMIKROBIOLOOGIA
Sissejuhatus.
Mikrobioloogia on teadus, mis uurib mikroskoopilisi olendeid, mida nimetatakse mikroorganismideks, nende bioloogilisi omadusi, süstemaatikat, ökoloogiat ja suhteid teiste organismidega.
Mikroorganismide hulka kuuluvad bakterid, aktinomütseedid, seened, sealhulgas niitseened, pärmseened, algloomad ja mitterakulised vormid – viirused, faagid.
Mikroorganismidel on looduses äärmiselt oluline roll - nad viivad läbi orgaaniliste ja anorgaaniliste (N, P, S jne) ainete ringlust, mineraliseerivad taimseid ja loomseid jääke. Kuid need võivad põhjustada suurt kahju – kahjustada toorainet, toiduaineid ja orgaanilisi materjale. See võib põhjustada mürgiste ainete moodustumist.
Paljud mikroorganismide tüübid on inimeste, loomade ja taimede haiguste põhjustajad.
Samas kasutatakse mikroorganisme praegu laialdaselt rahvamajanduses: eri tüüpi bakterite ja seente abil saadakse orgaanilisi happeid (äädik-, sidrun- jne), alkohole, ensüüme, antibiootikume, vitamiine, söödapärmi. . Mikrobioloogiliste protsesside alusel tegutsevad küpsetamine, veinivalmistamine, õlle valmistamine, piimatoodete tootmine, puu- ja juurviljade kääritamine, aga ka muud toiduainetööstuse harud.
Praegu on mikrobioloogia jagatud järgmisteks osadeks:
Meditsiiniline mikrobioloogia - uurib inimese haigusi põhjustavaid patogeenseid mikroorganisme ning töötab välja meetodeid nende haiguste diagnoosimiseks, ennetamiseks ja raviks. Uurib nende leviku viise ja mehhanisme ning nende vastu võitlemise meetodeid. Meditsiinilise mikrobioloogia kursusega külgneb eraldi kursus – viroloogia.
Veterinaarmikrobioloogia uurib patogeenseid mikroorganisme, mis põhjustavad loomadel haigusi.
Biotehnoloogia uurib rahvamajanduses ja meditsiinis kasutatavate ühendite ja ravimite saamiseks kasutatavate mikroorganismide omadusi ja arengutingimusi. See arendab ja täiustab teaduslikke meetodeid ensüümide, vitamiinide, aminohapete, antibiootikumide ja teiste bioloogiliselt aktiivsete ainete biosünteesiks. Biotehnoloogia ees seisab ka meetmete väljatöötamine tooraine, toidu ja orgaaniliste materjalide kaitsmiseks mikroorganismide riknemise eest ning nende ladustamisel ja töötlemisel toimuvate protsesside uurimine.
Mullamikrobioloogia uurib mikroorganismide rolli mulla tekkes ja viljakuses ning taimede toitumises.
Veemikrobioloogia uurib veekogude mikrofloorat, selle rolli toiduahelates, ainete ringelus, joogi- ja reovee saastamisel ja puhastamisel.
Mikroorganismide geneetika kui üks nooremaid distsipliine uurib mikroorganismide pärilikkuse ja varieeruvuse molekulaarseid aluseid, mutageneesiprotsesside mustreid, töötab välja meetodeid ja põhimõtteid mikroorganismide elutegevuse kontrollimiseks ning uute tüvede saamiseks kasutamiseks tööstuses, põllumajanduses ja meditsiinis. .
Mikrobioloogia arengu lühilugu.
Mikroorganismide avastamise au kuulub Hollandi loodusteadlasele A. Leeuwenhoekile (1632-1723), kes lõi esimese 300-kordse suurendusega mikroskoobi. Aastal 1695 ta andis välja raamatu "Looduse saladused" kokkide, varraste ja spirilla joonistustega. See äratas loodusteadlastes suurt huvi. Tolleaegne teaduse seis võimaldas kirjeldada ainult uusi liike (morfoloogiline periood).
Füsioloogilise perioodi algust seostatakse suure prantsuse teadlase Louis Pasteuri (1822-1895) tegevusega. Pasteuri nime seostatakse suurimate avastustega mikrobioloogia vallas: ta uuris käärimise olemust, tuvastas hapnikuta elu võimalikkuse (anaerobioos), lükkas tagasi spontaanse tekke teooria ning uuris veinide riknemise põhjuseid ja põhjuseid. õlut. Ta pakkus välja tõhusad viisid toidu riknemise patogeenide vastu võitlemiseks (pastöriseerimine), töötas välja vaktsineerimise põhimõtte ja vaktsiinide saamise meetodid.
Pasteuri kaasaegne R. Koch tutvustas külvi tahkele toitekeskkonnale, mikroorganismide loendamist, puhaste kultuuride eraldamist ja materjalide steriliseerimist.
Immunoloogiline periood mikrobioloogia arengus on seotud vene bioloogi nimega I.I. Mechnikov, kes avastas doktriini keha immuunsusest nakkushaigustele (immuunsus), oli immuunsuse fagotsütaarse teooria rajaja ja avastas mikroobide antagonismi. Samaaegselt I.I. Mechnikov uuris nakkushaiguste suhtes immuunsuse mehhanisme Saksa suurteadlase P. Ehrlichi juures, kes lõi humoraalse immuunsuse teooria.
Gamaleya N.F. – immunoloogia ja viroloogia rajaja, avastas bakteriofagia.
DI. Ivanovski avastas esmakordselt viirused ja temast sai viroloogia rajaja. Töötades Nikitski botaanikaaias tubakaistandustele tohutut kahju põhjustanud tubaka mosaiikhaiguse uurimisel, 1892. aastal. leidis, et selle Krimmis laialt levinud haiguse põhjustab viirus.
N.G. Gabrichevsky korraldas Moskvas esimese bakterioloogiainstituudi. Talle kuuluvad sarlakite, difteeria, katku ja muude nakkuste uurimise tööd. Ta korraldas Moskvas difteeriavastase seerumi tootmise ja kasutas seda edukalt laste raviks.
P.F. Zdrodovsky on immunoloog ja mikrobioloog, kes on tuntud oma põhitöö poolest immuunsuse füsioloogia, samuti riketsioloogia ja brutselloosi alal.
V.M. Ždanov on suur viroloog, üks planeedi rõugete ülemaailmse likvideerimise korraldajatest, kes seisis molekulaarviroloogia ja geenitehnoloogia algallikate eest.
M.P. Tšumakov on immunobiotehnoloog ja viroloog, poliomüeliidi ja viirusliku entsefaliidi instituudi korraldaja, suukaudse poliomüeliidi vaktsiini autor.
Z.V. Ermolyeva - kodumaise antibiootikumravi asutaja
KASAHSTANI VABARIIGI HARIDUS- JA TEADUSMINISTEERIUM
IDA-KASAHSTANI RIIKÜLIKOOLI NIME S.AMANZHOLOVA
bioloogia osakond
ABSTRAKTNE
Distsipliin: "Mikroorganismide ja viiruste bioloogia ja areng"
Teemal: “Mikrobioloogia arengulugu”
Lõpetanud: UBG-09 (A) rühma õpilased
Gruškovskaja D., Fefelova N.
Kontrollis: Kalenova K.Sh.
Ust-Kamenogorsk, 2011
Plaan:
Sissejuhatus……………………………………………………………………………3
1. MIKROORGANISMIDE AVASTAMINE…………………………………………………………… …4
2. KIRJELDEV (MORFOLOOGILINE) PERIOOD MIKROBIOLOOGIA ARENGUS (17. SAJANDI LÕPP – 19. SAJANDI KESKKOND)……………………..5
2.1.Käärimis- ja lagunemisprotsesside olemuse kohta ideede arendamine……5
2.2. Ideede arendamine nakkushaiguste mikroobse olemuse kohta………………………………………………………………………………………….7
3. FÜSIOLOOGILINE PERIOOD (PASTER) (19. SAJANDI TEINE POOL)…………………………………………………………………………………….8
3.1. Louis Pasteuri teaduslik tegevus………………………………………………………8
3.2. Mikrobioloogia areng 19. sajandi teisel poolel………………………10
4. MIKROBIOLOOGIA ARENG 20. SAJANDIL………………………………15
Järeldus.............................................................. ................................................................................ ...... 18
Kirjandus.............................................................. ...................................................... ...................... 19
SISSEJUHATUS
Mikrobioloogia on teadus, mis uurib väikeste ja palja silmaga nähtamatute organismide ehitust, süstemaatikat, füsioloogiat, biokeemiat, geneetikat ja ökoloogiat. Neid organisme nimetatakse mikroorganismideks või mikroobideks.
Inimene elas pikka aega ümbritsetuna nähtamatutest olenditest, kasutas oma elutegevuse saadusi (näiteks haputainast leiva küpsetamisel, veini ja äädika valmistamisel), kannatas, kui need olendid haigusi põhjustasid või toiduvarusid rikkusid, kuid ei kahtlusta nende olemasolu. Ma ei kahtlustanud, sest ma ei näinud, ja ma ei näinud, sest nende mikroolendite suurus jäi palju alla nähtavuse piiri, milleks inimsilm on võimeline. Teadaolevalt suudab normaalse nägemisega inimene optimaalsel kaugusel (25-30 cm) eristada punkti kujul objekti, mille mõõtmed on 0,07-0,08 mm. Inimene ei oska väiksemaid esemeid märgata. Selle määravad tema nägemisorgani struktuurilised omadused.
Tekkinud loodusliku barjääri ületamiseks ja inimsilma võimete avardamiseks tehti katseid juba ammu. Nii leiti Vana-Babüloni arheoloogiliste väljakaevamiste käigus kaksikkumerad läätsed - kõige lihtsamad optilised instrumendid. Objektiivid olid valmistatud poleeritud mäekristallist. Võib arvata, et nende leiutisega astus inimene esimese sammu mikromaailma teel.
Optilise tehnoloogia edasine täiustamine ulatub 16. ja 17. sajandisse. ja on seotud astronoomia arenguga. Sel ajal kujundasid Hollandi klaasiveskid esimesed teleskoobid. Selgus, et kui läätsed on paigutatud teisiti kui teleskoobis, saab suurendada väga väikeseid objekte. Seda tüüpi mikroskoobi lõi 1610. aastal G. Galileo. Mikroskoobi leiutamine avas uusi võimalusi eluslooduse uurimiseks.
Üks esimesi mikroskoope, mis koosnes kahest kaksikkumerast läätsest, mis suurendas ligikaudu 30 korda, kavandas ja kasutas taimede struktuuri uurimiseks inglise füüsik ja leiutaja R. Hooke. Korgilõike uurides avastas ta puitkoe korrapärase rakulise struktuuri. Hiljem nimetas ta neid rakke "rakkudeks" ja neid on kujutatud raamatus "Mikrograafia". R. Hooke võttis kasutusele termini "rakk", et tähistada neid struktuuriüksusi, millest on ehitatud keeruline elusorganism. Edasine tungimine mikromaailma saladustesse on lahutamatult seotud optiliste instrumentide täiustamisega.
1.MIKROORGANISMIDE AVASTAMINE
Mikroorganismid avastati 17. sajandi lõpus, kuid nende tegevust ja isegi praktilisi rakendusi teati palju varem. Näiteks valmistati ja kasutati iidsetel aegadel alkoholi-, piim- ja äädikhappekäärimisprodukte. Nende toodete kasulikkust seletati nendes elava vaimu olemasoluga. Idee nähtamatute olendite olemasolust hakkas aga ilmnema nakkushaiguste põhjuste tuvastamisel. Nii väitsid Hippokrates (6. sajand eKr) ja hiljem Varro (2. sajand), et nakkushaigusi põhjustavad nähtamatud olendid. Kuid alles 16. sajandil jõudis Itaalia teadlane Giralamo Fracastoro järeldusele, et haiguste edasikandumine inimeselt inimesele toimub kõige väiksemate elusolendite abil, kellele ta andis nime contagium vivum. Selliste oletuste kohta polnud aga tõendeid.
Kui eeldada, et mikrobioloogia tekkis hetkel, mil inimene nägi esimesi mikroorganisme, siis saame täiesti täpselt märkida mikrobioloogia “sünnipäeva” ja avastaja nime. See mees on hollandlane Antonie van Leeuwenhoek (1632-1723), Delfti tootja. Linakiu struktuuri vastu huvi tundes lihvis ta endale mitu krobelist läätse. Hiljem hakkas Leeuwenhoek selle õrna ja vaevarikka töö vastu huvi tundma ning saavutas suurepärase täiuslikkuse läätsede valmistamisel, mida ta nimetas "mikroskoopiaks". Välisel kujul olid need üksikud kaksikkumerad hõbedast või messingist raamitud klaasid, kuid oma optiliste omaduste poolest ei olnud Leeuwenhoeki läätsedel, mis võimaldasid suurenduseks 200–270 korda, võrdset. Nende hindamiseks piisab, kui meenutada, et kaksikkumera läätse suurenduse teoreetiline piir on 250–300 korda.
Loomuliku hariduseta, kuid loomupärase uudishimuga Leeuwenhoek vaatas huviga kõike, mis käepärast oli: tiigivett, hambakattu, pipraleotist, sülge, verd ja palju muud. Alates 1673. aastast hakkas Leeuwenhoek saatma oma vaatluste tulemusi Londoni Kuninglikule Seltsile, mille liikmeks ta seejärel valiti. Kokku kirjutas Leeuwenhoek Londoni Kuninglikule Seltsile üle 170 kirja ja pärandas sellele hiljem 26 oma kuulsast "mikroskoopiast". Siin on katkend ühest kirjast: „24. aprillil 1676 vaatasin vett mikroskoobi all ja nägin selles suure üllatusega tohutul hulgal tillukesi elusolendeid. Mõned neist olid laiusest 3-4 korda pikemad, kuigi ei olnud paksemad kui täi keha katvad karvad. Teised olid korrapärase ovaalse kujuga. Oli ka kolmandat tüüpi organisme – kõige arvukamaid – pisikesi sabaga olendeid. Võrreldes selles lõigus antud kirjeldust ja Leeuwenhoeki käsutuses olevate läätsede optilisi võimeid, võime järeldada, et Leeuwenhoek nägi 1676. aastal esimesena baktereid.
Leeuwenhoek avastas kõikjal mikroorganisme ja jõudis järeldusele, et teda ümbritsev maailm oli tihedalt asustatud mikroskoopiliste elanikega. Leeuwenhoek pidas kõiki nähtud mikroorganisme, sealhulgas baktereid, väikesteks loomadeks, keda ta nimetas "loomadeks", ja oli veendunud, et need on üles ehitatud samamoodi nagu suured organismid, st neil on seedeorganid, jalad, sabad jne. ..d.
Leeuwenhoeki avastused olid nii ootamatud ja isegi fantastilised, et põhjustasid peaaegu 50 järgneva aasta jooksul üldist hämmastust. 1698. aastal Hollandis viibides külastas Peeter I Leeuwenhoeki ja vestles temaga. Sellelt reisilt tõi Peeter I mikroskoobi Venemaale ja hiljem, 1716. aastal, valmistati tema õukonna töökodades esimesed kodumaised mikroskoobid.
2. KIRJELDEV (MORFOLOOGILINE) PERIOOD MIKROBIOLOOGIA ARENGUS (17. SAJANDI LÕPP – 19. SAJANDI KESKUS)
2.1. Ideede arendamine käärimis- ja lagunemisprotsesside olemuse kohta
Paljud mikroorganismide poolt läbiviidavad protsessid on inimestele teada juba ammusest ajast. Esiteks on see mädanemine ja käärimine. Vana-Kreeka ja Rooma autorite kirjutistest võib leida retsepte veini, hapupiima ja leiva valmistamiseks, mis viitavad kääritamise laialdasele kasutamisele igapäevaelus. Keskajal ei jätnud alkeemikud neid protsesse tähelepanuta ja uurisid neid koos teiste puhtkeemiliste transformatsioonidega. Just sel perioodil püüti välja selgitada käärimisprotsesside olemus.
Terminit "käärimine" ("fermentatio") gaasi eraldumisega seotud protsesside tähistamiseks kasutas esmakordselt Hollandi alkeemik J.B. van Helmont (1577-1644). J. van Helmont avastas sarnasusi viinamarjamahla kääritamisel tekkiva gaasi (süsinikdioksiid), söe põletamisel eralduva gaasi ja gaasi vahel, mis ilmneb “lubjakividele äädika valamisel”, s.t. kui leelis reageerib happega. Selle põhjal jõudis J. van Helmont järeldusele, et kõik ülalkirjeldatud keemilised muundumised on sama laadi. Hiljem hakati fermentatsioone eristama gaaside eraldumisega kaasnenud keemiliste protsesside rühmast. Käärimise materiaalse liikumapaneva jõu tähistamiseks kasutati selle toimeainet terminit "ensüüm". Vaatluse käärimisest ja mädanemisest kui puhtalt keemilistest protsessidest sõnastas 1697. aastal saksa arst ja keemik G.E. Stalem (1660-1734). Käärimine ja mädanemine on G. Stahli ideede järgi keemilised transformatsioonid, mis toimuvad “ensüüm” molekulide mõjul, mis annavad neile omase sisemise aktiivse liikumise edasi kääritava substraadi molekulidele, s.o. toimib omamoodi reaktsiooni katalüsaatorina. G. Stahli seisukohti lagunemis- ja käärimisprotsesside olemuse kohta jagas ja kaitses täielikult oma aja üks suurimaid keemikuid J. Liebig. Seda seisukohta aga ei aktsepteerinud kõik teadlased.
Üks esimesi oletusi Leeuwenhoeki kirjeldatud “gloobulite” (pärmi) seose kohta käärimis- ja mädanemisnähtustega kuulub prantsuse loodusteadlasele J.L.L. Buffon (1707-1788). Prantsuse keemik A. Lavoisier (1743-1794), kes uuris kvantitatiivselt suhkru keemilisi muundumisi alkohoolse kääritamise käigus, jõudis väga lähedale pärmi rolli mõistmisele käärimisprotsessis. 1793. aastal kirjutas ta: „Käärimisele esimese tõuke andmiseks piisab vähesest õllepärmist: siis jätkub see iseenesest. Ensüümi toimimise kohta üldiselt annan aru mujal." See tal aga ei õnnestunud: A. Lavoisier'st sai Prantsuse kodanliku revolutsiooni terrori ohver.
19. sajandi 30. aastatest algas intensiivsete mikroskoopiliste vaatluste periood. 1827. aastal kirjeldas prantsuse keemik J. Demasier (1783-1862) pärmi Mycoderma cerevisiae struktuuri, mis moodustab õlle pinnale kile, ning olles veendunud, et tegemist on kõige väiksemate loomadega, liigitas nad ripslasteks. Samas pole J. Demasieri töödes viidet võimalikule seosele käärimisprotsessi ja käärimisvedeliku pinnale tekkiva kile vahel. Kümme aastat hiljem võttis prantsuse botaanik C. Cagnard de Latour (1777-1859) ette alkohoolsel käärimisel tekkinud sette põhjaliku mikroskoopilise uurimise ja jõudis järeldusele, et see koosneb elusolenditest, kelle elutegevus on käärimise põhjuseks. Peaaegu samal ajal juhtis saksa loodusteadlane F. Kützing (1807-1893) alkoholist äädika teket uurides tähelepanu limamassile, mis nägi välja nagu kile alkoholi sisaldava vedeliku pinnal. Limasmassi uurides leidis F. Kützing, et see koosneb mikroskoopilistest elusorganismidest ja on otseselt seotud äädika akumuleerumisega keskkonda. Samasugustele järeldustele jõudis ka teine saksa loodusteadlane T. Schwann (1810-1882).
Nii jõudsid C. Cagniard de Latour, F. Kützing ja T. Schwann üksteisest sõltumatult ja peaaegu samaaegselt järeldusele käärimisprotsesside ja mikroskoopiliste elusolendite elutegevuse vahelise seose kohta. Peamise järelduse nendest uuringutest sõnastas selgelt F. Kützing: „Peame nüüd käsitlema iga käärimisprotsessi erinevalt, kui keemia on neid seni käsitlenud. Kogu alkohoolse kääritamise protsess sõltub pärmi olemasolust, äädikhappekäärimine aga äädikhappe ema olemasolust.
Siiski ei aktsepteeritud kolme teadlase esitatud ideid fermentatsiooni "ensüümi" bioloogilise olemuse kohta. Veelgi enam, kääritamise füüsikalis-keemilise olemuse teooria järgijad kritiseerisid neid tõsiselt, süüdistades oma teaduslikke vastaseid "järelduste kergemeelsuses" ja tõendite puudumises, mis toetaksid seda "veidrat hüpoteesi". Domineerivaks jäi käärimisprotsesside füüsikalis-keemilise olemuse teooria.
2.2.Ideede arendamine nakkushaiguste mikroobse olemuse kohta
Isegi Vana-Kreeka arst Hippokrates (umbes 460–377 eKr) oletas, et nakkushaigusi põhjustavad nähtamatud elusolendid. Avicenna (umbes 980-1037) kirjutas "Meditsiini kaanonis" katku, rõugete ja teiste haiguste "nähtamatutest" patogeenidest. Sarnaseid mõtteid võib leida ka itaalia arsti, astronoomi ja poeedi G. Fracastro (1478-1553) töödest.
Vene epidemioloog D. S. oli sügavalt veendunud, et nakkushaigusi põhjustavad elusad mikroskoopilised olendid. Samoilovitš (1744-1805), kes püüdis mikroskoobi all tuvastada katku tekitajat. Ta kukkus läbi mikroskoopide ja mikroskoopilise tehnoloogia ebatäiuslikkuse tõttu. D.S. Samoilovitši poolt tema idee kohaselt välja töötatud patsientide desinfitseerimise ja isoleerimise meetmed osutusid aga epideemiate vastases võitluses väga tõhusaks ja said laialdaselt tuntuks kogu maailmas.
Väärib mainimist, et D. Samoilovitši kaasaegne M. Terekhovsky (1740-1796), esimene vene protoloog-eksperimentaator, tegi kindlaks algloomade eluslooduse ja rakendas 1775. aastal esmakordselt maailmas eksperimentaalset mikroorganismide uurimismeetodit. , määrates kindlaks temperatuuri, elektrilahenduste, sublimaadi, oopiumi, hapete ja leeliste mõju nende elujõulisusele. Uurides mikroorganismide liikumist, kasvu ja paljunemist rangelt kontrollitud tingimustes, juhtis Terekhovsky esimesena tähelepanu sellele, et jagunemisele eelneb kasv ja suuruse suurenemine. Ta tõestas ka algloomade spontaanse tekke võimatust erinevates keedetud vedelikes (infusioonides). Ta kirjeldas oma tähelepanekuid oma töös "On Linnaeus' Pouring Chaos".
Itaalia loodusteadlane A. Bassi (1773-1856) avastas 1827. aastal siidiusside haigust uurides haiguse edasikandumise, kui mikroskoopiline seen kandub haigelt isendilt tervele. Seega oli A. Bassi esimene, kes katseliselt tõestas selle haiguse mikroobset olemust. Nakkushaiguste mikroobse olemuse idee pole pikka aega tunnustust leidnud. Domineeriv teooria oli, et haiguste põhjusteks peeti erinevaid häireid keemiliste protsesside kulgemises organismis.
1846. aastal määratles saksa anatoom F. Henle (1809-1885) oma raamatus “Ratsionaalse patoloogia käsiraamat” selgelt nakkushaiguste äratundmise aluspõhimõtted. Hiljem F. Henle üldises vormis sõnastatud ideed (F. Henle ise ei suutnud näha ainsatki inimese nakkushaiguste tekitajat) põhjendas R. Koch eksperimentaalselt ja sisenes teadusesse nimetuse „Henle-Koch“ all. kolmik”.
3. FÜSIOLOOGILINE PERIOOD (PASTER) (19. SAJANDI TEINE POOL)
3.1. Louis Pasteuri teaduslik tegevus
Füsioloogilise perioodi algus ulatub 19. sajandi 60. aastatesse ja on seotud väljapaistva prantsuse teadlase, elukutselt keemiku Louis Pasteuri (1822-1895) tegevusega. Mikrobioloogia võlgneb Pasteurile mitte ainult kiire arengu, vaid ka teaduse kujunemise. Pasteuri nime seostatakse suurimate avastustega, mis tõid talle maailmakuulsuse: käärimine (1857), spontaanne genereerimine (1860), veini- ja õllehaigused (1865), siidiusside haigused (1868), nakkus ja vaktsiinid (1881), marutaudi (1885) .
Pasteur alustas oma teaduslikku karjääri kristallograafiaga. Ta avastas, et optiliselt inaktiivse ratseemilise happe soolade ümberkristallimisel moodustuvad kahte tüüpi kristallid. Ühte tüüpi kristallidest valmistatud lahus pöörab polariseeritud valguse tasandit paremale ja teist tüüpi kristallidest vasakule. Lisaks avastas Pasteur, et ratseemilise viinhappe lahuses kasvatatud hallitus tarbib ainult ühte isomeerset vormi (paremale pöörav). See tähelepanek võimaldas Pasteuril teha järelduse mikroorganismide spetsiifilise mõju kohta substraatidele ja oli teoreetiliseks aluseks mikroorganismide füsioloogia edasisel uurimisel. Pasteuri tähelepanekud madalamate hallitusseente kohta äratasid tema tähelepanu mikroorganismidele üldiselt.
1854. aastal sai Pasteur täiskohaga professori koha Lille'i ülikoolis. Siin alustas ta mikrobioloogilisi uuringuid, mis pani aluse mikrobioloogiale kui iseseisvale teadusharule.
Käärimisprotsesside uurimisega alustamise põhjuseks oli Lille'i tootja pöördumine Pasteuri poole palvega aidata välja selgitada peedimahla alkoholi tootmiseks kääritamise süstemaatilise ebaõnnestumise põhjused. 1857. aasta lõpus avaldatud uurimistulemused tõestasid kahtlemata, et alkohoolse käärimise protsess on teatud mikroorganismide rühma – pärmseene – elutegevuse tulemus ja toimub tingimustes, kus õhku ei pääse.
Peaaegu samaaegselt alkohoolse kääritamise uurimisega alustas Pasteur piimhappekäärimise uurimist ja näitas ka, et seda tüüpi käärimist põhjustavad mikroorganismid, mida ta nimetas piimhappepärmiks. Pasteur tutvustas oma uurimistöö tulemusi avaldatud töödes “Memuaarid piimhappekäärimisest”.
Tõepoolest, Pasteuri uurimistöö tulemused ei ole lihtsalt uued teaduslikud andmed, need on tollal domineerinud kääritamise füüsikalise ja keemilise olemuse teooria julge ümberlükkamine, mida toetasid ja kaitsesid tolle aja suurimad teaduslikud autoriteedid: I. Berzelius, E. Mitscherlich, J. Liebig. Piimhappekääritamine on kõige lihtsam "keemiline" protsess suhkrumolekuli lagunemiseks kaheks trioosiks ja tõestus, et see lagunemine on seotud mikroskoopiliste organismide elutähtsa aktiivsusega, oli võimas argument, mis toetab käärimiste bioloogilise olemuse teooriat.
Teiseks argumendiks kääritamise bioloogilise olemuse toetuseks oli Pasteuri eksperimentaalne tõestus alkohoolse kääritamise võimalikkusest valguvabas keskkonnas. Kääritamise keemilise teooria kohaselt on viimane “ensüümi”, mis on valgulise iseloomuga aine, katalüütilise aktiivsuse tulemus.
Võihappe fermentatsiooni uurimine viis Pasteuri järeldusele, et mõnede mikroorganismide elu ei saa jätkuda mitte ainult vaba hapniku puudumisel, vaid viimane on neile kahjulik. Nende vaatluste tulemused avaldati 1861. aastal aruandes pealkirjaga "Loomad-ripsloomad, kes elavad ilma vaba hapnikuta ja põhjustavad käärimist". Vaba hapniku negatiivse mõju avastamine võihappe käärimisprotsessile oli võib-olla viimane punkt, mis kummutas täielikult käärimiste keemilise olemuse teooria, kuna just hapnikule määrati selle ühendi roll, mis andis selle. esimene tõuge "ensüümi" valguosakeste sisemisele liikumisele. Pasteur tõestas mitme kääritamise valdkonna uuringute kaudu veenvalt käärimiste keemilise teooria vastuolulisust, sundides oma vastaseid oma vigu tunnistama. 1861. aastal anaerobioosiga seotud töö eest sai Pasteur Prantsuse Teaduste Akadeemia auhinna ja Londoni Kuningliku Seltsi medali. Kahekümneaastase kääritamise alase uurimistöö tulemuse võttis Pasteur kokku raamatus „Õlle, selle haiguste, nende põhjuste, stabiilseks muutmise viiside uurimine uue kääritamise teooria rakendamisega” (1876).
1865. aastal pöördus Prantsuse valitsus Pasteuri poole palvega aidata siidiussikasvatajaid, kes kannatasid siidiussihaiguste tõttu suuri kaotusi. Pasteur pühendas selle probleemi uurimisele umbes viis aastat ja jõudis järeldusele, et siidiussihaigusi põhjustavad teatud mikroorganismid. Pasteur uuris üksikasjalikult haiguse kulgu - pebrine siidiussid ja töötas välja praktilised soovitused haigusega võitlemiseks: ta tegi ettepaneku otsida mikroskoobi all haiguse tekitajaid liblikate ja nukkude kehas, eraldada haiged isendid ja hävitada jne. .
Olles kindlaks teinud siidiusside nakkushaiguste mikroobse olemuse, jõudis Pasteur mõttele, et ka loomade ja inimeste haigusi põhjustavad mikroorganismide mõju. Tema esimene töö selles suunas oli tõestada, et kirjeldatud perioodil laialt levinud lapsevoodipalaviku põhjustas teatud mikroskoopiline patogeen. Pasteur tuvastas palaviku põhjustaja, näitas, et selle põhjuseks oli meditsiinitöötajate antiseptiliste reeglite eiramine, ja töötas välja kaitsemeetodid patogeeni kehasse tungimise eest.
Pasteuri edasine töö nakkushaiguste uurimisel viis tema avastamiseni kana koolera, osteomüeliidi, mädaste abstsesside ja ühe gaasigangreeni põhjustajatest. Nii näitas ja tõestas Pasteur, et iga haigust põhjustab konkreetne mikroorganism.
1879. aastal töötas Pasteur kanakoolerat uurides välja meetodi mikroobide kultuuride saamiseks, mis kaotavad võime olla haiguse põhjustajateks, st kaotavad virulentsuse, ja kasutas seda avastust keha kaitsmiseks järgneva nakatumise eest. Viimane pani aluse puutumatuse teooria loomisele.
Pasteur ühendas oma nakkushaiguste uurimise meetmete väljatöötamisega nende aktiivseks võitluseks. Tuginedes virulentsete mikroorganismide nõrgestatud kultuuride saamise tehnikale, mida nimetatakse "vaktsiinideks", leidis Pasteur viise siberi katku ja marutaudi vastu võitlemiseks. Pasteuri vaktsiinid said laialt levinud kogu maailmas. Asutused, kus marutaudi vastu vaktsineeritakse, nimetatakse Pasteuri auks Pasteuri jaamadeks.
Pasteuri töid hindasid tema kaasaegsed ja need pälvisid rahvusvahelise tunnustuse. 1888. aastal ehitati Pariisis Pasteuri jaoks teaduslik uurimisinstituut, kasutades rahalisi vahendeid, mis koguti rahvusvahelise abonemendi kaudu, mis praegu kannab tema nime. Pasteur oli selle instituudi esimene direktor. L. Pasteuri avastused näitasid, kui mitmekesine, ebatavaline ja aktiivne on silmale nähtamatu mikromaailm ning millist tohutut tegevusvaldkonda selle uurimine esindab.
3.2. Mikrobioloogia areng 19. sajandi teisel poolel
Hinnates 19. sajandi teisel poolel mikrobioloogiaga saavutatud kordaminekuid, kirjutas prantsuse teadlane P. Tennery oma teoses “Loodusteaduse arengu ajalooline visand Euroopas”: “Bakterioloogiliste avastuste ees on ajaloos muude loodusteadused 19. sajandi viimastel kümnenditel tunduvad mõnevõrra kahvatumad.
Mikrobioloogia edusammud sel perioodil on otseselt seotud uute ideede ja metodoloogiliste lähenemistega, mida L. Pasteur mikrobioloogiauuringutesse tutvustas. Esimeste seas, kes mõistis Pasteuri avastuste olulisust, oli inglise kirurg J. Lister, kes mõistis, et suure osa operatsioonijärgsetest surmajuhtumitest on põhjuseks esiteks teadmatusest tingitud haavade nakatumine bakteritega ja teiseks reeglite eiramine. põhiliste antiseptiliste reeglitega .
Üks meditsiinilise mikrobioloogia rajajaid oli koos Pasteuriga saksa mikrobioloog R. Koch (1843-1910), kes uuris nakkushaiguste patogeene. Koch alustas oma uurimistööd veel maaarstina siberi katku uurimisega ja 1877. aastal avaldas ta teose, mis oli pühendatud selle haiguse tekitajale - Bacillus anthracisele. Pärast seda tõmbas Kochi tähelepanu teisele tolle aja tõsisele ja laialt levinud haigusele – tuberkuloosile. 1882. aastal teatas Koch tuberkuloosi tekitaja avastamisest, mis tema auks nimetati "Kochi batsilliks". (1905. aastal pälvis Koch tuberkuloosialaste uuringute eest Nobeli preemia.) Ka avastas Koch 1883. aastal koolera tekitaja.
Koch pööras suurt tähelepanu mikrobioloogiliste uurimismeetodite arendamisele. Ta kavandas valgustusseadme, pakkus välja meetodi bakterite mikrofotograafiaks, töötas välja tehnikad bakterite värvimiseks aniliinvärvidega ja pakkus välja meetodi mikroorganismide kasvatamiseks tahkel toitainekeskkonnas, kasutades želatiini. Bakterite saamine puhaskultuuride kujul avas uusi lähenemisviise nende omaduste põhjalikumaks uurimiseks ja andis tõuke mikrobioloogia edasiseks kiireks arenguks. Eraldati koolera, tuberkuloosi, difteeria, katku, malleuse ja lobaarse kopsupõletiku tekitajate puhaskultuurid.
Koch põhjendas eksperimentaalselt F. Henle poolt varem välja pakutud sätteid nakkushaiguste tunnustamise kohta, mis jõudsid teadusesse nime all “Henle-Kochi triad” (hiljem aga selgus, et see ei kehti kõikide nakkustekitajate kohta).
Vene mikrobioloogia rajaja on L. Tsenkovski (1822-1887). Tema uurimisobjektid olid mikroskoopilised algloomad, vetikad ja seened. Ta avastas ja kirjeldas suure hulga algloomi, uuris nende morfoloogiat ja arengutsükleid. See võimaldas tal järeldada, et taimede ja loomade maailma vahel pole teravat piiri. Ta korraldas ka ühe esimese Pasteuri jaama Venemaal ja pakkus välja vaktsiini siberi katku vastu ("Tsenkovsky elusvaktsiin").
I. Mechnikovi (1845-1916) nimi on seotud mikrobioloogia uue suuna – immunoloogia – väljatöötamisega. Esimest korda teaduses töötas Mechnikov välja ja kinnitas eksperimentaalselt immuunsuse bioloogilise teooria, mis läks ajalukku Mechnikovi fagotsüütiteooriana. See teooria põhineb keha rakuliste kaitseseadmete ideel. Mechnikov tõestas loomkatsetes (dafnia, meritähe vastsed), et leukotsüütidel ja teistel mesodermaalse päritoluga rakkudel on võime püüda kinni ja seedida kehasse sisenevaid võõrosakesi (sh mikroobid). See nähtus, mida nimetatakse fagotsütoosiks, moodustas immuunsuse fagotsüütilise teooria aluse ja on saanud üldise tunnustuse. Arendades tõstatatud küsimusi, sõnastas Mechnikov üldise põletiku kui keha kaitsva reaktsiooni teooria ja lõi immunoloogias uue suuna - antigeeni spetsiifilisuse doktriini. Praegu muutub see üha olulisemaks seoses elundite ja kudede siirdamise probleemi arenemisega ning vähi immunoloogia uurimisega.
Mechnikovi olulisemad tööd meditsiinilise mikrobioloogia vallas hõlmavad koolera patogeneesi ja kooleralaadsete vibrioonide, süüfilise, tuberkuloosi ja retsidiveeruva palaviku bioloogia uuringuid. Mechnikov on mikroobse antagonismi doktriini rajaja, mis oli aluseks antibiootikumravi teaduse arengule. Mikroobse antagonismi ideed kasutas Mechnikov pikaealisuse probleemi väljatöötamisel. Uurides keha vananemise nähtust, jõudis Mechnikov järeldusele. Et selle kõige olulisem põhjus on keha krooniline mürgistus mädanevate bakterite poolt jämesooles toodetud lagunemissaadustega.
Praktilist huvi pakuvad Mechnikovi varajased tööd seene Isaria destructor kasutamisest põldkahjuri – viljamardika – tõrjumiseks. Need annavad põhjust pidada Mechnikovit põllumajandustaimede kahjurite tõrje bioloogilise meetodi rajajaks – meetod, mis leiab tänapäeval üha enam rakendust ja populaarsust.
Seega I.I. Mechnikov, silmapaistev vene bioloog, kes ühendas endas eksperimenteerija, õpetaja ja teaduslike teadmiste propageerija omadused, oli suure vaimu ja tööga mees, kelle kõrgeimaks autasuks oli Nobeli preemia määramine 1909. aastal fagotsütoosi uurimise eest.
Mikrobioloogia valdkonna üks suurimaid teadlasi on I. Mechnikovi sõber ja kolleeg N.F. Gamaleya (1859-1949). Gamaleya pühendas kogu oma elu nakkushaiguste uurimisele ja nende patogeenide vastu võitlemise meetmete väljatöötamisele. Gamaleya andis suure panuse tuberkuloosi, koolera ja marutaudi uurimisse, 1886. aastal korraldas ta koos I. Mechnikoviga Odessas esimese Pasteuri jaama ja juurutas marutaudivastase vaktsineerimise praktikasse. Ta avastas lindude vibrio – lindude kooleralaadse haiguse põhjustaja – ja nimetas selle Ilja Iljitši auks Mechnikovi vibrioks. Seejärel saadi inimese koolera vastane vaktsiin.
jne.................