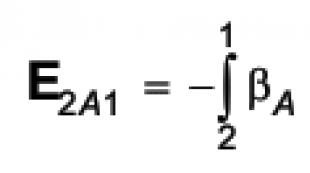Урвалын температурт Kno3 задрал. Хайлуулах өөр хувилбар. II. Урам зориг өгөх мөч
Давуу тал
Ялангуяа энэ төрлийн түлш хоргүй учраас их дуртай. Энэ нь хүнсний бүтээгдэхүүн, бордооноос бүрдэнэ. Ингэснээр би үүнийг зохицуулах эсвэл хашаандаа хэсэг хэсгээрээ алдах талаар санаа зовох шаардлагагүй болно. KNO3 нь хиамны үйлдвэрлэл, анагаах ухаанд махыг хадгалах бодис болгон ашигладаг. Залуу насандаа би KNO3-ийг эмийн сангаас авч байсан, хаана юу авахыг лонхонд бичсэн байсан бэ? шээс хөөх эм болгон усанд уусгасан халбага. Би үүнийг хиам үйлдвэрлэхэд ашигладаг махны дэлгүүрээс олсон. Мөн миний шүдний оонд мэдрэмтгий байдлыг арилгах үйлчилгээтэй KNO3 орсон болохыг анзаарсан. Тиймээс дунд зэргийн өртөлтөөс санаа зовох шаардлагагүй бөгөөд бага хэмжээний KNO3-ийг залгих нь ихэнх хүмүүст шууд хор хөнөөл учруулахгүй. Петрийн тусгай шингэн бордооны уутыг хараад калийн нитрат жагсаалтын эхнийх нь байгааг анзаарав. Ургамал үүнд дуртай.
KNO3-ийн анхааруулга:
- Нитрат/нитритийг хоол хүнсэнд хэрэглэх нь хорт хавдар үүсгэдэг гэсэн нотолгоо байдаг бөгөөд KNO3 хэрэглэх боломжтой ч хэрэглэхийг зөвлөдөггүй.
- Залгихад калийн нитрат нь калийн нитрит болж хувирдаг бөгөөд энэ нь хүүхдэд хортой бөгөөд ялангуяа аюултай! Тэдний гар хүрэхээс хол байлга!
- Зарим хүмүүс KNO3-д өртсөний дараа арьсны үрэвсэл үүсдэг. Хэрэв та үүнд өртөмтгий бол бээлий хэрэглээрэй.
- Их хэмжээний KNO3 тоосоор амьсгалах нь уушгины гэмтэл үүсгэдэг. Хэрэв та KNO3 тоосонд өртсөн бол тохирох амьсгалын аппарат өмс.
Ркандигийн бусад сайн зүйлс:
- Агаарын чийгээс тусгаарлагдсан тохиолдолд тогтвортой, нурж унахгүй
- Шинэчлэх боломжтой, халааж, бараг ямар ч хэлбэрт оруулах, эсвэл гараар дарж хэлбэрт оруулах боломжтой
- Маш сайн шахалтын бат бэх, сайн суналтын бат бэх.
- Цагаан утааны өтгөн үүл үүсгэдэг бөгөөд үүнийг мөшгөгч болгон ашиглаж болно.
- Шатаах хурдыг хоол хийх температураас гадна нэмэлт бодис оруулах замаар хянах боломжтой.
- Цохилт, үрэлтийн улмаас гал асаахад харьцангуй мэдрэмтгий биш, өрөмдөж, зүсэж, гал асаахгүйгээр цохиж болно.*
Алдаа дутагдал
- Шатахуун нь гигроскоптой, агаараас чийг шингээдэг нь надад таалагдахгүй байна. Энэ нь агаараас битүүмжлэгдсэн байх ёстой, эс тэгвээс богино хугацаанд ашиггүй болно, ялангуяа Флоридад 90% чийгшил бага гэж тооцогддог. Мөн энэ нь аюулгүй байдлын хүчин зүйл юм, учир нь алдагдсан жижиг түлш удаан хугацаанд шатамхай биш байх болно. Удалгүй тэд шингэн болж, газарт шингэж, ургамал идэх болно.
- Энэ түлш нь зарим талаараа хэврэг байдаг тул боловсруулах эсвэл шатаах явцад эвдэрч, хуваагдахгүй байхын тулд хөдөлгүүрт байрлуулсан байх ёстой. Савласан даам нь томорвол хагарч, бие биенээ мөргөчих вий гэсэн болгоомжлол үүсдэг. Хэт хурдатгалын улмаас зүсэх хүч нь блокуудыг сүйтгэж, хэсгүүд нь цорго бөглөрөх вий гэсэн болгоомжлол байсан. Хөдөлгүүрийн консерватив загвар нь эдгээр хязгаарлалтыг нөхөж болох боловч шалгагч геометрийн сонголтыг хязгаарлаж болно.
- Энэ түлш нь бусад түлш, ялангуяа нийлмэл түлшээс бага ISP (тодорхой импульс) байдаг.
- Энэ нь хөдөлгүүрт шатаах үед маш бага харагдахуйц дөл үүсгэдэг. Энэ нь илүү гоо зүйн асуудал юм - олон хүмүүс гялалзсан цагаан эсвэл өнгөт галыг харах дуртай байдаг бөгөөд энэ нь дагалдах хэрэгсэлтэй төстэй юм. Би харагдахуйц дөл эсвэл оч үүсгэдэг нэмэлтийг хараахан олж чадаагүй байна. Деннис Уэлч хэлэхдээ титан нь сайхан сүүл үүсгэдэг гэж мэдээлсэн ч би өөрөө үүнийг шалгах хэрэгтэй болно.
- Энэ түлшийг хийхэд ихэвчлэн гал тогооны өрөөнд байрладаг зуухыг ашиглах шаардлагатай байдаг. Анхаар! Энэ нь таны орон сууцанд аюул учруулж байна.
 |
Би энэ түлшийг гэрийн гал тогоонд хийхийг зөвлөдөггүйг анхаарна уу. Хэзээ нэгэн цагт сайн баримтжуулсан аюулгүй байдлын хөтөлбөр нь гал тогооны өрөөнд дунд зэргийн хэмжээтэй хоол хийх боломжийг олгоно гэж найдаж байна. Санамсаргүй эрсдэл нь гал тогооны өрөөнд цехээс илүү их биш байж болох ч үр дагавар нь илүү их сүйрэлд хүргэх магадлалтай. Ихэнх зуухнууд нь гал тогооны өрөөнд байрладаг тул амархан хөдөлгөж чадахгүй тул энэ нь олон хүнд хэцүү асуудлыг шийдэх болно. Би энэ асуудлыг шийдэх арга замыг хайж, санал хүсэлтийг хүлээж авах болно. Би одоогоор гэрийн гадаа ашиглах зориулалттай хатаах тавиур, термостат удирдлагатай хийн сараалжыг ашиглах боломжтой эсэхийг судалж байна. Эдгээр шийдлүүдийн аль нь ч хараахан туршиж үзээгүй байна. Миний арын тавцан дээрх шиг зөөврийн хийн зуухыг зөөврийн пропан саванд холбохыг илүүд үздэг. |
Зарим сайн мэдээ: Би саяхан шарсан талхны зууханд тохирох хэмжээтэй пирекс жигнэх аяга ашиглан хагас багц RCandy хийсэн. Хэрэв та цехийнхээ зууханд бэлэн биш байгаа бол энэ нь эхлэхэд тохиромжтой газар байж магадгүй юм.
Жор
Энэ баримт бичигт байгаа гэрэл зургууд нь өнгөц зураг бөгөөд том зургуудыг үзэхийн тулд дээр нь дарна уу.
Энэ хуудас руу буцахын тулд Буцах товчийг дарна уу.
Найрлага:
Тоног төхөөрөмжид дараахь зүйлс орно.
- 2 Pyrex 9 инчийн жигнэх таваг
- 2 чулуун хавтан эсвэл шилэн хавтан, бүрээс болгон ашигладаг
- Жижиг таваг - Би зэвэрдэггүй эсвэл пааландсан ганг илүүд үздэг ч бусдыг нь ашиглахгүй байх шалтгаан байхгүй.
- 100 гр ба түүнээс дээш жинтэй хөшүүрэг эсвэл бусад жингийн хэмжээ нь граммаар тодорхойлогддог.
- Ширээний хутга, халбага (заавал биш)
- Хэмжих халбага эсвэл аяга
- Урьдчилан халаасан зууханд Фаренгейтийн 300 градус (150 градус)
- Данхны бариул эсвэл бусад
- 35 мм-ийн хальстай сав эсвэл бусад жижиг савнууд нь агаар нэвтрэхгүй байх ба гал авалцахад хагардаггүй. Би энэ түлшний аяндаа шаталтыг хэзээ ч мэдэрч байгаагүй, гэхдээ хэн мэдэх вэ?
Мөн гал унтраагч шаардлагатай. Хэрэггүй бол сайн, гэхдээ ямар ч тохиолдолд авсан нь дээр.
KNO3
Би ихэвчлэн Firefox, Skylighter зэрэг салют нийлүүлэгчдээс худалдаж авсан калийн нитратыг ашигладаг. Тэд хоёулаа сайн. Тэд KNO3-ийг брэнд, нунтаглалтаас хамааран фунт тутамд 2,50-4,00 доллараар зардаг. Өндөр чанартай нунтаг нь илүү үнэтэй байдаг. Энэ процессыг хамгийн бүдүүн брэнд хийх болно, учир нь хужирыг уусгахад маш жижиг ширхэгтэй нунтагладаг.
Зөгийн бал нь эрдэнэ шишийн сиропыг орлуулж сайн ажилладаг боловч эцсийн түлшийг илүү гигроскоп болгодог тул би үүнийг зөвлөхгүй. Би саяхан эрдэнэ шишийн амттай сироп болох Honey Girl сироп хэрэглэсэн бөгөөд энэ нь бас сайн болсон. Maple сироп ажиллахгүй байсан - энэ нь түлшийг сайн шатаадаг боловч үүсэхгүй.




Савыг гал дээр тавьдаг. Энэ бол дунд зэргийн аюултай цэг юм. Фото зураг нь хайруулын тавган доор халаалтын дөл байгааг тодорхой харуулж байна. Хоёр өөр хавтанг тэмдэглэнэ үү. Хоёулаа ажилладаг. Заримдаа би маш сайн ажилладаг нүхтэй хавтанг ашигладаг. Үүнийг гал дээр хийж болно гэдэгт би итгэлтэй байна. KNO3 болон элсэн чихэр уусч байвал савыг яаж халаах нь хамаагүй. Холимог буцалгах, хатаахыг зөвшөөрөхгүй байх нь чухал юм!
Эцэст нь бүх зүйл ууссан, хольц нь тодорхой болно. Таван минут урт мэт санагдаж болох ч та зогсолтгүй үзэх хэрэгтэй!
Ойролцоогоор хагас нь хэв бүрт ордог. Би сав бүрт яг хагасыг нь хийх ёстой бололтой, гэхдээ бага зэргийн ялгаа нь тийм ч том асуудал биш юм. Би үүнийг хурдан хийх дуртай бөгөөд ингэснээр хурдан үүссэн царцдас нь миний хэрэглэж буй саванд үлдэхгүй бөгөөд ингэснээр хольцыг тэнцвэргүй болгодог.


 | 10 минутын дотор хэлбэржүүлнэ. Бөмбөлөгүүд үүсч эхэлдэг. |
 | 25 минутын дотор хэлбэржүүлнэ. Сайн үүссэн бөмбөлгүүд. Мөөгөнцөр бүрийн дунд бага зэрэг шингэн үлдсэн хэвээр байна. |
 | 35 минутын дотор хэлбэржүүлнэ. Шингэн байхгүй, харин хальс, бөмбөлөгүүд бүгд хөхөвтөр цагаан өнгөтэй. |
 | 40 минут ба түүнээс дээш хугацаанд хэлбэрждэг. Хольцын өнгө нь аажмаар хөхөвтөр цагаанаас зааны ясан хүртэл өөрчлөгддөг. Үүнийг зураг дээр харуулаагүй болно. Дахин хэлэхэд, алсын хэлбэрийн алтан өнгө нь хуурмаг зүйл гэдгийг анхаарна уу; хоёр хольц нь ижил өнгөтэй, ойрын хэлбэрийн өнгөтэй илүү төстэй байдаг. |
Хоол хийж дуустал хольцыг БҮҮ ХОТНО гэдгийг анхаарна уу. Бөмбөлгийг хагалах нь усны ууршилтыг удаашруулж, үйл явцыг удаашруулна. Тиймээс хэврэг байдлын туршилт хийхээс өмнө энэ хольцыг бүү хутга.



45 дахь минутанд хэвийг зуухнаас гаргаж аваад жижиг дээж авна.
Үүнийг вандуйны хэмжээтэй бөмбөг болгон өнхрүүлж, хүйтэн, хуурай гадаргуу дээр тэгшлээд 20 секунд орчим хөргөнө. Дээжийг хөргөх үед хэвийг зууханд буцааж өгнө.




Хөргөсөн дээжийг хоёр хэсэгт нугалав. Хэрэв дээж эвдрэлгүйгээр нугалж байвал хольц нь нойтон хэвээр байгаа тул илүү удаан хоол хийх шаардлагатай болно. Гурван минут тутамд эсвэл нугалсан дээж тасрах хүртэл дээж авна.
(Саяхан би хольц дахь чийгийн үлдэгдэл бага хэмжээгээр сайн бүтэцтэй болохыг олж мэдсэн. Хэрэв хөргөсөн дээж нь хэцүү нугалж байвал энэ нь сайн хэрэг байж болох юм. Энэ нь үүссэн түлшний хэврэг байдлыг бууруулж болох боловч Энэ хараахан тогтоогдоогүй байна.)



Энэ тохиолдолд би зуухнаас тогоонуудыг цаг тухайд нь гаргаж авсан. Хөргөсөн дээжийг цэвэрхэн эвдэж, жигд бүтэцтэй байна. Үнэндээ энэ нь бага зэрэг мөхлөгтэй, бараг хуурай байсан. Дахиад таван минутын дараа хольцыг хадгалах хэрэгтэй болно.*
*Хэмнэхийн тулд хайруулын тавган дээр 1 цайны халбага ус хийж, хайруулын тавган дээр таглаад 15 минутын турш зууханд хийнэ. Хүссэн бүтцэд хүрэх хүртэл туршилтыг үргэлжлүүлэн бэлтгэж, давтан хийнэ.
Холимог гулзайлтын туршилтыг давсны дараа бэлэн болсон тул нэн даруй боловсруулах шаардлагатай. Хусах цаг. Энэ бол бүх хамгаалалтын хэрэгслийг өмсөх ёстой аюулын цэг юм. Би хэзээ ч гал гаргаж байгаагүй, гэхдээ хэрвээ ширхэгүүд асвал бүх чиглэлд нисч, маш их хохирол учруулна гэж би бооцоо тавьсан.



Мөөгөнцөр тус бүрийн хайрсыг хусаж, нэг саванд нэгтгэнэ.



Би хатуу халбагаар хайрсыг нягтруулж эхлэх хүртэл дарж, хутгаж, хуванцар болгодог. Тэд эхлээд хоорондоо зууралдахыг эсэргүүцэж магадгүй юм. Тууштай бай. Хэрэв та хольцыг хэт хуурай болгоогүй бол энэ нь эцэстээ тохиолдох болно.
Өөр нэг шинэ заль мэх: хайрсыг асгаж, модон эсвэл хуванцар алхаар цохино. Энэ нь тэднийг зүгээр л хутгах, шахахаас илүү бага хүчин чармайлтаар нягтруулахад хүргэнэ.

Нэг эсвэл хоёр минут хөргөсний дараа түлш халуун хэвээр байгаа боловч бага зэрэг боловсруулах шаардлагатай. Би мэдрэлийн эсүүдтэйгээ сайн харилцаатай байхын тулд үүнийг нэг гараас нөгөө гарт дамжуулдаг.

Энд би жижиг дээжийг тасалж, саваа болгон өнхрүүлэв. Самбар нь даавуугаар хучигдсан байдаг гэдгийг анхаарна уу. Гөлгөр өнгөлгөө нь энэ түлшний гадаргууг маш сайн болгодог.

Та үүнийг шавар шиг сайхан саваа болгон өнхрүүлж болно. Энэ нь яг өнхрүүлснээр хатуурч, зориулалтын хэлбэрээ хадгална.




Шатахууныг илүү нягт бутлах замаар би хавтангаар бүрхэж чадна. Энэ нь надад илүү удаан дулаан, зөөлөн байлгах боломжийг олгодог. Зуухны температурыг 200 F (93 C) хүртэл бууруулна. Ийм температурт түлш нь удаан хугацаанд задрахгүйгээр зөөлөн байж чаддаг.
Түлшийг гараар бутлах өөр хувилбар: Хүнсний процессор ашигла! Энэ нь гадаа эсвэл маш аюулгүй байршилд байрлаж болно. Би комбайныг салгасан өргөтгөлийн утсанд залгаад дараа нь уртасгагч утсыг цахилгаан сүлжээнд найдвартай холбоно. Би хэзээ ч санамсаргүй гал гарч байгаагүй, гэхдээ үргэлж боломж байдаг.










1 минутын дараа түлш нь бөмбөг болно. Хэрэв сэтгэл хангалуун байвал машинаа унтраагаад түлшээ гаргаж авдаг. Ерөнхийдөө би үүнийг хөргөж, нягт битүүмжилсэн саванд хийж жижиг бөмбөлөг болгон өнхрүүлдэг.
Би шаталтын хурдыг шалгахын тулд саваа хийх хэсгүүдийг үргэлж хадгалдаг.





Нэг хэсэг түлшийг гараар 1/4 инчийн диаметртэй саваа болгон өнхрүүлдэг. 1 инч урттай хэсгийг хайчилж, нэг үзүүрийг нь галд хийнэ. Энэ хэлбэрийг түлшний саваа гэж нэрлэдэг. Гал асаахын тулд пропан бамбар ашиглах шаардлагагүй, энэ нь зүгээр л тогтвортой галын сайн эх үүсвэр бөгөөд нэг гараа утсыг, нөгөө гараараа секунд хэмжигчийг барихад чөлөөтэй үлдээдэг.
Шатахуун асахад би секунд хэмжигчээ асааж, шатах үед зогсооно. Түлш нь нэг захаас нөгөө зах хүртэл шатдаг тул энэ утга нь түлшний агаар дахь шаталтын хурд болно. Энэ дээж нь 11 секундын дотор нэг инч шатсан бөгөөд энэ нь түлшний хөнгөн тэсрэлтэд дундаж үзүүлэлт юм. Зарим дээж 8 эсвэл 9 секундэд нэг инч шатдаг. Энэ нь пуужингийн хөдөлгүүр шиг даралтын дор илүү хурдан шатах болно.

Саваа хөргөсөн тул би үүнийг хэсэг болгон хувааж, хальсан хайрцагт хийнэ. Агааргүй саванд түлшийг олон жилийн турш хадгалах боломжтой. Би эдгээр инчийн савааг эргүүлэг болон микро пуужинд ашигладаг.
Сав бүрийг тодорхой тэмдэглэж, аюулгүй газар байрлуул.
Магадгүй энэ түлшний хамгийн гайхамшигтай шинж чанар нь түүнийг дахин халааж, ямар ч хэлбэрт оруулах боломжтой байдаг. Үүнийг 200 F (93 C) зууханд хийж, халах хүртэл шаваас шиг болж, гараар шавар шиг хэлбэржүүлж, ямар ч хэлбэрт оруулж болно. Хөнгөн гар даралт нь матриц (мөөгөнцөр) хэлбэрийг өгч чадна.

Жишээлбэл, би хөдөлгүүрт түлшний бөмбөг хийнэ. Энэ нь ердөө 1/8" нүхтэй 5/8" диаметртэй цилиндр хэлбэртэй блок бөгөөд 10 грамм жинтэй. Энэ нь FFFG үр тарианы хэмжээтэй хар арилжааны нунтагтай хамт хэрэглэгддэг. 
Ойролцоогоор 10 грамм буюу түүнээс бага жинтэй хэсгийг хайчилж ав. 
Хөдөлгүүрийн орон сууцны хэмжээтэй диаметр бүхий цилиндрт өнхрүүл. Энэ тохиолдолд хоолой нь 5/8 инч диаметртэй байв.

Нэг тун хар нунтгийг өнхрөх тавцан дээр тавиад, үр тариа наалдахын тулд түлшээ өнхрүүлээрэй. Хэрэв тэдгээр нь наалдахгүй бол түлшийг дахин зөөлрүүлэх хүртэл хэдэн минутын турш 200 F (93 C) температурт зууханд хийнэ.

Түлшний цэнэгийн дундуур нүх гарга. Гал асаагчдаа хангалттай том болго. Энд би хулсан шорлог, шиш kebab эсвэл tempura-д хэрэглэдэг ижил шорлог хэрэглэдэг. Би эдгээр савааг олон зүйлд ашигладаг:

Одоо би 5/8 инчийн диаметртэй хоолойд блок оруулахыг оролдож байна. Энэ хэсэг хэтэрхий том байна.

Тиймээс би дахин эргэлддэг. Шатахуун нь бага зэрэг хатуурсан тул илүү нарийвчлалтай өнхрүүлж болно.

Энд харуулаагүй, гэхдээ би энэ таблетыг жинлэхэд 12 граммаас илүү жинтэй байсан. Энэ нь бүрхүүлийг урах нь дамжиггүй тул би хурц хутгаар нэг хэсгийг таслав. Үүний дараа жин нь 10.2 грамм байв. Хангалттай ойрхон.


Одоо бүх зүйл сайн байна, зүгээр л 5/8 инчийн хоолойд хийнэ үү.


Би энэ шалгагчийг шууд ашиглахгүй тул би үүнийг хальсан хайрцагт хийнэ. Энэ татаж авах бусад зүйлсийн хамт. Зүгээр л бөөн бөөн түлш хийж, саванд дулаацуулж, сайтар хаа. Савыг хөргөх хүртэл хажуу талд нь тавь. Хэрэв энэ нь хийгдээгүй бол түлш нь ёроол руу урсаж, хатуурах бөгөөд та үүнийг арилгахад маш их цаг зарцуулах болно.
Жимми Эвшээ
5/26/01
Илчлэлт 6/5/03
Инкубус орчуулав
ОРЧУУЛАГЧИЙН ТАЙЛБАР
1. ЭНЭ ТЕХНОЛОГИЙГ ЗОХИОГЧИЙН ЗӨВШӨӨРӨЛТЭЙ ОРЧУУЛЖ ХЭВЛЭГДЭЖ БАЙНА.
2. БҮХЭН БУЮУ ХЭСЭГЧИЛЭЭР ДАХИН ХЭВЛЭХЭД ЭХ ЭХ ЭХ СУУРЬ (WWW.JAMESYAWN.COM) ХОЛБООС ЗААВАЛ БАЙНА.
3. ОРЧУУЛГА ГОЛ ҮГИЙН ҮГЭЭР БУС МЭДРЭМЖТЭЙ. ТЕХНОЛОГИ, АЮУЛГҮЙ БАЙДАЛТАНД ОНЦГОЙ АНХААРЛАСАН.
Галт уулын термит (төмрийн исэл Fe 3 O 4 ба хөнгөн цагааны хольцын шаталт)
(№ 4 2009)
1898 онд Германы металлургийн инженер Ханс Голдшмидт бууруулагч бодис болгон хөнгөн цагааныг ашиглан металыг исэлээс нь хайлуулах аргыг зохион бүтээжээ. Энэ зорилгоор хөнгөн цагаан ба металл ислийн нунтаг хольцыг ашигласан бөгөөд үүнийг эрдэмтэн термит гэж нэрлэсэн (Грек хэлнээс "terme" - дулаан, дулаан).
Fe 3 O 4 ба хөнгөн цагааны термитийн хувьд ойролцоогоор 2400 ° C температур үүсдэг бөгөөд энэ урвал өөрөө 1000 ° C хүрэхэд эхэлдэг. Термит ашиглан металл үйлдвэрлэх аргыг алюминотерми гэж нэрлэдэг бөгөөд металлын исэл ба хөнгөн цагааны нунтаг холимгийг Голдшмидт термит гэж нэрлэдэг. Алюминотерми бол 1856 онд нээгдсэн металлотермийн онцгой тохиолдол юм. Н.Н. Бекетов.
Өнөөдөр олон төрлийн термитийн найрлагыг мэддэг. Зөвхөн хөнгөн цагаан төдийгүй магни, кальци, ферросиликон, бор, борид, цахиур, титан гэх мэт бодисууд нь ангижруулагчийн үүрэг гүйцэтгэдэг.Исэлдүүлэгчийн хувьд фторууд эсвэл бага идэвхжилтэй металлын хлоридууд, тэр ч байтугай тефлон (фторопластик-4) хүртэл ашиглагддаг. агентууд. Термитийг зөвхөн металл олж авахад төдийгүй гагнуурын ажилд ашигладаг бөгөөд цэргийн галын хольц болгон ашигладаг.
Одоо бид галт уулын тогооноос лаавын дэлбэрэлттэй төстэй Fe 3 O 4 + Al термитийн шаталтын урвалыг явуулна. Туршилтын хувьд бүрэн хатсан голын элсийг эхлээд зууханд эсвэл зүгээр л зууханд 200 ° C-т хатааж бэлтгэдэг. Үүний зэрэгцээ жижиг керамик савыг хатаана. Өргөн төмөр савыг (сав, хайруулын таваг гэх мэт) хуурай элсээр дүүргэж, дээрээс нь шавар цэцгийн савыг tripod цагирагт бэхэлж, доод нүхийг шүүлтүүрийн цаасаар бүрхсэн байна. Төмрийн исэл Fe 3 O 4, хөнгөн цагааны хатаасан нунтаг нь жингийн 3: 1 харьцаатай холилдоно. Энэ хольцоос 200 г-аас ихгүй хэмжээтэй морин шоргоолж (50 г Al, ойролцоогоор 150 г Fe 3 O 4) авч, эзэлхүүний 3/4 хүртэл саванд хийнэ. Термит хольц бэлтгэх Та хөнгөн цагааны нунтаг оронд хөнгөн цагаан нунтаг хэрэглэж болохгүй.. Хөнгөн цагааны нунтаг нь исэлдсэн хөнгөн цагааныг агуулдаг бөгөөд энэ нь урвал эхлэхэд ихээхэн саад болдог. Гэхдээ гол асуудал бол хөнгөн цагаан нунтаг нь маш их агаар агуулдаг бөгөөд энэ нь маш халуун хольцыг хүчтэй цацахад хүргэдэг.
Саванд асгасан термит хольцонд голд нь хонхорхой хийж, дотор нь гал хамгаалагч байрлуулна - нарийн ширхэгтэй зүлгүүрээр нунтагласан магнийн соронзон хальс. Урт хэлтэрхий ашиглан тэд магнийн туузыг асааж, 2-3 м зайд хурдан холддог.Гал хамгаалагч шатсаны дараа хүчирхийллийн урвал эхэлдэг. Савны дээгүүр дөл, утаа гарч, хольцын халуун хэсгүүд түүнээс нисч, урвалын үр дүнд үүссэн хайлсан төмрийн урсгал доод нүхнээс урсдаг.
8Al + 3Fe 3 O 4 = 6Fe + 4Al 2 O 3
Хөнгөн цагаан нь төмрөөс илүү реактив металл тул төмрийн ислээс хүчилтөрөгчийг авч, хөнгөн цагааны исэл болж хувирдаг. Хайлсан төмрийг хөргөхөд үүссэн ирмэгийг элснээс зайлуулж, шаар - хөнгөн цагаан исэлээс цэвэрлэнэ.
Элс яагаад бүрэн хуурай байх ёстой нь одоо тодорхой болж байна. Нойтон элснээс ус ууршиж, хайлсан төмрийн дусал цацаж эхэлнэ. Энэ тохиолдолд туршлага нь маш аюултай болно.
Хэрэв та туршилтыг гадаа хийвэл элсэнд булсан төмөр лааз нь нэг удаагийн урвалын сав болж ажиллах болно.
Fe (II) ба Fe (III) давсыг тэнцүү хэмжээгээр агуулсан уусмал дээр аммиакийн илүүдэл уусмалын үйлчлэлээр Fe 3 O 4 гаргаж авч болно. Тунадас үүсч, шүүж, усаар угааж, хатааж, ойролцоогоор 200 хэмд шохойжуулна.
__________________________________________________
Калийн нитрат нь калийн нитрат, калийн нитрат, калийн нитрат гэж нэрлэгддэг KNO 3 томъёогоор илэрхийлэгддэг органик бус хоёртын нэгдэл юм. KNO 3 нэгдэл нь өнгөгүй талст нунтаг, дэгддэггүй, үнэргүй, гигроскоп шинж чанартай. Уг бодис нь усанд маш сайн уусдаг. Амьтанд хоргүй. Байгалийн хувьд KNO 3 бодис нь нитрокалит эрдэс хэлбэрээр олддог бөгөөд хамгийн том орд нь Зүүн Энэтхэг, Чилид байдаг. Энэ нь ургамал, амьтны организмд бага хэмжээгээр агуулагддаг.
Химийн шинж чанар, калийн нитрат авах арга
Калийн нитрат KNO 3 нь 400°С-ийн температурт задарч калийн нитрит KNO 2 ба хүчилтөрөгч O 2 үүснэ. Энэ бодис нь хүчтэй исэлдүүлэгчийн үүрэг гүйцэтгэдэг бөгөөд шатамхай материал, бууруулагч бодисуудтай урвалд ордог. KNO 3 бодисыг ялгарах үед устөрөгчөөр багасгадаг.
Лабораторийн нөхцөлд KNO 3-ыг калийн Ca(NO 3) 2 ба кальцийн нитрат K 2 CO 3-ийн урвалаар олж авдаг бөгөөд энэ бодисыг үйлдвэрлэх хамгийн эртний арга юм. Одоогийн байдлаар калийн сульфат K 2 SO 4 нь калийн оронд ашиглагддаг. Калийн нитратын уусмалыг ижил урвалаар олж авна. Калийн нитрат KNO 3 үйлдвэрлэх орчин үеийн аргуудын дотроос калийн хлорид KCl ба натрийн нитрат NaNO 3-ийн урвал нь илүү хүртээмжтэй, хямд байдаг.
Калийн нитратын хэрэглээний талбарууд
Калийн нитрат KNO 3, түүнчлэн калийн нитратын уусмалыг бордоо болгон ашигладаг (ургамлын өсөлтөд шаардлагатай бүрэлдэхүүн хэсэг болох калигаар баялаг азотын бордооны нэг). Уг бодисыг цахилгаан вакуум үйлдвэрлэл, металлурги, оптик шил хайлуулах, дарь үйлдвэрлэх зэрэгт ашигладаг.
Калийн нитратын тэжээллэг чанар
Калийн нитратыг хүнсний үйлдвэрлэлд хадгалалтын бодис гэж ангилдаг E252 хүнсний нэмэлт болгон өргөн ашигладаг.
Хадгалах бодисууд нь бүтээгдэхүүн дэх бичил биетний өсөлтийг дарангуйлдаг химийн бодис, хүнсний нэмэлт E200 - E299 бөгөөд бүтээгдэхүүний тааламжгүй үнэр, амт, хөгц мөөгөнцөр үүсэх, бичил биетний гаралтай хорт бодис үүсэхээс сэргийлдэг. .
Калийн нитратыг дараахь үйлдвэрлэлд ашигладаг.
- бяслаг (хатуу, хагас хатуу, зөөлөн);
- сүүнд суурилсан бяслагны аналог;
- хиам, махан бүтээгдэхүүн (давсалсан, чанасан, тамхи татдаг), лаазалсан мах;
- загасны бүтээгдэхүүн (herring, давсалсан, marinated sprat);
- галууны элэгний бүтээгдэхүүн.
 Хүнсний нэмэлт нь мөн өнгө засах үйлчилгээтэй. Бүтээгдэхүүний дур булаам төрхийг удаан хугацаанд хадгалахын тулд уг бодисыг хүнсний бүтээгдэхүүнд нэмдэг. Бактерийн эсрэг сул нөлөөтэй.
Хүнсний нэмэлт нь мөн өнгө засах үйлчилгээтэй. Бүтээгдэхүүний дур булаам төрхийг удаан хугацаанд хадгалахын тулд уг бодисыг хүнсний бүтээгдэхүүнд нэмдэг. Бактерийн эсрэг сул нөлөөтэй.
Калийн нитратын биед үзүүлэх нөлөө
Калийн нитрат нь хорт хавдар үүсгэдэг - гадны хүчин зүйлийн нөлөөн дор хорт хавдар үүсгэдэг. Гэсэн хэдий ч санал болгож буй тунгаар E252 нь насанд хүрсэн хүний биед хортой нөлөө үзүүлэхгүй. Нитратуудын сөрөг нөлөөллийг хүний биед нитрит (калийн нитратыг нитрит болгон хяналтгүй хувиргах нь хүнсний бүтээгдэхүүнд тохиолддог) болон хорт хавдар үүсгэдэг нитрозаминууд болгон хувиргадагтай холбон тайлбарладаг. Хүнсний нэмэлтүүд, ялангуяа E252-тай хамт бие махбодид орж буй нитратын хэмжээ нь ундны ус, хүнсний ногоо (хэт бордооны үр дүнд) эдгээр бодисын агууламжтай харьцуулахад маш бага байдаг.
Бие махбодид E252-ийг бага тунгаар удаан хугацаагаар хэрэглэх нь дараахь шинж тэмдэг, өвчний хөгжилд хүргэдэг.
- Хэвлийн хүчтэй өвдөлт
- Сул тал
- Толгой эргэх
- Сэтгэцийн эмгэг
- Орон зайн чиг баримжааны эмгэг
- хэм алдагдал
- Бөөрний үрэвсэл
- Цус багадалт
хууль эрх зүйн мэдээлэл
Калийн нитратыг хүнсний нэмэлт болгон ОХУ, Украин, Европын Холбооны орнуудад хүнсний үйлдвэрлэлд ашиглахыг зөвшөөрсөн.
Буцаад урагшаа
Анхаар! Слайдыг урьдчилан үзэх нь зөвхөн мэдээллийн зорилгоор хийгдсэн бөгөөд үзүүлэнгийн бүх шинж чанарыг илэрхийлэхгүй байж болно. Хэрэв та энэ ажлыг сонирхож байвал бүрэн эхээр нь татаж авна уу.
Суралцах амжилт нь хүүхдийн сурах хүсэл эрмэлзлээс хамаарна. Химийн хичээлийг судлах сэдлийг нэмэгдүүлэхийн тулд би оюутнуудыг танин мэдэхүйн идэвхтэй үйл явцад оролцуулах боломжийг олгодог сургалтын янз бүрийн технологийг ашигладаг.
Хичээлийн зорилго:
- Химийн урвал, тэдгээрийн шинж тэмдэг, үүсэх нөхцлийн талаархи оюутнуудын мэдлэгийг нэгтгэх, өргөжүүлэх;
- задралын урвалыг танилцуулж, химийн урвалын тэгшитгэл зохиох чадварыг хөгжүүлж эхлэх;
- Оюутнуудын коэффициент тогтоох чадварыг үргэлжлүүлэн дадлагажуулах;
- Химийн урвалын тэгшитгэлийг ашиглан оюутнуудын асуудлыг шийдвэрлэх чадварыг үргэлжлүүлэн хөгжүүлэх;
- Ажиглах, харьцуулах чадварыг үргэлжлүүлэн хөгжүүлэх;
- Химийн соёл, анги, бүлэгт ажиллахдаа бусдыг сонсох чадварыг бий болгох.
Тоног төхөөрөмж:
- Үзүүлэн туршилт хийхэд: тигель хавчуур, хэлтэрхий, спиртийн чийдэн, талст KNO 3, нүүрс, HNO 3 (конц.), H 2 O 2, MnO 2., хөлтэй лабораторийн тавиур;
- Компьютер, проектор, "Задаргааны урвал" танилцуулга.
Хичээлийн үеэр
I. Зохион байгуулалтын мөч.
II. Урам зориг өгөх мөч.
Бидний эргэн тойрон дахь ертөнцийн хамгийн сонирхолтой зүйл бол энэ нь маш нарийн төвөгтэй бөгөөд үүнээс гадна байнга өөрчлөгдөж байдаг. Секунд тутамд тоо томшгүй олон тооны химийн урвал явагддаг бөгөөд үүний үр дүнд зарим бодис бусад бодис болж хувирдаг. Тэр хүн амьсгалж, бие махбодид органик бодисын исэлдэлтийн урвал эхэлсэн. Тэр амьсгалаа гаргаж, нүүрстөрөгчийн давхар исэл агаарт орж, дараа нь ургамал шингээж, нүүрс ус болж хувирав. Бид зарим урвалыг шууд ажиглаж болно, жишээлбэл, төмрийн объектын зэврэлт, цусны бүлэгнэл, автомашины түлшний шаталт. Гэсэн хэдий ч химийн үйл явцын дийлэнх нь үл үзэгдэх боловч хүрээлэн буй ертөнцийн шинж чанарыг тодорхойлдог. Бодисын өөрчлөлтийг хянахын тулд ийм урвалын мөн чанарыг сайтар ойлгох шаардлагатай. Бодисын шинж чанарыг судалж үзсэн бидний даалгавар бол олж авсан мэдлэгээ хүн төрөлхтний тусын тулд ашиглаж сурах явдал юм.
III. Мэдлэгийг шинэчлэх.
- Химийн урвалын талаар бид юу мэддэг вэ? (Слайд 2)
- Химийн урвал явагдахад ямар нөхцөл шаардлагатай вэ? (Слайд 3)
- Химийн урвалын шинж тэмдэг юу вэ? (Слайд 4)
- Химийн урвалын жишээг өг.
Дүгнэлт:Олон тооны химийн урвалууд байдаг. Тэд байнга гоожиж байдаг. Энэ олон төрлийн химийн урвалд төөрөлдөхгүйн тулд юу хийх хэрэгтэй вэ?
Химийн урвалыг ангилж сурах.
Задрах урвалын тухай ойлголтын танилцуулга.
1. “Усны электролиз” мультимедиа үзэх(химийн талаархи видео бичлэгийн дижитал мэдээллийн сан). Хавсралт 2
Дараа нь харилцан ярианы үеэр дараах зүйлийг тэмдэглэ.
ус → устөрөгч + хүчилтөрөгч
2H 2 O 2H 2 + O 2
2. Үзүүлэн үзүүлэх туршилт.
a) Калийн нитратын задрал. KNO 3-ийг туршилтын хоолойд хийж, туршилтын хоолойг тавиур дээр бэхлээд халаадаг - давс хурдан хайлж, өтгөн шингэн болж хувирдаг. Хайлмал руу халуун нүүрс шидэхэд туршилтын хоолой дахь нүүрс улам халуун болж, хүчилтөрөгчтэй харилцан үйлчилж үсэрч эхэлнэ.
2KNO 3 2KNO 2 + O 2 (Слайд 5)
b) Зэс (II) гидроксидын задрал. Туршилтын хоолойг Cu(OH) 2-ийн шинэхэн тунадасаар халаавал зэс (II) исэл үүссэний улмаас хар өнгөтэй болно.
Cu(OH) 2 CuO + H 2 O (Слайд 6)
в) Катализатор ашиглан устөрөгчийн хэт ислийг задлах (MnO 2, түүхий лууван, төмс).
H 2 O 2 2H 2 O + O 2 (Слайд 7)
d) Мөнгөн усны (II) оксидын задрал. Ж.Престлигийн туршлага
2HgO 2Hg + O2 (Слайд 8)
Хэлэлцсэн асуудлууд:
- Эдгээр бүх хариу үйлдэл нь нийтлэг зүйл юу вэ? (Слайд 9)
- Тэдний ялгаа юу вэ?
- Болж байгаа үйл явцыг нэг үгээр яаж нэрлэх вэ? (Слайд 9)
- Эдгээр урвал явагдахад ямар нөхцөл шаардлагатай вэ? (Слайд 9)
1. Бодисын задралын процесс явагдаж байна (задралын урвал). Бүх урвалд нэг бодис урвалд орж, хоёр ба түүнээс дээш шинэ бодис үүсдэг: энгийн ба нарийн төвөгтэй аль аль нь. Задрах урвалын тодорхойлолтыг томъёолж үзээрэй.
2. Дүрмээр бол бараг бүх задралын урвал нь эндотермик урвал юм, учир нь Урвал үүсэхийн тулд тодорхой нөхцөл шаардагдана: халаалт, цахилгаан гүйдэл, урвалыг хурдасгах бусад бодисууд - катализаторууд. (Слайд 10)
Машин дахь катализатор. (Слайд 11)
- Өдөр бүр сая сая машин энэ замаар явдаг бөгөөд тэдгээр нь тус бүр нь агаарын бохирдлын эх үүсвэр болдог. Энэ нь ялангуяа том хотуудад мэдрэгддэг бөгөөд автомашины утаа нь том асуудал үүсгэдэг.
- Орчин үеийн машинууд нь катализатор эсвэл машины катализатор . Автомашины катализаторын үүрэг бол яндангийн хий дэх хортой бодисын хэмжээг багасгах явдал юм. Тэдний дунд:
- Нүүрстөрөгчийн дутуу исэл (CO) нь хортой, өнгөгүй, үнэргүй хий юм.
- дэгдэмхий органик нэгдлүүд гэж нэрлэгддэг нүүрсустөрөгчид нь үндсэн бүрэлдэхүүн хэсгүүдийн нэг юм утаа , түлшний бүрэн шаталтаас болж үүссэн
- азотын исэл (NO ба NO2) нь мөн бүрэлдэхүүн хэсэг юм утаа , болон хүчиллэг бороо , нөлөө салст бүрхэвч хүн.
Катализатор нь байгальд хаа сайгүй байдаг. Амьд организм дахь бодисын бүх өөрчлөлт нь байгалийн катализаторын оролцоотойгоор явагддаг гэдгийг хэлэхэд хангалттай. ферментүүд тиймээс өндөр температур шаарддаггүй. Энэ нь маш чухал юм - эс тэгвээс химийн урвал явуулдаг амьд эдийг чанаж болно.Тусгай "биологийн" катализатор - ферментгүйгээр амттай талх, хоолны дуршилтай бяслаг, даршилсан байцаа ч авахгүй. Полифенол оксидаза фермент нь жимсний эсэд агуулагдах органик бодис болох полифенолын исэлдэлтийг хурдасгадаг тул зүссэн алим агаарт харанхуйлдаг. Шархыг устөрөгчийн хэт ислээр цутгахад устөрөгчийн хэт исэл "буцалж" - цусанд агуулагдах каталазын ферментийн нөлөөн дор ус, хүчилтөрөгч болж хурдан задардаг. Бие махбодид эсийн амьсгалын үед үүсдэг устөрөгчийн хэт ислийг устгахын тулд каталаза шаардлагатай байдаг.
Хоол боловсруулах шүүс нь олон арван фермент агуулдаг: өөх тосыг глицерин болон органик хүчил болгон задалдаг липазууд; уураг задалдаг протеазууд гэх мэт.
Катализаторыг химийн үйлдвэрт янз бүрийн бодис, түүний дотор аммиак NH 3, хүхрийн хүчил H 2 SO 4 зэрэг химийн чухал бүтээгдэхүүнүүдийг нийлэгжүүлэхэд ашигладаг.
Катализатор бол хамгийн хэрэгтэй бодисуудын нэг боловч заримдаа бид энэ талаар нэг их боддоггүй.
Үүний үр дүнд дулаан шингээх химийн урвалыг нэрлэдэг эндотермик.(Слайд 12)
Химийн урвалын хурдыг өөрчилдөг боловч урвалын үр дүнд хэрэглээгүй бодисыг нэрлэдэг катализаторууд.(Слайд 12)
IV. Нэгтгэх.
Даалгавруудыг гүйцээнэ үү.
(Слайд 13)
- Диаграммыг урвалын тэгшитгэл болгон хувиргах замаар коэффициентүүдийг зохион байгуул. Сонголтынхоо задралын урвалыг тодорхойл. Тайлбар өгөөч.
| Сонголт 1 CuO + H 2 → Cu + H 2 O CO + O 2 → CO 2 AI + CI 2 → AICI 3 CaCO 3 → CaO + CO 2 |
Сонголт 2 HCI + AI → AICI 3 + H 2 Na 2 O + H 2 O → NaOH KCIO 3 → KCI + O 2 Na + H 2 → NaH |
- Даалгавар.Хэрэв урвалын үр дүнд 2 моль бодис задарсан бол бодисын хэмжээ ба урвалын бүтээгдэхүүний аль нэгнийх нь массыг тодорхойл.
V. Гэрийн даалгавар§ 27, жишээ нь. 1, 2 хуудас 155 (Слайд 14).
VI. Ашигласан номууд:
- Габриелян О.С."Хими" 8-р анги. Сурах бичиг.
- О.С. Габриелян, Н.П. Воскобойникова, А.В.Яшукова"Хими", 8-р анги. Багшийн гарын авлага. М .: тоодог, 2002.
- О.С.Габриелян, Т.В.Смирнова.Бид 8-р ангидаа химийн хичээл үздэг.
- Л.Ю. Аликберова"Хөгжилтэй хими: Оюутан, багш, эцэг эхчүүдэд зориулсан ном", М.: AST - PRESS, 1999.
- Хүүхдэд зориулсан нэвтэрхий толь бичиг. 17-р боть. Хими. М .: Аванта +, 2000.
- Интернет материал.