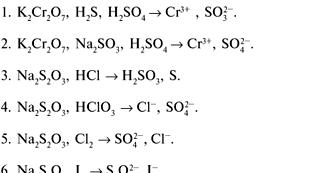Kvėpavimo grandinė. Audinių kvėpavimo grandinės struktūrinė organizacija Kvėpavimo grandinės struktūra
Redokso fermentai, katalizuojantys elektronų perdavimą ir oksidacinį fosforilinimą, yra lokalizuoti ląstelių mitochondrijų vidinės membranos lipidiniame sluoksnyje.
Elektronų pernešimas į deguonį mitochondrijose (13.3 pav.) vyksta keliais etapais ir yra elektronų nešėjų grandinė, kurios redokso potencialas didėja artėjant prie deguonies (redukcijos potencialas atitinkamai mažėja). Šios transporto sistemos vadinamos kvėpavimo grandinės.
Ryžiai. 13.3.
Dauguma elektronų porų patenka į kvėpavimo grandinę dėl fermentų (dehidrogenazių), kurie naudoja kofermentus NAD + ir NADP + kaip elektronų akceptorius, veikimo. Visa ši fermentų grupė vadinama nuo NAO (P) priklausomomis dehidrogenazėmis.
Kofermentai NAD + (nikotinamido adenino dinukleotidas), FAD ir FMN (flavino adenino dinukleotidas ir flavino mononukleotidas), kofermentas Q (CoQ), hemo turinčių baltymų šeima - citochromai (žymimi kaip citochromai b, Q, C, A, A 3 ) ir baltymai, kuriuose yra ne hemo geležies tarpiniai vežėjai aukštesniųjų organizmų kvėpavimo grandinėje. Procesas prasideda nuo protonų ir elektronų perkėlimo iš oksiduoto substrato į kofermentus NAD+ arba FAD ir NADH bei FADH2 susidarymu.
Vėlesnis elektronų judėjimas iš NADH ir FADH 2 į deguonį gali būti lyginamas su riedėjimu kopėčiomis, kurių laipteliai yra elektronų nešėjai. Su kiekvienu žingsniu nuo žingsnio iki žingsnio išsiskiria dalis laisvos energijos (žr. 13.3 pav.).
Pernešant elektronus iš organinių substratų į molekulinį deguonį dalyvauja trys baltymų kompleksai (I, III, IV) ir dvi judrios nešiklio molekulės: ubichinonas (kofermentas Q) ir citochromas C.

Ryžiai. 13.4. Hemo molekulės struktūra, z = 2* arba 3+
Sukcinato dehidrogenazė, kuri iš tikrųjų priklauso Krebso ciklui, taip pat gali būti laikoma II kvėpavimo grandinės kompleksu.
Kvėpavimo grandinės kompleksai yra sudaryti iš daugelio polipeptidų ir juose yra įvairių redokso kofermentų, susijusių su baltymais.
Elektronų nešikliai citochromai(taip pavadinti dėl savo spalvos) yra baltymai, turintys įvairių grupių kaip protezų grupę brangakmenių. Brangakmenių tipas b atitinka hemoglobiną. Hemas kovalentiškai jungiasi su baltymu (13.4 pav.).
Citochromams būdingas geležies jonų, esančių heme, gebėjimas pakeisti oksidacijos būseną, kai perduodamas elektronas: 
Nuo flavino priklausomos dehidrogenazės- tai baltymai, kuriuose cisteino, kuris yra baltymo dalis, sulfhidrilo grupės yra susijusios su geležies atomais, todėl susidaro geležies ir sieros kompleksai (centrai). Kaip ir citochromuose, tokiuose centruose esantys geležies atomai gali paaukoti ir priimti elektronus, pakaitomis pereidami į feri- (Fe +3) ir fero- (Fe +2) būsenas.
Geležies ir sieros centrai veikia kartu su flavino turinčiais fermentais FAD arba FMN.
Phpavin adenino dinukleotidas(FAD) yra vitamino B2 (riboflavino) darinys. Kai redukuojama, FAD (oksiduota forma) prideda du vandenilio atomus ir virsta FADH 2 (redukuota forma):

Kitas šiai grupei priklausantis elektronų nešiklis – flavino mononukleotidas (FMN) – taip pat yra vitamino B2 darinys (nuo vitamino B2 jis skiriasi tik tuo, kad yra fosfatų grupė).
Abu flavino kofermentai taip pat gali egzistuoti vadinamųjų formų puschinonai- laisvieji radikalai, susidarantys tik vienam elektronui perkeliant į FAD arba FMN:

Bendras įvairių flavoproteinų, kurie skiriasi fermento baltyminiu komponentu, pavadinimas yra FP“.
Nuo piridino priklausomos dehidrogenazės gavo šį pavadinimą, nes jų kofermentas yra NAD + ir NADP +, kurių molekulėse yra darinys piridinas - nikotinamidas:

Šių fermentų katalizuojamos reakcijos gali būti pavaizduotos taip:

Su NAD + susijusios dehidrogenazės daugiausia dalyvauja kvėpavimo procese, t.y. elektronų pernešimo iš substratų į deguonį procese, o su NADP + susijusios dehidrogenazės pirmiausia dalyvauja elektronų pernešime iš substratų, atsirandančių dėl katabolinių reakcijų į redukcines biosintetines reakcijas.
Vienintelis nebaltyminis elektronų nešėjas yra ubichinonas, taip pavadintas todėl, kad šis chinonas randamas visur (nuo visur esantis- visur esantis). Sutrumpintai jis vadinamas CoQ arba tiesiog Q. Redukuodamas ubikinonas prijungia ne tik elektronus, bet ir protonus. Vieno elektrono perdavimo metu virsta semichinonas, dviejų elektronų - in hidrochinonas.
Elektronų nešėjų seka mitochondrijų kvėpavimo grandinėje gali būti pavaizduota tokia diagrama:

Ši schema aprašyta nuoseklių reakcijų grandine: 

Tokiu būdu per kvėpavimo grandinę elektronai iš substratų pasiekia galutinį akceptorių – atmosferos deguonį. Vanduo, susidaręs dėl šio proceso, vadinamas metaboliniu vandeniu.
Vandenilio atskyrimas į protonus ir elektronus mitochondrijų membranoje yra elektronų transportavimo grandinė, veikianti kaip protonų siurblys, pumpuojantis vandenilio jonus iš tarpląstelinės erdvės į membranos išorę.
Įvadas
Kvėpavimo grandinė yra struktūriškai ir funkciškai susijusių transmembraninių baltymų ir elektronų nešėjų sistema.
ETC kaupia energiją, išsiskiriančią oksiduojant NADH ir FADH2 su molekuliniu deguonimi (aerobinio kvėpavimo atveju) arba kitomis medžiagomis (anaerobinio kvėpavimo atveju) transmembraninio potencialo pavidalu dėl nuoseklaus elektronų perdavimo išilgai grandinė kartu su protonų siurbimu per membraną.
Prokariotuose ETC yra lokalizuotas CPM, eukariotuose - ant vidinės mitochondrijų membranos. Nešėjai išsidėstę pagal jų redokso potencialą, elektronų pernešimas visoje grandinėje vyksta spontaniškai.
Mitochondrijos vadinamos ląstelės „energijos stotimis“, nes būtent šiose organelėse daugiausia sugaunama oksidacinių procesų tiekiama energija.
Kvėpavimo grandinė
Visa riebiųjų rūgščių ir aminorūgščių oksidacijos metu išsiskirianti naudingoji energija ir beveik visa angliavandenių oksidacijos energija panaudojama mitochondrijose redukuojančių ekvivalentų pavidalu. Mitochondrijose yra keletas katalizatorių, sudarančių kvėpavimo grandinę, kurie sugauna ir perneša redukuojančius ekvivalentus, nukreipdami juos reaguoti su deguonimi, todėl susidaro vanduo. Tuo pačiu metu mechanizmas veikia taip, kad gautų potencialią laisvą energiją, kaupiantis didelės energijos fosfatų pavidalu. Mitochondrijose taip pat yra fermentų sistemų, kurios užtikrina daugumos redukuojančių ekvivalentų susidarymą; tai yra -oksidacijos ir citrinų rūgšties ciklo fermentai (pastarasis yra įprastas metabolizmo kelias oksiduojantis visiems pagrindiniams maisto produktams). Šis ryšys parodytas 1.1 pav.
Kvėpavimo grandinės organizavimas mitochondrijose
Pagrindiniai kvėpavimo grandinės komponentai (1.1 pav.) yra išvardyti eilės tvarka pagal didėjantį redokso potencialą. Vandenilio atomai arba elektronai juda išilgai grandinės nuo elektroneigiamų komponentų iki elektropozityvesnio deguonies, redokso potencialo pokytis pereinant iš NAD/NADH sistemos į O2/H2O sistemą yra 1,1 V.
Pagrindinė kvėpavimo grandinė prasideda nuo NAD priklausomų dehidrogenazių, praeina per flavoproteinus ir citochromus ir baigiasi molekuliniu deguonimi. Ne visi substratai yra prijungti prie kvėpavimo grandinės per nuo NAD priklausomas dihidrogenazes; kai kurios iš jų, turinčios santykinai didelį redokso potencialą (pavyzdžiui, fumarato/sukcinato sistema yra susijusios su flavoproteinų dehidrogenazėmis, kurios savo ruožtu yra susijusios su kvėpavimo grandinės citochromais (1.3 pav.).
Neseniai buvo nustatyta, kad kvėpavimo grandinėje yra dar vienas transporteris, jungiantis flavoproteinus su citochromu b, turinčiu mažiausią redokso potencialą tarp nitochromų. Šis transporteris, vadinamas ubichinonu arba kofermentu Q (1.4 pav.), aerobinėmis sąlygomis mitochondrijose randamas oksiduoto chinono pavidalu, o anaerobinėmis sąlygomis – redukuojančio chinolio pavidalu. Kofermentas Q yra mitochondrijų lipidų komponentas; tarp kitų lipidų vyrauja fosfolipidai, kurie yra mitochondrijų membranos dalis. Kofermento Q struktūra panaši į vitaminų K ir E struktūrą. Plastochinonas, randamas chloroplastuose, taip pat turi panašią struktūrą. Visų šių medžiagų struktūroje yra poliizoprenoidinė šoninė grandinė. Kofermento Q kiekis žymiai viršija kitų kvėpavimo grandinės komponentų kiekį; tai rodo, kad kofermentas Q yra mobilus kvėpavimo grandinės komponentas, kuris gauna redukuojančius ekvivalentus iš fiksuotų flavoproteinų kompleksų ir perduoda juos citochromams.
Ryžiai. 1.1.
Papildomas komponentas, randamas funkciškai aktyviuose kvėpavimo grandinės vaistuose, yra geležies ir sieros blokas FeS. Jis yra susijęs su flavoproteinais ir citochromu b. Geležis ir siera dalyvauja redokso procese, kuris vyksta vieno elektrono mechanizmu (1.5 pav.).
Šiuolaikinės idėjos apie pagrindinių kvėpavimo grandinės komponentų seką parodytos Fig. 1.3. Elektronegatyviame grandinės gale dehidrogenazės katalizuoja elektronų perdavimą iš substratų į NAD kvėpavimo grandinėje. Tai vyksta dviem būdais. Tais atvejais, kai substratai yra α-keto rūgštys, piruvatas ir ketoglutaratas, kompleksinės dehidrogenazės sistemos, turinčios lipoato ir FAD, dalyvauja elektronų pernešime į NAD. Elektronų perdavimas kitomis dehidrogenazėmis, naudojant L(+)-3-hidroksiacil-CoA, D(-)-3-hidroksibutiratą, proliną, glutamatą, malitolį ir izocitratą kaip substratus, vyksta tiesiogiai NAD kvėpavimo grandinėje.
Sumažėjęs NADH kvėpavimo grandinėje savo ruožtu oksiduojamas metaloflavoproteino NADH dehidrogenazės. Šiame fermente yra FeS ir FMN ir jis yra glaudžiai susijęs su kvėpavimo grandine. Kofermentas Q yra redukuojančių ekvivalentų, kuriuos daugelis substratų per flavoproteinų dehidrogenazes tiekia į kvėpavimo grandinę, surinkėjas. Šie substratai yra sukcinatas, cholinas ir sarkozinas (1.3 pav.). Šių dehidrogenazių flavino komponentas yra FAD. Tada elektronų srautas iš kofermento Q pereina per eilę citochromų į molekulinį deguonį (1.3 pav.). Citochromai yra išdėstyti didėjimo redokso potencialo tvarka.

Ryžiai. 1.2.

Ryžiai. 1.3. Mitochondrijų kvėpavimo grandinės komponentai FeS yra grandinėje „O2 pusėje“ FP arba Cytb. Cyt – citochromas; EPFP – elektronų perdavimo flavoproteinas; FeS – geležies-sieros baltymas; FP – flavoproteinas; Q – ubikinonas.

Ryžiai. 1.4.

Ryžiai. 1.5.
Galutinis citochromas aa3 atlieka paskutinį redukuojančių ekvivalentų perdavimo į molekulinį deguonį proceso etapą. Fermentų sistemoje yra vario, esminio tikrųjų oksidazių komponento. Citochromo oksidazė turi labai didelį afinitetą deguoniui, todėl kvėpavimo grandinė gali veikti maksimaliu greičiu, kol audinyje praktiškai nebeliks O2. Ši citochromo oksidazės katalizuojama reakcija nėra grįžtama; ji nustato redukuojančių ekvivalentų judėjimo kryptį kvėpavimo grandinėje, kuri yra susijusi su ATP susidarymu.
Buvo iškelta keletas hipotezių, susijusių su struktūrine kvėpavimo grandinės organizacija. Svarbu, kad komponentų moliniai santykiai yra beveik pastovūs. Veikiantys kvėpavimo grandinės komponentai yra įterpti į vidinę mitochondrijų membraną keturių kvėpavimo grandinės baltymų-lipidų kompleksų pavidalu.

Ryžiai. 1.6.
Nurodomos sritys, kuriose greičiausiai įvyksta ryšys su fosforilinimu. BAL- dimerkaprolis; TTFA yra geležies kompleksonas. I-NADH kompleksas; ubichinono oksidoreduktazė; kompleksas II - sukcinatas: ubichinono oksidoreduktazė; kompleksas III – ubichinolis: fericitochromo c oksidoreduktazė; kompleksas IV-ferocitochromas c: deguonies oksidoreduktazė.
Tuo remiantis buvo padaryta išvada, kad šie kompleksai membranoje turi tam tikrą erdvinę orientaciją. Citochromas yra vienintelis tirpus citochromas ir kartu su kofermentu Q tarnauja kaip santykinai judrus kvėpavimo grandinės komponentas, bendraujantis tarp erdvėje fiksuotų kompleksų (1.6 pav.).
ETC yra lokalizuotas CPM, eukariotuose - ant vidinės mitochondrijų membranos. Nešėjai išsidėstę pagal jų redokso potencialą, elektronų pernešimas visoje grandinėje vyksta spontaniškai.
Protonų potencialą ATP sintazė paverčia energija cheminiai ryšiai ATP. Konjuguotas ETC ir ATP sintazės darbas vadinamas oksidaciniu fosforilinimu.
Mitochondrijų elektronų transportavimo grandinė
Oksidacinio potencialo įtaka
| Reduktorius | Oksidatorius | Ео´, В |
|---|---|---|
| H2 | 2 + | - 0,42 |
| NAD H + H+ | NAD + | - 0,32 |
| NADP H + H+ | NADP+ | - 0,32 |
| Flavoproteinai (sumažinti) | Flavoproteinai (oksiduoti) | - 0,12 |
| Kofermentas Q H2 | Kofermentas Q | + 0,04 |
| Citochromas B (Fe2+) | Citochromas B (Fe3+) | + 0,07 |
| Citochromas C 1 (Fe2+) | Citochromas C 1 (Fe3+) | + 0,23 |
| Citochromai A (Fe2+) | Citochromai A (Fe3+) | + 0,29 |
| Citochromai A3 (Fe2+) | Citochromai A3 (Fe3+) | +0,55 |
| H2O | ½ O2 | + 0,82 |
Kvėpavimo grandinės inhibitoriai
Kai kurios medžiagos blokuoja elektronų perdavimą per I, II, III, IV kompleksus.
- I komplekso inhibitoriai – barbitūratai, rotenonas, piericidinas
- II komplekso inhibitorius yra malonatas.
- III komplekso inhibitorius – antimicinas A, miksotiazolas, stigmatinas
- IV kompleksiniai inhibitoriai - vandenilio sulfidas, cianidas, anglies monoksidas, azoto oksidas, natrio azidas
Bakterijų elektronų transportavimo grandinės
Bakterijos, skirtingai nei mitochondrijos, naudoja didelį elektronų donorų ir akceptorių rinkinį, taip pat skirtingus elektronų perdavimo kelius tarp jų. Šie keliai gali būti atliekami vienu metu, pvz. E. coli kai auginami terpėje, kurios pagrindinis šaltinis yra gliukozė organinės medžiagos, naudoja dvi NADH dehidrogenazes ir dvi chinoloksidazes, o tai reiškia, kad yra 4 elektronų transportavimo keliai. Dauguma ETC fermentų yra indukuojami ir sintetinami tik tuo atveju, jei kelias, į kurį jie patenka, yra paklausus.
Be organinių medžiagų, elektronų donorais bakterijose gali būti molekulinis vandenilis, anglies monoksidas, amonis, nitritas, siera, sulfidas ir dvivalentė geležis. Vietoj NADH ir sukcinato dehidrogenazės gali būti formiato, laktato, gliceraldehido-3-fosfato dehidrogenazės, hidrogenazės ir kt. galutiniai elektronų akceptoriai: fumarato reduktazė, nitratų ir nitritų reduktazė ir kt.
taip pat žr
Parašykite apžvalgą apie straipsnį "Elektronų transportavimo kvėpavimo grandinė"
Pastabos
Ištrauka, apibūdinanti elektronų transportavimo kvėpavimo grandinę
- Jūsų garbė, generolui. Jie stovi čia, trobelėje, – pasakė fejerverkas, priėjęs prie Tušino.- Dabar, mano brangioji.
Tušinas atsistojo ir, užsisegęs paltą bei išsitiesęs, nuėjo nuo ugnies...
Netoli artilerijos ugnies, jam paruoštoje trobelėje, princas Bagrationas sėdėjo vakarieniaujant ir kalbėjosi su kai kuriais kartu su juo susirinkusiais dalinių vadais. Ten buvo senukas pusiau užmerktomis akimis, godžiai graužiantis avienos kaulą, ir dvidešimt dvejų metų nepriekaištingas generolas, paraudęs nuo degtinės taurės ir vakarienės, ir štabo karininkas su asmeniniu žiedu, ir Žerkovas, nerimastingai žvelgdamas į visus ir princą Andrejų, išbalusį, sučiaupusias lūpas ir karštligiškai blizgančias akis.
Trobelėje stovėjo kampe palinkęs paimtas prancūziškas plakatas, o revizorius naiviau veidu apčiuopė plakato audinį ir suglumęs papurtė galvą, galbūt dėl to, kad jį tikrai domina reklamjuostės išvaizda. nes alkanam jam buvo sunku žiūrėti į vakarienę, kuriai neužteko indų. Kitoje trobelėje buvo dragūnų sugautas prancūzų pulkininkas. Mūsų pareigūnai būriavosi aplink jį ir žiūrėjo į jį. Princas Bagrationas padėkojo atskiriems vadams ir paklausė apie bylos detales bei nuostolius. Netoli Braunau prisistatęs pulko vadas pranešė kunigaikščiui, kad, kai tik prasidėjo reikalas, jis pasitraukė iš miško, surinko medkirčius ir, paleisdamas juos pro save, su dviem batalionais smogė durtuvais ir nuvertė prancūzus.
- Kaip pamačiau, Jūsų Ekscelencija, kad pirmas batalionas suirzęs, stovėjau ant kelio ir galvojau: „Išleisiu šiuos ir pasitiksiu mūšio ugnimi“; Aš taip ir padariau.
Pulko vadas taip norėjo tai padaryti, labai apgailestavo, kad neturėjo laiko tai padaryti, kad jam atrodė, kad visa tai iš tikrųjų įvyko. Galbūt tai iš tikrųjų įvyko? Ar buvo įmanoma šioje painiavoje išsiaiškinti, kas buvo, o kas ne?
„Ir turiu pastebėti, jūsų Ekscelencija“, – tęsė jis, prisimindamas Dolokhovo pokalbį su Kutuzovu ir paskutinį jo susitikimą su pažemintu žmogumi, – kad eilinis, pažemintas Dolokhovas, mano akyse užfiksavo prancūzų karininką ir ypač pasižymėjo.
„Čia, jūsų Ekscelencija, pamačiau pavlogradiečių išpuolį“, – įsikišo Žerkovas, neramiai apsidairęs, tą dieną husarų visai nematęs, o apie juos girdėjęs tik iš pėstininkų karininko. - Jie sutraiškė du kvadratus, jūsų Ekscelencija.
Išgirdę Žerkovo žodžius, kai kurie nusišypsojo, kaip visada tikėdamiesi iš jo pokšto; bet pastebėję, kad tai, ką jis sako, taip pat linko į mūsų ginklų šlovę ir šiandieną, jie įgavo rimtą išraišką, nors daugelis puikiai žinojo, kad tai, ką Žerkovas pasakė, yra melas, nepagrįstas niekuo. Princas Bagrationas kreipėsi į senąjį pulkininką.
– Ačiū visiems, ponai, visi daliniai pasielgė didvyriškai: pėstininkai, kavalerija ir artilerija. Kaip centre liko du ginklai? – paklausė jis, ieškodamas ko nors akimis. (Princas Bagrationas neklausė apie ginklus kairiajame flange; jis jau pačioje reikalo pradžioje žinojo, kad visi ginklai ten buvo palikti.) „Manau, kad aš tavęs klausiau“, – jis kreipėsi į budintį pareigūną. būstinė.
„Vienas nukentėjo, – atsakė budintis pareigūnas, – o kito, nesuprantu; Aš pats visą laiką buvau, daviau įsakymus ir tiesiog nuvažiavau... Karšta buvo tikrai“, – kukliai pridūrė jis.
Kažkas pasakė, kad kapitonas Tušinas stovi čia, netoli kaimo, ir kad jie jau buvo išsiųsti jo.
„Taip, štai tu“, – pasakė princas Bagrationas, atsisukęs į princą Andrejų.
„Na, mes trumpam nesikraustėme kartu“, – maloniai nusišypsojo Bolkonskiui budintis pareigūnas.
„Neturėjau malonumo tavęs matyti“, – šaltai ir staigiai pasakė princas Andrejus.
Visi tylėjo. Tušinas pasirodė ant slenksčio, nedrąsiai verždamasis iš už generolų. Vaikščiodamas aplink generolus ankštoje trobelėje, susigėdęs, kaip visada, matydamas savo viršininkus, Tušinas nepastebėjo vėliavos stiebo ir užkliuvo už jo. Keli balsai nusijuokė.
– Kaip buvo atsisakyta ginklo? – paklausė Bagrationas, susiraukęs ne tiek į kapitoną, kiek į besijuokiančius, tarp kurių garsiausiai girdėjosi Žerkovo balsas.
Tik dabar Tušinas, matydamas didžiulę valdžią, su visu siaubu įsivaizdavo savo kaltę ir gėdą dėl to, kad, likęs gyvas, prarado du ginklus. Jis buvo toks susijaudinęs, kad iki tos akimirkos neturėjo laiko apie tai galvoti. Pareigūnų juokas jį dar labiau supainiojo. Jis stovėjo priešais Bagrationą su virpančiu apatiniu žandikauliu ir vos ištarė:
– Nežinau... Jūsų Ekscelencija... žmonių nebuvo, Jūsų Ekscelencija.
– Galėjai paimti iš priedangos!
Tušinas nesakė, kad priedangos nėra, nors tai buvo absoliuti tiesa. Jis bijojo nuvilti kitą viršininką ir tyliai, įsmeigęs akis, pažvelgė tiesiai į Bagrationo veidą, kaip sumišęs studentas žiūri į egzaminuotojo akis.
Tyla buvo gana ilga. Princas Bagrationas, matyt, nenorėdamas būti griežtas, neturėjo ką pasakyti; likusieji nedrįso kištis į pokalbį. Princas Andrejus pažvelgė į Tušiną iš po antakių ir jo pirštai nervingai judėjo.
- Jūsų Ekscelencija, - aštriu balsu pertraukė tylą princas Andrejus, - jūs nusiteikėte išsiųsti mane į kapitono Tušino bateriją. Buvau ten ir radau nužudytus du trečdalius vyrų ir žirgų, du ginklus sudaužyti ir be dangčio.
Princas Bagrationas ir Tušinas dabar vienodai atkakliai žiūrėjo į Bolkonskį, kuris kalbėjo santūriai ir susijaudinęs.
„Ir jei, jūsų Ekscelencija, leiskite man pareikšti savo nuomonę, – tęsė jis, – tai šios dienos sėkmę labiausiai dėkosime šios baterijos veiklai ir kapitono Tušino bei jo kuopos didvyriškam tvirtumui“, – sakė princas. Andrejus ir, nelaukęs atsakymo, iškart atsistojo ir nuėjo nuo stalo.
Kvėpavimo grandinės komponentai yra fermentiniai baltymai su santykinai tvirtai surištomis mažos molekulinės masės protezinėmis grupėmis. Tokie kompleksai eukariotuose yra lokalizuoti vidinėje mitochondrijų membranos pusėje, o prokariotuose – plazminėje membranoje. Kvėpavimo grandinės komponentų veikimo mechanizmas ir lokalizacija abiejose membranose iš esmės yra panašūs.
Kvėpavimo grandinės komponentai panardintas į lipidų dvisluoksnį. Kalbame apie daugybę fermentų, kofermentų ir protezinių grupių, įvairių dehidrogenazių ir transporto sistemų, dalyvaujančių elektronų ir vandenilio pernešime. Baltymų komponentus galima išskirti iš membranos. Kvėpavimo mikroorganizmų grandinės susideda iš šių svarbiausių, membranoje lokalizuotų vandenilio atomų arba elektronų nešiklių: flavoproteinai, geležies ir sieros baltymai, chinonai ir citochromai.
Flavoproteinai – kofermentai, kuriuose yra vitamino B2, o juose esančios protezinės grupės yra flavino mononukleotidas (FMN) arba flavino adenino dinukleotidas (FAD).
Flavoproteinai atlieka vandenilio atomų pernešimą, ty jie yra dehidrogenazės. Dehidrogenazė, kurioje FMN yra kaip protezų grupė, yra NADP H2 dehidrogenazė. Tai yra pradinis nešiklis kvėpavimo grandinėje, pernešantis vandenilį iš NADP H2 į šiuos kvėpavimo grandinės komponentus. Dehidrogenazė, esanti kaip protezinė FAD grupė, veikia kaip sukcinato dehidrogenazė. Jis katalizuoja gintaro rūgšties oksidaciją į fumaro rūgštį TCA cikle. Vandenilio atomai iš FAD H2 patenka tiesiai į chinonus, esančius paskutiniuose elektronų transportavimo grandinės etapuose.
Geležies-sieros baltymai (FeS baltymai) turi geležies ir sieros centrų, kuriuose geležies atomai yra prijungti, viena vertus, su aminorūgšties cisteino siera, kita vertus, su neorganine sulfido siera (4 pav.).
Geležies sieros centrai yra kai kurių flavoproteinų (pavyzdžiui, sukcinato dehidrogenazės ir NADP H2 dehidrogenazės) komponentai arba yra vienintelės protezuojamos baltymų grupės. Kvėpavimo grandinėse yra didelis skaičius FeS centrai. Geležies sieros centrai, priklausomai nuo jų struktūros, gali vienu metu perkelti vieną ar du elektronus, kurie yra susiję su geležies atomų valentingumo pasikeitimu.
Ryžiai. 4. Baltymų geležies sieros centrai (FeS centrai).
Chinonai – riebaluose tirpūs junginiai. Gramneigiamose bakterijose jas atstovauja ubichinonas (kofermentas Q) arba menachinonas (5 pav.).
 Ryžiai. 5. Gramneigiamų bakterijų chinonai: A – kofermentas Q (ubichinonas); B – menachinonas
Ryžiai. 5. Gramneigiamų bakterijų chinonai: A – kofermentas Q (ubichinonas); B – menachinonas
Chinonai yra lipofiliniai, todėl yra lokalizuoti membranos lipidinėje fazėje. Jie turi vandenilio atomus. Lyginant su kitais kvėpavimo grandinės komponentais, chinonų randama 10–15 kartų daugiau. Jie tarnauja kaip įvairių kofermentų ir protezinių grupių kvėpavimo grandinėje tiekiamo vandenilio „rinkėjai“ ir perneša jį į citochromus. Taigi jie veikia kvėpavimo grandinėje tarp flavoproteinų ir citochromų.
Citochromai dalyvauti paskutinis etapas elektronų transportavimo grandinėje. Elektronai į juos patenka iš chinonų. Citochromuose yra hemo kaip protezų grupė. Citochromai yra nudažyti; jie skiriasi vienas nuo kito sugerties spektrais ir redokso potencialais. Yra citochromų A, A 3 , b, c, o ir nemažai kitų. Plačiausiai paplitęs citochromas Su. Jis randamas beveik visuose organizmuose, turinčiuose kvėpavimo grandinę. Galutiniai (galiniai) kvėpavimo grandinės citochromai yra citochromai A+ A 3 arba citochromo oksidazė. Jie perkelia elektronus į molekulinį deguonį, t.y. katalizuoja molekulinio deguonies redukciją į vandenį. Citochromo oksidazės reakcijos centre, be dviejų hemų, yra du vario atomai.
Kvėpavimo grandinė turi šias savybes:
1) Kai kurie jo komponentai perneša tik vandenilio atomus, o kiti – tik elektronus.
2) Kvėpavimo grandinėje paeiliui keičiasi vandenilio atomų nešikliai ir elektronų nešikliai. Flavoproteinai ir chinonai atlieka vandenilio atomų perdavimą, o FeS baltymai ir citochromai – elektronus.
3) Nustatyti tam tikri mikroorganizmų kvėpavimo grandinių sudėties skirtumai.
PASKAITA apie BH
studentams_ 2 __ kursas terapinis fakultetas
Tema Biologinė oksidacija 2. Audinių kvėpavimas. Oksidacinis fosforilinimas.
Laikas 90 min.
Ugdymo ir ugdymo tikslai:
Pateikite įžangą:
Apie kvėpavimo grandinės (RC) struktūrą, inhibitorius; nuolatinės srovės veikimo mechanizmai; sąsajos taškai, nuolatinės srovės komponentų ORP reikšmės. Apie P/O santykį ir jo reikšmę.
Apie laisvą ir atjungtą kvėpavimą. Apie OF konjugacijos teorijas.
Apie generavimo mechanizmą Н +.
Apie protonų ATPazės struktūrą ir funkcijas; apie atskyrimo mechanizmą.
Apie oksidacinį fosforilinimą (pH ir ); apie termogenezės mechanizmus, rudojo riebalinio audinio vaidmenį.
Apie vaidmenį energijos apykaitą; H + ir ATP panaudojimo būdai. Apie taikomuosius bioenergijos aspektus.
Apie O 2 vartojimo būdus organizme (mitochondrijų, mikrosomų, peroksido). Dėl mikrosominės nuolatinės srovės savybių, palyginti su mitochondrijų DC. Apie citochromo P 450 savybes, funkcijas.
Apie peroksido oksidaciją. Apie reaktyviųjų deguonies rūšių O 2-, O 2, O 2 susidarymo mechanizmą. Apie peroksido procesų vaidmenį normaliomis ir patologinėmis sąlygomis. Apie lipidų peroksidaciją (LPO): (NEFA → R → dieno konjugatai → hidroperoksidai → MDA). Apie LPO veiklos vertinimo metodus.
Apie antioksidacinę apsaugą: fermentinė ir nefermentinė. Apie SOD, katalazės, glutationo peroksidazės, GSH reduktazės, NADPH dauginimosi sistemų charakteristikas. Apie nefermentinį AOS: vitaminai E, A, C, karotenoidai, histidinas, kortikosteroidai, bilirubinas, šlapalas ir kt.
LITERATŪRA
Berezovas T. T., Korovkinas B. F. Biologinė chemija. M.: Medicina, 1990. S. 213–220; 1998. 305–317 p.
Nikolajevas A. Ya. Biologinė chemija. M.: baigti mokyklą, 1989. 199–221 p.
Papildomas
Filippovičius B. Biochemijos pagrindai. M.: Aukštoji mokykla, 1993. 403–438 p.
Murray R. ir kt.Žmogaus biochemija. M.: Mir, 1993. T. 1. 111–139 p.
Leningeris A. Biochemijos pagrindai. M.: Mir, 1985. T. 2. 403–438, 508–550 p.
Alberts B. Ir ir tt, Ląstelių molekulinė biologija. M.: Mir, 1994.T. 1. 430–459 p.
Skulachev V.P. Biologinių membranų energija. M.: Mokslas. 1989 m.
MEDŽIAGINĖ PARAMA
1. Multimedijos pristatymas.
STUDIJŲ LAIKO APSKAIČIAVIMAS
|
Švietimo klausimų sąrašas |
Skirto laiko kiekis minutėmis |
|
|
Kvėpavimo grandinės (RC) struktūra, jos kompleksai, inhibitoriai. DC veikimo mechanizmas. Sąsajos taškai, nuolatinės srovės komponentų ORP reikšmės. R/O santykis, jo reikšmė. |
||
|
Laisvas ir atjungtas kvėpavimas. OF konjugacijos teorijos (cheminė, konformacinė, chemiosmotinė – P. Mitchell). |
||
|
H + generavimo mechanizmas, jo komponentai, H + /e stechiometrija. |
||
|
Protonų ATPazės struktūra ir funkcija. Atjungimo mechanizmas. |
||
|
OF (pH ir pašalinimas). Termogenezės mechanizmai. Rudojo riebalinio audinio vaidmuo. |
||
|
Pagrindinis energijos apykaitos vaidmuo. H + ir ATP panaudojimo būdai. Taikomieji bioenergijos aspektai. |
||
|
O2 suvartojimo organizme keliai (mitochondrijų, mikrosomų, peroksido). Mikrosominės nuolatinės srovės charakteristikos, jos palyginimas su mitochondrijų DC. Citochromų P 450 charakteristikos, jų funkcija. |
||
|
Peroksido oksidacija. Reaktyviųjų deguonies rūšių O 2 -, O 2, O 2 susidarymo mechanizmas. Peroksido procesų vaidmuo normaliomis ir patologinėmis sąlygomis. Bendras LPO supratimas (NEFA → R → dieno konjugatai → hidroperoksidai → MDA). LPO aktyvumo vertinimo metodai. |
||
|
Antioksidacinė apsauga: fermentinė ir nefermentinė. SOD, katalazės, glutationo peroksidazės, GSH reduktazės, NADPH atkuriančių sistemų charakteristikos. Nefermentinis AOS: vitaminai E, A, C, karotenoidai, histidinas, kortikosteroidai, bilirubinas, šlapalas ir kt. |
Iš viso 90 min
Kvėpavimo grandinės (RC) struktūra, kompleksai, inhibitoriai. Veikimo mechanizmas. Sąsajos taškai, nuolatinės srovės komponentų ORP reikšmės. R/o koeficientas, jo reikšmė.
Kvėpavimo grandinė.
Pakopinis „valdomas degimas“ pasiekiamas tarpiniu būdu įtraukiant kvėpavimo fermentus, turinčius skirtingą redokso potencialą. Redokso potencialas (redokso potencialas) nustato protonų ir elektronų perdavimo kryptį kvėpavimo grandinės fermentais (1 pav.).
Išreiškiamas redokso potencialas elektrovaros jėgos vertė (voltais), kuris atsiranda tirpale tarp oksidatoriaus ir redukcijos agento, kurio koncentracija 1,0 mol/l, esant 25 ˚ C temperatūrai (esant pH = 7,0, abu yra pusiausvyroje su elektrodu, kuris gali grįžtamai priimti elektronus iš reduktorius ). Esant pH=7,0 H 2 /2H + +2ē sistemos redokso potencialas lygus – 0,42 v. Pasirašyti – reiškia, kad ši redokso pora lengvai atsisako elektronų, t.y. atlieka redukcijos vaidmenį, ženklas + rodo redoksinės poros gebėjimą priimti elektronus, t.y. atlieka oksidatoriaus vaidmenį. Pavyzdžiui, poros NADH∙H + / NAD + redokso potencialas yra – 0,32 v, o tai rodo didelį jos gebėjimą atiduoti elektronus, o redokso poros ½O 2 /H 2 O didžiausia teigiama vertė yra +0,81 v, tie. Deguonis turi didžiausią gebėjimą priimti elektronus.
AcCoA oksidacijos metu TCA cikle redukuotos NADH2 ir FADH2 formos patenka į DC, kur elektronų ir protonų energija paverčiama didelės energijos ATP ryšių energija.
DC yra dehidrogenazių rinkinys, kuris perneša elektronus ir protonus iš substrato į deguonį.
Nuolatinės srovės veikimo principai pagrįsti 1-uoju ir 2-uoju termodinamikos dėsniais.
Varomoji nuolatinės srovės jėga yra ORP skirtumas. Bendras visos nuolatinės srovės skirtumas yra 1,1 V. Fosforilinimo taškų ORP skirtumas turėtų būti = 0,25 - 0,3 V.
1. NAD-H poros ORP = 0,32 V.
2. Q-b pora- / - /- - 0 V.
3. O2 - turi +0,82 V.
DC yra lokalizuota vidinėje mitochondrijų membranoje ir turi 2 elektronų ir protonų įvedimo būdus arba 2 įėjimus; DC sudaro 4 kompleksus.
1 įvestis: priklausoma nuo NAD (elektronai ir protonai atsiranda iš visų nuo NAD priklausančių reakcijų).
2 įvestis: priklauso nuo FAD
PER ----> AF
Q --->b--->c 1 --->c--->aa 3 ---->1/2O 2
Gintaro rūgštis ---->FP
Kvėpavimo grandinė yra biologinės oksidacijos įgyvendinimo forma.
Audinių kvėpavimas yra redokso reakcijų seka, vykstanti vidinėje mitochondrijų membranoje, dalyvaujant kvėpavimo grandinės fermentams. Kvėpavimo grandinė turi aiškią struktūrinę struktūrą kvėpavimo kompleksai, kurių išdėstymas priklauso nuo jų redokso potencialo vertės (5.1 pav.). Kvėpavimo grandinių skaičius vienoje mitochondrijoje iš skirtingų audinių ląstelių yra nevienodas: kepenyse - 5000, širdyje - apie 20 000, todėl miokardocitai išsiskiria intensyvesniu kvėpavimu nei hepatocitai.
Ryžiai.
Prieš apsistodami ties kiekvieno kvėpavimo grandinės komponento ypatumais, susipažinkime su audinių kvėpavimo substratais.
Audinių kvėpavimo substratai skirstomi į 2 grupes:
Priklauso nuo NAD– Krebso ciklo substratai izocitratas, α-ketoglutaratas ir malatas. Tai taip pat yra piruvatas, hidroksibutiratas ir β-hidroksiacil-CoA, glutamatas ir kai kurios kitos aminorūgštys. Naudojant vandenilį iš NAD priklausomų substratų Nuo NAD priklausomos dehidrogenazės perduodamas į pirmąjį kvėpavimo grandinės kompleksą.
Priklauso nuo FAD – sukcinatas, glicerolis-3-fosfatas, acil-CoA ir kai kurie kiti. Vandenilis iš nuo FAD priklausomų substratų perkeliamas į II kvėpavimo grandinės kompleksą.
Dehidrogenuojant substratus Nuo NAD priklausomos dehidrogenazės susidaro redukuota NAD forma (NADH∙H +).

Nurodyta oksiduota kofermento NAD+ forma. Šis kofermentas yra dinukleotidas ( nikotinamidas-Adeninas-dinukleotidas): viename nukleotide yra vitamino PP (nikotinamido), kitame yra AMP. Kofermento gebėjimas atlikti tarpinio vandenilio nešiklio vaidmenį yra susijęs su vitamino PP buvimu jo struktūroje. Elektronų-protonų formoje grįžtamojo hidrinimo-dehidrogenavimo procesą galima pavaizduoti lygtimi (R yra likusi kofermento dalis):

NADH∙H + gali susidaryti ne tik mitochondrijose, bet ir ląstelės citozolyje tam tikrų medžiagų apykaitos procesų metu. Tačiau citoplazminis kofermentas negali prasiskverbti į mitochondrijas. Redukuoto kofermento vandenilis pirmiausia turi būti perkeltas į substratus, kurie gali prasiskverbti į mitochondrijas. Tokie „H2 pernešantys substratai“ yra:
Oksalacetatas → malatas
Acetoacetatas → β-hidroksibutiratas
Dihidroksiacetono fosfatas → glicerolio-3-fosfatas

Tada NADH∙H+ oksiduoja kvėpavimo grandinės 1 kompleksas. Panagrinėkime šio komplekso veikimą.
aš – NADH∙H + -ubichinono oksidoduktazė.
Pirmasis kompleksas yra didžiausias kvėpavimo grandinėje (atstovaujamas 23-30 subvienetų). Jis katalizuoja vandenilio perdavimą iš NADH∙H + į ubichinoną (5.1 pav. ir 5.3 pav.). Jame yra kofermento FMN (flavino mononukleotido) ir geležies ir sieros baltymų, kurių sudėtyje yra ne hemo geležies. Šių baltymų funkcija yra atskiriant protonų ir elektronų srautus: elektronai iš FMN∙H 2 perkeliami į vidinės mitochondrijų membranos vidinį paviršių (atsukti į matricą), o protonai perkeliami į išorinį vidinės membranos paviršių ir išleidžiami į mitochondrijų matricą.
Pernešant protonus ir elektronus, pirmojo komplekso redokso potencialas sumažėja 0,38 v, to visiškai pakanka ATP sintezei. Tačiau pačiame komplekse ATP nesusidaro, o dėl komplekso veikimo išsiskirianti energija kaupiama (elektrocheminio potencialo susidarymą žr. toliau) ir iš dalies išsisklaido šilumos pavidalu.
Pagal savo struktūrą FMN yra mononukleotidas, kuriame azoto bazę sudaro riboflavino izoaloksazino šerdis, o pentozė yra ribitolis (kitaip tariant, FMN yra fosforilinta vitamino B2 forma).

FMN funkcija yra priimti 2 vandenilio atomus iš NADH∙H+ ir perkelti juos į geležies-sieros baltymus. Vandenilis (2 elektronai ir 2 protonai) prisijungia prie izoaloksazino žiedo azoto atomų, ir vyksta intramolekulinis dvigubų jungčių persitvarkymas ir susidaro tarpinis semichinonas – laisvųjų radikalų junginys (parodyta diagramoje). viso reakcijos lygtis, kur R yra likusi molekulės dalis)

II audinių kvėpavimo grandinės kompleksas – sukcinato ubichinono oksidoreduktazė.
Šis kompleksas turi mažiau molekulinė masė taip pat yra geležies ir sieros baltymų. Sukcinato ubichinono oksidoreduktazė katalizuoja vandenilio pernešimą iš sukcinatasį ubikinoną. Kompleksą sudaro kofermentas FAD (flavino adenino dinukleotidas) ir fermentas sukcinato dehidrogenazė, kuri taip pat yra Krebso ciklo fermentas. Acilas~SCoA, 3-fosfogliceratas ir dihidroksiacetono fosfatas Jie taip pat yra nuo FAD priklausomi audinių kvėpavimo substratai ir šio kofermento pagalba liečiasi su antruoju kompleksu.

Ryžiai. 5.3 Pirmasis kvėpavimo grandinės kompleksas
Vandenilio substratų įtraukimo į audinių kvėpavimo grandinės II kompleksą energija išsklaidoma daugiausia šilumos pavidalu, nes šioje grandinės dalyje redokso potencialas šiek tiek sumažėja ir šios energijos nepakanka ATP sintezei.

FAD atkūrimo procesas vyksta panašiai kaip ir FMN.
Kofermentas Q arba ubichinonas yra hidrofobinis junginys, yra ląstelių membranų komponentas, randamas didelėmis koncentracijomis ir priklauso vitaminų grupei. priklauso vitaminų grupei.
Ubichinonas (kofermentas Q). Ubichinonas yra maža lipofilinė molekulė, cheminė struktūra kuris yra benzochinonas su ilga šonine grandine (izoprenoidų vienetų skaičius svyruoja nuo 6 bakterijose iki 10 žinduoliuose).
Kvėpavimo grandinėje kofermentas Q yra tam tikras vandenilio depas (baseinas), kurį jis gauna iš įvairių flavoproteinų. Ubichinono molekulės lipofiliškumas lemia jos gebėjimą laisvai judėti mitochondrijų membranos lipidinėje fazėje, sulaikant protonus ir elektronus ne tik iš kvėpavimo grandinės I ir II kompleksų, bet ir gaudant protonus iš mitochondrijų matricos. Šiuo atveju ubichinonas redukuojamas, kad susidarytų tarpinis laisvųjų radikalų produktas – semichinonas.
Sumažėjusi ubichinono forma ubichinolis perneša protonus ir elektronus į kvėpavimo grandinės III kompleksą.

Citochromo oksidazė turi didelį afinitetą deguoniui ir gali veikti esant žemai deguonies koncentracijai.
aa 3 – susideda iš 6 subvienetų, kurių kiekviename yra hemo ir vario atomas. 2 subvienetai sudaro citochromą a, o likę 4 priklauso citochromui a 3.
Tarp NAD ir AF, b-c, a-a3 yra didžiausias ORP skirtumas. Šie taškai yra ATP sintezės vieta (ADP fosforilinimo vieta).
III audinių kvėpavimo grandinės kompleksas – ubichinolio-citochromo C oksidoreduktazė. III kompleksas apima citochromaib Ir Su 1 priklauso kompleksinių baltymų grupei chromoproteinai. Šių baltymų protezų grupė yra spalvota (chroma – dažai) ir savo chemine struktūra artima hemoglobino hemui. Tačiau, priešingai nei hemoglobinas ir oksihemoglobinas, kuriuose geležis turėtų būti tik dvivalentės formos, citochromuose esanti geležis kvėpavimo grandinės veikimo metu pereina iš dvivalentės į trivalentę būseną (ir atvirkščiai).
Kaip rodo pavadinimas, kompleksas III perkelia elektronus iš ubichinolio į citochromą C. Pirmiausia elektronai patenka į oksiduotą citochromo b formą (Fe 3+), kuri redukuojama (Fe 2+), tada redukuotas citochromas b perkelia elektronus į citochromą C. oksiduota citochromo c forma, kuri taip pat redukuojama ir, savo ruožtu, perkelia elektronus į citochromą C.
mitochondrijų membrana nuo III komplekso iki IV komplekso ir atgal. Šiuo atveju 1 citochromo C molekulė, pakaitomis oksiduojanti ir redukuojanti, perduoda 1 elektroną.

IV kvėpavimo grandinės kompleksas – citochromo C oksidazė. Kompleksas pavadintas oksidazė dėl galimybės tiesiogiai sąveikauti su deguonimi. Žinduolių organizme šis didelis (~ 200 kD) transmembraninis baltymas susideda iš 6-13 subvienetų, kai kuriuos iš jų koduoja mitochondrijų DNR. IV komplekse yra 2 chromoprotenai - citochromoA Ir citochromoA 3 . Skirtingai nuo kitų citochromų, citochromai A Ir A 3 kiekviename yra ne tik geležies, bet ir vario atomas. Varis šių citochromų sudėtyje elektronų pernešimo metu taip pat pakaitomis keičiasi tarp oksiduotos (Cu 2+) ir redukuotos (Cu +) būsenos.
Citochromas Su oksidazė katalizuoja 4 redukuotų citochromo molekulių vieno elektrono oksidaciją Su ir tuo pačiu metu atlieka visišką (4 elektronų) deguonies molekulės redukciją:
4 citochromai Su(Fe 2+) + 4 H + + O 2 4 citochromas Su(Fe 3+) + H2O
Vandens molekulių susidarymo protonai yra iš matricos. Reikėtų pažymėti, kad ši reakcija yra labai sudėtinga ir vyksta per tarpinius laisvųjų deguonies radikalų susidarymo etapus.
IV komplekso redokso potencialas yra didžiausias (+0,57 v), jo energijos visiškai pakanka 3 ATP molekulių sintezei, tačiau didžioji dalis šios energijos sunaudojama protonams „pumpuoti“ iš mitochondrijų matricos į tarpmembraninę erdvę. Dėl aktyvus transportas protonų citochromas Su- buvo pavadinta oksidazė "protonų siurblys".
Taigi audinių kvėpavimas yra elektronų ir protonų transportavimas iš NAD arba FAD priklausomų substratų į deguonį, taip pat protonų, tiekiamų mitochondrijų matrica, procesas. Transporto metu redokso potencialas mažėja, o kartu išsiskiria energija, esanti audinių kvėpavimo substratuose. Visišką molekulinio deguonies atkūrimą ore kvėpavimo grandinėje lydi vandens susidarymas.