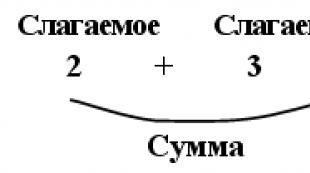
Գլուտամինաթթուն նեյրոհաղորդիչ է: Նեյրոհաղորդիչներ և հոգեկան հիվանդությունների բուժման հիմնական միջոցներ: Համկ. հիմնական արգելակի ընտրություն
· Գլուտամատի պարունակությունը բնության մեջ · Օգտագործումներ · Նշումներ · Առնչվող հոդվածներ · Պաշտոնական կայք և միջին կետ
Գլուտամատը ամենաառատ գրգռիչ նյարդային հաղորդիչն է նյարդային համակարգողնաշարավորներ. Քիմիական սինապսներում գլյուտամատը պահվում է նախասինապտիկ վեզիկուլներում (վեզիկուլներ): Նյարդային իմպուլսը խթանում է գլյուտամատի արտազատումը նախասինապտիկ նեյրոնից: Հետսինապտիկ նեյրոնի վրա գլուտամատը կապվում է հետսինապտիկ ընկալիչների հետ, ինչպիսիք են, օրինակ, NMDA ընկալիչները և ակտիվացնում դրանք։ Սինապտիկ պլաստիկության մեջ վերջինիս մասնակցության շնորհիվ գլուտամատը ներգրավված է այնպիսի ճանաչողական գործառույթներում, ինչպիսիք են ուսումն ու հիշողությունը։ Սինապտիկ պլաստիկության մի ձև, որը կոչվում է երկարաժամկետ հզորացում, տեղի է ունենում հիպոկամպուսի, նեոկորտեքսի և ուղեղի այլ մասերի գլյուտամատերգիկ սինապսներում: Գլուտամատը ներգրավված է ոչ միայն դասական վարքագծի մեջ նյարդային ազդակնեյրոնից նեյրոն, բայց նաև ծավալային նեյրոհաղորդման մեջ, երբ ազդանշանը փոխանցվում է հարևան սինապսներին՝ հարևան սինապսներում արձակված գլուտամատի գումարման միջոցով (այսպես կոչված էքստրասինապտիկ կամ ծավալային նյարդափոխադրում)) Բացի այդ, գլուտամատը որոշիչ դեր է խաղում։ ուղեղի զարգացման մեջ աճի կոնների և սինապսների կարգավորման մեջ, ինչպես նկարագրել է Մարկ Մաթսոնը:
Գլուտամատային փոխադրիչներ հայտնաբերվում են նեյրոնային և նեյրոգլիալ թաղանթների վրա: Նրանք արագ հեռացնում են գլյուտամատը արտաբջջային տարածությունից։ Ուղեղի վնասման կամ հիվանդության դեպքում նրանք կարող են աշխատել հակառակ ուղղությամբ, որի արդյունքում գլյուտամատը կարող է կուտակվել բջիջից դուրս: Այս գործընթացը հանգեցնում է NMDA ընկալիչների ուղիներով մեծ քանակությամբ կալցիումի իոնների ներթափանցմանը բջիջ, որն իր հերթին առաջացնում է բջիջի վնաս և նույնիսկ մահ, ինչը կոչվում է էքսիտոտոքսիկություն: Բջջային մահվան մեխանիզմները ներառում են նաև.
- միտոքոնդրիաների վնասում ներբջջային չափազանց բարձր կալցիումի պատճառով,
- Գլյու / Ca2 ± միջնորդավորված պրոապոպտոտիկ գեների տրանսկրիպցիոն գործոնների խթանմամբ կամ հակաապոպտոտիկ գեների տառադարձման նվազմամբ:
Գլյուտամատի արտազատման ավելացման կամ դրա նվազեցման հետ կապված էկզիտոտոքսիկությունը տեղի է ունենում իշեմիկ կասկադի ընթացքում և կապված է ինսուլտի հետ, ինչպես նաև նկատվում է այնպիսի հիվանդությունների դեպքում, ինչպիսիք են կողային ամիոտրոֆիկ սկլերոզը, լատիրիզմը, աուտիզմը, մտավոր հետամնացության որոշ ձևեր և Ալցհեյմերի հիվանդությունը: Ի հակադրություն, դասական ֆենիլկետոնուրիայի դեպքում նկատվում է գլյուտամատի արտազատման նվազում, ինչը հանգեցնում է գլյուտամատային ընկալիչների արտահայտման խանգարմանը: Գլուտամինաթթուն մասնակցում է էպիլեպտիկ նոպաների իրականացմանը: Գլուտամինաթթվի միկրոներարկումը նեյրոնների մեջ առաջացնում է ինքնաբուխ ապաբևեռացում, որը նման է նոպաների ժամանակ պարոքսիզմալ ապաբևեռացմանը: Էպիլեպտիկ ֆոկուսի այս փոփոխությունները հանգեցնում են լարման կախված կալցիումի ուղիների բացմանը, ինչը կրկին խթանում է գլուտամատի ընտրությունը և հետագա ապաբևեռացումը։ Գլուտամատային համակարգի դերն այսօր մեծ տեղ է հատկացվում այնպիսի հոգեկան խանգարումների պաթոգենեզում, ինչպիսիք են շիզոֆրենիան և դեպրեսիան։ Այսօր շիզոֆրենիայի էթիոպաթոգենեզի ամենաարագ ուսումնասիրված տեսություններից մեկը NMDA ընկալիչների հիպոֆունկցիայի վարկածն է. NMDA ընկալիչների անտագոնիստներ օգտագործելիս, ինչպիսին է ֆենցիկլինը, առողջ կամավորների մոտ ի հայտ են գալիս շիզոֆրենիայի ախտանիշները: Այս առումով ենթադրվում է, որ NMDA ընկալիչների հիպոֆունկցիան շիզոֆրենիայով հիվանդների մոտ դոֆամիներգիկ փոխանցման խանգարումների պատճառներից մեկն է: Ձեռք բերվեցին նաև ապացույցներ, որ իմունային-բորբոքային մեխանիզմով NMDA ընկալիչների պարտությունը («հակա-NMDA ընկալիչ էնցեֆալիտ») ունի սուր շիզոֆրենիայի կլինիկական պատկեր: Ենթադրվում է, որ չափից ավելի գլյուտամատերգիկ նեյրոհաղորդումը դեր է խաղում էնդոգեն դեպրեսիայի էթիոպաթոգենեզում, ինչի մասին վկայում է դիսոցիատիվ անզգայացնող կետամինի արդյունավետությունը փորձի ժամանակ բուժման դիմացկուն դեպրեսիայի դեպքում մեկ անգամ օգտագործմամբ:
Գլուտամատային ընկալիչներ
Տարբերում են իոնոտրոպ և մետաբոտրոպ (mGLuR 1-8) գլյուտամատային ընկալիչներ։
Ionotropic ընկալիչները NMDA ընկալիչներն են, AMPA ընկալիչները և kainate ընկալիչները:
Գլուտամատային ընկալիչների էնդոգեն լիգանդներն են գլուտամինաթթուն և ասպարտիկ թթուն: Գլիցինը նույնպես անհրաժեշտ է NMDA ընկալիչները ակտիվացնելու համար: NMDA ընկալիչների արգելափակողներն են PCP, կետամինը և այլն: AMPA ընկալիչները նույնպես արգելափակված են CNQX, NBQX-ով: Կաինաթթուն կաինատային ընկալիչների ակտիվացնող է:
Գլուտամատի «ցիկլը».
Նյարդային վերջավորությունների միտոքոնդրիումներում գլյուկոզայի առկայության դեպքում գլուտամինից գլուտամատի դեամինացում տեղի է ունենում գլուտամինազ ֆերմենտի օգնությամբ։ Նաև գլյուկոզայի աերոբիկ օքսիդացման ժամանակ գլյուտամատը շրջելիորեն սինթեզվում է ալֆա-կետօղլուտարատից (ձևավորվում է Կրեբսի ցիկլում)՝ օգտագործելով ամինոտրանսֆերազ։
Նեյրոնի կողմից սինթեզված գլյուտամատը մղվում է վեզիկուլների մեջ: Այս գործընթացը պրոտոններով զուգակցված տրանսպորտ է: H + իոնները մղվում են վեզիկուլ՝ օգտագործելով պրոտոնից կախված ATPase: Երբ պրոտոնները դուրս են գալիս գրադիենտի երկայնքով, գլյուտամատի մոլեկուլները մտնում են վեզիկուլ՝ օգտագործելով վեզիկուլյար գլյուտամատ փոխադրողը (VGLUTs):
Գլուտամատը արտազատվում է սինապտիկ ճեղքվածքի մեջ, որտեղից մտնում է աստղոցիտներ, որտեղից տրանսամինացվում է գլուտամինի։ Գլութամինը հետ է արտազատվում սինապտիկ ճեղքվածք և միայն դրանից հետո է այն գրավում նեյրոնը: Ըստ որոշ տեղեկությունների, գլուտամատը չի վերադարձվում ուղղակիորեն կլանման միջոցով:
Գլուտամատի դերը թթու-բազային հավասարակշռության մեջ
Գլուտամինազի ֆերմենտի միջոցով գլուտամինից գլուտամատի դեամինացումը հանգեցնում է ամոնիակի առաջացմանը, որն, իր հերթին, կապվում է ազատ պրոտոնի հետ և արտազատվում երիկամային խողովակի լույսի մեջ՝ հանգեցնելով acidosis-ի նվազմանը։ Գլուտամատի փոխակերպումը β-կետօղլուտարատի տեղի է ունենում նաև ամոնիակի ձևավորման հետ: Այնուհետև, ketoglutarate-ը քայքայվում է ջրի և ածխածնի երկօքսիդի: Վերջիններս ածխաթթվի միջով ածխածնի անհիդրազի օգնությամբ վերածվում են ազատ պրոտոնի և բիկարբոնատի։ Պրոտոնը արտազատվում է երիկամային խողովակի լույսի մեջ՝ նատրիումի իոնի հետ համատեղ փոխադրման շնորհիվ, և բիկարբոնատը մտնում է պլազմա։
Գլյուտամատերգիկ համակարգ
Կենտրոնական նյարդային համակարգում կա մոտ 10 6 գլյուտամատերգիկ նեյրոն։ Նեյրոնների մարմինները գտնվում են գլխուղեղի կեղևում, հոտառական լամպում, հիպոկամպում, նիգրա նյութում, ուղեղիկում: Ողնուղեղում - մեջքային արմատների առաջնային ներծծող հատվածներում:
GABAergic նեյրոններում գլուտամատը արգելակող միջնորդի՝ գամմա-ամինաբուտիրաթթվի նախադրյալն է, որն արտադրվում է գլուտամատ դեկարբոքսիլազա ֆերմենտի կողմից:
Ուղեղի աշխատանքի հիմքում ընկած է նյարդային բջիջների փոխազդեցությունը, և նրանք միմյանց հետ խոսում են նյարդային հաղորդիչներ կոչվող նյութերի միջոցով: Կան բավականին քիչ միջնորդներ, օրինակ՝ ացետիլխոլին, նորէպինեֆրին։ Ամենակարևոր միջնորդներից մեկը, և գուցե ամենակարևորը, կոչվում է գլուտամինաթթու կամ գլուտամատ: Եթե նայեք մեր ուղեղի կառուցվածքին և թե ինչ նյութեր են օգտագործվում տարբեր նյարդային բջիջների կողմից, ապա գլյուտամատն արտազատվում է նեյրոնների մոտ 40%-ի կողմից, այսինքն՝ սա նյարդային բջիջների շատ մեծ մասն է: Մեր ուղեղում, ուղեղում և ողնուղեղում գլյուտամատի արտազատման օգնությամբ փոխանցվում են հիմնական տեղեկատվական հոսքերը. այն ամենը, ինչ կապված է սենսացիայի հետ (տեսողություն և լսողություն), հիշողություն, շարժում, մինչև այն հասնի մկաններին. այս ամենը փոխանցվում է արտազատման միջոցով: գլուտամիկ թթու. Ուստի, իհարկե, այս միջնորդն արժանի է հատուկ ուշադրության և ակտիվորեն ուսումնասիրվում է։
Իր քիմիական կառուցվածքով գլուտամատը բավականին պարզ մոլեկուլ է։ Դա ամինաթթու է, և սննդային ամինաթթու, այսինքն՝ մենք ստանում ենք նմանատիպ մոլեկուլներ պարզապես այն սպիտակուցների բաղադրության մեջ, որոնք մենք ուտում ենք։ Բայց պետք է ասեմ, որ սննդի գլյուտամատը (կաթից, հացից կամ մսից) գործնականում ուղեղ չի անցնում։ Նյարդային բջիջները սինթեզում են այս նյութը հենց աքսոնների վերջավորություններում, հենց այն կառույցներում, որոնք սինապսների մաս են կազմում, «տեղում» և այնուհետև արտազատում են տեղեկատվություն փոխանցելու համար:
Շատ հեշտ է գլյուտամատ պատրաստել։ Ելակետային նյութը α-ketoglutaric թթու է: Սա շատ տարածված մոլեկուլ է, այն ստացվում է գլյուկոզայի օքսիդացման ընթացքում, բոլոր բջիջներում, բոլոր միտոքոնդրիումներում այն շատ է։ Եվ հետո այս α-կետօղլուտարաթթվի վրա բավական է փոխպատվաստել ցանկացած ամինաթթուից վերցված ցանկացած ամինախումբ, և այժմ դուք ստանում եք գլուտամատ՝ գլուտամինաթթու։ Գլութամինաթթուն կարող է սինթեզվել նաև գլուտամինից։ Սա նաև սննդի ամինաթթու է, գլուտամատը և գլուտամինը շատ հեշտությամբ փոխակերպվում են միմյանց: Օրինակ, երբ գլուտամատը կատարել է իր գործառույթը սինապսում և ազդանշան է փոխանցել, ապա այն ոչնչացվում է գլուտամինի ձևավորմամբ:
Գլուտամատը գրգռիչ նեյրոհաղորդիչ է, այսինքն՝ այն միշտ գտնվում է մեր նյարդային համակարգում, սինապսներում՝ առաջացնելով նյարդային հուզմունք և ազդանշանի հետագա փոխանցում։ Սա տարբերվում է գլյուտամատից, օրինակ, ացետիլխոլինից կամ նորէպինեֆրինից, քանի որ որոշ սինապսներում ացետիլխոլինը և նորէպինեֆրինը կարող են հուզմունք առաջացնել, մյուսներում՝ արգելակում, նրանք ունեն աշխատանքի ավելի բարդ ալգորիթմ: Եվ գլյուտամատն այս առումով ավելի պարզ և հասկանալի է, թեև դուք ընդհանրապես չեք գտնի այդպիսի պարզություն, քանի որ կան գլյուտամատի ընկալիչների մոտ 10 տեսակ, այսինքն՝ զգայուն սպիտակուցներ, որոնց վրա գործում է այս մոլեկուլը, և տարբեր ընկալիչներ տարբեր արագությամբ և տարբեր պարամետրերով անցկացնում է գլյուտամատային ազդանշան:
Բույսերի էվոլյուցիան հայտնաբերել է մի շարք տոքսիններ, որոնք գործում են գլյուտամատային ընկալիչների վրա: Թե ինչ է դա բույսերի համար, ընդհանուր առմամբ, միանգամայն պարզ է. Բույսերը, որպես կանոն, դեմ են կենդանիների կողմից ուտելուն, համապատասխանաբար, էվոլյուցիան հանդես է գալիս որոշ պաշտպանիչ թունավոր կառուցվածքներով, որոնք կանգնեցնում են բուսակերներին: Ամենաուժեղ բուսական տոքսինները կապված են ջրիմուռների հետ, և ջրիմուռների տոքսիններն են, որոնք կարող են շատ ուժեղ ազդել ուղեղի գլյուտամատային ընկալիչների վրա և առաջացնել ընդհանուր հուզմունք և ցնցումներ: Պարզվում է, որ գլյուտամատային սինապսների գերակտիվացումը ուղեղի շատ հզոր գրգռում է՝ ջղաձգական վիճակ։ Այս շարքի թերևս ամենահայտնի մոլեկուլը կոչվում է դոմոաթթու, այն սինթեզվում է միաբջիջ ջրիմուռներով. այդպիսի ջրիմուռներ կան, նրանք ապրում են արևմտյան մասում։ Խաղաղ օվկիանոս, ափին, օրինակ՝ Կանադա, Կալիֆորնիա, Մեքսիկա։ Այս ջրիմուռների թունավորումը շատ ու շատ վտանգավոր է: Եվ այս թունավորումը երբեմն տեղի է ունենում այն պատճառով, որ zooplankton-ը, բոլոր տեսակի մանր խեցգետնակերպերը կամ, օրինակ, երկփեղկանի փափկամարմինները, սնվում են միաբջիջ ջրիմուռներով, երբ նրանք զտում են ջուրը, քաշում են ջրիմուռների բջիջները, իսկ հետո միդիա կամ ոստրե շատ բարձր է: դոմոաթթվի կոնցենտրացիան, և դուք կարող եք լրջորեն թունավորվել:
Անգամ մարդկանց մահվան դեպքեր են գրանցվել։ Ճիշտ է, նրանք միայնակ են, բայց, այնուամենայնիվ, դա խոսում է այս թույնի ուժի մասին։ Իսկ դոմոյաթթվով թունավորումը շատ բնորոշ է թռչունների դեպքում։ Եթե որոշ ծովային թռչուններ, որոնք կրկին ուտում են zooplankton-ով սնվող մանր ձուկ, ստանում են չափից շատ դոմոյաթթու, ապա առաջանում է բնորոշ փսիխոզ. նրանք դառնում են ագրեսիվ... Նման թունավորման մի ամբողջ համաճարակ եղավ 1960-ականների սկզբին, և թերթերի հաղորդագրությունները «թռչունների փսիխոզի» այս համաճարակի մասին ոգեշնչեցին Դաֆնե Դյու Մորիեին գրել «Թռչուններ» վեպը, իսկ հետո Ալֆրեդ Հիչքոկը բեմադրեց «Թռչուններ» դասական թրիլլերը։ դուք տեսնում եք հազարավոր շատ ագրեսիվ ճայերի, որոնք տանջում են ֆիլմի գլխավոր հերոսներին: Բնականաբար, իրականում նման գլոբալ թունավորումներ չեն եղել, բայց, այնուամենայնիվ, դոմոյաթթուն շատ բնորոշ էֆեկտներ է առաջացնում, և դա և նմանատիպ մոլեկուլները, իհարկե, շատ վտանգավոր են ուղեղի համար։
Մենք գլուտամինաթթու և նմանատիպ գլուտամատ ենք ուտում մեծ քանակությամբ միայն սննդային սպիտակուցներով: Մեր սպիտակուցները, որոնք առկա են տարբեր մթերքներում, պարունակում են 20 ամինաթթուներ։ Լավագույն քսանյակում են գլյուտամատն ու գլուտամինաթթուն։ Ավելին, դրանք ամենաշատ ամինաթթուներն են, երբ ընդհանուր առմամբ նայում ես սպիտակուցների կառուցվածքին: Արդյունքում մենք օրական ուտում ենք 5-ից 10 գրամ գլյուտամատ և գլուտամին սովորական սննդով։ Ժամանակին շատ դժվար էր հավատալ, որ գլուտամատը ուղեղում հաղորդիչի գործառույթներ է կատարում, քանի որ պարզվում է, որ այն նյութը, որը մենք բառացիորեն օգտագործում ենք ձիու չափաբաժիններով, կատարում է ուղեղում նման նուրբ գործառույթներ։ Նման տրամաբանական անհամապատասխանություն կար. Բայց հետո նրանք հասկացան, որ իրականում սննդի գլյուտամատը գործնականում չի անցնում ուղեղ։ Դրա համար պետք է շնորհակալություն հայտնել այն կառուցվածքին, որը կոչվում է արյունաուղեղային արգելք, այսինքն՝ հատուկ բջիջները շրջապատում են բոլոր մազանոթները, բոլոր փոքր անոթները, որոնք ներթափանցում են ուղեղը և բավականին խստորեն վերահսկում են շարժումը։ քիմիական նյութերարյունից մինչև նյարդային համակարգ. Եթե սա չլիներ, ապա մեր կերած ինչ-որ կոտլետ կամ բուլկի մեր մեջ ջղաձգություն կառաջացներ, իսկ դա, իհարկե, ոչ մեկին պետք չէ։ Հետևաբար, սննդային գլյուտամատը գրեթե չի անցնում ուղեղ և, փաստորեն, սինթեզվում է՝ միջնորդական գործառույթները կատարելու հենց սինապսներում։ Այնուամենայնիվ, եթե միաժամանակ շատ գլուտամատ են ուտում, ապա փոքր քանակությունը դեռ թափանցում է ուղեղ։ Հետո կարող է լինել մի փոքր գրգռվածություն, որի ազդեցությունը համեմատելի է թունդ սուրճի հետ։ Դիետիկ գլյուտամատի բարձր չափաբաժինների այս ազդեցությունը հայտնի է և տեղի է ունենում բավականին հաճախ, երբ մարդը օգտագործում է մեծ քանակությամբ գլյուտամատ որպես սննդային հավելում:
Փաստն այն է, որ մեր համային համակարգշատ զգայուն է գլյուտամատի նկատմամբ: Կրկին դա պայմանավորված է նրանով, որ սպիտակուցներում շատ գլուտամատ կա: Պարզվում է, որ համային համակարգի էվոլյուցիան, կարգավորելով սննդի քիմիական անալիզը, մեկուսացրել է գլյուտամատը՝ որպես սպիտակուցային սննդի նշան, այսինքն՝ մենք պետք է սպիտակուց ուտենք, քանի որ սպիտակուցը մեր օրգանիզմի հիմնական շինանյութն է։ Նմանապես, մեր համային համակարգը սովորել է շատ լավ հայտնաբերել գլյուկոզան, քանի որ գլյուկոզան և նմանատիպ մոնոսաքարիդները էներգիայի հիմնական աղբյուրն են, իսկ սպիտակուցը՝ հիմնական շինանյութը։ Հետևաբար, համային համակարգը հարմարեցված է ճանաչելու գլուտամատը որպես սպիտակուցային սննդի մասին ազդանշան, և թթու, քաղցր, աղի, դառը համերի հետ մեկտեղ մենք ունենք զգայուն բջիջներ մեր լեզվի վրա, որոնք հատուկ արձագանքում են գլյուտամատին: Իսկ գլուտամատը հայտնի, այսպես կոչված, համային հավելում է: Այն համի ուժեղացուցիչ անվանելը լիովին ճիշտ չէ, քանի որ գլուտամատն ունի իր համը, որն իր կարևորությամբ նույնքան կարևոր է, որքան դառը, թթու, քաղցր և աղի:
Պետք է ասել, որ գլյուտամատային համի առկայությունը հայտնի է ավելի քան հարյուր տարի։ Ճապոնացի ֆիզիոլոգները հայտնաբերել են այս ազդեցությունը այն պատճառով, որ գլյուտամատը (սոյայի սոուսի կամ ծովային ջրիմուռից պատրաստված սոուսի տեսքով) շատ երկար ժամանակ օգտագործվել է ճապոնական և չինական խոհանոցում։ Ըստ այդմ՝ հարց առաջացավ՝ ինչո՞ւ են դրանք այդքան համեղ և ինչո՞ւ է այս համն այդքան տարբերվում ստանդարտ համերից։ Այնուհետև հայտնաբերվեցին գլյուտամատային ընկալիչներ, և այնուհետև գլյուտամատն արդեն օգտագործվում էր գրեթե մաքուր ձևով (E620, E621 - մոնոսոդիումի գլուտամատ), որպեսզի այն ավելացնեն սննդի լայն տեսականի: Երբեմն պատահում է, որ գլուտամատը մեղադրվում է բոլոր մահկանացու մեղքերի մեջ, որոնք կոչվում են «հաջորդ սպիտակ մահ»՝ աղ, շաքար և գլյուտամատ՝ սպիտակ մահ: Սա, իհարկե, խիստ ուռճացված է, քանի որ ևս մեկ անգամ կրկնում եմ. օրվա ընթացքում մենք ուտում ենք 5-ից 10 գրամ գլյուտամատ և գլուտամինաթթու սովորական կերակուրով։ Այսպիսով, եթե դուք մի քիչ գլուտամատ ավելացնեք ձեր սննդի մեջ՝ այդ մսային համը ստեղծելու համար, ապա դրանում ոչ մի վատ բան չկա, թեև, իհարկե, ավելցուկը լավ չէ։
Իրոք, կան բազմաթիվ ընկալիչներ գլյուտամատի համար (մոտ 10 տեսակի ընկալիչներ), որոնք տարբեր արագությամբ փոխանցում են գլյուտամատային ազդանշանները։ Իսկ այդ ընկալիչները ուսումնասիրվում են առաջին հերթին հիշողության մեխանիզմների վերլուծության տեսանկյունից։ Երբ մեր ուղեղում և կեղևում մեծ կիսագնդերհիշողություն է առաջանում, սա իսկապես նշանակում է, որ ինչ-որ տեղեկատվական հոսք փոխանցող նյարդային բջիջների միջև սինապսները սկսում են ավելի ակտիվ աշխատել: Սինապսի ակտիվացման հիմնական մեխանիզմը գլյուտամատային ընկալիչների արդյունավետության բարձրացումն է։ Վերլուծելով տարբեր գլյուտամատային ընկալիչները՝ մենք տեսնում ենք, որ տարբեր ընկալիչներ տարբեր կերպ են փոխում իրենց արդյունավետությունը: Հավանաբար ամենաշատ ուսումնասիրվածները, այսպես կոչված, NMDA ընկալիչներն են: Սա հապավում է և նշանակում է N-methyl-D-aspartate: Այս ընկալիչը արձագանքում է գլյուտամատին և NMDA-ին: NMDA ընկալիչը բնութագրվում է նրանով, որ այն ունակ է արգելափակվել մագնեզիումի իոնով, և եթե մագնեզիումի իոնը կցված է ընկալիչին, ապա այդ ընկալիչը չի գործում: Այսինքն՝ դուք ստանում եք սինապս, որն ունի ընկալիչներ, բայց այդ ընկալիչները անջատված են։ Եթե ինչ-որ ուժեղ, նշանակալի ազդանշան է անցել նեյրոնային ցանցով, ապա մագնեզիումի իոնները (նաև կոչվում են մագնեզիումի խրոցակներ) անջատվում են NMDA ընկալիչից, և սինապսը բառացիորեն անմիջապես սկսում է աշխատել մի քանի անգամ ավելի արդյունավետ: Տեղեկատվության փոխանցման մակարդակում դա պարզապես նշանակում է հիշողության որոշակի հետքի գրանցում: Մեր ուղեղում կա հիպոկամպուս կոչվող կառուցվածք, պարզապես կան շատ նման սինապսներ NMDA ընկալիչներով, իսկ հիպոկամպը, թերեւս, ամենաուսումնասիրված կառուցվածքն է հիշողության մեխանիզմների առումով:
Բայց NMDA ընկալիչները, մագնեզիումի խցանի տեսքն ու հեռանալը կարճաժամկետ հիշողության մեխանիզմ են, քանի որ խրոցը կարող է հեռանալ և հետո վերադառնալ, այդ դեպքում մենք ինչ-որ բան կմոռանանք: Եթե երկարաժամկետ հիշողություն է ձևավորվում, այնտեղ ամեն ինչ շատ ավելի բարդ է, և այնտեղ աշխատում են այլ տեսակի գլյուտամատային ընկալիչներ, որոնք ունակ են ազդանշան փոխանցել նյարդային բջջի թաղանթից անմիջապես միջուկային ԴՆԹ-ին։ Եվ ստանալով այս ազդանշանը՝ միջուկային ԴՆԹ-ն հրահրում է գլուտամինաթթվի լրացուցիչ ընկալիչների սինթեզը, և այդ ընկալիչները մտնում են սինապտիկ թաղանթների մեջ, և սինապսը սկսում է ավելի արդյունավետ աշխատել: Բայց դա անմիջապես տեղի չի ունենում, ինչպես մագնեզիումի խրոցը տապալելու դեպքում, այլ պահանջում է մի քանի ժամ, պահանջում է կրկնություններ: Բայց եթե դա եղել է, ապա լրջորեն և երկար ժամանակ, և սա մեր երկարաժամկետ հիշողության հիմքն է։
Իհարկե, դեղաբանները օգտագործում են գլյուտամատային ընկալիչները ուղեղի տարբեր գործառույթների վրա ազդելու համար, հիմնականում՝ նվազեցնելու նյարդային համակարգի գրգռումը: Շատ հայտնի դեղամիջոցը կոչվում է կետամին: Այն աշխատում է որպես անզգայացնող նյութ: Կետամինը, բացի այդ, հայտնի է որպես թմրամիջոցի ազդեցությամբ մոլեկուլ, քանի որ հալյուցինացիաները հաճախ առաջանում են անզգայացումից դուրս գալու ժամանակ, հետևաբար կետամինը կոչվում է նաև հալյուցինոգեն, հոգեներգործուն գործողության դեղամիջոց, որի հետ աշխատելը շատ դժվար է: Բայց դեղագիտության մեջ դա հաճախ է պատահում. մի նյութ, որը էական է դեղ, ունի որոշ կողմնակի ազդեցություններ, որոնք, ի վերջո, հանգեցնում են նրան, որ այս նյութի բաշխումն ու օգտագործումը պետք է խիստ վերահսկվի:
Մեկ այլ մոլեկուլ, որը շատ լավ հայտնի է գլուտամատի հետ կապված, մեմանտինն է, մի նյութ, որը կարող է բավականին մեղմ արգելափակել NMDA ընկալիչները և, որպես հետևանք, նվազեցնել ուղեղային ծառի կեղևի ակտիվությունը տարբեր գոտիներում: Մեմանտինը օգտագործվում է տարբեր իրավիճակներում: Դրա դեղատան անվանումն է Ակատինոլ։ Այն օգտագործվում է ընդհանուր գրգռման մակարդակն իջեցնելու համար՝ նվազեցնելու էպիլեպտիկ նոպաների հավանականությունը, և, հավանաբար, մեմանտինի ամենաակտիվ օգտագործումը նեյրոդեգեներացիոն իրավիճակներում և Ալցհեյմերի հիվանդության դեպքում է:
Պատմականորեն առաջին հայտնաբերված նեյրոհաղորդիչները ացետիլխոլինն ու մոնոամիններն էին: Դա պայմանավորված է ծայրամասային նյարդային համակարգում դրանց լայն տարածմամբ (առնվազն ացետիլխոլինի և նորէպինեֆրինի դեպքում): Այնուամենայնիվ, նրանք հեռու են կենտրոնական նյարդային համակարգի ամենատարածված միջնորդներից: Ուղեղի և ողնուղեղի նյարդային բջիջների ավելի քան 80%-ն օգտագործում է ամինաթթուներ որպես միջնորդներ, որոնք փոխանցում են զգայական, շարժիչ և այլ ազդանշանների մեծ մասը նեյրոնային ցանցերի երկայնքով (գրգռող ամինաթթուներ), ինչպես նաև վերահսկում են այս փոխանցումը (արգելակող ամինաթթուներ) . Կարելի է ասել, որ ամինաթթուները գիտակցում են տեղեկատվության արագ փոխանցումը, մինչդեռ մոնոամինները և ացետիլխոլինը ստեղծում են ընդհանուր մոտիվացիոն և հուզական ֆոն և «դիտարկում» զգոնության մակարդակը։ Գոյություն ունեն նույնիսկ ուղեղի գործունեության կարգավորման ավելի «դանդաղ» մակարդակներ՝ դրանք նեյրոպեպտիդների համակարգեր են և հորմոնալ ազդեցություն կենտրոնական նյարդային համակարգի վրա:
Մոնոամինների առաջացման համեմատ՝ ամինաթթուների միջնորդների սինթեզը բջջի համար ավելի պարզ գործընթաց է, և բոլորն էլ պարզ են քիմիական կազմով։ Այս խմբի միջնորդները բնութագրվում են սինապտիկ էֆեկտների ավելի մեծ յուրահատկությամբ. կամ գրգռիչ հատկությունները (գլուտամին և ասպարտիկ թթուներ), կամ արգելակող հատկությունները (գլիցին և գամմա-ամինաբուտիրաթթու - GABA) բնորոշ են որոշակի միացությանը: Ամինաթթուների ագոնիստներն ու անտագոնիստներն ավելի կանխատեսելի ազդեցություն են ունենում կենտրոնական նյարդային համակարգի վրա, քան ացետիլխոլինի և մոնոամինի ագոնիստներն ու հակառակորդները: Մյուս կողմից, գլյուտամատային կամ GABA-ergic համակարգերի վրա ազդեցությունը հաճախ հանգեցնում է ամբողջ կենտրոնական նյարդային համակարգի չափազանց «լայն» փոփոխությունների, ինչը ստեղծում է իր դժվարությունները:
Կենտրոնական նյարդային համակարգի հիմնական գրգռիչ միջնորդն է գլուտամիկ թթու.Նյարդային հյուսվածքում գլուտամինաթթվի և նրա պրեկուրսոր գլուտամինի փոխադարձ փոխակերպումները հետևյալն են.
Որպես սննդային ոչ էական ամինաթթու, այն լայնորեն տարածված է սպիտակուցների լայն տեսականիով, և դրա օրական ընդունումը կազմում է առնվազն 5-10 գ: Այնուամենայնիվ, սննդային գլյուտամինաթթուն սովորաբար շատ թույլ է ներթափանցում արյուն-ուղեղային պատնեշը, ինչը մեզ պաշտպանում է լուրջ հիվանդություններից: ուղեղի գործունեության խանգարումներ. Կենտրոնական նյարդային համակարգի համար պահանջվող գրեթե ամբողջ գլուտամատը սինթեզվում է անմիջապես նյարդային հյուսվածքում, բայց իրավիճակը բարդանում է նրանով, որ այս նյութը նաև միջբջջային ամինաթթուների նյութափոխանակության գործընթացների միջանկյալ փուլն է: Հետեւաբար, նյարդային բջիջները պարունակում են մեծ քանակությամբ գլուտամինաթթու, որի միայն մի փոքր մասն է կատարում միջնորդի գործառույթներ։ Նման գլյուտամատի սինթեզը տեղի է ունենում նախասինապտիկ տերմինալներում. Հիմնական պրեկուրսորի աղբյուրը ամինաթթու գլուտամինն է:
Ազատվելով սինապտիկ ճեղքում՝ միջնորդը գործում է համապատասխան ընկալիչների վրա։ Գլուտամինաթթվի ընկալիչների բազմազանությունը չափազանց մեծ է: Ներկայումս կան երեք տեսակի իոնոտրոպ և մինչև ութ տեսակի մետաբոտրոֆ ընկալիչներ: Վերջիններս քիչ տարածված են և քիչ ուսումնասիրված։ Դրանց ազդեցությունը կարող է իրականացվել ինչպես ացենիլատ ցիկլազի ակտիվությունը ճնշելու, այնպես էլ դիացիլգլիցերինի և ինոզիտոլ տրիֆոսֆատի ձևավորման ուժեղացման միջոցով:
Գլուտամինաթթվի իոնոտրոպ ընկալիչները անվանվել են հատուկ ագոնիստներից՝ NMDA ընկալիչները (N-methyl-D-aspartate ագոնիստ), AMPA ընկալիչները (ալֆա-ամինոհիդրօքսիմեթիլիզոքսանոլպրոպիոնաթթվի ագոնիստ) և կաինատը (կաինաթթվի ագոնիստ): Այսօր ամենաշատ ուշադրությունն է դարձվում դրանցից առաջինին։ NMDA ընկալիչները լայնորեն տարածված են կենտրոնական նյարդային համակարգում ողնուղեղից մինչև ուղեղի կեղև, որոնց մեծ մասը հիպոկամպում է: Ռեցեպտորը (նկ. 3.36) բաղկացած է չորս ենթամիավոր սպիտակուցներից, որոնք ունեն գլուտամինաթթվի միացման երկու ակտիվ տեղամաս։ 1 և գլիցինի միացման երկու ակտիվ տեղամաս 2. Ձևավորվում են նույն սպիտակուցները իոնային ալիքորը կարող է արգելափակվել մագնեզիումի իոնով 3 և ալիքների արգելափակումներ 4.
Ասույթը վերաբերում է այն միջնորդի ճակատագրին, ով կատարել է իր դերը ազդանշանի փոխանցման գործում՝ մավրն արել է իր գործը՝ մավրը պետք է հեռանա։ Եթե հաղորդիչը մնում է հետսինապտիկ մեմբրանի վրա, այն խանգարում է նոր ազդանշանների փոխանցմանը։ Օգտագործված հաղորդիչի մոլեկուլները վերացնելու մի քանի մեխանիզմներ կան՝ դիֆուզիոն, ֆերմենտային դեգրադացիա և վերաօգտագործում:
Դիֆուզիայի միջոցով միջնորդ մոլեկուլների մի մասը միշտ դուրս է գալիս սինապտիկ ճեղքվածքից, իսկ որոշ սինապսներում այդ մեխանիզմը գլխավորն է։ Ֆերմենտային դեգրադացիան նյարդամկանային սինապսում ացետիլխոլինի հեռացման հիմնական մեթոդն է. դա անում է խոլինեստերազը, որը կցված է ծայրամասային ափսեի ծալքերի եզրերին: Ստացված ացետատն ու քոլինը հատուկ գրավման մեխանիզմով վերադարձվում են նախասինապտիկ վերջ։
Հայտնի են երկու ֆերմենտներ, որոնք քայքայում են բիոգեն ամինները՝ մոնոամին օքսիդազը (MAO) և կատեխոլ-օ-մեթիլտրանսֆերազը (COMT): Սպիտակուցային նեյրոհաղորդիչների ճեղքումը կարող է տեղի ունենալ արտաբջջային պեպտիդազների ազդեցության ներքո, չնայած սովորաբար այդպիսի միջնորդները սինապսից անհետանում են ավելի դանդաղ, քան ցածր մոլեկուլային քաշը, և հաճախ հեռանում են սինապսից դիֆուզիայի միջոցով:
Նեյրոհաղորդիչների կրկնակի օգտագործումը հիմնված է տարբեր նեյրոհաղորդիչների համար հատուկ մեխանիզմների վրա, որոնք գրավում են իրենց մոլեկուլները և՛ նեյրոնների, և՛ գլիա բջիջների կողմից: Այս գործընթացում ներգրավված են հատուկ տրանսպորտային մոլեկուլներ: Հայտնի են նորեպինեֆրինի, դոֆամինի, սերոտոնինի, գլյուտամատի, GABA-ի, գլիկինի և քոլինի (բայց ոչ ացետիլխոլինի) վերաօգտագործման հատուկ մեխանիզմները: Որոշ հոգեֆարմակոլոգիական նյութեր արգելափակում են հաղորդիչի կրկնակի օգտագործումը (օրինակ՝ կենսագեն ամիններ կամ GABA) և դրանով իսկ երկարացնում դրանց գործողությունը։
Առանձին միջնորդական համակարգեր
Ամենակարևոր նեյրոհաղորդիչների քիմիական կառուցվածքը ներկայացված է Նկար 6.1-ում:
Ացետիլխոլին
Այն ձևավորվում է ացետիլտրանսֆերազ ֆերմենտով ացետիլ կոենզիմ A-ից և քոլինից, որը նեյրոնները չեն սինթեզում, այլ գրավում են սինապտիկ ճեղքվածքից կամ արյունից։ Այն ողնուղեղի և վեգետատիվ գանգլիաների բոլոր շարժողական նեյրոնների միակ միջնորդն է, այդ սինապսներում նրա գործողությունը միջնորդվում է H-խոլիներգիկ ընկալիչների միջոցով, իսկ ալիքների կառավարումն ուղղակի է, իոնոտրոպ։ Ացետիլխոլինն արտազատվում է նաև ինքնավար նյարդային համակարգի պարասիմպաթիկ բաժանման հետգանգլիոնային վերջավորություններով. այստեղ այն կապվում է M-քոլիներգիկ ընկալիչների հետ, այսինքն. գործում է մետաբոտրոֆիկ. Ուղեղում այն օգտագործվում է որպես նեյրոհաղորդիչ կեղևի բազմաթիվ բրգաձև բջիջների կողմից, որոնք գործում են բազալ գանգլիաների վրա, օրինակ՝ ուղեղում արտադրվող ացետիլխոլինի ընդհանուր քանակի մոտավորապես 40%-ը ազատվում է պոչուկային միջուկում: Ուղեղի նշագեղձերը ացետիլխոլինի օգնությամբ գրգռում են գլխուղեղի կեղեւի բջիջները։
Մ-խոլիներգիկ ընկալիչները հայտնաբերված են ուղեղի բոլոր հատվածներում (կեղև, լիմբիկ համակարգի կառուցվածքներ, թալամուս, միջքաղաքային), դրանք հատկապես առատ են ցանցաթաղանթում։ Խոլիներգիկ մանրաթելերի օգնությամբ միջնուղեղը կապվում է ցողունի վերին հատվածների, օպտիկական բլուրների և կեղևի այլ նեյրոնների հետ։ Հավանաբար, այս հատուկ ուղիների ակտիվացումը պահանջվում է քնից արթուն անցնելու համար, ամեն դեպքում, խոլինէսթերազային ինհիբիտորներ ընդունելուց հետո էլեկտրաէնցեֆալոգրամի բնորոշ փոփոխությունները հաստատում են այս տարբերակը:
Պրոգրեսիվ տկարամտության դեպքում, որը հայտնի է որպես Ալցհեյմերի հիվանդություն, բացահայտվել է ացետիլտրանսֆերազային ակտիվության նվազում Մեյներտի միջուկների նեյրոններում, որոնք տեղակայված են բազալային նախաուղեղում, անմիջապես ստրիատի տակ: Այս առումով խոլիներգիկ փոխանցումը խաթարված է, որը համարվում է հիվանդության զարգացման կարեւոր օղակ։
Ացետիլխոլինի հակառակորդները, ինչպես ցույց են տվել կենդանիների փորձերը, խոչընդոտում են պայմանավորված ռեֆլեքսների ձևավորմանը և նվազեցնում մտավոր գործունեության արդյունավետությունը: Խոլինեստերազի ինհիբիտորները հանգեցնում են ացետիլխոլինի կուտակմանը, որն ուղեկցվում է կարճաժամկետ հիշողության բարելավմամբ, պայմանավորված ռեֆլեքսների արագացված ձևավորմամբ և հիշողության հետքերի ավելի լավ պահպանմամբ։
Այն գաղափարը, որ ուղեղի խոլիներգիկ համակարգերը չափազանց անհրաժեշտ են նրա ինտելեկտուալ գործունեության իրականացման և հույզերի տեղեկատվական բաղադրիչի ապահովման համար, բավականին տարածված է:
Կենսածին ամիններ
Ինչպես արդեն նշվեց, կենսագեն ամինները սինթեզվում են թիրոզինից, և սինթեզի յուրաքանչյուր փուլ կառավարվում է հատուկ ֆերմենտի միջոցով։ Եթե բջիջն ունի նման ֆերմենտների ամբողջական հավաքածու, ապա այն կարտացոլի ադրենալին և, ավելի քիչ, նրա պրեկուրսորները՝ նորեպինեֆրինը և դոֆամինը: Օրինակ, այսպես կոչված. Վերերիկամային մեդուլլայի քրոմաֆինային բջիջները արտազատում են ադրենալին (սեկրեցիայի 80%), նորեպինեֆրին (18%) և դոֆամին (2%): Եթե չկա ադրենալինի ձևավորման ֆերմենտ, ապա բջիջը կարող է արտազատել միայն նորեպինեֆրին և դոֆամին, իսկ եթե նորէպինեֆրինի սինթեզի համար անհրաժեշտ ֆերմենտ չկա, ապա միակ ազատվող միջնորդը կլինի դոֆամինը, որի նախադրյալը՝ L- DOPA-ն չի օգտագործվում որպես միջնորդ:
Դոպամինը, նորէպինեֆրինը և էպինեֆրինը հաճախ կոչվում են կատեխոլամիններ: Նրանք վերահսկում են մետաբոտրոֆիկ ադրեներգիկ ընկալիչները, որոնք հայտնաբերված են ոչ միայն նյարդային, այլև մարմնի այլ հյուսվածքներում։ Ադրեներգիկ ընկալիչները բաժանվում են ալֆա-1 և ալֆա-2, բետա-1 և բետա-2. տարբեր ընկալիչներին կատեխոլամինների միացման հետևանքով առաջացած ֆիզիոլոգիական ազդեցությունները զգալիորեն տարբերվում են: Տարբեր ընկալիչների հարաբերակցությունը նույնը չէ տարբեր էֆեկտոր բջիջների համար: Բոլոր կատեխոլամինների համար ընդհանուր ադրեներգիկ ընկալիչների հետ մեկտեղ կան դոֆամինի հատուկ ընկալիչներ, որոնք հայտնաբերված են կենտրոնական նյարդային համակարգում և այլ հյուսվածքներում, ինչպիսիք են արյան անոթների հարթ մկանները և սրտի մկանները:
Ադրենալինը մակերիկամի մեդուլլայի հիմնական հորմոնն է, որի նկատմամբ հատկապես զգայուն են բետա-ընկալիչները։ Տեղեկություններ կան նաև ուղեղի որոշ բջիջների կողմից որպես միջնորդ ադրենալինի օգտագործման մասին։ Նորէպինեֆրինն արտազատվում է ինքնավար նյարդային համակարգի սիմպաթիկ բաժանման հետգանգլիոնային նեյրոնների կողմից, իսկ կենտրոնական նյարդային համակարգում՝ ողնուղեղի, ուղեղի և ուղեղի կեղևի առանձին նեյրոնների կողմից: Նորադրեներգիկ նեյրոնների ամենամեծ կուտակումը ներկայացված է կապույտ բծերով՝ ուղեղի ցողունի միջուկներով:
Ենթադրվում է, որ պարադոքսալ քնի փուլի սկիզբը կապված է այս նորադրեներգիկ նեյրոնների գործունեության հետ, սակայն նրանց գործառույթը միայն սրանով չի սահմանափակվում։ Կան նաև նորադրեներգիկ նեյրոններ՝ դեպի կապույտ բծերը, որոնց չափից ավելի ակտիվությունը առաջատար դեր է խաղում այսպես կոչված զարգացման գործում. խուճապի համախտանիշ, որն ուղեկցվում է ճնշող սարսափի զգացումով.
Դոպամինը սինթեզվում է միջին ուղեղի և դիէնցեֆալային շրջանի նեյրոնների կողմից, որոնք կազմում են ուղեղի երեք դոպամիներգիկ համակարգերը։ Սա, առաջին հերթին, նեգրոստրիատալ համակարգն է. այն ներկայացված է միջին ուղեղի նիգրայի նեյրոններով, որոնց աքսոններն ավարտվում են պոչավոր միջուկներով և թաղանթով։ Երկրորդ, սա մեզոլիմբիկ համակարգն է, որը ձևավորվում է պոնսի որովայնային օպերկուլի նեյրոնների կողմից, նրանց աքսոնները նյարդայնացնում են միջնապատը, նշագեղձերը, ճակատային ծառի կեղևի մի մասը, այսինքն. ուղեղի լիմբիկ համակարգի կառուցվածքները. Եվ, երրորդ, մեզոկորտիկային համակարգը. նրա նեյրոնները գտնվում են միջին ուղեղում, իսկ նրանց աքսոններն ավարտվում են առջևի ցինկուլային գիրուսով, ճակատային ծառի կեղևի խորը շերտերով, էնտորինալ և պիրիֆորմ (տանձաձև) կեղևով: Դոպամինի ամենաբարձր կոնցենտրացիան հայտնաբերվում է ճակատային ծառի կեղևում:
Դոպամիներգիկ կառույցները կարևոր դեր են խաղում դրդապատճառների և հույզերի ձևավորման, ուշադրության պահպանման մեխանիզմների և ծայրամասից կենտրոնական նյարդային համակարգ մուտք գործող ամենակարևոր ազդանշանների ընտրության գործում: Նիգրա սուբստանցիայի նեյրոնների դեգեներացիան հանգեցնում է շարժման խանգարումների համալիրի, որը հայտնի է որպես Պարկինսոնի հիվանդություն: Այս հիվանդության բուժման համար օգտագործվում է դոֆամինի պրեկուրսորը՝ L-DOPA-ն, որը, ի տարբերություն բուն դոֆամինի, ունակ է անցնել արյունաուղեղային պատնեշը։ Որոշ դեպքերում փորձեր են արվում բուժել Պարկինսոնի հիվանդությունը՝ պտղի վերերիկամային մեդուլլայի հյուսվածքը ուղեղային փորոքի մեջ ներարկելով։ Ներարկված բջիջները կարող են գոյատևել մինչև մեկ տարի և դեռ արտադրել զգալի քանակությամբ դոֆամին:
Շիզոֆրենիայի դեպքում հայտնաբերվում է մեզոլիմբիկ և մեզոկորտիկ համակարգերի ակտիվության բարձրացում, որը շատերի կողմից համարվում է ուղեղի վնասման հիմնական մեխանիզմներից մեկը: Ի հակադրություն, այսպես կոչված. հիմնական դեպրեսիան պետք է օգտագործի դեղամիջոցներ, որոնք մեծացնում են կատեխոլամինների կոնցենտրացիան կենտրոնական նյարդային համակարգի սինապսներում: Հակադեպրեսանտներն օգնում են շատ հիվանդների, բայց, ցավոք, նրանք չեն կարող ուրախացնել առողջ մարդկանց, ովքեր պարզապես դժբախտ ժամանակ են ապրում իրենց կյանքում:
Սերոտոնին
Այս ցածր մոլեկուլային քաշի նեյրոհաղորդիչը ձևավորվում է տրիպտոֆան ամինաթթուից երկու ֆերմենտների կողմից, որոնք ներգրավված են սինթեզում: Կարի միջուկներում հայտնաբերվում են սերոտոներգիկ նեյրոնների զգալի կուտակումներ՝ բարակ շերտ՝ պոչային ցանցանման գոյացության միջնագծի երկայնքով։ Այս նեյրոնների գործառույթը կապված է ուշադրության մակարդակի կարգավորման և քուն-արթուն ցիկլի կարգավորման հետ։ Սերոտոնիներգիկ նեյրոնները փոխազդում են մակուլայի պոնսի տեգմենտային և նորադրեներգիկ նեյրոնների քոլիներգիկ կառուցվածքների հետ: Սերոտոնիներգիկ ընկալիչների արգելափակողներից մեկը LSD-ն է, այս հոգեմետ նյութի ընդունման արդյունքը նման զգայական ազդանշանների գիտակցություն անխոչընդոտ անցումն է, որոնք սովորաբար ուշանում են:
Հիստամին
Կենսածին ամինների խմբի այս նյութը սինթեզվում է ամինաթթու հիստիդինից և ամենամեծ քանակությամբ հայտնաբերվում է մաստ բջիջներում և արյան բազոֆիլ գրանուլոցիտներում. այնտեղ հիստամինը մասնակցում է տարբեր գործընթացների կարգավորմանը, ներառյալ անմիջապես ալերգիկ ռեակցիաների ձևավորումը: . Անողնաշարավորների մոտ սա բավականին տարածված հաղորդիչ է, մարդկանց մոտ այն օգտագործվում է որպես հիպոթալամուսի նյարդային հաղորդիչ, որտեղ այն մասնակցում է էնդոկրին ֆունկցիաների կարգավորմանը:
Գլուտամատ
Ուղեղի ամենատարածված գրգռիչ նեյրոհաղորդիչը: Այն արտազատվում է զգայական նեյրոնների մեծ մասի աքսոններով, տեսողական ծառի կեղևի բրգաձեւ բջիջներով և ասոցիատիվ ծառի կեղևի նեյրոններով, որոնք ձևավորում են պրոեկցիաներ ստրիատի վրա:
Այս միջնորդի ընկալիչները բաժանվում են իոնոտրոպային և մետաբոտրոպային: Ionotropic glutamate ընկալիչները բաժանվում են երկու տեսակի՝ կախված իրենց ագոնիստներից և հակառակորդներից՝ NMDA (N-methyl-D-aspartate) և ոչ NMDA: NMDA ընկալիչները կապված են կատիոնային ալիքների հետ, որոնց միջոցով կարող են հոսել նատրիումի, կալիումի և կալցիումի իոնները, իսկ ոչ NMDA ընկալիչների ալիքները թույլ չեն տալիս կալցիումի իոններին անցնել: Կալցիումը, ներթափանցելով NMDA ընկալիչների ուղիներով, ակտիվացնում է կալցիումից կախված երկրորդային սուրհանդակների կասկադը: Ենթադրվում է, որ այս մեխանիզմը շատ կարևոր դեր է խաղում հիշողության հետքերի ձևավորման գործում։ NMDA ընկալիչների հետ կապված ալիքները բացվում են դանդաղ և միայն գլիցինի առկայության դեպքում. դրանք արգելափակված են մագնեզիումի իոններով և թմրամիջոցների հալյուցինոգեն ֆենցիկլիդինով (որը անգլիական գրականության մեջ կոչվում է «հրեշտակի փոշի»):
Հիպոկամպում NMDA ընկալիչների ակտիվացումը կապված է շատ հետաքրքիր երևույթի առաջացման հետ՝ երկարաժամկետ հզորացում, նեյրոնային գործունեության հատուկ ձև, որն անհրաժեշտ է երկարաժամկետ հիշողության ձևավորման համար (տե՛ս գլ. 17): Հետաքրքիր է նաև այն փաստը, որ գլյուտամատի չափազանց բարձր կոնցենտրացիան թունավոր է նեյրոնների համար. այս հանգամանքը պետք է հաշվի առնել ուղեղի որոշ վնասվածքների դեպքում (արյունազեղումներ, էպիլեպտիկ նոպաներ, դեգեներատիվ հիվանդություններ, օրինակ՝ Հանթինգթոնի խորեա):
GABA և գլիցին
Երկու ամինաթթուների նյարդային հաղորդիչները էական արգելակող միջնորդներ են: Գլիցինը արգելակում է ողնուղեղի միջնեյրոնների և շարժողական նեյրոնների գործունեությունը։ GABA-ի բարձր կոնցենտրացիան հայտնաբերվում է ուղեղային ծառի կեղևի մոխրագույն նյութում, հատկապես ճակատային բլթերում, ենթակեղևային միջուկներում (caudate և pallidum), թալամուսում, հիպոկամպում, հիպոթալամուսում և ցանցաթաղանթում: Ողնուղեղի, հոտառական ուղիների, ցանցաթաղանթի և ուղեղիկի որոշ նեյրոններ օգտագործվում են որպես GABA-ի արգելակող միջնորդ:
GABA-ից ստացված մի շարք միացություններ (պիրացետամ, ամինոլոն, նատրիումի օքսիբուտիրատ կամ GHB - գամմա-հիդրօքսիբուտիրաթթու) խթանում են ուղեղի կառուցվածքների հասունացումը և նեյրոնային պոպուլյացիաների միջև կայուն կապերի ձևավորումը: Սա նպաստում է հիշողության ձևավորմանը, ինչն էլ պատճառ հանդիսացավ կլինիկական պրակտիկայում այս միացությունների օգտագործմանը՝ ուղեղի տարբեր վնասվածքներից հետո վերականգնման գործընթացներն արագացնելու համար։
Ենթադրվում է, որ GABA-ի հոգեմետ ակտիվությունը որոշվում է նրա ընտրողական ազդեցությամբ ուղեղի ինտեգրացիոն ֆունկցիաների վրա, որը բաղկացած է ուղեղի փոխազդող կառույցների գործունեության հավասարակշռության օպտիմալացումից: Այսպես, օրինակ, վախի, ֆոբիաների պայմաններում հիվանդներին օգնում են հատուկ հակաապահովագրական դեղամիջոցները՝ բենզոդիազեպինները, որոնց գործողությունը GABA-ergic ընկալիչների զգայունության բարձրացումն է։
Նեյրոպեպտիդներ
Ներկայումս մոտ 50 պեպտիդներ համարվում են հնարավոր նեյրոհաղորդիչներ, որոնցից մի քանիսը նախկինում հայտնի էին որպես նյարդահորմոններ, որոնք արտազատվում են նեյրոնների կողմից, բայց գործում են ուղեղից դուրս՝ վազոպրեսին, օքսիտոցին: Այլ նեյրոպեպտիդներն առաջին անգամ ուսումնասիրվել են որպես մարսողական համակարգի տեղական հորմոններ, օրինակ՝ գաստրին, խոլեցիստոկինին և այլն, ինչպես նաև այլ հյուսվածքներում ձևավորված հորմոններ՝ անգիոտենզին, բրադիկինին և այլն։
Նրանց գոյությունը նույն որակով դեռ կասկածի ենթակա չէ, բայց երբ հնարավոր է հաստատել, որ որոշակի պեպտիդ է արտազատվում նյարդային վերջավորությամբ և գործում է հարևան նեյրոնի վրա, այն արդարացիորեն վերագրվում է նեյրոհաղորդիչներին: Ուղեղում զգալի քանակությամբ նեյրոպեպտիդներ օգտագործվում են հիպոթալամիկ-հիպոֆիզային համակարգում, թեև, օրինակ, պեպտիդների ֆունկցիան ողնուղեղի հետևի եղջյուրներում ցավի զգայունության փոխանցման գործում պակաս հայտնի չէ:
Բոլոր պեպտիդները ծագում են մեծ պրեկուրսորային մոլեկուլներից, որոնք սինթեզվում են բջջային մարմնում, փոխվում են ցիտոպլազմային ցանցում, փոխակերպվում Գոլջիի ապարատում և փոխանցվում նյարդային վերջավորության՝ արագ աքսոնային փոխադրմամբ սեկրետորային վեզիկուլներում: Նեյրոպեպտիդները կարող են հանդես գալ որպես գրգռիչ և արգելակող միջնորդներ: Նրանք հաճախ իրենց նեյրոմոդուլյատորների նման են պահում, այսինքն. իրենք չեն փոխանցում ազդանշանը, այլ, կախված անհրաժեշտությունից, ավելացնում կամ նվազեցնում են առանձին նեյրոնների կամ դրանց պոպուլյացիաների զգայունությունը գրգռիչ կամ արգելակող նեյրոհաղորդիչների գործողության նկատմամբ:
Ամինաթթուների շղթայի նմանատիպ մասերը կարող են օգտագործվել առանձին նեյրոպեպտիդների նմանությունները հայտնաբերելու համար: Օրինակ, բոլոր էնդոգեն օփիատ պեպտիդները շղթայի մի ծայրում ունեն նույն ամինաթթուների հաջորդականությունը՝ թիրոզին-գլիցին-գլիցին-ֆենիլալանին: Հենց այս տեղանքն է պեպտիդային մոլեկուլի ակտիվ կենտրոնը։ Հաճախ առանձին պեպտիդների նման նմանությունների հայտնաբերումը ցույց է տալիս նրանց գենետիկական կապը: Այս հարաբերությունների համաձայն՝ նեյրոակտիվ պեպտիդների մի քանի հիմնական ընտանիքներ են հայտնաբերվել.
1. Օփիատային պեպտիդներ՝ լեյցին-էնկեֆալին, մեթիոնին-էնկեֆալին, ալֆա-էնդորֆին, գամմա-էնդորֆին, բետա-էնդորֆին, դինորֆին, ալֆա-նեոէնդորֆին:
2. Նեյրոհիպոֆիզի պեպտիդներ՝ վազոպրեսին, օքսիտոցին, նեյրոֆիզին։
3. Տախիկինիններ՝ P նյութ, բումեզին, ֆիզալեմին, կասինին, ուպերոլեյն, էլեդոիզին, Կ նյութ։
4. Սեկրետիններ՝ սեկրեցին, գլյուկագոն, VIP (վազոակտիվ աղիքային պեպտիդ), սոմատոտրոպինի ազատման գործոն։
5. Ինսուլիններ՝ ինսուլին, ինսուլինանման մանրէային գործոններ I և II:
6. Սոմատոստատին. սոմատոստատին, ենթաստամոքսային գեղձի պոլիպեպտիդ:
7. Գաստրիններ՝ գաստրին, խոլեցիստոկինին։
Որոշ նեյրոններ կարող են միաժամանակ արձակել պեպտիդ և ցածր մոլեկուլային քաշի միջնորդներ, օրինակ՝ ացետիլխոլին և VIP, որոնք երկուսն էլ գործում են նույն թիրախի վրա, ինչ սիներգիստները: Բայց դա կարող է տարբեր լինել, ինչպես, օրինակ, հիպոթալամուսում, որտեղ մեկ նեյրոնի կողմից արտազատվող գլուտամատը և դինորֆինը գործում են մեկ հետսինապտիկ թիրախի վրա, բայց գլուտամատը հուզում է, իսկ օփիոիդ պեպտիդը արգելակում է: Ամենայն հավանականությամբ պեպտիդները նման դեպքերում գործում են որպես նեյրոմոդուլատորներ: Երբեմն նեյրոհաղորդիչի հետ միասին արտազատվում է նաև ATP-ն, որը որոշ սինապսներում նույնպես համարվում է միջնորդ, եթե, իհարկե, հնարավոր է ապացուցել դրա համար ընկալիչների առկայությունը հետսինապտիկ թաղանթում։
Օփիատային պեպտիդներ
Օփիատային պեպտիդների ընտանիքը պարունակում է ավելի քան մեկ տասնյակ նյութեր, որոնց մոլեկուլները պարունակում են 5-ից 31 ամինաթթուներ: Այս նյութերն ունեն ընդհանուր կենսաքիմիական բնութագրեր, թեև դրանց սինթեզի ուղիները կարող են տարբեր լինել: Օրինակ, բետա-էնդորֆինի սինթեզը կապված է ադրենոկորտիկոտրոպ հորմոնի (ACTH) ձևավորման հետ ընդհանուր մեծ նախադրյալ սպիտակուցի մոլեկուլից՝ պրոոպիոմելանոկորտինից, մինչդեռ էնկեֆալինները ձևավորվում են մեկ այլ պրեկուրսորից, իսկ դինորֆինը երրորդից:
Ափիոնային պեպտիդների որոնումը սկսվել է այն բանից հետո, երբ հայտնաբերվեցին ուղեղում ափիոնի ալկալոիդները (մորֆին, հերոին և այլն) կապող օփիատային ընկալիչները: Քանի որ դժվար է պատկերացնել նման ընկալիչների հայտնվելը միայն օտար նյութերը կապելու համար, նրանք սկսեցին դրանք փնտրել մարմնի ներսում: 1975-ին «Nature» ամսագիրը զեկուցեց երկու փոքր պեպտիդների հայտնաբերման մասին, որոնք բաղկացած էին հինգ ամինաթթուներից, կապված ափիոնային ընկալիչների հետ և ավելի ուժեղ էին գործում, քան մորֆինը: Այս հաղորդագրության հեղինակները (Hughes J., Smith T.W., Kosterlitz H.W. և ուրիշներ) հայտնաբերված նյութերն անվանել են enkephalins (այսինքն՝ գլխում): Կարճ ժամանակ անց հիպոթալամո-հիպոֆիզի էքստրակտից մեկուսացվեցին ևս երեք պեպտիդներ, որոնք կոչվում էին էնդորֆիններ, այսինքն. էնդոգեն մորֆիններ, ապա հայտնաբերվել է դինորֆին և այլն։
Բոլոր ափիոնային պեպտիդները երբեմն կոչվում են էնդորֆիններ: Նրանք ավելի լավ են կապվում ափիոնային ընկալիչների հետ, քան մորֆինը և 20-700 անգամ ավելի հզոր են, քան մորֆինը: Նկարագրված են ափիոնային ընկալիչների հինգ ֆունկցիոնալ տեսակներ, որոնք պեպտիդների հետ միասին կազմում են շատ բարդ համակարգ: Պեպտիդի կցումը ընկալիչին հանգեցնում է cAMP համակարգի հետ կապված երկրորդական սուրհանդակների ձևավորմանը։
Օփիոիդային պեպտիդների ամենաբարձր պարունակությունը հայտնաբերվում է հիպոֆիզի գեղձում, սակայն դրանք սինթեզվում են հիմնականում հիպոթալամուսում։ Բետա-էնդորֆինի զգալի քանակությունը հայտնաբերվում է ուղեղի լիմբիկ համակարգում, իսկ արյան մեջ: Էնկեֆալինների կոնցենտրացիան հատկապես բարձր է ողնուղեղի հետևի եղջյուրներում, որտեղ փոխանցվում են ցավի վերջավորության ազդանշանները. այնտեղ էնկեֆալինները նվազեցնում են P նյութի արտազատումը, որը միջնորդ է ցավի մասին տեղեկատվության փոխանցման համար:
Փորձարարական կենդանիների մոտ անզգայացում կարող է առաջանալ ուղեղի փորոքի մեջ բետա-էնդորֆինի միկրոներարկումով: Ցավը թեթևացնելու մեկ այլ մեթոդ է փորոքի շուրջ տեղակայված նեյրոնների էլեկտրական խթանումը. սա մեծացնում է էնդորֆինների և էնկեֆալինների կոնցենտրացիան ողնուղեղային հեղուկում: Նույն արդյունքին, այսինքն. բ-էնդորֆինների ներմուծումը և պերիփորոքային (պերփորոքային) շրջանի խթանումը քաղցկեղով հիվանդների մոտ հանգեցրել են անզգայացման: Հետաքրքիր է, որ ափիոնային պեպտիդների մակարդակը ողնուղեղային հեղուկում մեծանում է ինչպես ասեղնաբուժությամբ, այնպես էլ պլացեբոյի էֆեկտով (երբ հիվանդը ընդունում է դեղը, չիմանալով, որ դրա մեջ ակտիվ ակտիվ սկզբունք չկա):
Ի լրումն անալգետիկ, i.e. Օփիոիդային պեպտիդների անալգետիկ ազդեցությունը ազդում է երկարաժամկետ հիշողության ձևավորման, ուսուցման գործընթացի վրա, կարգավորում է ախորժակը, սեռական ֆունկցիան և սեռական վարքը, նրանք կարևոր օղակ են սթրեսի արձագանքման և հարմարվողականության գործընթացում, կապ են ապահովում նյարդային, էնդոկրին համակարգի միջև: և իմունային համակարգերը (ափիոնային ընկալիչները հայտնաբերված են լիմֆոցիտներում և արյան մոնոցիտներում):
Ամփոփում
Կենտրոնական նյարդային համակարգում ինչպես ցածր մոլեկուլային քաշը, այնպես էլ պեպտիդային նյարդային հաղորդիչները օգտագործվում են բջիջների միջև տեղեկատվության փոխանցման համար: Նեյրոնների տարբեր պոպուլյացիաներ օգտագործում են տարբեր նեյրոհաղորդիչներ, այս ընտրությունը որոշվում է գենետիկորեն և ապահովվում է սինթեզի համար անհրաժեշտ ֆերմենտների որոշակի հավաքածուով: Նույն նեյրոհաղորդիչի համար տարբեր բջիջներն ունեն տարբեր տեսակի հետսինապտիկ ընկալիչներ՝ իոնոտրոպ կամ մետաբոտրոֆիկ հսկողությամբ: Մետաբոտրոպային հսկողությունն իրականացվում է փոխակերպող սպիտակուցների մասնակցությամբ և տարբեր համակարգերերկրորդական միջնորդներ. Որոշ նեյրոններ միաժամանակ արտազատում են պեպտիդային միջնորդ ցածր մոլեկուլային քաշի հետ: Նեյրոնները, որոնք տարբերվում են արտազատվող նեյրոհաղորդիչից, որոշակի կարգով կենտրոնացած են ուղեղի տարբեր կառույցներում։
Հարցեր ինքնատիրապետման համար
81. Նշվածներից ո՞րը չափանիշ չէ նյութը նեյրոհաղորդիչ դասակարգելու համար.
Ա. Սինթեզված է նեյրոնում; B. Կուտակվում է նախասինապտիկ վերջավորության մեջ; B. Հատուկ ազդեցություն ունի էֆեկտորի վրա. D. արտազատվում է արյան մեջ; E. Երբ արհեստականորեն կառավարվում է, ազդեցություն է նկատվում, որը նման է բնական արտազատմանը:
Ա. Խոչընդոտում է միջնորդի ազատմանը նախասինապտիկ վերջավորությունից. B. Գործում է որպես միջնորդ. Բ. Գործում է այլ կերպ, քան միջնորդը. Դ. Արգելափակում է հետսինապտիկ ընկալիչները; D. Չի կապում հետսինապտիկ ընկալիչների հետ:
83. Նշվածներից ո՞րն է բնորոշ պեպտիդային նեյրոհաղորդիչներին.
Ա. ձևավորվում է ամինաթթուների ֆերմենտային օքսիդացումով; B. ձևավորվել է ամինաթթուների դեկարբոքսիլացման արդյունքում; Բ. Կարող է սինթեզվել նախասինապտիկ վերջավորությամբ. D. Դանդաղ աքսոպլազմիկ փոխադրման միջոցով փոխանցվել է նախասինապտիկ ծայրին; D. Ձևավորվել է նեյրոնի բջջային մարմնում:
84. Ինչո՞վ է պայմանավորված կալցիումի իոնների հոսանքը դեպի նախասինապտիկ տերմինալ սինապսի միջոցով տեղեկատվության փոխանցման ժամանակ:
Ա. Գործողության ներուժ; Բ. Հանգստի ներուժ; Բ. Էկզոցիտոզ; Դ. Սինապտիկ վեզիկուլների միացում ցիտոկմախքի հետ; D. առաջացման հետսինապտիկ ներուժի.
85. Ի՞նչն է փոխակերպում նախասինապտիկ տերմինալի գրգռումը ոչ էլեկտրական ակտիվության (նեյրոհաղորդիչի ազատում):
Ա. Էկզոցիտոզ; Բ. Կալցիումի իոնների մուտքային հոսանքը; B. Նատրիումի իոնների մուտքը գրգռման ավարտից հետո. D. Կալիումի իոնների արտազատում ռեբևեռացման ժամանակ; D. Միջնորդի սինթեզի համար անհրաժեշտ ֆերմենտների ակտիվության բարձրացում:
86. Ո՞րն է հետտետանիկ հզորացման պատճառը:
Ա. Միջնորդի քվանտների գումարում; Բ. Միջնորդի դիֆուզիայի արագության բարձրացում; Բ. Կալցիումի իոնների կոնցենտրացիայի ավելացում նախասինապտիկ տերմինալում; D. Միջնորդների սինթեզի համար ֆերմենտների ակտիվության բարձրացում; Դ. Ակտիվ գոտիների տարածքում կալցիումի ալիքների բարձր խտություն:
87. Հետևյալ իրադարձություններից ո՞րն է հանգեցնում G-սպիտակուցների ակտիվացմանը.
A. GDF-ի փոխակերպումը GTP-ի; B. ATP-ի փոխակերպումը cAMP-ի; B. Ադենիլատ ցիկլազի ակտիվացում; D. պրոտեին կինազի ակտիվացում; D. Հետսինապտիկ ներուժի ձևավորում:
88. Այս իրադարձություններից ո՞րը պետք է տեղի ունենա ավելի շուտ, քան մյուսները մետաբոտրոֆիկ կառավարման ժամանակ:
A. Ճամբարի կրթություն; B. պրոտեին կինազի ակտիվացում; B. Ադենիլատ ցիկլազի ակտիվացում; D. G-սպիտակուցի ակտիվացում; Դ. Իոնային ալիքի բացում:
89. Ի՞նչ գործառույթ ունեն նախասինապտիկ մեմբրանի ավտոընկալիչները:
Ա. Նեյրոհաղորդիչների հակադարձ տրանսպորտի իրականացում; B. Սինապտիկ ճեղքում նեյրոհաղորդիչի քանակի կարգավորում; Բ. Միջնորդների ճեղքման մեխանիզմների ակտիվացում; D. Նախասինապտիկ մեմբրանի ալիքների իոնոտրոպ հսկողություն; Դ. Հետսինապտիկ նեյրոնից ազատված նեյրոհաղորդիչի կապակցում:
90. Վերոհիշյալ մեխանիզմներից ո՞րը չի օգտագործվում սինապտիկ ճեղքվածքից միջնորդները հեռացնելու համար:
Ա. Ֆերմենտային դեգրադացիա; B. Նեյրոհաղորդիչների մոլեկուլների գրավում գլիալ բջիջների կողմից; B. Նեյրոհաղորդիչի մոլեկուլների առգրավում հետսինապտիկ նեյրոնի կողմից; D. Նեյրոհաղորդիչի մոլեկուլների տեղափոխում նախասինապտիկ նեյրոնի տերմինալ; D. դիֆուզիոն.
91. Պրոգրեսիվ դեմենցիայով (Ալցհեյմերի հիվանդություն) խանգարվում է նեյրոհաղորդիչներից մեկի սինթեզը։ Սա:
Ա. ացետիլխոլին; Բ. Գլուտամատ; Բ. Դոպամին; G. Norepinephrine; D. GABA.
92. Ի՞նչ նեյրոհաղորդիչ է արտազատվում կապույտ բծերի նեյրոնները:
Ա. Դոպամին; Բ. Գլիցին; Բ. Գլուտամատ; G. Norepinephrine; Դ.Ադրենալին.
93. Ի՞նչ նեյրոհաղորդիչ է սինթեզվում միջին ուղեղի նիգրա սուբստանցիայի նեյրոններում:
Ա. Դոպամին; B. Norepinephrine; B. ացետիլխոլին; G. բ-Էնդորֆին; D. Գլուտամատ.
94. Հետևյալ ուղեղի կառուցվածքներից ո՞րում է հայտնաբերվում դոֆամինի ամենաբարձր կոնցենտրացիան:
Ա. Ցանցային ձևավորում; B. Occipital kortex; B. Ճակատային ծառի կեղեվ; G. ուղեղիկ; Դ.Թալամուս.
95. Ի՞նչ նեյրոհաղորդիչ է արտազատվում կարի միջուկների նեյրոնները:
Ա. Դոպամին; B. Norepinephrine; B. Սերոտոնին; G. Histamine; Դ.Գլիցին.
96. Ի՞նչ միջնորդ է գործում NMDA ընկալիչների վրա:
Ա. ացետիլխոլին; Բ. Գլուտամատ; V. Գլիցին; G. Enkephalin; Դ.Ադրենալին.
97. Նեյրոհաղորդիչներից մեկի ածանցյալներն օգտագործվում են վերականգնողական գործընթացներն արագացնելու և ուղեղի վնասվածքից հետո հիշողությունը բարելավելու համար: Նշեք այն:
A. GABA; Բ. Գլիցին; B. ացետիլխոլին; G. Գլուտամատ; Դ. Դոպամին.
98. Հետևյալ նյութերից ո՞րը պեպտիդային նեյրոհաղորդիչ չէ.
Ա. Էնդորֆին; Բ. Գլիցին; B. նյութ R; G. Somatostatin; Դ.Էնկեֆալին.
99. Ո՞ր նեյրոհաղորդիչն է սինթեզվում ուղեղի որոշ նեյրոնների կողմից և ազդում ողնուղեղում ցավոտ գրգռիչների մասին տեղեկատվության փոխանցման վրա:
Ա. Էնդորֆին; B. Enkephalin; B. Նյութ R. G. Օքսիտոցին; D. Vasopressin.
100. Ուղեղի ո՞ր հատվածում են պեպտիդային նեյրոհաղորդիչները առավել հաճախ օգտագործվում որպես միջնորդներ:
A. ուղեղիկ; B. Ցանցային ձևավորում; Բ. Հիպոթալամուս և հիպոֆիզ; D. Ճակատային ծառի կեղեվ; D. Ենթակեղևային միջուկներ:
Նեյրոհաղորդիչներին նվիրված շարքի վեցերորդ (և վերջին) հոդվածը նվիրված կլինի գլյուտամատ... Այս նյութը մեզ ավելի ծանոթ է որպես սննդամթերքի համը ուժեղացնող միջոց, սակայն այն կարևոր դեր է խաղում մեր նյարդային համակարգի համար։ Գլուտամատը կաթնասունների նյարդային համակարգում ընդհանրապես և հատկապես մարդկանց նյարդային համակարգում ամենաառատ գրգռիչ նյարդային հաղորդիչն է:
Մոլեկուլներ և կապեր
Գլուտամատ (գլուտամինաթթու) 20 էական ամինաթթուներից մեկն է: Բացի սպիտակուցների սինթեզին մասնակցելուց, այն կարող է հանդես գալ որպես նեյրոհաղորդիչ՝ մի նյութ, որն ազդանշան է փոխանցում մի նյարդային բջջից մյուսը սինապտիկ ճեղքում: Պետք է նկատի ունենալ, որ սննդի մեջ պարունակվող գլյուտամատը չի թափանցում արյունաուղեղային արգելքը, այսինքն՝ ուղղակի ազդեցություն չի ունենում ուղեղի վրա։ Գլուտամատը մեր մարմնի բջիջներում արտադրվում է α-կետօղլուտարատից տրանսամինացիայի միջոցով: Ամին խումբը տեղափոխվում է ալանինից կամ ասպարտատից՝ փոխարինելով α-կետօղլուտարատի կետոնային ռադիկալին (նկ. 1): Արդյունքում մենք ստանում ենք գլյուտամատ և պիրուվատ կամ օքսալոքացախաթթու (կախված ամինո խմբի դոնորից): Վերջին երկու նյութերը ներգրավված են բազմաթիվ կարևոր գործընթացներում. օրինակ, օքսալոքացախաթթուն, մեծ և սարսափելի Կրեբսի ցիկլի մետաբոլիտներից մեկն է: Գլուտամատի քայքայումը տեղի է ունենում գլյուտամատդեհիդրոգենազ ֆերմենտի օգնությամբ, իսկ ռեակցիայի ընթացքում առաջանում են արդեն ծանոթ α-կետօղլուտարատը և ամոնիակը։
Նկար 1. Գլուտամատի սինթեզ:Գլուտամատը ձևավորվում է α-կետօղլուտարատից՝ փոխարինելով keto խումբը ամինային խմբով։ Ռեակցիայի ընթացքում բջիջներում ծախսվում է նիկոտինամիդ ադենին դինուկլեոտիդ ֆոսֆատ (NADP, NADP): Նկարչություն lecturer.ukdw.ac.id կայքից:
Գլուտամատը, ինչպես շատ այլ նեյրոհաղորդիչներ, ունի երկու տեսակի ընկալիչներ. իոնոտրոպ(որոնք բացում են մեմբրանի ծակոտիները իոնների համար՝ ի պատասխան լիգանդի միացման) և մետաբոտրոֆիկ(որոնք, լիգանդի միացման դեպքում, բջջում առաջացնում են նյութափոխանակության վերադասավորումներ): Իոնոտրոպ ընկալիչների խումբը բաժանված է երեք ընտանիքի՝ NMDA ընկալիչներ, AMPA ընկալիչներ և կաինաթթվի ընկալիչներ: NMDA ընկալիչներըայսպես կոչված, քանի որ նրանց ընտրովի ագոնիստը, մի նյութ, որն ընտրողաբար խթանում է այս ընկալիչները, N-methyl-D-aspartate (NMDA) է: Երբ AMPA ընկալիչներըայդպիսի ագոնիստ է α-ամինոմեթիլիզոքսազոլպրոպիոնաթթուն, և kainate ընկալիչներըընտրողաբար խթանվում են կաինաթթուով: Այս նյութը հայտնաբերված է կարմիր ջրիմուռներում և օգտագործվում է նյարդակենսաբանական հետազոտություններում՝ էպիլեպսիայի և Ալցհեյմերի հիվանդության նմանակման համար: Վերջերս ավելացվել են նաև իոնոտրոպ ընկալիչները δ ընկալիչներըԴրանք տեղակայված են կաթնասունների ուղեղիկի Պուրկինյեի բջիջների վրա: «Դասական» - NMDA, AMPA և kainate ընկալիչների խթանումը հանգեցնում է նրան, որ կալիումը սկսում է դուրս գալ բջիջից, իսկ կալցիումը և նատրիումը մտնում են բջիջ: Այս գործընթացների ընթացքում նեյրոնում առաջանում է գրգռում և ակտիվանում է գործողության ներուժը: Metabotropicընկալիչները կապված են G- սպիտակուցային համակարգի հետ և ներգրավված են նեյրոպլաստիկության գործընթացներում: Նեյրոպլաստիկությունը վերաբերում է նյարդային բջիջների՝ միմյանց հետ նոր կապեր ստեղծելու կամ դրանք ոչնչացնելու կարողությանը: Նաև նեյրոպլաստիկության հայեցակարգը ներառում է սինապսների կարողությունը՝ փոխելու ազատված նեյրոհաղորդիչի քանակը՝ կախված նրանից, թե ինչ վարքագծային ակտեր և մտքի գործընթացներ են տեղի ունենում տվյալ պահին և ինչ հաճախականությամբ:
Գլուտամատային համակարգը ոչ սպեցիֆիկ է՝ գրեթե ամբողջ ուղեղը «աշխատում է» գլուտամինաթթվի վրա։ Նախորդ հոդվածներում նկարագրված այլ նեյրոհաղորդիչ համակարգեր ունեին քիչ թե շատ նեղ առանձնահատկություններ, օրինակ՝ դոֆամինը ազդել է մեր շարժումների և մոտիվացիայի վրա: Գլուտամատի դեպքում դա տեղի չի ունենում. դրա ազդեցությունը ուղեղի ներսում պրոցեսների վրա չափազանց լայն է և անխտիր: Դժվար է առանձնացնել որևէ կոնկրետ գործառույթ, բացի հուզիչ... Այդ իսկ պատճառով մենք պետք է խոսենք գլյուտամատային համակարգի մասին՝ որպես ուղեղում մեծ թվով կապերի մի շարք: Նման հավաքածուն կոչվում է միացում... Մարդու ուղեղը պարունակում է մեծ գումարնեյրոններ, որոնք դեռ ձևավորվում են միմյանց միջև մեծ քանակությամբկապեր. Կոնեկտոմով մարդուն շարադրելը խնդիր է, որն այսօր գիտության ուժերից վեր է։ Սակայն դա արդեն նկարագրված է ճիճու կապով Caenorhabditis elegans(նկ. 2): Կոնեկտոմի գաղափարի երկրպագուները պնդում են, որ մեր ինքնությունը գրանցված է մարդկային կոնեկտոմներում՝ մեր անհատականությունը և հիշողությունը: Նրանց կարծիքով՝ մեր «ես»-ը թաքնված է բոլոր կապերի ամբողջության մեջ։ Նաև «հաղորդակցությունները» կարծում են, որ բոլոր նեյրոնային կապերը նկարագրելուց հետո մենք կկարողանանք հասկանալ բազմաթիվ հոգեկան և նյարդաբանական խանգարումների պատճառը և, հետևաբար, կկարողանանք հաջողությամբ բուժել դրանք։

Նկար 2. Connectome nematode Caenorhabditis elegans Որդի յուրաքանչյուր նեյրոն ունի իր անունը, և նեյրոնների միջև բոլոր կապերը հաշվի են առնվում և գծագրվում են դիագրամի վրա: Արդյունքում դիագրամն ավելի շփոթեցնող է, քան Տոկիոյի մետրոյի քարտեզը։ Նկարչություն connectomethebook.com-ից:
Ինձ թվում է, որ այս գաղափարը խոստումնալից է։ Պարզեցված ձևով նեյրոնների միջև կապերը կարող են ներկայացվել որպես լարեր, բարդ մալուխներ, որոնք միացնում են մի նեյրոնը մյուսին: Եթե այդ կապերը վնասված են՝ ազդանշանի աղավաղում, լարերի խզում, կարող է առաջանալ ուղեղի համակարգված աշխատանքի խախտում։ Այնպիսի հիվանդությունները, որոնք առաջանում են, երբ նյարդային կապի ուղիները խափանում են, կոչվում են կոնեկտոպաթիաներ... Տերմինը նոր է, սակայն դրա հետևում թաքնված են գիտնականներին արդեն հայտնի պաթոլոգիական գործընթացներ։ Եթե ցանկանում եք ավելին իմանալ Connectomes-ի մասին, խորհուրդ եմ տալիս կարդալ Սեբաստիան Սեունգի գիրքը « Connectome. Ինչպես է ուղեղը մեզ դարձնում այնպիսին, ինչպիսին կանք» .
Ցանցի գերբեռնվածություն

Նկար 3. Մեմանտինի կառուցվածքը:Մեմանտինը ադամանտանի ածխաջրածնի ածանցյալն է (չշփոթել ադամանտի հետ): Նկարչություն Վիքիպեդիայից։
Նորմալ աշխատող ուղեղում նեյրոնների ազդանշանները հավասարապես բաշխվում են բոլոր մյուս բջիջներում: Նեյրոհաղորդիչներն ազատվում են անհրաժեշտ քանակությամբ, իսկ վնասված բջիջներ չկան։ Այնուամենայնիվ, ինսուլտից (սուր վնասվածք) կամ դեմենցիայից (երկարատև շարունակվող գործընթաց) հետո գլուտամատը նեյրոններից սկսում է արտազատվել շրջակա տարածություն: Այն խթանում է այլ նեյրոնների NMDA ընկալիչները, և այդ նեյրոնները ստանում են կալցիում: Կալցիումի ներհոսքը գործարկում է մի շարք պաթոլոգիական մեխանիզմներ, որոնք, ի վերջո, հանգեցնում են նեյրոնի մահվան։ Մեծ քանակությամբ էնդոգեն տոքսինի (այս դեպքում՝ գլուտամատի) արտազատման հետևանքով բջիջների վնասման գործընթացը կոչվում է. էքսիտոտոքսիկություն.

Նկար 4. Մեմանտինի ազդեցությունը Ալցհեյմերի դեմենցիայի մեջ:Մեմանտինը նվազեցնում է գրգռիչ ազդանշանների ինտենսիվությունը, որոնք գալիս են կեղևային նեյրոններից դեպի Մայներտի միջուկ: Այս կառուցվածքը կազմող ացետիլխոլինային նեյրոնները կարգավորում են ուշադրությունը և մի շարք այլ ճանաչողական գործառույթներ։ Meinert միջուկի ավելորդ ակտիվացման նվազումը հանգեցնում է դեմենցիայի ախտանիշների նվազմանը։ Նկար -ից:
Էկզիտոտոքսիկության զարգացումը կանխելու կամ հիվանդության ընթացքի վրա դրա ազդեցությունը նվազեցնելու համար կարող եք նշանակել մեմանտին... Մեմանտինը շատ գեղեցիկ NMDA ընկալիչների հակառակորդ մոլեկուլ է (նկ. 3): Ամենից հաճախ այս դեղամիջոցը նշանակվում է անոթային դեմենցիայի և Ալցհեյմերի հիվանդության ժամանակ տկարամտության համար: Սովորաբար, NMDA ընկալիչները արգելափակվում են մագնեզիումի իոններով, բայց երբ գլուտամատը խթանվում է, այդ իոնները ազատվում են ընկալիչից, և կալցիումը սկսում է ներթափանցել բջիջ: Մեմանտինը արգելափակում է ընկալիչը և կանխում կալցիումի իոնների ներթափանցումը նեյրոն. դեղամիջոցն ունի իր նյարդապաշտպան ազդեցությունը՝ նվազեցնելով ընդհանուր էլեկտրական «աղմուկը» բջջային ազդանշաններում: Ալցհեյմերի դեմենցիայի ժամանակ, ի լրումն գլյուտամատով պայմանավորված խնդիրներին, նվազում է ացետիլխոլինի մակարդակը՝ նյարդահաղորդիչ, որը ներգրավված է այնպիսի գործընթացներում, ինչպիսիք են հիշողությունը, սովորելը և ուշադրությունը: Ալցհեյմերի հիվանդության այս հատկանիշի պատճառով հոգեբույժներն ու նյարդաբանները օգտագործում են ացետիլխոլինէսթերազի ինհիբիտորներ, ֆերմենտ, որը քայքայում է ացետիլխոլինը սինապտիկ ճեղքում։ Այս խմբի դեղերի օգտագործումը մեծացնում է ուղեղում ացետիլխոլինի պարունակությունը և նորմալացնում հիվանդի վիճակը: Մասնագետները խորհուրդ են տալիս մեմանտինի և ացետիլխոլինէսթերազի ինհիբիտորների համատեղ օգտագործումը՝ Ալցհեյմերի հիվանդության ժամանակ դեմենցիայի դեմ ավելի լավ պայքարելու համար: Երբ այս դեղամիջոցները միասին օգտագործվում են, ազդեցություն է լինում հիվանդության զարգացման միանգամից երկու մեխանիզմների վրա (նկ. 4):
Դեմենսիան ուղեղի երկարատև վնասվածք է, որի դեպքում նեյրոնների մահը դանդաղ է տեղի ունենում: Իսկ կան հիվանդություններ, որոնք հանգեցնում են նյարդային հյուսվածքի արագ ու լայնածավալ վնասմանը։ Էկզիտոտոքսիկությունը ինսուլտի ժամանակ նյարդային բջիջների վնասման կարևոր բաղադրիչն է: Այդ պատճառով մեմանտինի օգտագործումը կարող է արդարացված լինել ուղեղային շրջանառության խանգարումների դեպքում, սակայն այս թեմայով հետազոտությունները դեռ նոր են սկսվում։ Ներկայումս մկների վրա ուսումնասիրություններ կան, որոնք ցույց են տալիս, որ օրական 0,2 մգ/կգ դոզանով մեմանտինի ընդունումը նվազեցնում է ուղեղի վնասվածքի քանակը և բարելավում ինսուլտի կանխատեսումը: Թերևս այս թեմայով հետագա աշխատանքը կբարելավի մարդկանց մոտ ինսուլտների բուժումը:
Ձայներ իմ գլխում
Շիզոֆրենիայով հիվանդների մոտ ամենատարածված հալյուցինացիաները լսողական են՝ հիվանդը գլխում լսում է «ձայներ»։ Ձայնը կարող է նախատել, մեկնաբանել այն, ինչ կատարվում է շուրջը, ներառյալ հիվանդի գործողությունները: Իմ հիվանդներից մեկի մոտ «ձայները» կարդում էին այն փողոցի խանութների ցուցանակները, որտեղ նա քայլում էր. Մեկը ձայն լսեց, որ ասում էր. «Թոշակ կստանաս, գնանք սրճարան»։ Ներկայումս կա մի տեսություն, որը բացատրում է նման ձայների առաջացումը: Պատկերացրեք, որ հիվանդը քայլում է փողոցով: Նա տեսնում է նշանը, և ուղեղն ինքնաբերաբար «կարդում» է այն։ Լսողական ընկալման համար պատասխանատու ժամանակավոր բլթի ակտիվության բարձրացման դեպքում հիվանդը լսողական սենսացիաներ է ունենում: Նրանք կարող էին ճնշվել ճակատային ծառի կեղևի տարածքների բնականոն գործունեության պատճառով, բայց դա տեղի չի ունենում նրանց ակտիվության նվազման պատճառով (նկ. 5): Լսողական ծառի կեղևի չափազանց ակտիվությունը կարող է առաջանալ գլյուտամատային (գրգռիչ) համակարգի հիպերֆունկցիայի կամ մարդու ուղեղում նորմալ արգելակման համար պատասխանատու GABAergic կառուցվածքների թերության պատճառով: Ամենայն հավանականությամբ, շիզոֆրենիայի դեպքում ճակատային բլթի անբավարար ակտիվությունը նույնպես կապված է նյարդային հաղորդիչների հավասարակշռության խախտման հետ։ Գործողությունների անհամապատասխանությունը հանգեցնում է նրան, որ մարդը սկսում է լսել «ձայներ», որոնք հստակորեն կապված են շրջակա միջավայրի հետ կամ փոխանցում են իր մտքերը: Շատ հաճախ մենք մեր մտքերը «խոսում» ենք մեր գլխում, ինչը կարող է նաև «ձայների» աղբյուր հանդիսանալ շիզոֆրենիայով հիվանդ մարդու ուղեղում։

Նկար 5. Շիզոֆրենիայով հիվանդի ուղեղում լսողական հալյուցինացիաների առաջացում:Հիմնական սենսացիան նշանների ավտոմատ «ընթերցումից» կամ երբ մտքեր են առաջանում, տեղայնացված ժամանակավոր կեղևում (1), չի ճնշվում ճակատային ծառի կեղևով (2): Պարիետալ ծառի կեղևը (3) ֆիքսում է ուղեղի գործունեության ձևավորվող օրինաչափությունը և տեղափոխում նրա գործունեության կենտրոնացումը: Արդյունքում, մարդը սկսում է լսել «ձայնը»: Նկար -ից:
Սա ավարտում է մեր ճանապարհորդությունը դեպի նյարդային հաղորդիչների աշխարհ: Մենք ծանոթացանք մոտիվացնող դոֆամինի, հանգստացնող γ-ամինաբուտիրաթթվի և մեր ուղեղի չորս այլ հերոսների: Հետաքրքրվեք ձեր ուղեղով, քանի որ, ինչպես ասում է Դիկ Սվաաբի գրքի վերնագիրը,. Նեյրոտոքս. Ռես. 24 , 358–369;