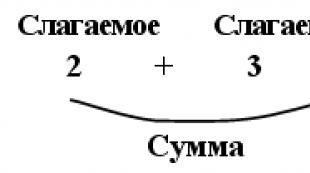
Eksogeni transport lipidov. Oddelek za biokemijo. Družinsko pomanjkanje apoproteina SP
Transportne oblike lipidov
Transport in presnovne transformacije lipidov v krvi
Na novo sintetizirani TAG, fosfolipidi in drugi absorbirani lipidi zapustijo celice črevesne sluznice, najprej vstopijo v limfo, z limfo pa v kri. Ker je večina lipidov netopnih v vodnem okolju, se njihov transport v limfo in nato v krvni plazmi izvaja v kombinaciji z beljakovinami.
Maščobne kisline v krvi so povezane z albuminom, drugi lipidi pa se prenašajo kot del posebnih delcev - lipoproteini .
Elektronska mikroskopija izoliranih vrst liproteinskih delcev je pokazala, da gre za sferične delce, katerih premer se z naraščajočo gostoto zmanjšuje (tabela 1). Lipoproteini so sestavljeni iz jedra, ki vključuje hidrofobne lipide - triacilgliceride, estre holesterola itd., medtem ko zunanji del, v stiku s krvno plazmo vsebuje amfifil ny lipidi: fosfolipidi, prosti holesterol. Beljakovine Komponente (apoproteini) s svojimi hidrofobnimi območji se nahajajo v notranjem delu lipoproteinskih delcev in hidrofilne - predvsem na površini.
Tabela 1. Značilnosti lipoproteinov.
| Lastnosti | VLDL | LDPP | LDL | HDL |
|
| Gostota g / l | < 0,95 | ||||
| Premer, nm | |||||
| Elektroforetska mobilnost | Ostanite na začetku | Plavajoči β | |||
| Kraj izobraževanja | Tanko črevo | Katabolizem VLDL | Katabolizem VLDL preko DID | Jetra, tanko črevo, katabolizem HM in VLDL |
|
| Glavna funkcija | Prevoz eksogenih TG | Transport endogenih TG | Predhodnik LDL | Prenos holesterola | Povratni transport holesterola |
| spojina: |
|||||
| holesterola | |||||
| Fosfolipidi | |||||
| Apoproteini | A, B-48, C, E | B-100, C, E | B-100, E | A, C, E |
|
Lipoproteinski delci - makromolekularni kompleksi, katerih notranji del vsebuje nevtralne lipide (TAG in estre holesterola), površinsko plast pa sestavljajo fosfolipidi in specifični lipidni transportni proteini, imenovani apolipoproteini.
Lipoproteini so razvrščeni glede na njihovo mobilnost v električnem polju (med elektroforezo). Med elektroforezo se lipoproteini razdelijo na frakcije, od katerih ena ostane na začetku (hilomikroni), druge migrirajo v globulinske cone - β-LP, pre-β-LP, α-LP.
Glede na velikost hidratacijske lupine jih je običajno razdeliti v 5 razredov: hilomikroni, VLDL, IDL, LDL, HDL.
V smislu elektroforetske mobilnosti VLDL ustreza pre-β-LP, LDL –β-LP, HDL do α-LP, CM pa ostaja na začetku.
Apoproteini - To so beljakovine lipoproteinske ovojnice, nekovalentno povezane s fosfolipidi in holesterolom. Apoproteini ohranjajo strukturno celovitost lipoproteinov, sodelujejo v presnovnih procesih med lipoproteini in so odgovorni za interakcijo lipoproteinov z njihovimi receptorji.
ApoLP pospešujejo tvorbo micel LP v endoplazmatskem retikulumu hepatocitov, služijo kot ligandi za specifične receptorje na površini plazemske membrane celic in kofaktorji (aktivatorji in zaviralci) lipolize in presnove LP v žilni postelji.
Nastali hilomikroni se sprva izločajo v limfne kapilare. Nato skozi limfni sistem žile z limfnim tokom, vstopijo v kri. Na trgu v krvi se apoproteinska sestava hilomikronov spremeni zaradi izmenjave z drugimi vrstami lipoproteinskih delcev (ali poproteini visoke gostote - HDL) . Zlasti na chi lomikroni prejmejo apoprotein C, ki je dodatno potreben za aktiviranje njihove lipolize.
Transformacije hilomikronov v krvni plazmi so v glavnem določene z delovanjem encima - lipoproteinska lipaza (LPL) ... Ta encim spada v družino lipaz. Sintetizira se v celicah mišičnega in maščobnega tkiva, vendar deluje na zunanji površini endotelijskih celic. oblikovanje stene posode od znotraj. LPL katalizira reakcijohidroliza triacilgliceridov v hilomikronih s kosmiči tvorba radikalov maščobnih kislin na položajih 1 in 3, pa tudi na položaju 1 v fosfolipidih. 2-monoacilgliceridi, ki nastanejo v primeru cepitve triacilgliceridov, se nato spontano izomerizirajo, spremenijo v 1- ali 3-monoacilgliceride in se nadalje cepijo s sodelovanjem istega LPL na glicerol in maščobno kislino. To se zgodi, dokler se količina triacil gliceridov v lipoproteinskih delcih ne zmanjša na 20 % začetne vsebnosti.
Med razpadom se sprostijo maščobne mucke veliko stikov plazemski albumin in v taki kepi plexa se prenašajo v celice organov in tkiv. celice absorbirajo maščobne kisline in jih uporabljajo kot energijo hetično gorivo ali gradbeni material (sinteza lastnih lipidov v celicah). Glavni porabniki maščobnih kislin so maščobno in mišično tkivo.
Kot posledica delovanja LPL hilomikronov se uničijo, ostanki teh delcev pa vstopijo v jetra, kjer se dokončno uničijo. V jetrih se razgradijo tako beljakovinska komponenta hilomikronov (na aminokisline) kot nerazcepljeni ali delno razcepljeni triacilgliceridi in drugi lipidi. V ta proces sodelujejo jetrna lipaza in drugi encimi.
Hkrati se intenzivno nadaljuje v jetrihsinteza lipidov iz originalnih substratov (ocetna kislina, glicerin, maščobne kisline itd.). Prevoz na novo sintetiziranih lipidov iz jeter v kri in od tam v organe in tkiva se izvaja z dvema drugim vrstama lipoproteinskih ur delci, ki nastanejo v jetrih - zelo nizki lipoproteini gostota (VLDL) in lipoproteini visoke gostote (HDL) ... Načela strukture teh delcev so podobna tistim pri hilomikronih. Razlika je v tem, da je velikost VLDL in še več - HDL manjša od velikosti hilomikronov. Delež beljakovinske komponente v njihovi sestavi je višji (10,4 oziroma 48,8 % mase delca), vsebnost triacilgliceridov pa je nižja (31,4 oz. 1,8 % mase). Posledično je gostota VLDL in HDL višja od gostote hilomikronov.
Glavna lipidna komponenta VLDL so triacilgliceridi. Vendar se za razliko od hilomikronov ti triacilgliceridi sintetizirajo v jetrnih celicah. Zato jih imenujemo endogeni, medtem ko v sestavi hilomikronov - eksogeni (vzeti iz hrane). VLDL sek se umaknejo iz jeter v kri. V njih so lipidi sestava, tako kot v primeru hilomikronov, so podvrženi cepljenju LPL. Izpuščeno maščobno kisline vstopajo v celice organov in tkiv.
Treba je opozoriti, da raven LPL v mišičnem in maščobnem tkivu niha tako, da zagotavlja maksimalno oskrbo celic maščobnega tkiva z maščobnimi kislinami za njihovo odlaganje po obrokih in v obdobju med obroki - v celice. mišičnega tkiva, da ohranijo svoje funkcije. Poleg tega je v maščobnem tkivu glavni dejavnik, ki povečuje sintezo katalitično aktivnih LPL je insulin. Zato hiperinzulinemija, ki Toraya spodbuja obdobje absorpcije produktov za prebavo hrane, spremlja povečan vnos produktov razgradnje triacilgliceridov iz hilomikronov in VLDL v maščobno tkivo za odlaganje.
Glavna pot nastajanja LDL- lipoliza VLDL z LPL. Pojavi se neposredno v krvnem obtoku. Pri tej reakciji nastanejo številni vmesni produkti. izdelki ali delci, ki vsebujejo različne količine tria cilgliceridi. Dobili so povzeto ime lipoprote vmesna gostota ins (IDP) . Nadaljnja usoda IDL se lahko razvijejo na dva načina: bodisi vstopijo v jetra iz krvnega obtoka ali pa se podvržejo nadaljnjim transformacijam (njihov mehanizem ni dobro razumljen), pri čemer se pretvorijo v LDL.
Glavna lipidna komponenta jedra LDL so estri holesterola. LDL je glavni nosilec za dostavo holesterola v celice organov in tkiv (slika). Prvič, delec LDL interagira z enim od 15.000 receptorjev, specifičnih za te lipoproteine na celični površini. V naslednjem koraku celica absorbira delce LDL, vezan na receptor. Znotraj oblikovanih endosomov se lipoproteini odcepijo od receptorjev.
V prihodnosti LDL vstopi v lizosome, kjer pride do uničenjapotepati se naokoli. V lizosomih,hidroliza etra in rovholesterola, ki so bili del LDL . Kot rezultat nastaja prosti holesterol ali njegove oksidirane oblike. Prosti holesterol se uporablja za različne namene:živi strukturna komponenta celičnih membran, substrat za sintezo steroidnih hormonov in žolčnih kislin. O produkti njegove oksidativne transformacije imajo regulacijski učinek. torični učinek na telo.
Nadzorni mehanizmi usklajujejo uporabo znotraj- in zunajcelični viri holesterola. Ko je na voljo natančna količina LDL, celice sesalcev, ki uporabljajo receptorje, pretežno uporabljajo LDL kot vir holesterola. V tem času je znotrajcelični sistem sinteze holesterola tako rekoč v rezervi, ne deluje s polno močjo.
Pomembno vlogo pri ciljni dostavi lipoproteinov na cene tram njihovega metabolizma sodi med apoproteine. Nasprotujejo povzroči interakcijo lipoproteinov z encimi in receptorji celične površine.
Povratni transport holesterola iz perifernih tkiv v jetra poteka s pomočjo HDL. Te lipoproteinski delci odstranijo presežek prostega (net rafinirani) holesterol s celične površine.
HDL je cel razred lipoproteinskih delcev, ki rži se med seboj bistveno razlikujejo po lipidih in sestava, velikost in funkcija apoproteinov. Oblikovano HDL v jetrih. Od tam se izločajo v krvni obtok v "ne zrela "oblika, to je diskoidna oblika. Ta oblika je posledica odsotnosti jedra nevtralnih lipidov v njih. dov. Njihova glavna lipidna sestavina je fosfol pids.
Prenos prostega holesterola iz celic v HDL zaradi razlike v njegovih koncentracijah na površini celičnih membran in lipoproteinskih delcev. Zato se nadaljuje, dokler se koncentracija holesterola med darovalcem (površino membrane) in akceptorjem (HDL) ne izenači. Vzdrževanje koncentracijskega gradienta je zagotovljeno s konstantno pretvorbo prostega holesterola, ki vstopa v HDL , v estre holesterola. Ta reakcija encimsko katalizirana lecitin-holesterolacnltrans ferase (LHAT) ... Nastali holesterolni estri so popolnoma hidrofobne spojine (za razliko od prostega holesterola, ki ima hidroksilno skupino, zaradi česar je hidrofilen). Na podlagi Zaradi svoje hidrofobnosti estri holesterola izgubijo sposobnost difuzije in se ne morejo vrniti nazaj v celico. V delcih tvorijo hidrofobno jedro, zaradi katerega HDL postane sferičen. V tej obliki HDL s pretokom krvi vstopi v jetra, kjer se uniči.
Sproščeni holesterolni estri služijo kot začetni substrat za tvorbo žolčnih kislin.
Tvorba lipoproteinov (LP) v telesu je nujna zaradi hidrofobnosti (netopnosti) lipidov. Slednje so odete v beljakovinsko membrano, ki jo tvorijo posebni transportni proteini – apoproteini, ki zagotavljajo topnost lipoproteinov. Poleg hilomikronov (CM) se v telesu živali in ljudi tvorijo lipoproteini zelo nizke gostote (VLDL), lipoproteini vmesne gostote (IDL), lipoproteini nizke gostote (LDL) in lipoproteini visoke gostote (HDL). Fino delitev na razrede dosežemo z ultracentrifugiranjem v gradientu gostote in je odvisna od razmerja med količino beljakovin in lipidov v delcih, ker lipoproteini so supramolekularne tvorbe, ki temeljijo na nekovalentnih vezi. V tem primeru se HM nahajajo na površini krvnega seruma zaradi dejstva, da vsebujejo do 85% maščobe in je lažji od vode, na dnu centrifugalne epruvete je HDL holesterol, ki vsebuje največjo količino beljakovine.
Druga klasifikacija LP temelji na elektroforetski mobilnosti. Med elektroforezo v poliakrilamidnem gelu CM kot največji delci ostanejo na začetku, VLDL tvorijo pre-β - LP frakcijo, LDL in CRLP - β - LP frakcijo, HDL - α - LP frakcijo.
Vsa zdravila so zgrajena iz hidrofobnega jedra (maščobe, estri holesterola) in hidrofilne membrane, ki jo predstavljajo beljakovine, pa tudi fosfolipidi in holesterol. Njihove hidrofilne skupine so obrnjene proti vodni fazi, medtem ko so njihovi hidrofobni deli obrnjeni proti središču, proti jedru. Vsaka vrsta LP se tvori v različnih tkivih in prenaša določene lipide. Torej, HM prenašajo maščobe, pridobljene iz hrane, iz črevesja v tkiva. XM je 84-96 % sestavljen iz eksogenih triacilgliceridov. Kot odgovor na obremenitev maščobe kapilarni endoteliociti sprostijo encim lipoprotein lipazo (LPL) v kri, ki hidrolizira maščobne molekule HM v glicerol in maščobne kisline. Maščobne kisline vstopajo v različna tkiva, topni glicerin pa se transportira v jetra, kjer se lahko uporabi za sintezo maščob. LPL je najbolj aktiven v kapilarah maščobnega tkiva, srca in pljuč, kar je povezano z aktivnim odlaganjem maščobe v adipocitih in posebnostjo presnove v miokardu, ki za energetske namene uporablja številne maščobne kisline. V pljučih se maščobne kisline uporabljajo za sintezo površinsko aktivne snovi in za zagotavljanje aktivnosti makrofagov. Ni naključje, da se jazbečeva in medvedja maščoba uporabljata v ljudskem zdravilstvu za pljučne patologije, severna ljudstva, ki živijo v težkih podnebnih razmerah, pa redko zbolijo za bronhitisom in pljučnico, pri čemer uživajo mastno hrano.
Po drugi strani pa visoka aktivnost LPL v kapilarah maščobnega tkiva prispeva k debelosti. Obstajajo tudi dokazi, da se med postom zmanjša, vendar se aktivnost mišične LPL poveča.
Preostale CM delce zajamejo hepatociti z endocitozo, kjer jih lizosomski encimi cepijo na aminokisline, maščobne kisline, glicerol in holesterol. En del holesterola in drugih lipidov se neposredno izloči z žolčem, drugi se pretvori v žolčne kisline, tretji pa je vključen v VLDL. Slednji vsebujejo 50-60% endogenih triacilgliceridov, zato so po izločanju v kri izpostavljeni, tako kot HM, delovanju lipoprotein lipaze. Posledično VLDL izgubijo TAG, ki ga nato uporabljajo celice maščobnega in mišičnega tkiva. Med katabolizmom VLDL se relativni odstotek holesterola in njegovih estrov (EF) poveča (zlasti pri uživanju hrane, bogate s holesterolom), VLDL pa se prenese v LDL, ki ga pri mnogih sesalcih, zlasti pri glodalcih, ujamejo jetra in se popolnoma razgradi v hepatocitih. Pri ljudeh, primatih, pticah, prašičih se velik, ki ga hepatociti ne zajamejo, del LDPE v krvi spremeni v LDL. Ta frakcija je najbogatejša s holesterolom in HM, in ker je visoka raven holesterola eden prvih dejavnikov tveganja za razvoj ateroskleroze, imenujemo LDL najbolj aterogena frakcija LP. LDL holesterol uporabljajo nadledvične celice in spolne žleze za sintezo steroidnih hormonov. LDL oskrbuje s holesterolom hepatocite, ledvični epitelij, limfocite in celice žilne stene. Zaradi dejstva, da so celice same sposobne sintetizirati holesterol iz acetil koencima A (AkoA), obstajajo fiziološki mehanizmi, ki ščitijo tkivo pred presežkom HM: zaviranje proizvodnje lastnega notranjega holesterola in receptorjev za LP apoproteine, saj je vsaka endocitoza receptorsko posredovano. Drenažni sistem HDL je priznan kot glavni stabilizator celičnega holesterola.
Prekurzorji HDL nastajajo v jetrih in črevesju. Vsebujejo visok odstotek beljakovin in fosfolipidov, so zelo majhni, prosto prodirajo skozi žilno steno, vežejo presežek CM in ga odstranijo iz tkiv, sami pa postanejo zrel HDL. Del EC gre neposredno v plazmo iz HDL v VLDL in LDL. Končno vse LP razcepijo lizosomi hepatocitov. Tako skoraj ves "odvečni" holesterol vstopi v jetra in se iz njih izloči kot del žolča v črevesje in se odstrani z blatom.
Lipoproteini igrajo ključno vlogo pri transportu in presnovi lipidov. .
lipoproteini- sferične strukture, ki nastanejo zaradi kombinacije holesterola, holesterolnih estrov in trigliceridov maščobnih kislin. Tvorijo jedro, obdano z 2 nm debelo lupino. Lupina vključuje - molekule fosfolipidov, neesterificiranega holesterola in specifične beljakovine - apoproteine, ki so vedno na površini lipoproteinov. Zdaj obstaja 5 razredov apoproteinov - A, B, C, D, E.
Funkcije apoproteinov:
Spodbujajte razpad ECS in TG
Uravnava reakcije lipidov z encimi
Vezava lipoproteine na celične receptorje
Določite funkcionalne lastnosti zdravila.
Vsi lipoproteini so razdeljeni v štiri razrede, ki se razlikujejo po sestavi jedra, vrsti apoproteinov in funkcijah. Višja kot je vsebnost beljakovin v zdravilu in nižja je vsebnost trigliceridov, manjša je velikost delcev zdravila in večja je njihova gostota.
V steni tankega črevesa, hilomikroni- veliki sferični delci, 90 % sestavljen iz trigliceridov. Naloga hilomikronov je transport holesterola in maščobnih kislin iz hrane iz črevesja v periferna tkiva (skeletne mišice, miokard, maščobno tkivo, kjer se uporabljajo kot energijski substrat) in jetra. Proteinski plašč hilomikronov vključuje apoprotein B-48. Apoprotein B-48 se sintetizira samo v črevesnih celicah. V njegovi odsotnosti se hilomikroni ne tvorijo. Hilomikroni vstopijo v krvni obtok skozi črevesni limfni sistem skozi torakalni limfni kanal. V krvi hilomikroni medsebojno delujejo s HDL in pridobivajo od njih apo C-II in apo E oblikovanje zrela obrazci. Beljakovine apo C-II je aktivator encima lipoprotein lipaze, je protein apoE potreben za odstranitev preostalih hilomikronov iz krvi.
VLDL (lipoprotein zelo nizke gostote). Sestoji iz 60% maščob in 18% fosfolipidov. Beljakovine in holesterol v približno enakih razmerjih.
Presnova VLDL
1. Primarni VLDLP nastanejo v jetrih iz prehranskih maščob, oskrbljenih s hilomikroni, in na novo sintetiziranih maščob iz glukoze. Vsebuje samo apoB-100;
2. V krvi primarni VLDLP medsebojno delujejo s HDL in iz njih pridobivajo apoC-II in apoE ter tvorijo zrele oblike.
3. Na kapilarnem endoteliju so zreli VLDLP izpostavljeni lipoprotein lipazi s tvorbo prostih maščobnih kislin. Maščobne kisline se premikajo v celice organa ali ostanejo v krvni plazmi in se v kombinaciji z albuminom s krvjo prenašajo v druga tkiva.
4. Preostali VLDL (imenovan tudi lipoprotein vmesne gostote, IDL)
LDL (lipoprotein nizke gostote) so najbolj aterogeni,
so glavna transportna oblika XC. Vsebujejo približno 6% TG, največjo količino holesterola (50%) in 22% beljakovin.
Delec LDL vsebuje kot beljakovinsko komponento eno molekulo apolipoproteina B-100 (apoB-100), ki stabilizira strukturo delcev in je ligand za LDL receptor. Velikosti LDL se gibljejo od 18 do 26 nm. ...
LDL nastane iz VLDL v procesu hidrolize slednjega z lipoprotein lipazo in jetrno lipazo. V tem primeru se relativna vsebnost trigliceridov v delcu izrazito zmanjša, holesterol pa se poveča. Tako je LDL zadnja stopnja v izmenjavi endogenih (sintetiziranih v jetrih) lipidov v telesu. V telo prenašajo holesterol, pa tudi trigliceride, karotenoide, vitamin E in nekatere druge lipofilne sestavine.
Ravni holesterola LDL so v korelaciji z visokim tveganjem za razvoj ateroskleroze in njenih manifestacij, kot so miokardni infarkt, možganska kap in HDL holesterol. Treba je opozoriti, da so majhni LDL-C bolj aterogeni kot večji.
Dedna oblika bolezni z visoka stopnja LDL je dedna hiperholesterolemija ali hiperlipoproteinemija tipa II.
Prevzem celic s LDL
Če celica potrebuje holesterol, sintetizira LDL receptorje, ki se po sintezi transportirajo v celična membrana... LDL, ki kroži v krvi, se veže na te transmembranske receptorje in ga celica endocitozira. Po absorpciji se LDL dostavi v endosome, nato pa v lizosome, kjer se estri holesterola hidrolizirajo in holesterol vstopi v celico.
HDL (lipoprotein visoke gostote) - nastanejo v jetrnih celicah. To so najmanjši lipoproteini. - 7-14 nm. Sestavljeni so iz beljakovin (50%), 75% je apoprotein A .; 30% je fosfolipidov.
Ko zapustijo hepatocit, imajo obliko v obliki diska, vendar se, ko krožijo v krvi in absorbirajo holesterol, spremenijo v sferične strukture. Naloga HDL je odstraniti presežek holesterola iz celic perifernih tkiv. To olajša jetrni encim - lecitin-holesterol-aciltransferaza, ki se nahaja na površini HDL, zaradi interakcije z apaproteinom A. Ta encim zagotavlja preoblikovanje holesterola v njegove estre in prenos v jedro. To je tisto, kar omogoča HDL, da odstrani presežek holesterola. Nadalje gre HDL v jetra, presežek holesterola pa se izloča v žolču.
V krvi najdemo lipoproteine in hilomikrone z dvema lipazama - lipoprotein lipazo in jetrno triacilglicerol lipazo.
Lipoproteinska lipaza se nahaja na površini kapilarnega endotelija mišičnega in maščobnega tkiva. Ta lipaza ima afiniteto za apoprotein-C, zato se veže na VLDL in hilomikrone. V jedru se maščobe razgradijo na maščobne kisline, ki vstopijo v celice maščobnega tkiva, kjer se trigliceridi pretvarjajo in kopičijo v rezervi, ter v mišične celice, kjer se uporabljajo kot energijski substrat. Ostanki hilomikrona izgubijo apoprotein C in se vežejo na HDL.
Jetrna trigliceridna lipaza razgrajuje tudi maščobe v hilomikronih in VLDL, vendar njene produkte cepitve uporabljajo miokardne celice in skeletne mišice. Hilomikroni se pretvorijo v ostanke hilomikronov, VLDL pa v LDL.
Vzdrževanje presnove holesterola poteka samodejno s sodelovanjem specifičnih lipoproteinskih receptorjev, ki se nahajajo na membrani hepatocitov. Sinteza holesterola v hepatocitih je določena s skupnim številom in preobremenjenostjo receptorjev za LDL in HDL. Pri nizki ravni holesterola in majhnem številu receptorjev se v hepatocitih aktivira sinteza holesterola. Interakcija molekularnega kompleksa holesterol-LDL z normalno ekspresijo LDL receptorja na celični površini vodi do pinocitoze molekularnega kompleksa. Po pinocitozi se kompleks vgradi v lizosome, kjer se sprosti prosti holesterol. Povečanje koncentracije prostega holesterola v celici zmanjša aktivnost ključnega encima za sintezo znotrajceličnega holesterola, hidroksimetilglutaril-koencim A-reduktaze. S starostjo je ta receptorski mehanizem omejen, povečan vnos holesterola pa ne spremlja omejitev njegove sinteze v jetrih. Poleg tega v aterogenih pogojih hepatociti preidejo na novo vrsto izločanja holesterola: v hepatocitih se aktivira sinteza apoproteina B in povečata tvorba in sproščanje VLDLP.
Tako se glavni del aterogenih lipoproteinov tvori, presnavlja in izloča iz telesa v jetrih, zato so motnje v regulaciji presnove teh delcev v jetrih odgovorne za razvoj ateroskleroze.
Osnova ateroskleroze kršitev presnove holesterola in prevlado aterogenih lipoproteinov (LDL, VLDL ). Zdaj je dokazano, da je izhodišče ateroskleroze oksidativna modifikacija lipoproteinov, povezana z dolgotrajnim neravnovesjem v telesu med pro in antioksidanti. LDL so še posebej občutljivi na oksidativne spremembe, saj vsebujejo veliko linolne kisline.
Izkazalo se je, da imajo lipoproteini lastno zaščito pred oksidativnim stresom v obliki ά-TF, β-karotena in drugih, katerih skupna vsebnost doseže 14 nM / mg beljakovin v lipoproteinu. Toda tudi v normi se v LDL nahaja visoka vsebnost hidroperoksidov. Sposobnost oksidacije LDL se poveča, ko vstopijo v žilno intimo.
Poleg tega je poškodba endotelija pomemben dejavnik pri aterosklerotičnih žilnih lezijah. Poškodbe endotelija spodbujajo vstop LDL v žilno steno . Endotelij se običajno najbolj poškoduje v velikih žilah pri povečani mehanski obremenitvi. LDL se pošilja na poškodovana območja in daje energijski substrat za obnovo, vendar na teh območjih pridejo v stik s prostimi kovinami spremenljive valence, kar povzroči njihovo oksidativno modifikacijo. Oksidirani LDL postane strupen za endotelij. Poleg hiperlipidemije na endotelij vplivajo tudi drugi dejavniki: arterijska hipertenzija, hormonska disfunkcija, spremembe reologije krvi, kajenje, sladkorna bolezen.
Mehanizem aterogeneze
1. Pod vplivom modificiranega LDL se poškoduje endotelij in se spremenijo površinske lastnosti monocitov in trombocitov, kar poveča njihovo adhezivnost.
2. Oksidirani LDL kaže lastnosti kemoatraktantov.
3. Po fiksaciji na endoteliju monocit migrira med endotelijskimi celicami v subendotelijsko plast in se spremeni v makrofag, ki s sodelovanjem posebnih receptorjev, »čistilcev«, začne zajemati lipide. Tudi prevzem lipidov poteka po nereceptorski poti. To povzroči nastanek penastih celic.
4. Makrofagi proizvajajo škodljive snovi (levkotriene, interlevkine), ki pa negativno vplivajo na sosednje endotelijske celice.
5. Aktivirani makrofagi proizvajajo več rastnih faktorjev, ki delujejo mitogeno na gladke mišične celice in povzročajo njihovo selitev v intimo, spodbujajo migracijo fibroblastov, pa tudi tvorbo vezivnega tkiva.
6. Pri poškodbi endotelija pa patogeno delujejo tudi trombociti, ki ob stiku z endotelijem povzročijo umik celic. Po tem začnejo trombociti medsebojno delovati s penastimi celicami in celicami vezivnega tkiva. Možno je tudi, da se trombociti združijo in tvorijo parietalni tromb. Rastni faktorji, ki se sproščajo med aktivacijo trombocitov, povzročajo proliferacijo gladkih mišičnih celic. Proliferirajoče celice pa proizvajajo rastni faktor, ki vodi do napredovanja lezije.
7. Do umika endotelijskih celic lahko pride zaradi kopičenja holesterola in lipoproteinov nizke gostote v njih. Njihova prekomerna vsebnost krši skladnost celic. Zato na mestih, ki so najbolj izpostavljena pretoku krvi (območja bifurkacije, izpusta žil), pride do ločitve endotelijskih celic zaradi togosti. Spremenjene endotelijske celice začnejo proizvajati tudi rastne faktorje, pod vplivom katerih nastanejo črte in plaki.
Ugotovljeno je bilo, da je celična sestava plakov podobna sestavi kroničnega vnetja, ki se pojavlja v intimi arterij. Trenutno se aterosklerotična lezija obravnava kot polietiološka reakcija žilne stene, podobna vnetju, ki se pojavi v zgodnjem otroštvu.
Množične epidemiološke raziskave prebivalstva različnih držav so razkrile številne dejavnike, ki vplivajo na pojavnost ateroskleroze – dejavnike tveganja. Pomen starosti, spola in družinske predispozicije ni pod vprašajem. Med drugimi dejavniki so glavni: hiperlipidemija, arterijska hipertenzija, kajenje, diabetes mellitus. Obstaja povezava med resnostjo ateroskleroze in učinki različnih stresorjev, depresije, telesne nedejavnosti, debelosti, hiperurikemije, uživanja močne kave in čaja.
Razmerje med različnimi razredi zdravil je odločilnega pomena za nastanek in napredovanje ateroskleroze: LDL, VLDL so aterogeni, HDL pa antiaterogeni. Največje tveganje za razvoj ateroskleroze opazimo pri posameznikih z visoko vsebnostjo LDL in VLDL ter nizko - HDL.
Norme holesterola
Skupna raven holesterola v krvi - 3,0-6,0 mmol/l.
norme vsebino LDL holesterol: za moških- 2,25-4,82 mmol / l, for ženske- 1,92-4,51 mmol / l.
norme ravni HDL holesterol: za moških- 0,7-1,73 mmol / l, for ženske- 0,86-2,28 mmol / l
Mehanizem aterogeneze
(tvorba aterosklerotičnih plakov)
Situacijske naloge za samostojno deloštudenti
Problem 1
Biokemična študija krvi bolnika H. je pokazala, da je vrednost holesterolnega koeficienta aterogenosti 5 (norma je ≤3). Kot je povedal bolnik, se je pred časom zdravil v endokrinološki ambulanti zaradi zmerno izražene hipofunkcije ščitnice.
Kontrolna vprašanja:
1. Ali je pri bolniku veliko tveganje za razvoj ateroskleroze?
2. Kakšen je mehanizem razmerja med hiperholesterolemijo in hipofunkcijo ščitnice? Utemeljite odgovor.
2. naloga
22-letnik je bil sprejet na kliniko s pritožbami zaradi bolečin v predelu srca. Bolnik je poročal, da so mu pred dvema letoma diagnosticirali angino pektoris pri naporu. Pregled je odkril aterosklerotične plake v subepikardnih koronarnih arterijah in velikih možganskih žilah. Vsebnost holesterola v krvi, LDL in HDL v krvni plazmi večkrat presega zgornjo mejo norme. Bolniku je bila opravljena biopsija jeter, ki je pokazala zmanjšanje števila receptorjev za LDL in LDL.
Kontrolna vprašanja:
1. Ali je pri nastanku in razvoju odkrite patologije pomembna dednost?
2. Ali obstaja povezava med zmanjšanjem števila receptorjev za LDL in hiperholesterolemijo?
3. Kakšni so preventivni ukrepi za to patologijo?
Problem 3
Bolnik K., star 58 let, trpi za arterijsko hipertenzijo. V zadnjih 1,5 letih je začela opažati povečanje telesne teže, mrzlico v nogah, odrevenelost in bolečine v telečnih mišicah pri hoji, nato pa v mirovanju (predvsem ponoči, zaradi česar je bil moten njen spanec). . Pred 5 meseci je nastala erozija v spodnji tretjini desne noge, nato pa razjeda, neboleča in nezdravljiva. Telesna temperatura je stalno zvišana (do 37,2-37,4 ° C). Bolnik je ob obisku pri zdravniku poleg naštetega poročal tudi o suhih ustih, žeji, povečanem vnosu tekočine (4-5 litrov na dan), pogostem obilnem uriniranju. Objektivno: koža na nogah je suha, bleda, hladna na dotik. Palpacija ni določena s pulziranjem arterij v poplitealni jami in na stopalu. Krvni test povišane ravni holesterola, fibrinogena, trombocitov, HPA 180 mg%
Kontrolna vprašanja:
1. Na katere oblike patologije poleg arterijske hipertenzije kažejo razpoložljivi klinični in laboratorijski podatki? Utemeljite odgovor.
2. Kaj bi lahko povzročilo te oblike patologije in kakšen je njihov odnos?
3. Kateri so glavni mehanizmi njihovega razvoja, pa tudi simptomi bolnika?
4. Ali obstaja patogenetska povezava med obliko patologije, ki ste jo ugotovili pri pacientu, in razvojem razjede na nogi? Če je tako, poimenujte in opišite glavne povezave te odvisnosti. Če ne, pojasnite mehanizem razvoja razjede v tem primeru?
Problem 4
Pacient M., 46 let, znanstveni delavec, se pritožuje zaradi motenj spomina, omotice, bolečine v predelu srca, kratkega dihanja pri naporu. Meni, da je bolan 3 leta. Ne ukvarja se s telesnim delom in telesno vzgojo. Veliko kadi. Dobro se prehranjuje, uživa veliko mesa in živalskih maščob ter premalo sadja in zelenjave. Objektivno: srednje višine, hiperstenik. Izgleda veliko starejši od svojih let. Koža in mišice so mlahave. Meje srca so razširjene. Toni so pridušeni. Pulz 86 / min, ritmični. HELL 140/90 mm. rt. Umetnost. EKG kaže znake koronarne insuficience. Fluoroskopija je pokazala razširitev aortnega loka. V krvi se močno poveča vsebnost holesterola in β-lipoproteinov. Bolniku so predpisali fizioterapevtske vaje in dieto, bogato z zelenjavo in sadjem, z zmanjšano vsebnostjo kalorij in omejevanjem živalskih maščob. Poleg tega je v dnevno prehrano priporočljivo vnesti vsaj 20 g naravnega rastlinskega olja.
Kontrolna vprašanja:
1. Kateri so verjetni vzroki in posledice hiperholesterolemije pri tem bolniku?
Testne naloge za kontrolo končne ravni znanja študentov
1. HIPERHOLESTERINEIJA JE V NASLEDNJIH PATOLOŠKIH STANJAH (3):
1.sufepatična zlatenica
2.ateroskleroza
3. diabetes mellitus
4.akutni glomerulonefritis
5.lipoidna nefroza
2. IZBERITE DEJAVNIKE TVEGANJA ZA RAZVOJ ATEROSKLEROZE (3)
1.hipotenzija
2.hipertenzija
3. diabetes mellitus
4. diabetes insipidus
5.debelost
3. PRI NASTANKU ATHER (3) SODELUJEJO NASLEDNJI CITOKINI:
1.interferoni
2.interlevkin-3
3.interlevkin-1
4.faktor nekroze tumorja-α
5.rastni faktor trombocitov
4. NAKAZITE RAVEN HOLESTEROLA V KRVNI PLAZMI, KI ODRAŽA NJEGOVI IZHOD IZ VASKULARNE STENE (A) IN ODLOŽITEV V Vmesnem delu žile (B)
1,4,7 mmol / l
2,5,2 mmol / l
3,6 mmol / l
5. IZBERITE, KAKŠNO RAZMERJE LIPOPROTEINSKIH FRAKCIJ V KRVNI PLAZMI Spodbuja tvorbo ATEROSKLEROTIČNIH PLOŠČ (2):
1.povečanje vsebnosti LDL
2.zmanjšanje LDL
3.povečanje vsebnosti HDL
4.Zmanjšanje vsebnosti HDL
5. Zmanjšanje VLDL
6. PRI NASTANKU ZAPLETOV ATEROSKLEROZE JE POMEMBNO STANJE "NESTABILNOSTI" MLADIH, ALI "MEHKIH" ATEROSKLEROTIČNIH PLOŠČ, PREDPOSTAVLJENIH ZA IZTISKANJE LUPINE. TO VODI DO NASLEDNJIH KRŠITEV (3):
1.bolečinski sindrom na mestu rupture plaka
2.povečajo trombogeni potencial krvi
3.nastanek parietalnega tromba
4.motnje reoloških lastnosti krvi v sistemskem obtoku
5. poslabšanje lokalnih hemodinamskih motenj
7. UČINEK PREPREČEVANJA ATEROSKLEROZE JE LAHKO POVEZAN Z NASLEDNJIMI MEHANIZMI (2):
1.zmanjšanje vsebnosti LDL v krvi
2.povišane ravni LDL v krvi
3.povečanje vsebnosti VLDL v krvi
4.povišane ravni HDL v krvi
5.Zmanjšanje vsebnosti HDL v krvi
8. RAZLOGI ZA SPREMEMBO LIPOPROTEINOV SO (2):
1.glikozilacija
2.razgradnjo lipidov s triglicerid lipazo
3.Esterifikacija holesterola
4.aktivacija SRO
5.resinteza lipoproteinov iz ketonskih teles in beljakovin
9. "PENANE CELICE", ki nastanejo z AKUMULACIJO LIPIDI V (2):
1.makrofagi
2. limfociti
3.nevtrofilci
4.gladke mišične celice
5.endotelijske celice
10. SODELUJOČI MAKROFAGI ABSORPIRAJO LIPOPROTEINE (2):
1.receptor za LDL
2.receptor za HDL
3.receptor za holesterol
4.receptor za VLDL
5.receptor za fosfolipide
11. GLAVNE KOMPONENTE Vlaknene plošče SO (1):
1.fibroblasti
2.eozinofili
3.bazofilci
4.makrofagi
12. IZBERI ZAPOREDJE SPREMEMBE ATEROGENEZE (1):
1) migracija makrofagov v žarišče kopičenja lipidov;
2) prevzem lipoproteinov s strani makrofagov, preobrazba v "penaste celice"
3) sproščanje rastnih in kemotaktičnih faktorjev za gladke mišične celice
4) poškodba endotelija in kopičenje lipoproteinov v intimi arterij
5) aktiviranje sinteze kolagena in elastina v gladkih mišičnih celicah
6) nastanek vlaknaste kapsule okoli žarišča kopičenja lipidov
A - 4.3.1.2.5.6
B - 4,2,3,1,5,6
B - 2,4,5,1,3,6
13. PRIMARNE ATEROSKLEROTIČNE SPREMEMBE V ARTERIJAH (LIPIDNI PASOVI) SE LAHKO POJAVIMO PRVIČ V STAROSTI (1):
1. do 10 let 2. 20-25 let 3. 30-35 let
4. 40-45 let 5. po 50 letih
14. NAJpogostejše posledice in zapleti ATEROSKLEROZE SO (2):
1.arterijska tromboza
2.Vinova tromboza
3.insuficienca aortne zaklopke
5.srčno popuščanje
15. MINIMALNO POVEČANJE ATEROGENOSTI HOLESTEROLA, KI KAŽE NA POMEMBNO TVEGANJE ATEROSKLEROZE (1):
1. 1 2. 5 3. 4 4. 3 5. 2
16. IZBIRAJTE POVEZANE IZJAVE ZA TROMBAGENO TEORIJO IZJAV (2):
1.zmanjšana proizvodnja dušikovega oksida z endoteliocitomom
2.zmanjšanje adhezivne sposobnosti trombocitov
3.povečana proizvodnja dušikovega oksida v endotelijskih celicah
4.povečanje agregacijske sposobnosti trombocitov
5.povečana proizvodnja prostaciklina I2
Z biološkega vidika so najpomembnejše fizikalno-kemijske lastnosti lipidov nasprotne lastnosti ogljikovih hidratov. Njihove molekule so topne v maščobah, velike in imajo relativno nizko vsebnost kisikovih atomov.
Lipidi so počasen energijski substrat. Zaradi nizke topnosti v vodi ne morejo doseči visoke koncentracije v krvi, zato ne morejo biti energijski substrat za tkiva.
Lipidov je kar nekaj. Prvič, zaradi majhnega števila atomov kisika je prosta energija lipidov precej visoka. Drugič, zaradi svoje hidrofobnosti lahko tvorijo velike kapljice, ki napolnijo skoraj celotno celico.
Lipidi so pomemben plastični material. Lahko tvorijo hidrofobno membrano, ki omejuje celico iz okoliške vodne raztopine. Zaradi tega so osnova za biološke membrane.
Podkožno maščobno tkivo je toplotni izolator. Odlaganje lipidov je pomembna mehanska funkcija.
Glavni lipidi človeškega telesa so holesterol, fosfolipidi, trigliceridi.
Maščobne kisline in trigliceridi delujejo predvsem kot energijski substrati. Holesterol in fosfolipidi se uporabljajo za druge namene – za tvorbo biološko aktivnih snovi in membran.
Uporaba trigliceridov:
Odlaganje v maščobnem tkivu, katabolizem - gradnja membrane.
Viri vnosa trigliceridov:
Prihajajo s hrano in se mobilizirajo iz maščobnega tkiva.
Tvorba iz ogljikovih hidratov in beljakovin. Ob povečanem vnosu substratov se v jetrih pretvorijo v trigliceride, s krvjo pa se prenesejo v maščobno tkivo, kjer ostanejo.
Glavna oblika odlaganja lipidov v maščobnem tkivu so trigliceridi.
Glavni energetski substrat, ki se celicam oskrbuje iz maščobnega tkiva, so maščobne kisline. To je posledica dejstva, da maščobne kisline bolje prodrejo skozi celične membrane.
Hitrejši energetski substrat so ketonska telesa. Ketonska telesa nastajajo v jetrih. Ketonska telesa se lahko uporabljajo s tkivi, ki se hitro presnavljajo. Toda za popolno oksidacijo ketonskih teles so potrebni produkti oksidacije ogljikovih hidratov. Zato se ob prisotnosti motenj v katabolizmu ogljikovih hidratov v krvi kopičijo ketonska telesa.
Maščobe so hidrofobne, zato obstajajo posebni mehanizmi za njihov transport v krvi. Proste (neesterificirane) maščobne kisline kri prenaša v obliki kompleksov z albuminom. Holesterol, njegovi estri, triacilgliceroli, fosfolipidi se prenašajo kot lipoproteini.
lipoproteini so molekularni kompleksi, sestavljeni iz lipidov in beljakovin.
riž. 10.2. Struktura lipoproteinov
Obstaja več razredov lipoproteinov (LP), vendar jih vse združujejo naslednje značilnosti: 1) površinsko plast lipoproteinov sestavljajo fosfolipidi, prosti holesterol in beljakovine; 2) vsak lipoprotein vsebuje poseben nabor površinskih beljakovin - apolipoproteinov (apo), ki so označeni s črkami latinske abecede (A, B, C); 3) jedro (jedro) lipoproteina sestavljajo hidrofobni triacilgliceroli, estri holesterola (slika 10.2).
Apolipoproteini izvajati naslednje funkcije: 1) so strukturne komponente lipoproteinov; 2) sodelujejo pri prepoznavanju in interakciji z membranskimi receptorji; 3) aktivirati encime presnove lipoproteinov.
Lipoproteine delimo v 4 glavne razrede glede na gostoto (določeno z ultracentrifugiranjem) in elektroforetično mobilnost (tabela 10.1).
Tabela 10.1.
Razvrstitev lipoproteinov po metodi ločevanja
Glavni parametri in sestava lipoproteinov so predstavljeni v tabeli. 10.2.
hilomikroni(HM) - največji delci. HM se sintetizirajo v črevesni sluznici in sodelujejo pri eksogeni transport lipidov hrane v različna tkiva... Glavni lipid je triacilgliceroli.
VLDL sintetizirano v jetrih. Glavni lipid je triacilgliceroli... Glavna funkcija je transport endogenih lipidov iz jeter v periferna tkiva.
LDL se tvori v krvnem obtoku iz VLDL. Vsebujejo veliko holesterol(glavni prenašalec holesterola), ki se prevaža v periferna tkiva.
HDL nastajajo v jetrih, vsebujejo veliko fosfolipidov in beljakovin; v teh zdravilih sestavine ovoja prevladujejo nad jedrom.
Tabela 10.2
Sestava lipoproteinov
TG - triacilgliceroli, PL - fosfolipidi. CS - holesterol
Ločimo eksogeni (prenos lipidov hrane) in endogeni (prenos lipidov, sintetiziranih v telesu) transport.
Eksogeni transport. Produkti prebave lipidov se absorbirajo v celice črevesne sluznice kot del micel. Maščobne kisline s številom ogljikovih atomov<12 всасываются в кровь и по воротной вене транспортируются в печень. Длинноцепочечные жирные кислоты (С >12) v črevesnih celicah se ponovno esterificirajo v triacilglicerole, ki so po sestavi podobni prehranskim maščobam. Dobljeni triacilgliceroli skupaj s fosfolipidi, holesterolom in beljakovinami (2%) tvorijo hilomikrone. Hilomikroni vsebujejo apoprotein B48 in apoA.
riž. 10.3. Eksogeni transport lipidov (po Murray R. et al., 2004)
Hilomikroni vstopijo v limfo. V krvi jih najdemo z delci HDL, ki vsebujejo apoE in apoC. Hilomikroni donirajo apoA delcem HDL, v zameno pa pridobijo apoE in apoC. Eden od apolipoproteinov skupine C - apoCII - služi kot aktivator encima lipoprotein lipaze (LPL). Ta encim sintetizirajo in izločajo maščobno in mišično tkivo, celice dojk. Izločeni encim se veže na plazemsko membrano endotelijskih celic kapilar tistih tkiv, kjer je bil sintetiziran. ApoCII, ki se nahaja na površini CM, aktivira LPL. Hidrolizira triacilglicerole v CM v glicerol in maščobne kisline. Te maščobne kisline bodisi vstopijo v celice maščobnega in mišičnega tkiva bodisi se združijo s plazemskim albuminom. Zaradi delovanja LPL se hilomikroni močno zmanjšajo v velikosti in jih imenujemo ostanki (ostanki). Ostanke HM zajamejo jetra preko receptorske poti (slika 10.3).
Endogeni transport. V jetrnih celicah se ponovno sintetizirajo triacilgliceroli in fosfolipidi, ki so značilni za ta organizem. Vključeni so v VLDL. VLDLP vsebuje apoB100 in apoC. To je glavna transportna oblika triacilglicerolov. Drugi razred lipoproteinov, ki nastanejo v jetrih - HDL - vključuje holesterol, fosfolipide, apoA. Ti delci so ploščati in se imenujejo nastajajoči HDL. (V njihovem jedru ni hidrofobnih molekul.) Ti HDL imajo pomembno vlogo pri povratnem transportu holesterola iz perifernih tkivnih celic v jetra.
V kapilarah maščobnega in mišičnega tkiva apoCII VLDLP aktivira LPL, ki katalizira hidrolizo VLDL triacilglicerolov in jih pretvori v IDL (lipoproteine vmesne gostote). Pod delovanjem krožeče jetrne triacilglicerolipaze, sintetizirane v jetrih, IDP izgubijo tudi nekaj triacilglicerolov in se pretvorijo v LDL. Glavni lipid LDL je holesterol, ki se kot del LDL prenaša v celice vseh tkiv. Zato se LDL tvori neposredno v žilni postelji (slika 10.4).
riž. 10.4. Endogeni transport lipidov (po Murray R. et al., 2004)
Tako se zaradi eksogenega in endogenega transporta v kapilarah maščobnega in mišičnega tkiva sproščajo maščobne kisline in glicerol. Maščobne kisline se vežejo na albumin in se prenašajo v potrošniška tkiva.