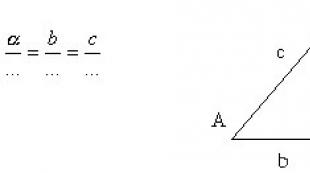Kuumutamisel vesi paisub või tõmbub kokku. Kui vesi külmub, siis see paisub või tõmbub kokku: lihtne füüsika. Vesi vajab jahtudes rohkem ruumi
Jaapani füüsik Masakazu Matsumoto on esitanud teooria, mis selgitab, miks vesi 0–4 °C kuumutamisel paisumise asemel kokku tõmbub. Tema mudeli järgi sisaldab vesi mikromoodustisi - “vitriteid”, mis on kumerad õõnsad hulktahukad, mille tipud sisaldavad veemolekule ja servad on vesiniksidemed. Temperatuuri tõustes võistlevad omavahel kaks nähtust: veemolekulide vaheliste vesiniksidemete pikenemine ja vitriitide deformatsioon, mis viib nende õõnsuste vähenemiseni. Temperatuurivahemikus 0 kuni 3,98°C domineerib viimane nähtus vesiniksidemete pikenemise mõjul, mis lõppkokkuvõttes annab vaadeldava vee kokkusurumise. Matsumoto mudelile, nagu ka teistele vee kokkusurumist selgitavatele teooriatele, pole veel eksperimentaalset kinnitust.
Erinevalt enamikust ainetest võib vesi kuumutamisel oma mahtu vähendada (joonis 1), see tähendab, et sellel on negatiivne soojuspaisumistegur. Kuid me ei räägi kogu temperatuurivahemikust, kus vesi on vedelas olekus, vaid ainult kitsast lõigust - 0 ° C kuni ligikaudu 4 ° C. Koos b O Kõrgematel temperatuuridel vesi, nagu ka teised ained, paisub.
Muide, vesi pole ainus aine, millel on omadus temperatuuri tõustes kokku tõmbuda (või jahtudes paisuda). Sarnase käitumisega võivad uhkustada ka vismut, gallium, räni ja antimon. Keerulisema siseehituse, aga ka levimuse ja olulisuse tõttu erinevates protsessides tõmbab teadlaste tähelepanu just vesi (vt Vee struktuuri uurimine jätkub, “Elemendid”, 09.10.2006 ).
Mõni aeg tagasi oli üldtunnustatud teooria, mis vastas küsimusele, miks vesi temperatuuri langedes oma mahtu suurendab (joonis 1), kahe komponendi – “normaalse” ja “jäätaolise” – segu mudeliks. Selle teooria pakkus esmakordselt välja 19. sajandil Harold Whiting ning hiljem arendasid ja täiustasid paljud teadlased. Suhteliselt hiljuti, avastatud vee polümorfismi raames, mõeldi Wietingi teooria ümber. Praegu arvatakse, et ülejahutatud vees on kahte tüüpi jäätaolisi nanodomeene: suure tihedusega ja madala tihedusega amorfse jäätaolised piirkonnad. Ülejahutatud vee kuumutamine viib nende nanostruktuuride sulamiseni ja kahte tüüpi vee ilmumiseni: suurema ja väiksema tihedusega. Kaval temperatuurikonkurents tekkiva vee kahe "klassi" vahel põhjustab tiheduse mittemonotoonse sõltuvuse temperatuurist. Seda teooriat pole aga veel eksperimentaalselt kinnitatud.
Selle selgitusega peate olema ettevaatlik. Pole juhus, et me räägime siin ainult struktuuridest, mis meenutavad amorfset jääd. Fakt on see, et amorfse jää ja selle makroskoopiliste analoogide nanoskoopilistel piirkondadel on erinevad füüsikalised parameetrid.
Jaapani füüsik Masakazu Matsumoto otsustas siin käsitletud mõjule seletuse leida "nullist", heites kõrvale kahekomponendilise segu teooria. Arvutisimulatsioonide abil uuris ta vee füüsikalisi omadusi laias temperatuurivahemikus – 200–360 K nullrõhul –, et mõista molekulaarsel skaalal vee jahtumisel paisumise tõelisi põhjuseid. Tema artikkel ajakirjas Füüsilise ülevaate kirjad selle nimi on: Miks vesi paisub, kui see jahtub? ("Miks vesi jahtudes paisub?").
Esialgu esitas artikli autor küsimuse: mis mõjutab vee soojuspaisumistegurit? Matsumoto usub, et selleks piisab vaid kolme teguri mõju väljaselgitamisest: 1) veemolekulide vaheliste vesiniksidemete pikkuse muutused, 2) topoloogiline indeks – sidemete arv veemolekuli kohta ja 3) veemolekulide vaheliste sidemete hälve. nurk sidemete vahel tasakaaluväärtusest (nurgamoonutus).

Enne kui räägime Jaapani füüsiku saadud tulemustest, teeme olulised kommentaarid ja täpsustused ülaltoodud kolme teguri kohta. Esiteks vastab vee tavaline keemiline valem H 2 O ainult selle auruolekule. Vedelal kujul liidetakse veemolekulid rühmadesse (H 2 O) vesiniksideme kaudu. x, Kus x- molekulide arv. Energeetiliselt soodsaim kombinatsioon viiest veemolekulist ( x= 5) nelja vesiniksidemega, milles sidemed tekivad tasakaal, nn tetraeedriline nurk, võrdne 109,47 kraadiga (vt joonis 2).
Olles analüüsinud veemolekulide vahelise vesiniksideme pikkuse sõltuvust temperatuurist, jõudis Matsumoto oodatud järeldusele: temperatuuri tõus põhjustab vesiniksidemete lineaarset pikenemist. Ja see omakorda toob kaasa vee mahu suurenemise, see tähendab selle paisumise. See asjaolu on vastuolus täheldatud tulemustega, mistõttu uuris ta täiendavalt teise teguri mõju. Kuidas sõltub soojuspaisumistegur topoloogilisest indeksist?
Arvuti modelleerimine andis järgmise tulemuse. Madalatel temperatuuridel hõivavad protsentuaalselt suurima veemahu veekogud, mille molekuli kohta on 4 vesiniksidet (topoloogiline indeks on 4). Temperatuuri tõus põhjustab assotsiatsioonide arvu vähenemise indeksiga 4, kuid samal ajal hakkab kasvama klastrite arv indeksiga 3 ja 5. Pärast arvulisi arvutusi avastas Matsumoto, et topoloogiliste klastrite lokaalne maht indeks 4 temperatuuri tõustes praktiliselt ei muutu ning indeksitega 3 ja 5 assotsieerunud kogumahu muutus mis tahes temperatuuril kompenseerib üksteist vastastikku. Järelikult ei muuda temperatuuri muutus vee kogumahtu ja seetõttu ei avalda topoloogiline indeks vee kokkusurumisele kuumutamisel mingit mõju.
Vesiniksidemete nurkmoonutuste mõju tuleb veel selgitada. Ja siit algabki kõige huvitavam ja olulisem. Nagu eespool mainitud, kipuvad veemolekulid ühinema nii, et vesiniksidemete vaheline nurk on tetraeedriline. Kuid veemolekulide termilised vibratsioonid ja vastasmõjud teiste klastris mittekuuluvate molekulidega takistavad neil seda tegemast, jättes vesiniksideme nurga kõrvale tasakaaluväärtusest 109,47 kraadi. Selle nurkdeformatsiooni protsessi kuidagi kvantitatiivseks iseloomustamiseks kasutasid Matsumoto ja kolleegid oma varasemat tööd 2007. aastal avaldatud vesiniksidemevõrkude topoloogilised ehitusplokid vees. Journal of Chemical Physics, oletas kolmemõõtmeliste mikrostruktuuride olemasolu vees, mis meenutavad kumeraid õõnsaid hulktahukaid. Hiljem, järgmistes väljaannetes, nimetasid nad selliseid mikrostruktuure vitriinid(joonis 3). Nendes on tipud veemolekulid, servade rolli mängivad vesiniksidemed ja vesiniksidemete vaheline nurk on nurkade vaheline nurk vitritis.
Matsumoto teooria kohaselt on vitriidi vorme tohutult palju, mis nagu mosaiikelemendid moodustavad suurema osa vee struktuurist ja mis samal ajal täidavad ühtlaselt kogu selle mahu.

Veemolekulid kalduvad tekitama vitritites tetraeedrilisi nurki, kuna vitrititel peab olema võimalikult väike energia. Kuid termiliste liikumiste ja kohalike interaktsioonide tõttu teiste vitriitidega ei esine mõnel mikrostruktuuril tetraeedriliste nurkade (või sellele väärtusele lähedaste nurkade) geomeetriat. Nad aktsepteerivad selliseid struktuurselt mittetasakaalulisi konfiguratsioone (mis ei ole neile energeetilisest vaatepunktist kõige soodsamad), mis võimaldavad kogu vitriitide “perekonnal” tervikuna saada võimalike seast madalaima energiaväärtuse. Sellist vitriiti, st vitriiti, mis näib end ohverdavat "ühiste energiahuvide nimel", nimetatakse frustratsiooniks. Kui pettumatu vitriidi korral on õõnsuse maht antud temperatuuril maksimaalne, siis frustreeritud vitriidi korral on see vastupidi minimaalne.
Matsumoto läbi viidud arvutimodelleerimine näitas, et vitriitõõnsuste keskmine maht väheneb temperatuuri tõustes lineaarselt. Sellisel juhul vähendab frustreeritud vitriit oluliselt selle mahtu, samas kui pettumatu vitriidi õõnsuse maht jääb peaaegu muutumatuks.
Niisiis, vee kokkusurumine temperatuuri tõusuga on põhjustatud kahest konkureerivast mõjust - vesiniksidemete pikenemisest, mis viib vee mahu suurenemiseni, ja frustreeritud vitriitide õõnsuste mahu vähenemiseni. Temperatuurivahemikus 0 kuni 4 °C on viimane nähtus, nagu arvutused on näidanud, valitseb, mis lõpuks viib vee täheldatud kokkusurumiseni temperatuuri tõustes.
Jääb oodata eksperimentaalset kinnitust vitriitide olemasolu ja nende käitumise kohta. Kuid paraku on see väga raske ülesanne.
Üks levinumaid aineid Maal: vesi. See, nagu õhk, on meile vajalik, kuid mõnikord ei märka me seda üldse. Ta lihtsalt on. Aga selgub
Üks levinumaid aineid Maal: vesi. See, nagu õhk, on meile vajalik, kuid mõnikord ei märka me seda üldse. Ta lihtsalt on. Kuid selgub, et tavaline vesi võib oma mahtu muuta ja kaaluda kas rohkem või vähem. Kui vesi aurustub, soojeneb ja jahtub, juhtub tõeliselt hämmastavaid asju, millest me täna õpime.
Muriel Mandell toob oma meelelahutuslikus raamatus “Füüsikalised eksperimendid lastele” välja huvitavaid mõtteid vee omadustest, mille põhjal ei saa mitte ainult noored füüsikud õppida palju uut, vaid ka täiskasvanud värskendavad oma teadmisi, mis on ei pidanud pikka aega kasutama, nii et see osutus kergelt ununenud.Täna räägime vee mahust ja kaalust. Selgub, et sama kogus vett ei kaalu alati sama. Ja kui valate klaasi vett ja see ei valgu üle ääre, ei tähenda see, et see mingil juhul sinna mahuks.
1. Kui vett kuumutatakse, paisub selle maht
Aseta veega täidetud purk pannile, mis on täidetud umbes viie sentimeetri jagu keeva veega. vesi ja keeda tasasel tulel. Vesi purgist hakkab üle ajama. See juhtub seetõttu, et kui vesi soojeneb, nagu teised vedelikud, hakkab see rohkem ruumi võtma. Molekulid tõrjuvad üksteist suurema intensiivsusega ja see toob kaasa vee mahu suurenemise.2. Kui vesi jahtub, tõmbub see kokku
Laske purgis oleval veel toatemperatuuril jahtuda või lisage uus vesi ja asetage see külmkappi. Mõne aja pärast avastad, et varem täis purk pole enam täis. Jahutades temperatuurini 3,89 kraadi Celsiuse järgi, väheneb vee maht temperatuuri langedes. Selle põhjuseks oli molekulide liikumiskiiruse vähenemine ja nende lähenemine üksteisele jahutamise mõjul.Näib, et kõik on väga lihtne: mida külmem on vesi, seda vähem see võtab, kuid ...
3. ...vee maht suureneb uuesti, kui see külmub
Täida purk ääreni veega ja kata papitükiga. Asetage see sügavkülma ja oodake, kuni see külmub. Näete, et papist "kaas" on välja lükatud. Temperatuuridel 3,89–0 kraadi Celsiuse järgi, st külmumispunktile lähenedes hakkab vesi uuesti paisuma. See on üks väheseid teadaolevaid selle omadusega aineid.Kui kasutate tihedat kaant, lööb jää purgi lihtsalt puruks. Kas olete kunagi kuulnud, et isegi veetorud võivad jääga puruneda?4. Jää on veest kergem
Asetage paar jääkuubikut veeklaasi. Jää hakkab pinnal hõljuma. Kui vesi külmub, suureneb selle maht. Ja selle tulemusena on jää veest kergem: selle maht on umbes 91% vastavast vee mahust.See vee omadus eksisteerib looduses põhjusega. Sellel on väga konkreetne eesmärk. Nad ütlevad, et talvel jõed jäätuvad. Kuid tegelikult pole see täiesti tõsi. Tavaliselt külmub vaid väike pealmine kiht. See jääkilp ei vaju, sest on vedelast veest kergem. See aeglustab vee külmumist jõe sügavuses ja toimib omamoodi tekina, mis kaitseb kalu ja muud jõgede ja järvede elukat tugevate talvekülmade eest. Füüsikat õppides hakkad mõistma, et looduses on paljud asjad otstarbekalt paigutatud.
5. Kraanivesi sisaldab mineraalaineid
Valage väikesesse klaaskaussi 5 supilusikatäit tavalist kraanivett. Kui vesi aurustub, jääb kausile valge ääris. Selle serva moodustavad mineraalid, mis lahustusid vees mullakihtide läbimisel.Vaadake oma veekeetja sisse ja näete maavarasid. Sama kattekiht tekib vanni äravooluavale.Proovige vihmavett aurustada, et ise kontrollida, kas see sisaldab mineraale. Veel on hämmastavad omadused, mis eristavad seda teistest vedelikest. Kuid see on hea, vastasel juhul, kui veel oleks "tavalised" omadused, oleks planeet Maa täiesti erinev.Valdav enamus aineid kipub kuumutamisel paisuma. Mida on soojuse mehaanilise teooria seisukohast üsna lihtne seletada. Selle järgi hakkavad kuumutamisel aine aatomid ja molekulid kiiremini liikuma. Tahketes ainetes saavutavad aatomivõnked suurema amplituudi ja nõuavad rohkem vaba ruumi. Selle tulemusena keha laieneb.
Sama protsess toimub vedelike ja gaasidega. See tähendab, et temperatuuri tõusu tõttu suureneb vabade molekulide soojusliikumise kiirus ja keha laieneb. Jahtudes tõmbub keha vastavalt kokku. See on tüüpiline peaaegu kõikidele ainetele. Välja arvatud vesi.
Jahutamisel vahemikus 0 kuni 4 °C vesi paisub. Ja kuumutamisel kahaneb. Kui vee temperatuur jõuab 4°C-ni, on sel hetkel vee maksimaalne tihedus, mis on 1000 kg/m3. Kui temperatuur on sellest märgist madalam või kõrgem, on tihedus alati veidi väiksem.
Tänu sellele omadusele, kui õhutemperatuur sügisel ja talvel langeb, toimub sügavates reservuaarides huvitav protsess. Kui vesi jahtub, vajub see madalamale põhja, kuid ainult seni, kuni selle temperatuur jõuab +4°C-ni. Just sel põhjusel on suurtes veekogudes külmem vesi pinnale lähemal ja soojem vesi vajub põhja. Nii et kui veepind talvel külmub, säilitavad sügavamad kihid jätkuvalt 4°C temperatuuri. Tänu sellele hetkele saavad kalad turvaliselt talvitada jääga kaetud veehoidlate sügavustes.
Veepaisumise mõju kliimale
Kuumutatud vee erakordsed omadused mõjutavad tõsiselt Maa kliimat, kuna umbes 79% meie planeedi pinnast on kaetud veega. Päikesekiirte toimel kuumenevad ülemised kihid, mis seejärel vajuvad madalamale ning nende asemele tekivad külmad kihid. Need omakorda soojenevad järk-järgult ja vajuvad põhja lähemale.Seega muutuvad veekihid pidevalt, mille tulemuseks on ühtlane kuumenemine kuni maksimaalsele tihedusele vastava temperatuuri saavutamiseni. Seejärel muutuvad ülemised kihid soojenedes vähem tihedaks ega vaju enam alla, vaid jäävad ülaosasse ja muutuvad lihtsalt järk-järgult soojemaks. Tänu sellele protsessile kuumenevad päikesekiirte toimel üsna kergesti tohutud veekihid.
Meid ümbritseb vesi iseenesest, osana teistest ainetest ja kehadest. See võib olla tahkel, vedelal või gaasilisel kujul, kuid vesi on alati meie ümber. Miks asfalt teedel praguneb, miks klaaspurk vett purskab külma käes, miks külmal aastaajal aknad uduseks lähevad, miks jätab lennuk taevasse valge jälje - kõigele sellele otsime vastuseid ja muud "miks" selles õppetunnis. Saame teada, kuidas muutuvad vee omadused kuumutamisel, jahutamisel ja külmutamisel, kuidas tekivad maa-alused koopad ja nendes veidrad kujud, kuidas töötab termomeeter.
Teema: Elutu loodus
Õppetund: Vedela vee omadused
Puhtal kujul pole veel maitset, lõhna ega värvi, kuid see pole peaaegu kunagi selline, sest lahustab enamiku aineid endas aktiivselt ja ühineb nende osakestega. Vesi võib tungida ka erinevatesse kehadesse (teadlased on leidnud vett isegi kividest).
Kui täidate klaasi kraaniveega, tundub see puhas. Kuid tegelikult on see paljude ainete lahus, mille hulgas on gaase (hapnik, argoon, lämmastik, süsinikdioksiid), õhus sisalduvaid erinevaid lisandeid, pinnasest lahustunud sooli, veetorudest pärit rauda, tillukesi lahustumata tolmuosakesi. , jne.

Kui pipeteerite kraanivee tilgad puhtale klaasile ja lasete sellel aurustuda, jäävad vaevu nähtavad laigud.

Jõgede ja ojade ning enamiku järvede vesi sisaldab mitmesuguseid lisandeid, näiteks lahustunud sooli. Kuid neid on vähe, sest see vesi on mage.

Vesi voolab maapinnal ja maa all, täidab ojasid, järvi, jõgesid, meresid ja ookeane, luues maa-aluseid paleesid.

Kergesti lahustuvate ainete kaudu tungib vesi sügavale maa alla, viies need endaga kaasa ning läbi pilude ja pragude kaljudes, moodustades maa-aluseid koopaid, tilkudes nende katustelt, luues veidraid skulptuure. Miljardid veepiisad aurustuvad sadade aastate jooksul ning vees lahustunud ained (soolad, lubjakivid) settivad koopavõlvidele, moodustades kivijääpurikad, mida nimetatakse stalaktiitideks.

Sarnaseid moodustisi koopa põrandal nimetatakse stalagmiitideks.

Ja kui stalaktiit ja stalagmiit kasvavad kokku, moodustades kivisamba, nimetatakse seda stalagnaadiks.

Jõel jää triivimist jälgides näeme vett tahkes olekus (jää ja lumi), vedelas (all voolab) ja gaasilises olekus (õhku tõusevad pisikesed veeosakesed, mida nimetatakse ka veeauruks).

Vesi võib olla korraga kõigis kolmes olekus: õhus ja pilvedes, mis koosnevad veepiiskadest ja jääkristallidest, on alati veeauru.

Veeaur on nähtamatu, kuid seda saab hõlpsasti tuvastada, kui jätate veeklaasi tunniks ajaks sooja ruumi külmkappi jahtuma, tekivad koheselt klaasi seintele veepiisad. Kokkupuutel klaasi külmade seintega muutub õhus sisalduv veeaur veepiiskadeks ja settib klaasi pinnale.

Riis. 11. Kondensatsioon külma klaasi seintel ()
Samal põhjusel uduneb külmal aastaajal aknaklaasi sisemus. Külm õhk ei saa sisaldada nii palju veeauru kui soe õhk, mistõttu osa sellest kondenseerub – muutub veepiiskadeks.

Taevas lendava lennuki taga olev valge jälg on samuti vee kondenseerumise tagajärg.

Kui tuua huultele peegel ja välja hingata, jäävad selle pinnale pisikesed veepiisad, mis tõestab, et hingates hingab inimene koos õhuga sisse veeauru.
Kui vett kuumutatakse, see "paisub". Seda saab tõestada lihtsa katsega: klaastoru lasti veekolbi ja mõõdeti veetaset selles; seejärel langetati kolb sooja veega anumasse ja pärast vee soojendamist mõõdeti uuesti tase torus, mis tõusis märgatavalt, kuna kuumutamisel vee maht suureneb.

Riis. 14. Toru, numbriga 1 ja joonega kolb näitab esialgset veetaset

Riis. 15. Toruga kolb, kus on number 2 ja joon, näitab veetaset kuumutamisel
Kui vesi jahtub, "pressib see kokku". Seda saab tõestada sarnase katsega: antud juhul langetati toruga kolb jääga anumasse, pärast jahutamist langes veetase torus esialgse märgiga võrreldes, kuna vee maht vähenes.

Riis. 16. Toru, numbriga 3 ja joonega kolb näitab veetaset jahutamise ajal
See juhtub seetõttu, et veeosakesed, molekulid, liiguvad kuumutamisel kiiremini, põrkuvad üksteisega, tõrjutakse anuma seintelt, molekulide vaheline kaugus suureneb ja seetõttu on vedelikul suurem maht. Kui vesi jahtub, aeglustub selle osakeste liikumine, molekulide vaheline kaugus väheneb ja vedelik vajab vähem mahtu.
Riis. 17. Vee molekulid normaaltemperatuuril
Riis. 18. Vee molekulid kuumutamisel
Riis. 19. Vee molekulid jahtumisel
Selliseid omadusi omavad mitte ainult vesi, vaid ka muud vedelikud (alkohol, elavhõbe, bensiin, petrooleum).
Teadmised vedelike selle omaduse kohta viisid alkoholi või elavhõbedat kasutava termomeetri (termomeetri) leiutamiseni.

Kui vesi külmub, siis see paisub. Seda saab tõestada, kui ääreni veega täidetud anum katta lõdvalt kaanega ja asetada sügavkülma, mõne aja pärast näeme, et tekkinud jää tõstab kaane üles, väljudes anumast.
Seda omadust arvestatakse veetorude paigaldamisel, mis tuleb isoleerida, et jäätumisel veest tekkiv jää torusid lõhkuma ei hakkaks.
Looduses võib külmutav vesi mägesid hävitada: kui vesi koguneb sügisel kivipragudesse, jäätub see talvel ning jää survel, mis võtab enda alla suurema mahu kui vesi, millest see tekkis, kivimid pragunevad ja varisevad.
Teepragudesse jääv vesi viib asfaltkatte hävimiseni.
Puutüvedel olevad volte meenutavad pikad rihmad on puidurebendid, mis on tekkinud selles külmuva puumahla survel. Seetõttu on külmadel talvedel kuulda pargis või metsas puude praksumist.
- Vahrušev A.A., Danilov D.D. Maailm meie ümber 3. M.: Ballas.
- Dmitrieva N.Ya., Kazakov A.N. Maailm meie ümber 3. M.: Kirjastus Fedorov.
- Pleshakov A.A. Maailm meie ümber 3. M.: Haridus.
- Pedagoogiliste ideede festival ().
- Teadus ja haridus ().
- Avalik klass ().
- Tee lühike test (4 küsimust kolme vastusevariandiga) teemal “Vesi meie ümber”.
- Tehke väike katse: asetage sooja ruumi lauale klaas väga külma vett. Kirjeldage, mis juhtub, selgitage, miks.
- *Joonistada veemolekulide liikumist kuumutatud, normaalses ja jahutatud olekus. Vajadusel kirjutage oma joonisele pealdised.